一种鉴定人类Mur血型基因的多重PCR方法与流程
本发明属于基因检测技术领域,具体涉及一种鉴定人类Mur血型基因的多重PCR方法。
背景技术:
1927年,Landsteiner和Levine使用人类血液免疫家兔并获得特异性抗体,从而发现了M和N抗原。在随后的研究中,MNS血型系统的抗原被不断发现,到目前为止已发现46种抗原,其复杂程度仅次于Rh血型系统。MNS血型系统中许多是高频或低频抗原,低频抗原多由单个氨基酸的改变或由GPA/GPB分子融合引起。
GPA及GPB由紧密的同源基因(GYPA/GYPB)控制编码,GYPA基因控制GPA的编码,GYPB基因控制GPB的编码。GYPA、GYPB基因具有高度同源性,可达95%以上。MNS血型系统抗原多态性与复杂性是GYP基因变异的结果,GYP基因变异包括单核苷酸或多核苷酸突变、交叉融合、基因转换、基因缺失、基因杂合等。Miltenberger亚系统中的许多低频抗原由杂合基因控制编码,如GP.Mur(GYPB.Mi.III)、GP.Hop(GYPB.Mi.IV)、GP.Bun(GYPB.Mi.VI)和GP.HF(GYPB.Mi.X)由GYP(B-A-B)杂合基因控制编码,其产物是B-A-B杂合糖蛋白[GP(B-A-B)]。基因杂合在MNS血型系统中出现频率较高。高度同源的GYPA、GYPB基因序列增加了基因杂合导致交换重组的机率,但这种交换是不对等的。不对等交换发生在减数分裂期,可产生两种新的单倍型:一种单倍型是由GYPA和GYPB基因组成的融合基因,而无单独的GYPA和GYPB基因。另一种单倍型被称为反-Lepore型(anti-lepore type),不仅有GYPA和GYPB基因的融合基因,而且在其两侧还有正常的GYPA和GYPB基因,Miltenberger亚系统中的Mur基因型GYP(B-A-B)Mur,即GP.Mur(GYPB.Mi.III)属于此类型。
Mur血型抗原是因GYPA和GYPB基因杂交而导致本不应该表达的GPB假外显子3表达后所产生,作为临床最为重要的稀有血型之一,目前正日益受到国内临床输血界的重视。Mur阳性血型在白种人中相当少见,但在亚洲人群中却有着相当高的阳性频率,特别是东南亚地区,约10%的泰国献血者为Mur抗原阳性。Mur血型在我国不同人群中分布频率有很大差异,香港和台湾地区Mur血型的平均频率分别为6.28%和7.3%,在台湾阿美山人中,Mur抗原阳性频率甚至可达88%;2014年有文献报导Mur抗原阳性在安徽省汉族人群中的分布频率为0.9%,而广州地区无偿献血者中Mur抗原阳性的频率为6.59%;广西侗族、壮族分布频率分别为15.4%和11.29%。Mur抗原可刺激机体产生抗-Mur,在香港抗-Mur在患者和孕妇中出现的频率分别为0.34%和0.46%,是常见的同种不规则抗体。抗-Mur可以导致急性和迟发性溶血性输血反应,以及严重的新生儿溶血病。因此鉴定Mur血型抗原对于了解人群分布频率,鉴定抗-Mur抗体,筛查和提供相合的血液,提高临床输血安全性都具有重要的应用价值。
目前检测Mur血型抗原仍十分困难,虽然可以用相应的抗-Mur检测出Mur抗原,但抗Mur的抗体没有市售商品,国内外只有少数免疫血清学实验室有筛查自人源的血清抗体,仅用于科研,无法大量用于临床,也更无法大规模推广应用。鉴于基因和表达蛋白的高度相关性,应用分子生物学的方法可以有效解决血型学方法抗体来源限制,导致难以推广的难题。
另外,目前市面已有Mur的基因分型试剂盒,但存在以下缺点:
1、价格昂贵:进口的Mur基因检测试剂虽然可靠性好,但每人份约需300~600人民币元,非常昂贵;国产试剂较便宜,每人份仍需100人民币元以上,可靠性较差,而且这个价格仍然是大规模检测难以承受的;
2、操作繁琐:上述试剂盒需4~8个反应管,样本DNA和耗材的消耗量很大,而且加样繁琐,容易出错,同时判读困难,不适于大规模的检测工作;
3、内对照均为人类生长激素基因,但我们实际使用中发现有因待检基因质量不好,造成内对照有扩增条带,但检测带无扩增产物,即假阴性的结果。
技术实现要素:
本发明所要解决的技术问题在于针对上述现有技术的不足,提供一种经济、简便和直观的鉴定人类Mur血型基因的多重PCR方法。
为解决上述技术问题,本发明采用的技术方案是,一种鉴定人类Mur血型基因的引物组,包括Mur上游引物和Mur下游引物,Mur上游引物序列如SEQ ID NO1所示:ACCCTCCAGAAGAGGAAACCGG;Mur下游引物序列如SEQ ID NO2所示:ACAGTGAAACGATGGACAAGTTGTC。
进一步地,该Mur上游引物位于GYPA基因与GYPB基因的杂交区域,Mur下游引物位于GYPA基因与GYPB基因杂交区域外的GYPB基因区域。
进一步地,还包括上游内对照引物和下游内对照引物,上游内对照引物序列如SEQ ID NO3所示:GAACATATCCGATGTTATACA;下游内对照引物序列如SEQ ID NO4所示:AGATGTGTCCAGCATCTGGCTA。
进一步地,该上游内对照引物位于GYPA基因与GYPB基因杂交区域外的GYPA基因的第一外显因子上;下游内对照引物位于GYPA基因与GYPB基因杂交区域外的GYPB基因的第一外显因子上。
进一步地,该Mur上游引物、Mur下游引物、上游内对照引物、下游内对照引物的体积比为:(0.5~3):(0.5~3):1:1。
进一步地,该Mur上游引物、Mur下游引物、上游内对照引物、下游内对照引物的体积比为:2:2:1:1。
进一步地,该Mur上游引物和Mur下游引物的PCR产物的长度均为988bp;上游内对照引物和下游内对照引物的PCR产物的长度均为592bp。
本发明还公开了一种用于鉴定人类Mur血型基因的试剂盒,包括上述的鉴定人类Mur血型基因的引物组。
进一步地,还包括如下:2.0μl 10倍缓冲溶液,2.0μl浓度为2.5mM的dNTP混合物,0.1μl浓度为5U/μl的Taq DNA聚合酶,1.0μl浓度为25mM的MgCl2溶液和13.7μl的双蒸水,Mur上游引物、Mur下游引物、上游内对照引物和下游内对照引物的总体积为2μl。
本发明还公开了一种鉴定人类Mur血型基因的多重PCR方法,该方法包括如下:将模板DNA与上述引物组或者试剂盒中的试剂混合,进行PCR扩增反应,再将PCR产物进行电泳得到结果。
本发明一种鉴定人类Mur血型基因的多重PCR方法具有如下优点:1.依据GenBank数据库中GYP(B-A-B)Mur相应序列(GenBank No:AF090739)、GYPA相应序列(GenBank No:NG_007470)和GYPB相应序列(GenBank No:NG_007483.2),根据GYP(B-A-B)Mur与GYPA/GYPB的差异位点,以保证扩增产物的特异性和鉴定的准确性。2.内对照设计在GYPA/GYPB的第1外显子上,为GYPA/GYPB共有序列,与待检基因位置接近,能够准确反映出待检基因的质量是否适于扩增,从而保证扩增实验能够准确,避免假阴性。3.Mur基因型为反-Lepore型,不仅有GYP(B-A-B)融合基因,还有正常的GYPA或GYPB基因,内对照引物设计于GYPA/GYPB上,当扩增出特异条带,也进一步验证了Mur基因型的反-Lepore型,提高了检出准确性。
附图说明
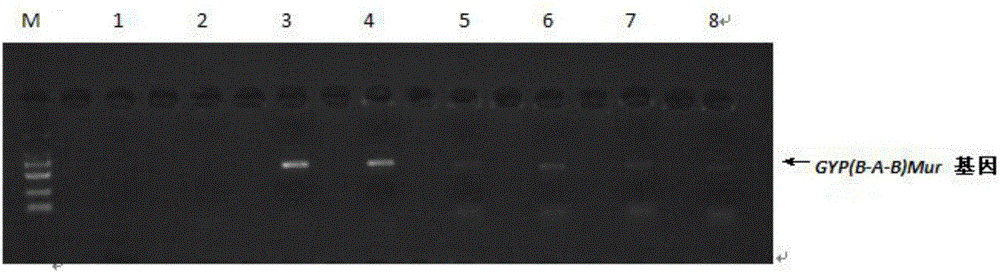
图1是本发明中GYP(B-A-B)Mur基因扩增结果;
其中:M:Marker,Takara,DL2000。1、2、3、5、6、7、8为阴性对照,4为GYP(B-A-B)Mur基因阳性样本;退火温度为57℃;
图2是本发明中GYP(B-A-B)Mur基因不同退火温度扩增结果;
其中:M:Marker,Takara,DL2000。1、2为阴性对照;3、4为GYP(B-A-B)Mur基因阳性样本,退火温度为57℃;5、6为GYP(B-A-B)Mur基因阳性样本,退火温度为58℃;7、8为GYP(B-A-B)Mur基因阳性样本,退火温度为59℃;
图3是本发明中GYP(B-A-B)Mur基因扩增产物测序结果;
图4是本发明中扩增产物在Genbank比对结果;
其中:Query为比对序列,Sbjct为目标参考序列GP.Mur(GYPB.Mi.III);
图5是本发明中GYP(B-A-B)Mur基因扩增结果;
其中:M:Marker,Takara,DL2000。1、2、3、5、6、7为阴性对照,4为GYP(B-A-B)Mur基因阳性样本;
图6是本发明中GYP(B-A-B)Mur基因扩增结果;
其中:M:Marker,Takara,DL2000。1、2为GYP(B-A-B)Mur基因阳性样本,3、4为阴性对照;
图7是48例样本中Mur基因检测结果;
其中:图中箭头所示为检测阳性结果。
具体实施方式
本发明一种鉴定人类Mur血型基因的引物组,一种鉴定人类Mur血型基因的引物组,包括Mur上游引物和Mur下游引物,Mur上游引物序列如SEQ ID NO1所示:ACCCTCCAGAAGAGGAAACCGG;Mur下游引物序列如SEQ ID NO2所示:ACAGTGAAACGATGGACAAGTTGTC。
该Mur上游引物位于GYPA基因与GYPB基因的杂交区域,Mur下游引物位于GYPA基因与GYPB基因杂交区域外的GYPB基因区域。
还包括上游内对照引物和下游内对照引物,上游内对照引物序列如SEQ ID NO3所示:GAACATATCCGATGTTATACA;下游内对照引物序列如SEQ ID NO4所示:AGATGTGTCCAGCATCTGGCTA。
该上游内对照引物位于GYPA基因与GYPB基因杂交区域外的GYPA基因的第一外显因子上;下游内对照引物位于GYPA基因与GYPB基因杂交区域外的GYPB基因的第一外显因子上。
该Mur上游引物、Mur下游引物、上游内对照引物、下游内对照引物的体积比为:(0.5~3):(0.5~3):1:1。
该Mur上游引物、Mur下游引物、上游内对照引物、下游内对照引物的体积比为:2:2:1:1。
该Mur上游引物和Mur下游引物的PCR产物的长度均为988bp;上游内对照引物和下游内对照引物的PCR产物的长度均为592bp。
本发明还公开了一种用于鉴定人类Mur血型基因的试剂盒,包括上述的鉴定人类Mur血型基因的引物组。
进一步地,还包括如下:2.0μl 10倍缓冲溶液,2.0μl浓度为2.5mM的dNTP混合物,0.1μl浓度为5U/μl的Taq DNA聚合酶,1.0μl浓度为25mM的MgCl2溶液和13.7μl的双蒸水,Mur上游引物、Mur下游引物、上游内对照引物和下游内对照引物的总体积为2μl。
本发明公开了一种鉴定人类Mur血型基因的多重PCR方法,该方法包括如下:将模板DNA与上述的引物组或者试剂盒中的试剂混合,进行PCR扩增反应,再将PCR产物进行电泳得到结果。
本发明的方法是利用人类Mur血型基因的特异性序列改变,设计2对引物,进行聚合酶链反应(PCR)来完成的。因此,本发明可被视为是基于PCR-SSP(Sequence specific primer,序列特异性引物)的原理而建立的。利用针对不同位点而设计出序列特异性引物,然后通过优化序列特异性引物的混合比例和PCR反应条件,从而达到准确检测出人类Mur血型基因型的目的,避免假阳性和假阴性出现。在本文中,术语“多重PCR”是指通过在同一个反应中同时完成多个基因的扩增的筛选检测方法。研究表明,对于成功进行多重PCR尤为重要的因素是:引物的特异性、引物混合比例和反应条件。
实施例1
本实施例中,验证了扩增Mur基因的引物的特异性,引物按照终浓度10μM稀释,阳性对照为上海血液中心提供的已确认为Mur抗原阳性的样本,提取全血基因组DNA作为阳性基因对照,该方法包括步骤:
(1)在0.5mL的Ependoff管内加入2.0μl的10倍缓冲溶液、2.0μl引物混合物、2.0μl浓度为2.5mM的dNTP混合物、0.1μl浓度为5U/μl的Taq DNA聚合酶、1.0μl浓度为25mM的MgCl2溶液、1.0μl模板DNA和13.7μl双蒸水,充分混合;
(2)将Ependoff管放入PCR扩增仪中,95℃变性5分钟,然后进行33个循环的PCR反应,即95℃下持续30秒,57℃下持续30秒和72℃下持续30秒,随后72℃延伸5分钟,然后将温度降低到4℃;
(3)取出PCR产物,4%琼脂糖凝胶电泳(200V,20分钟),紫外灯下观察结果并拍照,如图1所示。根据引物设计的扩增目的基因长度为988bp,图中4号样本有扩增产物,其扩增长度在与Marker相对照,略少于1000bp,符合扩增产物长度的设计;8个样本中,只有4号为GYP(B-A-B)Mur基因阳性样本,其它为阴性对照样本,从本发明设计的引物扩增结果可见,扩增结果符合样本设置预期,说明本发明所设计的引物具有很好的特异性。
在本实施方式中,所述引物混合物包含Mur上游引物和Mur下游引物,分别为特异性扩增GYP(B-A-B)Mur基因的上下游引物,扩增产物长度为988bp。Mur上游引物序列如SEQ ID NO1所示:ACCCTCCAGAAGAGGAAACCGG;Mur下游引物序列如SEQ ID NO2所示:ACAGTGAAACGATGGACAAGTTGTC。Mur上游引物位于GYPA基因与GYPB基因的杂交区域,Mur下游引物位于GYPA基因与GYPB基因杂交区域外的GYPB基因区域。扩增条件可选退火温度包括57℃、58℃和59℃,如图2所示,由图中可知,3个不同的退火温度条件下,57℃退火温度条件下的扩增产物电泳后观察条带清晰明亮,无杂带,说明扩增产物量大且特异性好;随着退火温度升高为58℃和59℃,扩增产物电泳后观察条带亮度减弱,也无杂带,显示随着退火温度升高,扩增产物量减少;说明在57℃退火温度条件下,扩增产物量大,利于电泳后观察结果,并且没有非特性的扩增产物,说明57℃是本发明的适宜退火温度。
还提供了扩增后的产物进行测序的结果,将扩增产物测序,测序引物为扩增引物。测序结果在Genbank上比对测序和比对结果见图3和图4所示。由图3可知,测序图中各碱基测序峰清晰,无杂合套叠峰,无错位峰;测序图底部为背景峰,峰值很低,显示扩增产物特异性高。测定的序列结果可以从图中直接读出,经比对,测序结果为GYP(B-A-B)Mur基因的序列,说明本发明建立的检测方法具有很好的特异性,能够特异性地扩增出GYP(B-A-B)Mur基因的序列。
由图4可知,扩增产物的测序结果与GP.Mur目标参考序列有很好的吻合度,说明本发明建立的检测方法具有很好的特异性,能够特异性地扩增出GYP(B-A-B)Mur基因的序列。
实施例2
在该实施例中,提供了一种检测Mur血型基因型的多重PCR方法,该方法包括如下步骤:
⑴在0.5mL的Ependoff管内加入2.0μl的10倍缓冲液、2.0μl的引物混合物、2.0μl浓度为2.5mM的dNTP混合物、0.1μl浓度为5U/μl Taq DNA聚合酶1.0μl浓度为25mM的MgCl2溶液、1.0μl模板DNA和13.7μl双蒸水,充分混合;
⑵将Ependoff管放入PCR扩增仪中,95℃变性5分钟,然后进行33个循环的PCR反应,即95℃下持续30秒,57℃下持续30秒和72℃下持续30秒,随后72℃延伸5分钟,然后将温度降低到4℃;
⑶取出PCR产物,4%琼脂糖凝胶电泳(200V,20分钟),紫外灯下观察结果并拍照。
所述引物混合物包含Mur上游引物、Mur下游引物、上游内对照引物、和下游内对照引物,Mur上游引物和Mur下游引物分别为特异性扩增GYP(B-A-B)Mur基因的上下游引物;上游内对照引物、下游内对照引物分别为特异性扩增GYPA和GYPB基因。Mur上游引物序列如SEQ ID NO1所示:ACCCTCCAGAAGAGGAAACCGG;Mur下游引物序列如SEQ ID NO2所示:ACAGTGAAACGATGGACAAGTTGTC。Mur上游引物位于GYPA基因与GYPB基因的杂交区域,Mur下游引物位于GYPA基因与GYPB基因杂交区域外的GYPB基因区域。上游内对照引物序列如SEQ ID NO3所示:GAACATATCCGATGTTATACA;游内对照引物序列如SEQ ID NO4所示:AGATGTGTCCAGCATCTGGCTA。上游内对照引物位于GYPA基因与GYPB基因杂交区域外的GYPA基因的第一外显因子上;下游内对照引物位于GYPA基因与GYPB基因杂交区域外的GYPB基因的第一外显因子上。基因GYP(B-A-B)Mur特异性扩增产物长度为988bp,内对照扩增产物长度为592bp。在本实施方式中,Mur上游引物、Mur下游引物、上游内对照引物、下游内对照引物的体积比为:2:2:1:1。也可以选用其他的体积比。扩增条件为:95℃变性5分钟,然后进行33个循环的PCR反应,即95℃下持续30秒,57℃下持续30秒和72℃下持续30秒,随后72℃延伸5分钟,然后将温度降低到4℃。
检测结果如图5和图6,由图5可知,由于不同引物对的扩增效率不同,故在Mur上游引物、Mur下游引物、上游内对照引物、下游内对照引物的体积比为:1:1:1:1的混合条件下,GYP(B-A-B)Mur基因的扩增产物比内对照的扩增产物少,不利于检测结果的判读,说明Mur上游引物、下游引物、上游内对照引物、下游内对照引物的体积比为:1:1:1:1的混合条件不是最佳混合比例。在上述体积比下均不会出现假阴性。
由图6可知,Mur上游引物、下游引物、上游内对照引物、下游内对照引物的体积比为:2:2:1:1,GYP(B-A-B)Mur基因的扩增产物清晰明确,内对照的扩增产物也能清晰显现,利于检测结果的判读,说明该混合条件下产物的量更为均衡,是最佳混合比例。
实施例3
本实施例中,检测了西安地区无偿献血人群中Mur基因的分布频率,检测方法为:
⑴在0.5mL的Ependoff管内加入2.0μl的10倍缓冲液、2.0μl的引物混合物、2.0μl浓度为2.5mM的dNTP混合物、0.1μl浓度为5U/μl Taq DNA聚合酶1.0μl浓度为25mM的MgCl2溶液、1.0μl模板DNA和13.7μl双蒸水,充分混合;
⑵将Ependoff管放入PCR扩增仪中,95℃变性5分钟,然后进行33个循环的PCR反应,即95℃下持续30秒,57℃下持续30秒和72℃下持续30秒,,随后72℃延伸5分钟,然后将温度降低到4℃;
⑶取出PCR产物,4%琼脂糖凝胶电泳(200V,20分钟),紫外灯下观察结果并拍照。
所述引物混合物包含Mur上游引物、Mur下游引物、上游内对照引物和下游内对照引物,Mur上游引物序列如SEQ ID NO1所示:ACCCTCCAGAAGAGGAAACCGG;Mur下游引物序列如SEQ ID NO2所示:ACAGTGAAACGATGGACAAGTTGTC。Mur上游引物位于GYPA基因与GYPB基因的杂交区域,Mur下游引物位于GYPA基因与GYPB基因杂交区域外的GYPB基因区域。上游内对照引物序列如SEQ ID NO3所示:GAACATATCCGATGTTATACA;游内对照引物序列如SEQ ID NO4所示:AGATGTGTCCAGCATCTGGCTA。上游内对照引物位于GYPA基因与GYPB基因杂交区域外的GYPA基因的第一外显因子上;下游内对照引物位于GYPA基因与GYPB基因杂交区域外的GYPB基因的第一外显因子上。Mur上游引物、Mur下游引物、上游内对照引物和下游内对照引物的体积比为:2:2:1:1。
检测结果如图7所示,图中显示的是48例样本的Mur基因检测结果,检出2例Mur基因阳性样本,这2例阳性样本在电泳图中显示有特异性的扩增条带(988bp)和内对照条带(592bp);其它样本显示只有内对照条带(592bp),说明PCR扩增反应成功,这些样本不具有Mur基因。在实际应用中,本方法稳定可靠,对于提取自不同个体的DNA均有良好的适应性,可以清晰明确地显示检测结果。
<110> 西安市中心血站
<120> 一种鉴定人类Mur血型基因的多重PCR方法
<130> 无
<160> 4
<170> PatentIn version 3.5
<210> SEQ ID NO1
<211> 22
<212> DNA
<213> 人工序列
<400> SEQ ID NO1
ACCCTCCAGA AGAGGAAACC GG 22
<210> SEQ ID NO2
<211> 25
<212> DNA
<213> 人工序列
<400> SEQ ID NO2
ACAGTGAAAC GATGGACAAG TTGTC 25
<210> SEQ ID NO3
<211> 21
<212> DNA
<213> 人工序列
<400> SEQ ID NO3
GAACATATCC GATGTTATAC A 21
<210> SEQ ID NO4
<211> 22
<212> DNA
<213> 人工序列
<400> SEQ ID NO4
AGATGTGTCC AGCATCTGGC TA 22
- 还没有人留言评论。精彩留言会获得点赞!