一种季鏻化壳聚糖及其作为疫苗免疫佐剂的应用的制作方法
本发明属于生物医用材料领域,涉及一种季鏻化壳聚糖及其作为疫苗免疫佐剂的应用。
背景技术:
疫苗接种是公认的近现代人类医学发展史上最重大的发明之一,至今仍然是人类预防、抵御和控制传染性疾病的最有效方法,例如流感、肝炎、肺结核等。
起初的疫苗由完全病原体或其裂解液制成,免疫原性好,但是会导致不良症状和感染。因此,一些更安全的疫苗正在研究和开发,包括dna、亚单位和重组疫苗。然而这些新型的疫苗仍具有免疫原性较低、免疫应答诱导较弱、靶向性弱等缺点。因此,探索和研发用以增强疫苗功效的技术具有重大意义,设计有助于提高免疫原性、改善安全性、增强机体特异性免疫应答的免疫佐剂成为首要任务。
自1925年起,免疫佐剂(immunoadjuvant)便引起了研究者们的广泛关注和浓厚兴趣。免疫佐剂是一类能帮助递送抗原、活化抗原递呈细胞(apc)并引发机体免疫细胞的活化与分化的非特异性免疫刺激分子。
理想的免疫佐剂必须具备以下特征:1.安全性好;2.增强弱免疫原性疫苗的免疫原性;3.增进免疫接触,增强机体的免疫应答;4.减少抗原接种剂量和接种次数;5.加快免疫应答的速度和延长持续时间等等。
常见的免疫佐剂有铝佐剂和弗氏佐剂两种。铝佐剂是第一种fda批准用于临床治疗的人用佐剂,但其诱导细胞免疫能力较弱,且会引发局部炎症。而弗氏佐剂主要应用为动物疫苗佐剂,毒副作用较大。因此研究开发新型、安全并且能有效诱导细胞和体液免疫的免疫佐剂具有重大的意义。
壳聚糖及其衍生物由于具有良好的生物相容性、生物可降解性、生物粘附性、免疫刺激活性、缓释控释、靶向性等优点,近年来已成为世界范围内免疫佐剂的研究热点。然而,壳聚糖的水溶性较差,只溶于稀酸,这严重限制了其在生物医药领域的应用。
技术实现要素:
为了克服现有的壳聚糖及其衍生物水溶性差的问题,本发明的首要目的在于提供一种季鏻化壳聚糖,采用酰胺反应合成,其水溶性良好,能溶于水和生理盐水中。
为了克服现有的免疫佐剂诱导细胞免疫能力较弱和毒副作用较大的缺陷,本发明的另一目的在于提供上述的季鏻化壳聚糖作为疫苗免疫佐剂的应用,季鏻化壳聚糖作为疫苗免疫佐剂可以提高机体特异性免疫应答。
本发明的目的通过下述技术方案实现:
一种季鏻化壳聚糖的制备方法,包括以下步骤:
(1)将壳聚糖(cs)和1-羟基苯并三唑(hobt)加入到水/二甲基亚砜混合液中,冰浴条件下搅拌2-3h,然后调节混合物的ph值至4.8-5.5;再加入3-羧丙基三苯基溴化磷(ctpb),搅拌至完全溶解;
(2)将1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐(edc·hcl)溶解于水/二甲基亚砜混合液中,然后加入到步骤(1)的反应体系中,反应1-2天,产物用丙酮/乙醚混合液进行沉淀,再将沉淀产物真空干燥1-2天后溶于超纯水中,并于超纯水中透析3-4天,冷冻干燥后得到季鏻化壳聚糖(npcs);
上述步骤中,壳聚糖的糖单元、hobt、ctpb、edc·hcl四者的摩尔比为1:2:1:2;
所述的水/二甲基亚砜混合液中,水与二甲基亚砜的体积比优选(1-2):1;
所述的丙酮/乙醚混合液中,丙酮与乙醚的体积比优选2:1。
由上述方法制得的季鏻化壳聚糖,其水溶性提高了,能溶于水和生理盐水中。
由于具有良好的生物相容性和免疫刺激活性,同时水溶性提高了,上述的季鏻化壳聚糖可以作为疫苗免疫佐剂使用,能显著提高机体特异性免疫应答;
所述的疫苗中,季鏻化壳聚糖与抗原的质量比为2:1;
所述的抗原优选卵清蛋白(ova),疫苗治疗免疫方式为腿部肌肉注射。
壳聚糖在免疫佐剂领域具有不俗的应用潜力,但是其较差的水溶性限制了其应用。为此,壳聚糖接枝上小分子季鏻盐,水溶性大大改善。
季鏻化壳聚糖作为佐剂用于疫苗治疗具有以下的优势:1.来源丰富、制备简单、生物安全性良好;2.水溶性好,便于免疫疫苗制剂的生产制备;3.生物粘附性好,且带丰富的正电荷,可高效包裹带负电荷的抗原,并通过静电相互作用粘附于带负电荷的细胞膜,使抗原更有效的被抗原递呈细胞(apc)识别、摄取;4.纳米尺寸,易于被apc识别和摄取,易于被细胞吞噬,有利于诱导机体的免疫应答;5.能够有效保护抗原免受体内的酸、碱、蛋白酶等破坏,提高抗原的利用率。
本发明研究发现,当将季鏻化壳聚糖/抗原疫苗制剂免疫于机体时,该疫苗递送系统能对抗原进行缓释,使机体不断接受免疫刺激从而诱导长期有效的免疫应答。
本发明相对于现有技术具有如下的优点及效果:
1、季鏻化壳聚糖具有良好的生物相容性,且合成简单、成本低廉,经济环保。同时,本发明改性后的季鏻化壳聚糖具有良好的水溶性,便于制备疫苗制剂。
2、本发明首次采用季鏻化壳聚糖作为免疫佐剂,季鏻化壳聚糖能促进dc2.4细胞对抗原的摄取,促进脾细胞增殖,诱导更高水平的抗原特异性igg抗体效价、ifn-γ、il-4和il-10,因此在疫苗治疗领域具有重要的应用价值。
附图说明
图1是季鏻化壳聚糖和壳聚糖的接触角实验结果图。
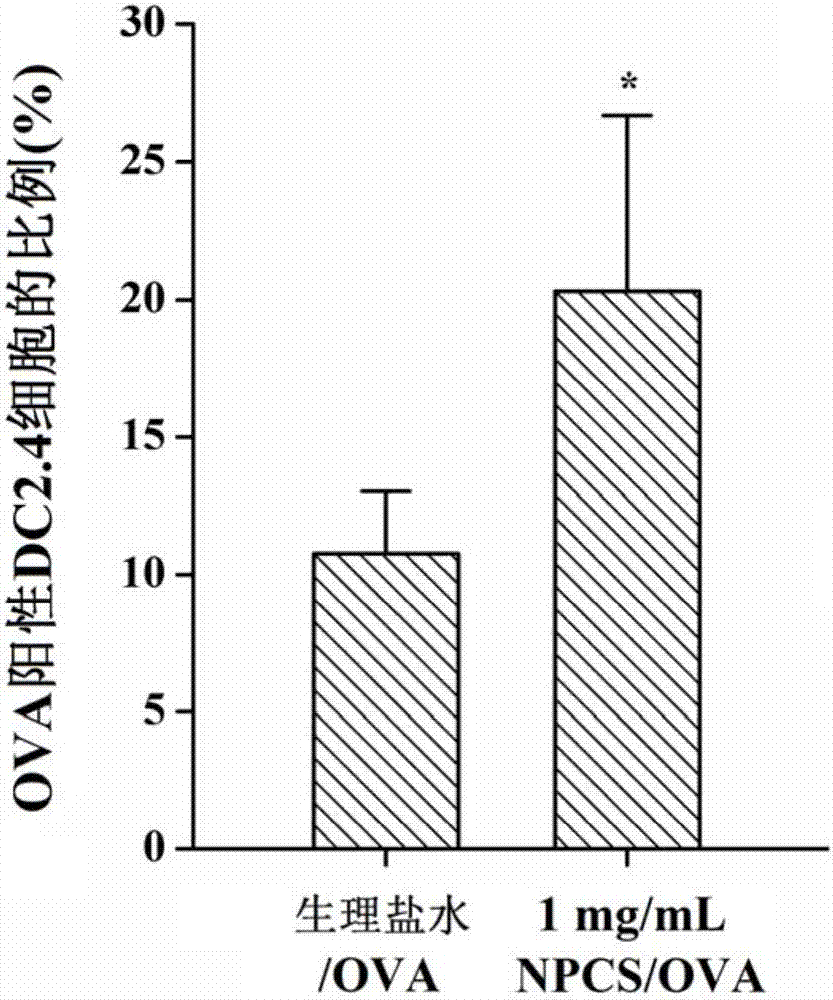
图2是dc2.4细胞对ova的摄取结果图。
图3是免疫组织化学染色的结果图。
图4是igg抗体效价的测定结果图。
图5是脾细胞的体外增殖实验结果图。
图6是ifn-γ的分泌实验结果图。
图7是il-12的分泌实验结果图。
图8是il-4的分泌实验结果图。
图9是il-10的分泌实验结果图。
具体实施方式
下面结合实施例及附图对本发明作进一步详细的描述,但本发明的实施方式不限于此。
实施例1
一种季鏻化壳聚糖,由以下步骤制得:
往250ml三口烧瓶中分别加入400mg壳聚糖(cs)和664mghobt,再加入30mlh2o/dmso(v/v=2/1)的混合液,冰浴条件下搅拌2.5h。随后调节ph值至4.8-5.5。再加入1.052gctpb(3-羧丙基三苯基溴化磷),搅拌至完全溶解。将940mgedc·hcl溶解于10mlh2o/dmso(v/v=1/1)的混合液,加入烧瓶中并搅拌反应24h。产物用丙酮/乙醚(v/v=2/1)的混合液进行沉淀,再将沉淀产物真空干燥24h后溶于超纯水中,并于超纯水中透析3天,冷冻干燥后得到季鏻化壳聚糖(npcs)。
壳聚糖(cs)与本实施例制得的季鏻化壳聚糖(npcs)的接触角实验:将壳聚糖(cs)与本实施例制得的季鏻化壳聚糖(npcs)制成溶液,滴于玻璃片上,铺匀,真空干燥制成薄膜,再用接触角测量仪(dsa100,kruss)测定。
结果如图1所示,cs的接触角为74.5°,而npcs的接触角为26.6°。接触角越小,则亲水性增强,这说明npcs的亲水性优于cs。
实施例2
上述的季鏻化壳聚糖作为疫苗免疫佐剂的应用:
一、制备疫苗制剂
以卵清蛋白ova为模型抗原,不同配方的疫苗按以表1进行配制,然后对小鼠进行肌肉注射。
表1肌肉注射用的疫苗制剂
二、小鼠免疫方案
肌肉注射:6-8周的雌性balb/c小鼠随机分成6组,每组5只;分别于第0、10、20天腿部注射100μl疫苗溶液(每次注射含50μgova,每只腿注射一半剂量)。第三次免疫10天后,取血,分离血清,-20℃下保存备用;取小鼠脾脏,研磨、重悬制备不同浓度的脾细胞悬浮液,备用。
三、各项免疫指标的测定
1.dc2.4细胞对ova的摄取
往24孔板中加入dc2.4细胞悬液(1×105cells/孔),于37℃,5%co2培养24h。cy5.5标记的ova分别与dmem基础培养基和npcs溶液混匀,然后每孔加入500μl,以dmem基础培养基为空白对照,每组三个平行,于37℃,5%co2培养6h。消化并收集细胞,然后用pbs洗涤和重悬。通过流式细胞仪检测dc2.4细胞在体外对抗原的摄取情况。
结果如图2所示,与阴性对照相比,1mg/mlnpcs/ova的疫苗制剂显著增强dc2.4细胞对抗原的摄取。这说明在npcs存在的情况下,dc2.4细胞对抗原的摄取显着增加,这有利于dc2.4细胞捕获并递呈更多的抗原,从而诱导更强烈的免疫应答。
2.免疫组化试验
分为4组(n=4),并用100μl不同的疫苗制剂(每只小鼠50μgova,每条腿半剂量)进行肌内免疫。在免疫后2或7天,对小鼠实施安乐死,并手术分离脾脏,固定在10%甲醛中,石蜡包埋,并在聚赖氨酸包被的载玻片上切成4μm厚的切片。根据制造商的说明书进行免疫组织化学染色。
结果如图3所示,含有npcs和弗氏佐剂的疫苗制剂在免疫后第2天和第7天均可在免疫小鼠的脾脏中检测到大量的抗原,而用阴性对照免疫的小鼠的脾脏中在第7天仅检测到少量的抗原。结合荧光活体成像结果,免疫组化结果进一步表明在npcs的帮助下,抗原从注射部位缓释并逐渐转移到脾脏中,从而增加脾脏中的抗原可利用性,进而诱导更有效的免疫应答。
3.igg抗体效价的测定
用10μg/ml的ova抗原包被液包被96孔板,4℃包被过夜。然后用的pbs-t洗板1次,在每孔中加入200μl的封闭液置于37℃的摇床上孵育1h。然后用pbs-t洗板3次,加入100μl小鼠血清稀释液,置于37℃的摇床上孵育1h。然后用pbs-t洗板3次,并在所有孔中加入50μlhrp标记的抗小鼠igg二抗,在37℃的摇床上孵育1h。然后用pbs-t洗板4次,每孔加入100μl的tmb显色液,在室温下避光孵育15min。随后每孔加入100μl的终止液。立即用酶标仪在450nm处检测吸收值。
结果如图4所示,与阴性对照相比,1mg/ml的npcs和阳性对照存在极显著差异(p<0.001)。这说明npcs能够有效地增强机体的体液免疫应答,提升igg的分泌水平。
4.脾细胞增殖实验
在96孔板中,每孔加100μl脾细胞悬液(2×106cells/ml),分别加100μl的卵清蛋白溶液(浓度为100μg/ml,rpmi1640基础培养液)或rpmi1640基础培养液(空白对照),每组3个平行。37℃、5%co2培养72h后,向每孔加入20μlcck-8溶液,将96孔板在培养箱内孵育4h,用酶标仪测定在450nm处的吸光度。
结果如图5所示,阴性对照组作用下的脾细胞增殖指数大约为1.2,相比之下,npcs/ova刺激的脾细胞增殖指数达到1.5左右,与阳性对照相当,均存在极显着性差异。这表明npcs可以有效地促进脾细胞增殖,从而增强免疫应答。
5.elisa测定脾细胞分泌的细胞因子水平
在24孔板中,每孔加750μl脾细胞悬液(2x106cells/ml),分别加750μl的卵清蛋白溶液(浓度为100μg/ml,rpmi1640培养液),每只小鼠脾细胞1个孔。37℃,5%co2培养60h,收集细胞悬液到1.5mlep管中,2000r/min,离心5min,收集上清,-80℃保存备用。通过elisa法测定脾细胞ifn-γ、il-12、il-10和il-4细胞因子水平。
结果如图6-9所示,与阴性对照相比,npcs/ova制剂诱导脾细胞分泌的il-12水平无统计学意义的显著性差异,而ifn-γ的分泌水平则显著增强,具有显著性差异。此外,npcs/ova制剂诱导il-4和il-10的分泌水平显着高于阴性对照。综上所述,npcs诱导的ifn-γ、il-4和il-10的分泌水平明显增加,特别是th1细胞因子(主要是ifn-γ)的分泌水平稍微强于th2细胞因子(主要是il-10)。
综上所述,本发明制得的季鏻化壳聚糖(npcs)的水溶性良好,与ova制成了不同的疫苗制剂,并对小鼠进行肌肉注射。结果表明,基于1mg/mlnpcs的制剂能够显著增强dc2.4细胞对抗原的摄取、脾细胞增殖、igg水平和细胞因子分泌(ifn-γ,il-10和il-4)。这主要归功于npcs对抗原的保护和缓释能力,有利于dcs摄取和递呈更多的抗原,产生更强的免疫应答。总之,npcs有潜力应用于肌内免疫的疫苗递送系统。
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!