一种十六核锰簇合物及其合成方法和应用与流程
本发明涉及一种十六核锰簇合物及其合成方法和应用,属于磁性材料技术领域。
背景技术:
有着规则形状和大孔穴的金属有机分子笼是当前配位化学领域的研究热点之一,因其不仅仅有着迷人的结构,且在分离和贮存、分子识别、客体交换、催化、磁性、传感技术等领域有着诱人的潜在应用价值而受到许多课题组的关注。
n-酰化水杨酰肼配体是一类配位模式丰富多样的多齿配体,其本身具有抗菌的生物活性,引入此类配体构筑的分子笼可能对其潜在的应用性能产生影响。但目前尚未见有以n,n’-二(水杨酰基)-(e)-丁烯二酰肼为配体合成的笼状十六核锰簇合物[mnⅱ4mnⅲ12(l)6(μ3-o)4(h2o)6(py)6]·h2o的相关报道。
技术实现要素:
本发明要解决的技术问题是提供一种结构新颖的十六核锰簇合物及其合成方法和应用。
本发明所述的十六核锰簇合物,其化学式为:[mnⅱ4mnⅲ12(l)6(μ3-o)4(h2o)6(py)6]·h2o,其中l表示n,n’-二(水杨酰基)-(e)-丁烯二酰肼脱去六个氢原子,带六个单位的负电荷;该簇合物属于单斜晶系,c2/c空间群,晶胞参数为:
申请人在研究中发现,本发明所述的十六核锰簇合物具有如下的磁学性质:分子内锰离子间存在反铁磁交换作用,其整体表现为顺磁性。此外,本申请人在研究中还发现,本发明所述族合物对气体物质具有良好的吸附作用。因此,本发明还包括上述十六核锰簇合物在制备磁性材料中的应用;以及十六核锰簇合物在制备吸附气体物质的吸附剂中的应用,更具体的说是在制备吸附二氧化碳气体的吸附剂中的应用。
本发明所述的十六核锰簇合物的合成方法为:取n,n’-二(水杨酰基)-(e)-丁烯二酰肼和mn(oac)2·4h2o用混合溶剂溶解,之后用吡啶调节所得溶液的ph=5.5~6.3,所得混合液置于容器中,经液氮冷冻后抽至真空,熔封,然后于加热条件下反应,反应物冷却,有晶体析出,即得目标产物;所述的混合溶剂为n,n’二甲基甲酰胺和甲醇的组合物。
在具体的合成过程中,申请人发现:
1)吡啶不仅仅起到调节溶液ph的作用,同时也参与了配位,其部分取代水分子参与配位。
2)吡嗪的加入对目标产物的生成起着至关重要的作用,申请人在合成时尝试不加吡嗪,反应所得的料液中无晶体生成。
3)虽然金属盐中的阴离子没有参与配位,但对生成目标产物却起到了关键作用,当我们换用不同的金属锰盐如甲酸锰、高氯酸锰、氯化锰或硫酸锰等,采用低温或高温溶剂热法、扩散法、常规溶液法均得不到晶体,可见,阴离子对晶体的合成有重要影响。
上述合成方法中,n,n’-二(水杨酰基)-(e)-丁烯二酰肼和mn(acac)3的摩尔比通常为化学计量比,具体可以是1:3~4,优选为1:2。所述n,n’-二(水杨酰基)-(e)-丁烯二酰肼、mn(acac)3和吡嗪的物质的量之比为1:2~3:0.2~0.5。
上述合成方法中,所述的混合溶剂中,n,n’二甲基甲酰胺和甲醇的体积比可以为任意配比,优选为1~3:1~3,较佳的选择为1:3、1:2或1:1。所述混合溶剂的用量可根据需要确定,通常以能溶解参加反应的原料为宜。具体地,以0.1mmol的n,n’-二(水杨酰基)-(e)-丁烯二酰肼为基准计算,全部原料所用混合溶剂的总用量一般为4~5ml。在具体溶解的步骤中,可将n,n’-二(水杨酰基)-(e)-丁烯二酰肼、mn(acac)3和吡嗪分别用混合溶剂中的一种成分溶解,再混合在一起反应,也可将n,n’-二(水杨酰基)-(e)-丁烯二酰肼、mn(acac)3和吡嗪混合后再加混合溶剂溶解。
上述合成方法中,优选调节溶液的ph=5.8~6.0。
上述合成方法中,所述反应优选是在60~120℃条件下进行,在上述温度条件下进行反应的时间通常为30~80h,也可以大于80h;优选是将反应时间控制在60~80h。反应更优选是在80~120℃条件下进行。通常采用一端封闭的厚壁硬质玻璃管来盛装调节ph值后所得的混合液。
本发明所述合成方法中涉及的n,n’-二(水杨酰基)-(e)-丁烯二酰肼可以参考现有文献(n.sreenivasachary;d.t.hickman;d.sarazin,etal.dynas:constitutionaldynamicnucleicacidanalogues[j].chemistry,2006,12(33):8581-8588.)进行合成,或者是自行设计路线合成。
与现有技术相比,本发明提供了一种结构新颖的十六核锰簇合物[mnⅱ4mnⅲ12(l)6(μ3-o)4(h2o)6(py)6]·h2o及其合成方法,合成方法简单、成本低廉、重复性好;申请人在研究中发现该簇合物分子内锰离子间存在反铁磁交换,可以用于制备磁性材料;还发现该簇合物对二氧化碳气体具有良好的吸附作用,可用于制备吸附二氧化碳气体的吸附剂。
附图说明
图1为本发明各实施例使用的配体n,n’-二(水杨酰基)-(e)-丁烯二酰肼的红外光谱图;
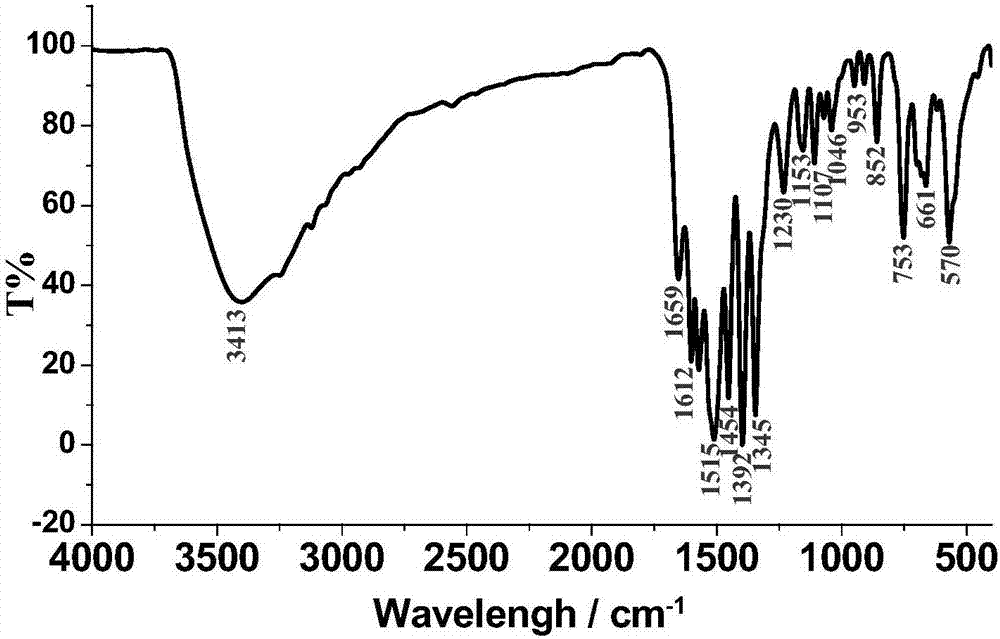
图2为本发明实施例1制得的最终产物的红外光谱图;
图3为本发明实施例1制得的最终产物的分子结构图;
图4为本发明实施例1制得的最终产物的热重曲线图;
图5为本发明实施例1制得的最终产物的变温磁化率图;
图6为本发明实施例1制得的最终产物在常压下对co2的吸附曲线图。
具体实施方式
下面结合具体实施例对本发明作进一步的详述,以更好地理解本发明的内容,但本发明并不限于以下实施例。
以下各实施例中涉及的n,n’-二(水杨酰基)-(e)-丁烯二酰肼(以下简称为配体或l)采用以下方法合成,其合成路线如下:
称取(e)-丁烯二羧酸(11mmol,1.8g)加入到250ml的圆底烧瓶中,缓慢滴加25mlsocl2,95℃条件下搅拌回流5小时后滴加半滴dmf,减压蒸馏得黄色稠状液体,再将其溶解在15mlthf中。同时将水杨酰肼(23.0mmol,3.6g)溶解在75mlthf溶液中,冰浴下将两者混合搅拌,逐滴加入2.5ml三乙胺,继续冰浴搅拌5h后转至室温搅拌反应三天,得浅黄色沉淀,过滤,用thf,少量水,无水乙醚洗涤,粗产品用dmf和h2o的混合溶液重结晶,真空干燥,得到目标产物,产率为70%。配体(c18h16n4o6)元素分析(%)理论值:c,56.25;h,4.20;n,14.58。实验值:c,56.24;h,4.04;n,13.98。红外光谱如图1所示,数据如下:ir(kbrpellet,cm-1):3370(m),3539(m),3231(m),2743(w),2590(w),1706(m),1614(vs),1490(vs),1316(m),1218(m),1156(m),974(s),877(m),821(m),731(m)。由红外谱图可知,配体在3539cm-1处的的吸收峰可归属为水分子的伸缩振动υ(ho-h),3231cm-1处宽的的吸收峰为酰胺基的ν(n-h)伸缩振动,2743cm-1处的吸收峰归属为酚羟基ν(o–h)伸缩振动,在1706cm-1处有吸收峰,可归属为羰基c=o的伸缩振动ν(c-o)峰,1614cm-1处的吸收峰归属为丁烯中c=c的特征吸收峰,1316cm-1处的吸收峰为–c-nh–nh-c–基团的伸缩振动ν(c-n)峰,1218cm-1处的吸收峰可归属为酚基伸缩振动ν(c–o),1490cm-1、1156cm-1、974cm-1、877cm-1、731cm-1处的吸收峰为苯环的特殊吸收峰。
实施例1
称取配体(0.025mmol,0.0096g),mn(acac)3(0.05mmol,0.0125g)和吡嗪(0.01mmol,0.008mg),然后将它们加入到长为22cm且一端封闭的pyrex管中,滴加由0.3mldmf和0.9ml甲醇组成的混合溶剂,之后再滴加4滴吡啶,摇匀(此时溶液的ph=5.9)。将该pyrex管抽真空,并封好另一端口,置于80℃条件下反应72h,取出,将其缓慢冷却至室温,析出黑色块状晶体,产率:50%。(c138h104mn16o47n30)元素分析(%),理论值:c,43.46;h,2.75;n,11.02;实验值:c,43.40;h,2.80;n,11.08。
对实施例1所得产物进行表征:
1)红外表征:
用美国nicolet360ft-ir型傅立叶变换红外光谱仪(kbr压片),对本实施例制得的产物进行红外分析,摄谱范围4000~400cm-1,所得红外光谱谱图如图2所示,数据如下:
ir(kbrpellet,cm-1):3413(m),1659(w),1612(m),1515(vs),1454(m),1392(vs),1345(s),1230(m),1107(m),953(w),852(m),753(s)。
2)晶体结构分析:
通过安捷伦公司supernova单晶衍射仪进行测定表面结构完好的黑色块状晶体以确定其单晶结构,所得晶体学参数数据见下述表1,键长键角数据见下述表2。
表1:簇合物[mnⅱ4mnⅲ12(l)6(μ3-o)4(h2o)6(py)6]·h2o的晶体学参数见表
表2:簇合物[mnⅱ4mnⅲ12(l)6(μ3-o)4(h2o)6(py)6]·h2o的部分键长
x-射线单晶衍射分析表明,所得黑色块状晶体属于单斜晶系,c2/c空间群,是由十六个锰离子,六个配体l,六个配位的水分子,六个配位的吡啶分子,四个μ3-o,和一个水溶剂分子组成的笼状簇合物,与配合物3结构相似。通过platon软件计算,配合物4的孔穴率vvoid约27.6%,孔穴直径约为
所得黑色块状晶体的分子结构如图3所示。本实施所得产物中的十六个锰离子有两种不同的配位环境,全是六配位,十六个六配位的锰离子均处于扭曲的八面体构型,其中四个独立锰离子的配位环境相同,为[mnn3o3],配位原子来源相同。另一种锰离子由μ3-o桥连三个锰离子形成锰三角的配位环境相似,或是[mnno5],或是[mnn2o4],配位原子来源类似,其参与配位的六个原子分别来自一个配体l中一个水杨酰基上的氧原子,水杨酰肼的一个氮原子,反式丁烯酰基上的一个氧原子,另一个配体l的反式丁烯酰基上的一个氧原子、一个水分子上的氧原子或是一个吡啶分子上的氮原子、一个μ3-o原子,六个配位原子构成一个扭曲的八面体构型。其中,轴向位置被水杨酰基上的氧原子和反式丁烯酰基上的一个氧原子所占据,赤道平面上被一个水分子上的氧原子或者一个吡啶分子上的氮原子,反式丁烯酰基上的一个氧原子,水杨酰肼的一个氮原子和μ3-o原子所占据,锰三角的三个锰离子间的距离为分别为
通过对配合物的键价计算(bvs)和价态平衡进行考虑,四个独立的锰离子均为正二价,而十二个锰三角离子均为正三价,mnⅱ-n/o平均键长为
综上,确定所得的黑色块状晶体为本发明所述的十六核锰簇合物[mnⅱ4mnⅲ12(l)6(μ3-o)4(h2o)6(py)6]·h2o,其中l表示n,n’-二(水杨酰基)-(e)-丁烯二酰肼,该配体脱去六个氢原子,带六个单位的负电荷。
3)热重表征:
用法国塞特拉姆仪器有限公司labsysevotg-dsc/dta,对本实施例制得的十六核锰簇合物[mnⅱ4mnⅲ12(l)6(μ3-o)4(h2o)6(py)6]·h2o进行热重测试与分析,测试条件为:氮气氛围下,以10℃/min速率从室温升至1000℃,热分析结果如图4所示。
由图4可知,本实施例制得的十六核锰簇合物的的失重分为三个过程,从35到219℃发生第一次失重行为,失去总质量的10%,对应于化合物中游离的溶剂分子的失去;继续升温,在219–424℃时,发生第二次失重行为,对应于配合物配位水分子和吡啶分子的失去;在424–1000℃时发生最后一次失重行为,配合物框架逐渐坍塌。
4)磁学性质测定:
取36.7mg本实施例制得的十六核锰簇合物[mnⅱ4mnⅲ12(l2)6(μ3-o)4(h2o)6(py)6]·h2o碾碎后在磁性测试仪器上进行磁性测试,具体是在2–300k温度区间内,直流外磁场为h=1000oe条件下,测量其摩尔磁化率随温度的变化情况,所得簇合物的变温磁化率图(χm-t,χmt-t曲线图)如图5所示。
由图5可知,在300k时,簇合物实验测得的χmt的值是43.48cm3kmol-1,理论值为53.5cm3kmol-1[对于四个s=5/2的mn(ii)和十二个s=2的mn(ⅲ)],低于理论值,随着温度的降低χmt缓慢降低,在100k达到37.93cm3kmol-1,随后急剧降低,在2k时达到最小值4.81cm3kmol-1。且χm–1-t曲线遵从居里-外斯定律,对其拟合得到得到weiss常数θ=-20.88k,居里常数为c=45.54cm3kmol–1。χmt-t曲线趋势及负的weiss常数均表明配合物4中锰离子间存在反铁磁交换作用。
5)吸附性能研究
将所得产物样品晾干后置于吸附仪样品腔,在100℃条件下抽真空处理4h直至真空度接近至真空泵最大真空度。195k干冰浴条件下,样品co2常压吸附曲线如图6所示。
由图6可知,co2吸附曲线在低压区(p/p0<0.1)吸附量值随压力升高而迅速增大,随后,再缓慢增加,最终趋于平衡。1.0bar处最大吸附量为24.23cm3g-1。该簇合物的co2常压吸附曲线图有个回滞环出现,说明co2分子与主体框架之间存在一定的相互作用力。
实施例2
重复实施例1,不同的是:
1)将n,n’-二(水杨酰基)-(e)-丁烯二酰肼、mn(acac)3和吡嗪的物质的量之比更改为1:2:0.5;
2)混合溶剂中,将dmf和甲醇的体积比更改为1:2;
3)将溶液的ph值调至5.7。
取出pyrex管,降至室温,pyrex管底部有黑色块状晶体析出。产率47%。
对所得产物进行结构表征,确定产物为目标产物[mnⅱ4mnⅲ12(l)6(μ3-o)4(h2o)6(py)6]·h2o,其中l表示n,n’-二(水杨酰基)-(e)-丁烯二酰肼,该配体脱去六个氢原子,带六个单位的负电荷。
对所得产物的磁学性质表征可知所得产物中锰离子间存在反铁磁交换作用。
对所得产物的吸附性能研究表明所得产物对二氧化碳气体有较强的吸附作用。
实施例3
重复实施例1,不同的是:
1)将n,n’-二(水杨酰基)-(e)-丁烯二酰肼、mn(acac)3和吡嗪的物质的量之比更改为1:3:0.2;
2)混合溶剂中,将dmf和甲醇的体积比更改为1:1;
3)将调好ph值的混合液置于80℃条件下反应100h。
取出pyrex管,降至室温,pyrex管底部有黑色块状晶体析出。产率51%。
对所得产物进行结构表征,确定产物为目标产物[mnⅱ4mnⅲ12(l)6(μ3-o)4(h2o)6(py)6]·h2o,其中l表示n,n’-二(水杨酰基)-(e)-丁烯二酰肼,该配体脱去六个氢原子,带六个单位的负电荷。
对所得产物的磁学性质表征可知所得产物中锰离子间存在反铁磁交换作用。
对所得产物的吸附性能研究表明所得产物对二氧化碳气体有较强的吸附作用。
实施例4
重复实施例1,不同的是:
1)将溶液的ph值调至6.1。
2)混合溶剂中,将dmf和甲醇的体积比更改为1:3;
3)将调好ph值的混合液置于120℃条件下反应30h。
取出pyrex管,降至室温,pyrex管底部有黑色块状晶体析出。产率49%。
对所得产物进行结构表征,确定产物为目标产物[mnⅱ4mnⅲ12(l)6(μ3-o)4(h2o)6(py)6]·h2o,其中l表示n,n’-二(水杨酰基)-(e)-丁烯二酰肼脱去六个氢原子,带六个单位的负电荷。
对所得产物的磁学性质表征可知所得产物中锰离子间存在反铁磁交换作用。
对所得产物的吸附性能研究表明所得产物对二氧化碳气体有较强的吸附作用。
实施例5
重复实施例1,不同的是:
1)将溶液的ph值调至5.6。
2)将调好ph值的混合液置于60℃条件下反应48h。
取出pyrex管,降至室温,pyrex管底部有黑色块状晶体析出。产率41%。
对所得产物进行结构表征,确定产物为目标产物[mnⅱ4mnⅲ12(l)6(μ3-o)4(h2o)6(py)6]·h2o,其中l表示n,n’-二(水杨酰基)-(e)-丁烯二酰肼脱去六个氢原子,带六个单位的负电荷。
对所得产物的磁学性质表征可知所得产物中锰离子间存在反铁磁交换作用。
对所得产物的吸附性能研究表明所得产物对二氧化碳气体有较强的吸附作用。
- 还没有人留言评论。精彩留言会获得点赞!