用于检测胆道闭锁患儿血浆miR‑140‑3p的引物组及包含该引物组的检测试剂盒的制作方法
本发明涉及引物及试剂盒,具体涉及用于检测胆道闭锁患儿血浆mir-140-3p的引物组及包含该引物组的检测试剂盒。
背景技术:
胆道闭锁(biliaryatresia,ba)是婴幼儿时期引起胆汁淤积性黄疸的常见疾病。ba是累及肝内外胆道系统的进行性炎性病变,最终导致肝外甚至肝外胆管消失,出现肝脏纤维化、门静脉高压等并发症,最终危及患儿生命。若不予早期及时手术治疗,自然死亡率可达100%。故早期筛查、诊断以及肝纤维化评估对ba患儿预后、有效降低地区新生儿死亡率有重要意义。然而目前ba依然缺乏特异且有效的实验室诊断和筛查指标,如何能够早期且无创性诊断仍是世界性难题。
mirna是近年来新发现的具有多基因调控功能的非编码单链小rna,在细胞生长、代谢、增值、分化、细胞凋亡、病毒感染、肿瘤发生等生物学功能中发挥重要的作用。研究证明外周血循环中存在着丰富且稳定的mirna。循环mirna在血清/血浆等体液中以稳定的形式存在。有研究提示mirna在ba的发生发展过程中起重要作用,涉及到疾病相关免疫细胞的发育分化,细胞表面分子的表达及细胞因子的释放,也可通过肝胆细胞的增值、凋亡、代谢等相关通路影响ba肝纤维化的进展。这就使得循环mirna这一无创性的检查作为ba的早期诊断、病理分级、预后评估和发病机制的研究开启了新的思路。发明在前期通过对ba患儿、胆汁淤积性患儿及健康婴幼儿的血浆进行高通量测序分析,发现mir-140-3p在ba患儿中特异性下调。
目前,mirna的检测方法有多种,包括northernblot技术、原位杂交技术、实时荧光定量pcr技术、微阵列芯片技术以及最新的高通量测序技术。其中northernblot是用于rna检测的早期手段之一,但其检测的敏感性和特异性较低,当血浆样本中rna含量低或存在rna降解时,可能检测不到。并且操作步骤繁琐,不适用于高通量分析。原位杂交技术主要用于检测细胞水平和组织水平mirna的分布情况,并进行半定量分析,但是不能准确的检测低表达量的mirna是其不足之处。微阵列芯片技术是一种高通量的检测技术,能同时检测一种或多种样本中大量的大量的mirna,单芯片上不同的探针分子和待测分析之间容易发生交叉反应,使得测定结果准确性低,重复性差。新一代的高通量测序技术准确度高、可重复性好,但是检测成本高,不利于推广。
实时荧光定量pcr(rt-qpcr)技术是目前最常用的基因检测技术之一,具有灵敏度高、特异性好,操作方法简便快捷等优点。rt-qpcr包括rna的逆转录和下游的pcr两部分,逆转录根据引物设计的不同分为poly(a)聚合加尾法和茎-环状引物反转录法。荧光定量pcr两部分分为染料法和探针法,探针法虽特异性好,但是每种mirna都需要设计相对应的taqman探针,成本高,不利于推广应用。染料法基于-环状结构的逆转录引物能特异识别并扩增成熟的miran序列,且经济实惠。
技术实现要素:
本发明的目的之一是提供一种用于检测胆道闭锁患儿血浆mir-140-3p的引物组。
本发明的目的之二是提供包含上述引物组的检测试剂盒。
本发明的引物组是根据ba中低表达的mir-140-3p基因序列进行设计的。在本发明中,所述的引物组为:
逆转录引物(rtprimer):
gtcgtatccagtgcagggtccgaggtattcgcactggatacgacccgtgg
正向引物(forwardprimer):tgccgtaccacagggtagaac
反向引物(reverseprimer):cagtgcagggtccgaggtat。
本发明提供的包含上述引物组的检测试剂盒,包括rna提取试剂瓶、茎环逆转录试剂瓶和荧光定量pcr试剂瓶。
rna提取试剂瓶内装血浆rna提取试剂,茎环逆转录试剂瓶内装茎环装逆转录试剂、荧光定量pcr试剂瓶内装荧光定量pcr试剂。
所述荧光定量pcr试剂包括如下组份:
所述rna提取试剂盒包括以下组份pssolutiona(psa)、pssolutionb(psb)、pssolutionc(psc)、清洗溶液(washsolution)、rna洗脱液(rnaelutionsolution)、迷你过滤离心柱(minifilterspincolumns)、收集管(collectiontubes)、洗脱管(elutiontubes)。进一步地还可包括95%的乙醇和β-巯基乙醇。
所述茎环逆转录试剂包括以下组份5×primescriptbuffer、primescriptrtenzymemixⅰ、rnasefreedh2o,2μm的rna逆转录引物seqidno:1。
本发明的有益效果:
1.本发明提供的用于检测mir-140-3p的荧光定量pcr的引物组及试剂盒的特异性和敏感性高,能应用于荧光定量pcr中快速特异检测血浆中mir-140-3p的含量,与传统的northernblot相比,特异性和敏感性更高,与mirna芯片相比,价格成本低。
2.基于.本发明提供的用于检测mir-140-3p的荧光定量pcr的引物组及试剂盒建立血浆mir-140-3p的荧光定量pcr,适用于芯片及高通量测序筛选出mir-140-3p后期临床样本的验证研究以及mir-140-3p在不同领域的差异性表达,推动了mir-140-3p与相关疾病的研究。
附图说明
图1是实时荧光定量pcr检测血浆mir-140-3p的扩增图;
扩增曲线均成“s”型,每个扩增曲线的ct值都小于35,数据有效可信。
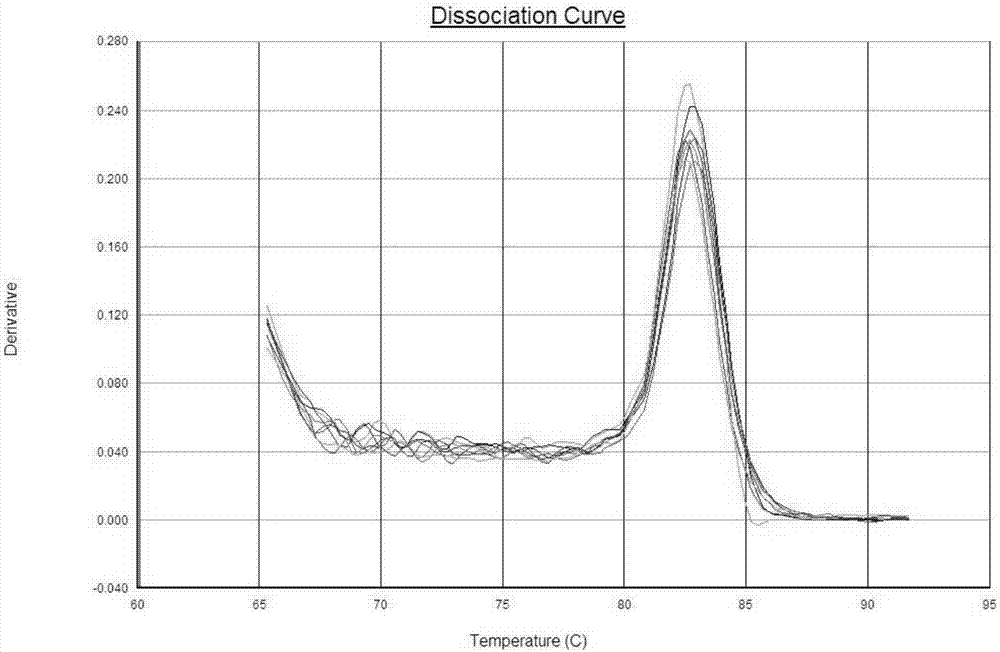
图2是实时荧光定量pcr检测血浆mir-140-3p的熔解曲线图;
mir-140-3p溶解曲线上显示溶解温度的峰值是82.7℃,溶解温度较均一,峰形较锐利,且均为单峰,提示无非特异性扩增,引物特异性良好。
图3是实时荧光定量pcr检测血浆中不同mirna表达量对比图;
nc表示正常对照组,dc表示胆汁淤积性疾病对照组,ba表示胆道闭锁组;a.与nc组相比,p<0.05,b.与dc组相比,p<0.05。
图4是胆道闭锁患儿与非胆道闭锁对照组中血浆mir-140-3p的roc曲线。
具体实施方式
下面结合具体实施例和附图对本发明作进一步详细说明。本实施案例在以本发明技术为前提下进行实施,现给出详细的实施方式和具体的操作过程,但本发明的保护范围不限于以下的实施例。
一、实施样本的高通量测序
1.测序样本分组采用“混合池”的方法对样本进行分组混合,将收集的9例ba患儿按年龄、性别分为a1~3三组(3人/组),9例正常对照儿童按年龄和性别与病例组匹配后同样分成n1~3三组;将组内的3例血浆样本等体积(200ul:200ul:200ul)混合为1份样本,最终分别得到3个疾病组和3个正常对照组血浆混合池样本。
2.血浆总rna提取按照试剂盒说明书(norgen42800)提取每组血浆总rna,以hsa-mir-16、hsa-mir-192为内参,用qrt-pcr对rna样本进行建库前质控;取通过质控检测的样本进入下游的文库构建实验。
3.文库构建使用illuminatruseqsmallrnapreparationkit试剂盒参照试剂盒说明illumina’struseqsmallrnasamplepreparationguide构建小rna测序文库。样本提取总rna后,利用mirna的属性,即5'端为磷酸基团,3'端为羟基集团,首先利用t4rna连接酶2(t4rnaligase2)将一个腺苷化单链dna3'端接头和5'端接头相继连接到小rna上。带有3'和5'连接接头的小rna序列,通过3端互补的rt引物进行反转录反应,最后进行pcr扩增cdna序列,用6%pega胶回收140-160bp碱基长度的pcr产物,完成cdna文库的制备工作。建库完成后,用bioanalyzer2100对文库的质量进行检测。
4.测序cdna经纯化后生成illumina,sclusterstation上的cluster即可加入测序仪(illuminahiseq2000)进行测序,测序过程中使用软件实时分析测序图片(illumina’ssequencingcontrolstudiosoftwareversion2.8,scsv2.8),提取原始数据用于基本数据分析(illumina’sreal-timeanalysisversion1.8.70,rtav1.7.8.0),测序输出的数据为程序读出的读段数据(reads)。
5.结果分析与处理以acgt101-mirv4.2(lcsciences)软件对两组样品的测序数据进行分析,通过获取非冗余序列和统计拷贝数目,得到可比对数据等基本分析,然后采用bowtie比对软件鉴定已知的mirna,以unafold二级结构折叠预测全新的mirna序列,同时对mirna的表达量进行归一化处理,组间mirna差异分析采用t检验,p<0.05被认为有统计学意义;采用excel2003软件对结果进行相关性分析和统计,得出差异倍数,筛选出差异显著的mirna;最后用mev4.0软件对差异显著的mirna进行聚类分析。采用在线工具targetscan,miranda和pita对差异mirna进行相关功能的初步预测。
6.根据高通量测序结果筛选出有表达显著差异的mirna用rt-qpcr进行进一步验证:
满足上述条件的mirna有6个,包括ba中高表达的mir-122-5p、mir-100-5p和低表达的mir-140-3p、mir-10b-5p、mir-26a-5p、mir-126-3p。
二、rt-qpcr验证样本
取经术中胆道造影和术后病理组织学检查证实为ba患儿的血浆样本44例(胆道闭锁组,ba组)。同ba组年龄相匹配并确诊为婴儿肝炎综合症患儿血浆样本15例、胆总管囊肿5例、citrin基因缺陷导致的新生儿肝内胆汁淤积症患儿(niccd)5例(疾病对照组,dc组)和同期进行常规体检,各项检查结果均正常,并且与ba患儿组年龄相匹配的健康婴幼儿血浆样本20例(正常对照组,nc组)。
具体步骤如下:
(一)血浆总rna的提取
采用循环rna提取试剂盒(norgen42800)提取血浆rna。
操作步骤:
1.从-70℃冰箱取出血浆至冰上解冻,解冻完全后,5000rpm离心3min,吸取上清0.5ml至15ml离心管中,静置。
2.在15ml离心管中,对应于每0.5ml血浆样品加入0.2ml的pssolutiona和0.8ml的pssolutionb(在加入β-巯基乙醇后使用,每1mlpssolutionb中加入10μlβ-巯基乙醇,现用现配)。涡旋15s混合均匀。
3.将步骤2中的混合液在60℃下温育10min。
4.在管中加入1.5ml的无水乙醇(自供),涡旋15s混合均匀。
5.1000rpm离心30s,小心倒出上清液,防止沉淀丢失。
6.加入0.3mlpssolutionc,涡旋15s混合均匀。
7.将步骤6中的混合液在60℃温育10min。
8.在管中加入0.3ml的无水乙醇,涡旋15s混合均匀。
9.将步骤8中的混合液加到试剂盒提供的柱上,14000rpm离心1mim,离心完后弃去收集管中的液体,将柱子重新装回到收集管中。
10.重复步骤9直到步骤8中的混合液全都转移到柱上。
11.加400μl的washsolution到柱上,14000rpm离心1min。弃去收集管中的液体,将柱子重新装回到收集管中。
12.重复步骤11两次,总的清洗次数为三次。
13.14000rpm空离3min,弃收集管。
将柱子转移到一个新的1.7ml的试剂盒提供的洗脱管中,加50μl的elutionsolution到柱中,2000rpm离心2min,然后14000rpm离心3min。洗脱管中的溶液即为rna溶液,如果不立即进行逆转录反应,将rna溶液置于-70℃保存待用。
(二)rna浓度和纯度的测定
上述提取的总rna可能含有dna或蛋白质等杂质,为保证后续逆转录反应和荧光定量pcr反应的顺利进行,对rna的浓度和纯度进行了检测,260nm/280nm介于1.65-2.15之间,浓度在7.2-12ng/μl之间。
(三)rna逆转录成cdna
将rna放于冰上,使用takara逆转录试剂盒(rr037a)进行逆转录,按试剂盒说明书进行操作。
(1)按下表逆转录体系加入反应试剂;
(2)在pcr仪上设置42℃15min→85℃5s→4℃保存进行逆转录反应,反应终产物即为cdna。如果立即进行荧光定量pcr扩增,则将所得产物放于4℃冰箱保存,否则放于-20℃冰箱保存,短期内待用。
rtprimer:gtcgtatccagtgcagggtccgaggtattcgcactggatacgacccgtgg(seqidno:1)
mirna逆转录成cdna的反应体系
(四)rt-qpcr检测mirna的表达量
采用
forwardprimer:tgccgtaccacagggtagaac(seqidno:2)
reverseprimer:cagtgcagggtccgaggtat(seqidno:3)。
4-1冰上融化反应试剂,在涡旋器上稍稍混匀并3000rpm离心2-3min。
4-2将试剂至于冰上,尽量在避光条件下配置体系,引入mir-16作为内参基因。正反向引物采用单一mirna特异性引物。
mir-16的引物组如下:
rtprimer:gtcgtatccagtgcagggtccgaggtattcgcactggatacgaccgccaa(seqidno:4)
forwardprimer:tggcgtagcagcacgtaaat(seqidno:5)
reverseprimer:cagtgcagggtccgaggtat(seqidno:6)。
在pcr8排连管中加入下列反应体系(注:需根据不同荧光定量pcr扩增仪选择不同的roxreferencedye),反应体积为20μl,每个样本设置3个复孔。
实时荧光定量pcr反应体系
4-3扩增按以下步骤在pcr仪上设置反应条件进行扩增:
预变性:1循环
95℃30s
pcr反应:40循环
95℃5s
60℃31s
溶解曲线:1循环
95℃15s
60℃1min
将配置好的混合液置于abi7300实时荧光定量pcr仪上,按上述设置的反应条件进行pcr反应,每次反应历经约2h。反应结束后,将pcr8排连管丢弃在pcr室指定的地方,根据扩增曲线和溶解曲线分析结果。
4-4实验结果分析得到循环阈值(ct值),采用δct值来表示样本中mirna的表达水平,应用相对定量分析方法(2-δδct)计算各组样本中目的mirna的相对表达量,其中δct=ct目的mirna-ctmir-16,δδct=δct疾病-δct对照。以疾病对照组和正常对照组目的mirna表达量为参照,计算ba组mirna的相对表达量。结合前期的高通量测序分析,mir-140-3p在ba患儿血浆中的表达量显著低于胆汁淤积性疾病对照组和正常对照组,差异均具有统计学意义(图3)。
4-5灵敏度和特异度分析mir-140-3p在阈值为0.083时,特异度为79.1%,灵敏度为66.7%(图4)。
4-6结论发明人发现mir-140-3p在ba患儿血浆中特异性表达,能作为ba和胆汁淤积性疾病和健康婴幼儿的鉴别诊断指标。采用本发明提供的特异性引物和试剂盒能够特异性地对mir-140-3p进行荧光定量检测。
序列表
<110>广州市妇女儿童医疗中心
<120>用于检测胆道闭锁患儿血浆mir-140-3p的引物组及包含该引物组的检测试剂盒
<160>6
<170>siposequencelisting1.0
<210>1
<211>50
<212>dna
<213>人工序列(artificial)
<400>1
gtcgtatccagtgcagggtccgaggtattcgcactggatacgacccgtgg50
<210>2
<211>21
<212>dna
<213>人工序列(artificial)
<400>2
tgccgtaccacagggtagaac21
<210>3
<211>20
<212>dna
<213>人工序列(artificial)
<400>3
cagtgcagggtccgaggtat20
<210>4
<211>50
<212>dna
<213>人工序列(artificial)
<400>4
gtcgtatccagtgcagggtccgaggtattcgcactggatacgaccgccaa50
<210>5
<211>20
<212>dna
<213>人工序列(artificial)
<400>5
tggcgtagcagcacgtaaat20
<210>6
<211>20
<212>dna
<213>人工序列(artificial)
<400>6
cagtgcagggtccgaggtat20
- 还没有人留言评论。精彩留言会获得点赞!