miR‑181a作为海洛因成瘾的生物标记物及其在制备抗海洛因复吸药物中的应用的制作方法
本发明属于基因工程技术领域,尤其涉及一种用于检测海洛因成瘾的生物标记物mir-181a及其在制备抗海洛因复吸药物中的应用。
背景技术:
药物成瘾(drugaddiction)作为一种慢性复发性脑部疾病,是一种严重危及人类健康并受全球关注的公共卫生问题,给社会和经济带来严重危害。海洛因作为传统阿片类毒品,在药物成瘾中扮演着重要角色。
海洛因作为阿片受体激动剂之一,主要通过激活位于中脑腹侧被盖区(ventraltegmentalarea,vta)gaba神经元阿片受体,通过突触前抑制,下调gaba神经元功能,使得多巴胺神经元脱抑制,释放多巴胺增加从而上调奖赏环路,导致海洛因成瘾的发生与发展。慢性海洛因使用会导致躯体和精神依赖,主要涉及了vta到伏隔核(nucleusaccumbens,nac)脑区多巴胺能投射系统的奖赏通路发生了适应性改变,如神经与突触结构和功能的可塑性改变。高复吸率是海洛因成瘾戒断的难点,目前还没有特别有效的干预方法,其原因之一是由于药物成瘾过程中,中枢神经系统发生了适应性改变,正常认知功能的损害导致冲动控制等行为的抑制功能减弱;另一方面是戒断综合征、心理渴求及一些生活事件等与毒品有关的线索均可以诱导复吸行为发生。目前关于海洛因成瘾是如何导致认知功能损害或造成海洛因复吸行为的详细机制还未完全清楚,因而缺乏行之有效的防复吸方法。
mirna是长18~24个左右核苷酸大小的一类非编码单链rna,其通过5′端种子序列与靶mrna的3′端非编码区(3'untranslatedregions,3′utr)通过碱基互补配对,再与rna诱导的沉默复合体(rsc)结合,剪切靶基因的转录产物或者抑制转录产物的翻译,从而起到转录后调控靶基因的表达。表观遗传学是指不涉及基因序列的改变,而是经过表观遗传修饰后调控机体基因的表达。表观遗传学包括dna甲基化、组蛋白修饰和非编码rna(mirna,lncrna等)调控。
因此,有必要提供一种新型的抗海洛因复吸药物,以减少海洛因成瘾后复吸行为的发生。
技术实现要素:
本发明所要解决的技术问题是,克服以上背景技术中提到的不足和缺陷,提供一种用于检测海洛因成瘾的生物标记物mir-181a及其在制备抗海洛因复吸药物中的应用,以减少海洛因成瘾后复吸行为的发生。
为解决上述技术问题,本发明提出的技术方案为:一种用于检测海洛因成瘾的生物标记物,所述生物标记物为hsa-mir-181a。
优选地,所述hsa-mir-181a的核苷酸序列如seqidno.1所示。
优选地,所述生物标记物为人外周血中的hsa-mir-181a。
本发明还提供了一种rno-mir-181a在制备抗海洛因复吸药物中的应用,通过过表达rno-mir-181a,以抑制海洛因复吸行为。
优选地,所述rno-mir-181a的核苷酸序列如seqidno.2所示。
优选地,通过转染带有所述rno-mir-181a核苷酸序列的慢病毒过表达所述rno-mir-181a。
优选地,所述rno-mir-181a用于下调mecp2蛋白的表达量以抑制海洛因复吸行为。
优选地,所述rno-mir-181a用于下调mecp2-mrna的表达,所述mecp2-mrna为所述mecp2蛋白的信使rna,其核苷酸序列如seqidno.3所示。
优选地,所述rno-mir-181a与靶基因mecp2的3'utr特异性结合,以下调所述mecp2蛋白的表达,所述mecp2蛋白为所述靶基因mecp2编码的蛋白质。
与现有技术相比,本发明的优点在于:可通过检测本发明提供的所述hsa-mir-181a的表达水平的变化量,作为一种海洛因成瘾行为相关的生物指标,采用分子生物学技术检测灵敏度高;可通过在体内过表达rno-mir-181a,以减少海洛因成瘾的复吸行为,为海洛因成瘾和复吸治疗提供新的分子靶标。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
图1为健康对照组和海洛因成瘾组的hsa-mir-181a表达情况数据图;
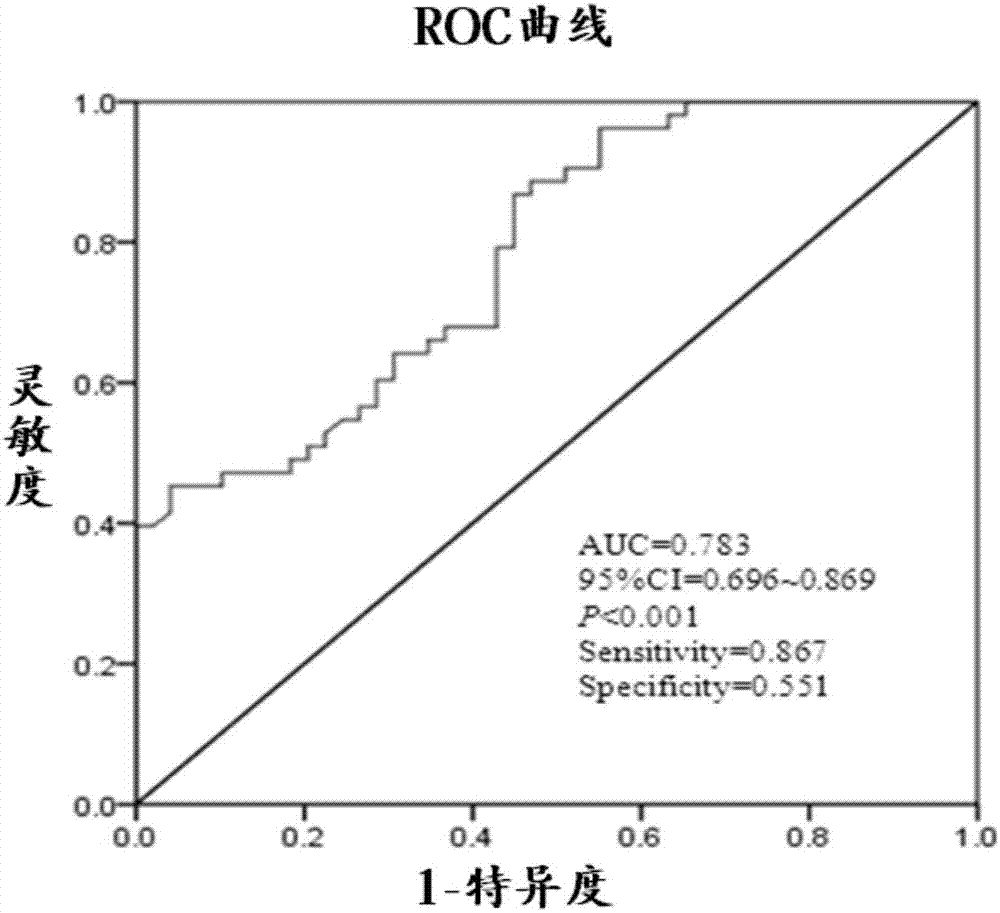
图2为hsa-mir-181a对海洛因成瘾的诊断价值的roc曲线图;
图3为real-time-pcr检测海洛因自身给药大鼠戒断后线索诱导海洛因复吸的rno-mir-181a表达量柱状图;
图4为细胞水平的双荧光素酶检测实验柱状图;
图5为海洛因自身给药大鼠条件性线索诱导复吸后mecp2蛋白表达量的柱状图;
图6为在大鼠nac脑区部位注射过表达rno-mir-181a慢病毒2周后转染情况图;
图7为海洛因自身给药大鼠nac脑区过表达rno-mir-181a后nac脑区rno-mir-181a表达量的柱状图;
图8为海洛因自身给药大鼠nac脑区过表达rno-mir-181a后,条件性线索诱导的海洛因复吸行为柱状图;
图9为海洛因自身给药大鼠nac脑区过表达rno-mir-181a后,mecp2-mrna表达量的柱状图;
图10为海洛因自身给药大鼠nac脑区过表达rno-mir-181a后,mecp2蛋白表达量的柱状图;
图11为海洛因自身给药大鼠nac脑区注射lv-sirna-mecp2后,mecp2-mrna表达柱状图;
图12为海洛因自身给药大鼠nac脑区注射lv-sirna-mecp2后,mecp2蛋白表达量柱状图;
图13为海洛因自身给药大鼠nac脑区注射lv-sirna-mecp2后,条件性线索诱导的海洛因复吸行为行为柱状图。
具体实施方式
为了便于理解本发明,下文将结合说明书附图和较佳的实施例对本文发明做更全面、细致地描述,但本发明的保护范围并不限于以下具体实施例。
除非另有定义,下文中所使用的所有专业术语与本领域技术人员通常理解含义相同。本文中所使用的专业术语只是为了描述具体实施例的目的,并不是旨在限制本发明的保护范围。
除非另有特别说明,本发明中用到的各种原材料、试剂、仪器和设备等均可通过市场购买得到或者可通过现有方法制备得到。
除非另有特别说明,以下实施例中采集血浆rna用到的mirneasyserum/plasmakit试剂盒、rna逆转录用到的
实施例1
验证hsa-mir-181a在海洛因成瘾患者血浆中的表达水平。
根据预设的纳入和排除标准,采集无海洛因成瘾疾病的志愿者的外周血血浆rna作为健康对照组,采集具有海洛因成瘾的戒毒患者的外周血血浆rna作为海洛因成瘾组;
具体地,纳入标准为:无重大传染病,无其他重大慢性疾病及家族史;知情同意后进行常规门诊实验室检测;海洛因成瘾者符合dsm-v诊断(diagnosticandstatisticalmanualofmentaldisorders,美国精神障碍诊断统计手册第五版)和尿检阳性。
排除标准为:既往有明确或现在有疾病史,重大传染病;知情同意不参加或无法完成知情同意者;海洛因成瘾者有明显情绪障碍或精神疾病,排除合并其他毒品滥用。
在本实施例中,血浆rna的提取采用德国qiagen公司mirneasyserum/plasmakit试剂盒完成。当然,具体如何实现,采用何种方法,本领域技术人员可根据实际情况进行选择。采集到的血浆rna做mirna表达谱分析;
将健康对照组和海洛因成瘾组的血浆rna送上海伯豪生物技术有限公司进行mirna表达谱分析,根据mirna表达芯片结果得出在健康对照组和海洛因成瘾组之间hsa-mir-181a的表达量具有差异。
采用real-time-pcr验证hsa-mir-181a在健康对照组和海洛因成瘾组中的差异表达。
具体地,将采集的血浆rna进行逆转录得到模板cdna,反应体系和反应程序可参阅表1和表2。
表1逆转录反应体系
表2逆转录反应程序
在本实施例中,采用real-time-pcr检测健康对照组和海洛因成瘾组血浆中hsa-mir-181a表达水平,具体采用德国qiagen公司
表3real-time-pcr反应体系
表4real-time-pcr反应程序
表5real-time-pcr反应溶解曲线
请参阅图1,为健康对照组和海洛因成瘾组的hsa-mir-181a表达情况数据图。其中,control为健康对照组,heroin为海洛因成瘾组。数据分析得到海洛因成瘾组与健康对照组△ct差异具有统计学差异[t=54.956,p<0.001],由图可知,海洛因成瘾组△ct小于健康对照组△ct,表明海洛因成瘾组外周血浆中hsa-mir-181a表达显著高于健康对照组,与mirna表达谱芯片检测的结果基本相符。
请参阅图2,hsa-mir-181a对海洛因成瘾的诊断价值的roc曲线图。对健康对照组和海洛因成瘾组中的hsa-mir-181a的表达量进行roc曲线分析发现,roc曲线下面积为0.783(95%ci=0.696~0.869),灵敏度(sensitivity)和特异度(specificity)分别为0.867和0.551,表明外周血浆中hsa-mir-181a的表达水平对海洛因成瘾诊断具有显著意义(p<0.001),可把外周血中的hsa-mir-181a的表达变化作为诊断海洛因成瘾的生物标记物。
实施例2
建立海洛因自身给药大鼠模型,并进行复吸行为测试。
通过mirna在线数据库的查阅,本实施例为mirbase、microcosm和targetscan,在ncbi数据库进行人体的hsa-mir-181a和大鼠rno-mir-181a序列比对,发现二者序列完全一致。具体地,人体的hsa-mir-181a和大鼠rno-mir-181a的核苷酸序列分别如seqidno.1和seqidno.2所示,且两者的核苷酸序列相同,即可能属于不同生物种属中具有相同功能的一类mirna。本实施例通过建立稳定的大鼠海洛因自身给药模型来模拟人类海洛因成瘾行为。具体方法如下:
在大鼠自身给药训练笼中设有有效鼻触和无效鼻触。取质量为300g左右的雄性sd大鼠经右侧颈静脉插管手术,术后抗感染恢复一周,将大鼠独立放置于自身给药训练笼进行海洛因自身给药训练,输液系统中注射器内含有训练大鼠的0.2mg/ml海洛因溶液,给药模式采用固定比率fr1程序,以4h/d,每天训练一次,测序开启有效鼻触灯亮,无效鼻触不亮,大鼠触碰有效鼻触时给予一针海洛因注射并记录次数,笼灯亮5s,注射剂量为0.05mg/kg/针,注射完毕后进入20s不应期,期间触碰有效鼻触不进行海洛因注射,但可记录触碰的次数,当触碰无效鼻触时仅记录次数不注射海洛因,笼灯不亮。大鼠不间断连续进行14d训练,以每天训练注射针数超过25针视为造模成功,最后3d有效鼻触数变化不超过10%视为模型稳定。
建立稳定的海洛因自身给药大鼠,置于饲养笼进行14天戒断,然后进行复吸行为的测试,大鼠独立放置于自身给药训练笼中,大鼠所处的环境与海洛因训练过程一样,但触碰有效鼻触时记录次数,笼灯亮,注射泵空打,不进行海洛因注射,每次复吸行为测试时间为2h。
实施例3
大鼠nac脑区mirna表达谱分析。
以下实施例中,为与人体内的hsa-mir-181a做出区别,应用于大鼠实验的mir-181a核苷酸序列表示为rno-mir-181a。本领域技术人员可以理解的是,hsa-mir-181a和rno-mir-181a的核苷酸序列一致,其实质是相同的。
将实施例2中成功建立稳定的大鼠海洛因自身给药模型设置为3个实验组,cs1实验组为海洛因自身给药大鼠戒断1天后条件性线索诱导复吸组;cs14实验组为海洛因自身给药大鼠戒断14天后条件性线索诱导复吸组;control对照组采用同等剂量的生理盐水取代海洛因进行大鼠自身给药训练,其他操作与cs1实验组和cs14实验组相同。将cs1实验组、cs14实验组和control对照组的大鼠复吸行为测试后立即处死,取nac脑区样品送至上海康成生物工程有限公司进行mirna表达谱分析。根据芯片表达量筛选出control对照组、cs1实验组和cs14实验组中具有显著性差异的mirna。发现rno-mir-181a在上述各组间有统计学差异(p<0.05)。
实施例4
在建立大鼠海洛因成瘾模型基础上,应用rt-pcr和real-time-pcr技术进一步验证cs1实验组、cs14实验组和control对照组间rno-mir-181a的表达水平差异。
提取cs1实验组、cs14实验组和control对照组的大鼠nac脑区总rna,具体步骤如下:
1)组织提取:各组大鼠复吸行为测试后麻醉断头取脑,根据大鼠脑图谱取出nac脑区,放置于2.5mlrnase-freeep管中;
2)裂解:加入1mltrizol,匀浆裂解,此时可置于-80℃长期保存;
3)分相:加入200ul氯仿,震荡混匀后室温放置15min,(注:禁用漩涡振荡器,以免基因组dna断裂);
4)吸取上层水相:4℃12000rpm高速离心15min后吸取上层水相(约300ul)至另一2.5mlrnase-freeep管,弃残夜(注:不要吸取中间及下层液面);
5)沉淀:加入500ul异丙醇,充分混匀,冰上放置5-10min;4℃12000rpm高速离心10min,弃上清,可见白色total-rna沉于管底;
6)清洗:加入1ml75%乙醇,温和震荡ep管,悬浮沉淀;4℃8000rpm离心5min,尽吸上清;
7)干燥:室温干燥5-10min,加入20uldepc水溶解total-rna,置冰上;
8)浓度及od测定:使用nanodrop2000测定样本total-rna的浓度及od值,od值在1.8-2.1证明样品提取质量好;
9)保存:-80℃长期保存。
对提取的总rna用miscriptⅱrtkit试剂盒逆转录为cdna。
1)根据提取出来的total-rna用nanodrop2000测得的浓度,计算出逆转录体系中rna的体积。
2)逆转录反应程序可参照表6和表7。
表6逆转录反应程序
表7逆转录反应体系(20ul体系)
采用real-time-pcr验证步骤二所逆转录的cdna,用miscriptsybrgreenpcrkit试剂盒进行pcr扩增。
pcr反应体系如表8所示:
表8pcr反应体系
pcr反应程序如表9所示
表9rt-pcr反应程序
rt-pcr反应溶解曲线如表10所示
表10rt-pcr反应溶解曲线
本实施例中使用的内参u6primer,如seqidno.4所示。
请参阅图3,为real-time-pcr检测海洛因自身给药大鼠戒断后线索诱导海洛因复吸的rno-mir-181a表达量柱状图。经统计分析三组间rno-mir-181a表达水平具有统计学差异[f(2,11)=4.074,p=0.047]。由图可知,cs1组中rno-mir-181a表达水平高于control组,表明大鼠吸食海洛因后rno-mir-181a表达水平显著升高,而海洛因自身给药大鼠戒断14天后线索诱导海洛因复吸后的cs14实验组和cs1组相比,rno-mir-181a表达水平却显著减少,表明随着戒断时间延长海洛因复吸后rno-mir-181a表达水平下降,与基因芯片筛选表达结果一致。
实施例5
确定rno-mir-181a的靶基因。具体地,依据在线数据库预测rno-mir-181a调控的靶基因,targenscan数据库预测到rno-mir-181a调控mecp2基因,对其预测的结果在细胞水平上进行体验证。
采用双荧光素酶实验细胞水平上验证rno-mir-181a对靶基因mecp2表达的影响。根据在线数据库targetscan预测到rno-mir-181a与靶基因mecp2的结合点,依据结合点构建两种mirna质粒,一种为mirna空载质粒,表示为mirna-nc;另一种为含有rno-mir-181a的质粒,表示为mirna-181a,各0.4ug;以上质粒均由上海吉凯基因化学技术有限公司包装完成。
构建mecp2基因三种荧光质粒:一种为mecp2-3'utr空载质粒,表示为control;另一种为含目的基因mecp23'utr荧光质粒,表示为mecp2-wt,mecp2-wt的核苷酸序列如seqidno.5所示;另一种为含目的基因mecp23'utr突变体质粒,表示为mecp2-mu,mecp2-mu的核苷酸序列如seqidno.6所示,各0.1ug;以上荧光质粒均由上海吉凯基因化学技术有限公司包装完成。
将mirna质粒和荧光质粒两两转染,得到以下六组,分别为:control+mirna-nc、control+mirna-181a、mecp2-wt+mirna-nc、mecp2-wt+mirna-181a、mecp2-mu+mirna-nc和mecp2-mu+mirna-181a组,使用x-tremegenehp转染试剂转染质粒,转染比例为每孔每转染1ug质粒需2ulx-tremegenehp转染试剂,转染体系为24孔板,500ul/well,目的细胞为293t细胞,质粒转染后48h后使用dual-luciferasereporterassaysystem测定各组报告基因的荧光表达量。
请参阅图4,为细胞水平的双荧光素酶检测实验柱状图。实验结果表明,mecp2-wt+mirna-181a组中双荧光素表达显著低于control+mirna-181a组[t(4)=11.480,p=3.28×10-4]和mecp2-wt+mirna-nc[t(4)=3.645,p=0.022]。上述结果证明:rno-mir-181a和mecp2的3'utr结合,从而抑制靶基因mecp2表达。
实施例6
验证海洛因自身给药戒断大鼠条件性线索诱导复吸后mecp2蛋白表达水平变化。
对control对照组、cs1实验组和cs14实验组大鼠复吸行为测试后立即麻醉断头取nac脑区组织提取蛋白进行westernblot分析。请参阅图5,为海洛因自身给药戒断大鼠条件性线索诱导复吸后mecp2蛋白表达量的柱状图。经westernblot蛋白分析表明,上述三组中nac脑区mecp2蛋白表达存在显著性差异[f(2,6)=34.467,p=5.13×10-4],由图可见,cs14组与control组及cs1组相比,nac脑区中mecp2蛋白表达均显著增加(p<0.05)。
实施例7
观察海洛因自身给药戒断大鼠nac脑区成功过表达rno-mir-181a对线索诱导的海洛因复吸行为的影响、以及mecp2mrna和mecp2蛋白表达变化情况。其中,所述mecp2-mrna为所述mecp2蛋白的信使rna,其核苷酸序列如seqidno.3所示。
1)海洛因自身给药大鼠nac脑区过表达rno-mir-181a对线索诱导复吸行为的影响。
成功建立海洛因成瘾的大鼠随机分为cs14组、lv-gfp组和lv-mirna-181a组。在戒断第1天在大鼠nac脑区微注射慢病毒载体,其中lv-mirna-181a组于大鼠nac脑区微注射带有rno-mir-181a核苷酸序列的慢病毒载体;lv-gfp组于大鼠nac脑区微注射不含目的基因的空病毒lv-gfp;cs14组为海洛因成瘾戒断后14天,不做病毒微注射,为对照组。病毒在脑内转染2周后进行2h线索诱导海洛因复吸行为测试。测试完毕后立即断头取大鼠nac脑区,提取rna逆转录为cdna进行rt-pcr实验。
请参阅图6,为在大鼠nac脑区部位注射过表达rno-mir-181a慢病毒2周后转染情况图。慢病毒在大鼠nac脑区部位注射2周后,荧光显微镜下观察到的大鼠nac脑区内转染情况,其中,a、b、c分别为放大20倍、4倍和40倍,由图可知,转染成功。
请参阅图7,为海洛因自身给药大鼠nac脑区过表达rno-mir-181a后nac脑区中rno-mir-181a表达量的柱状图。cs14组、lv-gfp组和lv-mir-181a组中nac脑区rno-mir-181a表达存在显著差异[f(2,13)=3.792,p<0.05]。由图可得lv-mir-181a组中大鼠nac脑区rno-mir-181a表达水平显著高于cs14组和lv-gfp组。表明lv-mir-181a在大鼠nac脑区成功过表达。
请参阅图8,为海洛因自身给药大鼠nac脑区过表达rno-mir-181a后对条件线索诱导的海洛因复吸行为柱状图。成功建立海洛因自身给药大鼠模型后,随机分为cs14组,lv-gfp组和lv-mir-181a组,每组8只。慢病毒载体在大鼠nac脑区转染2周后进行海洛因条件线索诱导复吸行为2h测试,测试结果显示上述三组中海洛因复吸行为存在显著性差异[f(2,21)=7.559,p=0.03]。lsd法进行两两比较,lv-mir-181a组分别与cs14组和lv-mir-181a组相比均有显著性差异(p<0.05),大鼠nac脑区过表达rno-mir-181a后能显著抑制大鼠海洛因条件线索诱导的复吸行为。
2)海洛因自身给药大鼠nac脑区过表达rno-mir-181a后,mecp2-mrna表达水平进行分析验证。
具体地,cs14组、lv-gfp组和lv-mirna-181a组大鼠复吸行为测试后立即处死,各组分别取部分大鼠nac脑区组织提取rna,进行mecp2-mrna表达水平测试,具体实验方法可参照实施例4。
采用的pcr引物序列如下:
mecp2正向引物:5'-caggcaaagcagagacatca-3',如seqidno.7所示;
mecp2反向引物:5'-caaggtggggtcatcataca-3',如seqidno.8所示;
内参引物如下:
gapdh正向引物:5'-gacatgccgcctggagaaac-3',如seqidno.9所示;
gapdh反向引物:5'-agcccaggatgccctttagt-3',如seqidno.10所示。
请参阅图9,为海洛因自身给药大鼠nac脑区过表达rno-mir-181a后,mecp2-mrna表达量的柱状图。海洛因自身给药大鼠nac脑区过表达rno-mir-181a后,real-time-pcr实验检测靶基因mecp2-mrna表达变化,经检测发现,在大鼠nac脑区过表达rno-mir-181a后lv-mir-181a组相比lv-gfp与cs14组mecp2-mrna表达降低
3)海洛因自身给药大鼠nac脑区过表达rno-mir-181a后,mecp2蛋白表达水平进行分析验证。
具体地,cs14组、lv-gfp组和lv-mir-181a组大鼠复吸行为测试后立即处死,各组分别取部分大鼠nac脑区组织提取蛋白,采用westernblot进行mecp2蛋白表达水平测试。
请参阅图10,为海洛因自身给药大鼠nac脑区过表达rno-mir-181a后,mecp2蛋白表达量的柱状图。实验分析发现,上述三组中大鼠nac脑区mecp2蛋白表达具有显著性差异[f(2,6)=41.008,p=3.17×10-4],lv-mir-181a组分别与cs14组和lv-gfp组相比均降低。证明rno-mir-181a过表达后能显著抑制mecp2蛋白表达。
实施例8
根据已知靶基因mecp2的核苷酸序列,设计特异性的sirna,以干扰mecp2mrna来调控靶基因mecp2的表达。验证海洛因自身给药大鼠nac脑区注射lv-sirna-mecp2后条件性线索诱导的海洛因复吸行为及mecp2表达变化。
成功建立海洛因自身给药大鼠模型,随机分为cs14组,lv-gfp组和lv-sirna-mecp2组。干扰mecp2蛋白表达的sirna慢病毒载体包装由上海吉凯基因化学技术有限公司包装完成,lv-sirna-mecp2构建发夹结构序列如seqidno.11和seqidno.12所示。包装后的含有目的基因mecp2sirna的慢病毒命名为lv-sirna-mecp2,并设含空载体慢病毒lv-gfp。大鼠自身给药训练结束后第1天进行大鼠nac脑区微量注射慢病毒,慢病毒转染2周后进行大鼠海洛因条件诱导复吸行为测试,测试结束后立即麻醉断头取nac脑区,rt-pcr检测mecp2mrna表达变化。
请参阅图11,为海洛因自身给药大鼠nac脑区注射lv-sirna-mecp2后mecp2mrna表达柱状图。由图可知,上述三组间mecp2mrna表达存在显著差异[f(2,12)=4.302,p=0.039],lv-sirna-mecp2分别与lv-gfp和cs14相比表达量显著降低。请参阅图12,为海洛因自身给药大鼠nac脑区注射lv-sirna-mecp2后mecp2蛋白表达柱状图。由图可知,上述三组间大鼠nac脑区中mecp2蛋白表达存在显著差异[f(2,6)=42.512,p=2.86×10-4],lv-sirna-mecp2分别与lv-gfp和cs14相比表达量显著降低。请参阅图13,为海洛因自身给药大鼠nac脑区注射lv-sirna-mecp2后,条件性线索诱导的海洛因复吸行为次数柱状图。由图可知,上述三组中,大鼠nac脑区中注射lv-sirna-mecp2后自身给药大鼠条件线索诱导海洛因复吸行为存在显著差异[f(2,21)=3.851,p=0.038],lv-sirna-mecp2组条件性线索诱导海洛因复吸行为显著低于cs14组及lv-gfp组。所以,通过干扰mecp2蛋白表达的sirna慢病毒载体可用于控制海洛因复吸行为。
以上所述仅为本发明的实施例,并非因此限制本发明的专利范围,凡是利用本发明说明书内容所作的等效流程变换,或直接或间接运用在其它相关的技术领域,均同理包括在本发明的专利保护范围内。
sequencelisting
<110>宁波市微循环与莨菪类药研究所
<120>mir-181a作为海洛因成瘾的生物标记物及其在制备抗海洛因复吸药物中的应
用
<130>1
<160>12
<170>patentinversion3.5
<210>1
<211>23
<212>rna
<213>人工序列
<400>1
aacauucaacgcugucggugagu23
<210>2
<211>23
<212>rna
<213>人工序列
<400>2
aacauucaacgcugucggugagu23
<210>3
<211>1711
<212>dna
<213>rattusnorvegicus
<400>3
gtccggaaaatggccgccgccgctgccgccgctgccgccgccgccgccgccgctgccgcc60
gccgccgccgccgccgccgccgcgccgagcggaggaggaggaggcgaggaggagagactg120
ctccataaaaatacagactcaccagttcctgctttgatgtgacatgtgactccccagaat180
acaccttgcttctgtagaccagctccaacaggattccatggtagctgggatgttagggct240
cagggaggaaaagtcagaagaccaggatctccagggcctcaaagagaaacccctgaagtt300
taagaaggtgaagaaagacaagaaggaagacaaagagggcaaacatgaaccactacagcc360
ttcagcccaccattctgcagagccagcagaggcaggcaaagcagagacatcagaaagctc420
aggctctgccccagcagtaccagaagcctctgcttctcccaaacagcgacgttccatcat480
tcgtgaccggggacctatgtatgatgaccccaccttgcctgaaggttggacgcgaaagct540
taaacagaggaagtctggtcgctctgctggaaagtatgatgtatatttgatcaatcccca600
gggaaaagcctttcgctctaaagtagaattgattgcatattttgaaaaggtgggagacac660
ctccttggaccctaatgattttgacttcactgtaactgggagagggagcccttccaggag720
agaacagaaaccacctaagaagcccaaatctcccaaagctccaggaactggcaggggtcg780
gggacgcccgaaagggagcggcactgggagaccaaaggcagcagcatcagaaggtgttca840
agtgaaaagggtcctggagaagagccctgggaaacttctcgtcaagatgcctttccaagc900
atcacctgggggtaagggtgagggaggtggggctaccacatctgcgcaggtcatggtgat960
caaacgccctggcagaaagcgaaaagctgaagctgacccccaggccattcctaagaaacg1020
gggtagaaagcctgggagtgtggtggcagctgctgctgcagaggccaaaaagaaagctgt1080
gaaggaatcttctatacggtctgtgcaggagactgtgctccccatcaagaagcgcaagac1140
ccgggaaaccgtcagcattgaggtcaaggaggtggtgaagcccctgctggtgtctacact1200
tggtgagaagagtggaaagggactgaagacatgcaagagccctgggcgtaaaagcaagga1260
gagcagccccaaggggcgcagcagcagtgcctcctcaccacctaagaaggagcaccatca1320
tcaccaccatcacgcagagtccccaaaggcccccatgccattgcttccacctccaccccc1380
acctgagcctcagagctctgaggaccccatcagcccccctgagcctcaggacttgagcag1440
cagcatctgcaaagaggagaagatgccccgagcaggctcactggaaagcgatggctgccc1500
caaggagccagctaagactcagcccatggttgctgccgccgccaccaccaccaccaccac1560
caccaccacagttgcagaaaagtacaaacaccgaggggagggagagcgcaaagacattgt1620
ttcatcctccatgccgaggccaaacagagaggagcctgtggacagccggacgcccgtgac1680
cgagagagttagctgactttacatagagcgg1711
<210>4
<211>23
<212>dna
<213>人工序列
<400>4
ctcgcttcggcagcacatatact23
<210>5
<211>220
<212>dna
<213>人工序列
<400>5
tctagaaaaggttctttgtgtatagccaaatgactgaaagcactgatatatttaaaaaca60
aaaggcaatttattaaggaaatttgtaccatttcagtaaacctgtcgtccgtgccctgta120
tacgtttcaaaaacacaccccactgaacccctgtaacctatttattatataaagagtttg180
ccttataaatttacataaaaatgtccgtttgtgttctaga220
<210>6
<211>220
<212>dna
<213>人工序列
<400>6
tctagaaaaggttctttgtgtatagccaaatgactgaaagcactgatatatttaaaaaca60
aaaggcaatttattaaggaaatttgtaccatttcagtaaacctgtctgaatgtacctgta120
tacgtttcaaaaacacaccccactgaacccctgtaacctatttattatataaagagtttg180
ccttataaatttacataaaaatgtccgtttgtgttctaga220
<210>7
<211>20
<212>dna
<213>人工序列
<400>7
caggcaaagcagagacatca20
<210>8
<211>20
<212>dna
<213>人工序列
<400>8
caaggtggggtcatcataca20
<210>9
<211>20
<212>dna
<213>人工序列
<400>9
gacatgccgcctggagaaac20
<210>10
<211>20
<212>dna
<213>人工序列
<400>10
agcccaggatgccctttagt20
<210>11
<211>58
<212>dna
<213>人工序列
<400>11
ccggaagcccaaatctcccaaagctctcgagagctttgggagatttgggctttttttg58
<210>12
<211>58
<212>dna
<213>人工序列
<400>12
aattcaaaaaaagcccaaatctcccaaagctctcgagagctttgggagatttgggctt58
- 还没有人留言评论。精彩留言会获得点赞!