用于分开单克隆抗体的同种型的方法与流程
本申请要求在2016年1月8日提交的美国专利申请号62/276378的优先权,将其内容以引用的方式整体并入本文中。本发明主要涉及蛋白生物化学和分析化学领域。更具体而言,本发明涉及用于分级分离单克隆抗体的电荷变体的分析色谱方法,其提供富集的或更均质的抗体制备物,也提供降低抗体制备物效力的电荷变体的除去。以引用的方式并入的序列表将创建于2017年1月4日且大小为6kb的命名为“onbi-007001wo_seqlist.txt”的文本文件的内容以引用的方式整体并入本文中。
背景技术:
:在本说明书各处引用了包括专利、公开的申请、登录号、技术论文和学术论文在内的各种出版物。这些所引用的出版物各自以引用的方式整体并入本文中用于所有目的。单克隆抗体(mab)可用作治疗蛋白。纯化的单克隆抗体通常多出现在复杂的异质混合物中。单克隆抗体具有电荷异质性,其优化得到有利的静电相互作用的平衡,并且决定它们的结构、稳定性、结合亲和力、化学性质,并因此决定它们的生物活性。存在由酶促过程或自发的降解和修饰引起的在蛋白表达和生产过程中产生的异质性形式。抗体通过几种不同的机制经历化学修饰,所述机制包括氧化、脱酰胺、糖化、异构化和片段化,导致形成各种电荷变体和异质性。化学修饰和酶修饰(例如脱酰胺和唾液酸化)导致mab的净负电荷增加,并引起pi值降低,由此导致形成酸性变体。c端赖氨酸切割导致净正电荷的丧失,并导致形成主要抗体或酸性变体。另一种产生酸性变体的机制是形成各种类型的共价加合物,例如糖化,其中如果制剂中存在还原糖,则葡萄糖或乳糖可在富含葡萄糖的培养基中生产过程中或储存过程中与赖氨酸或精氨酸残基的伯胺反应。碱性变体的形成可产生自一个或多个c端赖氨酸的存在或脯氨酸酰胺化、琥珀酰亚胺的形成、氨基酸氧化或唾液酸的除去,这引入额外的正电荷或除去负电荷,两种类型的修饰均引起pi值的增加。由于可能对效力产生影响,应对翻译后修饰(ptm)(例如天冬酰胺的脱酰胺、天冬氨酸的异构化和蛋氨酸氧化)进行评估。但是,考虑到生物治疗剂(例如mab)的复杂性,完整分子的ptm和效力分析通常提供有限的信息。因此,特别是就结构-功能关系而言,仍然需要针对其对制备物的大体上的影响来挑选和评估变体分子。技术实现要素:本公开的特征在于用于分开重组表达的抗体的同种型的方法。分开可允许例如评估抗体结构与功能之间的关系。这样的同种型包括酸性电荷变体、碱性电荷变体和主要抗体。这些同种型属于单克隆抗体。大体上,本文提供用于分开重组表达的抗体的同种型的方法,包括:将包含抗体和所述抗体的多种电荷变体的重组表达的抗体制备物加载到含有能够捕获所述抗体和电荷变体的配体的阳离子交换色谱载体上;和如下分级分离所述电荷变体:使含有约20mm~约30mm的mes且具有约6.1的ph的第一流动相缓冲液通过载体,在第一流动相缓冲液通过载体的同时,向第一流动相缓冲液中加入含有约40mm的磷酸钠~约60mm的磷酸钠和约95mm的氯化钠且具有约8.0的ph的第二流动相缓冲液,以得到约90体积%的第一流动相缓冲液和约10体积%的第二流动相缓冲液的混合物,通过逐渐增加所述混合物中第二流动相缓冲液的量以得到约55体积%的第一流动相缓冲液和约45体积%的第二流动相缓冲液,从配体梯度洗脱一种或多种电荷变体,并收集一种或多种电荷变体至分开的级分中。在一些优选的实施方案中,抗体包含曲妥单抗及其电荷变体和/或同种型。作为非限制性实例,曲妥单抗可包含具有seqidno:1的氨基酸序列的重链和具有seqidno:2的氨基酸序列的轻链。第一流动相缓冲液可含有约23mm~约25mm的mes,在一个优选的实施方案中,含有约24mm的mes。第二流动相缓冲液可含有约45mm~约55mm的磷酸钠,在一个优选的实施方案中含有约50mm的磷酸钠。在一个实施方案中,向第一流动相缓冲液中加入第二流动相缓冲液以得到约90体积%的第一流动相缓冲液和约10体积%的第二流动相缓冲液的混合物的步骤通过向第一流动相缓冲液中一次性加入第二流动相缓冲液以实质上立即得到所述混合物而发生。在另一个实施方案中,向第一流动相缓冲液中加入第二流动相缓冲液以得到约90体积%的第一流动相缓冲液和约10体积%的第二流动相缓冲液的混合物的步骤通过在一段时间内向第一流动相缓冲液中注入第二流动相缓冲液以得到所述混合物而发生。伴随着盐浓度和ph随第二流动相缓冲液占据更大比例的阳离子交换(cex)流通而增加,抗体的同种型从cex配体洗脱。酸性电荷变体、碱性电荷变体和主要抗体可根据该方法从柱洗脱。可将洗脱的同种型收集在分开的级分中。可将一种、二种、三种、四种、五种、六种、七种、八种、九种、十种、十一种或更多种同种型收集至分开的级分中,或组合收集至级分中。在本文所公开的任一方法中,该方法可包括收集两种或更多种电荷变体至分开的级分中,收集三种或更多种电荷变体至分开的级分中,收集四种或更多种电荷变体至分开的级分中,收集五种或更多种电荷变体至分开的级分中,收集六种或更多种电荷变体至分开的级分中,收集七种或更多种电荷变体至分开的级分中,收集八种或更多种电荷变体至分开的级分中,收集九种或更多种电荷变体至分开的级分中,和/或收集十种或更多种电荷变体至分开的级分中。根据本公开的方法,电荷变体可包含最多六种酸性电荷变体和最多四种碱性电荷变体。将各种分开的级分(即同种型级分或电荷变体级分)高度纯化。例如,一种或多种分开的级分可以以下述纯度含有所收集的同种型或电荷变体(或其组合):基于级分的总重量至少约90%,基于级分的总重量至少约91%,基于级分的总重量至少约92%,基于级分的总重量至少约93%,基于级分的总重量至少约94%,基于级分的总重量至少约95%,基于级分的总重量至少约96%,基于级分的总重量至少约97%,基于级分的总重量至少约98%,和/或基于级分的总重量至少约99%。作为非限制性实例,本公开的任一方法可另外包括从配体洗脱抗体(即曲妥单抗)。可重复纯化方法,随后可将级分混合并任选浓缩。例如,可将含有抗体及多种电荷变体和/或同种型的另外的重组表达的抗体制备物加载到载体上,可重复分级分离步骤,并可将来自各抗体制备物的相同电荷变体和/或同种型的分开的级分合并在一起。同样地,可将含有抗体及多种电荷变体和/或同种型的另外的重组表达的抗体制备物加载到载体上,可重复分级分离步骤,可重复洗脱步骤,并可将洗脱的抗体、其电荷变体和/或同种型合并在一起。在一个优选的实施方案中,混合的电荷变体和/或同种型为相同的电荷变体和/或同种型,但是可将不同的电荷变体和/或同种型混合在一起,包括将任何酸性变体与任何其它的酸性变体,或与任何碱性变体,或与主要抗体混合,或者包括将任何碱性变体与任何其它的碱性变体,或与任何酸性变体,或与主要抗体混合。可将主要抗体与主要抗体的其它的级分混合,或与酸性或碱性电荷变体的任意组合混合。根据本发明的任一方法,将一种或多种相对于抗体本身具有增强的效力的电荷变体和/或同种型的分开的级分合并在一起。作为非限制性实例,可将抗体与一种或多种相对于所述抗体具有增强的效力的电荷变体和/或同种型的分开的级分合并在一起。可使用同种型的组合物,例如以调节或控制特定的治疗抗体制剂的效力或治疗功效。例如,可将分开的同种型级分混合以便匹配参比抗体制剂的同种型或同种型类别(例如酸性或碱性电荷变体)的相对百分比,例如在生物相似的抗体生产中。可将分开的同种型级分混合以增强抗体制剂的效力或治疗功效,例如通过排除降低抗体制剂的效力或治疗功效的同种型,例如在生物增强的抗体生产中。作为非限制性实例,本文所公开的任一方法可另外包括将洗脱的抗体(例如曲妥单抗)与一种或多种电荷变体的分开的级分合并在一起,以制备具有实质上与美国食品药品监督管理局(u.s.foodanddrugadministration)批准的抗体(例如曲妥单抗)组合物中的抗体(例如曲妥单抗)及其电荷变体的比例相同的抗体(例如曲妥单抗)及其电荷变体的比例的生物相似的抗体(例如曲妥单抗)组合物。还提供根据本文所说明或示例的任一方法制备的抗体同种型或其组合和/或其制剂。适宜的制剂可连同一种或多种药学上可接受的载体和/或药学上可接受的赋形剂一起含有抗体同种型或其组合。制剂中的抗体同种型或其组合具有90%或更大水平的纯度、91%或更大水平的纯度、92%或更大水平的纯度、93%或更大水平的纯度、94%或更大水平的纯度、95%或更大水平的纯度、96%或更大水平的纯度、97%或更大水平的纯度、98%或更大水平的纯度或99%或更大水平的纯度,和/或实质上没有其它的抗体同种型。本文所说明的任一方面和实施方案可与
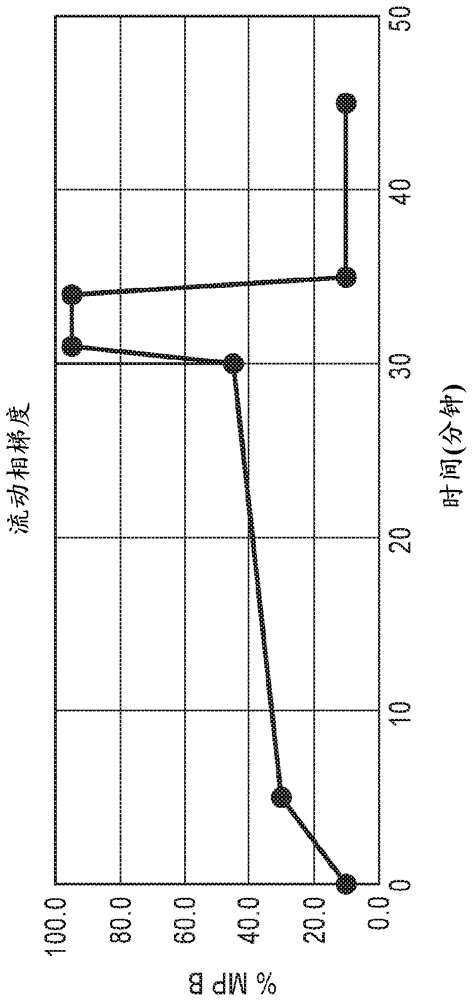
发明内容中、附图中和/或具体实施方式中公开的任何其它的方面或实施方案(包括下面的本发明的具体的非限制性的实施例/实施方案)组合。除非另有规定,本文所使用的所有技术术语和科学术语具有与本申请所属领域技术人员通常的理解相同的含义。在本说明书中,除非上下文清楚地另外指示,单数形式也包含复数。虽然与本文所说明的方法和材料相似或等同的方法和材料可用于本申请的实施和测试,但以下说明适宜的方法和材料。本文所提及的所有出版物、专利申请、专利和其它的文献均以引用的方式并入。本文所引用的文献不被视为是要求保护的申请的现有技术。在冲突的情况下,以包括定义在内的本说明书为准。另外,材料、方法和实施例仅是说明性的,而非旨在限制。本申请的其它的特征和优点会从以下详细说明以及实施例体现。附图说明图1显示未分级分离的曲妥单抗的阳离子交换色谱概况。图2显示曲妥单抗电荷变体的阳离子交换级分的纯度分析。图3显示流动相梯度的实例,其中向第一流动相缓冲液中随时间加入百分比的第二流动相缓冲液,示出第二流动相缓冲液的百分比。具体实施方式本发明的各方面所涉及的各种术语在整个说明书和权利要求书中使用。除非另有说明,这样的术语被赋予在本领域通常的含义。其它的具体定义的术语以与本文所提供的定义一致的方式解释。当在本文中使用时,除非另有明确的说明,单数形式“一个”、“一种”和“该”包含复数的所指对象。当在本文中使用时,术语“含有”、“具有”和“包含”包括更限制性的术语“基本上由…组成”和“由…组成”。当在本文中使用时,单克隆抗体的“片段”包含但不限于恒定区、可变区、重链、轻链、重链可变区、轻链可变区、重链cdr1、重链cdr2、重链cdr3、轻链cdr1、轻链cdr2和/或轻链cdr3。“功能上活性的”片段可包含能够结合抗原的任何单克隆抗体片段。一致地发现,与盐浓度的调节关联的阳离子交换(cex)色谱洗脱缓冲液的ph的调节可用于从cex载体洗脱特定的抗体电荷变体,以便将重组表达的抗体的制备物中的电荷变体与主要抗体分开。这种特定的技术可被用于获得更高纯度的主要(期望的)抗体分子,抗体制备物由此包含更少的酸性或碱性物类,或可被用于控制抗体制备物中特定变体的水平,例如以便使生物相似的抗体制备物匹配参比抗体制备物(例如以便作为生物相似的产品通过监管审查和维持状态)。包含变体物类(例如电荷物类)关系到抗体制备物的最终效力。因此,这些技术可被用于确定由特定的电荷物类对总体效力所作的积极或消极贡献,由此可富集制备物以包含更少的降低效力的电荷物类,并同时适当保留不影响或增强抗体制备物的总体效力的电荷物类。这些技术可以某种目的被用于改变纯化方案中的处理步骤,所述目的例如减少效力较差的电荷变体以便生产生物增强的抗体,或相对于参比产品抗体尽可能一致地维持生物相似的抗体的电荷变体概况。因此,本公开的特征在于用于分离在生物反应器中重组表达的单克隆抗体的电荷变体的方法。另外,本公开的特征在于调节单克隆抗体制备物中的电荷变体水平的方法。本公开的方法适合于其制备物包含电荷变体的任何重组表达的抗体(在本文中术语电荷变体和电荷物类可互换使用)。在一些优选的非限制性的实施方案中,抗体特异性结合her-2/neu上的表位,且该表位可为线性表位或构象表位。本文所说明的电荷变体分离方法既适合于同时含有可变区和恒定区的全长单克隆抗体,也适合于抗体衍生物以及全长抗体的片段和/或部分。在一些实施方案中,抗体为曲妥单抗。作为非限制性实例,抗体可包含具有seqidno:1的氨基酸序列的重链和/或具有seqidno:2的氨基酸序列的轻链。在一个优选的实施方案中,抗体包含重链恒定区和/或轻链恒定区。使用哺乳动物细胞表达抗体。适宜的哺乳动物表达宿主的非限制性实例包含中国仓鼠卵巢(cho)细胞和人胚肾293(hek293)细胞以及sp2/0和ns0细胞。一旦表达,则抗体可通过两阶段深层过滤或离心方法从其哺乳动物宿主细胞澄清。在深层过滤之后,可将材料通过0.2µm过滤器以得到澄清的细胞培养物上清液。然后,可使包含主要(期望的)抗体及其电荷变体和其它变体连同其它的细胞蛋白和可溶的细胞材料的澄清的细胞培养物上清液经受纯化方案,以分离主要抗体及其电荷变体。作为第一步,可将抗体制备物(在此早期时间点,澄清的细胞培养物上清液)加载到含有蛋白a的载体上,由此抗体与蛋白a相互作用。载体可含有可填充至色谱柱中的颗粒。蛋白a可具有约10g/l~约100g/l、约10g/l~约60g/l或约20g/l~约50g/l的抗体结合能力。mabselectsure®蛋白a介质为适宜的蛋白a载体的实例。unospheresupratm介质、prosep®ultraplus蛋白a介质和absolute®highcap蛋白a介质为适宜的蛋白a载体的其它的实例。可使用本领域可用的任何适宜的蛋白a载体。将抗体制备物加载到蛋白a载体上在一定温度下以一定体积进行一段时间,所述温度、体积和时间适合于使得单克隆抗体能够最大程度地吸附到蛋白a配体。在色谱过程中不吸附于蛋白a的不期望的材料流过载体,而包含fc区的抗体及其变体附着于载体上的蛋白a配体。为了进一步除去附着于配体或附着于抗体蛋白的不期望的材料,可洗涤吸附有抗体的载体。可使用任何适宜的次数的洗涤,且洗涤可含有缓冲液和足够除去不期望的材料而不从蛋白a洗脱抗体的严格性。在洗涤之后,将单克隆抗体及其变体从蛋白a载体洗脱。洗脱可在一定温度下以一定体积进行一定的时间,所述温度、体积和时间适合于使得从蛋白a配体得到单克隆抗体的最大洗脱收率。洗脱缓冲液可为酸性。单克隆抗体的洗脱产生含有单克隆抗体以及抗体变体的洗脱液。对于曲妥单抗的过程开发或生产,重要的是分析支持,例如准确确定过程控制步骤中的酸性变体和碱性变体的电荷概况以及百分比)。将来自2个独立运行的重量百分比分解的实例示出于表1。表1.蛋白a洗脱液的曲妥单抗电荷变体结果实例样品描述%酸性%主要%碱性蛋白洗脱液样品140.744.714.6蛋白洗脱液样品242.741.915.4可任选处理包含单克隆抗体的洗脱液以灭活洗脱液中存在的任何病毒。病毒灭活可包括在一定温度下将洗脱液酸化一段时间,所述温度和时间足以将洗脱液中存在的任何病毒灭活。酸化例如可通过向洗脱液中加入醋酸、柠檬酸、盐酸、甲酸或其组合至得到期望的ph而发生。可在酸化前、酸化过程中或酸化后加热洗脱液。一旦处于期望的灭活温度,则将洗脱液在该ph和温度下维持足够将洗脱液中的实质上所有潜伏病毒灭活的一段时间。在经过该病毒灭活维持时间后,可提高洗脱液的ph,例如通过加入适宜的碱性缓冲液。在病毒灭活步骤之后,或若不包含病毒灭活则在蛋白a洗脱之后,可将单克隆抗体用第二色谱步骤进一步纯化。在该色谱步骤过程中,可分离电荷变体。色谱技术为阳离子交换(cex)色谱。cex色谱介质可包含含有磺丙基(sulfapropyl)配体的载体。适宜的介质的非限制性实例包含capto®spimpres介质。在一些实施方案中,色谱介质包含含有羧甲基、磷酸酯、磺乙基或磺酸酯配体的载体。可将配体与任何适宜的载体连接,所述载体可包含琼脂糖、陶瓷、亲水聚合物、聚合物珠、聚苯乙烯-二乙烯基苯或聚乙烯基醚载体。载体可含有可填充至色谱柱中的颗粒。可将来自蛋白a色谱步骤的洗脱液(其可以是来自病毒灭活步骤的过滤的洗脱液)加载到cex色谱载体上,并使其流过载体,由此使抗体与配体相互作用。将包含单克隆抗体的流通合并物(flow-throughpool)加载到cex载体上在一定温度以一定体积进行一定的时间,所述温度、体积和时间适合于使得单克隆抗体能够最大程度地吸附到配体载体。主要抗体分子以及变体吸附于载体。不吸附于配体载体的不期望的材料在色谱过程中流过载体。为了进一步除去附着于配体的不期望的材料,可洗涤吸附有抗体的载体。cex色谱可与hplc偶联,以便更好地使分开可视化,并最终收集分开的电荷变体(和主要抗体)。大量加载到cex柱上可影响hplc峰分辨率和分离的抗体变体的收率。关于最佳加载,可考虑各分离的同种型的收率与纯度之间的平衡。观察到约1mg/各柱加载的蛋白质量提供合适的收率和纯度平衡。然后,可从cex配体洗脱酸性电荷变体,同时保留主要抗体和碱性电荷变体。在洗脱酸性电荷变体之后,从cex配体洗脱主要抗体,同时保留碱性电荷变体。在洗脱主要抗体之后,从cex配体洗脱碱性变体。由于(相继地)洗脱各抗体同种型,所以其作为分开的纯化级分被收集。收集分离的电荷变体作为实质上没有其它电荷变体以及主要抗体分子的级分。抗体的电荷变体的分级分离可结合cex和hplc技术,并使用两种流动相以改变缓冲条件,从而可从cex配体相继地洗脱各电荷变体。相对于第一流动相,第二流动相包含更高的盐和更高的ph,向第一流动相缓冲溶液中加入第二流动相缓冲溶液,以便建立相继地洗脱电荷变体的盐和ph梯度。随着电荷变体洗脱,它们被收集至单独的级分中。在一些实施方案中,第一流动相缓冲液含有约20mm~约30mm的2-(n-吗啉代)乙磺酸(mes)。mes缓冲液可作为mes水合物(游离酸)和mes钠盐的水性组合来制备,以得到期望的浓度。mes可用能够维持约5.9~约6.3且优选约6.1的期望的ph水平的任何适宜缓冲剂代替。可选的缓冲液的非限制性实例为醋酸钠和醋酸缓冲液。第一流动相缓冲液可含有约20mm~约28mm的mes、约21mm~约27mm的mes、约22mm~约26mm的mes、约23mm~约25mm的mes或约24mm的mes,并具有约5.9~约6.3、约6~约6.2或约6.1的ph。在一些实施方案中,第一流动相缓冲液含有约24mm的mes,并具有约6.1的ph。第二流动相缓冲液可含有约40mm的磷酸钠~约60mm的磷酸钠和约90mm~约100mm的氯化钠。磷酸钠可用能够维持约7.8~约8.2且优选约8的期望的ph水平的任何适宜缓冲剂代替。第二流动相缓冲液可含有约45mm的磷酸钠~约55mm的磷酸钠、约46mm的磷酸钠~约54mm的磷酸钠、约47mm的磷酸钠~约53mm的磷酸钠、约48mm的磷酸钠~约52mm的磷酸钠、约49mm的磷酸钠~约50mm的磷酸钠或约50mm的磷酸钠,和约91mm~约99mm的氯化钠、92mm~约98mm的氯化钠、93mm~约97mm的氯化钠、94mm~约96mm的氯化钠或约95mm的氯化钠,并具有约7.8~约8.2、约7.9~约8.1或约8的ph。在一些实施方案中,第二流动相缓冲液含有约50mm的磷酸钠和约95mm的氯化钠,并具有约8的ph。适宜的第二流动相缓冲液的非限制性实例为trizmahcl-trizma碱缓冲液,其可代替磷酸钠使用。在洗脱电荷变体之前,使第一流动相缓冲液通过cex载体。随着第一流动相缓冲液通过cex载体,向第一流动相缓冲液中加入第二流动相缓冲液,直到这些缓冲液的混合物为约90体积%的第一流动相缓冲液和约10体积%的第二流动相缓冲液。可将缓冲液一次性地混合在一起,例如通过加入第二流动相缓冲液以实质上立即达到90%:10%的比例。备选地,可通过向第一流动相缓冲液中注入第二流动相缓冲液,以在一段时间(通常为几分钟)内从100%的第一流动相缓冲液变为90%的第一流动相缓冲液和10%的第二流动相缓冲液的混合物,将缓冲液更逐渐地混合在一起。使90%-10%混合物流过载体足够用该缓冲液组合平衡载体的时间,通常为几分钟。为了洗脱电荷变体,通过增加流过cex载体的第二流动相缓冲液的量和减少流过cex载体的第一流动相缓冲液的量,来梯度增加第二流动相缓冲液的量(以体积计)。随着流通液体(flow-throughliquid)中的盐和ph增加,电荷变体开始相继地从cex配体洗脱:首先是酸性电荷变体,然后是主要抗体(非变体),随后是碱性电荷变体。各变体即酸性变体或碱性变体以及主要抗体可在其洗脱时鉴定,并作为级分收集。随着第二流动相缓冲液的量增加(以体积计),电荷变体通过梯度洗脱相继地洗脱。第二流动相缓冲液的体积从约10%梯度增加至约45%。当第二流动相缓冲液为约45体积%且第一流动相缓冲液为约55体积%时,最后的碱性变体从cex配体洗脱。梯度持续一段时间,通常为几分钟。将适宜的梯度时间的非限制性实例列于以下表2中(时间和量为近似值)。表2.以第一(a)和第二(b)流动相缓冲液的体积百分比计的两步梯度实例随着第二流动相缓冲液的百分比增加,通过cex载体的混合物的ph增加,盐(nacl)的浓度也增加。随着盐和ph增加,抗体依次地从cex配体洗脱:首先洗脱酸性电荷变体,然后洗脱主要抗体,随后洗脱碱性电荷变体。观察到曲妥单抗抗体制备物包含至少十种电荷变体,其中六种为酸性电荷变体,四种为碱性电荷变体。除主要抗体外,还可根据本文所说明或示例的方法分级分离并收集这十种变体的任何子集。对于曲妥单抗,确定用于洗脱各酸性和碱性变体的第二流动相缓冲液的体积百分比以及ph和盐(nacl)浓度。将变体和主要抗体的cex概况示出于图1中。将洗脱概况概述于表3中。表3.用于同种型的洗脱的流动相组成实例(ph和盐浓度)在各种实施方案中,可分级分离并收集一种或多种抗体变体、两种或更多种抗体变体、三种或更多种抗体变体、四种或更多种抗体变体、五种或更多种抗体变体、六种或更多种抗体变体、七种或更多种抗体变体、八种或更多种抗体变体、九种或更多种抗体变体和/或十种或更多种抗体变体。无需分开并收集所有抗体变体。在一些实施方案中,仅将所选择的变体与抗体制备物分开,例如降低总抗体制备物的效力的那些变体。可保留增强或不影响总抗体制备物的效力的电荷变体。相对于主要抗体的效力,测量来自电荷变体的效力贡献。收集的各变体是实质上纯的,且实质上没有其它的电荷变体以及主要抗体。收集的电荷变体具有至少约90%的纯度。例如,级分中收集的至少约90重量%的材料(例如蛋白内容物)为电荷变体。收集的电荷变体具有至少约91%、92%、93%、94%、95%、96%、97%、98%和/或99%的纯度。这样的百分比基于级分中收集的材料(例如蛋白)的重量。根据本文所说明和示例的技术,电荷变体以及主要抗体的分级分离和分离可重复任何适宜的次数,例如用多种细胞培养物表达的抗体制备物。重复方法共同地增加各抗体同种型的总体收率,这对于例如将抗体配制为治疗剂是期望的。因此,可将抗体的级分混合在一起。混合的级分可任选地根据本领域的任何适宜程序浓缩。在一些优选的实施方案中,仅将主要抗体的纯化的级分混合在一起,使得所得的制备物实质上不含酸性电荷变体和碱性电荷变体。在一些实施方案中,仅将特定的酸性电荷变体或碱性电荷变体的纯化的级分混合在一起——例如将纯化的酸性变体1的一种级分与纯化的酸变体1的另外的级分混合,而不与其它的酸性变体或其它的碱性变体或主要抗体混合。通过将相同的电荷变体级分混合在一起,可测试特定的电荷变体相对于例如主要抗体或抗体的其它电荷变体的效力。可将所选择的变体的级分与其它的所选择的变体的级分和/或与主要抗体的级分混合。作为实例而非限制,可将纯化的酸性变体1的级分与纯化的酸性变体4的级分混合,或可将纯化的酸性变体3的级分与纯化的酸性变体5和主要抗体的级分混合,等等。将变体和/或主要抗体混合在一起可调整为特定的效力值。例如,抗体制备物的电荷变体的分离使得能够单独地评估各变体的相对亲和力、免疫效应子作用、生物学活性和/或其它的特性,从而可确定各电荷变体整体上对抗体制备物的治疗功效有何贡献——积极的或消极的。一旦确定电荷变体降低治疗性抗体制备物的效力,则可期望在纯化方案期间分离这样的电荷变体。若确定特定的电荷变体增强治疗性抗体制备物的效力,则可期望保留这样的电荷变体,而不是在纯化方案期间收集它,或关于其被分离并收集的程度,可期望在制备治疗性抗体制剂时将该变体与主要抗体合并在一起。备选地,可期望将具有增强的效力的电荷变体配制为单独的治疗性抗体制剂。在生物相似的生产中,监管机构(例如美国食品药品监督管理局(fda)或欧洲药品局(europeanmedicinesagency,ema))可能要求生物相似的抗体制备物维持与参比抗体制备物近似的酸性和/或碱性电荷变体与主要抗体的比例。因此,本文所说明和示例的方法可在匹配这样的比例方面显示出功用,因为所述方法使得能够通过选择性洗脱或通过重新组合所收集的级分来控制抗体制备物中电荷变体的量。通过选择性除去降低抗体制备物的治疗功效的电荷变体和/或通过建立更高水平纯度的主要抗体,所述方法可在建立生物增强的抗体制备物方面显示出功用。提供以下实施例以更详细地说明本发明。这些实施例旨在说明本发明,而非限制本发明。实施例1材料与方法在生物反应器细胞培养物中重组表达曲妥单抗,并且首先采用蛋白a亲和色谱纯化。然后使蛋白a纯化的抗体制备物经受包括阳离子交换色谱在内的后续的色谱纯化步骤。典型地,通过分析型cex色谱分析从中间过程控制(in-processcontrol)步骤取样的材料,以评估电荷变体,并将期望的抗体与这些带电同种型分开。dionex为柱制造商。用于cex柱的树脂含有无孔性芯颗粒,其中亲水层具有与芯珠连接的羧化的官能团。使用装备有级分收集器的agilent1260bio-inerthplc系统,实现曲妥单抗的主峰与酸性和碱性电荷变体的分开。将具有10微米粒径且尺寸为内径9mm和长度250mm的半制备型propac™wcx-10柱用于电荷变体的分离。用注射用水(wfi)重构为约25mg/ml的曲妥单抗用于电荷同种型的分离。流动相(mp)a包含24mm的mes缓冲液,ph为6.1,而流动相(mp)b包含50mm的磷酸钠缓冲液和95mm的氯化钠,ph为8.0。用两步mp梯度从柱洗脱同种型,所述梯度是在5分钟内b相从10%达到30%,随后在25分钟内b相从30%达到45%。将柱和自动取样器温度分别设定为35℃和5℃。流动相流速为2.0ml/min,进样体积为40µl,采用uv在280nm下检测,且运行时间为45分钟。将具有10微米粒径且尺寸为内径4mm和长度250mm的分析型propac™wcx-10柱用于未分级分离的曲妥单抗电荷变体的分析,或用于分离的电荷同种型级分的数量和纯度的评估。除用于分析型柱的mp流速设定为0.5ml/min以外,流动相组合物和梯度与用于半制备规模的那些相同。为了将各同种型浓缩为约1mg/ml的目标浓度,对分离的级分进行缓冲液更换,换为曲妥单抗制剂缓冲液。将未分级分离的曲妥单抗的cex色谱概况实例示出于图1中。将分离的级分的叠加的cex色谱图的实例示出于图2中。将cex色谱的两步梯度流动相概况的实例示出于图3中。等同物在以上所附的说明中示出了本发明的一个或多个实施方案的细节。虽然与本文所说明的那些相似或等同的任何方法和材料可用于实施或测试本发明,但现在说明优选的方法和材料。上述说明仅提供用于说明的目的,而不旨在将本发明限制为所公开的精确形式,而是通过在此附加的权利要求书来限制。序列表曲妥单抗重链(seqidno:1)曲妥单抗轻链(seqidno:2)<110>jang,eungangloff,scottpandey,pradeepjerajani,kushal<120>用于分开单克隆抗体的同种型的方法<130>onbi-007/001wo<160>2<170>patentinversion3.5<210>1<211>449<212>prt<213>人工序列<220><223>合成构建体<400>1gluvalglnleuvalgluserglyglyglyleuvalglnproglygly151015serleuargleusercysalaalaserglypheasnilelysaspthr202530tyrilehistrpvalargglnalaproglylysglyleuglutrpval354045alaargiletyrprothrasnglytyrthrargtyralaaspserval505560lysglyargphethrileseralaaspthrserlysasnthralatyr65707580leuglnmetasnserleuargalagluaspthralavaltyrtyrcys859095serargtrpglyglyaspglyphetyralametasptyrtrpglygln100105110glythrleuvalthrvalserseralaserthrlysglyproserval115120125pheproleualaproserserlysserthrserglyglythralaala130135140leuglycysleuvallysasptyrpheprogluprovalthrvalser145150155160trpasnserglyalaleuthrserglyvalhisthrpheproalaval165170175leuglnserserglyleutyrserleuserservalvalthrvalpro180185190serserserleuglythrglnthrtyrilecysasnvalasnhislys195200205proserasnthrlysvalasplyslysvalgluprolyssercysasp210215220lysthrhisthrcysproprocysproalaprogluleuleuglygly225230235240proservalpheleupheproprolysprolysaspthrleumetile245250255serargthrprogluvalthrcysvalvalvalaspvalserhisglu260265270aspprogluvallyspheasntrptyrvalaspglyvalgluvalhis275280285asnalalysthrlysproargglugluglntyrasnserthrtyrarg290295300valvalservalleuthrvalleuhisglnasptrpleuasnglylys305310315320glutyrlyscyslysvalserasnlysalaleuproalaproileglu325330335lysthrileserlysalalysglyglnproarggluproglnvaltyr340345350thrleuproproserarggluglumetthrlysasnglnvalserleu355360365thrcysleuvallysglyphetyrproseraspilealavalglutrp370375380gluserasnglyglnprogluasnasntyrlysthrthrproproval385390395400leuaspseraspglyserphepheleutyrserlysleuthrvalasp405410415lysserargtrpglnglnglyasnvalphesercysservalmethis420425430glualaleuhisasnhistyrthrglnlysserleuserleuserpro435440445gly<210>2<211>214<212>prt<213>人工序列<220><223>合成构建体<400>2aspileglnmetthrglnserproserserleuseralaservalgly151015aspargvalthrilethrcysargalaserglnaspvalasnthrala202530valalatrptyrglnglnlysproglylysalaprolysleuleuile354045tyrseralaserpheleutyrserglyvalproserargphesergly505560serargserglythraspphethrleuthrileserserleuglnpro65707580gluaspphealathrtyrtyrcysglnglnhistyrthrthrpropro859095thrpheglyglnglythrlysvalgluilelysargthrvalalaala100105110proservalpheilepheproproseraspgluglnleulyssergly115120125thralaservalvalcysleuleuasnasnphetyrproarggluala130135140lysvalglntrplysvalaspasnalaleuglnserglyasnsergln145150155160gluservalthrgluglnaspserlysaspserthrtyrserleuser165170175serthrleuthrleuserlysalaasptyrglulyshislysvaltyr180185190alacysgluvalthrhisglnglyleuserserprovalthrlysser195200205pheasnargglyglucys210当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1