与TMEM132A结合的抗体、抗癌剂、以及癌症检查方法与流程
本发明提供与tmem132a结合的抗体、抗癌剂、以及癌症检查方法。
背景技术:
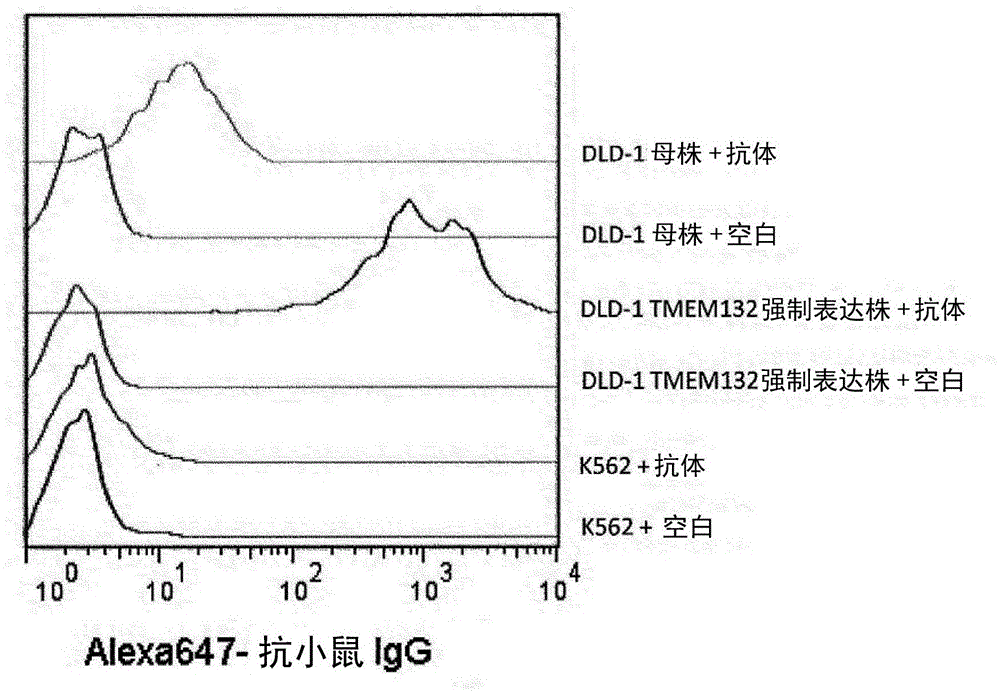
:近年来,作为抗癌剂,正在开发多种特异性地作用于特定分子的分子靶向药物。特别是,以在某种癌细胞中特异性地表达的分子、在癌细胞中表达水平亢进的分子作为抗原的各种抗体医药的开发正在推进中。在这类抗体医药的开发中,首先,将在手术时采集的癌组织中的mrna表达与从其附近采集的正常组织中的mrna的表达进行比较,确定出仅在癌组织中特异性地表达的分子、在癌组织中表达水平亢进的分子,将其作为抗原来制作抗体。大肠癌是从大肠粘膜的细胞产生的癌症。迄今为止,开发出作为以表皮生长因子受体(epidermalgrowthfactorreceptor;egfr)作为靶标的抗体的西妥昔单抗(cetuximab),并将其应用于大肠癌中(非专利文献1-3)。然而,由于egfr在正常组织中也会表达,因此西妥昔单抗有可能也作用于正常组织,期望开发出以更加特异性地在大肠癌中表达的分子作为靶标的分子靶向药物。就这一点而言,由于发生大肠癌的粘膜组织仅少量地存在,因此存在难以通过比较癌化的粘膜细胞与正常的粘膜细胞来确定靶分子的问题。对于该问题,正在开发tmem-180作为靶分子的候选(专利文献1)。现有技术文献专利文献专利文献1:wo2016039321a1非专利文献非专利文献1:cunninghamd.etal.,thenewenglandjournalofmedicine.,vol.351,no.4,2004,p.p.337-345.非专利文献2:goldsteinni.etal.,clincancerres.vol.1,1311-1318,1995.非专利文献3:karapetiscs.etal.,thenewengljmed.vol.359,1757-1765.技术实现要素:发明所要解决的问题本发明提供与tmem132a结合的抗体、抗癌剂、以及癌症检查方法。本发明人等发现,tmem132a蛋白质在癌症中特异性地表达。另外,本发明人等发现,tmem132a蛋白质的表达的有无可以特别地用于大肠癌的诊断。本发明人等还发现,tmem132a蛋白质在癌症的细胞表面露出,并且与tmem132a蛋白质结合的抗体能够与癌细胞的表面结合。本发明是基于这些见解的发明。例如,根据本发明,可以提供以下的发明。[1]一种抗体或其抗原结合性片段,所述抗体是与tmem132a结合的抗体、且为选自以下抗体中的抗体:(1)包含重链可变区和轻链可变区的抗体,所述重链可变区包含具有以序列号1表示的氨基酸序列的重链cdr1、具有以序列号2表示的氨基酸序列的重链cdr2、以及具有以序列号3表示的氨基酸序列的重链cdr3,所述轻链可变区包含具有以序列号5表示的氨基酸序列的轻链cdr1、具有以序列号6表示的氨基酸序列的轻链cdr2、以及具有以序列号7表示的氨基酸序列的轻链cdr3;(2)包含重链可变区和轻链可变区的抗体,所述重链可变区包含具有以序列号9表示的氨基酸序列的重链cdr1、具有以序列号10表示的氨基酸序列的重链cdr2、以及具有以序列号11表示的氨基酸序列的重链cdr3,所述轻链可变区包含具有以序列号13表示的氨基酸序列的轻链cdr1、具有以序列号14表示的氨基酸序列的轻链cdr2、以及具有以序列号15表示的氨基酸序列的轻链cdr3;(3)包含重链可变区和轻链可变区的抗体,所述重链可变区包含具有以序列号17表示的氨基酸序列的重链cdr1、具有以序列号18表示的氨基酸序列的重链cdr2、以及具有以序列号19表示的氨基酸序列的重链cdr3,所述轻链可变区包含具有以序列号5表示的氨基酸序列的轻链cdr1、具有以序列号21表示的氨基酸序列的轻链cdr22、以及具有以序列号7表示的氨基酸序列的轻链cdr23;以及(4)包含重链可变区和轻链可变区的抗体,所述重链可变区包含具有以序列号25表示的氨基酸序列的重链cdr1、具有以序列号26表示的氨基酸序列的重链cdr2、以及具有以序列号27表示的氨基酸序列的重链cdr3,所述轻链可变区包含具有以序列号29表示的氨基酸序列的轻链cdr1、具有以序列号30表示的氨基酸序列的轻链cdr2、以及具有以序列号31表示的氨基酸序列的轻链cdr3;以及(5)在上述(1)~(4)的抗体与tmem132a的结合中竞争的抗体;以及(6)在上述(1)~(4)的抗体和其cdr的氨基酸序列中具有一个至多个氨基酸的插入、取代、缺失或添加的抗体。[2]根据上述[1]中记载的抗体或其抗原结合性片段,其中,抗体为:(1)包含重链可变区和轻链可变区的抗体,所述重链可变区包含具有以序列号1表示的氨基酸序列的重链cdr1、具有以序列号2表示的氨基酸序列的重链cdr2、以及具有以序列号3表示的氨基酸序列的重链cdr3,所述轻链可变区包含具有以序列号5表示的氨基酸序列的轻链cdr1、具有以序列号6表示的氨基酸序列的轻链cdr2、以及具有以序列号7表示的氨基酸序列的轻链cdr3;或者在上述(1)中记载的抗体与tmem132a的结合中竞争的抗体。[3]根据上述[2]中记载的抗体或其抗原结合性片段,其中,包含具有以序列号4表示的重链可变区的氨基酸序列的重链可变区、和具有以序列号8表示的轻链可变区的氨基酸序列的轻链可变区。[4]根据上述[1]中记载的抗体或其抗原结合性片段,其中,抗体为:(2)包含重链可变区和轻链可变区的抗体,所述重链可变区包含具有以序列号9表示的氨基酸序列的重链cdr1、具有以序列号10表示的氨基酸序列的重链cdr2、以及具有以序列号11表示的氨基酸序列的重链cdr3,所述轻链可变区包含具有以序列号13表示的氨基酸序列的轻链cdr1、具有以序列号14表示的氨基酸序列的轻链cdr2、以及具有以序列号15表示的氨基酸序列的轻链cdr3;或者在上述(2)中记载的抗体与tmem132a的结合中竞争的抗体。[5]根据上述[4]中记载的抗体或其抗原结合性片段,其中,包含具有以序列号12表示的重链可变区的氨基酸序列的重链可变区、和具有以序列号16表示的轻链可变区的氨基酸序列的轻链可变区。[6]根据上述[1]中记载的抗体或其抗原结合性片段,其中,抗体为:(3)包含重链可变区和轻链可变区的抗体,所述重链可变区包含具有以序列号17表示的氨基酸序列的重链cdr1、具有以序列号18表示的氨基酸序列的重链cdr2、以及具有以序列号19表示的氨基酸序列的重链cdr3,所述轻链可变区包含具有以序列号5表示的氨基酸序列的轻链cdr1、具有以序列号21表示的氨基酸序列的轻链cdr22、以及具有以序列号7表示的氨基酸序列的轻链cdr23;或者在上述(3)中记载的抗体与tmem132a的结合中竞争的抗体。[7]根据上述[6]中记载的抗体或其抗原结合性片段,其中,包含具有以序列号20表示的重链可变区的氨基酸序列的重链可变区、和具有以序列号24表示的轻链可变区的氨基酸序列的轻链可变区。[8]根据上述[1]中记载的抗体或其抗原结合性片段,其中,抗体为:(4)包含重链可变区和轻链可变区的抗体,所述重链可变区包含具有以序列号25表示的氨基酸序列的重链cdr1、具有以序列号26表示的氨基酸序列的重链cdr2、以及具有以序列号27表示的氨基酸序列的重链cdr3,所述轻链可变区包含具有以序列号29表示的氨基酸序列的轻链cdr1、具有以序列号30表示的氨基酸序列的轻链cdr2、以及具有以序列号31表示的氨基酸序列的轻链cdr3;或者在上述(4)中记载的抗体与tmem132a的结合中竞争的抗体。[9]根据上述[8]中记载的抗体或其抗原结合性片段,其中,包含具有以序列号28表示的重链可变区的氨基酸序列的重链可变区、和具有以序列号32表示的轻链可变区的氨基酸序列的轻链可变区。[10]一种癌症诊断试剂,其包含与tmem132a结合的抗体。[11]根据上述[10]中记载的癌症诊断试剂,其中,抗体为以上述[1]~[9]中任一项定义的抗体。[12]一种方法,是在对象中检测癌细胞的方法,该方法包括确定在从对象得到的生物体试样中是否存在tmem132a蛋白质的操作。[13]根据上述[12]中记载的癌细胞的检测方法,其中,利用与tmem132a结合的抗体确定是否存在tmem132a蛋白质。[14]根据上述[13]中记载的癌细胞的检测方法,其中,抗体为以上述[1]~[9]中任一项定义的抗体。[15]一种医药组合物,其包含与tmem132a结合的抗体,用于在处置癌症时使用。[16]根据上述[15]中记载的医药组合物,其中,抗体为以上述[1]~[9]中任一项定义的抗体。[17]根据上述[15]或[16]中记载的医药组合物,其中,抗体为与细胞毒性剂的缀合物的形态。附图说明图1是表示在癌细胞的表面表达出tmem132a蛋白质的图。图2是表示新得到的抗tmem132a单克隆抗体可以将使tmem132a蛋白质强制表达的dld-1株染色的图。图3是表示对大肠癌组织板用抗tmem132a单克隆抗体染色的结果的图。图4是表示对正常脑组织及正常心脏组织用抗tmem132a单克隆抗体染色的结果的图。图5是表示对正常肺组织及正常肝脏组织用抗tmem132a单克隆抗体染色的结果的图。图6是表示对正常肾脏组织及正常小肠组织用抗tmem132a单克隆抗体染色的结果的图。图7是表示对正常皮肤用抗tmem132a单克隆抗体染色的结果的图。具体实施方式本说明书中,所谓“对象”,可以是哺乳动物,优选为人。对象可以是罹患间皮瘤或其他肿瘤或癌症的、或存在该风险的对象。本说明书中,所谓“处置”,是指治疗及预防。因而,本说明书中所谓“在处置癌症时使用的医药组合物”,是指在治疗或预防癌症时使用的医药组合物,以包含抗癌剂作为一例的意味使用。本说明书中,“抗体”是指免疫球蛋白,包含多克隆抗体及单克隆抗体。优选的抗体为单克隆抗体。抗体的来源没有特别限定,例如可以举出非人动物的抗体、非人哺乳动物的抗体、以及人抗体。另外,抗体也可以是嵌合抗体、人源化抗体、或人抗体。另外,抗体也可以是双特异性抗体。抗体采取2条重链与2条轻链缔合而成的结构。重链包含重链可变区(vh)、重链恒定区(ch1)、铰链区、ch2、以及ch3,轻链包含轻链可变区(vl)和轻链恒定区(cl)。本说明书中,所谓“抗原结合性片段”,是指维持了与抗原的结合性的抗体的一部分。抗原结合性片段可以包含本发明的抗体的重链可变区或轻链可变区或其双方。抗原结合性片段也可以被嵌合化或人源化。作为抗原结合性片段,例如可以举出fab、fab’、f(ab’)2、fv、scfv(单链fv)、二聚抗体(diabody)、sc(fv)2(单链(fv)2)。这类抗体的片段没有特别限定,例如可以用酶处理抗体而得到。例如,若用木瓜蛋白酶消化抗体,则可以得到fab。或者,若用胃蛋白酶消化抗体,则可以得到f(ab’)2,若将其进一步还原,则可以得到fab’。本发明中可以使用这类抗体的抗原结合性片段。根据本发明,可以提供与tmem132a结合、且选自以下抗体中的抗体、或其抗原结合性片段:(1)包含重链可变区和轻链可变区的抗体,所述重链可变区包含具有以序列号1表示的氨基酸序列的重链cdr1、具有以序列号2表示的氨基酸序列的重链cdr2、以及具有以序列号3表示的氨基酸序列的重链cdr3,所述轻链可变区包含具有以序列号5表示的氨基酸序列的轻链cdr1、具有以序列号6表示的氨基酸序列的轻链cdr2、以及具有以序列号7表示的氨基酸序列的轻链cdr3;(2)包含重链可变区和轻链可变区的抗体,所述重链可变区包含具有以序列号9表示的氨基酸序列的重链cdr1、具有以序列号10表示的氨基酸序列的重链cdr2、以及具有以序列号11表示的氨基酸序列的重链cdr3,所述轻链可变区包含具有以序列号13表示的氨基酸序列的轻链cdr1、具有以序列号14表示的氨基酸序列的轻链cdr2、以及具有以序列号15表示的氨基酸序列的轻链cdr3;(3)包含重链可变区和轻链可变区的抗体,所述重链可变区包含具有以序列号17表示的氨基酸序列的重链cdr1、具有以序列号18表示的氨基酸序列的重链cdr2、以及具有以序列号19表示的氨基酸序列的重链cdr3,所述轻链可变区包含具有以序列号5表示的氨基酸序列的轻链cdr1、具有以序列号21表示的氨基酸序列的轻链cdr22、以及具有以序列号7表示的氨基酸序列的轻链cdr23;(4)包含重链可变区和轻链可变区的抗体,所述重链可变区包含具有以序列号25表示的氨基酸序列的重链cdr1、具有以序列号26表示的氨基酸序列的重链cdr2、以及具有以序列号27表示的氨基酸序列的重链cdr3,所述轻链可变区包含具有以序列号29表示的氨基酸序列的轻链cdr1、具有以序列号30表示的氨基酸序列的轻链cdr2、以及具有以序列号31表示的氨基酸序列的轻链cdr3;(5)在上述(1)~(4)的抗体与tmem132a的结合中竞争的抗体;(6)在上述(1)~(4)的抗体和其cdr的氨基酸序列中具有一个至多个氨基酸的插入、取代、缺失或添加的抗体;(7)具有与上述(1)~(4)的抗体的重链可变区及轻链可变区的氨基酸序列具有80%以上的同源性的重链可变区及轻链可变区的抗体;以及(8)作为cdr具有上述(1)~(4)的抗体的cdr中的1个、2个、3个、4个、5个、或全部的抗体。根据本发明,可以提供与tmem132a结合的抗体或其抗原结合性片段,它们是(1)包含重链可变区和轻链可变区的抗体,所述重链可变区包含具有以序列号1表示的氨基酸序列的重链cdr1、具有以序列号2表示的氨基酸序列的重链cdr2、以及具有以序列号3表示的氨基酸序列的重链cdr3,所述轻链可变区包含具有以序列号5表示的氨基酸序列的轻链cdr1、具有以序列号6表示的氨基酸序列的轻链cdr2、以及具有以序列号7表示的氨基酸序列的轻链cdr3;在上述(1)中记载的抗体与tmem132a的结合中竞争的抗体;在上述(1)中记载的抗体和其cdr的氨基酸序列中具有一个至多个氨基酸的插入、取代、缺失或添加的抗体;或作为cdr具有上述(1)中记载的抗体的cdr中的1个、2个、3个、4个、5个、或全部的抗体;或其抗原结合性片段。根据本发明,可以提供与tmem132a结合的抗体或其抗原结合性片段,它们是(1a)包含具有以序列号4表示的重链可变区的氨基酸序列的重链可变区、和具有以序列号8表示的轻链可变区的氨基酸序列的轻链可变区的抗体;在上述(1a)中记载的抗体与tmem132a的结合中竞争的抗体;在上述(1a)中记载的抗体和其cdr的氨基酸序列中具有一个至多个氨基酸的插入、取代、缺失或添加的抗体;或作为cdr具有上述(1a)中记载的抗体的cdr中的1个、2个、3个、4个、5个、或全部的抗体;或其抗原结合性片段。根据本发明,可以提供与tmem132a结合的抗体或其抗原结合性片段,它们是(2)包含重链可变区和轻链可变区的抗体,所述重链可变区包含具有以序列号9表示的氨基酸序列的重链cdr1、具有以序列号10表示的氨基酸序列的重链cdr2、以及具有以序列号11表示的氨基酸序列的重链cdr3,所述轻链可变区包含具有以序列号13表示的氨基酸序列的轻链cdr1、具有以序列号14表示的氨基酸序列的轻链cdr2、以及具有以序列号15表示的氨基酸序列的轻链cdr3;在上述(2)中记载的抗体与tmem132a的结合中竞争的抗体;在上述(2)中记载的抗体和其cdr的氨基酸序列中具有一个至多个氨基酸的插入、取代、缺失或添加的抗体;或作为cdr具有上述(2)中记载的抗体的cdr中的1个、2个、3个、4个、5个、或全部的抗体;或其抗原结合性片段。根据本发明,可以提供与tmem132a结合的抗体或其抗原结合性片段,它们是(2a)包含具有以序列号12表示的重链可变区的氨基酸序列的重链可变区、和具有以序列号16表示的轻链可变区的氨基酸序列的轻链可变区的抗体、在上述(2a)中记载的抗体与tmem132a的结合中竞争的抗体、在上述(2a)中记载的抗体和其cdr的氨基酸序列中具有一个至多个氨基酸的插入、取代、缺失或添加的抗体;或作为cdr具有上述(2a)中记载的抗体的cdr中的1个、2个、3个、4个、5个、或全部的抗体;或其抗原结合性片段。根据本发明,可以提供与tmem132a结合的抗体或其抗原结合性片段,它们是(3)包含重链可变区和轻链可变区的抗体,所述重链可变区包含具有以序列号17表示的氨基酸序列的重链cdr1、具有以序列号18表示的氨基酸序列的重链cdr2、以及具有以序列号19表示的氨基酸序列的重链cdr3,所述轻链可变区包含具有以序列号5表示的氨基酸序列的轻链cdr1、具有以序列号21表示的氨基酸序列的轻链cdr22、以及具有以序列号7表示的氨基酸序列的轻链cdr23;在上述(3)中记载的抗体与tmem132a的结合中竞争的抗体;在上述(3)中记载的抗体和其cdr的氨基酸序列中具有一个至多个氨基酸的插入、取代、缺失或添加的抗体;或作为cdr具有上述(3)中记载的抗体的cdr中的1个、2个、3个、4个、5个、或全部的抗体;或其抗原结合性片段。根据本发明,可以提供与tmem132a结合的抗体或其抗原结合性片段,它们是(3a)包含具有以序列号20表示的重链可变区的氨基酸序列的重链可变区、和具有以序列号24表示的轻链可变区的氨基酸序列的轻链可变区的抗体;在上述(3a)中记载的抗体与tmem132a的结合中竞争的抗体、在上述(3a)中记载的抗体和其cdr的氨基酸序列中具有一个至多个氨基酸的插入、取代、缺失或添加的抗体;或作为cdr具有上述(3a)中记载的抗体的cdr中的1个、2个、3个、4个、5个、或全部的抗体;或其抗原结合性片段。根据本发明,可以提供与tmem132a结合的抗体或其抗原结合性片段,它们是(4)包含重链可变区和轻链可变区的抗体,所述重链可变区包含具有以序列号25表示的氨基酸序列的重链cdr1、具有以序列号26表示的氨基酸序列的重链cdr2、以及具有以序列号27表示的氨基酸序列的重链cdr3,所述轻链可变区包含具有以序列号29表示的氨基酸序列的轻链cdr1、具有以序列号30表示的氨基酸序列的轻链cdr2、以及具有以序列号31表示的氨基酸序列的轻链cdr3;在上述(4)中记载的抗体与tmem132a的结合中竞争的抗体;在上述(4)中记载的抗体和其cdr的氨基酸序列中具有一个至多个氨基酸的插入、取代、缺失或添加的抗体;或作为cdr具有上述(4)中记载的抗体的cdr中的1个、2个、3个、4个、5个、或全部的抗体;或其抗原结合性片段。根据本发明,可以提供与tmem132a结合的抗体或其抗原结合性片段,它们是(4a)包含具有以序列号28表示的重链可变区的氨基酸序列的重链可变区、和具有以序列号32表示的轻链可变区的氨基酸序列的轻链可变区抗体、在上述(4a)中记载的抗体与tmem132a的结合中竞争的抗体、在上述(4a)中记载的抗体和其cdr的氨基酸序列中具有一个至多个氨基酸的插入、取代、缺失或添加的抗体;或作为cdr具有上述(4a)中记载的抗体的cdr中的1个、2个、3个、4个、5个、或全部的抗体;或其抗原结合性片段。根据本发明,可以提供一种抗体,其是与tmem132a结合的抗体或其抗原结合性片段,并且其与tmem132a的细胞外区域的一部分结合。在本发明的某个方式中,tmem132a的细胞外区域的一部分没有特别限定,例如可以是genbankaccessionno.:np_060340的氨基酸序号143~317位的区域或氨基酸序号411~597位的区域。本说明书中,所谓“具有一个至多个氨基酸的插入、取代、缺失或添加”,只要是可以获得具有与tmetm132a的结合性的抗体,则无论具有何种插入、取代、缺失或添加都可以。所谓“具有一个至多个氨基酸的插入、取代、缺失或添加”,例如可以以包含具有1个、2个、3个或4个氨基酸的插入、取代、缺失或添加的意味来使用。氨基酸的取代例如可以设为保守性的氨基酸的取代。只要是本领域技术人员,则可以利用位点特异性突变导入法等实现这类插入、取代、缺失或添加。另外,有时也在竞争抗体中发现这类插入、取代、缺失或添加。本说明书中,所谓“具有80%以上的同源性”,是指在相对于参照抗体确认目标抗体的氨基酸序列的同源性的情况下,以使氨基酸序列的一致达到最大的方式比对2个氨基酸序列时,共同的氨基酸的个数相对于参照抗体的氨基酸序列为80%以上。上述同源性可以设为80%以上,可以设为85%以上,可以设为90%以上,可以设为95%以上,可以设为98%以上,可以设为99%以上。只要是本领域技术人员,就可以利用位点特异性突变导入法等实现“具有80%以上的同源性的”抗体。另外,有时也在竞争抗体中发现这类插入、取代、缺失或添加。本发明的抗体可以以抗原作为tmem132a蛋白质(例如,人tmem132a的氨基酸序列可以设为genbankaccessionno.:np_060340)利用本领域技术人员公知的方法得到。即,通过用抗原和佐剂对动物进行免疫、获得免疫了的动物的血浆,可以得到多克隆抗体。或者,也可以用抗原和佐剂对动物进行免疫,从免疫了的动物获得b淋巴细胞,使之与骨髓瘤进行细胞融合而形成杂交瘤,对产生所期望的抗体的杂交瘤进行克隆而得到。嵌合抗体可以利用本领域中公知的方法来制作。例如,可以通过将抗体的恒定区替换为人的抗体的恒定区来制作。人源化抗体例如包含来自人以外的动物的互补性决定区(cdr)和来自人抗体的框架区及来自人抗体的恒定区。人源化抗体例如可以将上述的cdr移植到人抗体中而得到。人抗体例如可以通过对产生人抗体的基因改造小鼠进行抗原的免疫而得到。双特异性抗体是可以与2种不同的表位或抗原结合的抗体,可以利用本领域技术人员公知的方法制备。双特异性抗体例如可以利用如下方法来制作,即,将2个产生不同抗体的细胞进一步融合,制作杂化杂交瘤;或者使vh区域和vl区域借助在上述2个区域间无法形成配对的短的连接体在1条多肽链上表达,与另外的多肽链、即与所述vh区域和vl区域形成配对的具有互补的vh区域和vl区域的多肽链形成复合体。在某个抗体与抗原的结合中竞争的抗体可以利用本领域技术人员公知的竞争测定等得到。竞争测定中,例如若可以阻断至少20%、优选为至少20~50%、更优选为至少50%的所期望的抗体的结合,则可以在与相同抗原的结合中作为进行竞争的抗体。进行竞争的抗体可以利用交叉阻断测定、优选利用竞争elisa测定进行确认。交叉阻断测定中,将抗原涂布于例如微量滴定板上、向其中添加成为候选的竞争抗体存在并进行温育,形成抗原与候选抗体的结合。其后,在标记所期望的抗体后再添加到孔中并进行温育,清洗,对所期望的抗体的结合量进行定量,由此可以判断抗体是否进行了竞争。在进行竞争的情况下,残留于孔中的标记量应当变少。根据本发明,tmem132a在癌细胞中广泛地表达。tmem132a特别是在上皮性的癌细胞(例如大肠癌细胞、胰脏癌细胞、卵巣癌细胞、以及乳腺癌细胞)中表达。另一方面,tmem132a在正常组织中观察不到表达。因而,根据本发明,可以提供一种方法,是癌症诊断方法,包括确定在从对象得到的生物体试样中是否存在tmem132a蛋白质的操作。另外,根据本发明,提供一种方法,是癌细胞的检测方法,包括确定在从对象得到的生物体试样中是否存在tmem132a蛋白质的操作。根据本发明,可以使用与tmem132a结合的抗体,确定是否存在tmem132a蛋白质。根据本发明,可以使用本发明的抗体,确定是否存在tmem132a蛋白质。本发明的癌症诊断方法可以还包括对诊断为癌症的对象实施化学疗法及放射线疗法等癌症的治疗法。根据本发明,tmem132a在癌细胞的细胞表面露出。因而,根据本发明,可以提供与tmem132a结合的抗体与细胞毒性剂的缀合物。作为本发明中所用的细胞毒性剂,例如可以举出具有抗癌活性的物质。具有抗癌活性的物质是指在与癌接触的情况下产生癌的尺寸的减小、癌的尺寸的增大的延迟或停止、癌的增殖的延迟或停止、或癌的转移的阻碍的物质。作为具有抗癌活性的物质,可以举出抗癌剂、毒素、以及放射性同位素等,可以在本发明中使用。另外,根据本发明,可以提供包含与tmem132a结合的抗体与细胞毒性剂的缀合物的、用于在处置癌症时使用的医药组合物。癌症可以设为上皮性的癌症(例如大肠癌、胰脏癌、卵巣癌、以及乳腺癌)。本发明的某个方式中,本发明的抗体可以具有抗体依赖性细胞毒活性(adcc活性)或补体依赖性细胞毒活性(cdc活性)等细胞毒活性。特别是由于tmem132a是在癌细胞的表面露出的蛋白质,因此优选作为本发明的抗体的靶标。抗体从提高其adcc活性的观点考虑,例如可以将恒定区中所用的人的抗体的亚型设为igg1。抗体从提高其adcc活性的观点考虑,例如也可以是在fc区结合1个以上的n-结合型糖链、在该n-结合型糖链的还原末端的n-乙酰葡萄糖胺没有结合岩藻糖的抗体。作为有效成分包含本发明的抗体的医药组合物或药剂可以利用公知的制剂学方法进行制剂化。例如本发明的医药组合物或药剂可以包含药学上可以容许的赋形剂。赋形剂可以设为能够为了向对象提供作为有效成分的本发明的抗体的有效量而恰当地施用的赋形剂。某个方式中,本发明的医药组合物或药剂可以设为注射剂,注射用的赋形剂可以设为无菌的水性溶液,例如林格氏液、hank′s溶液或生理盐水等药学上可以容许的缓冲液、包含葡萄糖或其他辅助剂的等渗液。作为辅助剂,可以举出乙醇等醇、聚乙二醇等多元醇、聚山梨醇酯80等非离子性表面活性剂等,可以在制剂化时添加。作为注射用的油性液,可以使用芝麻油、椰子油及大豆油,作为辅助剂,可以使用苯甲酸苄酯或苄基醇。本发明的医药组合物或药剂可以以注射剂的形式进行非经口施用(例如静脉内施用或胸腔内施用)。抗体的adcc活性或cdc活性可以利用本领域技术人员公知的方法测定。adcc活性例如可以通过将癌细胞和表达fc受体的效应细胞(例如nk细胞、单核细胞)在本发明的抗体的存在下在生理条件下进行温育、并计数间皮瘤细胞的活细胞数和/或死细胞数来确定。cdc活性例如可以通过将癌细胞在包含补体的溶液(例如人血清)和抗体存在下在生理条件下进行温育、并计数癌细胞的活细胞数和/或死细胞数来确定。细胞毒活性可以利用本领域技术人员公知的各种方法来增强。例如已知有利用缺失了fc区糖链的岩藻糖的抗体、在糖链上结合有平分型n-乙酰葡萄糖胺(glcnac)的抗体、fc区的氨基酸取代来增强效应细胞的fc受体与抗体的结合并由此增强细胞毒活性的方法,如此所述地改造了的抗体也可以作为本发明的抗体使用。以使人的抗体自身的抗原性降低等为目的,抗体可以利用本领域技术人员公知的方法制成基因改造抗体、例如嵌合抗体、人源化抗体或人抗体。在本发明的医药组合物或药剂中,本发明的抗体可以是嵌合抗体、人源化抗体或人抗体。另外,抗体也可以是双特异性抗体。另外,根据本发明,可以提供本发明的抗体或其抗原结合性片段与成像探针(イメージングプローブ)的缀合物。根据本发明,可以提供包含本发明的抗体或其抗原结合性片段与成像探针的缀合物的用于在对癌症进行成像时所用的组合物、癌症诊断试剂盒、或癌症诊断试剂。用于在对癌症进行成像时所用的组合物、癌症诊断试剂盒、或癌症诊断试剂中,癌症可以设为上皮性的癌细胞(例如大肠癌细胞、胰脏癌细胞、卵巣癌细胞、以及乳腺癌细胞)。作为本发明中可以使用的成像探针,例如可以举出荧光成像探针、核磁共振成像(mri)用造影剂等增强剂(例如顺磁性离子)及pet分子成像探针等成像用的放射性核素。根据本发明,可以提供用于制造处置癌症的医药的与tmem132a结合的抗体或其抗原结合性片段的用途。根据本发明,可以提供用于在对癌症进行成像时使用的组合物、癌症诊断试剂盒、或用于制造癌症诊断试剂的与tmem132a结合的抗体或其抗原结合性片段的用途。根据本发明,可以提供一种方法,是在有该必要的对象中处置癌症的方法,该方法包括对所述对象施用与tmem132a结合的抗体的操作。另外,根据本发明,提供一种方法,是在有该必要的对象中处置癌症的方法,该方法包括对所述对象施用与tmem132a结合的抗体或其抗原结合性片段与细胞毒性剂的缀合物的操作。[实施例]实施例1:tmem132a蛋白质的纯化与单克隆抗体的制作本实施例中,为了取得针对tmem132a蛋白质的抗体,作为抗原制作tmem132a蛋白质而得到纯化蛋白质。1)抗原制作对导入了tmem132a的基因的载体(origenerc214846),使用以下的引物依照常法进行了pcr扩增。作为dna聚合酶,使用primestarhsdnapolymerase(takarar010a),以向各个抗原的c末端添加6×his标签序列的方式进行了设计。免疫抗原i扩增用引物序列catatgttccacctcaaagggcaggattg(序列号33)gtcgaccttgaagcggtctagcttggcagtc(序列号34)免疫抗原ii扩增用引物序列catatgaatacagcaccactgactggagtg(序列号35)gtcgacttccagagaggctacacgcgagtccag(序列号36)此处,免疫抗原i对应于tmem132a的细胞外区域的一部分(genbankaccessionno.:np_060340的氨基酸序号143~317位的区域)。免疫抗原ii对应于tmem132a的细胞外区域的另外的一部分(genbankaccessionno.:np_060340的氨基酸序号411~597位的区域)。然后,将所得的pcr扩增产物导入表达载体pet21b。具体而言,对pet21b和pcr扩增产物,分别依照制造者的操作流程使ndei及sali(takara)反应2小时。其后,利用1%琼脂糖凝胶电泳分离dna切割片段,从凝胶中切出后使用promegawizardsvgalandpcrclean-upsystem试剂盒进行纯化。使用ligationhigh(东洋纺)使上述表达载体与包含免疫抗原i或ii的插入片段反应30分钟。使用competenthighdh5α(东洋纺)进行转化,在lb培养基(50μg/ml)平板中培养。从转化了的大肠菌中提取质粒,进行序列分析,确认目标基因被插入了载体。然后,对具有目标基因的表达载体通过转化导入作为蛋白质表达用大肠杆菌的bl21(de3)。其后,对经过转化的bl21(de3)进行克隆。将经过转化的bl21(de3)接种到10ml的lb培养基中,将在37℃培养16小时的培养基转移至1l的lb培养基中,在37℃培养。在od600nm的值达到0.6时,以使最终浓度为1mm的方式添加iptg而诱发基因表达,再培养4小时。4小时后,对大肠菌进行菌体破碎,将其沉淀物悬浮于改性缓冲液(50mmtris-hcl、500mmnacl、6m盐酸胍)中,使之浸透16小时后,回收样品的上清液,用镍柱纯化。2)tmem132a强制表达株细胞的制作将导入了tmem132a基因(genbankaccessionno.:nm_017870.3)及flag序列的pires2-acgfp1(clontech)质粒0.5μg用0.1ml的opti-mem(invitrogen)稀释,添加2.5μl的lipofectionamineltx,得到转染用的调配液。在室温下静置25分钟后,将利用上述操作得到的调配液添加到包含dld1细胞(4×104细胞/孔)的24孔板(corning)中。转染后,将0.5mg/ml的g418(thermofisher)加入培养基,对于培养了14天的细胞,使用facsaria细胞分选仪(bd),仅取得gfp表达细胞。将所得的细胞在96孔板中超稀释(限外希釈)。对细胞的菌落单一的孔,进行蛋白质印迹。将可以确认到flag序列的细胞设为强制表达细胞。3)抗体制作将用pbs稀释为1mg/ml的上述免疫抗原i或免疫抗原ii与弗氏完全佐剂(freundcompleteadjuvant)以1:1混合,将所制备的乳液对小鼠(日本slc、balb/c、雌性、6~8周龄)腹腔内分别施用100μl。以后每14天对腹腔施用与佐剂(gerbuadjuvant100、gerbugmbh.等)混合的免疫抗原。从第3次的免疫起免疫7天后,使用用pbs从100个尾静脉采血、制备的抗血清,利用使免疫抗原固相化的elisa或对dld-1细胞或k562细胞的流式细胞术评价血清抗体效价,选择用于细胞融合的免疫小鼠个体。对判断为抗体效价充分地提高的个体,作为最终免疫将用pbs稀释为1μg/ml的免疫抗原从腹腔施用100μl,从尾静脉施用400μl。从最终免疫起3天后摘出脾脏、髂骨淋巴结、腹股沟淋巴结、腋下淋巴结及膝下淋巴结,利用peg法与小鼠骨髓瘤细胞p3x63融合。在融合10天至14天后回收杂交瘤的培养上清液。利用流式细胞术选择对dld-1细胞呈现阳性、对dld-1tmem132a强制表达细胞呈现强阳性、对k562细胞呈现阴性的产生抗体的杂交瘤细胞。将所选择的产生抗体的杂交瘤细胞利用有限稀释法单克隆化,建立细胞株。如此所述地操作,由免疫抗原ii得到t6-0429克隆、t6-1022克隆、以及t6-1179克隆,由免疫抗原i得到t6-1475克隆。将由这些克隆得到的单克隆抗体称作t6-0429抗体、t6-1022抗体、t6-1179抗体及t6-1475抗体。利用同种型特异性elisa(bethyl)判定抗体的同种型。t6-0429抗体为igg2a,t6-1022抗体为igg2a,t6-1179抗体为igg1,此外t6-1475抗体为igg2a。实施例2:利用与tmem132a结合的单克隆抗体的癌细胞的识别能力本实施例中发现,与tmem132a结合的单克隆抗体不与正常组织反应,另一方面,识别癌细胞。流式细胞术将作为测定对象的癌细胞悬浮于培养基中,以达到1×105个/孔的方式添加到v底96孔板(corning)中。将板以440×g、4℃离心3分钟后除去上清液,向细胞团块以50μl/孔加入产生抗体的杂交瘤培养上清液或抗体溶液并悬浮。在4℃反应45分钟后,以0.1%bsa/2mmedta/pbs200μl/孔清洗3次。除去上清液,向细胞团块以50μl/孔加入二次抗体并悬浮。需要说明的是,作为二次抗体,使用了将alexafluor647山羊抗大鼠igg(h-l)(lifetechnologies)用0.1%bsa/2mmedta/pbs稀释为400倍的二次抗体。在4℃反应45分钟后,以0.1%bsa/2mmedta/pbs200μl/孔清洗3次。除去上清液,向细胞团块以200μl/孔加入1μg/ml碘化丙啶/0.1%bsa/2mmedta/pbs并悬浮。使用guavaeasycyte8ht(merckmillipore)等流式细胞仪测定如此所述地染色的细胞,对所得的数据利用flowjo(tomydigitalbiology)进行了分析。如上述流式细胞仪的方法所示,使用人大肠癌细胞株dld-1或实施例1中制作的tmem132a强制表达dld-1株或tmem132a阴性的细胞株k562和t6-0429抗体确认了抗体的癌细胞识别能力。利用进行了alexa647标记的抗小鼠igg抗体检测出t6-0429抗体。结果如图1所示。如图1所示,可知在dld-1株上结合作为tmem132a抗体的t6-0429抗体。另外,可知在tmem132a强制表达dld-1株中,更多地结合t6-0429抗体。此外,对于k562株,无法确认到t6-0429抗体的结合。根据该结果可知,tmem132a可以检测大肠癌。另外还可知,tmem1232a在癌的细胞膜上露出。然后显示出,通过使用大肠癌组织阵列,与tmem132a结合的单克隆抗体可以检测出大肠癌。首先,为了确认t6-0429抗体为免疫组织学染色中可以利用的抗体,以dld-1株和tmem132a强制表达dld-1株作为对象,使用t6-0429抗体进行了免疫化学染色。首先,将适量的细胞接种于腔室载玻片,在37℃进行孵化(过夜)。除去上清液,用dpbs清洗孔后,添加冷丙酮(丙酮固定)。在室温静置10分钟,用pbs-t清洗3次后,添加3%h2o2(用超纯水稀释30%h2o2)。在室温静置20分钟。用pbs-t清洗3次后,添加包含5%脱脂牛奶的pbs-t,在室温静置30分钟。用pbs-t清洗3次后,添加hrp直接标记-t6-0429抗体(10μg/ml),在室温静置1小时。用pbs-t清洗3次后,进行dab染色(在室温静置5分钟)。用超纯水清洗后,进行苏木素染色(在室温静置2分钟)。浸渍于自来水中,进行10分钟静置。继而,分别在乙醇中进行2分钟×3次浸渍,在二甲苯中进行2分钟×3次浸渍,使之脱水透彻。使用mount-quick封入,使之干燥后,利用显微镜观察了染色像。结果如图2所示。如图2所示,人大肠癌细胞株dld-1为t6-0429抗体阳性。另外,tmem132a强制表达dld-1株强烈地表达tmem132a,对t6-0429抗体显示出强阳性反应。大肠癌组织阵列从biochaininstitueinc.(newark,ca)获得,用于实验。依照制造者手册,将各组织阵列染色。作为抗体使用了t6-0429抗体(10μg/ml)。结果如图3所示。如图3所示,在正常大肠组织中,无法得到可以利用t6-0429抗体检出的染色像,然而对于大肠癌组织,其三成左右为t6-0429抗体阳性。该结果显示,与tmem132a结合的抗体可以检出大肠癌。乳腺癌组织阵列也从biochaininstitueinc.(newark,ca)获得,同样地进行了确认,其结果是发现约20%为阳性。该结果显示,与tmem132a结合的抗体可以检出乳腺癌。此外,使用t6-0429抗体(10μg/ml)确认了是否可以识别正常组织。由正常组织样品基于常法制作石蜡切片,使用t6-0429抗体(10μg/ml)进行了免疫组织学染色。具体而言,使薄切样品或冷冻保存样品风干(在室温下30分钟左右)。添加冷丙酮,在室温静置10分钟(丙酮固定)。用pbs-t清洗3次后,添加3%h2o2(用超纯水稀释30%h2o2),在室温静置20分钟。用pbs-t清洗3次后,添加包含5%脱脂牛奶的pbs-t,在室温静置30分钟。用pbs-t清洗3次后,添加hrp直接标记t6-0429抗体(10μg/ml),在室温静置1小时。用pbs-t清洗3次后,进行了dab染色(在室温静置5分钟)。用超纯水清洗后,依照常法进行了苏木素染色(在室温静置2分钟)。浸渍于自来水中,静置10分钟。再分别在乙醇中进行2分钟×3次浸渍,在二甲苯中进行2分钟×3次浸渍,使之脱水透彻。使用mount-quick封入,使之干燥后,利用显微镜观察了染色像。结果如图4~7所示。如图4~7所示,t6-0429抗体在皮肤、脑、小肠、肝脏、心脏、肺及肾脏的任意一个的正常组织中均为阴性。但是,在正常皮肤组织中确认到有限的阳性部位(参照图7)。另外,使用抗tmem132a抗体,尝试了利用各种上皮性癌细胞株的facs的检测。具体而言,将作为测定对象的癌细胞悬浮于培养基中,以达到1×105个/孔的方式添加到v底96孔板(corning)中。将板以440×g、4℃离心3分钟后除去上清液,向细胞团块以50μl/孔加入产生抗体的杂交瘤培养上清液或抗体溶液并悬浮。在冰上反应45分钟后,以0.1%bsa/2mmedta/pbs200μl/孔清洗3次。除去上清液,向细胞团块以50μl/孔加入二次抗体并悬浮。作为二次抗体,使用了将alexafluor647山羊抗大鼠igg(h-l)(lifetechnologies)用0.1%bsa/2mmedta/pbs稀释为400倍的二次抗体。在冰上反应45分钟后,以0.1%bsa/2mmedta/pbs200μl/孔清洗3次。除去上清液,向细胞团块以250μl/孔加入50ng/ml碘化丙啶/0.1%bsa/2mmedta/pbs并悬浮。使用guavaeasycyte8ht(merckmillipore)等流式细胞仪测定如此所述地染色的细胞,对所得的数据利用flowjo(tomydigitalbiology)进行了分析。作为癌细胞株,使用了乳腺癌细胞株、大肠癌细胞株、卵巣癌细胞株、胰脏癌细胞株。结果如下述表1所示。[表1]表1:癌细胞株的细胞表面的tmem132a的表达细胞株的来源阳性株数/总株数乳腺癌细胞株2/4大肠癌细胞株7/7卵巢癌细胞株3/5胰脏癌细胞株10/10(对于3个细胞为与herceptine同等以上的反应)如表1所示,通过facs分析表明,tmem132a在乳腺癌细胞株、大肠癌细胞株、卵巣癌细胞株及胰脏癌细胞株等癌细胞的细胞表面广泛地表达。该结果表明,抗tmem132a抗体对于癌症的检测而言有用。另外还暗示,通过使抗tmem132a抗体保持adcc活性或cdc活性(例如将抗体的同种型变换为igg1、igg3等adcc活性高的异形体),对于癌症的处置而言有用。实施例3:单克隆抗体的序列确定本实施例中,确定了单克隆抗体的重链可变区及轻链可变区的序列。从实施例1中得到的t6-0429克隆、t6-1022克隆、t6-1179克隆及t6-1475克隆中,使用rneasyminikit(qiagen)提取总rna。由上述总rna,使用smarterrace5’/3’kit(takara)利用5’末端race(cdna末端快速扩增)法合成出cdna。以所得的cdna作为模板,使用kodfxneo(东洋纺)扩增了目标基因。使用了递降pcr法,其扩增条件为:变性98℃、10秒,退火68℃、30秒,延伸72℃、90秒5循环,变性98℃、10秒,退火65℃、30秒,延伸68℃、90秒5循环,变性98℃、10秒,退火63℃、30秒,延伸68℃、90秒25循环。pcr使用pcr装置(appliedbiosystemproflexpcrsystem)实施。在上述pcr中,使用了以下的引物序列。重链用正向引物:ctaatacgactcactatagggcaagcagtggtatcaacgcagagt(序列号37)或ctaatacgactcactatagggc(序列号38)重链用反向引物:cccatggccaccarattctyatcagacag(序列号39)轻链用正向引物:ctaatacgactcactatagggcaagcagtggtatcaacgcagagt(序列号40)ctaatacgactcactatagggc(序列号41)轻链用反向引物:gttgttcawgargcacacgactgaggca(序列号42)对扩增了的h链及l链的pcr产物使用targetclone-plus-(东洋纺)进行ta克隆。克隆后,转化到dh5α(东洋纺),从单菌落中使用plasmidminikit(qiagen)提取质粒。对克隆了的h链、l链各自的基因使用abiprism3100基因测序仪分析出基因的碱基序列。结果如以下表中所示。在重链可变区中,氨基酸序号1~19位为信号序列,在轻链可变区中,氨基酸序号1~20为信号序列。但是,关于t6-1475克隆的重链可变区,氨基酸序号1~18位为信号序列。t6-0429克隆的重链可变区(序列号4)cdr1:序列号1、cdr2:序列号2、cdr3:序列号3[化1]t6-0429克隆的轻链可变区(序列号8)cdr1:序列号5、cdr2:序列号6、cdr3:序列号7[化2]t6-1022克隆的重链可变区(序列号12)cdr1:序列号9、cdr2:序列号10、cdr3:序列号11[化3]t6-1022克隆的轻链可变区(序列号16)cdr1:序列号13、cdr2:序列号14、cdr3:序列号15[化4]t6-1179克隆的重链可变区(序列号20)cdr1:序列号17、cdr2:序列号18、cdr3:序列号19[化5]t6-1179克隆的轻链可变区(序列号24)cdr1:序列号21、cdr2:序列号22、cdr3:序列号23[化6]t6-1475克隆的重链可变区(序列号28)cdr1:序列号25、cdr2:序列号26、cdr3:序列号27[化7]t6-1475克隆的轻链可变区(序列号32)cdr1:序列号29、cdr2:序列号30、cdr3:序列号31[化8]在序列表中记载有以下的序列。[表2]序列号序列的内容序列号1~3t6-0429克隆的重链cdr1~3序列号4t6-0429克隆的重链可变区序列号5~7t6-0429克隆的轻链cdr1~3序列号8t6-0429克隆的轻链可变区序列号9~11t6-1022克隆的重链cdr1~3序列号12t6-1022克隆的重链可变区序列号13~15t6-1022克隆的轻链cdr1~3序列号16t6-1022克隆的轻链可变区序列号17~19t6-1179克隆的重链cdr1~3序列号20t6-1179克隆的重链可变区序列号21~23t6-1179克隆的轻链cdr1~3序列号24t6-1179克隆的轻链可变区序列号25~27t6-1475克隆的重链cdr1~3序列号28t6-1475克隆的重链可变区序列号29~31t6-1475克隆的轻链cdr1~3序列号32t6-1475克隆的轻链可变区序列号33免疫抗原i扩增用正向引物序列号34免疫抗原i扩增用反向引物序列号35免疫抗原ii扩增用正向引物序列号36免疫抗原ii扩增用反向引物序列号37重链用正向引物1序列号38重链用正向引物2序列号39重链用反向引物序列号40轻链用正向引物1序列号41轻链用正向引物2序列号42轻链用反向引物当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1