抗-GREMLIN-1(GREM1)抗体及其用于治疗肺动脉高血压的使用方法与流程
本申请要求2016年8月29日提交的u.s.临时专利申请no.62/380,562的优先权权益,其全部内容由此通过引用并入本文。
序列表
本申请包含以ascii格式电子提交的序列表且由此通过引用全文并入。2017年8月10日生成的所述ascii拷贝名称为118003_28820_sl.txt且大小为195,927字节。
背景技术:
肺动脉高血压(pah)是一种进行性疾病,其特征是肺动脉压的持续升高,这同时损害大和小的肺动脉。pah血流动力学定义为大于30mmhg的收缩期肺动脉压或大于25mmhg的平均肺动脉压及肺毛细血管或左心房压等于或小于15mmhg的评估。参见,例如,zaiman等,am.j.respir.cellmoi.biol.33:425-31(2005)。pah中持续的血管收缩导致结构重构,在此期间肺血管平滑肌细胞和内皮细胞经历从收缩性正常表型到合成型表型的表型转换,导致细胞生长和基质沉积。随着最小血管的壁增厚,它们在血液和肺部之间正常转移氧和二氧化碳的能力较低,并且随时间,肺动脉高血压导致肺动脉增厚和血液流过的通道变窄。最终,血管平滑肌和内皮细胞的增殖导致血管的重构及肺血管系统的管腔闭塞。来自肺动脉高血压患者的组织样品的组织学检查显示内膜增厚,以及平滑肌细胞肥大,特别是对于<100μm直径的血管。当血液抽运通过减小的管腔面积时,这导致肺血压逐渐升高。因此,心脏的右侧更难以补偿,并且增加的工作量导致右心室变大和变厚。增大的右心室使人处于肺栓塞的风险中,因为血液倾向于在心室和腿中汇集。如果在汇集的血液中形成凝块,它们最终可能会移动并停留在肺部中。最终,强加于右心室的额外工作量引起心脏衰竭并导致这些患者的过早死亡。
用于治疗患有pah的受试者的标准疗法主要是血液动力学的(其影响血管张力),并且包括例如前列环素类似物、内皮素受体拮抗剂、磷酸二酯酶抑制剂和可溶性鸟苷酸环化酶激活剂/刺激剂(其提供症状缓解和改善预后)。然而,这些疗法是不足的并且不能重建肺血管系统的结构和功能完整性以为患有pah的患者提供无障碍的长期存活。
有许多细胞途径可导致pah的发展和pah中的结构重构,例如转化生长因子-β(tgf-β)途径和/或骨形态发生蛋白(bmp)途径。tgf-β超家族的成员在pah中的致病性作用已通过编码tgf-β受体超家族蛋白bmpr2、acvrl1或eng或者信号转导子smad9的基因中的突变(其增加了人对pah的可遗传形式的易感性)的发现而提出。还已证明pah患者具有降低的bmpr2表达/信号传导(atkinson等circulation.105(14):1672-1678,2002;alastalo等j.clin.invest.121:3735-3746,2011),肺动脉平滑肌细胞的tgf-β激活对伴随bmpr2缺失的生长抑制不敏感(morrell等circulation.104(7):790-7952001;yang等circ.res.102,1212-1221,2008),和bmpr2的bmp9激活逆转了临床前pah(long等natmed.21:777-785,2015)。对bmp的生物反应通过bmp拮抗剂(其可直接与bmp结合并抑制受体结合)负调节。
可直接与bmp结合并抑制受体结合和bmp信号传导的一种这样的拮抗剂是人gremlin-1(grem1),半胱氨酸结超家族的一个成员(hsu,d.r.等1998,mol.cell1:673-683),其以高亲和力结合bmp2、bmp4和bmp7(yanagita等(2005)cytokinegrowthfactorrev16:309-317)。已发现在缺氧期间grem1在小鼠的小型肺内血管的壁中升高。gremlin1的单倍体不足增强了bmp信号传导,并且通过抑制血管重构与降低的血管阻力相关(cahill等(2012)circulation125(7):920-30)。此外,在缺氧条件下人肺内皮细胞中grem1表达增加(costello等(2008)amjphysiollungcellmolphysiol295(2):l272-84)并且grem1在特发性和遗传性pah患者的肺的重构血管中表达(cahill等(2012)circulation125(7):920-30)。
然而,尽管pah的治疗中取得的所有进展,但尚无治愈这种致命疾病的前景,并且大多数患者继续发展为右心室衰竭。因此,本领域需要靶向由tgfβ和bmp途径调节的血管重构以通过抑制grem1来降低tgfβ信号传导和增加bmp信号传导的临床上有益的方法和组合物。
技术实现要素:
本发明至少部分地基于以下发现:抗gremlin-1(grem1)抗体或其抗原结合片段在肺动脉高血压动物模型中有效地缓解血管重构的效应。
因此,在一个方面,本发明提供治疗患有肺动脉高血压(pah)的受试者的方法。该方法包括向受试者施用治疗有效量的抗-grem1抗体或其抗原结合片段,其中抗-grem11抗体或其抗原结合片段施用于受试者抑制受试者中肺动脉的增厚,从而治疗患有pah的受试者。
在另一方面,本发明提供了治疗患有肺动脉高血压(pah)的受试者的方法。该方法包括向受试者施用治疗有效量的抗-grem1抗体或其抗原结合片段,其中向受试者施用抗-grem1抗体或其抗原结合片段增加受试者的每搏输出量,从而治疗患有pah的受试者。
在又一方面,本发明提供了治疗患有肺动脉高血压(pah)的受试者的方法。该方法包括向受试者施用治疗有效量的抗-grem1抗体或其抗原结合片段,其中向受试者施用抗-grem1抗体或其抗原结合片段增加受试者的右心室心输出量,从而治疗患有pah的受试者。
在另一方面,本发明提供了治疗患有肺动脉高血压(pah)的受试者的方法。该方法包括向受试者施用治疗有效量的抗-grem1抗体或其抗原结合片段,其中向受试者施用抗-grem1抗体或其抗原结合片段延长受试者的存活时间,从而治疗患有pah的受试者。
在一个实施方案中,受试者是人。
在一个实施方案中,受试者患有i类(who)pah。
本发明的方法还可包括向受试者施用至少一种另外的治疗剂,如抗凝剂、利尿剂、强心苷、钙通道阻滞剂、血管舒张剂、前列环素类似物、内皮拮抗剂、磷酸二酯酶抑制剂、内肽酶抑制剂、降血脂剂和/或血栓烷抑制剂。
用于本发明的抗体或其抗原结合片段可以阻断grem1与骨形态发生蛋白-2(bmp2)、bmp4、bmp7或肝素之一的结合。
在一个实施方案中,抗体或其抗原结合片段表现出选自以下的一种或多种性质:
(a)在37℃下以低于约275nm的结合解离平衡常数(kd)结合grem1,如通过表面等离子体共振测量的;
(b)在37℃下以大于约3分钟的解离半衰期(t1/2)结合grem1,如通过表面等离子体共振测量的;
(c)在25℃下以低于约280nm的kd结合grem1,如通过表面等离子体共振测量的;
(d)在25℃下以大于约2分钟的t1/2结合grem1,如通过表面等离子体共振测量的;
(e)以低于约1.9nm的ic50阻断grem1与bmp4的结合,如在25℃下的竞争elisa分析中测量的;
(f)阻断grem1-介导的bmp信号传导的抑制和促进细胞分化;和
(g)阻断grem1与肝素的结合。
在另一个实施方案中,抗体或其抗原结合片段与包含重链可变区(hcvr)的互补决定区(cdrs)的抗体或其抗原结合片段竞争特异性地结合grem1,其中所述hcvr具有选自seqidno:2、18、34、50、66、82、98、114、130、146、162、178、194、210、226、242、258、274、290、306、322、338、354、370、386、402、418、434、450、466、482、498、514、530、546、562和578的氨基酸序列。
在又一个实施方案中,抗体或其抗原结合片段与包含轻链可变区(lcvr)的cdrs的抗体或其抗原结合片段竞争特异性地结合grem1,其中所述lcvr具有选自seqidno:10、26、42、58、74、90、106、122、138、154、170、186、202、218、234、250、266、282、298、314、330、346、362、378、394、410、426、442、458、474、490、506、522、538、554、570和586的氨基酸序列。
在一个实施方案中,抗体或其抗原结合片段包含选自seqidno:2、18、34、50、66、82、98、114、130、146、162、178、194、210、226、242、258、274、290、306、322、338、354、370、386、402、418、434、450、466、482、498、514、530、546、562和578的重链可变区(hcvr)序列任一中所含的三个重链互补决定区(cdrs)(hcdr1、hcdr2和hcdr3);和选自seqidno:10、26、42、58、74、90、106、122、138、154、170、186、202、218、234、250、266、282、298、314、330、346、362、378、394、410、426、442、458、474、490、506、522、538、554、570和586的轻链可变区(lcvr)序列任一中所包含的三个轻链cdrs(lcdr1、lcdr2和lcdr3),例如,抗体或其抗原结合片段包含具有选自seqidno:2、18、34、50、66、82、98、114、130、146、162、178、194、210、226、242、258、274、290、306、322、338、354、370、386、402、418、434、450、466、482、498、514、530、546、562和578的氨基酸序列的hcvr;和/或抗体或其抗原结合片段包含具有选自seqidno:10、26、42、58、74、90、106、122、138、154、170、186、202、218、234、250、266、282、298、314、330、346、362、378、394、410、426、442、458、474、490、506、522、538、554、570和586的氨基酸序列的lcvr;和/或抗体或其抗原结合片段包含:(a)具有选自seqidno:2、18、34、50、66、82、98、114、130、146、162、178、194、210、226、242、258、274、290、306、322、338、354、370、386、402、418、434、450、466、482、498、514、530、546、562和578的氨基酸序列的hcvr;和(b)具有选自seqidno:10、26、42、58、74、90、106、122、138、154、170、186、202、218、234、250、266、282、298、314、330、346、362、378、394、410、426、442、458、474、490、506、522、538、554、570和586的氨基酸序列的lcvr。
在另一个实施方案中,抗体或其抗原结合片段包含
(a)具有选自seqidno:4、20、36、52、68、84、100、116、132、148、164、180、196、212、228、244、260、276、292、308、324、340、356、372、388、404、420、436、452、468、484、500、516、532、548、564和580的氨基酸序列的hcdr1域;
(b)具有选自seqidno:6、22、38、54、70、86、102、118、134、150、166、182、198、214、230、246、262、278、294、310、326、342、358、374、390、406、422、438、454、470、486、502、518、534、550、566和582的氨基酸序列的hcdr2域;
(c)具有选自seqidno:8、24、40、56、72、88、104、120、136、152、168、184、200、216、232、248、264、280、296、312、328、344、360、376、392、408、424、440、456、472、488、504、520、536、552、568和584的氨基酸序列的hcdr3域;
(d)具有选自seqidno:12、28、44、60、76、92、108、124、140、156、172、188、204、220、236、252、268、284、300、316、332、348、364、380、396、412、428、444、460、476、492、508、524、540、556、572和588的氨基酸序列的lcdr1域;
(e)具有选自seqidno:14、30、46、62、78、94、110、126、142、158、174、190、206、222、238、254、270、286、302、318、334、350、366、382、398、414、430、446、462、478、494、510、526、542、558、574和590的氨基酸序列的lcdr2域;和/或
(f)具有选自seqidno:16、32、48、64、80、96、112、128、144、160、176、192、208、224、240、256、272、288、304、320、336、352、368、384、400、416、432、448、464、480、496、512、528、544、560、576和592的氨基酸序列的lcdr3域。
在又一个实施方案中,抗体或其抗原结合片段包含选自seqidno:2/10、18/26、34/42、50/58、66/74、82/90、98/106、114/122、130/138、146/154、162/170、178/186、194/202、210/218、226/234、242/250、258/266、274/282、290/298、306/314、322/330、338/346、354/362、370/378、386/394、402/410、418/426、434/442、450/458、466/474、482/490、498/506、514/522、530/538、546/554、562/570和578/586的hcvr/lcvr氨基酸序列对。
在又一个实施方案中,抗体或其抗原结合片段与包含重链可变区(hcvr)的互补决定区(cdrs)和轻链可变区(lcvr)的cdrs的抗体或抗原结合片段结合grem1上的相同表位,其中所述hcvr具有选自seqidno:2、18、34、50、66、82、98、114、130、146、162、178、194、210、226、242、258、274、290、306、322、338、354、370、386、402、418、434、450、466、482、498、514、530、546、562和578的氨基酸序列;且其中所述lcvr具有选自seqidno:10、26、42、58、74、90、106、122、138、154、170、186、202、218、234、250、266、282、298、314、330、346、362、378、394、410、426、442、458、474、490、506、522、538、554、570和586的氨基酸序列。
在其它实施方案中,适合用于本发明中的抗体或其抗原结合片段是结合人grem1的全人单克隆抗体或其抗原结合片段,其中该抗体或其片段表现出以下特性中的一种或多种:(i)包含具有选自seqidno:2、18、34、50、66、82、98、114、130、146、162、178、194、210、226、242、258、274、290、306、322、338、354、370、386、402、418、434、450、466、482、498、514、530、546、562和578的氨基酸序列或其具有至少90%、至少95%、至少98%或至少99%序列同一性的基本上相似的序列的hcvr;(ii)包含具有选自seqidno:10、26、42、58、74、90、106、122、138、154、170、186、202、218、234、250、266、282、298、314、330、346、362、378、394、410、426、442、458、474、490、506、522、538、554、570和586的氨基酸序列或其具有至少90%、至少95%、至少98%或至少99%序列同一性的基本上相似的序列的lcvr;(iii)包含具有选自seqidno:8、24、40、56、72、88、104、120、136、152、168、184、200、216、232、248、264、280、296、312、328、344、360、376、392、408、424、440、456、472、488、504、520、536、552、568和584的氨基酸序列或其具有至少90%、至少95%、至少98%或至少99%序列同一性的基本上相似的序列的hcdr3域;和具有选自seqidno:16、32、48、64、80、96、112、128、144、160、176、192、208、224、240、256、272、288、304、320、336、352、368、384、400、416、432、448、464、480、496、512、528、544、560、576和592的氨基酸序列或其具有至少90%、至少95%、至少98%或至少99%序列同一性的基本上相似的序列的lcdr3域;(iv)包含具有选自seqidno:4、20、36、52、68、84、100、116、132、148、164、180、196、212、228、244、260、276、292、308、324、340、356、372、388、404、420、436、452、468、484、500、516、532、548、564和580的氨基酸序列或其具有至少90%、至少95%、至少98%或至少99%序列同一性的基本上相似的序列的hcdr1域;具有选自seqidno:6、22、38、54、70、86、102、118、134、150、166、182、198、214、230、246、262、278、294、310、326、342、358、374、390、406、422、438、454、470、486、502、518、534、550、566和582的氨基酸序列或其具有至少90%、至少95%、至少98%或至少99%序列同一性的基本上相似的序列的hcdr2域;具有选自seqidno:12、28、44、60、76、92、108、124、140、156、172、188、204、220、236、252、268、284、300、316、332、348、364、380、396、412、428、444、460、476、492、508、524、540、556、572和588的氨基酸序列或其具有至少90%、至少95%、至少98%或至少99%序列同一性的基本上相似的序列的lcdr1域;和具有选自seqidno:14、30、46、62、78、94、110、126、142、158、174、190、206、222、238、254、270、286、302、318、334、350、366、382、398、414、430、446、462、478、494、510、526、542、558、574和590的氨基酸序列或其具有至少90%、至少95%、至少98%或至少99%序列同一性的基本上相似的序列的lcdr2域;(v)以等于或低于10-7m的kd结合grem1;(vi)阻断grem1与bmp2、bmp4或bmp7中的一个的结合;(vii)阻断bmp信号传导的grem1抑制和促进细胞分化;和(viii)阻断grem1与肝素的结合。
在一个实施方案中,适合用于本发明的方法中的分离的人抗体或其抗原结合片段以等于或低于10-7m的kd结合grem1,如通过表面等离子体共振测量的。
在一个实施方案中,用于本发明的方法中的结合grem1的分离的人抗体或其抗原结合片段包含选自seqidno:2、18、34、50、66、82、98、114、130、146、162、178、194、210、226、242、258、274、290、306、322、338、354、370、386、402、418、434、450、466、482、498、514、530、546、562和578的重链可变区(hcvr)序列任一中所含的三个重链互补决定区(cdrs)(hcdr1、hcdr2和hcdr3);和选自seqidno:10、26、42、58、74、90、106、122、138、154、170、186、202、218、234、250、266、282、298、314、330、346、362、378、394、410、426、442、458、474、490、506、522、538、554、570和586的轻链可变区(lcvr)序列任一中所含的三个轻链cdrs(lcdr1、lcdr2和lcdr3)。
在一个实施方案中,本发明的方法包括使用结合grem1并包含选自seqidno:2/10、18/26、34/42、50/58、66/74、82/90、98/106、114/122、130/138、146/154、162/170、178/186、194/202、210/218、226/234、242/250、258/266、274/282、290/298、306/314、322/330、338/346、354/362、370/378、386/394、402/410、418/426、434/442、450/458、466/474、482/490、498/506、514/522、530/538、546/554、562/570和578/586的hcvr/lcvr氨基酸序列对的分离的人抗体或其抗原结合片段。
在另一个实施方案中,本发明的方法包括使用结合grem1的分离的人抗体或其抗原结合片段,其中该抗体或其片段表现出以下的一种或多种特性:(i)包含具有选自seqidno:2、18、34、50、66、82、98、114、130、146、162、178、194、210、226、242、258、274、290、306、322、338、354、370、386、402、418、434、450、466、482、498、514、530、546、562和578的氨基酸序列或其具有至少90%、至少95%、至少98%或至少99%序列同一性的基本上相似的序列的hcvr;(ii)包含具有选自seqidno:10、26、42、58、74、90、106、122、138、154、170、186、202、218、234、250、266、282、298、314、330、346、362、378、394、410、426、442、458、474、490、506、522、538、554、570和586的氨基酸序列或其具有至少90%、至少95%、至少98%或至少99%序列同一性的基本上相似的序列的lcvr;(iii)包含具有选自seqidno:8、24、40、56、72、88、104、120、136、152、168、184、200、216、232、248、264、280、296、312、328、344、360、376、392、408、424、440、456、472、488、504、520、536、552、568和584的氨基酸序列或其具有至少90%、至少95%、至少98%或至少99%序列同一性的基本上相似的序列的hcdr3域;和具有选自seqidno:16、32、48、64、80、96、112、128、144、160、176、192、208、224、240、256、272、288、304、320、336、352、368、384、400、416、432、448、464、480、496、512、528、544、560、576和592的氨基酸序列或其具有至少90%、至少95%、至少98%或至少99%序列同一性的基本上相似的序列的lcdr3域;(iv)包含具有选自seqidno:4、20、36、52、68、84、100、116、132、148、164、180、196、212、228、244、260、276、292、308、324、340、356、372、388、404、420、436、452、468、484、500、516、532、548、564和580的氨基酸序列或其具有至少90%、至少95%、至少98%或至少99%序列同一性的基本上相似的序列的hcdr1域;具有选自seqidno:6、22、38、54、70、86、102、118、134、150、166、182、198、214、230、246、262、278、294、310、326、342、358、374、390、406、422、438、454、470、486、502、518、534、550、566和582的氨基酸序列或其具有至少90%、至少95%、至少98%或至少99%序列同一性的基本上相似的序列的hcdr2域;具有选自seqidno:12、28、44、60、76、92、108、124、140、156、172、188、204、220、236、252、268、284、300、316、332、348、364、380、396、412、428、444、460、476、492、508、524、540、556、572和588的氨基酸序列或其具有至少90%、至少95%、至少98%或至少99%序列同一性的基本上相似的序列的lcdr1域;和具有选自seqidno:14、30、46、62、78、94、110、126、142、158、174、190、206、222、238、254、270、286、302、318、334、350、366、382、398、414、430、446、462、478、494、510、526、542、558、574和590的氨基酸序列或其具有至少90%、至少95%、至少98%或至少99%序列同一性的基本上相似的序列的lcdr2域;(v)以等于或低于10-7的kd结合grem1,如通过表面等离子体共振测量的。
在又一个实施方案中,本发明的方法包括使用结合grem1且包含重链可变区(hcvr)的互补决定区(cdrs)和轻链可变区(lcvr)的cdrs的分离的人抗体或其抗原结合片段,其中该hcvr具有选自seqidno:2、18、34、50、66、82、98、114、130、146、162、178、194、210、226、242、258、274、290、306、322、338、354、370、386、402、418、434、450、466、482、498、514、530、546、562和578的氨基酸序列,和其中该lcvr具有选自seqidno:10、26、42、58、74、90、106、122、138、154、170、186、202、218、234、250、266、282、298、314、330、346、362、378、394、410、426、442、458、474、490、506、522、538、554、570和586的氨基酸序列。
在一个实施方案中,本发明提供包括使用分离的抗体或其抗原结合片段的方法,该抗体或其抗原结合片段与包含重链可变区(hcvr)的cdrs和轻链可变区(lcvr)的cdrs的抗体或其抗原结合片段结合人grem1上的相同表位,其中该hcvr具有选自seqidno:2、18、34、50、66、82、98、114、130、146、162、178、194、210、226、242、258、274、290、306、322、338、354、370、386、402、418、434、450、466、482、498、514、530、546、562和578的氨基酸序列;且其中该lcvr具有选自seqidno:10、26、42、58、74、90、106、122、138、154、170、186、202、218、234、250、266、282、298、314、330、346、362、378、394、410、426、442、458、474、490、506、522、538、554、570和586的氨基酸序列。
在一个实施方案中,本发明的方法包括使用阻断人grem1与bmp2、bmp4、bmp7或肝素任一的结合的分离的人抗体或其抗原结合片段,该抗体包含重链可变区(hcvr)的互补决定区(cdrs)和轻链可变区(lcvr)的cdrs,其中该hcvr具有选自seqidno:2、18、34、50、66、82、98、114、130、146、162、178、194、210、226、242、258、274、290、306、322、338、354、370、386、402、418、434、450、466、482、498、514、530、546、562和578的氨基酸序列,和其中该lcvr具有选自seqidno:10、26、42、58、74、90、106、122、138、154、170、186、202、218、234、250、266、282、298、314、330、346、362、378、394、410、426、442、458、474、490、506、522、538、554、570和586的氨基酸序列。
在另一个实施方案中,本发明包括使用结合grem1的全人单克隆抗体或其抗原结合片段,其中该抗体或其片段表现出以下特性中的一种或多种:(i)包含具有选自seqidno:2、18、34、50、66、82、98、114、130、146、162、178、194、210、226、242、258、274、290、306、322、338、354、370、386、402、418、434、450、466、482、498、514、530、546、562和578的氨基酸序列或其具有至少90%、至少95%、至少98%或至少99%序列同一性的基本上相似的序列的hcvr;(ii)包含具有选自seqidno:10、26、42、58、74、90、106、122、138、154、170、186、202、218、234、250、266、282、298、314、330、346、362、378、394、410、426、442、458、474、490、506、522、538、554、570和586的氨基酸序列或其具有至少90%、至少95%、至少98%或至少99%序列同一性的基本上相似的序列的lcvr;(iii)包含具有选自seqidno:8、24、40、56、72、88、104、120、136、152、168、184、200、216、232、248、264、280、296、312、328、344、360、376、392、408、424、440、456、472、488、504、520、536、552、568和584的氨基酸序列或其具有至少90%、至少95%、至少98%或至少99%序列同一性的基本上相似的序列的hcdr3域;和具有选自seqidno:16、32、48、64、80、96、112、128、144、160、176、192、208、224、240、256、272、288、304、320、336、352、368、384、400、416、432、448、464、480、496、512、528、544、560、576和592的氨基酸序列或其具有至少90%、至少95%、至少98%或至少99%序列同一性的基本上相似的序列的lcdr3域;(iv)包含具有选自seqidno:4、20、36、52、68、84、100、116、132、148、164、180、196、212、228、244、260、276、292、308、324、340、356、372、388、404、420、436、452、468、484、500、516、532、548、564和580的氨基酸序列或其具有至少90%、至少95%、至少98%或至少99%序列同一性的基本上相似的序列的hcdr1域;具有选自seqidno:6、22、38、54、70、86、102、118、134、150、166、182、198、214、230、246、262、278、294、310、326、342、358、374、390、406、422、438、454、470、486、502、518、534、550、566和582的氨基酸序列或其具有至少90%、至少95%、至少98%或至少99%序列同一性的基本上相似的序列的hcdr2域;具有选自seqidno:12、28、44、60、76、92、108、124、140、156、172、188、204、220、236、252、268、284、300、316、332、348、364、380、396、412、428、444、460、476、492、508、524、540、556、572和588的氨基酸序列或其具有至少90%、至少95%、至少98%或至少99%序列同一性的基本上相似的序列的lcdr1域;和具有选自seqidno:14、30、46、62、78、94、110、126、142、158、174、190、206、222、238、254、270、286、302、318、334、350、366、382、398、414、430、446、462、478、494、510、526、542、558、574和590的氨基酸序列或其具有至少90%、至少95%、至少98%或至少99%序列同一性的基本上相似的序列的lcdr2域;(v)以等于或低于10-7m的kd结合grem1,如通过表面等离子体共振测量的;(vi)阻断grem1与bmp2、bmp4或bmp7中的一个的结合;(vii)阻断bmp信号传导的grem1-抑制和促进细胞分化;和(viii)阻断grem1与肝素的结合。
在另一个实施方案中,本发明提供包括使用抗体或其片段的方法,该抗体或其片段包含通过选自seqidno:1、17、33、49、65、81、97、113、129、145、161、177、193、209、225、241、257、273、289、305、321、337、353、369、385、401、417、433、449、465、481、497、513、529、545、561和577的核酸序列或其具有至少90%、至少95%、至少98%或至少99%同源性的基本上相同的序列编码的hcvr。
在一个实施方案中,抗体或其片段还包含通过选自seqidno:9、25、41、57、73、89、105、121、137、153、169、185、201、217、233、249、265、281、297、313、329、345、361、377、393、409、425、441、457、473、489、505、521、537、553、569和585的核酸序列或其具有至少90%、至少95%、至少98%或至少99%同源性的基本上相同的序列编码的lcvr。
在一个实施方案中,本发明的方法包括使用抗体或抗体的抗原结合片段,其包含通过选自seqidno:7、23、39、55、71、87、103、119、135、151、167、183、199、215、231、247、263、279、295、311、327、343、359、375、391、407、423、439、455、471、487、503、519、535、551、567和583的核酸序列或其具有至少90%、至少95%、至少98%或至少99%序列同一性的基本上相似的序列编码的hcdr3域;和通过选自seqidno:15、31、47、63、79、95、111、127、143、159、175、191、207、223、239、255、271、287、303、319、335、351、367、383、399、415、431、447、463、479、495、511、527、543、559、575和591的核酸序列或其具有至少90%、至少95%、至少98%或至少99%序列同一性的基本上相似的序列编码的lcdr3域。
在另一个实施方案中,本发明的方法包括使用抗体或其片段,其还包含通过选自seqidno:3、19、35、51、67、83、99、115、131、147、163、179、195、211、227、243、259、275、291、307、323、339、355、371、387、403、419、435、451、467、483、499、515、531、547、563和579的核酸序列或其具有至少90%、至少95%、至少98%或至少99%序列同一性的基本上相似的序列编码的hcdr1域;通过选自seqidno:5、21、37、53、69、85、101、117、133、149、165、181、197、213、229、245、261、277、293、309、325、341、357、373、389、405、421、437、453、469、485、501、517、533、549、565和581的核酸序列或其具有至少90%、至少95%、至少98%或至少99%序列同一性的基本上相似的序列编码的hcdr2域;通过选自seqidno:11、27、43、59、75、91、107、123、139、155、171、187、203、219、235、251、267、283、299、315、331、347、363、379、395、411、427、443、459、475、491、507、523、539、555、571和587的核酸序列或其具有至少90%、至少95%、至少98%或至少99%序列同一性的基本上相似的序列编码的lcdr1域;和通过选自seqidno:13、29、45、61、77、93、109、125、141、157、173、189、205、221、237、253、269、285、301、317、333、349、365、381、397、413、429、445、461、477、493、509、525、541、557、573和589的核酸序列或其具有至少90%、至少95%、至少98%或至少99%序列同一性的基本上相似的序列编码的lcdr2域。
附图说明
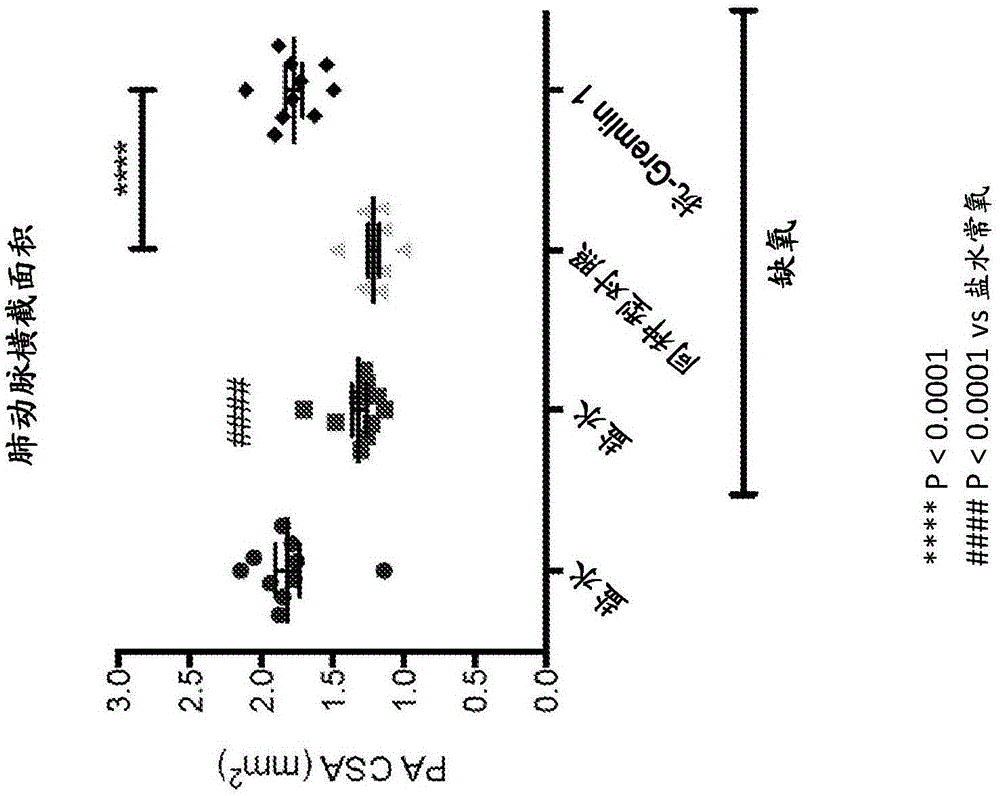
图1a和1b是证明h4h6245p的施用在肺动脉高血压的慢性缺氧小鼠模型中使肺动脉大小(横截面积)和右心室搏出量恢复到接近常氧水平的图。
图1a是描绘在肺动脉高血压的慢性缺氧小鼠模型中施用regn2477对肺动脉(pa)横截面积(csa)的影响的图。
图1b是描绘在肺动脉高血压的慢性缺氧小鼠模型中施用regn2477对右心室搏出量的影响的图。
具体实施方式
本发明至少部分地基于以下发现:抗-grem1抗体或其抗原结合片段有效地缓解肺动脉高血压动物模型中血管重构的效应。以下的详细描述公开了如何制备和使用含抗-grem1抗体或其抗原结合片段的组合物以选择性地抑制grem1的活性,以及公开了用于治疗患有肺动脉高血压(pah)的受试者的组合物、用途和方法。
i.定义
为了可以更容易地理解本发明,首先定义某些术语。另外,应当注意,每当列举参数的值或值范围时,意图是所述值中间的值和范围也旨在成为本发明的部分。
本文使用的冠词“一”和“一个”是指一个或多于一个(即至少一个)该冠词的语法对象。举例来说,“一元素”表示一个元素或多于一个元素,例如,多个元素。
术语“包括”在本文中用于表示短语“包括但不限于”,并且可与其互换使用。
除非上下文另有明确说明,否则术语“或”在本文中用于表示术语“和/或”并且可与术语“和/或”互换使用。
在数字或数字系列之前的术语“至少”应理解为包括与术语“至少”相邻的数字,以及逻辑上可包括的所有后续数字或整数,如从上下文中清楚的那样。当至少在一系列数字或范围之前存在时,应理解“至少”可以修饰该系列或范围中的每个数字。
如本文所用,范围包括上限和下限。
术语“骨形态发生蛋白”或“bmp”是指起到关键的形态发生信号的作用的一组生长因子,其在整个身体内协调组织架构。最初通过它们诱导骨和软骨形成的能力被发现,bmp现在已知在胚胎发育过程中具有多种不同的功能,以参与身体成形(bodypatterning)和形态发生级联,并且在器官内稳态中是关键的。迄今为止,已发现20种bmp,其中bmp2至bmp7属于转化生长因子β超家族。
术语“grem1”是指人gremlin-1,半胱氨酸结超家族的一个成员。人grem1的氨基酸序列在genbank中以登录号np_037504提供,并且在本文中也称为seqidno:594。grem1由本文提供为seqidno:593的核酸编码,并且也在genbank中以登录号nm_013372发现。grem1是一种高度保守的184aa蛋白质,其已被定位于染色体15q13-q15。该蛋白含有信号肽(aa1-24)、预测的糖基化位点(在aa42处)、富半胱氨酸区域和半胱氨酸结基序(aa94-184),其结构是转化生长因子-β(tgf-β)超家族的成员共有的。grem1以分泌的和细胞结合的(例如,膜结合的)两种形式存在。grem1也称为gremlinl,半胱氨酸结超家族1-bmp拮抗剂1(cktsf1b1),dan结构域家族成员2(dand2),mos转化细胞蛋白中下调(drm),gremlin,gremlin,gremlin-1前体,高葡萄糖蛋白提高2(ihg-2),mgc126660,增殖诱导基因2蛋白(pig2)或gremlin1-样蛋白。grem1是骨形态发生蛋白(bmps)的拮抗剂。它与bmp结合并抑制其与其受体的结合。grem1和bmp之间的相互作用微调可用bmp的水平,并影响发育和疾病过程。grem1可以结合并抑制bmp-2、bmp-4和bmp-7。
术语“肺部高血压”(“ph”)是用于描述任何原因引起的肺中高血压的术语。另一方面,术语“高血压”或“高的血压”是指全身动脉中的高血压。
术语“肺动脉高血压”(“pah”)是指进行性肺障碍,其特征在于肺动脉压的持续升高。那些pah患者的肺动脉压通常等于或大于25mmhg,而肺毛细血管或左心房压等于或小于15mmhg。通常使用右心插管在静息的受试者中测量这些压力。未经治疗的pah在被诊断后的2.8年内导致死亡(平均)。
世界卫生组织(who)已经提供了五组pah的临床分类(simonneau等jamcollcardiol.2013;62(25_s),其全部内容通过引用在此并入):
1.肺动脉高血压(pah)
1.1.特发性的
1.2.遗传性的
1.2.1.bmpr2
1.2.2.alk1,eng,smad9,cav1,kcnk3
1.2.3.未知的
1.3.药物-和毒素-诱导的
1.4.与以下相关的:
1.4.1.结缔组织病
1.4.2.hiv感染
1.4.3.门脉高压
1.4.4.先天性心脏病
1.4.5.血吸虫病
1’.肺静脉闭塞性疾病(pvod)和/或肺毛细血管瘤(pch)
1”.新生儿的持续性肺动脉高压(pphn)
2.左心疾病所致肺部高血压
2.1.左心室收缩功能障碍
2.2.左心室舒张功能障碍
2.3.瓣膜病
2.4.先天性/获得性左心流入/流出道梗阻和先天性心肌病
3.肺部疾病和/或缺氧导致的肺部高血压
3.1.慢性阻塞性肺病
3.2.间质性肺病
3.3.其他限制性和阻塞性混合型肺疾病
3.4.睡眠呼吸障碍
3.5.肺泡低通气障碍
3.6.长期高原暴露
3.7.发育异常
4.慢性血栓栓塞性肺部高血压(cteph)
5.不明多因素机制的肺部高压
5.1.血液学障碍:慢性溶血性贫血、骨髓增殖性疾病、脾切除术
5.2.系统性障碍:肉状瘤病、肺组织细胞增生症、淋巴管平滑肌瘤病
5.3.代谢性障碍:糖原贮积病、戈谢病、甲状腺失调
5.4.其它:肿瘤阻塞、纤维性纵隔炎、接受透析的慢性肾衰竭、节段性ph。
在一个实施方案中,受益于本发明方法的受试者是具有i类(who)pah的受试者。
基线(例如,当诊断时)的pah可以是轻度、中度或重度的,例如通过who功能分级测定的,who功能分级是pah患者的疾病严重程度的量度。who功能分类是纽约心脏病协会(nyha)系统的改编本,且常规用于定性评估活动耐力,例如,在监测疾病进展和对治疗的反应中(rubin(2004)chest126:7-10)。世界卫生组织系统中具有四个公认的功能分级:
i级:没有导致体力活动的限制的肺部高血压;普通的体力活动不会引起过度的呼吸困难或疲劳、胸痛或近晕厥;
ii级:导致体力活动受到轻微限制的肺部高血压;病人休息时舒适;普通体力活动导致过度的呼吸困难或疲劳、胸痛或近晕厥;
iii级:导致体力活动明显受限的肺部高血压;病人休息时舒适;低于普通的活动导致过度呼吸困难或疲劳、胸痛或近晕厥;和
iv级:导致无法在无症状的情况下完成任何体力活动的肺部高血压;患者表现出右心衰竭的迹象;即使在休息时也可能出现呼吸困难和/或疲劳;任何体力活动导致不适感增加。
在一个实施方案中,受益于本发明的方法的受试者是在基线时具有whoi级的pah(例如i类(who)pah)的受试者。在另一个实施方案中,受益于本发明的方法的受试者是在基线时具有whoii级的pah(例如,i类(who)pah)的受试者。在另一个实施方案中,受益于本发明的方法的受试者是在基线时具有whoiii级的pah(例如,i类(who)pah)的受试者。
如本文所用,“受试者”是动物,如哺乳动物,包括灵长类动物(如人、非人灵长类动物,例如猴和黑猩猩)、非灵长类动物(如奶牛、猪、骆驼、美洲驼、马、山羊、兔、绵羊、仓鼠、豚鼠、猫、狗、大鼠、小鼠、马和鲸)或者鸟(例如,鸭子或鹅)。
在一个实施方案中,受试者是人,例如治疗或评估pah(例如i类(who)pah)的人;具有pah(例如i类(who)pah)的风险的人;患有pah(例如i类(who)pah)的人;和/或如本文所述,正在治疗pah(例如i类(who)pa)的人。
如本文所用的术语“治疗”或“疗法”是指有益或希望的结果,包括但不限于与pah(例如,i类(who)pah)相关的一种或多种症状的缓解或改善。“治疗”还可以意味着减缓疾病的进程或减少疾病症状的发生,减轻晚期发生疾病的严重性或与没有治疗的情况下预期的存活相比延长存活期。例如,与这种疾病、障碍或病症相关的症状的发生减少(例如,对于该疾病或障碍在临床上接受的尺度上减少至少约10%),或延迟症状的表现(例如,延迟数天、数周、数月或数年)被认为是有效的治疗。
如本文所用,“治疗有效量”旨在包括当施用于患有pah(例如i类(who)pah)的受试者时足以实现疾病的治疗(例如,通过减少、改善或维持现有疾病或疾病的一种或多种症状)或控制疾病的抗-grem1抗体或其抗原结合片段的量。“治疗有效量”可根据抗-grem1抗体或其抗原结合片段、抗-grem1抗体或其抗原结合片段如何施用、疾病及其严重程度和病史、年龄、体重、家族史、遗传构成、pah分期、先前或伴随治疗的类型(如果有的话)以及待治疗患者的其他个体特征而有所不同。
“治疗有效量”还意图包括当施用于受试者时足以改善疾病或疾病的一种或多种症状的抗-grem1抗体或其抗原结合片段的量。改善疾病包括减缓疾病进程或减轻晚期发生疾病的严重程度。
“治疗有效量”还包括以适用于任何治疗的合理的利益/风险比产生一些所需的局部或系统作用的抗-grem1抗体或其抗原结合片段的量。用于本发明方法的抗grem1抗体或其抗原结合片段可以以足够的量施用以产生适用于这种治疗的合理的利益/风险比。
ii.本发明的方法
本发明提供了治疗患有肺动脉高血压的受试者的方法。该方法一般地包括向受试者施用治疗有效量的抗-grem1抗体或其抗原结合片段。
在本发明的一些方面,抗-grem1抗体或其抗原结合片段的施用抑制受试者中肺动脉的增厚,例如,抑制受试者中肺动脉从基线(例如,在诊断时)的进一步增厚。肺动脉的增厚可以通过例如胸部ct(例如,非增强的轴向10mmct断面)来确定,并用于计算主肺动脉直径(mpa)。正常受试者的主肺动脉直径为约2.4cm至约3.0cm。具有肺动脉高血压的受试者中的主肺动脉直径为约3.1cm至约3.8cm或更大。参见,例如,edwards等(1998)brjradiol71(850):1018-20。
在本发明的其他方面,抗-grem1抗体或其抗原结合片段的施用增加了受试者的每搏输出量和/或每搏输出量-收缩末期容积比率(“sv/esv”)。“每搏输出量”(“sv”)是每单次收缩从右心室或左心室泵出的血液量。每搏输出量可以使用来自超声心动图的心室体积的测量来计算,并且通过从紧接心搏前心室中的血液体积(称为“舒张末期容积”,“esv”)减去心搏结束时心室中的血液体积(称为“收缩末期容积”,“edv”)来计算。每搏输出量还可以计算为,例如,通过在右心导管插入期间的热稀释测量的心输出量除以心率,或为edv减去esv且针对体表面积进行索引(indexed)。术语每搏输出量可适用于心脏的两个心室中的每一个。每个心室的每搏输出量通常相等,在健康受试者中均为约70ml。健康受试者的sv/esv为约0.9至约2.2,且患有pah的受试者的sv/esv为约0.2至约0.9。参见,例如,b.rewis等(2016)intjcardiol218:206-211。
在本发明的再其他方面,抗-grem1抗体或其抗原结合片段的施用增加受试者的右心室心输出量和/或心脏指数(ci)。“心输出量”(“co”)定义为单位时间内心室泵送的血液量。“心脏指数”(“ci”)是将一分钟内左心室的心输出量(co)与“体表面积”(“bsa”)相关联的血液动力学参数,从而将心脏性能与个体的体型相关联。超声心动图技术和放射性核素成像技术可用于估计心室尺寸的实时变化,因此计算每搏输出量,其在乘以心率时给出心输出量,并且bsa可以使用本领域普通技术人员已知的任何一种公式计算,包括例如dubois公式(verbraecken,j等(2006)metabolism-clinexper55(4):515-24)或mosteller公式(mosteller(1987)nengljmed317:1098)。未患pah的受试者的心输出量在约4.0-8.0l/min的范围内,且心脏指数为约2.6-约4.2l/分钟/平方米。患有pah的受试者的心脏指数为每平方米约1.9至约2.3l/分钟(ryan和archer(2016)circres115:176-188)。
在本发明的方法中向患有pah的受试者施用抗-grem1抗体或其抗原结合片段可以改善患有pah的受试者的其他血液动力学测量,例如右心房血压、肺动脉压、在呼气末期压存在下的肺毛细血管楔压、系统动脉压、心搏、肺血管阻力和/或全身血管阻力。用于测量右心房血压、肺动脉压、在呼气末期压存在下的肺毛细血管楔压、全身动脉压、心搏、肺血管阻力和/或全身血管阻力的方法和装置是本领域普通技术人员已知的。
未患pah的受试者的右心房血压为约1mmhg至约5mmhg;患有pah的受试者的右心房血压为约11mmhg至约13mmhg。
未患pah的受试者的肺动脉压为约9mmhg至约20mmhg;患有pah的受试者具有约57mmhg至约61mmhg的肺动脉压。
未患pah的受试者在呼气末期压存在下的肺毛细血管楔压为约4mmhg至约12mmhg;患有pah的受试者在呼气末期压存在下的肺毛细血管楔压为约9mmhg至约11mmhg。
未患pah的受试者具有约90mmhg至约96mmhg的系统动脉压;患有pah的受试者具有约87mmhg至约91mmhg的系统动脉压。
未患pah的受试者的心搏为约每分钟60次(bpm)至约90bpm;患有pah的受试者具有约84bpm88bpm的系统动脉压。
未患pah的受试者具有约20达因s/cm5至约130达因s/cm5(或约0.25至约1.625wood单位)的肺血管阻力,患有pah的受试者具有约1200达因s/cm5至约1360达因s/cm5(或约15至约17wood单位)的肺血管阻力。
未患pah的受试者具有约700达因s/cm5至约1600达因s/cm5(或约9至约20wood单位)的全身血管阻力,患有pah的受试者具有约1840达因s/cm5至约2000达因s/cm5(或约23至约25wood单位)的全身血管阻力。
本发明的方法还可以改善所治疗的受试者中的其他临床参数,例如肺功能。例如,在治疗期间或治疗期之后,受试者可具有增加的运动能力或活动,例如通过6分钟步行距离(6mwd)的测试或活动度量,或降低borg呼吸困难指数(bdi)测量的。
本发明的方法还可以相对于基线改善一种或多种生活质量参数,例如
可以使用任何合适的运动能力量度来确定受试者是否具有增加的运动能力或活动。一种合适的量度是6分钟步行测试(6mwt),其测量受试者在6分钟内可以走多远,即6分钟步行距离(6mwd)。另一个合适的量度是borg呼吸困难指数(bdi),其是用于评估感知的呼吸困难(呼吸不适)的数字尺度。它测量在完成6分钟步行测试(6mwt)后的呼吸急促程度,其中0的bdi表示无呼吸急促,和10表示最大呼吸急促。在一个实施方案中,本发明的方法向受试者提供从6mwd的从基线至少约10分钟的增加,例如约10、15、20或约30分钟。在6mwt后,本发明的方法向受试者提供从基线bdi的至少约0.5至约1.0个指数点的降低。
可以使用任何合适的生活质量测量。例如,
本发明的方法还可以改善所治疗的受试者的预后。例如,本发明的方法可以向受试者提供治疗期间临床恶化事件的概率的降低,和/或血清脑钠尿肽(bnp)或者ntpro-bnp或其n-末端激素原,nt-pro-bnp浓度从基线的降低,其中在基线时,距受试者病症的首次诊断的时间不大于约2年。
在各个方面,距第一次诊断的时间可以是,例如,不大于约1.5年,不大于约1年,不大于约0.75年,或不大于约0.5年。临床恶化事件(cwe)包括死亡、肺移植、由于pah住院、房间隔造口术、另外的肺动脉高压治疗的开始或其组合。到pah临床恶化的时间定义为从治疗开始到第一次cwe发生的时间。
在一个实施方案中,本发明的方法提供了bnp或nt-pro-bnp浓度相对于基线至少约15%,例如至少约25%,至少约50%或至少约75%的降低。
在一个实施方案中,本发明的方法提供了死亡概率、肺移植、由于肺动脉高血压的住院、房间隔造口术和/或在治疗期间开始额外的肺动脉高血压治疗方面至少约25%,例如至少约50%,至少约75%或至少约80%的降低。
本发明的方法还可以延长患有pah的受试者从治疗开始时的寿命(延长存活时间),例如,至少约30天。
用于本发明的方法中的治疗有效量的抗-grem1抗体或其抗原结合片段可以是约0.05mg-约600mg;例如,约0.05mg、约0.1mg、约1.0mg、约1.5mg、约2.0mg、约10mg、约20mg、约30mg、约40mg、约50mg、约60mg、约70mg、约80mg、约90mg、约100mg、约110mg、约120mg、约130mg、约140mg、约150mg、约160mg、约170mg、约180mg、约190mg、约200mg、约210mg、约220mg、约230mg、约240mg、约250mg、约260mg、约270mg、约280mg、约290mg、约300mg、约310mg、约320mg、约330mg、约340mg、约350mg、约360mg、约370mg、约380mg、约390mg、约400mg、约410mg、约420mg、约430mg、约440mg、约450mg、约460mg、约470mg、约480mg、约490mg、约500mg、约510mg、约520mg、约530mg、约540mg、约550mg、约560mg、约570mg、约580mg、约590mg、约600mg、约610mg、约620mg、约630mg、约640mg、约650mg、约660mg、约670mg、约680mg、约690mg、约700mg、约710mg、约720mg、约730mg、约740mg、约750mg、约760mg、约770mg、约780mg、约790mg、约800mg、约810mg、约820mg、约830mg、约840mg、约850mg、约860mg、约870mg、约880mg、约890mg、约900mg、约910mg、约920mg、约930mg、约940mg、约950mg、约960mg、约970mg、约980mg、约990mg或约1000mg的相应抗体。
单个剂量中包含的抗-grem1抗体或其抗原结合片段的量可以以每千克患者体重的抗体毫克数(即mg/kg)表示。例如,可以将抗-grem1抗体或其抗原结合片段以约0.0001-约50mg/kg患者体重(例如0.1mg/kg、0.5mg/kg、1.0mg/kg、1.5mg/kg、2.0mg/kg、2.5mg/kg、3.0mg/kg、3.5mg/kg、4.0mg/kg、4.5mg/kg、5.0mg/kg、5.5mg/kg、6.0mg/kg、6.5mg/kg、7.0mg/kg、7.5mg/kg、8.0mg/kg、8.5mg/kg、9.0mg/kg、9.5mg/kg、10.0mg/kg、10.5mg/kg、11.0mg/kg、11.5mg/kg、12.0mg/kg、12.5mg/kg、13.0mg/kg、13.5mg/kg、14.0mg/kg、14.5mg/kg、15.0mg/kg、15.5mg/kg、16.0mg/kg、16.5mg/kg、17.0mg/kg、17.5mg/kg、18.0mg/kg、18.5mg/kg、19.0mg/kg、19.5mg/kg、20.0mg/kg等)的剂量施用于患者。
可以在限定的时间段内向受试者施用多个剂量的抗-grem1抗体或其抗原结合片段或者包含抗-grem1抗体或其抗原结合片段的药物组合物。根据本发明的这一方面的方法包括向受试者顺序地施用多个剂量的本发明的活性成分。如本文所用,“顺序施用”是指每个剂量的活性成分在不同的时间点施用于受试者,例如在隔开预定间隔(例如,数小时、数天、数周或数月)的不同日期。本发明包括的方法包括顺序地向患者施用单一初始剂量的活性成分,然后施用一个或多个二级剂量的活性成分,并任选地随后施用一个或多个三级剂量的活性成分。
术语“初始剂量”、“二级剂量”和“三级剂量”是指抗-grem1抗体或其抗原结合片段或本发明的组合疗法的施用的时间顺序。因此,“初始剂量”是在治疗方案开始时施用的剂量(也称为“基线剂量”);“二级剂量”是初始剂量后施用的剂量;“三级剂量”是在二级剂量后施用的剂量。初始、二级和三级剂量可以全部含有相同量的抗-grem1抗体或其抗原结合片段,但在给药频率方面可以彼此不同。然而,在某些实施方案中,包含在初始、二级和/或三级剂量中的抗grem1抗体或其抗原结合片段的量在治疗过程中彼此不同(例如,适当地向上或向下调整)。在某些实施方案中,在治疗方案开始时施用两个或更多个(例如,2、3、4或5个)剂量作为“负荷剂量”,然后是以较低频率施用的后续剂量(例如,“维持剂量”)。
在本发明的某些示例性实施方案中,每个二级和/或三级剂量在紧接前一剂量之后施用1至26(例如,1、11/2、2、21/2、3、31/2、4、41/2、5、51/2、6、61/2、7、71/2、8、81/2、9、91/2、10、101/2、11、111/2、12、121/2、13、131/2、14、141/2、15、151/2、16、161/2、17、171/2、18、181/2、19、191/2、20、201/2、21、211/2、22、221/2、23、231/2、24、241/2、25、251/2、26、261/2或更多)周。本文所用的短语“紧接前一剂量”是指在多次施用的序列中,在序列中的每一下个剂量的施用之前施用于患者而没有中间剂量的抗grem1抗体或其抗原结合片段的剂量。
根据本发明的这一方面的方法可包括向患者施用任何数量的二级和/或三级剂量。例如,在某些实施方案中,仅向患者施用单一二级剂量。在其它实施方案中,对患者施用两个或更多个(例如,2、3、4、5、6、7、8或更多个)二级剂量。同样地,在某些实施方案中,仅向患者施用单一三级剂量。在其它实施方案中,向患者施用两个或更多个(例如,2、3、4、5、6、7、8或更多个)三级剂量。
在涉及多个二级剂量的实施方案中,每个二级剂量可以与其他二级剂量相同的频率施用。例如,每个二次剂量可以在紧接前一剂量后1至2周或1至2个月施用于患者。类似地,在涉及多个三级剂量的实施方案中,每个三级剂量可以与其他三级剂量以相同的频率施用。例如,每个三级剂量可以在紧接前一剂量后2至12周向患者施用。在本发明的某些实施方案中,二级和/或三级剂量施用于患者的频率可以在治疗方案的过程中变化。施用频率也可以根据临床检查后个体患者的需要由医生在治疗过程中调整。
在本发明的一些实施方案中,抗-grem1抗体或其抗原结合片段可以作为单一疗法(即,作为唯一的治疗剂)施用。在本发明的其他实施方案中,抗-grem1抗体或其抗原结合片段可以与一种或多种另外的治疗剂组合施用。
在包括向受试者施用抗-grem1抗体或其抗原结合片段和至少一种另外的治疗剂的本发明的组合方法中,抗体和另外的治疗剂可以同时或基本上同时施用于受试者,例如,以单一治疗剂量,或以两个单独的剂量给药(其同时施用或在彼此少于约5分钟内施用)。或者,抗体和另外的治疗剂可以顺序地施用于受试者,例如,以时间上彼此分开超过约5分钟的单独治疗剂量施用。
因此,在一个实施方案中,本发明的方法还包括施用治疗有效量的至少一种选自抗凝剂、利尿剂、强心苷、钙通道阻滞剂、血管舒张剂、前列环素类似物、内皮拮抗剂、磷酸二酯酶抑制剂、内肽酶抑制剂、降血脂剂和血栓烷抑制剂的治疗剂。在一个实施方案中,本发明的方法还包括施用治疗有效量的至少一种或多种另外的一个或多个治疗性抗体或者一个或多个其抗原结合片段。在一个实施方案中,另外的一个或多个抗体选自一个或多个抗-grem1抗体或抗体、一个或多个抗-pdgfrβ抗体、一个或多个抗-tlr4抗体或抗体、一个或多个抗-tlr2抗体或抗体、一个或多个抗-edn1抗体以及一个或多个抗-asic1抗体。
合适的抗凝剂的实例包括但不限于,例如,可用于治疗具有增加的血栓形成和血栓栓塞风险的肺动脉高血压患者的华法林。
合适的钙通道阻滞剂的实例包括但不限于地尔硫
合适的血管扩张剂包括但不限于,例如,前列环素、依前列醇、曲前列环素和一氧化氮(no)。
合适的示例性磷酸二酯酶抑制剂包括但不限于,特别地,磷酸二酯酶v抑制剂,例如他达拉非、西地那非和伐地那非。
合适的内皮素拮抗剂的实例包括但不限于,例如,波生坦和西他生坦。
合适的前列环素类似物包括但不限于,例如,ilomedin、曲前列环素和依前列醇。
合适的降脂剂包括但不限于,例如,hmgcoa还原酶抑制剂,如辛伐他汀、普伐他汀、阿托伐他汀、洛伐他汀、伊伐他汀、氟伐他汀、匹伐他汀、罗苏伐他汀、zd-4522和西立伐他汀。
适用于本发明的联合治疗的利尿剂包括但不限于,例如,氯噻酮、吲达帕胺、bendro-flumethiazid、metolazon、cyclopeiaziazid、polythiazid、mefrusid、ximapid、氯噻嗪和hydrochlorothiaziaz。
其他治疗剂的实例包括但不限于,例如,ace抑制剂,如依那普利、雷米普利、卡托普利、西拉普利、群多普利、福辛普利、喹那普利、莫西普利、赖诺普利和培哚普利,或atii抑制剂,如氯沙坦、坎地沙坦、厄贝沙坦、恩布沙坦、缬沙坦和替米沙坦,或伊洛前列素、betaprost、l-精氨酸、奥帕曲拉、氧和/或地高辛。
本发明的方法还可包括激酶抑制剂(例如,bms-354825、卡奈替尼、厄洛替尼、吉非替尼、伊马替尼、拉帕替尼、来他替尼、洛那法尼、哌加他尼、培利替尼、司马沙尼、坦度替尼、替比法尼、瓦他拉尼、氯尼达明、法舒地尔、来氟米特、硼替佐米、伊马替尼、厄洛替尼和格列卫)和/或弹性蛋白酶抑制剂的组合使用。
另外的治疗活性组分可以在施用本发明的抗-grem1抗体之前向受试者施用。例如,如果第一组分在第二组分的施用之前一周,之前72小时,之前60小时,之前48小时,之前36小时,之前24小时,之前12小时,之前6小时,之前5小时,之前4小时,之前3小时,之前2小时,之前1小时,之前30分钟,之前15分钟,之前10分钟,之前5分钟或之前不到1分钟施用,则第一组分可以认为在第二组分“之前”施用。在其它实施方案中,另外的治疗活性成分可以在施用抗-grem1抗体或其抗原结合片段后施用于受试者。例如,如果第一组分在第二组分的施用之后1分钟,之后5分钟,之后10分钟,之后15分钟,之后30分钟,之后1小时,之后2小时,之后3小时,之后4小时,之后5小时,之后6小时,之后12小时,之后24小时,之后36小时,之后48小时,之后60小时,之后72小时施用,则第一组分可以认为在第二组分“之后”施用。
在再其他实施方案中,另外的治疗活性组分可以在施用本发明的抗-grem1抗体或其抗原结合片段的同时施用于受试者。出于本发明的目的,“同时”施用包括例如以单一剂型向受试者施用抗-grem1抗体和另外的治疗活性组分,或者在彼此约30分钟或更少时间内以单独剂型施用于受试者。如果以单独的剂型施用,每个剂型可以通过相同的途径施用(例如,抗-grem1抗体和另外的治疗活性组分两者可以静脉内、皮下、玻璃体内施用等);或者,每个剂型可以通过不同的途径施用(例如,抗-grem1抗体可以局部施用(例如,玻璃体内),和另外的治疗活性组分可以全身施用)。在任何情况下,出于本公开的目的,以单一剂型、通过相同途径以单独剂型或通过不同途径以单独剂型施用组分均被认为是“同时施用”。出于本公开的目的,在施用另外的治疗活性组分“之前”、“同时”或“之后”(如上文定义的那些术语)施用抗-grem1抗体被认为是与另外的治疗活性成分“组合”施用抗-grem1抗体或其抗原结合片段。
iii.适用于本发明的方法中的结合蛋白
用于本发明方法的合适的抗gremlin-1(grem1)结合蛋白描述于,例如,u.s.专利公开no.2016/0024195中,其全部内容通过引用在此并入。
在一个实施方案中,适用于本发明的grem1结合蛋白是抗原特异性结合蛋白。
如本文所用,表述“抗原特异性结合蛋白”是指包含至少一个特异性结合特定抗原的结构域的蛋白质。抗原特异性结合蛋白的示例性类别包括抗体、抗体的抗原结合部分、与特定抗原特异性相互作用的肽(例如,肽抗体(peptibody))、与特定抗原特异性相互作用的受体分子以及包含与特定抗原特异性结合的受体的配体结合部分的蛋白质。
因此,本发明包括特异性结合grem1的抗原特异性结合蛋白,即“grem1特异性结合蛋白”的用途。
在一个实施方案中,用于本发明方法的抗原特异性结合蛋白可包含抗体或抗体的抗原结合片段或者由其组成。
在一个实施方案中,用于本发明的grem1特异性结合蛋白是特异性结合seqidno:594或seqidno:595的grem1的人单克隆抗体。
如本文所用,术语“抗体”意指由通过二硫键相互连接的四条多肽链(两条重链(h)和两条轻链(l))组成的免疫球蛋白分子(即,“完全抗体分子”),以及其多聚体(例如,igm)或其抗原结合片段。每条重链由重链可变区(“hcvr”或“vh”)和重链恒定区(由结构域ch1,ch2和ch3组成)组成。每条轻链由轻链可变区(“lcvr”或“vl”)和轻链恒定区(cl)组成。vh和vl区可以进一步细分为散布在更保守的区域(称为框架区(fr))间的高变区域(称为互补决定区(cdr))。每个vh和vl由三个cdr和四个fr组成,其按照以下顺序从氨基末端到羧基末端排列:fr1、cdr1、fr2、cdr2、fr3、cdr3、fr4。在本发明的某些实施方案中,抗体(或其抗原结合片段)的fr可以与人种系序列相同,或者可以是天然地或人工地修饰的。可以基于两个或更多个cdr的并列分析来定义氨基酸共有序列。
用于确定hcvr和lcvr氨基酸序列内的cdr的方法和技术是本领域熟知的,并且可用于鉴定本文公开的指定的重链可变区(hcvr)和/或轻链可变区(lcvr)氨基酸序列内的cdr。可用于确定cdr的边界的示例性规则包括例如kabat定义、chothia定义和abm定义。一般而言,kabat定义基于序列变异性,chothia定义基于结构环区域的位置,和abm定义是kabat和chothia方法之间的折衷。参见,例如,kabat,“sequencesofproteinsofimmunologicalinterest,”nationalinstitutesofhealth,bethesda,md.(1991);al-lazikani等,(1997),j.mol.biol.273:927-948;及martin等,(1989),proc.natl.acad.sci.usa86:9268-9272。公共数据库也可用于鉴定抗体内的cdr序列。
一个或多个cdr残基的置换或一个或多个cdr的省略也是可能的。已经在科学文献中描述了其中对于结合可以省去一个或两个cdr的抗体。padlan等(fasebj.1995,9:133-139)基于公开的晶体结构分析了抗体与其抗原之间的接触区域,并得出结论:只有约五分之一至三分之一的cdr残基实际上与抗原接触。padlan还发现了其中一个或两个cdr没有与抗原接触的氨基酸的许多抗体(也参见vajdos等,2002jmolbiol320:415-428)。
可以基于先前的研究,通过分子建模和/或经验地从kabatcdr位于chothiacdr之外的区域鉴定不接触抗原的cdr残基(例如,cdrh2中的残基h60-h65通常是不需要的)。如果省略cdr或其残基,则其通常被占据另一人抗体序列或此类序列的共有序列中相应位置的氨基酸置换。也可以经验地选择cdr内的置换位置和待置换的氨基酸。经验置换可以是保守或非保守置换。
用于本文公开的方法的全人抗-grem1单克隆抗体可以在重链和轻链可变结构域的框架和/或cdr区中包含与对应的种系序列相比的一个或多个氨基酸置换、插入和/或删除。通过将本文公开的氨基酸序列与可从例如公共抗体序列数据库获得的种系序列进行比较,可以容易地确定这些突变。本发明包括源自本文公开的任何氨基酸序列的抗体及其抗原结合片段,其中一个或多个框架和/或cdr区内的一个或多个氨基酸突变为该抗体所来源的种系序列中的相应残基,或突变为另一人种系序列的相应残基,或突变为相应种系残基的保守氨基酸置换(此类序列变化在本文中统称为“种系突变”)。本领域普通技术人员从本文公开的重链和轻链可变区序列开始,可以容易地产生包含一个或多个单个种系突变或其组合的许多抗体和抗原结合片段。在某些实施方案中,vh和/或vl结构域内的所有框架和/或cdr残基突变回抗体由其来源的原始种系序列中发现的残基。在其他实施方案中,只有某些残基突变回原始种系序列,例如,仅在fr1的前8个氨基酸内或在fr4的最后8个氨基酸内发现的突变残基,或者仅在cdr1、cdr2或cdr3中发现的突变残基。在其它实施方案中,一个或多个构架和/或cdr残基突变为不同种系序列(即,与抗体最初来源的种系序列不同的种系序列)的相应残基。此外,本发明的抗体可以包含框架和/或cdr区内的两个或更多个种系突变的任何组合,例如,其中某些单个残基突变为特定种系序列的相应残基,而与原始种系序列不同的某些其他残基维持或突变为不同种系序列的相应残基。一旦获得,可以容易地测试含有一个或多个种系突变的抗体和抗原结合片段的一种或多种所需特性,例如改善的结合特异性、增加的结合亲和力、改善或增强的拮抗或激动性生物学特性(视情况而定)、降低的免疫原性等。以这种一般方式获得的抗体和抗原结合片段包括在本发明中。
本发明还包括全人抗grem1单克隆抗体的用途,所述单克隆抗体包含本文公开的任何hcvr、lcvr和/或cdr氨基酸序列具有一个或多个保守置换的变体。例如,本发明包括具有相对于本文公开的任何hcvr、lcvr和/或cdr氨基酸序列具有例如10个或更少、8个或更少、6个或更少、4个或更少等的保守氨基酸置换的hcvr、lcvr和/或cdr氨基酸序列的抗grem1抗体。
如本文所用,术语“人抗体”旨在包括具有衍生自人种系免疫球蛋白序列的可变区和恒定区的抗体。本发明的人mab可包括非由人种系免疫球蛋白序列编码的氨基酸残基(例如,通过体外随机或定点诱变或者通过体内体细胞突变引入的突变),例如在cdr中和特别是在cdr3中。然而,如本文所用,术语“人抗体”不旨在包括其中衍生自另一哺乳动物物种(例如小鼠)的种系的cdr序列已经移植到人fr序列上的mab。
术语“特异性结合”或“特异性结合于”等意指抗体或其抗原结合片段与抗原形成在生理条件下相对稳定的复合物。特异性结合可以通过至少约1x10-6m或更小的平衡解离常数表征(例如,较小的kd表示更紧密的结合)。用于确定两个分子是否特异性结合的方法是本领域公知的,且包括例如平衡透析、表面等离子体共振等。已经通过表面等离振子共振(例如biacoretm)鉴定了用于本文用途的与人grem1特异性结合的合适抗体。此外,结合grem1中的一个结构域和一个或多个另外的抗原的多特异性抗体或者结合grem1的两个不同区域的双特异性抗体仍然被认为是如本文所用的“特异性结合”的抗体。
术语“高亲和力抗体”是指对grem1具有至少10-7m,优选10-8m,更优选10-9m,甚至更优选10-10m,甚至更优选10-11m的结合亲和力(表示为kd)的那些mab,如通过表面等离子体共振例如biacoretm或溶液亲和elisa测量的。
术语“慢解离速率”、“koff”或“kd”是指以1x10-3s-1或更小,优选1x10-4s-1或更小的速率常数与grem1解离的抗体,如通过表面等离子共振例如biacoretm确定的。
如本文所用,术语抗体的“抗原结合部分”、抗体的“抗原结合片段”等包括任何天然存在的、可酶促获得的、合成的或遗传工程化的多肽或糖蛋白,其特异性地结合抗原以形成复合物。本文所用的术语抗体的“抗原结合片段”或“抗体片段”是指保留结合grem1的能力的一个或多个抗体片段。
在本发明方法的具体实施方案中,抗体或抗体片段可以与治疗部分如抗生素、第二抗grem1抗体或者针对细胞因子如il-1、il-6或tgf-β的抗体,或用于治疗pah的任何其他治疗性部分缀合(“免疫缀合物”)。
如本文所用,“分离的抗体”意指基本上不含具有不同抗原特异性的其他抗体(abs)的抗体,例如,特异性结合人grem1的分离的抗体或其片段基本上没有特异性地结合grem1以外的抗原的abs。
如本文所用的“阻断抗体”或“中和抗体”(或“中和grem1活性的抗体”)意指其与grem1的结合导致grem1的至少一种生物学活性的抑制的抗体。这种grem1的生物学活性的抑制可以通过几种标准体外测定(例如本文所述的中和分析)中的一种或多种或本领域已知的体内分析(例如,在施用本文所述的一种或多种抗体后观察针对grem1活性的保护的动物模型)测量grem1生物学活性的一种或多种指标来评估。
如本文所用,术语“表面等离子体共振”是指通过检测生物传感器矩阵内蛋白质浓度的变化,例如使用biacoretm系统(pharmaciabiosensorab,uppsala,sweden和piscataway,n.j.),来分析实时生物分子相互作用的光学现象。
如本文所用,术语“kd”意指特定抗体-抗原相互作用的平衡解离常数。
术语“表位”是指与称为互补位的抗体分子可变区中的特定抗原结合位点相互作用的抗原决定簇。单一抗原可具有多于一个表位。因此,不同的抗体可以结合抗原上的不同区域并且可以具有不同的生物学效应。术语“表位”还指b和/或t细胞对其响应的抗原上的位点。它还指被抗体结合的抗原区域。表位可以定义为结构的或功能的。功能性表位通常是结构表位的子集,并且具有直接造成相互作用的亲和力的那些残基。表位也可以是构象的,即由非线性氨基酸组成。在某些实施方案中,表位可以包括作为化学活性的表面分子集群如氨基酸、糖侧链、磷酰基或磺酰基的决定簇,并且在某些实施方案中,可以具有特定的三维结构特征和/或特定的电荷特征。
当提及核酸或其片段时,术语“实质同一性”或“基本上相同”表明,当以适当的核苷酸插入或删除与另一核酸(或其互补链)最佳比对时,存在至少约90%,更优选至少约95%、96%、97%、98%或99%的核苷酸碱基的核苷酸序列同一性,如通过任何公知的序列同一性算法如fasta、blast或gap测量的,如下所述。在某些情况下,与参考核酸分子具有实质同一性的核酸分子可编码具有与参考核酸分子编码的多肽相同或基本相似的氨基酸序列的多肽。
当应用于多肽时,术语“实质相似性”或“基本上相似”是指两个肽序列在最佳比对时,例如通过程序gap或bestfit使用默认空位权重进行比对时,共有至少90%的序列同一性,甚至更优选至少95%、98%或99%的序列同一性。优选地,不相同的残基位置不同在于保守氨基酸置换。
“保守氨基酸置换”是其中氨基酸残基被具有相似化学性质(例如电荷或疏水性)的侧链(r基团)的另一氨基酸残基取代的氨基酸置换。通常,保守氨基酸置换不会显著改变蛋白质的功能特性。在其中两个或更多个氨基酸序列彼此差异在于保守置换的情况下,可以向上调整相似性的百分比或程度以针对置换的保守性质进行校正。进行这种调整的方式是本领域技术人员所熟知的。参见,例如,pearson(1994)methodsmol.biol.24:307-331,其通过引用并入本文。具有化学性质相似的侧链的氨基酸组的实例包括1)脂族侧链:甘氨酸、丙氨酸、缬氨酸、亮氨酸和异亮氨酸;2)脂族-羟基侧链:丝氨酸和苏氨酸;3)含酰胺的侧链:天冬酰胺和谷氨酰胺;4)芳族侧链:苯丙氨酸、酪氨酸和色氨酸;5)碱性侧链:赖氨酸、精氨酸和组氨酸;6)酸性侧链:天冬氨酸和谷氨酸;和7)含硫侧链:半胱氨酸和蛋氨酸。优选的保守氨基酸置换组是:缬氨酸-亮氨酸-异亮氨酸,苯丙氨酸-酪氨酸,赖氨酸-精氨酸,丙氨酸-缬氨酸,谷氨酸-天冬氨酸和天冬酰胺-谷氨酰胺。或者,保守替代是在gonnet等(1992)science256:1443-45(在此引入作为参考)中公开的pam250对数-似然率矩阵中具有正值的任何变化。“中度保守”的替代是pam250对数似然率矩阵中具有非负值的任何变化。
通常使用序列分析软件测量多肽的序列相似性。蛋白质分析软件使用分配给各种置换、删除和其他修饰(包括保守氨基酸置换)的相似性量度来匹配相似的序列。例如,gcg软件包含诸如gap和bestfit的程序,其可以以默认参数使用以确定密切相关的多肽(例如来自不同物种生物体的同源多肽)之间的或野生型蛋白质与其突变蛋白之间的序列同源性或序列同一性。参见,例如,gcg版本6.1。多肽序列也可以使用具有默认或推荐参数的fasta(gcg版本6.1中的程序)进行比较。fasta(例如,fasta2和fasta3)提供查询和检索序列之间最佳重叠区域的比对和百分比序列同一性(pearson(2000)同上)。当将本发明的序列与包含来自不同生物体的大量序列的数据库进行比较时,另一种优选的算法是使用默认参数的计算机程序blast,尤其是blastp或tblastn。参见,例如,altschul等(1990)j.mol.biol.215:403-410和(1997)nucleicacidsres.25:3389-3402,其各自通过引用并入本文。
在具体的实施方案中,用于本发明的方法中的抗体或抗体片段可以是单特异性的、双特异性的或多特异性的。多特异性抗体可以对一种靶多肽的不同表位是特异性的,或者可以含有对一种以上靶多肽的表位特异性的抗原结合结构域。可用于本发明的情况中的示例性双特异性抗体形式涉及使用第一免疫球蛋白(ig)ch3结构域和第二igch3结构域,其中第一和第二igch3结构域彼此相差至少一个氨基酸,并且其中与缺乏该氨基酸差异的双特异性抗体相比,该至少一个氨基酸差异降低了双特异性抗体与蛋白a的结合。在一个实施方案中,第一igch3结构域结合蛋白a,和第二igch3结构域含有降低或消除蛋白a结合的突变,例如h95r修饰(按照imgt外显子编号;按照eu编号的h435r)。第二ch3可进一步包含y96f修饰(按照imgt;按照eu的y436f)。可以在第二ch3中发现的进一步修饰包括:在igg1mab的情况中的d16e、l18m、n44s、k52n、v57m和v82i(按照imgt;按照eu的d356e、l358m、n384s、k392n、v397m和v422i);在igg2mab的情况中的n44s、k52n和v82i(imgt;按照eu的n384s、k392n和v422i);及igg4mab的情况中的q15r、n44s、k52n、v57m、r69k、e79q和v82i(按照imgt;按照eu的q355r、n384s、k392n、v397m、r409k、e419q和v422i)。上述双特异性抗体形式的变异涵盖在本发明的范围内。
应理解,除非另有明确说明,本文所用的术语“抗体”包括含有两个免疫球蛋白重链和两个免疫球蛋白轻链的抗体分子(即“完全抗体分子”)以及其抗原结合片段。如本文所用,术语抗体的“抗原结合部分”、抗体的“抗原结合片段”等包括任何天然存在的、可酶促获得的、合成的或遗传工程化的多肽或糖蛋白,其特异性地结合抗原以形成复合物。如本文所用,术语抗体的“抗原结合片段”或“抗体片段”是指保留特异性结合人grem1的能力的一种或多种抗体片段。抗体片段可包括fab片段、f(ab')2片段、fv片段、dab片段、含cdr的片段或分离的cdr。抗体的抗原结合片段可以例如使用任何合适的标准技术如蛋白水解消化或涉及操纵和表达编码抗体可变和(任选地)恒定结构域的dna的重组基因工程技术从完全抗体分子衍生。这种dna是已知的和/或易于从例如商业来源、dna文库(包括例如噬菌体-抗体文库)获得,或可以合成。dna可以进行测序和通过化学方法或通过使用分子生物学技术操纵,例如,以将一个或多个可变和/或恒定结构域排列成合适的构型或者引入密码子、产生半胱氨酸残基、修饰、添加或删除氨基酸等。
抗原结合片段的非限制性实例包括:(i)fab片段;(ii)f(ab')2片段;(iii)fd片段;(iv)fv片段;(v)单链fv(scfv)分子;(vi)dab片段;和(vii)由模拟抗体高变区的氨基酸残基组成的最小识别单元(例如,分离的互补决定区(cdr),例如cdr3肽),或受约束的fr3-cdr3-fr4肽。其他工程化分子,如结构域特异性抗体、单结构域抗体、结构域删除抗体、嵌合抗体、cdr嫁接抗体、双抗体、三抗体、四抗体、微型抗体、纳米抗体(例如单价纳米抗体、二价纳米抗体等)、小模块免疫药物(smips)和鲨鱼可变ignar结构域也包括在本文所用的表述“抗原结合片段”内。
抗体的抗原结合片段通常包含至少一个可变结构域。可变结构域可以具有任何大小或氨基酸组成,并且通常包含至少一个cdr,其与一个或多个框架序列相邻或同框。在具有与vl结构域相关的vh结构域的抗原结合片段中,vh和vl结构域可以以任何合适的排列相对于彼此定位。例如,可变区可以是二聚的并含有vh-vh、vh-vl或vl-vl二聚体。或者,抗体的抗原结合片段可含有单体vh或vl结构域。
在某些实施方案中,抗体的抗原结合片段可含有与至少一个恒定结构域共价连接的至少一个可变结构域。可以在本发明的抗体的抗原结合片段中发现的可变和恒定结构域的非限制的示例性构型包括:(i)vh-ch1;(ii)vh-ch2;(iii)vh-ch3;(iv)vh-ch1-ch2;(v)vh-ch1-ch2-ch3;(vi)vh-ch2-ch3;(vii)vh-cl;(viii)vl-ch1;(ix)vl-ch2;(x)vl-ch3;(xi)vl-ch1-ch2;(xii)vl-ch1-ch2-ch3;(xiii)vl-ch2-ch3;和(xiv)vl-cl。在可变和恒定结构域的任何构型中(包括上文列出的任何示例性构型),可变和恒定结构域可以彼此直接连接或可以通过完整或部分铰链或接头区连接。铰链区可以由至少2个(例如,5、10、15、20、40、60或更多个)氨基酸组成,其导致单一多肽分子中相邻的可变和/或恒定结构域之间的柔性或半柔性连接。此外,本发明的抗体的抗原结合片段可以包含彼此和/或与一个或多个单体vh或vl结构域非共价结合(例如,通过二硫键)的上文列出的任何可变和恒定结构域构型的同二聚体或异二聚体(或其它多聚体)。
与完整抗体分子一样,抗原结合片段可以是单特异性的或多特异性的(例如,双特异性的)。抗体的多特异性抗原结合片段通常包含至少两个不同的可变结构域,其中每个可变结构域能够特异性结合单独的抗原或同一抗原上的不同表位。任何多特异性抗体形式(包括本文公开的示例性双特异性抗体形式)可以使用本领域可获得的常规技术适应以用于本发明抗体的抗原结合片段的情况中。
用于本发明的抗-人grem1抗体和抗体片段包括具有与所述抗体的氨基酸序列不同的氨基酸序列,但保留结合人grem1的能力的蛋白质。当与亲本序列比较时,此类变体抗体和抗体片段包含一个或多个氨基酸添加、删除或置换,但显示出与所述抗体的生物学活性基本相同的生物学活性。同样地,与公开的序列相比,本发明的抗体编码dna序列包括包含一个或多个核苷酸添加、缺失或取代的序列,但是编码与本发明的抗体或抗体片段基本上生物等效的抗体或抗体片段。
如果例如两种抗原结合蛋白或抗体是在相似的实验条件下以相同的摩尔剂量(单剂量或多剂量)施用时其吸收速率和程度不显示显著差异的药物等效物或药物替代物,它们被认为是生物等效的。如果一些抗体在其吸收程度上而不是吸收速率上等同,那么它们将被视为等同物或药物替代品,且仍可被认为是生物等效的,因为吸收率的这种差异是有意的并且反映在标签中,它们对于例如长期使用时的有效体内药物浓度的获得不是必需的,并且对于所研究的特定药物产品而言被认为是医学上无关紧要的。
在一个实施方案中,如果在两种抗原结合蛋白的安全性、纯度和效力方面没有临床上有意义的差异,则它们是生物等效的。
在一个实施方案中,如果患者可以在参考产品和生物产品之间转换一次或多次而与没有这种转换的持续治疗相比没有预期的不良反应风险(包括临床上显著的免疫原性变化或减弱的有效性)的增加,则两种抗原结合蛋白是生物等效的。
在一个实施方案中,如果两种抗原结合蛋白对于使用的一种或多种病症均通过共同的一种或多种机制起作用,只要这些机制是已知的,则这两种抗原结合蛋白是生物等效的。
生物等效性可以通过体内和/或体外方法证明。生物等效性测量包括,例如,(a)在人或其他哺乳动物中的体内测试,其中抗体或其代谢物的浓度在血液、血浆、血清或其他生物流体中随时间测量;(b)与人体内生物利用度数据相关并可合理预测人体内生物利用度的体外测试;(c)在人或其他哺乳动物中的体内测试,其中随时间测量抗体(或其靶标)的适当急性药理作用;和(d)在确定抗体的安全性、效力或者生物利用度或生物等效性的良好控制的临床试验中。
本发明抗体的生物等效变体可以通过例如进行残基或序列的各种置换或者删除生物活性不需要的末端或内部残基或序列来构建。例如,可以删除不是生物学活性必需的半胱氨酸残基或用其他氨基酸替代以防止在复性时形成不必要的或不正确的分子内二硫键。在其他情况下,生物等效抗体可包括包含氨基酸变化的抗体变体,其改变抗体的糖基化特征,例如消除或去除糖基化的突变。
根据本发明的某些实施方案,用于本发明方法的抗grem1抗体包含fc结构域,所述fc结构域包含增强或减弱抗体与fcrn受体的结合的一个或多个突变,例如,在与中性ph值相比的酸性ph下。例如,本发明包括包含fc结构域的ch2或ch3区中的突变的抗grem1抗体,其中所述突变在酸性环境中(例如,在其中ph范围为约5.5-约6.0的核内体中)增加fc结构域对fcrn的亲和力。当施用于动物时,这类突变可导致抗体的血清半衰期增加。此类fc修饰的非限制性实例包括,例如,250位的修饰(例如,e或q);250和428位的修饰(例如,l或f);252位的修饰(例如,l/y/f/w或t)、254位的修饰(例如,s或t)和256位的修饰(例如,s/r/q/e/d或t);或428和/或433位的修饰(例如,h/l/r/s/p/q或k)和/或434位的修饰(例如,a、w、h、f或y[n434a、n434w、n434h、n434f或n434y]);或250和/或428位的修饰;或者307或308位(例如,308f、v308f)和434位的修饰。在一个实施方案中,该修饰包括428l(例如,m428l)和434s(例如,n434s)修饰;428l、259i(例如,v259i)和308f(例如,v308f)修饰;433k(例如,h433k)和434(例如,434y)修饰;252、254和256(例如,252y、254t和256e)修饰;250q和428l修饰(例如,t250q和m428l);及307和/或308修饰(例如,308f或308p)。在又一个实施方案中,该修饰包括265a(例如,d265a)和/或297a(例如,n297a)修饰。
例如,本发明包括包含fc结构域的抗grem1抗体,所述fc结构域包含选自下组的一个或多个突变对或突变组:250q和248l(例如,t250q和m248l);252y、254t和256e(例如,m252y、s254t和t256e);428l和434s(例如,m428l和n434s);257i和311i(例如,p257i和q311i);257i和434h(例如,p257i和n434h);376v和434h(例如,d376v和n434h);307a、380a和434a(例如,t307a、e380a和n434a);及433k和434f(例如,h433k和n434f)。前述fc结构域突变和本文公开的抗体可变结构域内的其他突变的所有可能组合都包括在本发明的范围内。
本发明还包括包含嵌合重链恒定(ch)区的抗grem1抗体,其中嵌合ch区包含源自超过一种免疫球蛋白同种型的ch区的区段。例如,本发明的抗体可包含嵌合ch区,其包含与源自人igg1、人igg2或人igg4分子的部分或全部ch3结构域组合的源自人igg1、人igg2或人igg4分子的部分或全部ch2结构域。根据某些实施方案,本发明的抗体包含具有嵌合铰链区的嵌合ch区。例如,嵌合铰链可包含与源自人igg1、人igg2或人igg4铰链区的“下铰链”序列(根据eu编号的228至236位的氨基酸残基)组合的源自人igg1、人igg2或人igg4铰链区的“上铰链”氨基酸序列(根据eu编号的216至227位的氨基酸残基)。
根据某些实施方案,嵌合铰链区包含源自人igg1或人igg4上铰链的氨基酸残基和源自人igg2下铰链的氨基酸残基。在某些实施方案中,包含如本文所述的嵌合ch区的抗体可以表现出改变的fc效应子功能而不会不利地影响抗体的治疗或药代动力学特性(参见,例如,2013年2月1日提交的美国临时申请号61/759,578,其公开内容通过引用整体并入本文)。
通常,用于本发明方法的抗体可通过与人grem1结合起作用。在一些实施方案中,本发明的抗体可以结合人grem1的催化结构域或其片段。在一些实施方案中,本发明的抗体可以与分泌形式的人grem1或与膜结合形式的人grem1结合。在一些实施方案中,本发明的抗体可以结合超过一个结构域(交叉反应性抗体)。
在本发明的某些实施方案中,抗体可以结合位于seqidno:594或seqidno:595的氨基酸残基25-184之间的区域中的表位。
在某些实施方案中,用于本发明方法的抗体可通过与全长天然蛋白的任何其他区域或片段结合来阻断或抑制bmp信号传导而起作用,该全长天然蛋白的氨基酸序列显示于seqidno:594中,其由seqidno:593中所示的核酸序列编码。在一个实施方案中,本发明的抗体可通过结合全长grem1或其片段来逆转bmp2、bmp4或bmp7的抑制而起作用。在一些实施方案中,本发明的抗体可通过促进bmp信号传导起作用或可阻断grem1和bmp(包括bmp2、bmp4或bmp7)之间的结合。
在某些实施方案中,用于本发明方法的抗体可通过阻断grem1与肝素的结合和/或通过抑制肝素介导的vegfr-2活化而起作用。
在某些实施方案中,用于本发明方法的抗体可以是双特异性抗体。本发明的双特异性抗体可以结合人grem1的一个结构域中的一个表位,且也可以结合人grem1的第二结构域中的一个表位。在某些实施方案中,本发明的双特异性抗体可以结合相同结构域中的两个不同表位。
在一个实施方案中,结合人grem1的全人单克隆抗体或其抗原结合片段可用于本发明的方法,其中所述抗体或其片段表现出一种或多种以下特征:(i)包含具有选自seqidno:2、18、34、50、66、82、98、114、130、146、162、178、194、210、226、242、258、274、290、306、322、338、354、370、386、402、418、434、450、466、482、498、514、530、546、562和578的氨基酸序列或者其具有至少90%、至少95%、至少98%或至少99%的序列同一性的基本相似的序列的hcvr;(ii)包含具有选自seqidno:10、26、42、58、74、90、106、122、138、154、170、186、202、218、234、250、266、282、298、314、330、346、362、378、394、410、426、442、458、474、490、506、522、538、554、570和586的氨基酸序列或者其具有至少90%、至少95%、至少98%或至少99%的序列同一性的基本相似的序列的lcvr;(iii)包含具有选自seqidno:8、24、40、56、72、88、104、120、136、152、168、184、200、216、232、248、264、280、296、312、328、344、360、376、392、408、424、440、456、472、488、504、520、536、552、568和584的氨基酸序列或者其具有至少90%、至少95%、至少98%或至少99%的序列同一性的基本相似的序列的hcdr3结构域;和具有选自seqidno:16、32、48、64、80、96、112、128、144、160、176、192、208、224、240、256、272、288、304、320、336、352、368、384、400、416、432、448、464、480、496、512、528、544、560、576和592的氨基酸序列或者其具有至少90%、至少95%、至少98%或至少99%的序列同一性的基本相似的序列的lcdr3结构域;(iv)包含具有选自seqidno:4、20、36、52、68、84、100、116、132、148、164、180、196、212、228、244、260、276、292、308、324、340、356、372、388、404、420、436、452、468、484、500、516、532、548、564和580的氨基酸序列或者其具有至少90%、至少95%、至少98%或至少99%的序列同一性的基本相似的序列的hcdr1结构域;具有选自seqidno:6、22、38、54、70、86、102、118、134、150、166、182、198、214、230、246、262、278、294、310、326、342、358、374、390、406、422、438、454、470、486、502、518、534、550、566和582的氨基酸序列或者其具有至少90%、至少95%、至少98%或至少99%的序列同一性的基本相似的序列的hcdr2结构域;具有选自seqidno:12、28、44、60、76、92、108、124、140、156、172、188、204、220、236、252、268、284、300、316、332、348、364、380、396、412、428、444、460、476、492、508、524、540、556、572和588的氨基酸序列或者其具有至少90%、至少95%、至少98%或至少99%的序列同一性的基本相似的序列的lcdr1结构域;和具有选自seqidno:14、30、46、62、78、94、110、126、142、158、174、190、206、222、238、254、270、286、302、318、334、350、366、382、398、414、430、446、462、478、494、510、526、542、558、574和590的氨基酸序列或者其具有至少90%、至少95%、至少98%或至少99%的序列同一性的基本相似的序列的lcdr2结构域;(v)以等于或小于10-7的kd与grem1结合;(vi)阻断grem1与bmp2、bmp4或bmp7之一的结合;(vii)阻断bmp信号传导的grem1抑制并促进细胞分化;和(viii)阻断grem1与肝素的结合。
如通过体外或体内测定所确定的,用于本发明方法的某些抗-grem1抗体能够结合并中和grem1的活性。本发明的抗体结合并中和grem1活性的能力可以使用本领域技术人员已知的任何标准方法测量,包括如本文所述的结合分析或活性分析。
用于测量结合活性的非限制性的示例性体外测定包括在例如t200biacore仪器上进行的表面等离子体共振。阻断分析可用于确定抗-grem1抗体在体外阻断grem1的bmp4结合能力的能力。抗-grem1抗体在促进bmp4信号传导和响应于bmp4信号传导的成骨细胞祖细胞的细胞分化中的活性可以作为使用本文所述的抗grem1抗体的grem1-肝素结合相互作用的抑制评估。
本发明还包括抗-grem1抗体及其抗原结合片段,其与以下任何蛋白质或肽的至少一种生物活性片段结合:用于本发明的方法中的seqidno:594(全长天然人grem1)或seqidno:595(人grem1的重组形式)。本文所述的任何grem1肽或其片段可用于产生抗grem1抗体。
可以修饰肽以包括某些残基的添加或置换用于标记或用于与载体分子(如klh)缀合的目的。例如,可以在肽的n末端或c末端添加半胱氨酸,或者可以添加接头序列以制备用于免疫的与例如klh缀合的肽。
对grem1特异性的抗体可以不含另外的标记或部分,或者它们可以含有n-末端或c-末端标记或部分。在一个实施方案中,标记或部分是生物素。在结合分析中,标记(如果有的话)的位置可以决定肽相对于肽结合于其上的表面的定向。例如,如果表面涂布有抗生物素蛋白,则含有n-末端生物素的肽将被定向以使得肽的c-末端部分位于表面的远端。在一个实施方案中,标记可以是放射性核素、荧光染料或mri可检测标记。在某些实施方案中,此类标记的抗体可用于诊断分析(包括成像分析)。
本发明包括抗-grem1抗体的用途,所述抗-grem1抗体与grem1的一个或多个区域内存在的一个或多个氨基酸相互作用。抗体与其结合的表位可以由3个或更多个(例如,3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20或更多个)位于grem1分子的任何前述区域内的氨基酸的单一连续序列组成(例如结构域中的线性表位)。或者,表位可以由位于grem1分子的前述区域任一或两者内的多个非连续氨基酸(或氨基酸序列)组成(例如构象表位)。
可以使用本领域普通技术人员已知的各种技术来确定抗体是否与多肽或蛋白质内的“一个或多个氨基酸相互作用”。示例性技术包括,例如,常规交叉阻断分析,如antibodies,harlowandlane(coldspringharborpress,coldspringharbor,ny)中所述的。其他方法包括丙氨酸扫描突变分析、肽印迹分析(reineke(2004)methodsmolbiol248:443-63)、肽裂解分析晶体学研究和nmr分析。另外,可以使用如表位切除、表位提取(epitopeextraction)和抗原的化学修饰的方法(tomer(2000)proteinscience9:487-496)。可用于鉴定多肽内抗体与其相互作用的氨基酸的另一种方法是通过质谱法检测的氢/氘交换。一般而言,氢/氘交换方法涉及对感兴趣的蛋白质进行氘标记,然后将抗体与氘标记的蛋白质结合。接下来,将蛋白质/抗体复合物转移到水中,并且受抗体复合物保护的氨基酸内的可交换质子以比不是界面的部分的氨基酸内的可交换质子更慢的速率进行氘-氢反向交换。结果,形成蛋白质/抗体界面的部分的氨基酸可以保留氘,且因此与未包括在界面中的氨基酸相比表现出相对高的质量。在抗体解离后,对靶蛋白进行蛋白酶切割和质谱分析,从而揭示对应于抗体与其相互作用的特定氨基酸的氘标记的残基。参见,例如,ehring(1999)analyticalbiochemistry267(2):252-259;engen和smith(2001)anal.chem.73:256a-265a。
术语“表位”是指b和/或t细胞所响应的抗原上的位点。b-细胞表位可以由连续氨基酸或者通过蛋白质的三级折叠并置的非连续氨基酸形成。由连续氨基酸形成的表位通常在暴露于变性溶剂时保留,而通过三级折叠形成的表位通常在用变性溶剂处理时丧失。表位通常包括处于独特空间构象中的至少3个,更通常至少5个或8-10个氨基酸。
修饰辅助分析(modification-assistedprofiling,map),也称为基于抗原结构的抗体分析(asap)是根据每种抗体对化学或酶促修饰的抗原表面的结合特征的相似性而对针对相同抗原的大量单克隆抗体(mabs)进行分类的方法(参见,例如,美国专利公开no.2004/0101920,在此特别地通过引用整体并入)。每个类别可以反映与另一类别代表的表位明显不同或部分重叠的独特表位。该技术允许快速过滤遗传上相同的抗体,使得表征可以集中于遗传上不同的抗体。当应用于杂交瘤筛选时,map可以帮助鉴定产生具有所需特征的mab的稀有杂交瘤克隆。map可用于将本发明的抗体分选成结合不同表位的抗体组。
在某些实施方案中,用于本发明的方法中的抗-grem1抗体或其抗原结合片段结合天然形式(如seqidno:594中所例示的)或重组产生的(如seqidno:595中所例示的)grem1或其片段中例示的任何一个或多个区域内的表位。在某些实施方案中,如表1中所示,用于本发明的方法中的抗体与选自seqidno:594的约1-约24位范围的氨基酸残基或seqidno:594的约25位-约184位范围的氨基酸残基的至少一个氨基酸序列相互作用。这些区域在seqidno:595中进一步举例说明。
本发明包括抗-人grem1抗体的用途,所述抗-人grem1抗体与本文表1中描述的任何特定示例性抗体或具有表1中描述的任何示例性抗体的cdr序列的抗体结合相同表位或表位的一部分。同样地,本发明还包括与表1中描述的任何特定示例性抗体或具有表1中描述的任何示例性抗体的cdr序列的抗体竞争结合grem1或grem1片段的抗-人grem1抗体。
通过使用本领域已知的常规方法,可以容易地确定抗体是否与参考抗-grem1抗体结合相同的表位,或与之竞争结合。例如,为了确定测试抗体是否与本发明的参照抗-grem1抗体结合相同的表位,使参照抗体在饱和条件下与grem1蛋白或肽结合。接下来,评估测试抗体结合grem1分子的能力。如果测试抗体在参照抗-grem1抗体的饱和结合后能够结合grem1,则可以得出结论:测试抗体与参考抗-grem1抗体结合不同的表位。另一方面,如果测试抗体在参照抗-grem1抗体的饱和结合后不能与grem1蛋白结合,那么测试抗体可能结合与本发明的参照抗-grem1抗体所结合的表位相同的表位。
为了确定抗体是否与参照抗-grem1抗体竞争结合,上述结合方法以两个方向进行:在第一方向,允许参照抗体在饱和条件下与grem1蛋白结合,然后评估测试抗体与grem1分子的结合。在第二方向,使测试抗体在饱和条件下与grem1分子结合,然后评估参照抗体与grem1分子的结合。如果在两个方向上,仅第一(饱和)抗体能够结合grem1分子,则得出结论:测试抗体和参照抗体竞争结合grem1。如本领域普通技术人员所理解的,与参考抗体竞争结合的抗体可能不一定与参照抗体结合相同的表位,但可能通过结合重叠或相邻的表位来空间阻断参照抗体的结合。
如果每种抗体竞争性地抑制(阻断)另一抗体与抗原的结合,则两种抗体结合相同或重叠的表位。也就是说,如在竞争性结合分析中测量的,1倍、5倍、10倍、20倍或100倍过量的一种抗体抑制另一抗体的结合至少50%,但优选75%、90%或甚至99%(参见,例如,junghans等,cancerres.199050:1495-1502)。或者,如果抗原中减少或消除一种抗体的结合的基本上所有氨基酸突变减少或消除另一抗体的结合,则两种抗体具有相同的表位。如果减少或消除一种抗体的结合的一些氨基酸突变减少或消除另一抗体的结合,则两种抗体具有重叠的表位。
然后可以进行额外的常规实验(例如,肽突变和结合分析)以确认观察到的测试抗体缺乏结合是否实际上是由于与参照抗体结合相同的表位或者是否是空间阻断(或另一现象)造成观察到的结合的缺乏。可以使用elisa、ria、表面等离子体共振、流式细胞术或本领域可获得的任何其他定量或定性抗体结合分析来进行这一类的实验。
本发明包括与治疗部分缀合的人抗-grem1单克隆抗体(“免疫缀合物”)的用途。如本文所用,术语“免疫缀合物”是指与放射性试剂、细胞因子、干扰素、靶标或报告体部分、酶、毒素或治疗剂化学或生物学连接的抗体。抗体可以在沿着分子的任何位置与放射性试剂、细胞因子、干扰素、靶标或报告体部分、酶、毒素或治疗剂连接,只要它能够结合其靶标即可。免疫缀合物的实例是抗体药物缀合物。在一些实施方案中,试剂可以是针对人grem1,或针对细胞因子例(如il-1、il-6)或趋化因子(如tgf-β)的第二种不同抗体。可以与抗-grem1抗体缀合的治疗部分的类型将考虑待治疗的病症和要实现的所需治疗效果。用于形成免疫缀合物的合适试剂的实例是本领域已知的;参见例如wo05/103081。免疫缀合物和免疫毒素的制备通常是本领域熟知的(参见,例如,美国专利no.4,340,535)。免疫缀合物详细描述于例如美国专利号7,250,492,7,420,040和7,411,046中,其各自以其整体并入本文。
用于本发明方法的抗体可以是单特异性的、双特异性的或多特异性的。多特异性抗体可以对一种靶多肽的不同表位是特异性的,或者可以含有对一种以上靶多肽特异性的抗原结合结构域。参见,例如,tutt等,1991,j.immunol.147:60-69;kufer等,2004,trendsbiotechnol.22:238-244。本发明的抗体可以与另一功能分子(例如,另一肽或蛋白质)连接或共表达。例如,抗体或其片段可以与一种或多种其他分子实体(如另一抗体或抗体片段)功能性连接(例如,通过化学偶联、遗传融合、非共价结合或其他方式)以产生具有第二结合特异性的双特异性或多特异性抗体。例如,本发明包括双特异性抗体,其中免疫球蛋白的一个臂对grem1的n-末端区域或其片段是特异性的,并且免疫球蛋白的另一臂对grem1的c-末端区域或第二治疗靶标是特异性的,或与治疗部分缀合。可以在本发明的情况中使用的示例性双特异性抗体形式涉及使用第一免疫球蛋白(ig)ch3结构域和第二igch3结构域,其中第一和第二igch3结构域彼此至少一个氨基酸不同,并且其中与缺乏该氨基酸差异的双特异性抗体相比,至少一个氨基酸差异降低了双特异性抗体与蛋白a的结合。在一个实施方案中,第一igch3结构域结合蛋白a,且第二igch3结构域含有降低或消除蛋白a结合的突变,例如h95r修饰(按照imgt外显子编号;按照eu编号的h435r)。第二ch3可进一步包含y96f修饰(按照imgt;按照eu的y436f)。可以在第二ch3中发现的进一步修饰包括:在igg1抗体的情况下,d16e、l18m、n44s、k52n、v57m和v82i(按照imgt;按照eu的d356e、l358m、n384s、k392n、v397m和v422i);在igg2抗体的情况下,n44s、k52n和v82i(imgt;按照eu的n384s、k392n和v422i);及在igg4抗体的情况下,q15r、n44s、k52n、v57m、r69k、e79q和v82i(按照imgt;按照eu的q355r、n384s、k392n、v397m、r409k、e419q和v422i)。上述双特异性抗体形式的变化涵盖在本发明的范围内。
可以在本发明的情况中使用的其他示例性双特异性形式包括但不限于例如基于scfv的或双抗体双特异性形式、igg-scfv融合体、双可变结构域(dvd)-ig、quadroma、杵臼(knobs-into-holes)、共同轻链(例如,带有杵臼的共同轻链等)、crossmab、crossfab、(seed)体、亮氨酸拉链、duobody、igg1/igg2、双重作用fab(daf)-igg和mab2双特异性形式(参见,例如,klein等,2012,mabs4:6,1-11,以及其中引用的参考文献,用于前述形式的综述)。还可以使用肽/核酸缀合构建双特异性抗体,例如,其中使用具有正交化学反应性的非天然氨基酸来产生位点特异性抗体-寡核苷酸缀合物,其然后将自组装成具有确定的组成、化合价和几何形状的多聚复合物(参见,例如,kazane等,j.am.chem.soc.[epub:dec.4,2012])。
用于产生适用于本发明方法的单克隆抗体(包括全人单克隆抗-grem1抗体或其抗原结合片段)的方法是本领域已知的。可以在本发明的情况中使用任何这样的已知方法来制备特异性结合人grem1的人抗体。
在某些实施方案中,用于本发明的抗体或其抗原结合片段获自用初级免疫原如天然的全长人grem1(参见,例如,genbank登录号np_037504(seqidno:594))或用重组形式的grem1(seqidno:595)或grem1片段免疫的小鼠,然后用第二免疫原或用grem1的免疫原性活性片段免疫。
免疫原可以是人grem1的免疫原性片段或编码其片段的dna。免疫原可以是与组氨酸标签和/或与抗体fc区的片段偶联的grem1。
全长人grem1的氨基酸序列(也称为genbank登录号np-037504)显示为seqidno:594。重组grem1的全长氨基酸序列(与fc区和组氨酸标签偶联的氨基酸残基25-184grem1)显示为seqidno:595。
grem1的全长dna序列显示为seqidno:593。
在某些实施方案中,可以使用上述区域的片段或通过从本文描述的区域的n或c末端之一或两者延伸超出指定区域约5-约20个氨基酸残基的肽来制备与人grem1特异性结合的抗体。在某些实施方案中,上述区域或其片段的任何组合可用于制备人grem1特异性的抗体。在某些实施方案中,人grem1或其片段的任何一个或多个上述区域可用于制备单特异性、双特异性或多特异性抗体。
在转基因小鼠中产生人抗体的方法也是本领域已知的。可以在本发明的情况中使用任何这样的已知方法来制备特异性结合人grem1的人抗体。
使用velocimmunetm技术(参见,例如,美国专利号6,596,541,regeneronpharmaceuticals,
通常,用目标抗原攻击
最初,分离具有人可变区和小鼠恒定区的高亲和力嵌合抗体。如在下面的实验部分中,对抗体进行表征和针对所需的特征进行选择,包括亲和力、选择性、表位等。用期望的人恒定区替换小鼠恒定区以产生本发明的全人抗体,例如野生型或修饰的igg1或igg4。虽然选择的恒定区可根据具体用途而变化,但高亲和力抗原结合和靶特异性特征存在于可变区中。
通常,用于本发明方法的抗-grem1抗体具有非常高的亲和力,当通过与固定在固相上或在溶液相中的抗原结合来测量时,通常具有约10-12至约10-7m的kd。虽然抗体的恒定区可根据具体用途而变化,但高亲和力抗原结合和靶特异性特征存在于可变区中。
用于本发明方法的抗-grem1抗体或其抗原结合片段可以存在于药物组合物中。这些药物组合物与合适的载体、赋形剂和其它提供改善的转移、递送、耐受性等的试剂一起配制。在所有药物化学家都知道的处方集中可以找到大量合适的制剂:remington'spharmaceuticalsciences,mackpublishingcompany,easton,pa。这些制剂包括,例如,粉末、糊剂、油膏、凝胶、蜡、油、脂质,含脂质(阳离子或阴离子)的囊泡(如lipofectintm,lifetechnologies,carlsbad,ca)、dna缀合物、无水吸收糊剂、水包油和油包水乳液、乳液碳蜡(各种分子量的聚乙二醇)、半固体凝胶和含有碳蜡的半固体混合物。也参见powell等“compendiumofexcipientsforparenteralformulations”pda,jpharmscitechnol52:238-311(1998)。
各种递送系统是已知的并且可用于施用包含抗-grem1抗体或其抗原结合片段的药物组合物,例如包封在脂质体、微粒、微胶囊中、能够表达抗体的重组细胞、受体介导的内吞作用(参见,例如,wu等,jbiolchem262:4429-4432(1987))。抗体也可以通过基因治疗技术递送。引入方法包括但不限于皮内、肌肉内、腹膜内、静脉内、皮下、鼻内、硬膜外和口服途径。组合物可以通过任何方便的途径施用,例如通过输注或推注,通过上皮或粘膜内衬(例如口腔粘膜,直肠和肠粘膜等)吸收,并且可以与其他生物活性剂一起施用。施用可以是系统的或局部的。
包含抗-grem1抗体或其抗原结合片段的药物组合物可以用标准针头和注射器皮下或静脉内递送。另外,就皮下递送而言,笔式递送装置易于应用于递送本发明的药物组合物。这种笔式递送装置可以是可重复使用的或一次性的。可重复使用的笔式递送装置通常使用包含药物组合物的可更换的药盒。一旦施用了药盒内的所有药物组合物并且药盒是空的,就可以容易地丢弃空药盒并用含有药物组合物的新药盒替换。然后可以重复使用该笔式递送装置。在一次性笔式递送装置中,没有可更换的盒。相反,一次性笔式递送装置预填充保持在装置内的储器中的药物组合物。一旦储器清空药物组合物,就丢弃整个装置。
许多可重复使用的笔式和自动注射器递送装置可用于皮下递送本发明的药物组合物。实例包括但不限于autopentm(owenmumford,inc.,woodstock,uk),disetronictmpen(disetronicmedicalsystems,bergdorf,switzerland),humalogmix75/25tmpen,humalogtmpen,humalin70/30tmpen(elilillyandco.,indianapolis,in),novopentmi、ii和iii(novonordisk,copenhagen,denmark),novopenjuniortm(novonordisk,copenhagen,denmark),bdtmpen(bectondickinson,franklinlakes,nj),optipentm,optipenprotm,optipenstarlettm和opticliktm(sanofi-aventis,frankfurt,germany),仅举几例。具有皮下递送本发明的药物组合物的应用的一次性笔式递送装置的实例包括但不限于solostartmpen(sanofi-aventis),flexpentm(novonordisk)和kwikpentm(elililly),sureclicktmautoinjector(amgen,thousandoaks,ca),penlettm(haselmeier,stuttgart,germany),epipen(dey,l.p.)和humiratmpen(abbottlabs,abbottparkil),仅举几例。
在某些情况下,药物组合物可以在控释系统中递送。在一个实施方案中,可以使用泵(参见langer,同上;sefton,crccrit.ref.biomed.eng.14:201(1987))。在另一个实施方案中,可以使用聚合物材料;参见,medicalapplicationsofcontrolledrelease,langer和wise(eds.),1974,crcpres.,bocaraton,florida。在又一个实施方案中,控释系统可以放置在组合物的靶标附近,因此仅需要全身剂量的一小部分(参见,例如,goodson,1984,inmedicalapplicationsofcontrolledrelease,同上,vol.2,pp.115-138)。langer,science249:1527-1533(1990)的综述中讨论了其他控释系统。
可注射制剂可包括用于静脉内、皮下、皮内和肌肉内注射、滴注等的剂型。这些可注射制剂可通过公知的方法制备。例如,可注射制剂可以通过例如将上述抗体或其盐溶解、悬浮或乳化在常规用于注射的无菌水性介质或油性介质中来制备。作为用于注射的水性介质,例如有生理盐水、含有葡萄糖和其他助剂等的等渗溶液,其可以与适当的增溶剂如醇(例如乙醇)、多元醇(例如,丙二醇、聚乙二醇)、非离子表面活性剂[例如,聚山梨醇酯80、hco-50(氢化蓖麻油的聚氧乙烯(50摩尔)加合物)]等组合使用。作为油性介质,使用例如芝麻油、大豆油等,其可以与增溶剂如苯甲酸苄酯、苯甲醇等组合使用。这样制备的注射剂优选填充在适当的安瓿中。
有利地,将上述用于口服或肠胃外使用的药物组合物制备成适于配合一定剂量活性成分的单位剂量的剂型。单位剂量的这种剂型包括例如片剂、丸剂、胶囊剂、注射剂(安瓿)、栓剂等。包含的上述抗体的量通常为单位剂量的每剂型约5-约500mg;特别地在注射形式中,优选上述抗体以约5-约100mg包含和对于其他剂型,以约10-约250mg包含。
通过以下实施例进一步说明本发明,这些实施例不应解释为限制。本申请中引用的所有参考文献、专利和公开的专利申请的全部内容以及附图和序列表在此引入作为参考。
实施例
实施例1.gremlin1结合蛋白
美国专利公开号2016/0024195(其全部内容通过引用在此并入)描述了适用于本发明的嵌合和全人抗-grem1抗体(即,具有人可变结构域和人恒定结构域的抗体)的产生和表征。例如,获得了几种抗-grem1抗体,其作为交叉反应性和嵌合的抗体(即,具有人可变结构域和小鼠恒定结构域的抗体)包括,并且包括命名为h1m2907n、h2m2780n、h2m2782n、h2m2783n、h4h2783n2、h2m2784n、h2m2785n、h2m2786n、h2m2889n、h2m2890n、h2m2891n、h2m2892n、h2m2895n、h2m2897n、h2m2898n、h2m2899n、h2m2901n、h2m2906n、h2m2926n、h3m2788n和h3m2929n的那些抗体。
还获得了另外的全人抗-grem1抗体,且包括命名如下的那些抗体:h4h6232p、h4h6233p、h4h6236p、h4h6238p、h4h6240p、h4h6243p、h4h6245p、h4h6246p、h4h6248p、h4h6250p、h4h6251p、h4h6252s、h4h6256p、h4h6260p、h4h6269p和h4h6270p。
表1给出了适用于本发明方法的对人grem1特异性的选定抗体的重链和轻链可变区氨基酸序列对及其相应抗体标识。抗体通常根据以下命名法在本文中提及:fc前缀(例如“h4h”、“h1m”、“h2m”),然后是数字标识(例如,如表1中所示的“2907”),接着是“p”或“n”后缀。因此,根据该命名法,抗体可以被称为例如“h1h2907”。本文使用的抗体名称上的h4h、h1m和h2m前缀表示抗体的特定fc区。例如,“h2m”抗体具有小鼠igg2fc,而“h4h”抗体具有人igg4fc。如本领域普通技术人员所理解的,h1m或h2m抗体可以转化为h4h抗体,反之亦然,但无论如何,由表1中所示的数字标识指明的可变结构域(包括cdr)保持相同。具有相同数字抗体名称但字母后缀n、b或p不同的抗体是指具有cdr序列相同的重链和轻链但落在cdr序列之外的区域(即,框架区域)中的序列具有变异的抗体。因此,特定抗体的n、b和p变体在其重链和轻链可变区内具有相同的cdr序列,但在它们的框架区内彼此不同。
表1
实施例2.抗-gremlin-1抗体治疗在小鼠慢性缺氧模型中恢复肺动脉直径且恢复右心室心功能
为了评估抗-gremlin-1抗体h4h6245p2在肺动脉高血压中的作用,使用慢性缺氧诱导的肺动脉高血压小鼠模型进行了两项独立的研究。
以下材料和方法用于这些研究。
材料和方法
小鼠
对于这两项研究,使用11至13周龄的taconicc57bl/6小鼠。将小鼠按重量分成处理组,使得不同组间的起始体重相似。选择笼子以保持在约21%o2(常压常氧)或置于10%o2(常压低氧)室(改良的3'半刚性隔离器单元,charlesriver)中,通过调节对稳定的室内空气进气的n2流保持低o2水平。
对于第一项研究(研究1),从第14天开始给小鼠施用药物或盐水。将饲养在常压常氧笼中的一组小鼠(n=10)以5ml/kg皮下施用盐水,每周两次,持续两周,而将在常压低氧笼中饲养的小鼠分成3个处理组,包括每周两次用5ml/kg盐水皮下处理两周的一组小鼠(n=10),每周两次皮下施用25mg/kg的同种型对照抗体持续两周的一组小鼠(n=10),和每周两次用抗-gremlin-1抗体h4h6245p2以25mg/kg皮下处理持续两周的一组小鼠(n=10)。
对于第二项研究(研究2),从第14天开始给小鼠施用药物或盐水。将在常压常氧笼中饲养的一组小鼠(n=10)每周两次以5ml/kg皮下施用盐水,持续四周,而将饲养在常压低氧笼中的小鼠分成5个处理组,包括每周两次以5ml/kg用盐水皮下处理4周的一组小鼠(n=10),每周两次皮下施用25mg/kg的同种型对照抗体持续4周的一组小鼠(n=10),每周两次用抗-gremlin-1抗体h4h6245p2以10mg/kg皮下处理持续4周的一组小鼠(n=10),每周两次用抗-gremlin-1抗体h4h6245p2以25mg/kg皮下处理持续4周的一组小鼠(n=9),和每周两次用抗gremlin-1抗体h4h6245p2以40mg/kg皮下处理持续四周的一组小鼠(n=10)。
表2中提供了研究1和研究2的给药时间表。
表2.小鼠慢性缺氧模型研究中的治疗性给药和治疗方案
sc=皮下
超声评估和分析
在每项研究的最后一天,使用高频超声系统(vevo2100,visualsonics)在每只小鼠中评估肺动脉大小及右心室功能和尺寸。为了评估,将小鼠麻醉(使用1.5%异氟烷,速率为1.0cc/ml医用级空气),并用直肠温度探针监测其温度和用加热平台(mousemonitors,indusinstruments)和加温灯保持在约37℃。使用亮度模式(b-模式)和运动模式(m-模式)成像。使用小鼠心脏横截面的b-模式成像来确定肺动脉瓣水平处的肺动脉截面积(pacsa)。m-模式成像用于确定脉冲波速度时间积分(vti),其源自通过肺动脉的血流的代表性多普勒描记的曲线下面积。从pacsa和vti的乘积计算右心室心搏量(rvsv)。从sv和心率(hr)的乘积计算右心室心输出量(rvco)。m-模式成像用于确定舒张期和收缩期中的右心室游离壁(rvfw)厚度。在右心室压评估之前将动物放回其居住笼中。
右心室压评估
随后评估所有处理组的右心室压。用异氟烷麻醉小鼠,并使用加热平台(heatedhardpad1,braintreescientific)和循环热水泵(t/pumpclassic,gaymarindustries)将其保持在约37℃。通过在右颈总动脉和右颈静脉上脱毛来准备每只小鼠的颈部区域用于手术。进行切开并小心分离右颈静脉以免损伤颈动脉和/或迷走神经。将一段5-0丝线缝合线置于分离的颈静脉下以允许血管头向回缩,然后使用30号针将一个孔引入颈静脉中。将压力导管(micro-尖端导管换能器spr-1000,millarinstruments,inc.)插入颈静脉的开口中并经过右心房推进到右心室中。将导管连接到压力/体积仪(mpvs-300,millarinstruments,inc.),其测量心率以及舒张和收缩期右心室压。使用数据采集系统(powerlab4/35,adinstruments)数字地获取这些参数。labchartpro7.0软件(adinstruments)用于分析右心室压。读数从压力描记的60秒间隔(在记录2分钟之后以允许压力稳定)量化。分析的参数是右心室收缩压(rvsp)、心率(hr)和右心室压升高率(dp/dtmax)。
血清/组织收集和右心室肥大的评估
完成右心室压测量后,取出导管并处死每只动物。打开腹腔并从腔静脉抽取血液用于血细胞比容评估和血清收集。然后打开胸腔,且右肺的中叶用5-0丝线缝合线结扎,切除,置于rnalater(sigma-aldrich,cat#r0901)中,并在24小时后在-80℃下冷冻。从每只动物切除心脏,并且小心地将右心室(rv)从左心室和隔膜(lv+s)切除。将两片心脏组织分别在微量天平(aj000,mettler)上称重以计算rv肥大指数[rv/(lv+s);fultonindex]。
来自每个处理组的一半动物用磷酸盐缓冲溶液(pbs,ph7.4)以20-25mmhg灌注肺,然后用10%中性缓冲福尔马林(nbf)固定。在组织处理和石蜡包埋之前,将肺保持于10%nbf中24小时和然后置于70%乙醇中至少48小时。对于未进行肺的灌注-固定的动物,在切除之前将右下叶用5-0丝线缝合线结扎,称重并在液氮中冷冻。
结果
gremlin-1抑制恢复慢性缺氧中的肺动脉直径
在研究1中,小鼠心脏横截面的b-模式超声成像显示,与常氧盐水处理的小鼠相比,暴露于缺氧4周使盐水处理小鼠中的pacsa降低~28%(表3)。用同种型对照抗体治疗没有显著影响缺氧盐水处理小鼠中观察到的pacsa值。用抗-gremlin-1抗体治疗导致pacsa大小比缺氧同种型对照抗体治疗小鼠测量的大~46%,并且来自缺氧抗-gremlin-1治疗组的这一计算的pacsa与常氧盐水处理的小鼠组的相似。因此,抗-gremlin-1抗体能够恢复缺氧中的肺动脉直径。
在研究2中,小鼠心脏横截面的b-模式超声成像显示,相对于常氧盐水处理的小鼠,6周的缺氧暴露在盐水处理的小鼠中使pacsa降低~32%(表3)。同种型对照抗体治疗的动物的pacsa值与缺氧中的盐水处理相似。用10mg/kg较低浓度的抗-gremlin-1抗体治疗导致计算的pacsa值比同种型对照抗体治疗的计算值大21%(显著)。较高浓度(25和40mg/kg)的抗-gremlin-1导致pacsa值与常氧盐水处理小鼠中测量的相似,并且显著大于同种型对照抗体处理。这些结果证明了抗-gremlin-1抗体对解决由慢性缺氧诱导的肺动脉直径变化的剂量依赖性的作用。
gremlin-1抑制恢复右心室心功能
在研究1中,脉冲波vti的超声m-模式成像显示,在暴露于慢性缺氧的动物中通过肺动脉的血流的速度没有显著差异(最高5%增加)(数据未显示)。如表3所示,盐水-和同种型对照-处理的小鼠两者的计算的右心室搏出量(vti和pacsa的乘积)在暴露于缺氧时显著降低23-30%。用抗-gremlin-1抗体治疗导致右心室搏出量的降低逆转到与常氧盐水治疗的小鼠相似的值。这意味着gremlin-1抑制可以恢复缺氧中的搏出量。心率(其被测量并发现各组之间没有显著差异)用于确定右心室心输出量。相对于常氧盐水处理的小鼠,发现暴露于慢性缺氧的动物中的右心室心输出量显著降低21%。与低氧同种型对照抗体治疗相比,低氧抗-gremlin-1治疗小鼠的测量的心输出量值高大约48%;该值比常氧盐水处理组的测量值高7%,表明gremlin-1抑制恢复了缺氧中的心输出量。总的来说,这些超声结果表明慢性缺氧中的抗-gremlin-1抗体治疗改善心脏搏出量和心输出量,而具有最小的心率变化。
在研究2中,脉冲波vti的超声m-模式成像显示,在常氧与低氧条件下用盐水治疗的动物通过肺动脉的血流速度没有显著差异(最高11%增加)。如表3所示,与常氧小鼠相比时,缺氧使盐水处理动物的搏出量降低32%。与低氧盐水治疗组相比,同种型对照治疗组的计算搏出量大16%(非显著的),且由于这一点,与用10或40mg/kg抗-gremlin-1抗体治疗的动物的值的比较不是统计学显著的,尽管该值比低氧盐水处理组的值高26-41%并且与常氧盐水处理组中的值相当。用25mg/kg的抗-gremlin-1抗体治疗导致平均搏出量与常氧盐水治疗小鼠的计算值相似,并且这些值显著大于同种型对照抗体治疗的计算值38%(表3)。测量心率并发现在不同条件之间是相当的。在盐水治疗组中,6周的慢性缺氧使右心室心输出量降低35%,并且使用同种型对照抗体对恢复心输出量没有影响(与常氧盐水相比降低27%)。使用10mg/kg抗-gremlin-1抗体增加缺氧中的心输出量(超过同种型对照抗体治疗的测量值15%)但比常氧盐水处理小鼠中发现的值低16%。使用25或40mg/kg的抗-gremlin-1抗体显示出比用同种型对照抗体处理高30-35%并且与常氧盐水处理的小鼠中发现的值相当的心输出量增加的益处。总的来说,这些数据表明,在慢性缺氧中使用高剂量(25或40mg/kg)的抗-gremlin-1抗体改善心脏功能。
表3:在每项研究结束时测量的平均肺动脉截面积(pacsa)、搏出量、心率和右心室心输出量
具有sidak’s多重比较的单因素anova检验:*、**、***、****p<0.05、0.01、0.001、0.0001相对于常压常氧盐水治疗;#、##、###、####p<0.01、0.001、0.0001相对于常压低氧同种型对照治疗。
实施例3.抗-gremlin-1抗体治疗在肺动脉高血压的sugen5416/慢性缺氧小鼠模型中恢复肺动脉直径
为了进一步评价抗-grem1抗体h4h6245p2在治疗肺动脉高血压中的功效,使用了血管内皮生长因子受体拮抗剂sugen5416/慢性缺氧小鼠模型。
以下材料和方法用于该研究。
材料和方法
小鼠
使用11至13周龄的taconicc57bl/6小鼠。将小鼠按重量分成处理组使得不同组的起始体重相似。选择笼子以保持在约21%o2(常压常氧)下或置于10%o2(常压低氧)室(改良的3'半刚性隔离器单元,charlesriver)中,通过调节到稳定的室内空气进气的n2流保持低o2水平。从第21天开始给小鼠施用sugen5416(sigma,cat#s8442;vegfr抑制剂,每周以20mg/kg皮下注射,6周)和药物或盐水。将饲养在常压常氧笼中的一组小鼠(n=10)皮下施用5ml/kg盐水,每周两次,持续3周,而将常压低氧笼中的小鼠分成5个处理组,包括每周两次用5ml/kg盐水皮下处理三周的一组小鼠(n=10),每天口服施用300mg/kg波生坦(sequoiaresearchproductscatsrp02325b)持续三周的一组小鼠(n=9),每周两次皮下施用25mg/kg同种型对照抗体持续三周的一组小鼠(n=10),每周两次用抗-gremlin-1抗体以25mg/kg皮下治疗持续三周的一组小鼠(n=10),每周两次用抗-gremlin-1抗体以25mg/kg皮下治疗持续三周并每天口服施用300mg/kg波生坦持续三周的一组小鼠(n=9)。表4中显示了小鼠组的实验给药和治疗方案。
表4:sugen5416/慢性缺氧小鼠模型研究中各组的治疗性给药和治疗方案
sc=皮下
po=口服
超声评估和分析
在研究的最后一天,使用高频超声系统(vevo2100,visualsonics)在每只小鼠中评估肺动脉大小及右心室功能和尺寸。为了评估,将小鼠麻醉(使用1.5%异氟烷,速率为1.0cc/ml医用级空气),且用直肠温度探针监测其温度且用加热平台(mousemonitors,indusinstruments)和加温灯保持在约37℃。使用亮度模式(b-模式)和运动模式(m-模式)成像两者。使用小鼠心脏横截面的b-模式成像来确定肺动脉瓣水平处的肺动脉截面积(pacsa)。m-模式成像用于确定脉冲波速度时间积分(vti),其来自通过肺动脉的血流的代表性多普勒描记的曲线下面积。从pacsa和vti的乘积计算右心室搏出量(rvsv)。从sv和心率(hr)的乘积计算右心室心输出量(rvco)。m-模式成像用于确定舒张期和收缩期中的右心室游离壁(rvfw)厚度。在右心室压评估之前将动物放回其居住笼中。
右心室压评估
随后评估所有处理组的右心室压。用异氟烷麻醉小鼠,并使用加热平台(heatedhardpad1,braintreescientific)和循环热水泵(t/pumpclassic,gaymarindustries)将其保持在约37℃。通过使右侧颈总动脉和右颈静脉脱毛将每只小鼠的颈部区域准备用于手术。进行切开并小心地分离右颈静脉以免损伤颈动脉和/或迷走神经。将一段5-0丝线缝合线置于分离的颈静脉下以允许血管的头向回缩,然后使用30号针将孔引入颈静脉中。将压力导管(micro-尖端导管换能器spr-1000,millarinstruments,inc.)插入颈静脉的开口中并经过右心房推进到右心室中。将导管连接到压力/体积仪器(mpvs-300,millarinstruments,inc.),其测量心率以及舒张和收缩期右心室压。使用数据采集系统(powerlab4/35,adinstruments)数字地获取这些参数。labchartpro7.0软件(adinstruments)用于分析右心室压。读数从压力描记的60秒间隔(在记录2分钟之后以允许压力稳定)量化。分析的参数是右心室收缩压(rvsp)、心率(hr)和右心室压力升高率(dp/dtmax)。
血清/组织收集和右心室肥大的评估
完成右心室压力测量后,取出导管并处死每只动物。打开腹腔并从腔静脉抽取血液用于血细胞比容评估和血清收集。然后打开胸腔,右肺的中叶用5-0丝线缝合线结扎,切除,置于rna的(sigma-aldrich,cat#r0901)中,和24小时后在-80℃下冷冻。从每只动物切除心脏,并且右心室(rv)小心地从左心室和隔膜(lv+s)切除。将两片心脏组织分别在微量天平(aj000,mettler)上称重以计算rv肥大指数[rv/(lv+s);fultonindex]。
来自每个处理组的一半动物用磷酸盐缓冲溶液(pbs,ph7.4)在20-25mmhg下灌注肺,然后用10%中性缓冲福尔马林(nbf)固定。在组织处理和石蜡包埋之前,将肺保持于10%nbf中24小时,然后置于70%乙醇中至少48小时。对于未进行肺的灌注-固定的动物,右下叶在切除之前用5-0丝线缝合线结扎,称重并在液氮中冷冻。
结果
gremlin-1抑制恢复sugen5416/缺氧中的肺动脉直径。
如表5中所示,小鼠心脏横截面的b-模式超声成像显示,在盐水处理的小鼠中6周sugen5416/缺氧暴露使pacsa降低29%(与常氧小鼠相比)。在缺氧中,同种型对照抗体处理的动物的pacsa值与盐水处理的相似。内皮素受体拮抗剂波生坦的使用导致pacsa值比低氧盐水处理组(显著)高约43%,但仍然与常氧中测量的相似。类似地,使用抗-gremlin-1抗体导致pacsa值比在同种型对照抗体治疗组中测量的值显著更高(28%),但仍然与在常氧盐水处理的小鼠中观察到的值相似。然而,使用波生坦和抗-gremlin-1抗体的组合对pacsa几乎没有影响,并且与缺氧中盐水或同种型对照抗体治疗发现的值相似。
表5:在研究结束时治疗组的平均肺动物截面积(pacsa)、博出量和右心室心输出量
具有sidak’s多重比较的单因素anova检验:**p<0.01vs.常压常氧盐水-治疗;%%、%%%p<0.01、0.001vs.常压低氧盐水治疗;#p<0.05vs.常压低氧同种型对照抗体治疗。
等同
本领域技术人员会认识到或能够仅使用常规试验确定本文中所描述的具体实施方案的许多等同物。这样的等同物旨在被以下权利要求的范围所涵盖。
- 还没有人留言评论。精彩留言会获得点赞!