TMEM63C在制备深静脉血栓诊断产品中的应用的制作方法
本发明涉及生物医药领域,具体涉及人tmem63c在制备深静脉血栓诊断产品中的应用。
背景技术:
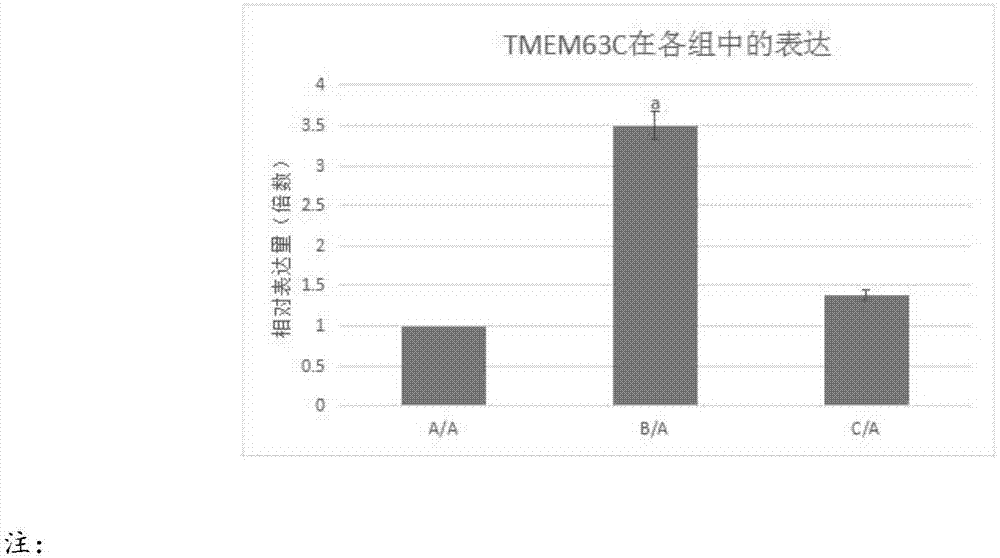
深静脉血栓是指血液在深静脉腔内不正常的凝结,并阻塞静脉腔,导致静脉回流障碍而引起的临床症状,多发于下肢,血栓脱落可引起肺动脉栓塞,每年造成大量的死亡。我国每年深静脉血栓人群发病率约为1/1000,且无性别和年龄差别,是骨折、大手术病人、肿瘤、及其他慢性病患者的主要合并症,尤其是严重创伤或大手术后的老年患者,卧床或制动时间较长,下肢静脉血流瘀滞,已发生深静脉血栓而阻塞静脉,严重者可发生缺血性坏死,若血栓脱落,可导致大面积肺栓塞而危及生命,慢性期常伴发深静脉形成后综合征。因此深静脉血栓的早期预测诊断和预防显得非常重要。深静脉血栓的形成机制很复杂,凝血功能亢进、血流停滞、静脉壁损伤是静脉栓塞形成的三要素。对于血栓形成早期,静脉内皮细胞调控、白细胞和血小板功能变化等机制均有影响。经过大量的临床和实验研究,深静脉血栓形成的病因及发病机制有了很大的进步,尤其是随着分子生物学的发展和dna重组技术的发展,特别是人类基因组计划的逐步开展,致病基因的研究为深静脉血栓发病机制的研究提供了新的思路和方法,一些血栓易感基因成为研究热点,如纤维蛋白原(fibrinogen,fg)、激肽原、内皮细胞蛋白c受体(endothelialproteincreceptor,epcr)、5,10-亚甲基四氢叶酸还原酶(methylenetetra-hydrofolatereductase,mthfr)和血管紧张素转换酶(angiotensin-convertingenzyme,ace)等。tmem63c(transmembraneprotein63c,跨膜蛋白200c)是蛋白编码基因,位于第14号染色体上。目前,还没有关于tmem63c与深静脉血栓相关的报道。因此,本领域迫切需要开发早期判断深静脉血栓的特异性标志物,并开发预防深静脉血栓的靶向药物。技术实现要素:为了实现深静脉血栓的早期发现,早期干预,本发明的目的在于提供一种新的深静脉血栓相关mrna,以及该mrna的表达产物。本发明的目的还在于提供深静脉血栓相关mrna或其表达产物在用于制备深静脉血栓诊断产品中的应用。为实现上述目的,本发明首先提供tmem63c或其表达产物在用于制备深静脉血栓诊断产品中的应用。优选地,所述tmem63c包含如seqidno:1所示的特异核苷酸序列。优选地,所述tmem63c或该mrna的表达产物在深静脉血栓组织中表达上调。优选地,所述诊断产品包括检测试剂或试剂盒。进一步地,本发明提供一种诊断深静脉血栓的生物试剂,所述检测试剂包括tmem63c的特异性引物对或抗tmem63c蛋白的特异性抗体。优选地,所述tmem63c的特异性引物对具有seqidno:2和seqidno:3所示的核苷酸序列;所述引物对通过转录介导扩增技术来检测人体血白细胞内tmem63c基因的表达水平,以判断深静脉血栓发生的风险。优选地,所述所述抗tmem63c蛋白的特异性抗体为anti-tmem63cantibody。进一步地,本发明提供了一种用于检测深静脉血栓的诊断试剂盒,所述试剂盒包括特异性扩增深静脉血栓相关mrna的引物和说明书,所述深静脉血栓相关mrna是tmem63c。优选地,所述引物具有seqidno:2和seqidno:3所示的核苷酸序列。所述说明书中记载所用试剂的用量和方法,以及判断检测样本患深静脉血栓风险的标准。优选地,所述试剂盒还包括10×buffer、dntp、mgcl2、taq酶、逆转录酶和rna酶抑制剂。本发明的有益效果如下:本发明公开了一种与深静脉血栓相关的tmem63c,并进一步证实该tmem63c或该mrna的表达产物在深静脉血栓患者血白细胞中表达上调。利用tmem63c基因及含有tmem63c基因或表达产物的诊断试剂或试剂盒不仅能够快速有效的做到早期诊断,而且为深静脉血栓发病风险预测、新药开发、诊断和个体化治疗等临床应用提供了治疗靶点和重要依据。附图说明图1tmem63c基因cdna在各组中的表达;其中b/a=血栓形成组/正常对照组;c/a=无血栓形成组/正常对照组;a表示与其他两组相比p<0.05;图2wb分析各组中tmem63c蛋白表达情况;其中b/a=血栓形成组/正常对照组;c/a=无血栓形成组/正常对照组;a表示与其他两组相比p<0.01。具体实施方式以下实施例用于说明本发明,但不用来限制本发明的范围。若未特别指明,实施例中所用的技术手段为本领域技术人员所熟知的常规手段,所用的试剂可以商业购买得到。实施例中未注明具体条件的实验方法,通常为本领域常规方法,如按照常规条件如sambrook等人,分子克隆,实验手册(第三版)(科学出版社,2002)中的所述条件,或按照试剂制造厂家所建议的条件。本发明的发明人对深静脉血栓患者血白细胞、无血栓进行组血白细胞以及正常对照组血白细胞中的mrna进行高通量转录组测序,通过生物信息学方法进行基因筛选,挑选出候选mrnatmem63c,现有研究中并没有tmem63c和深静脉血栓相关的报道,进一步,发明人进行了分子生物学方法验证,证实了tmem63c在深静脉血栓患者血白细胞中表达上调。本发明的tmem63c是在本发明之前的已知mrna,其基本信息如下:genbank登录号:tmem63cgeneid:57156,ncbi参考序列:nm_020431.3,来源于人类基因组。本发明还采用rt-pcr方法和western-blot方法检测上述mrna在深静脉血栓患者、无血栓进行组和正常对照组血白细胞中的表达,并验证了该mrna在深静脉血栓中表达上调。本文使用的术语“表达上调”指对应于所表达基因的序列,其中序列量的测量证明,与从正常个体或从通过深静脉血栓确认或无深静脉血栓进行的个体中分离的生物学样品中的同一基因相比,所述基因在从患深静脉血栓个体中分离的生物学样品中的表达水平增加。根据本发明,“表达上调”是指通过本发明方法杂交强度测量的至少1%、2%、3%、4%、5%、6%、7%、8%、9%、10%或更高的表达增加,例如20%、30%、40%、50%、60%、70%、80%、90%或更高或者高于1倍,最高为2倍、3倍、4倍、5倍、10倍、50倍、100倍或更高。实施例1高通量测序筛选差异表达基因1、研究对象与分组选取下肢静脉曲张患者65例为深静脉血栓观察对象,其中15例患者术前发生股静脉血栓者纳入血栓形成组,行抗凝加溶栓规范治疗,待血栓消退,深静脉血流通畅,能保证肢体静脉回流后,再行浅静脉抽剥术,50例术前未发现深静脉血栓者均行浅静脉抽剥术,术后5例发生深静脉血栓,亦纳入血栓形成组,故血栓形成组共纳入20例患者。45例未发生深静脉血栓者,随机选取20例纳入无血栓形成组。另选20名健康志愿者作为正常对照组。深静脉血栓观察、诊断考虑以下几个方面及要点:由一组高年资医生实施,系统掌握深静脉血栓相关理论;能够准确动态观察症状变化及进行正确的体格检查;掌握相关手术技术,能保证手术质量;结合相应情况及时行超声检查,筛查有无血栓形成;必要时再行静脉造影确诊,确保所采集到的血液样本与相应状态尽可能相符。研究对象均为吉林大学中日联谊医院血管外科在2016年10月到2017年12月期间招募,所有程序均按照当地医院伦理审查委员会批准的方案进行,并从所有参与者获得知情同意书。2、血液样本采集、保存和总rna的提取确保所采集血液样本与相应状态尽可能相符,按不同组别采血,每例研究对象在相应状态,每次从肘静脉采集静脉血10ml(真空枸橼酸钠抗凝抽血管),立即颠倒混匀20次以便充分混匀,避免血液部分凝固、血栓形成。采用血液样本保存试剂盒(paxgenebloodrnatube,brt,美国qiagen公司)保存样本,并与30min内将血样倒入brt管内,立刻盖上盖颠倒20次充分混匀血样。然后,将brt管置室温静置2h以上(不超过24h),使血样与brt管中试剂充分反应,达到最佳rna提取效率。采用血白细胞中总rna提取试剂盒(paxgenebloodrnakit,美国qiagen公司)提取血白细胞中总rna约45μl,具体操作按说明书进行。从每份rna样本中取5μl按1:200稀释,检测吸光度260/280(a260/a280)比值均在1.8~2.0。3、高通量测序测序平台为illumina公司的hiseq2500高通量测序平台,进行高通量转录组深度测序,测序后我们运用fast-qc(http://www.bioinformatics.babraham.ac.uk/projects/fastqc/)软件对测序数据的质量进行整体评估,包括碱基的质量值分布,质量值的位置分布,gc含量,pcrduplication含量,kmer的frequency等。对血栓形成组、无血栓形成组和正常对照组血液样本分别进行差异基因表达分析,根据得到的fpkm值,采用国际公认算法ebseq进行差异筛选。其中,筛选时,log2fc>1或<-1,fdr<0.05。为了更好的理解差异表达基因的功能,我们对差异表达基因进行了geneontology和信号通路分析,并对差异表达基因进行功能注释,鉴于以上数据分析的结果,结合文献我们筛选了差异表达基因tmem63c,tmem63c在血栓形成组和无血栓形成组间以及血栓形成组与正常对照组间存在明显差异,而在无血栓形成组和正常对照组间差异无统计学意义,并且tmem63c在血栓形成组中的表达明显高于无血栓形成组和正常对照组,因此我们得出结论tmem63c在深静脉血栓患者血白细胞中表达上调。实施例2rt-pcr验证tmem63c在深静脉血栓患者中的表达情况1、研究对象与分组选取下肢静脉曲张患者55例为深静脉血栓观察对象,其中10例患者术前发生股静脉血栓者纳入血栓形成组,行抗凝加溶栓规范治疗,待血栓消退,深静脉血流通畅,能保证肢体静脉回流后,再行浅静脉抽剥术,45例术前未发现深静脉血栓者均行浅静脉抽剥术,术后5例发生深静脉血栓,亦纳入血栓形成组,故血栓形成组共纳入15例患者。40例未发生深静脉血栓者,随机选取15例纳入无血栓形成组。另选15名健康志愿者作为正常对照组。深静脉血栓观察、诊断考虑以下几个方面及要点:由一组高年资医生实施,系统掌握深静脉血栓相关理论;能够准确动态观察症状变化及进行正确的体格检查;掌握相关手术技术,能保证手术质量;结合相应情况及时行超声检查,筛查有无血栓形成;必要时再行静脉造影确诊,确保所采集到的血液样本与相应状态尽可能相符。研究对象均为吉林大学中日联谊医院血管外科在2016年10月到2017年12月期间招募,所有程序均按照当地医院伦理审查委员会批准的方案进行,并从所有参与者获得知情同意书。2、方法2.1对血液样本进行采集、保存和总rna提取,同实施例1的方法。2.2逆转录合成cdna采用iiireversetranscriptase(invitrogen,货号18080-044)进行cdna反转录,实验操作按产品说明书进行,具体操作如下:使用逆转录试剂盒,用逆转录缓冲液对lμg总rna进行逆反录合成cdna。采用25μl反应体系,每个样品取1μg总rna作为模板rna。获得的cdna保存放-20℃冰箱备用。2.3real-timepcr2.3.1仪器及分析方法用abi7500型荧光定量pcr仪,采用2-δδct法进行数据相对定量分析。2.3.2引物设计采用在线引物引物设计,基因序列参照ncbi:nm_020431.3(tmem63c),内参选gapdh,引物设计后由invitrogen公司合成。具体引物序列如下:表1引物序列(2)反应体系:用powergreenpcrmastermix(invitrogen,货号4367659)进行扩增,实验操作按产品说明书进行。扩增程序为:95℃5min,(95℃15sec,59℃45sec,72℃35sec)×40个循环。表2realtime反应体系组分加入量2×mix10μl上游引物(10μm)0.5μl下游引物(10μm)0.5μl模板2μl加入灭菌蒸馏水至25μl(4)样本realtime-pcr检测以sybrgreen作为荧光标记物,在abi7500型荧光定量pcr仪上进行pcr反应,通过融解曲线分析和电泳确定目的条带,采用2-△△ct法进行数据的相对定量分析。(5)统计学方法重复检测3次,用spss11.5统计学软件进行分析,组间比较采用单因素方差分析(q检验)。p<0.05为差异有统计学意义。(6)实验结果实时定量pcr扩增曲线拐点清楚,扩增曲线整体平行性好,表明各反应管的扩增效率相近,极限平而无上扬现在,曲线指数期斜率较大,说明扩增效率较高;样本扩增产物溶解曲线都是单峰,说明扩增产物只有一条,为特异性扩增;rt-pcr产物琼脂糖电泳后切胶回收,在abi3730全自动测序仪上测序,该328bp片段的核苷酸序列如seqidno.1所示。用vectorntiadvance10软件(invitrogen公司)将该序列与tmem63c整个mrna序列进行比对,比对结果显示,如seqidno.1所示的核苷酸序列为tmem63c基因的一部分序列,符合率为100%。根据qrt-pcr的相对定量公式:2-δδct×100%,比较tmem63c在血栓形成组、无血栓形成组及正常对照者中的表达水平。结果显示:qrt-pcr扩增结果稳定,其中tmem63c在血栓形成组中的表达水平明显高于tmem63c在血栓形成组中的表达明显高于无血栓形成组和正常对照组(p<0.05),而在无血栓形成组和正常对照组间差异无统计学意义(p>0.05),如图1所示。以上结果验证了高通量转录组表达数据的整合分析tmem63c在深静脉血栓患者血白细胞中表达上调的结果。实施例3wb检测深静脉血栓患者血白细胞中tmem63c的蛋白表达水平1、研究对象与分组同实施例22、各组样本白细胞的分离与培养(1)肘静脉取血5ml,肝素抗凝,1500r/min离心5min,取白细胞层。(2)加入1/3体积的3%明胶生理盐水溶液混匀,4℃静置20min。细胞成分分层,将上层混悬液移入另一试管中。直角离心机1750r/min离心10min。弃上清液,于底层细胞中加入蒸馏水3ml,充分振荡30s,加入等体积1.8%nacl3ml以除去混杂的红细胞。(3)1700r/min离心10min,弃上清液,底层细胞用pbs洗涤,1750r/min离心10min,弃上清液,加pbs配成1×106/ml细胞浓度备用。(4)细胞均置于含有10%胎牛血清(fbs)、100u/ml青霉素及100μg/ml链霉素、5%小牛血清的dmem培养基中于37℃、5%co2培养箱中传代培养。3、细胞总蛋白提取(1)将细胞从co2培养箱中取出,置于相差显微镜下观察,选择生长良好且铺满整个培养瓶瓶底的细胞用于蛋白质提取。提前准备预冷离心机至4℃。(2)准备冰盒备用,倒掉培养瓶中的旧培养基,用pbs洗涤培养瓶中残余培养基三次,倒置于滤纸上,尽量吸干水分后,迅速用细胞刮板将细胞刮下,加入1-2mlpbs2-3次,充分洗涤并收集pbs洗涤液置于离心管中并放入冰盒中。(3)将收集好的细胞1500rmp低温离心5min,弃上清。(4)每1x107个细胞加ripa裂解液(beyotime)1ml,置于冰上,并在在超声细胞破碎仪中超声3-5min。(5)放置10min后4℃下12000g离心10min,取上清,置于冰盒中备用。4、利用bca蛋白浓度测定试剂盒进行总蛋白定量采用康为世纪微量bca蛋白定量试剂盒(货号:cw2011),具体步骤见其说明书。5、sds-聚丙烯酰胺凝胶电泳(sds-page)(1)蛋白质样品变性:a)根据bca蛋白质浓度测定结果,每个凝胶加样孔中加入相同质量的总蛋白提取物。按照每1微升蛋白样品加入0.25微升蛋白上样缓冲液的比例,混合蛋白样品和蛋白上样缓冲液(5x)。b)100℃或沸水浴加热3-5分钟,以充分变性蛋白。c)冷却到室温后,直接上样到sds-page胶加样孔内即可。(2)胶板制备:采用bio-rad公司的微型垂直板电泳装置制备0.75mm厚的凝胶,照说明书安装好玻璃板后,先在小烧杯中配制5ml10%的分离胶,配方如下:表3分离胶配方组分用量30%丙烯酰胺溶液1.7mltris-hcl(1.5m,ph8.8)1.3ml10%sds0.05ml10%ap0.05mltemed0.002ml灭菌ddh2o补充至5ml混匀后立即灌胶,然后加lml蒸馏水覆盖,室温下放置约30min待胶聚合后,用蒸馏水洗2-3次,再用滤纸吸干。然后制备2ml5%的浓缩胶,配方如下:表4浓缩胶配方组分用量30%丙烯酰胺溶液0.33mltris-hcl(1.0m,ph6.8)0.25ml10%sds0.02ml10%ap0.02mltemed0.002ml灭菌ddh2o补充至2ml混匀后立即灌胶,插入样品梳,避免产生气泡,待胶凝固后,取出样品梳,后用蒸馏水和1x蛋白电泳缓冲液先后冲洗样品孔。6、上样及电泳将凝胶板装在电泳装置上,内槽中加满lx蛋白电泳缓冲液,外槽中lx蛋白电泳缓冲液应超过铂丝,按顺序上样。在末端泳道中加入蛋白质质量标准蛋白梯度。电泳时蓝色染料到达胶的底端处附近即可停止电泳。7、蛋白质印迹1、按照上述方法先进行sds-page凝胶电泳分离蛋白。2、预先用转印缓冲液浸泡nc膜、滤纸、海棉垫。sds-page结束后取出凝胶,去除浓缩胶,在tris/甘氨酸缓冲液中漂洗数秒,然后置于转印缓冲液中浸泡15-30min。打开电转印夹,每侧垫上一块专用的用转印缓冲液浸泡透的海棉垫,再各放一块转印液浸透的滤纸,滤纸与海棉垫大小相同或与nc膜,凝胶大小相同均可,将凝胶平放在阴极侧滤纸上,最后将nc膜平放在凝胶上,去除气泡,夹好电转印夹。在电泳槽加满电转印液,插入电转印夹,将电泳槽放入冰箱内(电转印液之前要放入冰箱内预冷),连接好电极,接通电流,转印夹的nc膜应对电泳槽的正极。3、封闭:用1xtbs漂洗一次。加入含5%的无脂奶粉tbs封闭缓冲液,置于振荡培养箱中进行封闭;4、一抗杂交:弃封闭液,加入用一抗稀释液稀释的一抗(anti-tmem63cantibody(ab90266))杂交溶液,置于4℃杂交过夜,第二天在振荡培养箱中进行杂交;5、回收一抗杂交液,用tbst洗膜3次;6、弃tbst,加入用封闭缓冲液稀释的二抗(goatanti-rabbitigg,hrpconjugated(cw0103))杂交溶液,置于振荡培养箱中进行杂交;7、弃二抗溶液,用tbst洗膜3次;8、ecl化学发光及图像采集和分析:按照高灵敏度化学发光检测试剂盒(康为世纪货号cw0049b),具体步骤参照说明书。9、以β-actin作为内参进行数据标准化,以正常对照组血白细胞中tmem63c作为参照样本,计算血栓形成组和无血栓形成组血白细胞中tmem63c蛋白的相对表达水平。五、实验结果血栓形成组与正常对照组相比,tmem63c蛋白表达明显升高(p<0.01),无血栓形成组与正常对照组相比,tmem63c蛋白表达无显著差异,具体参见图2所示。实施例4深静脉血栓诊断试剂盒基于实施例2得到的引物组,组装本发明所述的用于深静脉血栓诊断的试剂盒,所述试剂盒包括特异扩增如seqidno.1所示的核苷酸序列的引物对如seqidno:2和seqidno:3所示,和特异扩增内参基因(gapdh)的引物对如seqidno:4和seqidno:5所示;还包括sybrgreen聚合酶链式反应体系,如pcr缓冲液、sybrgreen荧光染料、dntps。所述pcr缓冲液的成分为25mmkcl,2.5mmmgcl2,200mm(nh4)2so4。通过对引物浓度和退火温度的优化,最终确定反应体系如表5所示:表5pcr反应体系组分加入量sybrgreen聚合酶链式反应体系12.5μl上游引物(10μm)0.5μl(sprr1a)+0.5μl(gapdh)下游引物(10μm)0.5μl(sprr1a)+0.5μl(gapdh)模板cdna2.0μl加入灭菌蒸馏水至25μl最佳反应条件为:95℃预变性5min,(95℃变性15sec,59℃退火45sec,72℃延伸35sec)×40个循环,72℃延伸15min。为方便使用,该试剂盒还可包含对照:正常人血液白细胞cdna。取受检者血液样本,使用常规方法(或使用特定的试剂盒)从血液样本的白细胞中提取rna,使用试剂盒中试剂,按照最佳反应体系与条件进行pcr反应,使用试剂盒中正常血液白细胞cdna作为real-timepcr定量检测中的对照cdna,检测受试者血白细胞中如seqidno.1所示的核苷酸序列相对血白细胞中表达量变化。虽然,上文中已经用一般性说明及具体实施方案对本发明作了详尽的描述,但在本发明基础上,可以对之作一些修改或改进,这对本领域技术人员而言是显而易见的。因此,在不偏离本发明精神的基础上所做的这些修改或改进,均属于本发明要求保护的范围。序列表<110>吉林大学<120>tmem63c在制备深静脉血栓诊断产品中的应用<130>p18030<160>5<170>patentinversion3.5<210>1<211>328<212>dna<213>人工序列<400>1gggatcctcccaggatgtctgcctcaccagacgacctgagtacagggggaaggttacaga60acatgacagtggatgaatgcttccagtctcggaacaccgtcctccaggggcagccctttg120ggggtgtccccaccgtgctgtgcctcaacatcgccctgtgggtgctcgtccttgtggttt180actccttcctccggaaagctgcgtgggactatgggcgcctggctctgctgatacacaatg240acagcctgacctcgctgatctatggggagcagagcgagaagacatctccctcggagactt300ccttggagatggaacgcagagacaaggg328<210>2<211>20<212>dna<213>人工序列<400>2gggatcctcccaggatgtct20<210>31<211>20<212>dna<213>人工序列<400>3cccttgtctctgcgttccat20<210>4<211>21<212>dna<213>人工序列<400>4ggagcgagatccctccaaaat21<210>5<211>23<212>dna<213>人工序列<400>5ggctgttgtcatacttctcatgg232当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1