一种用于预测慢性乙肝炎症损伤的miRNA组合物的制作方法
本发明涉及一种用于预测慢性乙肝炎症损伤的mirna组合物,属于医学检验技术领域。
背景技术
微小rna(microrna)是一类内源性非编码单链小分子rna,长度为18~24个核苷酸。近年对微小rna生物功能的研究越来越多,发现其在机体生理及病理方面起重要作用,生理情况下参与细胞的增殖、分化过程,若表达及功能失调则可能导致包括白血病在内的肿瘤的发生,以及病毒、细菌感染等多种病理现象。
微小rna普遍存在于人类的体液中,性质稳定,可以定量检测,且存在显著的疾病特异性。近年的研究表明,血液、唾液、尿液、乳汁及脑脊液等体液mirna检测可应用于妊娠等生理状态的判断以及口腔癌、膀胱癌及阿尔海默茨病等疾病的诊断和预后判断。体液特异性mirna检测的临床意义及应用前景已引起高度关注,mirna作为一类非编码调节性的小分子rna有可能取代传统的特异蛋白为代表的生物标志物。体液mirna含量丰富且性质稳定,具备成为优异生物标志物的潜质,并且拥有以蛋白质为代表的传统生物标志物不具备的特性,无需抗体制备且易于精确定量,可能克服抗原抗体类生物标志物的制备瓶颈。
肝脏是人体内重要的器官之一,肝脏疾病尤其是病毒性肝炎、肝细胞癌、酒精性肝炎等病情重,治疗棘手,严重困扰着人类的健康,研究肝脏疾病的发病机制对其治疗至关重要。不断有研究发现,微小rna与多种肝脏疾病相关,肝脏中的微小rna表达异常或缺失可导致肝细胞凋亡、再生,甚至感染等,微小rna参与众多肝脏疾病的病理发病过程。在众多肝脏疾病中,肝细胞癌和微小rna的相互关系研究最多。近年研究发现,微小rna失调和癌症发生发展密切相关,微小rna参与癌症的病理发病过程。肝细胞癌的发生同样受微小rna的调控,已发现在肝细胞癌中表达上调的微小rna有mir-2l、mir-34a、mir-22l/222和mir-224等,而表达下调的有mir-122、mir-145和mir-199a等。
alt是肝功能损害最敏感的检测指标,也是各种指南关于慢性乙肝抗病毒治疗和预后判断的重要指标,但很多alt正常的慢性hbv感染者肝组织学均提示有严重的炎症反应损伤,一部分患者甚至出现肝硬化表现。因此2010年我国慢性乙肝防治指南明确建议对>40岁或有hcc家族史的男性,即使alt正常建议肝组织学检查,以明确肝组织的损伤,以免耽误抗病毒治疗。肝组织学检查虽然是确切了解肝组织损伤的金标准,但其有创性和局限性,不能被大多患者接受。因此,寻找到新的诊断方法和更敏感的生物学标志是慢性乙肝迫切要解决的问题。
技术实现要素:
本发明的目的是解决上述不足,提供一种用于预测慢性乙肝的mirna组合物。
技术方案
一种用于预测慢性乙肝炎症损伤的mirna组合物,所述组合物包括hsa-mir-1285-5p、hsa-mir-193a-5p和hsamir-26a-5p。
进一步,所述hsa-mir-1285-5p的核苷酸序列如seqidno.1所示。
seqidno.1:gaucucacuuuguugcccagg。
进一步,所述hsa-mir-193a-5p的核苷酸序列如seqidno.2所示。
seqidno.2:ugggucuuugcgggcgagauga。
进一步,所述hsamir-26a-5p的核苷酸序列如seqidno.3所示。
seqidno.3:uucaaguaauccaggauaggcu。
用于检测上述mirna组合物的引物组,包括针对hsa-mir-1285-5p的特异性引物,针对hsa-mir-193a-5p的特异性引物以及针对hsamir-26a-5p的特异性引物;所述针对hsa-mir-1285-5p的特异性引物包括seqidno.4所示的正向引物和seqidno.5所示的反向引物,所述针对hsa-mir-193a-5p的特异性引物包括seqidno.6所示的正向引物和seqidno.7所示的反向引物,所述针对hsamir-26a-5p的特异性引物包括seqidno.8所示的正向引物和seqidno.9所示的反向引物。
上述用于检测mirna组合物的引物组在预测或诊断慢性乙肝炎症损伤方面的应用。采用该引物组,通过qrt-pcr对上述mirna组合物进行检测,可以实现对慢性乙肝炎症损伤的早期诊断,为慢性乙肝炎症损伤的早期发现和诊断提供参考。
一种慢性乙肝炎症损伤的诊断试剂盒,包括上述用于检测mirna组合物的引物组。
进一步,所述mirna组合物的筛选方法包括如下步骤:
(1)样品采集:采集患者新鲜血液,2h内分离,收集血清,并将血清转移至一次性使用无rna酶的无菌微量离心管中,-80℃保存,备用;
(2)总rna提取:采用lcstrk1001试剂盒(lcsciences)操作说明书进行;
(3)文库构建:使用illuminatruseqsmallrnapreparationkit试剂盒参照试剂盒说明书illumina’struseqsmallrnasamplepreparationguide构建小rna文库,总rna链接5'接头和3'接头后经rt-pcr扩增形成小分子rna的cdna文库,经过6%tbe变性胶电泳分离,将长度范围在147bp的小分子rna切胶回收;
(4)第二代测序:cdna经纯化后在illumina’sclusterstation上生成dna簇后上机(illuminagaiix)进行测序,通过illumina’ssequencingcontrolstudiosoftwareversion2.8(scsv2.8)软件实时分析测序图片并使用illumina'sreal-timeanalysisversion1.8.70(rtav1.8.70)提取base-calling,提取的原始序列利用acgt101-mirv4.2(lcsciences)软件分析,生成rawdata数据库,同时去除由于样品制备、测序化学与处理以及测序仪器的光学数码处理而产生的非纯序列,剩下的序列(长度在15和32bases)按照families进行分组,生成mappablereads。mappable序列与最新版本的mirbase数据库以及测序物种基因组进行序列比对,鉴定该物种已知的mirna;同时发现新的5p或者3pmirna序列,鉴定在其它近源物种中已有报道,在该物种中崭新的mirna序列。其中mappable序列能与rfam(ierrna,trna,snrna,snornaandothers),repbase以及mrna序列比对上的均被去除。除此之外,为了保证筛选到高质量的基因结果,把reads数小于10的基因剔除掉。最后分析实验组和对照组之间差异表达的mirnas,最终获得hsa-mir-1285-5p、hsa-mir-193a-5p和hsamir-26a-5p。
本发明的有益效果是:
本发明提供了一种用于预测慢性乙肝炎症损伤的mirna组合物,通过qrt-pcr对该mirna组合物进行定量检测,实现对慢性乙肝肝纤维化的早期诊断和预测,mirna作为生物学标志物是一种非侵入性取样,可以在无创条件下通过单独的mirna或mirna组合物的表达谱来辅助诊断被试者是否有慢性乙肝炎症损伤,提高了病情判断的准确率。
附图说明
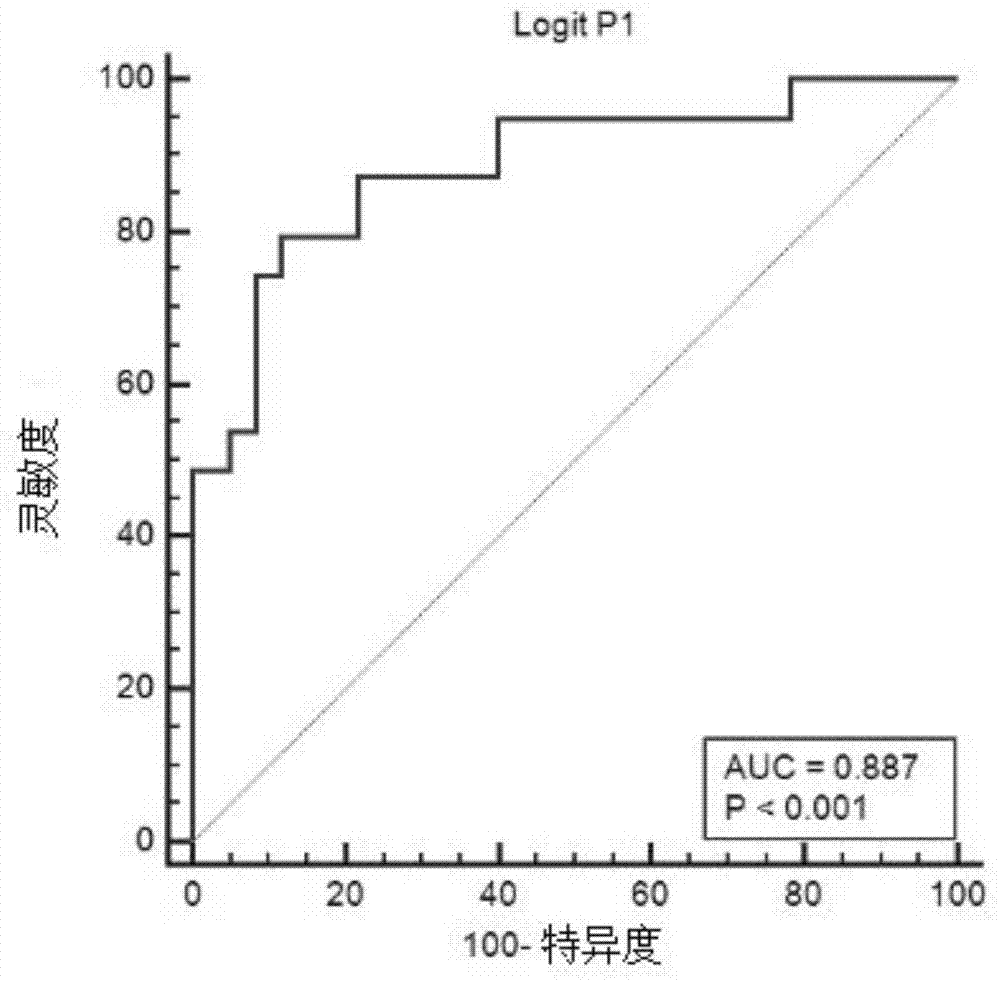
图1为本发明的mirna组合物在验证集炎症坏死组的roc曲线。
具体实施方式
下面结合具体实施例对本发明作进一步说明。
实施例1慢性乙肝炎症损伤相关mirna的筛选
采用四步筛选法:
(1)发现阶段,我们采用新一代深度测序技术(illuminahiseq2000),对发现集混合样本进行检测,发现表达差异的mirna,轻、中度以上炎症坏死分别选择6例;
(2)筛选阶段,使用qrt-pcr的方法,选定内参mirna,建立均一的少量队列筛选集,2-△△ct测定循环数(ct),淘汰mirnactvalue<35和detectionrate>75%;p<0.05的mirna,轻、中度以上炎症坏死分别选择20例;
(3)训练阶段,训练筛选阶段选出的目的mirna,使用qrt-pcr对大样本训练集(轻、中度以上炎症坏死分别选择136例,201例)检验目的mirna,并使用logiticp建立mirna模型。
(4)验证阶段,利用训练集建立的mirna模型,对独立建立的队列验证集(轻、中度以上炎症坏死分别选择75例,125例)进行验证,评价其诊断价值。
具体如下:
病例选择:病例来自于镇江市第三人民医院2008年8月至2013年12月所有的慢性乙肝感染者进行肝穿刺病理检查的患者。病例入选标准:(1)hbsag阳性至少6月;(2)hbvdna>1000拷贝/毫升。排除标准如下:(1)合并其他病毒性肝炎和病毒性疾病,如hav,hcv,hev,hiv;(2)药物性肝损以及有规律嗜酒史;(3)标本不符合要求;(4)有使用抗乙肝病毒药物史或者肝穿刺前已开始抗病毒治疗;(5)肝穿刺前12月内有保肝药使用。共入选1210例进行过肝穿刺慢性乙肝病例,排除621例(合并其他病毒性肝炎,n=83;药物性肝损或者有规律嗜酒史,n=169;样本不符合要求,n=35;有使用抗病毒药物史,n=156;随访期间有保肝药使用,n=178)。共589例入选病例,pnalt共129例,其中hbeag阳性48例,hbeag阴性81例;pialt(alt1-2uln,n=186),其中hbeag阳性87例,hbeag阴性99例;pialt(alt≥2uln,n=274),其中hbeag阳性86例,hbeag阴性,168例。
1.样品采集
患者在首次门诊或住院时采集新鲜血液5ml于医用血清管中(无肝素抗凝),上下轻轻颠倒混匀,立即将全血置于4℃冰盒中保存,并在2h内4000g,离心10min。将上层血清转移至1.5ml离心管(rnasefree)中,13000g,离心2min。最后将上清液转移至2ml旋盖尖底离心管中(rnasefree),每个管子吸入250ul血清进行分装,弃去血细胞沉淀。置于-80℃长期保存。
2.总rna提取及质检
血清rna的抽提采用lcstrk1001试剂盒(lcsciences)操作说明书进行。随机抽取两个在血清中稳定表达的mirna作为标准检测总rna提取质量,分别为hsa-mir-16、hsa-mir-192。然后各取2μl,以上述引物对应的逆转录引物分别逆转录(反应体系为10μl);以1μl/孔的cdna为模板,进行realtimepcr,反应体系为20μl,复孔为三个,同时做引物ntc(模板以水代替)。然后检测hsa-mir-16和hsa-mir-192pcr扩展曲线、溶解曲线以及ct值。
3.文库构建
使用illuminatruseqsmallrnapreparationkit试剂盒参照试剂盒说明书illumina’struseqsmallrnasamplepreparationguide构建小rna文库。总rna链接5’接头和3’接头后经rt-pcr扩增形成小分子rna的cdna文库,经过6%tbe变性胶电泳分离,将长度范围在147bp的小分子rna切胶回收。
4.第二代测序
cdna经纯化后在illumina’sclusterstation上生成dna簇后上机(illuminagaiix)进行测序。通过illumina’ssequencingcontrolstudiosoftwareversion2.8(scsv2.8)软件实时分析测序图片并使用illumina'sreal-timeanalysisversion1.8.70(rtav1.8.70)提取base-calling。提取的原始序列利用acgt101-mirv4.2(lcsciences)软件分析,生成rawdata数据库,同时去除由于样品制备、测序化学与处理以及测序仪器的光学数码处理而产生的非纯序列。剩下的序列(长度在15和32bases)按照families进行分组,生成mappablereads。mappable序列与最新版本的mirbase数据库以及测序物种基因组进行序列比对,鉴定该物种已知的mirna;同时发现新的5p或者3pmirna序列,鉴定在其它近源物种中已有报道,在该物种中崭新的mirna序列。其中mappable序列能与rfam(ierrna,trna,snrna,snornaandothers),repbase以及mrna序列比对上的均被去除。除此之外,为了保证筛选到高质量的基因结果,我们把reads数小于10的基因剔除掉。最后分析实验组和对照组之间差异表达的mirnas。
通过上述测序分析,轻度炎症坏死和中度以上炎症坏死组经过初级分析后得到8,580,434和7,485,507条原始序列,经过去除冗余后剩余659,447和441,182条可比对序列。对三数据归一化后比较,在炎症坏死不同损伤,血清mirna在mpchb和spchb两者的表达差异。p<0.05表示有统计学差异。共发现143条有差异显著性的mirnas,其中表达上调的有105条,表达下调的有38条。符合表达差异倍数2倍以上,p<0.05的14个mirna为上调基因,3个下调mirna表达基因,见表1:
表1慢性乙肝炎症损伤轻中度分组的mirna的差异表达
5、表达差异的mirna进一步筛选:对上述表达差异的17个差异mirna进一步筛选,筛选条件为:ct值〈35,检测率〉75%,共筛选出5个候选mirna,分别为:hsa-mir-1285-5p,hsa-mir-122-5p,hsa-mir-193a-5p,hsa-mir-433-3p,和hsamir-26a-5p。见表2:
表2慢性乙肝轻中度炎症损伤在训练集mirna的差异表达
6、训练集rt-pcr进一步筛选目的mirna
对上阶段筛选出的5个候选mirna使用新的训练集进行qrt-pcr检验,发现炎症坏死组比较有3个差异表达mirna,分别为:hsa-mir-1285-5p,hsa-mir-193a-5p,和hsamir-26a-5p。logistic回归分析建立联合预测因子,经过逐步logistic回归建立logitp。炎症坏死组,有3个mirna进入方程,logitp1=-4.0262-0.28851*mir_1285-0.50803*mir_193+0.85701*mir_26a,见表3:
表3训练集慢性乙肝轻中度炎症损伤的logistic回归分析
验证集验证mirna组合:
本发明的mirna组合物在验证集炎症坏死组的roc曲线见图1,可以看出,acu为0.887(95%ci=0.775–0.878,灵敏度=70.8%,特异度=83.4%),说明mirna组合物可以作为预测慢性乙肝炎症损伤的生物标志物。
序列表
<110>镇江市第三人民医院
<120>一种用于预测慢性乙肝炎症损伤的mirna组合物
<160>9
<170>siposequencelisting1.0
<210>1
<211>21
<212>rna
<213>mirna组合物(hsa-mir-1285-5p)
<400>1
gaucucacuuuguugcccagg21
<210>2
<211>22
<212>rna
<213>mirna组合物(hsa-mir-193a-5p)
<400>2
ugggucuuugcgggcgagauga22
<210>3
<211>22
<212>rna
<213>mirna组合物(hsamir-26a-5p)
<400>3
uucaaguaauccaggauaggcu22
<210>5
<211>21
<212>dna
<213>mirna组合物(hsa-mir-1285-5p)
<400>5
tcgctggatctcactttgttg21
<210>6
<211>20
<212>dna
<213>mirna组合物(hsa-mir-1285-5p)
<400>6
cagtgcagggtccgaggtat20
<210>7
<211>22
<212>dna
<213>mirna组合物(hsa-mir-193a-5p)
<400>7
ggtacccggggttttgagggcg22
<210>7
<211>20
<212>dna
<213>mirna组合物(hsa-mir-193a-5p)
<400>7
cagtgcagggtccgaggtat20
<210>8
<211>22
<212>dna
<213>mirna组合物(hsamir-26a-5p)
<400>8
gccgccttcaagtaatccagga22
<210>9
<211>20
<212>dna
<213>mirna组合物(hsamir-26a-5p)
<400>9
cagtgcagggtccgaggtat20
- 还没有人留言评论。精彩留言会获得点赞!