氯代三蝶烯四甲酸二酐化合物及其制备方法和聚酰亚胺及其制备方法与流程
本发明涉及功能高分子材料领域,特别涉及氯代三蝶烯四甲酸二酐化合物及其制备方法和聚酰亚胺及其制备方法。
背景技术:
:聚酰亚胺是一种性能优异的高性能聚合物,由于其突出的综合性能而被广泛应用到航空航天、高性能纤维、介电材料、膜分离和液晶显示器等领域。但由于二酐单体合成成本高昂以及聚合物不易加工、有颜色等缺点严重限制了它更广泛的发展应用。目前,现有的商品化最广泛的聚酰亚胺薄膜(商品名kapton@)采用二胺单体4,4’-二氨基二苯醚(oda)聚合得到,二胺单体的数量已有上千种,合成技术工艺比较成熟,而采用二酐单体合成聚酰亚胺的种类很少且二酐单体的设计合成相比之于二胺要困难复杂得多。如何改进聚酰亚胺在应用中存在的不足,克服二酐合成中的困难,得到高性能的聚酰亚胺,是本领域技术人员长期研究的课题。技术实现要素:为解决上述
背景技术:
中提到的问题,本发明提供如下方案:本发明提供一种氯代三蝶烯四甲酸二酐化合物,分子结构式如下式所示:进一步地,其合成路线如下式所示:式中,化合物1为14-氯-2,3,6,7-四甲基三蝶烯,化合物2为14-氯-2,3,6,7-三蝶烯四甲酸,化合物3为14-氯-2,3,6,7-三蝶烯四甲酸二酐。进一步地,包括以下合成步骤:步骤1、合成氯代四甲基三蝶烯将氯代邻氨基苯甲酸和亚硝酸异戊酯分别溶于二乙二醇二甲醚和1,2-二氯乙烷中,分别加入溶有2,3,6,7-四甲基蒽的1,2-二氯乙烷中;反应后,蒸出溶剂,加入顺丁烯二酸酐,加热回流发生diels-alder反应后,冷却后加入naoh-乙醇水溶液,加热回流,静置,抽滤,取固体,烘干,过柱纯化,旋蒸,得到白色粉末状固体,烘干,得氯代四甲基三蝶烯;步骤2、合成氯代三蝶烯四甲酸取步骤1所制备的氯代四甲基三蝶烯溶于吡啶与水的混合溶剂中并在高锰酸钾作用下加热搅拌回流;反应后,取滤液蒸馏出溶剂,用活性炭脱色,调节ph值小于1,取过滤后所得的固体进行干燥,得氯代三蝶烯四甲酸;步骤3、合成氯代三蝶烯四甲酸二酐取步骤2所制备的氯代三蝶烯四甲酸溶于乙酸,加热抽滤,滤液加入乙酸酐,并于反应釜中进行反应,待析出白色晶体,进行抽滤,真空干燥后,即得氯代三蝶烯四甲酸二酐。优选地,步骤1中,所述2,3,6,7-四甲基蒽、氯代邻氨基苯甲酸和亚硝酸异戊酯的摩尔比为2:1~2.5:7~9。优选地,步骤1中,进行过柱纯化时,固定相用100~200目的中性氧化铝,淋洗剂为二氯甲烷与石油醚,二氯甲烷与石油醚的体积比为5:95。优选地,步骤2中,所述混合溶剂中吡啶与水的体积比为8~10:1,所述氯代四甲基三蝶烯与高锰酸钾的摩尔比为1:35~40。优选地,所述反应釜的反应条件设置为:30min升温至150℃保温10小时,每小时降10℃至室温。本发明提供一种聚酰亚胺的制备方法:采用如上任意所述氯代三蝶烯四甲酸二酐化合物制备而成,合成路线如下式所示:进一步地,包括以下制备步骤:在惰性气氛下,依次加入等摩尔比的4,4’-二氨基二苯醚二胺单体和所制备的氯代三蝶烯四甲酸二酐单体;加入溶剂、脱水剂和/或催化剂;于150℃~160℃脱去甲苯-水共沸物,再于180℃反应4~6h,最后将聚合物溶液倒入剧烈搅拌下的甲醇溶液中沉降,抽滤即得到聚酰亚胺;其中,所述溶剂为间甲酚,固含量为10~20wt%;所述脱水剂为无水甲苯;所述脱水剂与氯代三蝶烯四甲酸二酐单体的摩尔比为14~30:1;所述催化剂为异喹啉。本发明还提供一种如上任意所述聚酰亚胺的制备方法所制备的聚酰亚胺。为了解决
背景技术:
中提到的问题,本发明首次提出设计新型的二酐单体,通过合理的分子设计合成氯取代的三蝶烯四甲酸二酐,该单体进行氯取代,拥有较大内自由体积的刚性骨架二酐单体对弥补聚酰亚胺的缺陷。由于氯原子的3d空轨道可以容纳更多电子,因此引入氯原子可以更有效地降低分子的homo和lumo能级。在三蝶烯四甲酸二酐中引入氯原子以后,不仅可以降低聚合物的homo能级,进而得到高的开路电压,同时可以调控聚合物在共混薄膜中的分子取向,进而提升电荷迁移率,提高器件效率。由于氯取代的化合物合成相对简单,价格便宜,因而非常适合于大规模的加工生产,实现下一代产业化应用,此外对研究新型聚酰亚胺超分子聚集体拓扑结构及其与性能关系的影响,具有十分重要的意义。此外,本技术方案与
背景技术:
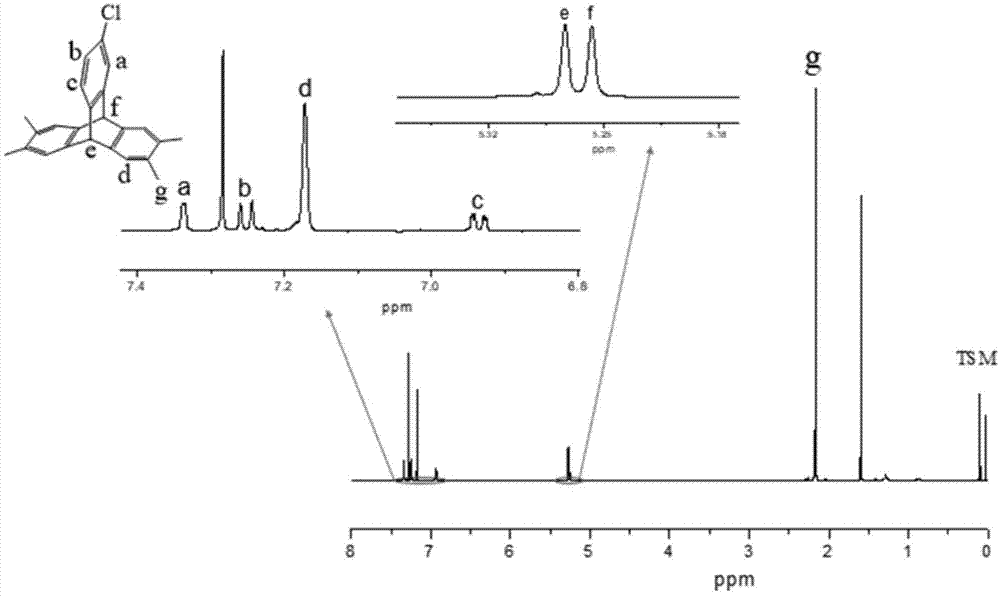
相比,具有如下优点:1)首次提出在通过分子设计合成氯取代的三蝶烯四甲酸二酐,并以此来合成制备聚酰亚胺。2)合成过程中原料廉价易得,产品合成路线简单,产率高,纯度高。3)氯元素的取代在diels-alder反应过程中极大的缩短了反应时间,更有利于产品的工业化;本发明采用绿色环保的溶剂热方法对系列氯代二酐进行了制备,且所得到的二酐单体具有高纯度。4)对于高分子这种软物质而言,单体的微小变化就会使得材料性能的巨大变化,该氯取代的二酐单体对研究二酐多尺度调控聚酰亚胺大分子链间的相互作用,进而调控聚酰亚胺超分子聚集体堆砌组装及其凝聚态拓扑结构具有重要意义。5)所制备的氯代三蝶烯四甲酸二酐化合物与二胺单体(oda)聚合得到系列新型聚酰亚胺高分子材料,引入了带有氯元素取代的三蝶烯,研究原子级别的调控对聚酰亚胺的影响。所制备的聚酰亚胺薄膜几乎为无色透明,热失重温度比kapton@更高,热稳定性良好,在膜分离材料、介电材料、分子互锁功能材料等领域拥有较大的应用价值。附图说明为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作一简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动性的前提下,还可以根据这些附图获得其他的附图。下面结合附图和实施例对本发明作进一步说明。图1为本发明中氯代四甲基三蝶烯的1hnmr图谱;图2为本发明中氯代四甲基三蝶烯的13cnmr图谱;图3为本发明中氯代三蝶烯四甲酸的1hnmr图谱图4为本发明中氯代三蝶烯四甲酸二酐的1hnmr图谱;图5为本发明中氯代三蝶烯四甲酸二酐的13cnmr图谱;图6为本发明制备的聚酰亚胺pi2的1hnmr图谱。具体实施方式为使本发明实施例的目的、技术方案和优点更加清楚,下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。本发明提供的氯代三蝶烯四甲酸二酐化合物的合成路线如下:式中,化合物1为14-氯-2,3,6,7-四甲基三蝶烯,化合物2为14-氯-2,3,6,7-三蝶烯四甲酸,化合物3为14-氯-2,3,6,7-三蝶烯四甲酸二酐。本发明中氯代三蝶烯四甲酸二酐中的氯元素不限于所给出的位置,还可以是在其他位置上的等效取代。氯代三蝶烯四甲酸二酐化合物的制备方法包括以下合成步骤步骤1、合成氯代四甲基三蝶烯将氯代邻氨基苯甲酸和亚硝酸异戊酯分别溶于二乙二醇二甲醚和1,2-二氯乙烷中,分别加入溶有2,3,6,7-四甲基蒽的1,2-二氯乙烷中;反应后,蒸出溶剂,加入顺丁烯二酸酐,加热回流发生diels-alder反应后,冷却后加入naoh-乙醇水溶液,加热回流,静置,抽滤,取固体,烘干,过柱纯化,旋蒸,得到白色粉末状固体,烘干,得氯代四甲基三蝶烯;步骤2、合成氯代三蝶烯四甲酸取步骤1所制备的氯代四甲基三蝶烯溶于吡啶与水的混合溶剂中并在高锰酸钾作用下加热搅拌回流;反应后,取滤液蒸馏出溶剂,用活性炭脱色,调节ph值小于1,取过滤后所得的固体进行干燥,得氯代三蝶烯四甲酸;步骤3、合成氯代三蝶烯四甲酸二酐取步骤2所制备的氯代三蝶烯四甲酸溶于乙酸,加热抽滤,加入乙酸酐,并于反应釜中进行反应,待析出白色晶体,进行抽滤,真空干燥后,即得氯代三蝶烯四甲酸二酐。根据上述制备方法:本发明提供以下四甲基蒽的制备实施例机械搅拌条件下,于500ml三口烧瓶中冰浴,依次加入80g无水三氯化铝和100ml邻二甲苯,100ml二氯甲烷于250ml恒压滴液漏斗中5℃以下缓慢滴加,待二氯甲烷滴加完毕,室温下反应0.5小时于70℃水浴4小时。水浴完成于冰浴降至5℃以下,约350ml3mol/l硫酸冰水混合溶液滴加至不再有明显气体放出,将剩余倒入,室温搅拌30分钟后倒出含有盐的上层液,加入80ml二甲苯,加热搅拌回流0.5h,冷却至室温,抽滤,滤饼用二甲苯洗涤3次,得到灰白色固体,于红外灯下烘干,二甲苯索提48小时,得到白色针状2,3,6,7-四甲基蒽晶体12g,产率12.8%,熔点为299℃。1hnmr(400mhz,cdcl3):δ=2.43(s,12h),7.68(s,4h),8.13(s,2h)。本发明提供氯代四甲基三蝶烯的制备实施例氯代四甲基三蝶烯的制备:于500ml三口烧瓶中加入4g2,3,6,7-四甲基蒽,100ml1,2-二氯乙烷(dce),磁力搅拌,加热至回流,3g2-氨基-5-氯苯甲酸溶于30ml二乙二醇二甲醚(dgdem);取10ml亚硝酸异戊酯溶于30ml1,2-二氯乙烷,分别将两恒压漏斗置于三口瓶两侧,控制两边滴速一样,约1h左右滴加完毕,回流反应4小时,随后蒸除溶剂至馏分温度达到150℃,剩余反应液取1.5g顺丁烯二酸酐加入回流0.5h,该过程将发生发生diels-alder反应,冷却后取2g氢氧化钠溶于75ml去离子水和75ml乙醇的混合溶液中加入到三口瓶中回流0.5h,过夜抽滤得深褐色固体,烘干后柱色谱分离纯化,固定相为100~200目中性氧化铝,淋洗液为二氯甲烷:石油醚=5:95,最终得到14-氯-2,3,6,7-四甲基三蝶烯白色固体2.2g,产率为41%。对本实施例3中所得氯代四甲基三蝶烯结构鉴定,进行了1hnmr测试,测试条件为500mhz,所用溶剂为cdcl3,测试结果见图1;对所得氯代四甲基三蝶烯进行13cnmr测试,测试条件为126mhz,所用溶剂为cdcl3,测试结果见图2;结合图1和图2可知,成功制备了氯代四甲基三蝶烯。图1中,氯代四甲基三蝶烯结构所对应的峰的位置及峰数具体数据如下:δ=7.34(d,1h),7.25(d,1h),7.18(d,4h),6.94(m,1h),5.27(s,1h),5.26(s,1h),2.17(d,12h),其中s表示单峰,d表示双峰,m表示多重峰。图2中所对应的峰的位置的具体数据如下:δ=147.81,144.50,142.44,133.13,133.08,130.33,125.05,124.98,124,67,124.28,123.80,52.91,52.61,19.50ppm。本发明提供氯代三蝶烯四甲酸的制备实施例机械搅拌条件下,于500ml三口烧瓶中加入上述实施例制备的氯代四甲基三蝶烯,然后取100ml吡啶和10ml去离子水加入,加热至回流,分批次加入高锰酸钾,每次间隔1小时左右,每次取3g高锰酸钾溶于15ml去离子水中,加热至完全溶解后再加入三口瓶中,待高锰酸钾全部加毕后,继续回流24小时,然后停止加热,抽滤出上清液并且取2g氢氧化钠溶于100ml去离子水中然后加入到滤饼中,加热回流0.5小时,再抽滤取滤液并且与前一次的滤液合并,蒸馏除溶剂约为原体积的1/3后加入适量活性炭加热搅拌15~20分钟脱色,然后稍冷藏后加入3mol/l盐酸调节ph值小于1,大量白色固体析出,抽滤,滤饼于40℃~50℃真空干燥8~12小时,即得到氯代三蝶烯四甲酸,产率为76%;图3为氯代三蝶烯四甲酸的1hnmr谱图,结合谱图可知,成功制备了氯代三蝶烯四甲酸,具体为14-氯-2,3,6,7-三蝶烯四甲酸。图3中,氯代三蝶烯四甲酸所对应的峰的位置及峰数具体数据如下:δ=13.10(s,4h),7.78(s,4h),7.60(d,1h),7.52(d,1h),7.15(dd,1h),6.04(s,1h),6.02(s,1h)。本发明提供氯代三蝶烯四甲酸二酐的制备实施例将0.2g14-氯-2,3,6,7-三蝶烯四甲酸溶于10ml的乙酸中,加热5~10分钟后趁热滤掉不溶物,滤液剩余8ml,滤液加入2ml乙酸酐(乙酸/乙酸酐为4/1)混合溶液于反应釜中,马弗炉程序设定为:30min升温至150℃保温10小时,每小时降10℃至室温,析出晶体,抽滤,120℃真空干燥箱干燥;即得氯代三蝶烯四甲酸二酐,产率为65%。对所制得的氯代三蝶烯四甲酸二酐进行1hnmr测试,测试条件为500mhz,所用溶剂为dmso-d6,13cnmr测定,测试条件为126mhz,所用溶剂为dmso-d6;其中图4、图5分别为氯代三蝶烯四甲酸二酐的1hnmr谱图、13cnmr谱图,结合图4和图5可知,成功制备了氯代三蝶烯四甲酸二酐,且对1hnmr中峰进行积分,可知所制备的氯代三蝶烯四甲酸二酐纯度为99.31%。图4中,氯代三蝶烯四甲酸二酐结构所对应的峰的位置及峰数具体数据如下:δ=8.19(s,2h),8.18(s,2h),7.68(d,1h),7.60(d,1h),7.22(dd,1h),6.40(s,1h),6.39(s,1h)。其中s表示单峰,d表示双峰,dd表示双二重峰。图5中所对应的峰的位置的具体数据如下:δ=163.33,152.38,152.06,144.75,141.45,131.11,130.51,130.41,127.00,126.70,125.58,121.53,121.39,52.66,52.44ppm。本发明的基于氯代三蝶烯四甲酸二酐合成的全芳香型聚酰亚胺,合成聚酰亚胺的路线如下:以下结合聚酰亚胺合成实例作进一步说明在氮气保护下,于在25ml两口烧瓶中,加入4,4’-二氨基二苯醚(oda)0.5mmol(0.1001g),间甲酚2.8ml,室温搅拌20min后加入14-氯-2,3,6,7-三蝶烯四甲酸二酐0.5mmol(0.2144g),无水甲苯(1ml)冲粘附在瓶壁上的二酐。40℃搅拌1h,之后10min升温至80℃保持并加入3滴异喹啉保持2h,完全溶解。升温至120℃,加上分水器,于120℃保持1h后升至160℃,反应于160℃脱去甲苯-水,于160℃保持1h后升至180℃,于180℃保持4h后,停止反应,缓慢倒入200ml快速搅拌的甲醇溶液,然后过滤得到白色的丝状的聚酰亚胺,即为pi2。产物溶解在间甲酚中再倒入甲醇中沉降,反复沉降4次,获得干燥的白色絮状聚合物0.2613g。聚合物pi2核磁氢谱1hnmr如图6所示,测试条件为500mhz,所用溶剂为dmso-d6,由图6可以判断聚合物结构骨架基本正确。将pi2与kapton@相比,其热性能测试结果见表1表1样品tg(℃)td5(℃)td10(℃)800℃残重(%)pi2>30052858158.2kapton@>30053058562注)表1中td5为失重5wt%对应的温度,td10为热失重10wt%对应的温度。本发明还提供一种如上任意所述聚酰亚胺的制备方法所制备的聚酰亚胺,得到聚酰亚胺的热失重温度高,热稳定性良好,在膜分离材料、介电材料、分子互锁功能材料等领域拥有较大的应用价值。氯取代的化合物合成相对简单,价格便宜,因而非常适合于大规模的加工生产,实现下一代产业化应用,此外对研究新型聚酰亚胺超分子聚集体拓扑结构及其与性能关系的影响,具有十分重要的意义。尽管本文中较多的使用了术语,但并不排除使用其它术语的可能性。使用这些术语仅仅是为了更方便地描述和解释本发明的本质;把它们解释成任何一种附加的限制都是与本发明精神相违背的。最后应说明的是:以上各实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述各实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的范围。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1