与蛋鸭卵泡发育相关的miRNAapla-mir-145-4及其检测引物、抑制物和应用的制作方法
本发明涉及基因工程技术领域,尤其涉及与蛋鸭卵泡发育相关的mirnaapla-mir-145-4以及检测引物、抑制物和应用。
背景技术:
卵泡发育与蛋鸭的产蛋性能密切相关,直接影响蛋鸭的产蛋量。已有研究表明,禽类卵泡发育是极为复杂的生物学过程,目前人们已对家禽的卵泡发育模式有了一定的了解,但是作为决定产蛋量的重要因素,卵泡发育的具体调控机理仍需深入研究。
然而目前,缺乏检测蛋鸭的卵泡发育状况的mirna标志物。
鉴于此,特提出本发明。
技术实现要素:
为了克服现有技术的缺陷与不足,本发明的目的包括但不限于提供一种与蛋鸭卵泡发育相关的mirna。该mirna可以作为标志物,用于检测蛋鸭卵泡颗粒细胞增殖分化状况,为判断目标蛋鸭的产蛋性能提供参考。
本发明的另一个目的包括但不限于提供上述mirna的应用。
本发明的另一个目的包括但不限于提供上述mirna的检测引物。
本发明的另一个目的包括但不限于提供一种抑制上述mirna结合至其靶基因的抑制物。
本发明的另一个目的包括但不限于提供一种重组表达载体。
本发明的另一个目的包括但不限于提供一种调控蛋鸭卵泡发育的方法。
为实现上述目的,本发明通过下述技术方案实现:
随着“基因组时代”的来临,在全基因组水平上解析性状相关基因表达模式的整体特征,以揭示蛋鸭产蛋表型性状形成的分子基础是今后蛋鸭育种工作的重要研究方向之一。microrna(mirna)作为一类小的单链内源性非编码rna,能够通过降解靶mrna或抑制翻译发挥其基因转录后的调控作用。近年来,大量研究表明,mirnas在细胞分化与凋亡、生长发育、糖脂代谢、炎症、免疫应答以及肿瘤发生等多个生理和病理过程中均扮演着关键的角色,其中在卵泡发育过程中一些影响卵泡颗粒细胞分化和增殖的mirna已经被筛选和确定。
颗粒细胞的生长状况直接影响到卵泡的发育情况,卵泡颗粒细胞可以分泌性腺激素及生长因子调控卵泡膜细胞和卵母细胞的生长、分化和成熟,同时也精确的调控卵泡的生长发育。因此,保障良好的卵泡发育、掌握卵泡发育的调控规律有助于进一步提高蛋鸭的繁殖力,对于提高蛋鸭生产性能具有重要意义。
然而目前关于蛋鸭组织特异性mirna的研究尤其是蛋鸭卵泡mirna及其调控机制的研究尚未见报道。因此,迫切需要提高蛋鸭卵泡mirna研究水平和完整性,从而为蛋鸭基因组及其非编码rna的研究提供科学的理论依据,以便更为深入了解蛋鸭卵泡发育的调控机制,为提高蛋鸭的繁殖性能提供理论支撑。
本发明通过对不同发育时期两组卵泡组织样品进行高通量全转录组测序,筛选与蛋鸭卵泡发育相关的mirna,经过生物信息学差异表达分析初步选定在黄卵泡中显著高表达的mirnaapla-mir-145-4,其能通过靶向pik3ca基因调控卵泡发育,抑制细胞增殖标记基因cyclinb2的表达,促进细胞凋亡标志基因bcl2的表达。该mirna对研究蛋鸭繁殖性状的遗传本质及提高蛋鸭繁殖力具有重要的意义,其具有重要的实际应用价值。
基于此,在本发明的第一方面,提供了一种与蛋鸭卵泡发育相关的mirna,所述mirna为apla-mir-145-4,其核苷酸序列如seqidno:1所示。
在本发明的第二方面,提供了上述的与蛋鸭卵泡发育相关的mirna作为分子标志物在检测蛋鸭卵泡颗粒细胞增殖分化状况中的应用。
经过研究,本发明提供的mirna即apla-mir-145-4分子在蛋鸭黄卵泡中的表达量极显著高于蛋鸭白卵泡中的表达量(p<0.01),首次发现蛋鸭apla-mir-145-4与蛋鸭卵泡发育相关,由此本发明的蛋鸭apla-mir-145-4可作为分子标志物用于鉴别蛋鸭卵泡的发育情况例如卵泡颗粒细胞的增殖分化状况,弥补了本领域现有的空缺,为解析蛋鸭卵泡发育的遗传机理提供理论基础和科学依据;此外,其对于研究蛋鸭繁殖性状的遗传本质、提高蛋鸭繁殖力以及遗传辅助育种都具有重要的意义。
在本发明的第三方面,提供了检测上述mirna的引物。
进一步地,在本发明的一些实施方案中,所述引物包括seqidno:2所示的上游引物、seqidno:3所示的下游引物和seqidno:5所示的loop引物。
在本发明的第四方面,提供了一种能抑制上述的与蛋鸭卵泡发育相关的mirna结合靶基因的抑制物,所述靶基因为pik3ca基因,所述抑制物与所述mirna的结合位点为aactgga;
优选地,所述抑制物选自pik3ca基因的3’utr中长约240bp区段。
进一步地,在本发明的一些实施方案中,所述抑制物序列如seqidno.4所示;
优选地,所述抑制物的5’末端和3’末端分别添加限制性酶切位点序列;
优选地,所述限制性酶切位点序列在酶切后产生粘性末端;
更优选地,所述的限制性酶切位点序列分别为pmei限制性酶切位点和xhoi限制性酶切位点对应的核苷酸序列;
更优选地,所述pmei酶切位点位于5’末端,所述xhoi酶切位点位于3’末端。
在本发明的第五方面,提供了一种重组表达载体,所述重组表达载体包含如上所述的抑制物。
进一步地,在本发明的一些实施方案中,所述重组表达载体中的标记基因为双荧光素酶报告基因;
优选地,所述重组表达载体是通过将所述抑制物连接到报告载体pmirglo中获得。
在本发明的第六方面,提供了一种检测上述与蛋鸭卵泡发育相关的mirna的试剂盒,其含有检测上述mirna的引物组。
进一步地,在本发明的一些实施方案中,所述引物组包括:反转录引物、上游引物和下游引物,反转录引物序列如seqidno:5所示;上游引物序列如seqidno:2所示,下游引物序列如seqidno:3所示。
采用该引物组,可通过茎环法检测出上述的与蛋鸭卵泡发育相关的mirna。
进一步地,在本发明的一些实施方案中,所述的试剂盒含有针对反转录试剂、反转录引物、特异性引物、内参引物、荧光定量pcr反应试剂。
所述的内参引物包括u6内参基因的上游引物和下游引物,上游引物序列如seqidno:6所示,下游引物序列如seqidno:7所示。
作为本发明所述试剂盒的优选实施方式,所述试剂盒还包括rna提取试剂、逆转录反应体系和荧光定量pcr反应体系,其中所述荧光定量pcr反应体系包括thunderbirdsybrqpcrmix、ddh2o、所述逆转录反应体系逆转录得到的cdna以及所述的检测引物对。
作为以上具体实施方式,所述荧光定量pcr反应体系如下:thunderbirdsybrqpcrmix10μl,10um蛋鸭apla-mir-145-4上游引物0.4μl,10um蛋鸭apla-mir-145-4下游引物0.4μl,待检测cdna模板2.0μl,ddh2o7.2μl,总体积20μl。
在本发明的第七方面,提供了所述试剂盒的使用方法,包括如下步骤:
步骤1、提取待检测样品中的rna;
步骤2、利用反转录引物在反转录酶的作用下进行apla-mir-145-4反转录生成cdna;
步骤3、利用如上所述的引物(例如seqidno:2所示的上游引物、seqidno:3所示的下游引物和seqidno:5所示的loop引物),对待检测样品cdna进行荧光定量pcr扩增,采用2-δδct方法计算并获得不同来源卵泡样本中apla-mir-145-4的相对表达量;
步骤4、根据pcr扩增产物及基因相对表达量判断待检测样本是否存在蛋鸭apla-mir-145-4及其表达情况。
作为以上具体实施方式,所述步骤3中的荧光定量pcr反应条件为,98℃,10s;94℃,15s,54℃,15s,60℃,15s,40个循环;95℃,10s;65℃,60s,97℃,1s,1个循环。
本发明的第八方面,提供了mirnaapla-mir-145-4的模拟物(即mimic),其序列如seqidno:1和seqidno:8所示。
本发明的第九方面,提供了上述apla-mir-145-4模拟物在检测蛋鸭卵泡颗粒细胞增殖分化中的应用。
经过研究,发明人发现,本发明的蛋鸭mirnaapla-mir-145-4的mimic转染进入蛋鸭卵泡颗粒细胞中,与nc组相比,mimic组细胞增殖标记基因cyclinb2的表达量极显著降低(p<0.01),细胞凋亡标志基因bcl2的表达量极显著增加(p<0.01),表明该mirna可作为分子标志物应用于检测蛋鸭卵泡颗粒细胞中细胞增殖分化状况。
在本发明的第十方面,本发明提供了一种调控蛋鸭卵泡发育的方法,其包括:向目标蛋鸭卵泡颗粒细胞施用试剂,所述试剂含有作为活性成分的如seqidno:1和seqidno:8所示的rna。
优选地,所述调控蛋鸭卵泡发育是指:抑制蛋鸭卵泡颗粒细胞增殖和/或促进蛋鸭卵泡颗粒细胞调亡。
使用seqidno:1和seqidno:8所示的mirnamimic转染蛋鸭卵泡颗粒细胞,令人惊喜地发现,细胞增殖标记基因cyclinb2的表达量降低,细胞凋亡标志基因bcl2的表达量增加,该结果表明seqidno:1所示的mirna可以用于调控蛋鸭卵泡发育。
附图说明
为了更清楚地说明本发明实施例的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,应当理解,以下附图仅示出了本发明的某些实施例,因此不应被看作是对范围的限定,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他相关的附图。
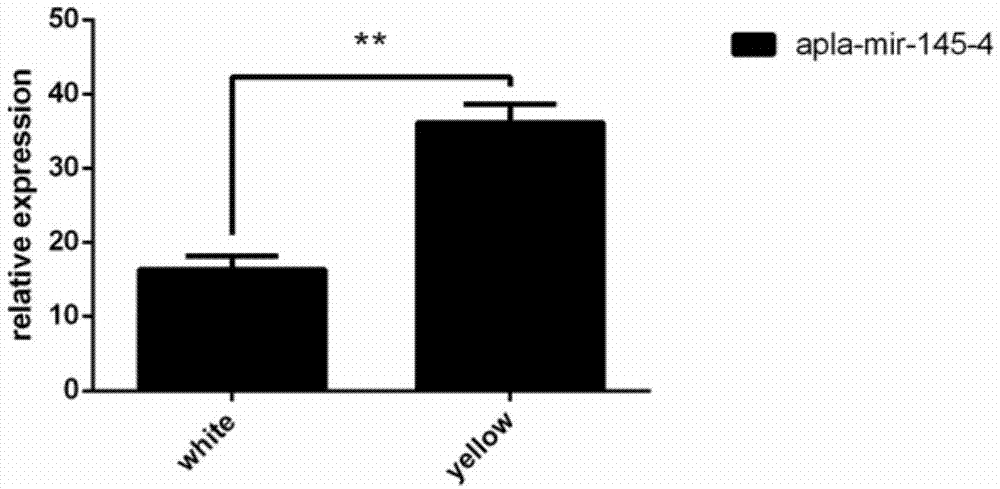
图1为本发明提供的蛋鸭apla-mir-145-4在蛋鸭白卵泡和黄卵泡中的相对定量表达结果;
图2为实施例2中过表达蛋鸭apla-mir-145-4后,过表达apla-mir-145-4组与对照组中apla-mir-145-4表达变化情况;
图3为实施例2中过表达蛋鸭apla-mir-145-4后,过表达apla-mir-145-4组与对照组中细胞增殖与凋亡关键基因表达变化情况。
图4为pmirglo载体的结构示意图。
图5为双荧光素酶方法验证apla-mir-145-4与pik3ca的3’-utr的结合结果。
具体实施方式
实施例1蛋鸭mirnaapla-mir-145-4的获得pcr及其荧光定量检测试剂盒与方法
一、蛋鸭apla-mir-145-4获得
本实施例所述蛋鸭apla-mir-145-4对应的核苷酸序列如seqidno:1所示,本发明的蛋鸭apla-mir-145-4是发明人基于前期完成的蛋鸭卵泡组织全转录组测序结果,通过对不同发育时期两组卵泡组织样品的测序结果进行大量生物信息学分析筛选获得的一个新的mirna分子。申请人将其命名为蛋鸭apla-mir-145-4。
二、蛋鸭mirnaapla-mir-145-4的荧光定量pcr检测引物对及其检测试剂盒与方法
本实施例设计荧光定量pcr检测引物对并识别鉴定所述蛋鸭apla-mir-145-4在蛋鸭卵泡颗粒细胞中的客观存在。本实施例识别鉴定的方法包括以下步骤:
1、样品采集
采集产蛋高峰期蛋鸭白卵泡和黄卵泡样品各3份,pbs清洗干净后用针头刺破卵泡挤出卵泡液,放入无酶的1.5mlep管中,做好标记后投入液氮或-80℃冰箱保存。
2、样品总rna提取
利用传统的trizol、氯仿法提取卵泡组织总rna,具体步骤如下:
1)液氮研磨,取50-100mg组织样品放于研钵中,倒入液氮少许,迅速研磨,待液氮挥发干净再加入少量液氮,直至组织样品研为粉末,将组织样品转入1.5ml离心管中,加入1mltrizol,试温放置5min,使其充分裂解;
2)4℃12000g离心10min,将上清转入干净的无rnaase的1.5ml离心管中;
3)按照每1ml匀浆液加0.2ml氯仿,剧烈15s,室温放置15min;
4)4℃12000g离心10min;
5)小心吸出上层无色溶液于另一个1.5ml无rnaase的离心管中,加入0.5倍的异丙醇混匀,试温静置5-10min;
6)4℃12000g离心10min,弃上清,rna沉于管底;
7)加入1ml75%乙醇,温和振荡离心管,悬浮沉淀;
8)4℃8000g离心5min,弃上清;
9)加入1ml无水乙醇,温和振荡离心管,悬浮沉淀;
10)4℃8000g离心5min,弃上清,室温晾干;
11)使用30-50μl无rnaase去离子水溶解rna,-80℃保存备用。
3、rna样品质量检测分析
使用nanodrop1000微量分光光度计检测rna样品浓度与od值,利用1%琼脂糖凝胶电泳检测rna的完整性
4、反转录
采用takara公司的反转录试剂盒
1)基因组dna的除去反应
表1
反应条件如下:
42℃2min;4℃保存。
2)反转录反应
反应液配制过程在冰上进行。
表2
反应条件如下:
37℃、15min;85℃、5sec;4℃保存。
5、荧光定量pcr反应
apla-mir-145-4荧光定量检测引物核苷酸序列如seqidno:2和seqidno:3所示,用于内参基因荧光定量检测的引物核苷酸序列如seqidno:6和seqidno:7所示。
利用takara公司的realtime试剂盒thunderbirdsybrqpcrmix说明书步骤进行荧光定量pcr,反应体系如下(20μl):
表3
利用roche
反应结束后导出数据,结果利用2-δδct方法进行分析。利用graphadprism软件对分析结果进行作图。
白卵泡和黄卵泡组织中apla-mir-145-4表达结果见图1,结果显示,第一,白卵泡中以及黄卵泡中均有apla-mir-145-4的表达,所述蛋鸭apla-mir-145-4在蛋鸭卵泡颗粒细胞中的客观存在。第二,黄卵泡中apla-mir-145-4的表达量极显著高于白卵泡中(p<0.01)。因此,可以看出,apla-mir-145-4与卵泡的发育具有重要的相关性。
实施例2apla-mir-145-4作为分子标志物在检测蛋鸭卵泡颗粒细胞增殖分化中的应用
一、蛋鸭卵泡颗粒细胞分离
蛋鸭卵泡颗粒细胞的分离采用如下步骤:
1、选择产蛋高峰期的产蛋鸭,颈静脉放血处死;取出整个卵巢组织,置于装有预冷pbs的无菌培养皿中;
2、用加有双抗的pbs缓冲液冲洗血污,漂洗3次;
3、将漂洗干净的卵泡移入装有预冷pbs缓冲液的平皿中,剥净卵泡外膜、结缔组织及血管网;
4、用手术刀在卵泡表面划一道1-2cm长的切口(动作要快),释放卵黄,用pbs缓冲液将剩余的卵黄液漂洗干净,剩下的卵泡膜即为:基膜和卵泡颗粒细胞层;
5、将漂洗干净的卵泡膜尽量剪碎,置于15ml离心管中,加4ml培养基,用1ml移液枪反复吹打1min,4℃1000rpm离心后弃上清;
6、向沉淀中加入4ml0.2%ⅱ型胶原酶,重悬沉淀,置于37℃恒温摇床80rpm消化30min;
7、消化结束,加入4mlm199完全培养基(含10%血清)终止消化;用200目不锈钢筛过滤,并用2mlm199完全培养基清洗网筛,收集滤液,4℃1000rpm离心10min;
8、弃上清,加入10mlm199完全培养基,4℃1000rpm离心10min;
9、弃上清,加入m199完全培养基(含10%fbs及1%双抗)重悬后,测定细胞密度,调整悬浮液细胞密度为1×106个/ml,接种于6孔培养皿,置于37℃、5%co2培养箱内静置培养;
10、颗粒细胞培养24小时后,换新鲜含有胎牛血清的m199培养基,贴壁细胞可用于进一步研究中。
二、细胞转染
1、分别取125μlopti-mem培养基稀释合成的apla-mir-145-4mimic(即seqidno:1和seqidno:8)和nc;
2、取250μlopti-mem培养基稀释
3、分别向(1)中两管混合物中加入125μl(2)中的混合物,室温孵育5min;
4、将250μl混合物转入细胞。
各实验组设置3个重复孔,转染细胞分组如下:①转染nc,②转染apla-mir-145-4。各转染组转染细胞24h后,利用trizol消化细胞,提取细胞总rna后用于过表达后荧光定量分析。
三、荧光定量分析
1、细胞中总rna的提取
参照实施例1中总rna的提取方法提取细胞中总rna。
2、反转录
同实施例1中反转录的方法。
3、荧光定量pcr反应
(1)荧光定量pcr反应条件和方法同实施例1,其中apla-mir-145-4荧光定量引物核苷酸序列如seqidno:2和seqidno:3所示,扩增条件为:98℃,10s;94℃,15s,54℃,15s,60℃,15s,40个循环;95℃10s,65℃60s,97℃1s,1个循环;
(2)细胞增殖标志基因cyclinb2荧光定量引物核苷酸序列如seqidno:9和seqidno:10所示,扩增条件为:98℃,10s;94℃,15s,56℃,15s,60℃,15s,40个循环;95℃10s,65℃60s,97℃1s,1个循环;
(3)细胞凋亡标志基因bcl2荧光定量引物核苷酸序列如seqidno:11和seqidno:12所示,扩增条件为:98℃,10s;94℃,15s,54℃,15s,60℃,15s,40个循环;95℃10s,65℃60s,97℃1s,1个循环;
(4)内参基因荧光定量引物核苷酸序列如seqidno:6和seqidno:7所示,扩增条件为:98℃,10s;94℃,15s,54℃,15s,60℃,15s,40个循环;95℃10s,65℃60s,97℃1s,1个循环。
4、结果分析
反应结束后导出数据,结果利用2-δδct方法进行分析。利用graphadprism软件对分析结果进行作图。转染蛋鸭apla-mir-145-4后环apla-mir-145-4的表达量及细胞增殖、凋亡标志基因的表达量分析结果见图2-3。
由图2可以看出,过表达apla-mir-145-4后,与nc组相比,过表达蛋鸭apla-mir-145-4后apla-mir-145-4的表达量极显著高于nc组(p<0.01)。
由图3可以看出,过表达蛋鸭apla-mir-145-4后,与nc组相比,过表达蛋鸭apla-mir-145-4后,细胞增殖标记基因cyclinb2的表达量极显著降低(p<0.01),细胞凋亡标志基因bcl2的表达量极显著增加(p<0.01),说明该mirna促进了细胞的凋亡。由此可见,该mirna可作为分子标志物应用于检测蛋鸭卵泡颗粒细胞中细胞增殖分化状况。
综上所述,本发明中的合成的蛋鸭apla-mir-145-4mimic可以稳定表达蛋鸭apla-mir-145-4,且可以作为检测指标反映蛋鸭apla-mir-145-4的表达量,并可以应用于检测蛋鸭卵泡颗粒细胞中细胞增殖分化状况。
实施例3蛋鸭apla-mir-145-4靶基因pik3ca双荧光素酶报告基因检测系统的设计与构建
首先,针对选定的mirnaapla-mir-145-4,在全转录组测序结果中进行关联分析,从mrna的测序结果中筛选出与apla-mir-145-4相互作用的靶基因pik3ca,利用mirbase分析获得apla-mir-145-4与pik3ca的结合位点为atcccca。
随后,从ncbi获得pik3ca的3’-utr序列(即apla-mir-145-4的抑制物),利用突变的方法将apla-mir-145-4的抑制物中的aactgga突变为gtaattc,分别将上述两个基因片段克隆到pmirglo载体中,得到相应的含有apla-mir-145-4的抑制物序列的载体(pmirglo-pik3ca-wt)和含有apla-mir-145-4的抑制物突变序列的载体(pmirglo-pik3ca-mut)。载体构建具体包括如下步骤:
(1)pmirglo载体的双酶切处理
pmirglo载体的结构示意图如图4所示,载体含有限制性内切酶pmei和xhoi酶切位点。用两种内切酶pmei和xhoi对上述载体进行双酶切,酶切反应体系如下,体系总体积为50μl:
表4
反应条件为:37℃酶切6h,随后对酶切产物进行纯化回收。
(2)突变前后的蛋鸭pik3ca基因3’utr片段的获得与验证
针对蛋鸭pik3ca基因3’utr中与apla-mir-25-42的结合位点突变前后的序列,分别设计引物扩增突变前后的pik3ca基因3’utr片段,采用的突变前后的扩增引物核苷酸序列分别如seqidno:13、seqidno:14、seqidno:15和seqidno:16所示,反应体系如下(20μl)。
表5
扩增条件为:95℃,300s;94℃,30s,56℃,30s,72℃,30s,30个循环;72℃,600s。对扩增获得的pcr产物利用1%琼脂糖凝胶电泳进行检测并送测序验证。
(3)突变前后的蛋鸭pik3ca基因3’utr片段的双酶切
对验证正确的pcr产物进行纯化,用两种内切酶pmei和xhoi对回收的上述pcr产物进行双酶切,酶切反应体系如下,体系的总体积为50μl:
表6
反应条件为:37℃酶切6h,随后对酶切产物进行纯化回收。
(3)pmirglo-pik3ca-wt和pmirglo-pik3ca-mut载体的构建
将pcr扩增并双酶切后的pik3ca基因3’utr片段与同样经过双酶切后的载体进行连接,连接反应体系如下(总体积10μl):
表7
反应条件为:16℃过夜连接。
将连接产物转化入感受态细胞,对阳性克隆进行菌落pcr鉴定和测序验证,测序结果如seqidno:4和seqidno:17所示;成功构建的重组载体,分别命名为pmirglo-pik3ca-wt和pmirglo-pik3ca-mut。
实施例4apla-mir-145-4促进蛋鸭卵泡颗粒细胞凋亡的机制
分离蛋鸭卵泡颗粒细胞,按照5×104/孔接种在24孔板中,用pmirglo、pmirglo-pik3ca-wt、pmirglo-pik3ca-mut分别与apla-mir-145-4mimic共转染。在共转染24h后收集细胞,利用
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
sequencelisting
<110>湖北省农业科学院畜牧兽医研究所
<120>与蛋鸭卵泡发育相关的mirnaapla-mir-145-4以及检测引物、抑制物和应用
<160>17
<170>patentinversion3.5
<210>1
<211>25
<212>rna
<213>人工序列
<400>1
guccaguuuucccaggaaucccuua25
<210>2
<211>34
<212>dna
<213>人工序列
<400>2
acactccagctggggtccagttttcccaggaatc34
<210>3
<211>16
<212>dna
<213>人工序列
<400>3
tggtgtcgtggagtcg16
<210>4
<211>240
<212>dna
<213>人工序列
<400>4
agtttaagtaaggctctatctgtccaaaaagatgtgtagctcagcacccctgcagctgat60
cacatgtgggttgttttttaatctgtgttgatgaaagaagccaactggaaactagataaa120
gaagctttctgtctgcatacattaaccaaatcgataggtgctctggtgttggagaaaatc180
tgatttcactttatgctgatacaatgctgatttcatgagaatcactctggattcacacta240
<210>5
<211>44
<212>dna
<213>人工序列
<400>5
ctcaactggtgtcgtggagtcggcaattcagttgagtaagggat44
<210>6
<211>17
<212>dna
<213>人工序列
<400>6
ctcgcttcggcagcaca17
<210>7
<211>20
<212>dna
<213>人工序列
<400>7
aacgcttcacgaatttgcgt20
<210>8
<211>25
<212>rna
<213>人工序列
<400>8
uaagggauuccugggaaaacuggac25
<210>9
<211>18
<212>dna
<213>人工序列
<400>9
ttacaacaagaggaacgc18
<210>10
<211>18
<212>dna
<213>人工序列
<400>10
tccatagggacaggagac18
<210>11
<211>18
<212>dna
<213>人工序列
<400>11
acggctctcgctcctgct18
<210>12
<211>18
<212>dna
<213>人工序列
<400>12
cggttgacgctctccacg18
<210>13
<211>54
<212>dna
<213>人工序列
<400>13
atcgccgtgtaattctagttgtttaaacgtgctttgtatattgttcatcattat54
<210>14
<211>46
<212>dna
<213>人工序列
<400>14
gcaggtcgactctagactcgaggctagcctgtcaccctccgcaagg46
<210>15
<211>55
<212>dna
<213>人工序列
<400>15
gtttaaacgctctttcctcccctccttctctttattttttcttttggcgttagac55
<210>16
<211>30
<212>dna
<213>人工序列
<400>16
cctcgagggagaaggaggggaggaaagagc30
<210>17
<211>240
<212>dna
<213>人工序列
<400>17
agtttaagtaaggctctatctgtccaaaaagatgtgtagctcagcacccctgcagctgat60
cacatgtgggttgttttttaatctgtgttgatgaaagaagccgtaattcaactagataaa120
gaagctttctgtctgcatacattaaccaaatcgataggtgctctggtgttggagaaaatc180
tgatttcactttatgctgatacaatgctgatttcatgagaatcactctggattcacacta240
- 还没有人留言评论。精彩留言会获得点赞!