含香豆素骨架的有机金属铱配合物磷光材料及其制备方法与流程
本发明涉有机电致发光领域,尤其涉及一种含香豆素骨架的有机金属铱配合物磷光材料及其制备方法。
背景技术:
有机电致发光是指有机发光材料在所施加电场激发下从基态跃迁到激发态,再由激发态回到基态的过程中辐射发光的现象。电致发光与光致发光不同,载流子自旋统计规律表明:载流子从两电极注入,在有机电致发光器件(oled)中产生的单线态激子与三线态激子的比例约为1:3。传统的荧光材料只能利用器件中产生的25%的单线态激子发光,器件的外量子效率通常小于5%,严重限制了oled技术的应用。磷光材料中通常引入了铱,铂等重金属原子,重金属原子强的自旋轨道耦合效应增强了电子态的系间窜越作用,致使基于磷光材料的oled器件的内量子效率理论上为100%,所以基于磷光材料器件的eqe将极大优于基于荧光材料的器件。磷光材料中铱和铂的配合物研究的最为成熟,而铱配合物的电致发光性能通常优于铂配合物。因此,研究开发有机金属铱磷光发光材料一直是有机电致发光器件领域的热点方向。
香豆素骨架属于刚性的苯并杂环结构,大的刚性有助于发光材料的辐射跃迁,减小非辐射跃迁的几率,提高材料的发光量子效率,通常香豆素衍生物均具有较高的发光量子产率。又由于香豆素骨架结构简单,易于合成和功能化,将其应用于合成性能优异的有机金属铱配合物磷光材料必是高度可行的方案。通常,铱配合物发光颜色的调控需要对配体进行复杂的修饰才能实现;而香豆素骨架仅通过在苯环上不同取代位置的修饰得到的ir(c^n)2(acac)型就可实现红、橙和绿颜色的调控,获得的配合物均具有高的发光量子产率。研究表明:非对称ir(c1^n)(c2^n)(acac)型配合物是实现量子产率和发光颜色双重调控的有效手段,将具有香豆素骨架的配体与2-苯基喹啉合成具有非对称结构的铱配合物磷光材料可进一步实现对材料性能的调控。
近年来随着oled在显示与照明技术产业化进程的加快,京东方,天马,微信诺等公司投入巨资建成众多产线。基于产业化的进一步发展,设计并合成结构简单且性能优异的有机电致磷光材料仍然具有重大的实用前景。
技术实现要素:
有鉴于此,本发明要解决的技术问题在于提供一种含香豆素骨架的有机金属铱配合物磷光材料,利用香豆素骨架结构高度刚性,简单,易于合成,强的发光特性等特点;通过控制取代位置的变化以及采用非对称结构类型同时,实现对所得铱配合物发光波长和发光效率的双重调控,获得具有结构简单且性能优异的有机电致磷光材料。
为了达到上述目的,本发明的技术方案是这样实现的:
含香豆素骨架的有机金属铱配合物磷光材料,其结构通式为:
其中ar取自下列c5–c8任意一种结构:
上述含香豆素骨架的有机金属铱配合物磷光材料的制备方法,包括以下步骤:
第一步:合成含有香豆素骨架的2-苯基吡啶类有机配体;
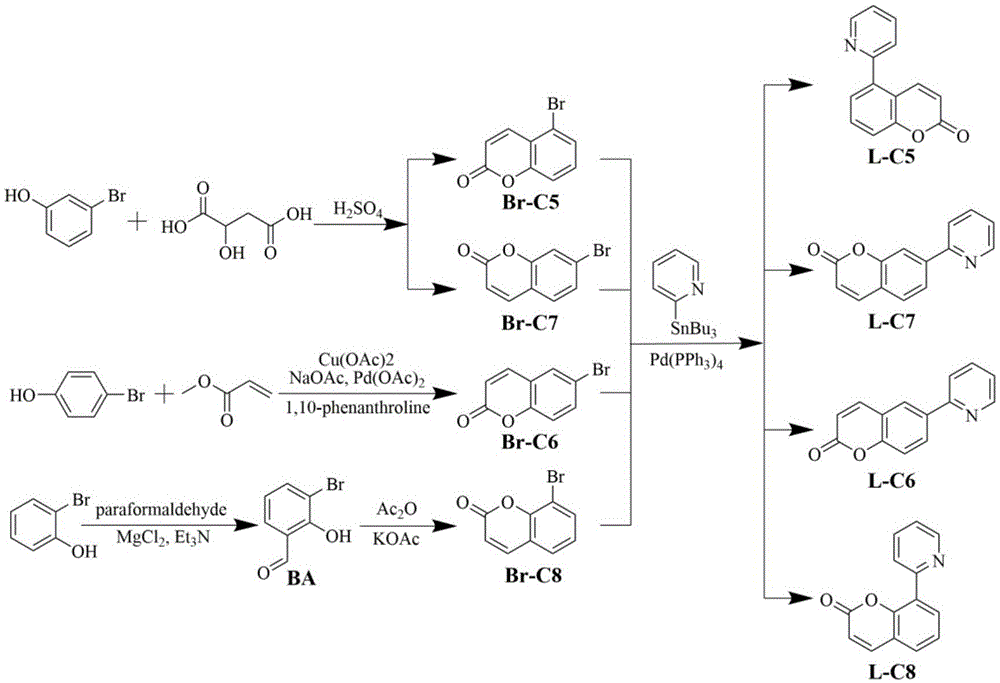
(1)对于有机配体l-c5和l-c7合成方案如下:①在氮气氛围下,将dl-苹果酸和间溴苯酚按物质的量1:(1.4-1.8)的比例投入反应器中,冰水浴搅拌条件下滴入质量分数98%的浓硫酸,其加入量为每10克间溴苯酚加入13毫升浓硫酸;随后氮气氛围下加热至115℃至125℃,搅拌反应6-8小时后冷却至室温;将反应混合液滴入冰冷的饱和食盐水中,过滤并水洗数次后得到粗产品,然后将其用层析硅胶柱纯化即可得产品br-c5和br-c7;②在甲苯溶液中,pd(pph3)4的催化下,br-c5或br-c7与三正丁基2-吡啶锡发生stille偶联反应,生成最终的有机配体l-c5或l-c7。
所述的br-c5、br-c7、l-c5和l-c7分别对应的分子或配体如下式:
(2)对于有机配体l-c6合成方案如下:①将对溴苯酚与丙烯酸甲酯按物质的量1:(1-2.5)的比例投入于含1,2-二氯乙烷溶剂的反应器中完全溶解,再相继加入0.5倍摩尔量的醋酸铜、5%摩尔量的醋酸钯、1.5倍摩尔量的醋酸钠、10%摩尔量的1,10-菲啰啉和适量的分子筛,110℃下反应20-36小时,反应完后冷却至室温,过滤除去不溶杂质,二氯甲烷洗涤滤饼,滤液减压旋蒸除去溶剂,用硅胶柱色谱分离纯化发生环化反应生成br-c6;②甲苯溶液中,在pd(pph3)4的催化下,br-c6与三正丁基2-吡啶锡发生stille偶联反应,生成最终的有机配体l-c6;
所述的br-c6、l-c6分别对应的分子或配体如下式:
(3)对于有机配体l-c8合成方案如下:①环境条件下,加入乙腈溶剂于反应容器中,将邻溴苯酚和多聚甲醛以物质的量1:(3-7)的比例加入溶剂中,再加入1.5-2.5倍摩尔量的无水氯化镁、2-4倍摩尔量的三乙胺,回流条件下反应8-10小时后恢复至室温;过滤除去不溶物,所得滤液浓缩得粗产品,然后将其用层析硅胶柱纯化即可得产品ba;②在氮气氛围下,将ba和醋酸钾以物质的量(1.4-1.8):1的比例放入反应容器,再加入13-20倍摩尔量于ba的醋酸酐,170℃搅拌回流6-8小时;反应结束后冷却至室温,加水稀释,搅拌状态下缓慢加碳酸钠水溶液直至溶液呈中性,二氯甲烷萃取中和后的液体,合并所有的有机相,无水硫酸钠干燥,浓缩有机相得粗产品,然后将其用层析硅胶柱纯化即可得产品br-c8;③甲苯溶液中,在pd(pph3)4的催化下,br-c5或br-c7与三正丁基2-吡啶锡发生stille偶联反应,生成最终的有机配体l-c8。
所述的ba、br-c8、l-c8分别对应的分子或配体如下式:
第二步:金属铱二聚体配合物的合成,具体为:
(1)对于对称ir(c^n)2(acac)型电致磷光材料:将步骤一所得的有机配体与水合三氯化铱按物质的量(2-3):1的比例投入反应容器,在氮气氛围下,向所述反应容器中再加入可将反应物完全溶解的四氢呋喃与水的混合溶剂,混合溶剂中四氢呋喃与水的体积比为(2-5):1,氮气氛围中加热至100℃至110℃,搅拌16小时后冷至室温;将反应混合液转移至分液漏斗中分液,得到上层为四氢呋喃有机层,并用无水硫酸钠将四氢呋喃有机层干燥,用旋转蒸发仪除去四氢呋喃溶剂,即可得到反应中间产物—金属铱二聚体配合物;
(2)对于非对称ir(c1^n)(c2^n)(acac)型电致磷光材料:将含香豆素骨架有机配体与2-苯基喹啉以及水合三氯化铱按照物质的量1:1:1的比例投入反应容器中,在氮气氛围下,向所述反应容器中再加入可将反应物完全溶解的四氢呋喃与水的混合溶剂,混合溶剂中四氢呋喃与水的体积比为(2-5):1,氮气氛围中加热至100℃至110℃,搅拌16小时后冷至室温;将反应混合液转移至分液漏斗中分液,得到上层为四氢呋喃有机层,并用无水硫酸钠将四氢呋喃有机层干燥,用旋转蒸发仪除去四氢呋喃溶剂,即可得到反应中间产物—金属铱二聚体配合物;
第三步:含有香豆素骨架的有机金属铱配合物磷光材料的合成:
直接将金属铱二聚体配合物与乙酰丙酮铊完全溶解于二氯甲烷中,金属铱二聚体配合物与乙酰丙酮铊按照物质的量比例为1:(2-3),氮气氛围中室温搅拌16小时,所得的反应溶液浓缩得到粗产品,然后将其在层析硅胶柱或自制薄层硅胶色谱板上纯化,得到最终产品即有机金属铱配合物发光材料,分别为:式irc5、irc7、airc7、irc8、airc5、airc6out、airc6in、airc7out、airc7in、airc8的结构:
本发明的优点:通过将香豆素骨架引入到传统的2-苯基吡啶类配体中,利用香豆素骨架结构高度刚性,简单,易于合成,强的发光特性等特点,通过控制取代位置的变化以及采用非对称结构类型同时实现对所得铱配合物发光波长和发光效率的双重调控。
附图说明
图1为本发明中含香豆素骨架的有机金属铱配合物磷光材料实施例一至十所需配体的合成路线。
图2为本发明中含香豆素骨架的有机金属铱配合物磷光材料实施例一至四配合物的合成路线。
图3为本发明中含香豆素骨架的有机金属铱配合物磷光材料实施例五至十配合物的合成路线。
图4为本发明实施例一所制备的有机金属铱配合物irc5在二氯甲烷溶液中的室温紫外吸收光谱图。
图5为本发明实施例二所制备的有机金属铱配合物irc7在二氯甲烷溶液中的室温紫外吸收光谱图。
图6为本发明实施例三所制备的有机金属铱配合物airc7在二氯甲烷溶液中的室温紫外吸收光谱图。
图7为本发明实施例四所制备的有机金属铱配合物irc8在二氯甲烷溶液中的室温紫外吸收光谱图。
图8为本发明实施例五所制备的有机金属铱配合物airc5在二氯甲烷溶液中的室温紫外吸收光谱图。
图9为本发明实施例六所制备的有机金属铱配合物airc6out在二氯甲烷溶液中的室温紫外吸收光谱图。
图10为本发明实施例七所制备的有机金属铱配合物airc6in在二氯甲烷溶液中的室温紫外吸收光谱图。
图11为本发明实施例八所制备的有机金属铱配合物airc7out在二氯甲烷溶液中的室温紫外吸收光谱图。
图12为本发明实施例九所制备的有机金属铱配合物airc7in在二氯甲烷溶液中的室温紫外吸收光谱图。
图13为本发明实施例十所制备的有机金属铱配合物airc8在二氯甲烷溶液中的室温紫外吸收光谱图。
图14为本发明实施例一所制备的有机金属铱配合物irc5在二氯甲烷溶液中的室温光致发光光谱图。
图15为本发明实施例二所制备的有机金属铱配合物irc7在二氯甲烷溶液中的室温光致发光光谱图。
图16为本发明实施例三所制备的有机金属铱配合物airc7在二氯甲烷溶液中的室温光致发光光谱图。
图17为本发明实施例四所制备的有机金属铱配合物irc8在二氯甲烷溶液中的室温光致发光光谱图。
图18为本发明实施例五所制备的有机金属铱配合物airc5在二氯甲烷溶液中的室温光致发光光谱图。
图19为本发明实施例六所制备的有机金属铱配合物airc6out在二氯甲烷溶液中的室温光致发光光谱图。
图20为本发明实施例七所制备的有机金属铱配合物airc6in在二氯甲烷溶液中的室温光致发光光谱图。
图21为本发明实施例八所制备的有机金属铱配合物airc7out在二氯甲烷溶液中的室温光致发光光谱图。
图22为本发明实施例九所制备的有机金属铱配合物airc7in在二氯甲烷溶液中的室温光致发光光谱图。
图23为本发明实施例十所制备的有机金属铱配合物airc8在二氯甲烷溶液中的室温光致发光光谱图。
具体实施方式
下面结合附图以及具体实施方式对本发明做详细叙述。
实施例一
含香豆素骨架的红色磷光有机电致发光材料irc5,化学式为:c33h23irn2o6,分子结构式为:
参照附图1和附图2,其具体操作过程如下:
步骤一
(1)称取5.2gdl-苹果酸(38.78mmol)于schlenk反应管,n2氛围下,加入10g间溴苯酚(58.17mmol),冰浴搅拌下滴加13ml质量分数98%的浓硫酸,120℃搅拌反应6h。反应完后冷却至室温,将反应液缓慢滴入搅拌的饱和食盐水中,过滤得固体,将其重新溶于二氯甲烷中,水洗3次,有机相用无水硫酸钠干燥,浓缩。用硅胶柱色谱分离纯化,流动相为石油醚/二氯甲烷=3/2。最终获得br-c5和br-c7均为白的固体,分别为1.60g,5.66g。
br-c5产率:18.4%;1hnmr(400mhz,cdcl3,δ):8.07(d,j=10.0hz,1h),7.51(dd,j=8.0,1.2hz,1h),7.38(t,j=8.2hz,1h),7.29(d,j=8.4hz,1h),6.49(d,j=10.0hz);13cnmr(100mhz,cdcl3,δ):159.95,154.72,142.19,132.19,128.46,122.33,118.81,117.73,116.47.
br-c7产率:64.8%;1hnmr(400mhz,cdcl3,δ):7.67(d,j=9.6hz,1h),7.52(d,j=1.6hz,1h),7.42(dd,j=8.2,2.0hz,1h),7.35(d,j=8.0hz,1h),6.44(d,j=9.6hz);13cnmr(100mhz,cdcl3,δ):159.87,154.28,142.69,128.74,127.87,125.79,120.22,117.73,116.90.
(2)称取1.5g的br-c5(6.67mmol),0.23g的pd(pph3)4(0.20mmol)于schlenk反应管,n2氛围下,加入35ml甲苯,滴加2.94g三正丁基2-吡啶锡(8.00mmol),110℃搅拌反应16h。反应结束后冷却至室温,减压旋蒸除去溶剂。用硅胶柱色谱分离纯化,流动相为二氯甲烷。最终获得l-c5为白色固体1.26g(产率:84.8%)。
1hnmr(400mhz,cdcl3,δ):8.76(dd,j=4.8,0.8hz,1h),8.20(d,j=10.0hz,1h),7.86(td,j=7.8hz,1h),7.60(t,j=7.8hz,1h),7.56(d,j=8.0hz,1h),7.42(d,j=2.4hz,1h),7.40(d,j=3.2hz,1h),7.37(ddd,j=7.6,4.8,1.2hz,1h),6.42(d,j=9.6hz,1h).13cnmr(100mhz,cdcl3,δ):160.48,156.81,154.89,149.52,144.15,141.98,139.34,137.11,131.31,125.56,124.52,122.75,117.32,116.62.
步骤二
(1)称取0.25gl-c5(1.12mmol),0.18g水合三氯化铱(0.56mmol)于schlenk反应管,n2氛围下,加入30ml的thf和水的混合溶剂(v/v,3/1),110℃搅拌反应16h。待反应体系冷却到室温后,二氯甲烷萃取3次,合并有机相并用无水硫酸钠干燥,减压旋蒸除去大部分溶剂,石油醚沉析获得氯桥二聚体固体0.35g,产率93.5%。
步骤三
在schlenk反应管中加入0.35g二聚体(0.26mmol)和0.17g乙酰丙酮铊(0.57mmol),n2氛围下,加入30ml无水二氯甲烷,室温搅拌反应16h。离心除去不溶物,上清液用旋转蒸发仪除去溶剂,用薄层色谱分离纯化,展开剂为二氯甲烷/乙酸乙酯=30/1。最终得红色固体0.24g,产率63.7%。
1hnmr(400mhz,cdcl3,δ):8.67(dd,j=5.6,0.8hz,2h),8.53(d,j=10.0hz,2h),8.06(d,j=8.4hz,2h),7.88(td,j=8.0,1.6hz,2h),7.28(m,2h),6.72(d,j=8.4hz,2h),6.43(d,j=10.0hz,2h),6.23(d,j=8.4hz,2h),5.27(s,1h),1.81(s,6h).13cnmr(100mhz,cdcl3,δ):185.15,167.13,160.50,151.75,149.14,145.45,140.48,139.25,137.46,136.11,122.80,122.42,117.37,116.62,115.93,100.76,28.68.
图4包含本实施例最终合成出来含香豆素骨架的有机金属铱配合物磷光材料irc5在二氯甲烷中的紫外吸收光谱图。
图14包含本实施例最终合成出来含香豆素骨架的有机金属铱配合物磷光材料irc5在二氯甲烷中的光致发光光谱图。
实施例二
含香豆素骨架的红色磷光有机电致发光材料irc7,化学式为:c33h23irn2o6,分子结构式为:
参照附图1和附图2,其具体操作过程如下:
步骤一
(1)该实施例最终合成出的含香豆素骨架的有机金属铱配合物磷光材料与实施例一共用实施例一中的步骤一(1)的反应过程,由于实施例一中步骤一(1)可同时获得br-c5和br-c7两种产物,因此该实施例中的具体操作过程中的步骤一(1)在此省略,直接列出操作过程中步骤一(2),但并不表示该实施例中所示的含香豆素骨架的有机金属铱配合物磷光材料的操作过程中不包括上述步骤一(1)。
(2)称取2.00g的br-c7(8.89mmol),0.31g的pd(pph3)4(0.27mmol)于schlenk反应管,n2氛围下,加入40ml甲苯,滴加3.92g三正丁基2-吡啶锡(10.67mmol),110℃搅拌反应16h。反应结束后冷却至室温,减压旋蒸除去溶剂。用硅胶柱色谱分离纯化,流动相为二氯甲烷。最终获得l-c7为白色固体1.66g(产率:83.7%)。
1hnmr(400mhz,cdcl3,δ):8.74(dd,j=4.8,0.8hz,1h),7.98(dd,j=8.0,1.6hz,1h),7.95(s,1h),7.81(m,2h),7.75(d,j=9.2hz,1h),7.58(d,j=8.0hz,1h),7.31(m,1h),6.46(dd,j=9.4,1.4hz,1h).13cnmr(100mhz,cdcl3,δ):160.80,155.28,154.46,150.00,142.99,142.94,137.04,128.14,123.19,122.96,120.92,119.10,116.94,115.00.
步骤二
由于配体l-c7的不对称型和存在两个碳配位螯合位点与铱离子配位形成碳金属键(c-m),所以当用配体l-c7与金属铱离子反应合成二聚体时,将产生几种二聚体的混合物,而下图所给出的二聚体分子式仅是考虑到此实施例子最终获得irc7所需要的二聚体结构。
(1)称取0.44gl-c7(1.96mmol),0.32g水合三氯化铱(0.98mmol)于schlenk反应管,n2氛围下,加入40ml的thf和水的混合溶剂(v/v,3/1),110℃搅拌反应16h。待反应体系冷却到室温后,二氯甲烷萃取3次,合并有机相并用无水硫酸钠干燥,减压旋蒸除去大部分溶剂,石油醚沉析获得氯桥二聚体固体0.62g,产率94.1%。
步骤三
在schlenk反应管中加入0.62g二聚体(0.46mmol)和0.31g乙酰丙酮铊(1.01mmol),n2氛围下,加入50ml无水二氯甲烷,室温搅拌反应16h。离心除去不溶物,上清液用旋转蒸发仪除去溶剂,用薄层色谱分离纯化,展开剂为二氯甲烷/乙酸乙酯=50/1。最终得红色固体0.22g,产率32.3%。
1hnmr(400mhz,cdcl3,δ):8.55(d,j=5.2hz,2h),7.96(d,j=8.0hz,2h),7.90(td,j=7.6,1.2hz,2h),7.55(s,2h),7.31(m,2h),7.30(d,j=9.6hz,2h),6.23(s,2h),6.20(d,j=9.6hz,2h),5.27(s,1h),1.81(s,6h).13cnmr(100mhz,cdcl3,δ):185.09,166.70,161.30,150.65,148.67,148.53,143.57,139.52,137.63,130.72,123.28,119.97,119.78,116.25,111.55,100.81,28.74.
图5包含本实施例最终合成出来含香豆素骨架的有机金属铱配合物磷光材料irc7在二氯甲烷中的紫外吸收光谱图。
图15包含本实施例最终合成出来含香豆素骨架的有机金属铱配合物磷光材料irc7在二氯甲烷中的光致发光光谱图。
实施例三
含香豆素骨架的橙色磷光有机电致发光材料airc7,化学式为:c33h23irn2o6,分子结构式为:
参照附图1和附图2,其具体操作过程如下:
该实施例所最终合成出的含香豆素骨架的有机金属铱配合物磷光材料与实施例二共用实施例二中的步骤一的反应过程,由于实施例三与实施例二是l-c7与水合三氯化铱反应所产生的两个配位异构体,因此该例中的具体操作过程中的步骤一在此省略,直接列出操作过程中步骤二,但并不表示该例中所示的含香豆素骨架的有机金属铱配合物磷光材料的操作过程中不包括上述步骤一。
步骤二
(1)由于配体l-c7的不对称型和存在两个碳配位螯合位点与铱离子配位形成碳金属键(c-m),所以当用配体l-c7与金属铱离子反应合成二聚体时,将产生几种二聚体的混合物,而下图所给出的二聚体分子式仅是考虑到此实施例子最终获得airc7所需要的二聚体结构。
称取0.44gl-c7(1.96mmol),0.32g水合三氯化铱(0.98mmol)于schlenk反应管,n2氛围下,加入40ml的thf和水的混合溶剂(v/v,3/1),110℃搅拌反应16h。待反应体系冷却到室温后,二氯甲烷萃取3次,合并有机相并用无水硫酸钠干燥,减压旋蒸除去大部分溶剂,石油醚沉析获得氯桥二聚体固体0.62g,产率94.1%。
步骤三
在schlenk反应管中加入0.62g二聚体(0.46mmol)和0.31g乙酰丙酮铊(1.01mmol),n2氛围下,加入50ml无水二氯甲烷,室温搅拌反应16h。离心除去不溶物,上清液用旋转蒸发仪除去溶剂,用薄层色谱分离纯化。展开剂为二氯甲烷/乙酸乙酯=50/1,最终得橙色固体0.21g,产率30.8%。
1hnmr(400mhz,cdcl3,δ):8.53(d,j=5.6hz,1h),8.51(d,j=6.0hz,1h),8.00(d,j=8.4hz,1h),7.91(dd,j=6.4,1.6hz,2h),7.86(td,j=7.8,1.6hz,1h),7.61(d,j=8.0hz,1h),7.54(s,1h),7.39(d,j=9.6hz,1h),7.31-7.23(m,3h),6.99(d,j=8.0hz,1h),6.16(d,j=9.6hz,1h),6.11(s,1h),6.03(d,j=9.6hz,1h),5.29(s,1h),1.81(s,3h),1.78(s,3h).13cnmr(100mhz,cdcl3,δ):185.08,184.55,167.74,165.79,161.52,161.42,160.89,150.95,150.38,149.66,149.21,148.42,143.63,143.30,137.70,137.34,136.85,133.54,130.49,123.10,122.54,121.56,120.11,119.74,119.15,119.02,116.56,115.61,110.95,100.78,28.68.
图6包含本实施例最终合成出来含香豆素骨架的有机金属铱配合物磷光材料airc7在二氯甲烷中的紫外吸收光谱图。
图16包含本实施例最终合成出来含香豆素骨架的有机金属铱配合物磷光材料airc7在二氯甲烷中的光致发光光谱图。
实施例四
含香豆素骨架的绿色磷光有机电致发光材料irc8,化学式为:c33h23irn2o6,分子结构式为:
参照附图1和附图2,其具体操作过程如下:
步骤一
(1)加入80ml乙腈于250ml单口瓶,加入3.17g邻溴苯酚(18.32mmol),随后加入7.4g多聚甲醛,2.62gmgcl2(27.53mmol),6.4ml三乙胺(46.04mmol),回流反应8h。反应结束后冷去至室温,过滤除去不溶物,二氯甲烷洗涤滤饼,滤液浓缩。用硅胶柱色谱分离纯化,流动相为石油醚/二氯甲烷=1/5。最终获得ba为淡黄色固体3.24g,产率为87.9%。
1hnmr(400mhz,cdcl3,δ):11.61(s,1h),9.85(d,j=2.0hz,1h),7.78(dd,j=7.6,1.6hz,1h),7.55(dd,j=7.8,1.6hz,1h),6.94(td,j=7.8,2.0hz,1h).13cnmr(100mhz,cdcl3,δ):195.99,158.03,139.94,132.90,121.26,120.76,111.15.
(2)称取6.37gba(31.69mmol),1.85g醋酸钾(18.85mmol)于schlenk反应管,n2氛围下,加入26ml醋酸酐。170℃搅拌回流反应6h。反应结束后冷却至室温,加水稀释,搅拌状态下缓慢加碳酸钠水溶液直至溶液呈中性,二氯甲烷萃取中和后的液体,合并所有的有机相,无水硫酸钠干燥,减压旋蒸除去溶剂。用硅胶柱色谱分离纯化,流动相为石油醚/乙酸乙酯=10/1。最终获得br-c8为白色固体5.08g,产率为72.4%。
1hnmr(400mhz,cdcl3,δ):7.75(d,j=8.0hz,1h),7.68(d,j=9.2hz,1h),7.44(dd,j=7.6,1.2hz,1h),7.16(t,j=7.8hz,1h),6.45(d,j=9.6hz,1h).13cnmr(100mhz,cdcl3,δ):159.60,150.74,143.09,135.33,127.11,125.12,120.08,117.32,110.41.
(3)称取1.8g的br-c8(8.89mmol),0.28g的pd(pph3)4(0.24mmol)于schlenk反应管,n2氛围下,加入35ml甲苯,滴加3.53g三正丁基2-吡啶锡(9.60mmol),110℃搅拌反应16h。反应结束后冷却至室温,减压旋蒸除去溶剂。用硅胶柱色谱分离纯化,流动相为二氯甲烷。最终获得l-c8为白色固体1.49g,产率为83.2%。
1hnmr(400mhz,cdcl3,δ):8.75(dd,j=4.8,0.8hz,1h),8.11(dd,j=8.0,1.6hz,1h),8.03(d,j=8.0hz,1h),7.83(td,j=7.8,1.6hz,1h),7.79(d,j=9.6hz,1h),7.54(dd,j=7.6,1.6hz,1h),7.41(t,j=7.6hz,1h),7.31(ddd,j=7.6,4.8,0.8hz,1h),6.47(d,j=9.6hz,1h).13cnmr(100mhz,cdcl3,δ):160.27,157.04,153.06,151.24,149.81,143.97,136.45,133.66,128.57,125.39,124.56,122.78,119.21,116.43.
步骤二
(1)称取0.21gl-c7(0.94mmol),0.15g水合三氯化铱(0.47mmol)于schlenk反应管,n2氛围下,加入30ml的thf和水的混合溶剂(v/v,3/1),110℃搅拌反应16h。待反应体系冷却到室温后,二氯甲烷萃取3次,合并有机相并用无水硫酸钠干燥,减压旋蒸除去大部分溶剂,石油醚沉析获得氯桥二聚体固体0.29g,产率92.8%。
步骤三
在schlenk反应管中加入0.29g二聚体(0.22mmol)和0.14g乙酰丙酮铊(0.47mmol),n2氛围下,加入30ml无水二氯甲烷,室温搅拌反应16h。离心除去不溶物,上清液用旋转蒸发仪除去溶剂,用薄层色谱分离纯化。展开剂为二氯甲烷/乙酸乙酯=30/1,最终得黄色固体0.20g,产率62.3%。
1hnmr(400mhz,cdcl3,δ):9.12(d,j=8.4hz,2h),8.53(dd,j=5.6hz,2h),7.94(td,j=8.0,1.6hz,2h),7.54(d,j=9.6hz,2h),7.28(m,2h),6.75(d,j=8.0hz,2h),6.23(d,j=1.6hz,2h),6.21(s,2h),5.27(s,1h),1.81(s,6h).13cnmr(100mhz,cdcl3,δ):185.17,165.33,160.88,159.60,151.79,148.10,145.38,138.27,132.20,129.54,127.97,124.82,122.32,113.74,111.34,100.71,28.67.
图7包含本实施例最终合成出来含香豆素骨架的有机金属铱配合物磷光材料irc8在二氯甲烷中的紫外吸收光谱图。
图17包含本实施例最终合成出来含香豆素骨架的有机金属铱配合物磷光材料irc8在二氯甲烷中的光致发光光谱图。
实施例五
含香豆素骨架的红色磷光有机电致发光材料airc5,化学式为:c34h25irn2o6,分子结构式为:
参照附图1和附图3,其具体操作过程如下:
该实施例所最终合成出的含香豆素骨架的有机金属铱配合物磷光材料与实施例一共用实施例一中的步骤一的反应过程,由于实施例五所使用的配体之一与实施例一所使用的配体均为l-c5,因此该实施例中的具体操作过程中的步骤一在此省略,直接列出操作过程中步骤二,但并不表示该实施例中所示的含香豆素骨架的有机金属铱配合物磷光材料的操作过程中不包括上述步骤一。
步骤二
(2)称取0.18g2-苯基喹啉(0.88mmol),0.20gl-c5(0.89mmol),0.28g水合三氯化铱(铱含量60%)(0.88mmol)于schlenk反应管,n2氛围下,加入35mlthf和水的混合溶剂(v/v=3/1),110℃搅拌反应16h。待反应体系冷却到室温后,二氯甲烷萃取3次,合并有机相并用无水硫酸钠干燥,减压旋蒸除去大部分溶剂,石油醚沉析获得氯桥二聚体固体0.53g,产率为92.6%。
步骤三
在schlenk反应管中加入0.53g二聚体(0.41mmol)和0.27g乙酰丙酮铊(0.89mmol),n2氛围下,加入40ml无水二氯甲烷,室温搅拌反应16h。离心除去不溶物,上清液用旋转蒸发仪除去溶剂,用薄层色谱分离纯化。展开剂为二氯甲烷/乙酸乙酯=30/1,最终得红色固体0.19mg,产率33.4%。
1hnmr(400mhz,cdcl3,δ):8.62(d,j=10.0hz,1h),8.59(m,1h),8.48(dd,j=6.0,1.2hz,1h),8.18(d,j=8.8hz,1h),8.12(d,j=8.4hz,1h),8.02(d,j=8.4hz,1h),7.89–7.83(m,2h),7.75(d,j=7.6hz,1h),7.56–7.52(m,2h),7.22(td,j=6.6,1.2hz,1h),6.94(td,j=7.2,1.2hz,1h),6.77(d,j=8.4hz,1h),6.71(td,j=7.6,1.2hz,1h),6.65(d,j=8.4hz,1h),6.45(d,j=10.0hz,1h),6.05(d,j=7.6hz,1h),4.95(s,1h),1.71(s,3h),1.59(s,3h).13cnmr(100mhz,cdcl3,δ):185.68,185.13,169.48,167.83,160.73,151.60,150.20,149.85,149.18,146.65,146.54,140.74,139.45,139.42,137.95,137.37,132.95,130.66,128.91,128.01,127.18,126.16,126.12,125.84,122.28,122.12,121.52,117.16,116.79,116.76,115.63,100.49,28.55,28.27.
图8包含本实施例最终合成出来含香豆素骨架的有机金属铱配合物磷光材料airc5在二氯甲烷中的紫外吸收光谱图。
图18包含本实施例最终合成出来含香豆素骨架的有机金属铱配合物磷光材料airc5在二氯甲烷中的光致发光光谱图。
实施例六
含香豆素骨架的橙色磷光有机电致发光材料airc6out,化学式为:c34h25irn2o6,分子结构式为:
参照附图1和附图3,其具体操作过程如下:
步骤一
(1)加入120ml1,2-二氯乙烷于250ml三口瓶,紧接着滴入丙烯酸甲酯5.2ml(57.80mmol),再加入5g对溴苯酚(28.90mmol),3.56g醋酸钠(43.35mmol),2.89g醋酸铜(14.45mmol),0.49g的1,10-菲啰啉(2.89mmol),0.32g醋酸钯(1.45mmol)和适量分子筛,110℃搅拌回流反应20h。反应完后冷却至室温,过滤除去不溶杂质,二氯甲烷洗涤滤饼,滤液减压旋蒸除去溶剂。用硅胶柱色谱分离纯化,流动相为石油醚/乙酸乙酯=30/1。最终获得橙色固体4.14g,产率为63.7%。
1hnmr(400mhz,cdcl3,δ):7.65–7.60(m,3h),7.22(d,j=9.2hz,1h),6.46(d,j=9.6hz,1h).13cnmr(100mhz,cdcl3,δ):160.13,153.17,143.20,134.75,130.33,120.51,118.89,118.06,117.17.
(2)称取2.1g的br-c8(9.33mmol),0.32g的pd(pph3)4(0.28mmol)于schlenk反应管,n2氛围下,加入35ml甲苯,滴加4.12g三正丁基2-吡啶锡(11.20mmol),110℃搅拌反应16h。反应结束后冷却至室温,减压旋蒸除去溶剂。用硅胶柱色谱分离纯化,流动相为二氯甲烷。最终获得l-c6为白色固体1.73g,产率为83.1%。
1hnmr(400mhz,cdcl3,δ):8.71(d,j=4.8hz,1h),8.19(d,j=2.4hz,1h),8.14(dd,j=8.4hz,1h),7.81(d,j=9.2hz,1h),7.79(dd,j=7.2,1.6hz,1h),7.75(d,j=8.0hz,1h),7.43(d,j=8.4hz,1h),7.30–7.27(m,1h),6.47(d,j=9.6hz,1h).13cnmr(100mhz,cdcl3,δ):160.59,155.50,154.50,149.87,143.58,137.05,135.84,130.19,126.32,122.57,120.25,119.06,117.23,117.08.
步骤二
由于配体l-c6的不对称型和存在两个碳配位螯合位点与铱离子配位形成碳金属键(c-m),所以当用配体l-c6与金属铱离子反应合成二聚体时,将产生几种二聚体的混合物,而下图所给出的二聚体分子式仅是考虑到此实施例子最终获得airc6out所需要的二聚体结构。
(2)称取0.40g2-苯基喹啉(1.95mmol),0.44gl-c6(1.95mmol),0.62g水合三氯化铱(铱含量60%)(1.95mmol)于schlenk反应管,n2氛围下,加入50mlthf和水的混合溶剂(v/v=3/1),110℃搅拌反应16h。待反应体系冷却到室温后,二氯甲烷萃取3次,合并有机相并用无水硫酸钠干燥,减压旋蒸除去大部分溶剂,石油醚沉析获得氯桥二聚体固体1.18g,产率为92.9%。
步骤三
在schlenk反应管中加入1.18g二聚体(0.90mmol)和0.60g乙酰丙酮铊(1.98mmol),n2氛围下,加入50ml无水二氯甲烷,室温搅拌反应16h。离心除去不溶物,上清液用旋转蒸发仪除去溶剂,用薄层色谱分离纯化。展开剂为二氯甲烷/乙酸乙酯=60/1,最终得橙色固体0.24mg,产率18.5%。
1hnmr(400mhz,cdcl3,δ):8.23–8.20(m,2h),8.18(d,j=8.8hz,1h),8.08(d,j=8.8hz,1h),7.93(d,j=8.4hz,1h),7.88(d,j=8.8hz,1h),7.85–7.79(m,3h),7.50(td,j=7.2,1.2hz,1h),7.45(td,j=7.8,1.6hz,1h),7.07(td,j=6.6,1.2hz,1h),7.04–7.00(m,2h),6.77(td,j=7.2,1.2hz,1h),6.63(d,j=9.6hz,1h),6.34(d,j=7.2hz,1h),5.37(d,j=9.6hz,1h),4.77(s,1h),1.60(s,3h),1.48(s,3h).13cnmr(100mhz,cdcl3,δ):185.71,184.75,169.27,167.73,161.74,155.24,153.55,149.48,149.20,148.20,147.86,146.56,143.50,138.12,137.69,134.56,130.70,128.88,127.95,127.48,126.55,126.45,126.37,126.25,126.11,121.90,121.10,118.39,117.09,112.75,110.74,100.08,28.46,27.93.
图9包含本实施例最终合成出来含香豆素骨架的有机金属铱配合物磷光材料airc6out在二氯甲烷中的紫外吸收光谱图。
图19包含本实施例最终合成出来含香豆素骨架的有机金属铱配合物磷光材料airc6out在二氯甲烷中的光致发光光谱图。
实施例七
含香豆素骨架的红色磷光有机电致发光材料airc6in,化学式为c34h25irn2o6,分子结构式为:
参照附图1和附图3,其具体操作过程如下:
该实施例所最终合成出的含香豆素骨架的有机金属铱配合物磷光材料与实施例六共用实施例六中的步骤一的反应过程,由于实施例七与实施例六是由于l-c6与水合三氯化铱反应存在不同配位方式,所以产生了两个配位异构体,因此该实施例中的具体操作过程中的步骤一在此省略,直接列出操作过程中步骤二,但并不表示该实施例中所示的含香豆素骨架的有机金属铱配合物磷光材料的操作过程中不包括上述步骤一。
步骤二
由于配体l-c6的不对称型和存在两个碳配位螯合位点与铱离子配位形成碳金属键(c-m),所以当用配体l-c6与金属铱离子反应合成二聚体时,将产生几种二聚体的混合物,而下图所给出的二聚体分子式仅是考虑到此实施例子最终获得airc6in所需要的二聚体结构。
(2)称取0.40g2-苯基喹啉(1.95mmol),0.44gl-c6(1.95mmol),0.62g水合三氯化铱(铱含量60%)(1.95mmol)于schlenk反应管,n2氛围下,加入50mlthf和水的混合溶剂(v/v=3/1),110℃搅拌反应16h。待反应体系冷却到室温后,二氯甲烷萃取3次,合并有机相并用无水硫酸钠干燥,减压旋蒸除去大部分溶剂,石油醚沉析获得氯桥二聚体固体1.18g,产率为92.9%。
步骤三
在schlenk反应管中加入1.18g二聚体(0.90mmol)和0.60g乙酰丙酮铊(1.98mmol),n2氛围下,加入50ml无水二氯甲烷,室温搅拌反应16h。离心除去不溶物,上清液用旋转蒸发仪除去溶剂,用薄层色谱分离纯化。展开剂为二氯甲烷/乙酸乙酯=60/1,最终得红色固体0.25mg,产率19.4%。
1hnmr(400mhz,cdcl3,δ):8.69–8.66(m,1h),8.38(d,j=4.8hz,1h),8.20(d,j=8.8hz,1h),8.02(d,j=8.8hz,1h),7.96(d,j=8.0hz,1h),7.87–7.83(m,2h),7.75(d,j=7.2hz,1h),7.71(s,1h),7.59(d,j=9.6hz,1h),7.57–7.53(m,2h),7.22(td,j=6.6,1.2hz,1h),6.94(td,j=7.2,1.2hz,1h),6.72(td,j=7.2,1.2hz,1h),6.50(s,1h),6.18(d,j=7.2hz,1h),6.12(d,j=9.6hz,1h),4.98(s,1h),1.72(s,3h),1.61(s,3h).13cnmr(100mhz,cdcl3,δ):185.78,185.00,169.52,166.86,161.52,157.13,154.11,149.32,149.19,148.82,146.55,144.38,143.07,138.19,137.55,132.63,130.88,128.90,128.10,127.36,126.28,126.18,125.83,123.15,122.34,122.20,121.77,118.51,116.71,113.19,111.85,100.60,28.56,28.31.
图10包含本实施例最终合成出来含香豆素骨架的有机金属铱配合物磷光材料airc6in在二氯甲烷中的紫外吸收光谱图。
图20包含本实施例最终合成出来含香豆素骨架的有机金属铱配合物磷光材料airc6in在二氯甲烷中的光致发光光谱图。
实施例八
含香豆素骨架的橙色磷光有机电致发光材料airc7out,化学式为c34h25irn2o6,分子结构式为:
参照附图1和附图3,其具体操作过程如下:
该实施例所最终合成出的含香豆素骨架的有机金属铱配合物磷光材料与实施例二共用实施例二中的步骤一的反应过程,由于实施例八所使用的配体之一与实施例二所使用的配体均为l-c7,因此该例中的具体操作过程中的步骤一在此省略,直接列出操作过程中步骤二,但并不表示该实施例中所示的含香豆素骨架的有机金属铱配合物磷光材料的操作过程中不包括上述步骤一。
步骤二
由于配体l-c7的不对称型和存在两个碳配位螯合位点与铱离子配位形成碳金属键(c-m),所以当用配体l-c7与金属铱离子反应合成二聚体时,将产生几种二聚体的混合物,而下图所给出的二聚体分子式仅是考虑到此实施例子最终获得airc7out所需要的二聚体结构。
(2)称取0.44g2-苯基喹啉(2.14mmol),0.48gl-c7(2.14mmol),0.68g水合三氯化铱(铱含量60%)(2.14mmol)于schlenk反应管,n2氛围下,加入50mlthf和水的混合溶剂(v/v=3/1),110℃搅拌反应16h。待反应体系冷却到室温后,二氯甲烷萃取3次,合并有机相并用无水硫酸钠干燥,减压旋蒸除去大部分溶剂,石油醚沉析获得氯桥二聚体固体1.31g,产率为93.4%。
步骤三
在schlenk反应管中加入1.31g二聚体(0.90mmol)和0.67g乙酰丙酮铊(2.21mmol),n2氛围下,加入60ml无水二氯甲烷,室温搅拌反应16h。离心除去不溶物,上清液用旋转蒸发仪除去溶剂,用薄层色谱分离纯化。展开剂为二氯甲烷/乙酸乙酯=60/1,最终得橙色固体0.27mg,产率18.7%。
1hnmr(400mhz,cdcl3,δ):8.68–8.66(m,1h),8.40(d,j=5.2hz,1h),8.19(d,j=8.8hz,1h),8.03(d,j=8.8hz,1h),8.00(d,j=8.0hz,1h),7.89(dd,j=7.2,1.6hz,1h),7.88–7.84(m,1h),7.76(d,j=7.6hz,1h),7.64(s,1h),7.57–7.52(m,2h),7.24(td,j=7.2,1.2hz,1h),7.18(d,j=9.6hz,1h),6.94(td,j=7.6,0.8hz,1h),6.73(td,j=7.2,1.2hz,1h),6.59(s,1h),6.21(d,j=7.2hz,1h),6.13(d,j=9.6hz,1h),4.95(s,1h),1.70(s,3h),1.58(s,3h).13cnmr(100mhz,cdcl3,δ):185.57,185.12,169.80,167.14,161.49,150.56,150.45,149.44,149.36,149.03,146.52,143.74,139.80,137.87,137.60,133.74,132.98,130.64,128.97,128.00,127.17,126.42,126.08,125.81,123.09,121.46,119.73,119.60,116.76,116.00,111.55,100.50,28.56,28.28.
图11包含本实施例最终合成出来含香豆素骨架的有机金属铱配合物磷光材料airc7out在二氯甲烷中的紫外吸收光谱图。
图21包含本实施例最终合成出来含香豆素骨架的有机金属铱配合物磷光材料airc7out在二氯甲烷中的光致发光光谱图。
实施例九
含香豆素骨架的橙色磷光有机电致发光材料airc7in,化学式为c34h25irn2o6,分子结构式为:
参照附图1和附图3,其具体操作过程如下:
该实施例所最终合成出的含香豆素骨架的有机金属铱配合物磷光材料与实施例八共用实施例八中的步骤一的反应过程,由于实施例九与实施例八是由于l-c7与水合三氯化铱反应存在不同配位方式,所以产生了两个配位异构体,因此该实施例中的具体操作过程中的步骤一在此省略,直接列出操作过程中步骤二,但并不表示该实施例中所示的含香豆素骨架的有机金属铱配合物磷光材料的操作过程中不包括上述步骤一。
步骤二
由于配体l-c7的不对称型和存在两个碳配位螯合位点与铱离子配位形成碳金属键(c-m),所以当用配体l-c7与金属铱离子反应合成二聚体时,将产生几种二聚体的混合物,而下图所给出的二聚体分子式仅是考虑到此实施例最终获得airc7in所需要的二聚体结构。
(2)称取0.44g2-苯基喹啉(2.14mmol),0.48gl-c7(2.14mmol),0.68g水合三氯化铱(铱含量60%)(2.14mmol)于schlenk反应管,n2氛围下,加入50mlthf和水的混合溶剂(v/v=3/1),110℃搅拌反应16h。待反应体系冷却到室温后,二氯甲烷萃取3次,合并有机相并用无水硫酸钠干燥,减压旋蒸除去大部分溶剂,石油醚沉析获得氯桥二聚体固体1.31g,产率为93.4%。
步骤三
在schlenk反应管中加入1.31g二聚体(0.90mmol)和0.67g乙酰丙酮铊(2.21mmol),n2氛围下,加入60ml无水二氯甲烷,室温搅拌反应16h。离心除去不溶物,上清液用旋转蒸发仪除去溶剂,用薄层色谱分离纯化。展开剂为二氯甲烷/乙酸乙酯=60/1,最终得橙色固体0.26mg,产率17.9%。
1hnmr(400mhz,cdcl3,δ):8.53(d,j=8.4hz,1h),8.40(d,j=4.8hz,1h),8.22(d,j=8.4hz,1h),8.03(d,j=8.8hz,1h),8.02(d,j=7.6hz,1h),7.87–7.83(m,2h),7.76(d,j=7.6hz,1h),7.66(d,j=8.0hz,1h),7.49–7.41(m,2h),7.33(d,j=9.2hz,1h),7.20(td,j=6.6,1.2hz,1h),7.00(d,j=8.0hz,1h),6.93(t,j=7.2hz,1h),6.69(td,j=7.2,0.8hz,1h),6.16(d,j=7.2hz,1h),5.81(d,j=9.2hz,1h),4.96(s,1h),1.70(s,3h),1.58(s,3h).13cnmr(100mhz,cdcl3,δ):185.14,185.12,168.29,168.02,161.08,160.89,150.90,150.25,148.85,147.65,147.56,143.03,137.77,137.36,134.69,132.87,129.53,128.16,127.58,127.57,127.14,125.51,125.36,122.38,121.40,121.19,120.17,119.35,118.71,116.57,116.48,100.54,28.58,28.26.
图12包含本实施例最终合成出来含香豆素骨架的有机金属铱配合物磷光材料airc7in在二氯甲烷中的紫外吸收光谱图。
图22包含本实施例最终合成出来含香豆素骨架的有机金属铱配合物磷光材料airc7in在二氯甲烷中的光致发光光谱图。
实施例十
含香豆素骨架的橙色磷光有机电致发光材料airc8,化学式为c34h25irn2o6,分子结构式为:
参照附图1和附图3,其具体操作过程如下:
该实施例所最终合成出的含香豆素骨架的有机金属铱配合物磷光材料与实施例四共用实施例四中的步骤一的反应过程,由于实施例十所使用的配体之一与实施例四所使用的配体均为l-c8,因此该实施例中的具体操作过程中的步骤一在此省略,直接列出操作过程中步骤二,但并不表示该例中所示的含香豆素骨架的有机金属铱配合物磷光材料的操作过程中不包括上述步骤一。
步骤二
(2)称取0.23g2-苯基喹啉(1.12mmol),0.25gl-c7(1.12mmol),0.36g水合三氯化铱(铱含量60%)(1.12mmol)于schlenk反应管,n2氛围下,加入50mlthf和水的混合溶剂(v/v=3/1),110℃搅拌反应16h。待反应体系冷却到室温后,二氯甲烷萃取3次,合并有机相并用无水硫酸钠干燥,减压旋蒸除去大部分溶剂,石油醚沉析获得氯桥二聚体固体0.67g,产率为92.6%。
步骤三
在schlenk反应管中加入0.67g二聚体(0.51mmol)和0.34g乙酰丙酮铊(1.12mmol),n2氛围下,加入60ml无水二氯甲烷,室温搅拌反应16h。离心除去不溶物,上清液用旋转蒸发仪除去溶剂,用薄层色谱分离纯化。展开剂为二氯甲烷/乙酸乙酯=30/1,最终得橙色固体0.25mg,产率33.7%。
1hnmr(400mhz,cdcl3,δ):9.17(d,j=8.4hz,1h),8.66–8.63(m,1h),8.41(d,j=4.8hz,1h),8.19(d,j=8.8hz,1h),8.02(d,j=8.8hz,1h),7.93(td,j=8.0,1.6hz,1h),7.86–7.84(m,1h),7.75(d,j=7.6hz,1h),7.56–7.53(m,3h),7.22(td,j=6.6,1.2hz,1h),6.95(t,j=7.2hz,1h),6.75(t,j=7.6hz,1h),6.62(q,j=7.4hz,2h),6.23(d,j=9.6hz,1h),6.20(d,j=7.6hz,1h),4.94(s,1h),1.70(s,3h),1.58(s,3h).13cnmr(100mhz,cdcl3,δ):185.76,185.04,169.48,165.80,161.60,161.20,152.14,149.69,149.22,148.55,146.40,145.53,138.16,137.95,133.05,132.74,132.59,130.58,129.01,127.97,127.53,127.18,126.39,126.10,125.75,124.37,122.10,121.74,116.83,113.22,110.70,100.46,28.55,28.66.
图13包含本实施例最终合成出来含香豆素骨架的有机金属铱配合物磷光材料airc8在二氯甲烷中的紫外吸收光谱图。
图23包含本实施例最终合成出来含香豆素骨架的有机金属铱配合物磷光材料airc8在二氯甲烷中的光致发光光谱图。
- 还没有人留言评论。精彩留言会获得点赞!