抗HSVgB单克隆抗体或其抗原结合片段的制作方法
本发明涉及抗hsvgb单克隆抗体或其抗原结合片段。
背景技术:
单纯疱疹病毒(herpessimplexvirus;hsv)为嗜神经性的病原体,在首次感染粘膜上皮后转移到感觉神经,在三叉神经节或骶神经节中终生潜伏感染。潜伏状态的hsv时而会激活而引起各种病情(非专利文献1)。
已知hsv存在2种血清型(hsv-1、hsv-2),hsv-1主要为口唇·角膜疱疹的病因,hsv-2主要为生殖器疱疹的病因。但是,近年由于性行为的多样化等,也存在hsv-1屡屡成为生殖器疱疹的病因、hsv-2屡屡成为口唇疱疹的病因的情况。日本的抗体阳性者(已感染者)比率在hsv-1的情况下为60~80%、hsv-2则为10%,即使仅限于hsv-2,推测疫苗的潜在需求也为1000万人(非专利文献2)。另外,美国的抗体阳性者(已感染者)比率在hsv-1的情况下为57%、hsv-2则为20%(其中约10%为明显的生殖器疱疹)(非专利文献3)。
已知在hsv对细胞建立感染中,在吸附和侵入这2个阶段中有5个包膜糖蛋白(glycoprotein)参与。这5个包膜糖蛋白分别被称为包膜糖蛋白b(gb)、包膜糖蛋白c(gc)、包膜糖蛋白d(gd)、包膜糖蛋白h(gh)、包膜糖蛋白l(gl)(非专利文献4)。
首先,gb及gc结合到细胞表面的硫酸乙酰肝素上这一点成为吸附过程的契机(非专利文献5、6)。该过程在hsv侵入细胞时并非必不可少,但是一般认为关系到更有效的侵入。接着,gb及gd与各自的宿主细胞受体结合,病毒包膜与宿主细胞膜融合,从而开始侵入过程。
作为宿主细胞受体,已知有gb受体和gd受体。作为gb受体,已鉴定出nm-iia(非专利文献7、8)及mag(非专利文献9)。作为gd受体,已鉴定出结合素1(非专利文献10)、hvem(非专利文献11)及3-o-硫酸化硫酸乙酰肝素(非专利文献12)。另外,已知gh/gl的杂二聚体与gb及gd相互作用而在膜融合中发挥重要的作用(非专利文献13)。
2006年破解了hsv-1gb的结构,结果获知,gb形成具有5个结构域的三聚体(非专利文献14)。另外,gb的结构采取与作为膜融合蛋白而已知的vsv(vesicularstomatitisvirus,疱疹性口炎病毒)的gg相似的结构,这一点支持gb为hsv的膜融合蛋白。另外,gb在其它疱疹病毒中也高度保守,可认为其功能在疱疹病毒中是相同的。
截至目前为止,为了确定hsvgb的功能性区域,有多个研究小组一直在使用gb的突变体、单克隆抗体进行该分析(非专利文献15~18)。其结果是,发现了几个功能性区域。
目前,在hsv的治疗中使用阿昔洛韦等抗病毒药,但不能彻底清除病毒,若停止服用则病毒会再次激活。这起因于hsv采取了在神经节中潜伏感染这一特殊的感染方式。因此,期望开发出防御hsv感染本身的预防用疫苗、或减轻·缓和感染症状·激活症状的治疗用疫苗,但是,目前不存在有效的疫苗,对其需求较高。
另外,担心通过高频度或长期使用阿昔洛韦、膦甲酸钠等抗病毒药而导致抗药病毒株增加(非专利文献19)。另外,这些抗病毒药有肝功能异常、精子产生能力下降、消化管障碍、肾功能异常等各种副作用,偶尔还可能发生不可避免的减少药量、停药的情况。
已知hsv为无法通过现有疫苗、病原体感染史获得充分的保护性免疫的病原体之一。一般认为,这是由于hsv具有各种免疫逃逸机制,巧妙地逃避了宿主的免疫反应。
现有技术文献
非专利文献
非专利文献1:roizman,b.等、herpessimplexviruses,p.2501-2602.ind.m.knipeandp.m.howley(ed.),“fieldsvirology”,5thed.lippincottwilliams&wilkins,philadelphia,p.a.2007
非专利文献2:hashidom1等、anepidemiologicstudyofherpessimplexvirustype1and2infectioninjapanbasedontype-specificserologicalassays,epidemiolinfect.1998mar;120(2):179-86
非专利文献3:decisionresources;emergingvaccines2008
非专利文献4:ウイルス2010第60卷第2号,pp.187-196
非专利文献5:herold,b.c.等、glycoproteinc-independentbindingofherpessimplexvirustocellsrequirescellsurfaceheparansulphateandglycoproteinb.jgenvirol199475(pt6):1211-22
非专利文献6:herold,b.c.等、glycoproteincofherpessimplexvirustype1playsaprincipalroleintheadsorptionofvirustocellsandininfectivity.jvirol199165:1090-8
非专利文献7:arii,j.等、non-musclemyosiniiaisafunctionalentryreceptorforherpessimplexvirus-1.nature2010467:859-62
非专利文献8:satoh,t.等、pilralphaisaherpessimplexvirus-1entrycoreceptorthatassociateswithglycoproteinb.cell2008132:935-44
非专利文献9:suenaga,t.等、myelin-associatedglycoproteinmediatesmembranefusionandentryofneurotropicherpesviruses.procnatlacadsciusa2010107:866-71
非专利文献10:geraghty,r.j.等、entryofalphaherpesvirusesmediatedbypoliovirusreceptor-relatedprotein1andpoliovirusreceptor.science1998280:1618-20
非专利文献11:montgomery,r.i.等、herpessimplexvirus-1entryintocellsmediatedbyanovelmemberofthetnf/ngfreceptorfamily.cell(1996)87:427-36
非专利文献12:shukla,d.,等、anovelrolefor3-o-sulfatedheparansulfateinherpessimplexvirus1entry.cell199999:13-22
非专利文献13:eisenbergrj等、herpesvirusfusionandentry:astorywithmanycharacters.viruses20124:800-83210.3390/v4050800
非专利文献14:science2006313,14,217-220
非专利文献15:virology1989172(1),11-24
非专利文献16:virology1991180(1),135-152
非专利文献17:virology1992186(1),99-112
非专利文献18:benderfc等、antigenicandmutationalanalysesofherpessimplexvirusglycoproteinbrevealfourfunctionalregions.jvirol.2007apr;81(8):3827-41.epub2007jan31
非专利文献19:pottagejcjr等、herpessimplexvirusresistancetoacyclovir:clinicalrelevance.infectagentsdis.1995sep;4(3):115-24
非专利文献20:krawczyka等、impactofvalencyofaglycoproteinb-specificmonoclonalantibodyonneutralizationofherpessimplexvirus.jvirol.2011feb;85(4):1793-803.doi:10.1128/jvi.01924-10.epub2010dec1
技术实现要素:
发明要解决的问题
本发明的课题在于,提供对hsv显示中和效果、抑制hsv的细胞间传播、可用于hsv感染症的预防和/或治疗的新颖的抗hsvgb单克隆抗体或其抗原结合片段。
用于解决问题的方案
本发明人们通过使用人抗体文库实施的抗hsvgb抗体的详尽搜索而得到44种抗gb抗体。将这些抗体供于病毒中和试验,结果发现,被命名为单克隆抗体d48的细胞株显示出对hsv-1及hsv-2的较强的病毒中和活性(噬斑数减少活性)及抑制细胞间传播(细胞间感染扩散)的活性,其活性强度与其它抗体相比有绝对优势。本发明人们对单克隆抗体d48进行了更详细的分析,从而完成了本发明。
即,本发明涉及以下的各发明。
(1)一种抗hsvgb单克隆抗体或其抗原结合片段,其为与单纯疱疹病毒(hsv)的包膜糖蛋白b(gb)特异地结合的抗hsvgb单克隆抗体或其抗原结合片段,其包含重链可变区和轻链可变区
所述重链可变区包含由序列号3记载的氨基酸序列构成的重链cdr1、由序列号4记载的氨基酸序列构成的重链cdr2及由序列号5记载的氨基酸序列构成的重链cdr3;
轻链可变区包含由序列号6记载的氨基酸序列构成的轻链cdr1、由序列号7记载的氨基酸序列构成的轻链cdr2及由序列号8记载的氨基酸序列构成的轻链cdr3。
(2)根据上述(1)的抗hsvgb单克隆抗体或其抗原结合片段,其包含:
包括序列号1记载的氨基酸序列的重链可变区、和
包括序列号2记载的氨基酸序列的轻链可变区。
(3)根据上述(1)或(2)的抗hsvgb单克隆抗体或其抗原结合片段,子,hsv为hsv-1或hsv-2。
(4)一种多核苷酸,其编码上述(1)~(3)中任一项的抗hsvgb单克隆抗体或其抗原结合片段。
(5)一种表达载体,其包含上述(4)的多核苷酸、和与该多核苷酸可操作地连接的1或多个调控序列。
(6)一种转化体,其导入了上述(5)的表达载体。
(7)一种使用上述(4)的多核苷酸、上述(5)的表达载体、上述(6)所述的转化体制造上述(1)~(3)中任一项的抗hsvgb单克隆抗体或其抗原结合片段的方法。
(8)一种用于预防或治疗hsv感染症的药物组合物,其包含上述(1)或(2)的抗hsvgb单克隆抗体或其抗原结合片段。
(9)根据上述(8)的药物组合物,其中,hsv感染症为hsv-1感染症或hsv-2感染症。
(10)根据上述(8)或(9)的药物组合物,其中,hsv感染症选自由口唇疱疹、角膜疱疹、生殖器疱疹、系统性新生儿疱疹以及起因于hsv的口疮、皮肤病、脑炎、髓膜炎及脊髓炎组成的组。
(11)一种抗hsvgb单克隆抗体或其抗原结合片段,其与下述区域中的至少1个氨基酸残基结合,所述区域由序列号10中记载的单纯疱疹病毒-1(hsv-1)的包膜糖蛋白b(gb)的第383-388位的氨基酸残基构成、和/或由序列号11中记载的单纯疱疹病毒-2(hsv-2)的包膜糖蛋白b(gb)的第386-391位的氨基酸残基构成。
(12)根据上述(11)的抗hsvgb单克隆抗体或其抗原结合片段,其包含重链可变区和轻链可变区,
所述重链可变区包含由序列号3记载的氨基酸序列构成的重链cdr1、由序列号4记载的氨基酸序列构成的重链cdr2及由序列号5记载的氨基酸序列构成的重链cdr3;
所述轻链可变区包含由序列号6记载的氨基酸序列构成的轻链cdr1、由序列号7记载的氨基酸序列构成的轻链cdr2及由序列号8记载的氨基酸序列构成的轻链cdr3。
(13)根据上述(12)的抗hsvgb单克隆抗体或其抗原结合片段,其包含:
包括序列号1记载的氨基酸序列的重链可变区、和
包括序列号2记载的氨基酸序列的轻链可变区。
(14)一种多核苷酸,其编码上述(11)~(13)中任一项的抗hsvgb单克隆抗体或其抗原结合片段。
(15)一种表达载体,其包含上述(14)的多核苷酸、和与该多核苷酸可操作地连接的1或多个调控序列。
发明的效果
本发明的抗hsvgb单克隆抗体或其抗原结合片段在体外具有对hsv-1及hsv-2的较强的病毒中和活性(噬斑数减少活性),并且具有强烈抑制细胞间感染扩散(细胞间传播)的活性,另外,不仅是在体内预防性给药中,在生物体已被hsv感染的情况下的治疗性给药中也显示显著的抗感染效果。从而,可以用于预防和/或治疗hsv感染、以及防止hsv感染激活,特别是可以作为针对hsv感染风险高的免疫缺陷患者或者正在给药免疫抑制剂的骨髓移植、血液干细胞移植或器官移植患者的预防药、或作为针对反复发生hsv激活的患者的治疗药来用作现有抗病毒药的替代药或联用药。
附图说明
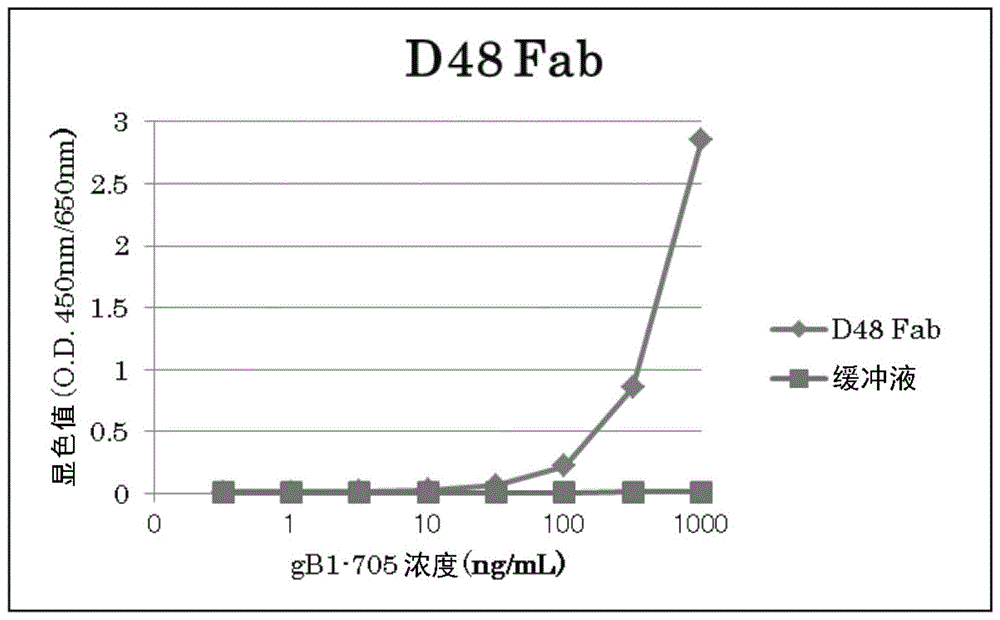
图1是示出实施例2的利用elisa的抗hsvgb抗体(fab)的反应性分析的结果的图。
图2是示出实施例2的利用elisa的抗hsvgb抗体(人-小鼠嵌合igg2a)的反应性分析的结果的图。
图3是示出实施例3的利用免疫印迹的抗hsvgb抗体的反应性分析的结果的图。
图4是示出实施例6的利用氢-氘交换质谱(hdx-ms)的表位分析的结果的图。
图5是示出实施例8的利用抗体d48、f67及e31的小鼠抗感染试验的存活率的比较结果的图。
图6是示出实施例8的利用抗体d48对小鼠进行预防性给药的存活率的结果的图。
图7是示出实施例8的利用抗体d48对小鼠进行预防性给药的症状评分的结果的图。
图8是示出实施例8的利用抗体d48对小鼠进行治疗性给药的存活率的结果的图。
图9是示出实施例8的利用抗体d48对小鼠进行治疗性给药的症状评分的结果的图。
图10是示出实施例9的利用抗体d48对豚鼠进行预防性给药的症状评分的结果的图。
图11是示出实施例9的利用抗体d48对豚鼠进行治疗性给药的症状评分的结果的图。
图12是示出实施例9的利用抗体d48对豚鼠进行治疗性给药的阴道拭液中的hsv释放量的结果的图。
图13是示出对hsv-1来源的gb氨基酸序列(序列号10)及hsv-2来源的gb氨基酸序列(序列号11)进行多重比对的比较结果的图,斜体部表示前导序列,下划线部表示hsv-1来源的gb的结构域ii的第383-388位的氨基酸残基(i383-r388)及hsv-2来源的gb的结构域ii的第386-391位的氨基酸残基(i386-r391)。
具体实施方式
以下详细说明用于实施本发明的方式。但是,本发明不受以下实施方式限定。
本发明的一实施方式的抗hsvgb单克隆抗体或其抗原结合片段与单纯疱疹病毒(hsv)的包膜糖蛋白b(gb)特异地结合。本发明的抗hsvgb单克隆抗体或其抗原结合片段包含重链可变区和轻链可变区,所述重链可变区包含由序列号3记载的氨基酸序列构成的重链cdr1、由序列号4记载的氨基酸序列构成的重链cdr2及由序列号5记载的氨基酸序列构成的重链cdr3;所述轻链可变区包括由序列号6记载的氨基酸序列构成的轻链cdr1、由序列号7记载的氨基酸序列构成的轻链cdr2及由序列号8记载的氨基酸序列构成的轻链cdr3。
本发明人们通过使用人抗体文库实施的抗hsv―2gb抗体的详尽搜索而得到44种抗gb抗体。将这些抗体供于病毒中和试验的结果是,单克隆抗体d48显示出较强的噬斑数减少活性及细胞间感染扩散抑制活性。
抗体d48具有:具有表1所示的序列号1的氨基酸序列的重链可变区(vh);及,具有序列号2的氨基酸序列的轻链可变区(vl),另外具有:包括由序列号3~5的氨基酸序列构成的重链cdr1、重链cdr2及重链cdr3的重链可变区;以及,包括由序列号6~7的氨基酸序列构成的轻链cdr1、轻链cdr2及轻链cdr3的轻链可变区。
[表1]
表1抗体d48的vh、vl氨基酸序列及各自的cdr
本发明的抗hsvgb单克隆抗体或其抗原结合片段由于包含单克隆抗体d48的cdr序列,因此对hsv-1及hsv-2具有较强的病毒中和活性(噬斑数减少活性),并且具有强烈的抑制细胞间感染扩散(细胞间传播)的活性。
抗hsvgb单克隆抗体或其抗原结合片段可以包含:包括序列号1记载的氨基酸序列的重链可变区、和包括序列号2记载的氨基酸序列的轻链可变区。
抗hsvgb单克隆抗体至少为包含重链的可变结构域及轻链的可变结构域的抗体,可以为完全抗体。完全抗体具有2条全长的轻链和2条全长的重链,各轻链和重链通过二硫键而连接。完全抗体包括iga、igd、ige、igm及igg,igg包括igg1、igg2、igg3及igg4作为亚型。
抗原结合片段也称为抗体片段,是指具有与抗原结合的功能的片段(抗原结合片段)。抗原结合片段包括例如单链可变区片段(scfv)、fab、fab’、f(ab’)2、scab、scfvfc及fv。fab具有1个抗原结合部位作为具有轻链及重链的可变区、以及轻链的恒定区及重链的原有的恒定区(ch1结构域)的结构。fab’与fab的不同在于,在重链ch1结构域的c末端具有至少包含半胱氨酸残基的铰链区。f(ab’)2抗体是通过fab’的铰链区的半胱氨酸残基间的二硫键而生成的。fv(可变片段)是指仅具有重链可变部位及轻链可变区部位的最小抗原结合片段。双链fv(dsfv)是重链可变部位与轻链可变部位通过二硫键连接而成的,单链fv(scfv)通常是重链可变区通过肽接头与轻链可变区以共价键连接而成的。scab是在scfv上键合有l链或h链的恒定区的部分结构域(c结构域)的类型。scfvfc是在scfv上键合有h链的ch1及ch2的类型。
抗原结合片段例如可以用蛋白水解酶由完全抗体得到。例如,将完全抗体用木瓜蛋白酶切断则可以得到fab片段,用胃蛋白酶切断则可以得到f(ab’)2片段。另外,抗原结合片段也可以使用基因重组技术来制作。轻链及重链的可变区包括被称为互补性决定区(以下称为“cdr”)的3个变化较多的区域。cdr主要发挥与抗原的表位结合的作用。3个cdr从n-末端起依次分别称为cdr1、cdr2、cdr3。
抗hsvgb单克隆抗体可以为人抗体(全人抗体)、人源化抗体或嵌合抗体,特别优选为人单克隆抗体或人源化单克隆抗体。
本实施方式的抗hsvgb单克隆抗体或其抗原结合片段与单纯疱疹病毒(hsv)的包膜糖蛋白b(gb)特异地结合。hsvgb包括hsv-1来源gb及hsv-2来源gb,图13示出对hsv-1来源gb的氨基酸序列(序列号10)及hsv-2来源gb的氨基酸序列(序列号11)进行多重比对的比较结果。根据图13,两者的序列同一性为87%,但本实施方式的抗hsvgb单克隆抗体或其抗原结合片段与hsv-1来源gb及hsv-2来源gb均特异地结合,特别是与gb的结构域ii、进一步特别与对应于hsv-1来源gb的结构域ii的i383-r388、或hsv-2来源gb的结构域ii的i386-r391的区域中的至少1个、或至少2个、进一步至少3个氨基酸残基特异地结合。
作为本实施方式的抗hsvgb单克隆抗体或其抗原结合片段相对于现有抗病毒药的优点,可以认为有(1)副作用少、(2)出现抗药病毒株的风险低这两点。特别是关于后者,本实施方式的抗hsvgb单克隆抗体或其抗原结合片段为与对于病毒复制周期而言不可或缺的hsv-1及hsv-2外膜的表面糖蛋白b(gb)上的表位序列特异地结合的抗体,因此,认为可能源于gb蛋白中的该表位序列的突变的hsv抗性的出现会导致该突变本身丧失病毒感染效价,因此认为可能性低。
本发明的另一实施方式的抗hsvgb单克隆抗体或其抗原结合片段与下述区域中的至少1个氨基酸残基特异地结合,所述区域由序列号10中记载的单纯疱疹病毒-1(hsv-1)的包膜糖蛋白b(gb)的第383-388位的氨基酸残基构成、和/或由序列号11中记载的单纯疱疹病毒-2(hsv-2)的包膜糖蛋白b(gb)的第386-391位的氨基酸残基构成。作为该抗hsvgb单克隆抗体或其抗原结合片段,可列举例如包含如下重链可变区和轻链可变区的抗hsvgb单克隆抗体或其抗原结合片段,所述重链可变区包含由序列号3记载的氨基酸序列构成的重链cdr1、由序列号4记载的氨基酸序列构成的重链cdr2及由序列号5记载的氨基酸序列构成的重链cdr3的重链可变区;所述轻链可变区包含由序列号6记载的氨基酸序列构成的轻链cdr1、由序列号7记载的氨基酸序列构成的轻链cdr2及由序列号8记载的氨基酸序列构成的轻链cdr3。
作为另一实施方式,提供编码上述单克隆抗体或其抗原结合片段的多核苷酸、包含上述多核苷酸和与多核苷酸可操作地连接的1或多个调控序列的表达载体及包含上述表达载体的转化体。
多核苷酸可以是编码完全抗体的多核苷酸、以及分别编码包含序列号1~8记载的氨基酸序列的抗原结合片段的多核苷酸,可以将多个编码cdr的多核苷酸整合成一个多核苷酸。这样的多核苷酸可通过例如化学合成而得到。
作为包含本实施方式的编码抗hsvgb单克隆抗体或其抗原结合片段的多核苷酸、和与该多核苷酸可操作地连接的1或多个调控序列的表达载体,没有特别限定,可以为能够在宿主细胞中复制和/或表达多核苷酸的载体。可列举例如pcag、pet等。调控序列为控制宿主细胞中的多核苷酸表达的序列(例如启动子、增强子、核糖体结合序列、转录终止序列等),可根据宿主的种类适宜选择。按照在宿主细胞中表达多核苷酸的方式将该表达载体与合适的启动子可操作地连接,另外,可以为包含筛选标记的载体。另外,可以将分别编码包含序列号1~8记载的氨基酸序列的抗原结合片段的多核苷酸、例如编码重链可变区的多核苷酸和编码轻链可变区的多核苷酸用不同的载体来表达。
作为宿主细胞,只要可表达抗体就没有特别限定,可列举例如:人、中华仓鼠、小鼠、大鼠、兔、猪、猴、山羊、马等哺乳类动物细胞、植物细胞、酵母细胞、昆虫细胞、或细菌细胞等。
作为转化宿主细胞的方法,没有特别限定,可适宜使用电穿孔法、磷酸钙法、脂质体法、deae葡聚糖法等现有公知的方法。
单克隆抗体或其抗原结合片段可通过例如已知的基因程方法来制作。单克隆抗体或其抗原结合片段例如可通过在宿主细胞中表达包含编码上述抗hsvgb单克隆抗体或其抗原结合片段的多核苷酸的载体来制作。关于多核苷酸的设计,可根据人抗体、人源化抗体或嵌合抗体由本领域技术人员适宜地进行。例如,在人抗体或其抗原结合片段的情况下,除了编码序列号1及2中记载的重链及轻链的可变区、或序列号3~8中记载的重链cdr1~3及轻链cdr1~3的多核苷酸以外,还可进一步包含编码人抗体的这些部分以外的部分的氨基酸序列的多核苷酸的至少一部分。在完全抗体的情况下,可通过将编码上述可变区或cdr1~3的多核苷酸和编码此外的部分的多核苷酸按照正确的顺序以有功能的方式连接而得到。可以将编码重链及轻链的多核苷酸整合到一个多核苷酸中,也可以整合到不同的多核苷酸中。另外可以进一步包含用于表达的启动子、编码确认表达所需要的标签的多核苷酸。在嵌合抗体或其抗原结合片段的情况下,在编码序列号1及2中记载的重链及轻链的可变区、或序列号3~8中记载的重链cdr1~3及轻链cdr1~3的多核苷酸以外的部分,可包含编码小鼠或豚鼠等动物来源的氨基酸序列的多核苷酸。
进一步的实施方式提供一种用于预防或治疗hsv感染症的药物组合物,所述药物组合物包含抗hsvgb单克隆抗体或其抗原结合片段。hsv感染症为由hsv-1及hsv-2引起的感染症,可列举例如口唇疱疹、角膜疱疹、生殖器疱疹、系统性新生儿疱疹、以及起因于hsv的口疮、皮肤病、脑炎、髓膜炎及脊髓炎等。
预防是指:通过对有hsv感染风险的对象、特别是hsv感染风险高的免疫缺陷患者或给予免疫抑制剂的骨髓移植·血液干细胞移植·器官移植患者进行给药而实现的、抑制或延迟感染的发病或者缓和症状。治疗是指:通过对生物体已感染hsv的对象进行给药而实现的、症状的缓和、好转或治愈,也包括通过对反复发生hsv复发的对象进行给药而实现的、防止复发。用于治疗hsv感染症的药物组合物可以作为现有抗病毒药的替代药或联用药使用。
药物组合物可进一步包含药学上可接受的载体。作为药学上可接受的载体,没有特别限定,可列举水、盐类溶液、磷酸缓冲生理盐水、葡聚糖、甘油、乙醇等。这些载体可以单独使用1种,另外也可以将两种以上组合使用。
药物组合物可以制成片剂、颗粒、胶囊、注射剂、滴眼剂、吸入剂、泥罨剂。作为用于该药物组合物的制剂化剂,例如可以进一步包含润滑剂、乳化剂、防腐剂、缓冲剂、稳定化剂等增加抗体或抗体部分的保存性或有效性的少量辅助物质。
实施例
以下基于实施例更具体地说明本发明。但是,本发明不受以下的实施例限定。
实施例1抗hsvgb单克隆抗体d48的制作
对于通过使用人抗体文库实施的抗hsv-2gb(hsvgb2)抗体的详尽搜索而得到的抗体d48,制作scfv-hfc型、fab型、人-小鼠嵌合igg2a型及人-豚鼠嵌合igg2κ型这4种分子形态的抗体d48,进一步进行分析。
<单链抗体噬菌体(scfv-hfc)>
将编码序列号9所示的氨基酸序列的分离出的抗体d48scfv(singlechainfv,单链抗体)基因与来自人igg1的fc基因(ch2-ch3)连接,克隆到pcag载体中而构建scfv-fc表达质粒。表达时,使用freestyle293或expi293表达系统(lifetechnology公司)。将表达质粒转染至细胞,4~6天时回收培养上清。将培养上清用ab-rapidpure10(protenova)或ab-rapidpureex(protenova)纯化,得到scfv-hfc。
<fab>
将分离出的抗体d48scfv基因的vh区与来自小鼠igg2a的ch1基因连接,克隆到pcag载体中而构建h链表达质粒。另外,将抗体d48scfv基因的vl区与小鼠cl基因连接,克隆到pcag载体而构建l链表达质粒。为了易于纯化,在ch1基因之后(c末端侧)连接his标签基因。表达时,使用freestyle293或expi293表达系统。使表达质粒转染细胞,在4~6天时回收培养上清。将培养上清用nintaagarose(qiagen)纯化,得到fab。
<人-小鼠嵌合igg2a>
将分离出的抗体d48scfv基因的vh区与来自小鼠igg2a的h链恒定区基因(ch1-ch2-ch3)连接,克隆到pcag载体中而构建h链表达质粒。另外,将抗体d48scfv基因的vl区与小鼠cl基因连接,克隆到pcag载体中而构建l链表达质粒。表达时,使用freestyle293或expi293表达系统。使表达质粒转染细胞,在4~6天时回收培养上清。将培养上清用hitrapproteinahpcolumn(gehealthcare)纯化,得到人-小鼠嵌合igg2a。
<人-豚鼠嵌合igg2κ>
将分离出的抗体d48scfv基因的vh区与来自豚鼠igg2的h链恒定区基因(ch1-ch2-ch3)连接,克隆到pcag载体中而构建h链表达质粒。另外,将抗体d48scfv基因的vl区与小鼠cl基因连接,克隆到pcag载体中而构建l链表达质粒。表达时,使用freestyle293或expi293表达系统。使表达质粒转染细胞,4~6天时回收培养上清。将培养上清用hitrapproteinahpcolumn纯化,得到人-豚鼠嵌合igg2κ。
实施例2利用elisa的抗hsvgb抗体的反应性分析
<fab的反应性分析>
利用elisa来评价所得到的fab的结合活性。将fab用pbs稀释为2μg/ml,向maxisorpplate(nunc)中加入100μl,在室温下孵育2小时而使fab固相化。固相化后,用pbs洗涤平板,以3.16倍从1μg/ml梯度稀释至0.316ng/ml,向重组hsv-1gb(gb1-705-strep)平板的孔中加入100μl,在37℃下孵育。1小时后用pbst洗涤,向平板的孔中加入检测抗体抗链球菌素(strep-tactin)/hrp(funakoshi)100μl,在37℃下孵育。1小时后用pbst洗涤,向平板的孔中加入tmb(3,3’,5,5’-四甲基联苯胺)100μl而显色。30分钟后,用1n硫酸终止反应,用酶标仪(moleculardevices)测定显色值(o.d.450nm/650nm)。使用的重组gb(gb1-705-strep)为在由序列号11所示的氨基酸序列的1~705氨基酸残基构成的、hsv-2的333株来源的野生型gb的胞外结构域的c末端结合有链酶标签ii(streptagii)的重组gb,使用该标签进行纯化、用elisa的检测。
其结果如图1所示,重组gb(gb1-705-strep)对抗体d48fab显示出特异性结合。
<人-小鼠嵌合igg2a的反应性分析>
利用elisa来评价所得到的人-小鼠嵌合igg2a的结合活性。将重组gb(gb1-705-strep)用pbs稀释为1μg/ml,向maxisorpplate加入100μl,在室温下孵育1小时而使重组gb(gb1-705-strep)固相化。固相化后,用pbs洗涤平板,各以3.16倍从1μg/ml梯度稀释到0.316ng/ml,向平板的孔中加入人-小鼠嵌合igg2a100μl,在37℃下孵育。1小时后用pbst洗涤,向平板的孔中加入作为检测抗体的兔抗小鼠igg/hrp(invitrogen)100μl,在37℃下孵育。1小时后用pbst洗涤,向平板的孔中加入tmb100μl而显色。30分钟后,用1n硫酸终止反应,用酶标仪测定显色值(o.d.450nm/650nm)。
其结果如图2所示,人-小鼠嵌合igg2a对重组gb(gb1-705-strep)显示出特异性结合。
实施例3利用免疫印迹的抗hsvgb抗体的反应性分析
将gb1-705-strep以2μg/泳道注入到8-16重量%sds-page用凝胶中,进行电泳。电泳后,将凝胶向到硝酸纤维素膜(immobilon-p、millipore)转印,用2%脱脂乳(wako)-pbst进行封闭。封闭后的硝酸纤维素膜在用pbst洗涤后与2%脱脂乳-pbst、以及10μg/ml的scfv-hfc、fab、人-小鼠嵌合igg2a或人-豚鼠嵌合igg2κ在室温下反应60分钟。再次洗涤之后,使硝酸纤维素膜在2%脱脂乳-pbst中分别与抗higg(h+l)/hrp(biorad)、抗his标签/hrp(r&d)、抗小鼠igg(h+l)/hrp或抗豚鼠(h+l)/hrp(invitrogen)反应,用immobilonwesterndetectionregent(millipore)进行显色。制作未变性gb1-705-strep、变性gb1-705-strep及、还原·变性gb1-705-strep。还原·变性gb1-705-strep是通过加入1mdtt并在96℃下煮沸5分钟而得到的。变性gb1-705-strep是通过在96℃下煮沸5分钟而得到的。未变性gb1-705-strep则不进行这些操作。将制作的未变性gb1-705-strep、变性gb1-705-strep及、还原·变性gb1-705-strep直接注入到凝胶中。
将结果示于图3。泳道1~3依次为未变性gb1-705-strep、变性gb1-705-strep及还原·变性gb1-705-strep,泳道m及m′分别为benchmarkprestainedladder及magicwesternstandard。左侧的照片为sds-page,条带染色时,进行cbb染色。右侧的4张照片为蛋白质印迹(wb)的结果。由图3可知,作为原型的scfv-hfc具有如下颇具意味的特征:与未变性gb1-705-strep相比,与还原·变性gb1-705-strep强烈反应,即使是改变了分子形态的fab型、人-小鼠嵌合igg2a型及人-豚鼠嵌合igg2κ型的情况下也延续了该特征。一般认为,与变性抗原强烈反应的抗体很可能识别线性序列的表位。因此,根据该结果推测抗体d48识别gb的线性的序列。
实施例4利用表面等离子共振(spr)的分析
使用biacoret200(gehealthcare)来进行。在所有的实验中,使用hbs-ep+缓冲液,温度设为25℃,流速设为30μl/分钟。传感器芯片使用cm5(gehealthcare),将gb1-705-strep以约100响应单位(resonanceunits,ru)固相化。以单循环动力学模式实施测定,对于scfv-hfc,稀释为128nm、64nm、32nm、16nm、8nm而使用,对于fab,稀释为64nm、32nm、16nm、8nm、4nm而使用,对于人-小鼠嵌合igg2a、人-豚鼠嵌合igg2κ、单克隆抗体e31、单克隆抗体f67,稀释为256倍、128倍、64倍、32倍、16倍而使用。所有的样品均仅测定一次。单克隆抗体e31和单克隆抗体f67均为识别gb的结构域iv的抗体。
结果如表2所示。使用spr的动力学分析还表明,为维持了亲和性的状态。另外,由该动力学分析还明确了:作为使用人抗体文库详尽检索抗hsvgb2抗体而得到的另一抗体株的f67及e31,具有与抗体d48相比低1个数量级的亲和性。
[表2]
表2.对各种分子形态的抗体d48的动力学分析的结果:
实施例5利用丙氨酸扫描的表位分析
为了鉴定抗体d48的表位,制作将gb1-705中所含的带电氨基酸置换为丙氨酸的187克隆,确认抗体d48与scfv-hfc的反应性。
利用pcr构建将gb1-705中的带电氨基酸残基(187个位置)分别修饰为丙氨酸的基因,克隆到pcaggs1-dhfr-neo中。表达时,使用freestyle293或expi293表达系统。利用elisa评价所得到的gb丙氨酸置换体的表达量、以及丙氨酸置换体与抗体片段的结合活性。
将包含gb丙氨酸置换体的培养上清加入到maxisorpplate中,在室温下孵育1小时而使gb丙氨酸置换体固相化。固相化后,用pbst洗涤平板,向平板的孔中加入检测抗体链球菌素/hrp(iba)100μl,在室温下孵育。1小时后用pbst洗涤,向平板的孔中加入tmb100μl而显色。30分钟后,用1n硫酸终止反应,用酶标仪测定显色值(o.d.450nm/650nm),求出表达量。
另一方面,将包含gb丙氨酸置换体的培养上清加入到固定有链球菌素(iba)的maxisorpplate中,在室温下孵育1小时而将gb丙氨酸置换体固相化。固相化后,用pbst洗涤平板,向平板的孔中加入抗体片段100μl,在室温下孵育。1小时后用pbst洗涤,向平板的孔中加入检测抗体抗人fc/hrp(biocosmo)100μl,在室温下孵育。1小时后用pbst洗涤,向平板的孔中加入tmb100μl而显色。30分钟后,用1n硫酸终止反应,用酶标仪测定显色值(o.d.450nm/650nm),求出结合活性。通过与未经丙氨酸置换的野生型gb1-705相比单位表达量的反应性是否有变化来选出候选表位。
其结果表明,gb的结构域ii上的r391作为表位是重要的氨基酸残基。
实施例6利用氢-氘交换质谱(hdx-ms)的表位分析
丙氨酸扫描是仅以亲水性残基为靶的分析,可充分预测其它非亲水性残基为表位的可能性。
因此,使用氢/氘交换质谱法(hdx-ms)实施抗体d48的详细的表位分析。该方法利用了下述现象:当蛋白质暴露于d2o时,未形成稳定氢键的结构表面及天然无序(disorder)区域的酰胺氢会迅速从h被交换为d。例如,在抗体形成了紧密(tight)结合的抗体-蛋白质界面处,d2o仅可通过摇摆运动(breathingmotion)而侵入,因此得到保护而免于hdx,结果是仅发生低速的hdx。另一方面,在抗体-蛋白质界面以外,得不到保护而无法避免hdx,因此结果是发生高速的hdx。通过基于ms的肽作图来分析由于该hdx速度差异而引起了不均匀hdx状态的抗体-蛋白质复合体的质量变化,从而能够进行抗体的详细的表位分析。hdx-ms是已经有多方面的应用成绩的既有方法,特别是在抗体的表位分析中,由于可以在于溶液中保持立体结构的状态下分析构象表位而成为一种重要的技术。
实验方法如下。将120μm的gb1-705和400μm的抗体d48fab等量混合,制备gb1-705/抗体d48fab复合体。该复合体用pbs(ph7.2)来制备,作为氘缓冲剂,使用pbs(pd7.2),在20℃下进行h/d交换反应。向反应后的复合体中加入quench缓冲液(100mm磷酸钠、150mm氯化钠、4m盐酸胍、150mm三(2-羧基乙基)膦盐酸盐(tcep)),调节为ph2.4。使用胃蛋白酶柱将复合体制成肽片段,用lc-ms进行分析。此时的切断、洗脱条件为:注射试样(injectedsample):75pmol、胃蛋白酶消化+脱盐时间:6分钟、lc的梯度条件:9分钟。在该条件下,在gb1-705、gb1-705/抗体d48fab复合体的3次测定中均存在的肽为192条,序列覆盖度(sequencecoverage)为99.2%。
将利用氢-氘交换质谱(hdx-ms)的表位分析结果示于图4。使用gb1-705和抗体d48fab实施分析的结果是,命中的肽为v380-d389。另外,由于判断l377-c385为氘交换率无差异的肽,因此表明i386-d389为抗体d48的表位。其非常靠近本发明人们的此前的分析结果、即r391。
另外,此次研究中使用了胃蛋白酶作为消化酶,未能得到包含r391的肽,综合考虑,认为序列号11中记载的hsv-2gb的i386-r391为抗体d48的表位的可能性非常高。另外,认为可能仅d389、r388、g387、i386中的任一者为表位。进一步地,r391之后也可能构成了表位的一部分。同样地,认为由对应于序列号11中记载的hsv-2gb的i386-r391的、序列号10中记载的hsv-1gb的i383-r388构成的区域为抗体d48的表位的可能性非常高。
若观察立体结构,i386-r391形成位于gb结构域ii的溶剂面的α螺旋,可以说是抗体容易靠近的部位。另外,虽然没有满足命中的判别式,但l416-l422经检测也没有氘交换率差异。l416-l422比i386-r391更位于结构内部侧,存在不易暴露于溶剂的部位,因此认为,该氘交换率差异是由于变构所产生的影响,
作为已经报道的抗体中的在结构域ii上具有表位的抗hsvgb单克隆抗体,已知有c226、h1838及h1781,虽然已经报道了大致的表位及体外的生物活性,但没有报道体内生物活性的详细情况(非专利文献18)。
实施例7病毒中和试验
<细胞及病毒的培养>
在病毒的培养、感染效价测定、中和抗体效价测定中,使用购自atcc的vero细胞(ccl.81)。在37℃、5%co2条件下培养vero细胞。在扩大培养、维持、分析平板制作时,使用含有10%fbs的mem培养基,在感染效价测定及中和抗体效价测定时,使用含有2%fbs的mem培养基。中和试验及抗感染能力分析中使用的病毒库购自atcc,以m.o.i=0.01~1对整片的vero细胞接种人类疱疹病毒2(hsv-2)ms株(vr-540)及人类疱疹病毒1(hsv-1)kos株(vr-1493),在含有2%fbs的mem培养基中培养2~3天。将回收的感染细胞培养瓶进行3次冷冻解冻而破碎细胞后,用tomy离心器在室温下以3500rpm离心10分钟,将上清作为hsv-2病毒库及hsv-1病毒库。
<中和试验>
中和试验使用噬斑数减少活性(噬斑减少活性)测定和细胞间感染扩散抑制活性测定这2种方法来进行。作为对象的病毒使用hsv-2ms株和hsv-1kos株这2种。
关于噬斑减少活性测定,将受试抗体调整为规定浓度,与约100pfu的hsv-2ms株或hsv-1kos株混合后,在37℃下反应1小时。在48孔平板中,对整片的vero细胞接种反应液,在30℃下吸附1小时后,用含有1%甲基纤维素的mem(2%fbs)培养基培养24小时后,用50%甲醇/50%乙醇(-20℃)在-20℃下进行30分钟失活及固定。然后,使抗hsvgb单克隆抗体在37℃下反应1小时,用抗小鼠igg/hrp(dakop0447)和tmbh进行免疫染色,用elispot分析仪(immunospots6analyzerctl公司)捕获各孔的图像,用分析软件(biospotctl公司)统计噬斑数。
关于细胞间感染扩散抑制活性测定,在48孔平板中对整片的vero细胞接种约100pfu的hsv-2ms株或hsv-1kos株,在30℃下吸附1小时后,添加含有规定浓度的受试抗体的含有1%甲基纤维素的mem(2%fbs)培养基(抗体浓度为5μg/ml、25μg/ml及125μg/ml),对hsv-2ms株培养约40小时,对hsv-1kos株培养约48小时,然后用50%甲醇/50%乙醇(-20℃)在-20℃下进行30分钟的失活及固定。然后,使自制的抗hsvgb单克隆抗体在37℃下反应1小时,用抗小鼠igg/hrp和tmbh进行免疫染色,用elispot分析仪捕获各孔的图像,用分析软件分析噬斑尺寸的平均值。
将结果示于表3。抗体d48的scfv-hfc、fab、人-小鼠嵌合igg2a及人-豚鼠嵌合igg2k均对于kos(hsv-1)、ms(hsv-2)这两病毒株显示了1nm以下或数nm的强的50%噬斑数减少活性。另外,抗体d48的scfv-hfc及人-小鼠嵌合igg2a对ms(hsv-2)株分别在40nm及48nm下显示强的50%细胞间感染扩散抑制活性。
[表3]
表3.各种分子形态的抗体d48的中和活性
n.t.:未进行试验
抗体d48对体外的hsv-1及hsv-2的50%噬斑数减少活性在已报道的各种抗hsvgb单克隆抗体中也是突出的。
实施例8小鼠抗感染试验
<试验方法>
使用小鼠生殖器疱疹感染模型,实施抗hsvgb单克隆抗体(人-小鼠嵌合igg2a)的预防性给药及治疗性给药时的抗感染试验。使用balb/c小鼠(5周龄、雌性)。将规定量的抗体溶解于注射用生理盐水(saline),对小鼠给药抗体。在预防性给药的情况下,在接种病毒24小时前以200μl/只的体积腹腔内给药。在治疗性给药的情况下,在接种病毒48小时后,以200μl/只的烯基腹腔内给药。每组设定n=10的样本数。为了提高接种病毒时的感染效率,在接种病毒6天前以2mg/只皮下接种depo-provera。在麻醉下经阴道接种5×105pfu/20μl的hsv-2ms株,进行21天追踪观察。以存活天数(存活率)及症状评分为指标表示抗感染能力。关于症状评分,根据阴道病变症状的有无及程度给出评分,示出各组的平均值。打分的方法如下:0:无变化、1:局部性的红斑和肿胀、2:广泛的肿胀和浮肿、3:溃疡和出血、4:死亡。在观察到预期无法恢复的严重全身症状(竖毛、麻痹、震颤、痉挛等)的情况下,当天将评分设为3.5,处死,次日按照死亡处理,评分设为4。
<利用抗体d48、f67及e31的小鼠抗感染试验>
关于表4所示的3种抗hsvgb2抗体d48、f67及e31(均为人-小鼠嵌合igg2a),评价并比较各小鼠抗感染能力。抗体d48是在hsvgb的结构域ii区域具有表位且具有较强的病毒中和活性(50%噬斑数减少活性)的抗体,与此相对地,f67及e31均在结构域iv区域具有表位,前者不具有病毒中和活性,后者具有中等程度的病毒中和活性。
[表4]
表4.抗体d48、f67及e31的中和活性及表位区域
将各组的动物样本数设为n=7而进行预防性给药,表5示出感染后的存活天数及其平均值,图5示出感染后的存活率(%)的平均值。关于小鼠抗感染能力,抗体d48在30μg/只/次及3μg/只/次下显示出明显的存活天数延长效果,在0.3μg/只/次下也显示出显著的存活天数延长效果,与此相对地,f67及e31均止步于显示有限的效果。该结果表明,抗体d48与其它抗hsvgb2抗体相比,不仅在体外,在体内也具有明显的抗感染活性,其优秀性可能基于表位区域及亲和性的差异。
[表5]
表5.抗体d48、f67及e31的igg2a对小鼠预防性给药的存活天数
[差异显著性检验]***:p<0.001/**:0.001=<p<0.01/*:0.01=<p<0.05(kaplan-meier法)
<利用抗体d48的小鼠抗感染试验结果>
示出使用小鼠生殖器疱疹感染模型(n=10)的、抗体d48(人-小鼠嵌合igg2a)的预防性给药及治疗性给药时的抗感染试验结果。预防性给药的结果如表6(按照给药量分类的存活天数)、图6(存活率)及图7(症状评分)所示。治疗性给药的结果如表7(按照给药量分类的存活天数)、图8(存活率)及图9(症状评分)所示。
在预防性给药中,与阴性对照组(盐水给药组)相比,所设定的所有给药量(10mg/kg、3mg/kg、1mg/kg、0.5mg/kg、0.3mg/kg)下均显示显著的存活天数延长效果。特别是在作为高用量区的10mg/kg及3mg/kg的2种用量下,显示出显著的存活率及症状评分的改善效果。
[表6]
表6.抗体d48igg2a对小鼠预防性给药的存活天数
***:p<0.0001/**:0.0001=<p<0.001/*:0.001=<p<0.05(kaplan-meier法)
就治疗性给药而言,有报道指出:从感染局部起,hsv会在侵入体内后48小时以内转移到神经节。但是,在感染后48小时的时刻进行抗体d48的治疗性给药的情况下,在10mg/kg及3mg/kg的2种用量下显示明显的存活率及症状评分的改善效果。由这些结果可确认,抗体d48不仅在预防性给药中,在治疗性给药中也显示强的抗感染效果。
[表7]
表7.抗体d48igg2a对小鼠治疗性给药的存活天数
***:p<0.0001/**:0.0001=<p<0.001/*:0.001=<p<0.05(kaplan-meier法)
实施例9豚鼠抗感染试验
<试验方法>
使用豚鼠生殖器疱疹感染模型,实施抗hsvgb单克隆抗体d48(人-豚鼠嵌合igg2k)的预防性给药及治疗性给药时的抗感染试验。使用购自slc公司的hartley豚鼠(3~5周龄、雌性)。将规定量的抗体溶解于注射用生理盐水(saline),在预防性给药的情况下,在接种病毒24小时前、另外在治疗性给药的情况下在接种病毒4天后,均以1mg/kg~30mg/kg的体积进行腹腔内给药。在治疗性给药的情况下,在给药前进行症状观察,筛选呈现出阴道症状的个体,按照各组的平均评分无偏差的方式随机分组。关于各组的动物样本数,预防性给药时设定为n=9,治疗性给药时设定为n=15。关于病毒接种,在麻醉下经阴道接种5×105pfu/50μl的hsv-2ms株,在接种后2~3周观察急性期症状。关于症状评分,设为0:无明确的病变、0.5-1:红斑、1.5-2:局部性的水泡、2.5-3:局部性的溃疡或痂皮、3-5:广泛的水泡·溃疡或痂皮、3-7:伴有失禁的广泛的溃疡或痂皮、7.5:由于症状严重而安乐死、8:死亡。另外,在接种病毒后第7天,收集阴道拭液(vaginalswab),利用噬斑法测定病毒释放量。阴道拭液通过将用mem培养基润湿的棉棒插入阴道内、然后擦拭阴道内壁的粘膜的方式来收集。将收集的各阴道拭液悬浮于以1ml分注到硅化管中的mem培养基,冷冻保存直至使用。在测定病毒释放量时,将阴道拭液设为原液,进行10倍稀释、100倍稀释、1000倍稀释,以100μl/孔接种于96孔或48孔中的成为整片的vero细胞中。接种阴道拭液后,在37℃下进行1小时的病毒吸附,用含有1%甲基纤维素的2%fbsmem培养基培养24~72小时后,通过规定方法计测噬斑数。
<结果>
将使用豚鼠生殖器疱疹感染模型(急性期)的、抗体d48(人-豚鼠嵌合igg2κ)的预防性给药的抗感染试验的症状评分结果示于图10,将治疗性给药抗感染试验的症状评分结果示于图11,将治疗性给药抗感染试验的阴道拭液中的hsv释放量示于图12。
如图10所示,预防性给药时,在所设定的给药量(30mg/kg、10mg/kg、3mg/kg、1mg/kg)的所有用量下,与阴性对照组(盐水给药组)相比均可见显著的症状评分改善效果。
如图11所示,对感染后4天时已呈现出阴道症状的豚鼠以30mg/kg给药抗体d48,结果与阴性对照组(盐水给药组)相比症状评分显著减轻。另外,在接种病毒后第7天收集阴道拭液(vaginalswab)并利用噬斑法测定病毒释放量,结果如图12所示,与阴性对照组相比,病毒释放量显著减少。由以上确认,抗体d48不仅在预防性给药时,在治疗性给药时也显示显著的抗感染效果。
产业上的可利用性
根据本发明,可以提供对hsv显示强的中和效果、可以抑制hsv的细胞间传播的新颖的抗hsvgb单克隆抗体。从而,可以用于预防和/或治疗hsv感染,特别是作为对hsv感染风险高的免疫缺陷患者或给药免疫抑制剂的骨髓移植·血液干细胞移植·器官移植患者的预防药、或作为对hsv反复复发的患者的治疗药,可以作为现有抗病毒药的替代药或联用药使用。
序列表
<110>km生物医薬股份公司(kmbiologicsco.,ltd.)
<120>抗hsvgb单克隆抗体或其抗原结合片段
<130>fp18-0826-00
<150>jp2017-165968
<151>2017-08-30
<160>11
<170>patentinversion3.5
<210>1
<211>124
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>d48vh
<400>1
gluvalglnleuvalgluthrglyglyglyvalvalargproglyarg
151015
serleuargleusercysthrthrserglypheserpheserglyser
202530
alamethistrpvalargglnalaproglylysglyleuglutrpval
354045
alavalileserhisaspglyasnileileglntyrhisaspserval
505560
lysglyargphethrileserargaspasnserlysasnvalleuleu
65707580
leuglnmetasnserleuargvalaspaspthralamettyrtyrcys
859095
alaargaspvaltrpleuleuproalathrilesertyralapheasp
100105110
phetrpglyglnglythrmetvalthrvalserser
115120
<210>2
<211>107
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>d48vl
<400>2
valiletrpmetthrglnserproproserleuseralaserilegly
151015
aspthrvalthrilethrcysargalaserglnglyileserasnser
202530
ilealatrptyrglnargargproglylysalaprogluleuleuval
354045
tyralaalatyrargleuglnserglyvalproserargleusergly
505560
serglyserglyalaglutyrthrleuthrilelysasnmetglnpro
65707580
gluaspphealathrtyrtyrcysglnglntyrtyraspasnproleu
859095
thrpheglyglyglythrlysvalgluilelys
100105
<210>3
<211>6
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>d48vhcrd1
<400>3
serglyseralamethis
15
<210>4
<211>17
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>d48vhcdr2
<400>4
valileserhisaspglyasnileileglntyrhisaspservallys
151015
gly
<210>5
<211>15
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>d48vhcdr3
<400>5
aspvaltrpleuleuproalathrilesertyralapheaspphe
151015
<210>6
<211>11
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>d48vlcdr1
<400>6
argalaserglnglyileserasnserileala
1510
<210>7
<211>7
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>d48vlcdr2
<400>7
alaalatyrargleuglnser
15
<210>8
<211>9
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>d48vlcdr3
<400>8
glnglntyrtyraspasnproleuthr
15
<210>9
<211>249
<212>prt
<213>人工序列(artificialsequence)
<220>
<223>d48scfv
<400>9
gluvalglnleuvalgluthrglyglyglyvalvalargproglyarg
151015
serleuargleusercysthrthrserglypheserpheserglyser
202530
alamethistrpvalargglnalaproglylysglyleuglutrpval
354045
alavalileserhisaspglyasnileileglntyrhisaspserval
505560
lysglyargphethrileserargaspasnserlysasnvalleuleu
65707580
leuglnmetasnserleuargvalaspaspthralamettyrtyrcys
859095
alaargaspvaltrpleuleuproalathrilesertyralapheasp
100105110
phetrpglyglnglythrmetvalthrvalserseralaserthrgly
115120125
glyglyglyserglyglyglyglyserglyglyglyglyservalile
130135140
trpmetthrglnserproproserleuseralaserileglyaspthr
145150155160
valthrilethrcysargalaserglnglyileserasnserileala
165170175
trptyrglnargargproglylysalaprogluleuleuvaltyrala
180185190
alatyrargleuglnserglyvalproserargleuserglysergly
195200205
serglyalaglutyrthrleuthrilelysasnmetglnprogluasp
210215220
phealathrtyrtyrcysglnglntyrtyraspasnproleuthrphe
225230235240
glyglyglythrlysvalgluilelys
245
<210>10
<211>874
<212>prt
<213>单纯疱疹病毒1(herpessimplexvirus1)
<400>10
alaprothrserproglythrproglyvalalaalaalathrglnala
151015
alaasnglyglyproalathrproalaproproproleuglyalaala
202530
prothrglyaspprolysprolyslysasnlyslysprolysasnpro
354045
thrproproargproalaglyaspasnalathrvalalaalaglyhis
505560
alathrleuarggluhisleuargaspilelysalagluasnthrasp
65707580
alaasnphetyrvalcysproproprothrglyalathrvalvalgln
859095
phegluglnproargargcysprothrargprogluglyglnasntyr
100105110
thrgluglyilealavalvalphelysgluasnilealaprotyrlys
115120125
phelysalathrmettyrtyrlysaspvalthrvalserglnvaltrp
130135140
pheglyhisargtyrserglnphemetglyilephegluaspargala
145150155160
provalpropheglugluvalileasplysileasnalalysglyval
165170175
cysargserthralalystyrvalargasnasnleugluthrthrala
180185190
phehisargaspasphisgluthraspmetgluleulysproalaasn
195200205
alaalathrargthrserargglytrphisthrthraspleulystyr
210215220
asnproserargvalglualaphehisargtyrglythrthrvalasn
225230235240
cysilevalglugluvalaspalaargservaltyrprotyraspglu
245250255
phevalleualathrglyaspphevaltyrmetserprophetyrgly
260265270
tyrarggluglyserhisthrgluhisthrthrtyralaalaasparg
275280285
phelysglnvalaspglyphetyralaargaspleuthrthrlysala
290295300
argalathralaprothrthrargasnleuleuthrthrprolysphe
305310315320
thrvalalatrpasptrpvalprolysargproservalcysthrmet
325330335
thrlystrpglngluvalaspglumetleuargserglutyrglygly
340345350
serpheargpheserseraspalaileserthrthrphethrthrasn
355360365
leuthrglutyrproleuserargvalaspleuglyaspcysilegly
370375380
lysaspalaargaspalametaspargilephealaargargtyrasn
385390395400
alathrhisilelysvalglyglnproglntyrtyrglnalaasngly
405410415
glypheleuilealatyrglnproleuleuserasnthrleualaglu
420425430
leutyrvalarggluhisleuarggluglnserarglysproproasn
435440445
prothrproproproproglyalaseralaasnalaservalgluarg
450455460
ilelysthrthrserserilegluphealaargleuglnphethrtyr
465470475480
asnhisileglnarghisvalasnaspmetleuglyargvalalaile
485490495
alatrpcysgluleuglnasnhisgluleuthrleutrpasngluala
500505510
arglysleuasnproasnalailealaservalthrvalglyargarg
515520525
valseralaargmetleuglyaspvalmetalavalserthrcysval
530535540
provalalaalaaspasnvalilevalglnasnsermetargileser
545550555560
serargproglyalacystyrserargproleuvalserpheargtyr
565570575
gluaspglnglyproleuvalgluglyglnleuglygluasnasnglu
580585590
leuargleuthrargaspalailegluprocysthrvalglyhisarg
595600605
argtyrphethrpheglyglyglytyrvaltyrphegluglutyrala
610615620
tyrserhisglnleuserargalaaspilethrthrvalserthrphe
625630635640
ileaspleuasnilethrmetleugluasphisgluphevalproleu
645650655
gluvaltyrthrarghisgluilelysaspserglyleuleuasptyr
660665670
thrgluvalglnargargasnglnleuhisaspleuargphealaasp
675680685
ileaspthrvalilehisalaaspalaasnalaalametphealagly
690695700
leuglyalaphephegluglymetglyaspleuglyargalavalgly
705710715720
lysvalvalmetglyilevalglyglyvalvalseralavalsergly
725730735
valserserphemetserasnpropheglyalaleualavalglyleu
740745750
leuvalleualaglyleualaalaalaphephealapheargtyrval
755760765
metargleuglnserasnprometlysalaleutyrproleuthrthr
770775780
lysgluleulysasnprothrasnproaspalaserglygluglyglu
785790795800
gluglyglyasppheaspglualalysleualaglualaargglumet
805810815
ileargtyrmetalaleuvalseralametgluargthrgluhislys
820825830
alalyslyslysglythrseralaleuleuseralalysvalthrasp
835840845
metvalmetarglysargargasnthrasntyrthrglnvalproasn
850855860
lysaspglyaspalaaspgluaspaspleu
865870
<210>11
<211>882
<212>prt
<213>单纯疱疹病毒-2(herpessimplexvirus-2)
<400>11
alaproalaalaproalaalaproargalaserglyglyvalalaala
151015
thrvalalaalaasnglyglyproalaserargproproprovalpro
202530
serproalathrthrlysalaarglysarglysthrlyslyspropro
354045
lysargproglualathrproproproaspalaasnalathrvalala
505560
alaglyhisalathrleuargalahisleuarggluilelysvalglu
65707580
asnalaaspalaglnphetyrvalcysproproprothrglyalathr
859095
valvalglnphegluglnproargargcysprothrargproglugly
100105110
glnasntyrthrgluglyilealavalvalphelysgluasnileala
115120125
protyrlysphelysalathrmettyrtyrlysaspvalthrvalser
130135140
glnvaltrppheglyhisargtyrserglnphemetglyilepheglu
145150155160
aspargalaprovalpropheglugluvalileasplysileasnala
165170175
lysglyvalcysargserthralalystyrvalargasnasnmetglu
180185190
thrthralaphehisargaspasphisgluthraspmetgluleulys
195200205
proalalysvalalathrargthrserargglytrphisthrthrasp
210215220
leulystyrasnproserargvalglualaphehisargtyrglythr
225230235240
thrvalasncysilevalglugluvalaspalaargservaltyrpro
245250255
tyraspgluphevalleualathrglyaspphevaltyrmetserpro
260265270
phetyrglytyrarggluglyserhisthrgluhisthrsertyrala
275280285
alaaspargphelysglnvalaspglyphetyralaargaspleuthr
290295300
thrlysalaargalathrserprothrthrargasnleuleuthrthr
305310315320
prolysphethrvalalatrpasptrpvalprolysargproalaval
325330335
cysthrmetthrlystrpglngluvalaspglumetleuargalaglu
340345350
tyrglyglyserpheargpheserseraspalaileserthrthrphe
355360365
thrthrasnleuthrglntyrserleuserargvalaspleuglyasp
370375380
cysileglyargaspalaargglualaileaspargmetphealaarg
385390395400
lystyrasnalathrhisilelysvalglyglnproglntyrtyrleu
405410415
alathrglyglypheleuilealatyrglnproleuleuserasnthr
420425430
leualagluleutyrvalargglutyrmetarggluglnasparglys
435440445
proargasnalathrproalaproleuargglualaproseralaasn
450455460
alaservalgluargilelysthrthrserserilegluphealaarg
465470475480
leuglnphethrtyrasnhisileglnarghisvalasnaspmetleu
485490495
glyargilealavalalatrpcysgluleuglnasnhisgluleuthr
500505510
leutrpasnglualaarglysleuasnproasnalailealaserala
515520525
thrvalglyargargvalseralaargmetleuglyaspvalmetala
530535540
valserthrcysvalprovalalaproaspasnvalilevalglnasn
545550555560
sermetargvalserserargproglythrcystyrserargproleu
565570575
valserpheargtyrgluaspglnglyproleuilegluglyglnleu
580585590
glygluasnasngluleuargleuthrargaspalaleugluprocys
595600605
thrvalglyhisargargtyrpheilepheglyglyglytyrvaltyr
610615620
phegluglutyralatyrserhisglnleuserargalaaspvalthr
625630635640
thrvalserthrpheileaspleuasnilethrmetleugluasphis
645650655
gluphevalproleugluvaltyrthrarghisgluilelysaspser
660665670
glyleuleuasptyrthrgluvalglnargargasnglnleuhisasp
675680685
leuargphealaaspileaspthrvalileargalaaspalaasnala
690695700
alametphealaglyleucysalaphephegluglymetglyaspleu
705710715720
glyargalavalglylysvalvalmetglyvalvalglyglyvalval
725730735
seralavalserglyvalserserphemetserasnpropheglyala
740745750
leualavalglyleuleuvalleualaglyleuvalalaalaphephe
755760765
alapheargtyrvalleuglnleuglnargasnprometlysalaleu
770775780
tyrproleuthrthrlysgluleulysthrseraspproglyglyval
785790795800
glyglygluglyglugluglyalagluglyglyglypheaspgluala
805810815
lysleualaglualaargglumetileargtyrmetalaleuvalser
820825830
alametgluargthrgluhislysalaarglyslysglythrserala
835840845
leuleuserserlysvalthrasnmetvalleuarglysargasnlys
850855860
alaargtyrserproleuhisasngluaspglualaglyaspgluasp
865870875880
gluleu
- 还没有人留言评论。精彩留言会获得点赞!