一种一步合成烯基取代的1,2,3-三氮唑衍生物的方法与流程
本发明属于1,2,3-三氮唑衍生物领域,具体涉及一种一步合成烯基取代的1,2,3-三氮唑衍生物的方法。
背景技术:
1,2,3-三氮唑衍生物被广泛应用于医药、农药、染料、防腐等领域,很多抗真菌药物比如三唑巴坦等都具有1,2,3-三氮唑的骨架,同时该类型化合物也是非常好的耐光性材料。值得一提的是,1,2,3-三氮唑因为与酰胺键具有生物相似性,可以作为生物电子等排体,取代肽主链中的酰胺键,保留受体亲和力,增强蛋白水解稳定性,并提高肿瘤靶向能力。因而,在近几十年,高收率地合成各种官能团化的1,2,3-三氮唑衍生物,成为化学家、医学家非常感兴趣的主题(m.j.paterson,m.a.robb,l.blancafortanda.d.debellis,j.am.chem.soc.,2004,126,2912-2922.;g.biagi,o.livi,v.scartoniande.verugi,farmacosci.,1988,43,597-611.;s.iqbal,m.a.khan,k.javaid,r.sadiq,s.fazal-ur-rehman,m.i.choudharyandf.z.basha,bioorg.chem.,2017,74,72-81.)。
传统制备1,2,3-三氮唑的方法是通过叠氮化物与炔烃作为起始原料合成得到的。(1)热诱导的1,3-偶极环化合成法,该方法是由迈克尔教授于19世纪末发现,并在惠思根教授课题组的研究下得到显著拓展。然而该方法得到的产物区域选择性相对较差,该策略应用非常受限。(2)一价铜催化的惠思根1,3-偶极环化反应,沙普利斯教授课题组首次报道该类型反应。(3)有机胺催化策略,反应在氨基酸或胺的催化下进行。然而后两种策略都需要预制备烯基叠氮底物,该原料极不稳定,容易发生各类型裂解,且非商业可得,不具备工业化大规模应用的潜力。(a.michael,j.prakt.chem.,1893,48,94.;r.huisgen,angew.chem.int.ed.engl.,1963,2,565.;r.huisgen,angew.chem.int.ed.engl.1963,2,633.;j.e.hein,j.c.tripp,l.b.krasnova,k.b.sharplessandv.v.fokin,angew.chem.int.ed.2009,48,8018-8021.)。
其中,烯基取代的1,2,3-三氮唑是合成1,2,3-三氮唑结构药物的主要中间体,随着医药、染料、农药等行业的迅速发展,国内外对烯基取代的1,2,3-三氮唑的需求日益增加。因此,研究更优的烯基取代的1,2,3-三氮唑合成工艺十分必要。
技术实现要素:
针对以上现有技术存在的缺点和不足之处,本发明的目的在于提供一种一步合成烯基取代的1,2,3-三氮唑衍生物的方法。
本发明目的通过以下技术方案实现。
一种一步合成1,2,3-三氮唑衍生物的方法,包括以下步骤:
在反应器中,加入化合物1、化合物2、化合物3、金属催化剂、碱和溶剂,在25~130℃下搅拌反应,反应结束后冷却至室温,减压旋蒸除去溶剂即可得到粗产物,粗产物经柱层析提纯得到所述1,2,3-三氮唑衍生物;
所述的化合物1是指具有式(1)结构的1,3-二羰基化合物;所述的化合物2是指端炔类化合物,所述的化合物3是指叠氮化物;
其中,r1、r2表示烷基、芳基、亚氨基或氢,但r1、r2不同时为氢。
上述合成方法所涉及的反应方程式如下式所示:
优选的,所述的反应器为schlenk管(史兰克管)。
优选的,所述化合物1,化合物2和化合物3的摩尔比为1:(1~20):(1~20);优选1:1:1.6。
优选的,所述的金属催化剂为碳酸银、硫酸银、醋酸银、三氟乙酸银、三氟甲烷磺酸银、六氟锑酸银、碘化银、氟化银、溴化银中的一种或两种以上的混合。
优选的,所述的碱为氢氧化钠、氢氧化钾、氢氧化钙、碳酸铯、碳酸氢钾、碳酸钾等无机碱或醇钠、氨基钠、三苯甲基钠、叔丁醇钾等有机碱中的一种或两种以上的混合。
优选的,所述的溶剂为乙腈、四氢呋喃、乙醇、叔戊醇、异丙醇、异丁醇、n,n-二甲基甲酰胺、二甲基亚砜、甲苯、对二甲苯、甲醇和水中的一种或两种以上的混合。
优选的,所述反应的时间为1~24h。
优选的,所述的柱层析提纯所用的洗脱液为石油醚:二氯甲烷:乙酸乙酯的体积比为(0~20):(0~20):1的混合溶剂。
本发明的合成方法具有如下优点及有益效果:
本发明以端炔类化合物,1,3-二酮类化合物,叠氮化物为原料一步合成烯基取代的1,2,3-三氮唑衍生物,具有合成步骤简单、原料商业可得、合成方法对功能团兼容性好、原子经济性高的优点。
附图说明
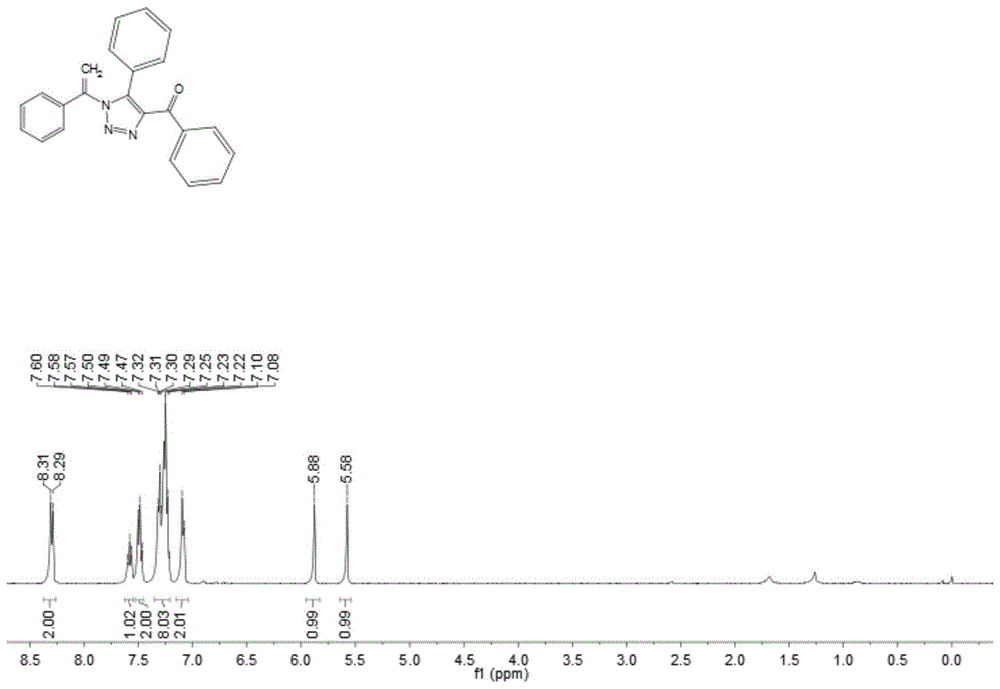
图1和图2分别为实施例1所得产物的氢谱图和碳谱图;
图3和图4分别为实施例2所得产物的氢谱图和碳谱图;
图5和图6分别为实施例3所得产物的氢谱图和碳谱图;
图7和图8分别为实施例4所得产物的氢谱图和碳谱图;
图9和图10分别为实施例5所得产物的氢谱图和碳谱图;
图11和图12分别为实施例6所得产物的氢谱图和碳谱图。
具体实施方式
下面结合实施例及附图对本发明作进一步详细的描述,但本发明的实施方式不限于此。
实施例1
在schlenk管中加入0.25毫摩尔二苯甲酰基甲烷、0.25毫摩尔苯乙炔、0.4毫摩尔叠氮基三甲基硅烷、0.05毫摩尔硝酸银,0.25毫摩尔碳酸钾,1.5毫升二甲基亚砜,在77.5℃,搅拌反应12小时后,停止加热及搅拌,冷却至室温,减压旋蒸除去溶剂,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液的体积比为20:1:1的石油醚:二氯甲烷:乙酸乙酯混合溶剂,产率78%。
所得产物的氢谱图及碳谱图分别如图1和图2所示,结构表征数据如下:
1hnmr(400mhz,cdcl3)δ8.30(d,j=8.0hz,2h),7.58(t,j=6.8hz,1h),7.49(t,j=7.6hz,2h),7.32–7.22(m,8h),7.09(d,j=7.2hz,2h),5.88(s,1h),5.58(s,1h)。
13cnmr(101mhz,cdcl3)δ186.64,143.22,142.38,142.11,137.23,134.69,133.21,130.80,129.81,129.75,129.63,128.71,128.35,128.22,126.02,125.90,115.68。
ir(kbr):3054,1660,1483,1448,1257,1178,1008,914,770,693cm-1。
hrms(esi):calcd.forc23h18n3o[m+h]+:352.1444;found:352.1445。
根据以上数据推断所得产物的结构如下式所示:
实施例2
在schlenk管中加入0.25毫摩尔二苯甲酰基甲烷、0.3毫摩尔4-甲基苯乙炔、0.4毫摩尔叠氮基三甲基硅烷、0.05毫摩尔溴化银,0.25毫摩尔碳酸氢钾,1.5毫升二甲基亚砜,在25℃,搅拌反应16小时后,停止加热及搅拌,冷却至室温,减压旋蒸除去溶剂,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液的体积比为20:2:1的石油醚:二氯甲烷:乙酸乙酯混合溶剂,产率36%。
所得产物的氢谱图及碳谱图分别如图3和图4所示,结构表征数据如下:
1hnmr(400mhz,cdcl3)δ8.29(d,j=7.6hz,2h),7.58(t,j=7.3hz,1h),7.48(t,j=7.6hz,2h),7.33–7.24(m,5h),7.02(dd,j=24.8,8.4hz,4h),5.83(s,1h),5.47(s,1h),2.29(s,3h)。
13cnmr(101mhz,cdcl3)δ186.70,143.15,142.27,142.15,139.84,137.26,133.19,131.92,130.80,129.79,129.73,129.43,128.34,128.22,126.07,125.74,114.76,21.23。
ir(kbr):3057,1660,1484,1450,1420,1258,1179,1009,920,823,745,695,527cm-1。
hrms(esi):calcd.forc24h20n3o[m+h]+:366.1601;found:366.1600。
根据以上数据推断所得产物得结构如下式所示:
实施例3
在schlenk管中加入0.25毫摩尔二苯甲酰基甲烷、0.25毫摩尔4-甲氧基苯乙炔、0.4毫摩尔叠氮基三甲基硅烷、0.05毫摩尔三氟甲烷磺酸银,0.5毫摩尔叔丁醇钾,1.5毫升二甲基亚砜,130℃,搅拌反应12小时后,停止加热及搅拌,冷却至室温,减压旋蒸除去溶剂,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液的体积比为20:1:1的石油醚:二氯甲烷:乙酸乙酯混合溶剂,产率37%。
所得产物的氢谱图及碳谱图分别如图5和图6所示,结构表征数据如下:
1hnmr(400mhz,cdcl3)δ8.29(d,j=7.6hz,2h),7.58(t,j=7.2hz,1h),7.48(t,j=7.6hz,2h),7.33–7.25(m,5h),7.03(d,j=8.4hz,2h),6.76(d,j=8.4hz,2h),5.76(s,1h),5.42(s,1h),3.76(s,3h)。
13cnmr(101mhz,cdcl3)δ186.70,160.69,143.19,142.11,141.97,137.29,133.20,130.82,129.82,129.71,128,36,128.24,127.32,126.13,114.15,113.73,55.42。
ir(kbr):3068,1660,1484,1450,1420,1258,1179,1009,920,823,745,695,531cm-1。
hrms(esi):calcd.forc24h19n3nao2[m+na]+:404.1369;found:404.1374。
根据以上数据推断所得产物得结构如下式所示:
实施例4
在schlenk管中加入0.25毫摩尔n-乙酰乙酰苯胺、2.625毫摩尔苯乙炔、2.625毫摩尔叠氮基三甲基硅烷、0.05毫摩尔碳酸银,0.5毫摩尔叔丁醇钾,1.5毫升二甲基亚砜,80℃,搅拌反应12小时后,停止加热及搅拌,冷却至室温,减压旋蒸除去溶剂,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液的体积比为20:1:1的石油醚:二氯甲烷:乙酸乙酯混合溶剂,产率58%。
所得产物的氢谱图及碳谱图分别如图7和图8所示,结构表征数据如下:
1hnmr(400mhz,cdcl3)δ9.08(s,1h),7.71(d,j=8.0hz,2h),7.40–7.36(m,5h),7.18–7.16(m,3h),6.05(s,1h),5.62(s,1h),2.44(s,3h)。
13cnmr(101mhz,cdcl3)δ159.29,141.96,138.48,138.10,137.77,134.15,130.15,129.22,125.73,124.50,119.96,115.29,9.57。
ir(kbr):3058,2926,1681,1598,1528,1443,1312,1247,1160,1057,980,913,883,774,755,693,587,509cm-1。
hrms(esi):calcd.forc18h16n4nao[m+na]+:327.1216;found:327.1217。
根据以上数据推断所得产物得结构如下式所示:
实施例5
在schlenk管中加入0.25毫摩尔3-氯乙酰乙酰苯胺、5毫摩尔苯乙炔、5毫摩尔叠氮基三甲基硅烷、0.05毫摩尔硫酸银,0.5毫摩尔碳酸钾,1.5毫升n,n-二甲基甲酰胺,80℃,搅拌反应12小时后,停止加热及搅拌,冷却至室温,减压旋蒸除去溶剂,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液的体积比为20:1:1的石油醚:二氯甲烷:乙酸乙酯混合溶剂,产率52%。
所得产物的氢谱图及碳谱图分别如图9和图10所示,结构表征数据如下:
1hnmr(400mhz,cdcl3)δ9.08(s,1h),7.90(s,1h),7.49(d,j=8.0hz,1h),7.40(d,j=7.2hz,3h),7.29(t,j=8.0hz,1h),7.18–7.12(m,3h),6.06(s,1h),5.62(s,1h),2.44(s,3h)。
13cnmr(101mhz,cdcl3)δ159.30,141.91,138.92,138.33,138.18,134.90,134.08,130.18,130.16,129.24,125.71,124.49,120.00,117.84,115.36,9.56。
ir(kbr):2926,1683,1593,1522,1483,1426,1274,1159,1099,912,774,695,441cm-1。
hrms(esi):calcd.forc18h15cln4nao[m+na]+:361.0827;found:361.0828。
根据以上数据推断所得产物得结构如下式所示:
实施例6
在schlenk管中加入0.25毫摩尔2-甲基乙酰乙酰苯胺、0.25毫摩尔苯乙炔、0.25毫摩尔叠氮基三甲基硅烷、0.05毫摩尔碳酸银,0.5毫摩尔碳酸钾,1.5毫升n,n-二甲基甲酰胺,80℃,搅拌反应24小时后,停止加热及搅拌,冷却至室温,减压旋蒸除去溶剂,再通过柱层析分离纯化,得到目标产物,所用的柱层析洗脱液的体积比为20:1:1的石油醚:二氯甲烷:乙酸乙酯混合溶剂,产率41%。
所得产物的氢谱图及碳谱图分别如图11和图12所示,结构表征数据如下:
1hnmr(400mhz,cdcl3)δ9.02(s,1h),8.10(d,j=8.0hz,1h),7.39(d,j=6.4hz,3h),7.26(m,2h),7.18(d,j=6.4hz,2h),7.10(t,j=7.4hz,1h),6.05(s,1h),5.62(s,1h),2.43(d,j=5.6hz,6h)。
13cnmr(101mhz,cdcl3)δ159.29,142.00,138.67,137.97,135.68,134.19,130.65,130.12,129.21,128.68,126.90,125.75,124.98,122.21,115.24,17.87,9.54。
ir(kbr):2924,1685,1611,1588,1529,1456,1331,1254,1160,887,775,755,696,627cm-1。
hrms(esi):calcd.forc19h18n4nao[m+na]+:341.1373;found:341.1377。
根据以上数据推断所得产物得结构如下式所示:
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其它的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!