一种脂肪酶在拆分外消旋2-溴代异戊酸乙酯中的应用的制作方法
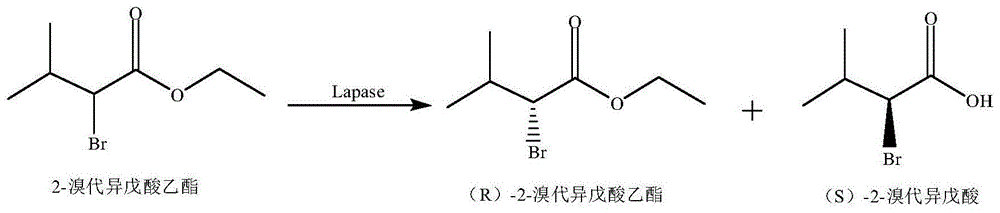
本发明属于生物催化技术领域,涉及一种脂肪酶立体选择性催化水解拆分2-溴代异戊酸乙酯对映体合成单一构型的(r)-2-溴代异戊酸乙酯对映体的应用。
(二)
背景技术:
氟胺氰菊酯是非环丙烷梭酸类的拟除虫菊酯,具有和氰戊菊酯相似的结构。它共有四个光学异构体。工业品是由右旋酸和消旋氰醇组成的一对高效体,具有广谱的杀虫活性具触杀和胃毒作用,还有拒食和驱避活性。其毒力和氰戊菊酯相当能有效地防治棉花、果树、蔬菜、玉米、茶叶、烟草等作物上包括鳞翅目、鞘翅目、同翅目、和双翅目、在内的主要害虫。另外它还能防治牲畜害虫如血红扁头蜂、羊鼻蝇角蝇、厩蝇、狗栉头蚤等。文献中多数用原料d-缬氨酸来合成得到氟胺氰菊酯,d-缬氨酸法虽然可以直接得到手性产物,但价格比较昂贵。而从价格较为低廉的2-溴代异戊酸乙酯来合成氟胺氰菊酯的消旋体,再通过手性拆分来得到工业品应用的高效体,可以降低生产成本,提高经济效益。然而我们提供了一种脂肪酶来催化水解拆分2-溴代异戊酸乙酯来高效生产(r)-2-溴代异戊酸乙酯的有效方法,可以直接得到手性产物,从而大大降低了成本。
脂肪酶(lipase,ec3.1.1.3)全称为三酰基甘油酰基水解酶(triacylglycerolacylhydrolase),是目前研究与工业化应用最多的一类水解酶。脂肪酶能催化酯水解、酯合成、醇解、酸解、酯酯交换和氨解反应。脂肪酶广泛存在于自然界的各种生物体,特别是在微生物和动植物组织中。动物脂肪酶主要存在于胰脏等器官组织,比如猪肝酯酶和猪胰脂肪酶,但由于动物脂肪酶活性较低、酶提取纯化成本较高和原料来源有限等因素,限制了其在工业中的应用。微生物脂肪酶来源丰富,种类繁多,不受季节气候等因素的影响,微生物生长产酶周期较短,而且具有耐有机溶剂、底物专一性强、催化选择性高和催化活性高等特点,因而微生物来源的脂肪酶有较高的工业化应用价值。目前市场上大部分商品化脂肪酶都通过细菌、真菌和酵母等微生物培养发酵获得。丹麦novonordisk公司、日本amano公司和美国genencor公司等主要酶制造商开发了多种的商品化酶制剂。这些酶制剂公司利用分子改造技术对微生物脂肪酶进行改造,提高酶活力、稳定性和立体选择性等酶学性质,以满足不同工业领域应用的需求。因而构建脂肪酶基因工程菌从而大量生产重组脂肪酶具有十分重要意义。
(三)
技术实现要素:
本发明目的是提供一种立体选择性脂肪酶在生物法拆分2-溴代异戊酸乙酯中的应用,可以直接获得手性产物,大大降低成本。
本发明采用的技术方案是:
本发明提供一种脂肪酶在拆分2-溴代异戊酸乙酯中的应用(如图1所示),所述脂肪酶的氨基酸序列如seqidno.1所示,编码基因序列为seqidno.2所示,脂肪酶基因源自米曲霉wz007(aspergillusoryzaewz007),该菌保藏于中国典型培养物保藏中心,地址:中国武汉,武汉大学,430072,保藏编号:cctccno:m206105,保藏日期:2006年10月8日,已在先前申请专利(中国专利cn101186938)中提交了相关菌种保藏信息并披露了其遗传资源来源。本发明在此专利申请的基础上,进行目标脂肪酶和基因的挖掘。具体的应用方法为:从本米曲霉wz007出发,提取mrna经反转录得到cdna,根据ncbi查得的米曲霉基因组genbank:nwui02000090.1碱基序列的基础上,设计上游引物为5'-ccatgggcatgaagattcaaaaactcattctgtacagtct-3'和下游引物为5'-ctcgagttaatatgcatactttgcaatgtcaggc-3',进行pcr,得到碱基基因序列seqidno.2片段,测序验证正确,将该片段连接至载体pet-28b(+),转化至rosetta感受态,经发酵培养获得的湿菌体提取的粗酶为催化剂,以2-溴代异戊酸乙酯为底物,以ph7.0磷酸盐缓冲液为反应介质,在20-45℃、800-1000rpm条件下进行拆分反应,反应完全后,将反应液分离纯化,获得产物(r)-2-溴代异戊酸乙酯。所述催化剂用量以缓冲液体积计为15-30g/l(优选30g/l),所述底物终浓度以缓冲液体积计为5-10g/l(优选6g/l)。
进一步,优选反应时间为3-7h,更优选反应条件为35℃、1000rpm反应5h。
进一步,所述缓冲液为ph7.0,0.2mm的na2hpo4/nah2po4缓冲溶液。
进一步,所述催化剂按如下方法制备:将含脂肪酶编码基因的工程菌(优选大肠杆菌rosetta)接种在lb培养基中,37℃培养od600至0.4-0.6,加iptg至终浓度0.02mm,30℃培养10-12h,菌液8000rpm,4℃离心10min,收集菌体,再用pbs缓冲液洗涤菌体2次,8000rpm,4℃离心10min,收集菌体,冻干,得到脂肪酶粗酶粉;lb培养基组成:胰蛋白胨10g/l、酵母粉5g/l、nacl5g/l,溶剂为去离子水,ph值自然。
进一步,本发明所述反应液分离纯化的方法为:反应结束后,反应液用4mmhcl进行酸化至ph2.0,然后用等体积乙酸乙酯萃取,分液漏斗分离出有机相,再经纯水洗涤两次,饱和nacl洗涤两次,干燥,旋蒸,得到产物(r)-2-溴代异戊酸乙酯。
本发明脂肪酶氨基酸序列如seqidno.1所示:
mkiqklilykfaneltasglipskaltclngyaiidlnsihrhnpspenlsiypykaksdapysiaentlragihiprsfshkrdkkipvllvpgtavpaaitfyfnfgklrralpeselvwidlpqaslddiqlsaeyvayalnyvsaltsskiaviswsqgaldiqwalkywpstrgvvndfiaispdfhgtivkwlvcpllndlactpsiwqqgwdanfiqalrsqggdsayvptttiyssfdkivrpmsgenasarlldyrgvgvsnnhlqticannaagglythegvlynplawaltvdallhdgpsnitridtqkiceqvlppyleltdmlgtealllvalakiltyspkvsgepdiakyay
由于氨基酸序列的特殊性,任何含有seqidno.1所示氨基酸序列的多肽的片段或其变体,如其保守性变体、生物活性片段或衍生物,只要该多肽的片段或多肽变体与前述氨基酸序列同源性在90%以上、且具有相同的酶活性,均属于本发明保护范围之列。具体的,所述改变可包括氨基酸序列中氨基酸的缺失、插入或替换;其中,对于变体的保守性改变,所替换的氨基酸具有与原氨基酸相似的结构或化学性质,如用亮氨酸替换异亮氨酸,变体也可具有非保守性改变,如用色氨酸替换甘氨酸。
本发明所述蛋白的片段、衍生物或类似物是指基本上保持本发明所述的蛋白酶相同的生物学功能或活性的蛋白,可以是下列情形:(ⅰ)一个或多个氨基酸残基被保守或非保守氨基酸残基(优选的是保守氨基酸残基)取代,并且取代的氨基酸可以是也可以不是由遗传密码子编码的;(ⅱ)一个或多个氨基酸残基上的某个基团被其它基团取代;(iii)成熟蛋白与另一种化合物(比如延长蛋白半衰期的化合物,例如聚乙二醇)融合;(ⅳ)附加的氨基酸序列融合进成熟的蛋白而形成的蛋白序列(如用来纯化此蛋白的序列或蛋白原序列)。
所述蛋白可以是重组蛋白、天然蛋白或合成蛋白,可以是纯天然纯化的产物,或是化学合成的产物,或使用重组技术从原核或真核宿主(例如:细菌、酵母、高等植物、昆虫和哺乳动物细胞)中产生。根据重组生产方案所用的宿主,本发明的蛋白可以是糖基化的。本发明的蛋白还可以包括或不包括起始的甲硫氨酸残基。
本发明所述脂肪酶的编码基因核苷酸序列如seqidno.2所示:
atgaaaatccagaaactgattttatataaatttgcaaacgagctcaccgcatcaggcctgataccttcaaaggcactgacatgcctgaatggctacgcgatcattgacctcaattcgattcaccgtcacaacccatccccagaaaacttgagcatatacccatacaaagcaaagagcgatgcgccttactccattgcggaaaatactctccgggctggaattcacattcctagatcattctcacacaaacgggacaagaaaataccggtgctcctggtaccaggaactgctgttcctgcggccataaccttttatttcaactttggcaagttgaggagagccttacccgaaagtgagctagtttggatcgatctccctcaggcctcgttggatgacattcaattgagcgctgaatatgtcgcctatgcgctcaattatgtttccgctttgacctcatctaagattgccgtgatttcttggtcccaaggtgcactggatattcagtgggcactgaagtactggccatctacccggggcgtcgtcaacgacttcattgctatcagccccgacttccatggaacaatagtcaagtggctggtatgccctctattaaatgatttagcctgtactccttcgatttggcagcaagggtgggatgcaaactttatacaggccttgcggagccaagggggagactctgcctatgtccccacgaccaccatttactcttcattcgacaagattgtgcgacccatgagtggggaaaatgcttctgctcggctactggactacaggggggtgggcgtttccaataaccatctacagaccatctgcgcaaataatgccgctggtggcctctatacgcatgaaggcgtgttgtacaaccctcttgcatgggcccttactgttgacgcactccttcacgatgggcctagcaatattacgcgaatcgatacccagaagatctgtgaacaagtacttccgccatatctcgaattaactgatatgctgggaaccgaagccctccttttagtagccctagcaaagattcttacatattccccgaaagtctccggtgagcctgacattgcaaagtatgcatattaa
由于核苷酸序列的特殊性,任何seqidno.2所示多核苷酸的变体,只要其与该多核苷酸具有70%以上同源性、且具有相同的功能,均属于本发明保护范围之列。所述多核苷酸的变体是指一种具有一个或多个核苷酸改变的多核苷酸序列。此多核苷酸的变体可以是天然发生的等位变异体或非天然发生的变异体,包括取代变异体、缺失变异体和插入变异体。如本领域所知的,等位变异体是一个多核苷酸的替换形式,它可能是一个或多个核苷酸的取代、缺失或插入,但不会从实质上改变其编码的氨基酸的功能。
另外,可与seqidno:2所示多核苷酸序列杂交的多核苷酸(至少具有50%同源性,优选具有70%同源性),也在本发明保护范围之列,特别是在严格条件下可与本发明所述核苷酸序列杂交的多核苷酸。所述“严格条件”是指:(1)在较低离子强度和较高温度下的杂交和洗脱,如0.2ssc,0.1%sds,60℃;或(2)杂交时加用变性剂,如50%(v/v)甲酰胺,0.1%小牛血清,0.1%ficoll,42℃;或(3)仅在两条序列之间的同源性至少在95%以上,更好是97%以上时才发生杂交。并且,可杂交的多核苷酸编码的蛋白与seqidno:1所示的蛋白有相同的生物学功能和活性。
本发明还涉及含有所述编码基因的重组载体,以及利用所述重组载体转化得到的重组基因工程菌。
与现有技术相比,本发明的有益效果主要体现在:本发明提供了一种脂肪酶基因核苷酸序列;该脂肪酶基因可与表达载体连接构建得到含该基因的胞内表达重组质粒,再转化至大肠杆菌菌株中,获得重组大肠杆菌,再利用重组大肠杆菌或重组脂肪酶为生物催化剂催化拆分2-溴代异戊酸乙酯,可以得到产物(r)-2-溴代异戊酸乙酯,对映体过量值>99%和转化率达到50.8%,产物(r)-2-溴代异戊酸乙酯的质量收率达到96.4%。本发明生物催化的手性合成反应具有条件温和、效率高,高度的化学选择性、区域选择性以及对映体选择性等优点,而且生物催化过程具有无毒、无污染和能耗低等特点,是一种环境友好的合成方法。
(四)附图说明
图1为脂肪酶对映选择性水解拆分2-溴代异戊酸乙酯的反应示意图;
图2为外消旋2-溴代异戊酸乙酯标样气相色谱图;
图3为实施例4脂肪酶催化2-溴代异戊酸乙酯水解反应5h的气相色谱图。
(五)具体实施方式
下面结合具体实施例对本发明进行进一步描述,但本发明的保护范围并不仅限于此,本领域的普通技术人员根据这些实施方式所做出的方法上的变换均包含在本发明的保护范围内。
实施例1米曲霉wz007发酵,cdna制备,脂肪酶基因克隆和工程菌构建
1、米曲霉wz007发酵条件:斜面培养基(g/l):去皮马铃薯200,蔗糖20,琼脂20,溶剂为去离子水,ph自然。发酵培养基(g/l):蛋白胨20,橄榄油1%(v/v),kh2po41,mgso40.5,nacl0.5,溶剂为去离子水,ph7.0。
将米曲霉wz007(aspergillusoryzaewz007)接种至斜面培养基,30℃培养6-8d,获得斜面菌种。米曲霉wz007保藏于中国典型培养物保藏中心,地址:中国武汉,武汉大学,430072,保藏编号:cctccno:m206105,保藏日期:2006年10月8日,已在专利申请cn101186938a中公开。
取斜面菌种接种至含100ml发酵培养基的500ml摇瓶中,在温度30℃,转速200rpm的恒温摇床培养12h,制成种子液。将1l种子液倒入到含18l发酵培养基的30l发酵罐进行发酵培养,其中温度和转速分别控制在30℃和200rpm,发酵培养48h收集湿菌体。
2、米曲霉wz007cdna制备:取1g上述米曲霉湿菌体,使用全式金公司的transzolupplusrnakit试剂盒提取mrna,再使用toyobo公司的revertraaceqpcrrtkit,高效率地合成适用于realtimepcr的cdna模板。
3、米曲霉脂肪酶基因的克隆:根据ncbi查得的米曲霉基因组
genbank:nwui02000090.1碱基序列的基础上,设计上游引物为
5'-ccatgggcatgaagattcaaaaactcattctgtacagtct-3'和下游引物为5'-ctcgagttaatatgcatactttgcaatgtcaggc-3',以cdna为模板,进行pcr,得到核苷酸序列为seqidno.2所示的基因片段,测序验证正确。seqidno.2所示基因片段的编码蛋白氨基酸序列为seqidno.1所示。
4、大肠杆菌工程菌的构建:将该seqidno.2所示的基因片段连接至载体pet-28b(+),转化至大肠杆菌rosetta感受态,获得含脂肪酶的大肠杆菌工程菌(记为工程菌m5)。
实施例2含脂肪酶的大肠杆菌工程菌(m5)的发酵培养
将实施例1获得的大肠杆菌工程菌(m5)接种在lb培养基中,37℃培养od600至为0.5(大概培养2h),加iptg至终浓度0.02mm,30℃培养10-12h。300ml菌液8000rpm,4℃离心10min,收集菌体,再用pbs缓冲液洗涤菌体2次,8000rpm,10min收集菌体。将收集的菌体冻干后得到脂肪酶粗酶粉,记为脂肪酶m5,放于4℃冰箱保存。lb培养基组成:胰蛋白胨10g/l、酵母粉5g/l、nacl5g/l,溶剂为去离子水,ph自然。
实施例3酶催化拆分2-溴代异戊酸乙酯的反应
称取0.03g实施例2方法制备的脂肪酶粗酶粉于2mlep管中,加入1mlpb(ph7.0、0.2mm)作为反应溶剂,然后加入0.006g底物2-溴代异戊酸乙酯,以不加菌体为空白对照,置于35℃,1000rpm恒温混匀仪中反应3h。反应结束后,反应液经4mmhcl酸化,再加入1ml乙酸乙酯,涡旋振荡器振荡2min,充分萃取,离心(1200rpm,3min),得到有机相。取700μl乙酸乙酯层通过气相色谱检测菌体的立体选择性及酶催化水解活性,得到底物的对映体过量值>99%和转化率达到50.8%。
具体气相分析条件:采用agilent6890气相色谱仪,bgb-175手性毛细管色谱柱(30.0m×0.25mm×0.25um),fid检测器;检测条件为柱温从初始温度100℃(恒温保持5min)升温至120℃,升温速率2℃/min,进样温度250℃,检测器温度250℃,空气流量和氢气流量分别为300ml/min和30ml/min。载气为高纯n2,柱头压98.7kpa;尾吹气流量30.0ml·min-1;分流比30:1,进样体积为1ul。如gc的结果所示,(r)-2-溴代异戊酸乙酯和(s)-2-溴代异戊酸乙酯的保留时间分别为8.58min和8.75min,见图2。
实施例4不同脂肪酶水解拆分2-溴代异戊酸乙酯的效果比较
在ph7.0,0.2mm的na2hpo4/nah2po4缓冲溶液1ml中,加入终浓度30g/l的不同脂肪酶(实施例2制备的脂肪酶粗酶粉、novozym435、lipozymetlim、lipozymermim、amanolipasepsim),0.006g底物2-溴代异戊酸乙酯,于恒温混匀仪35℃,1000rpm条件下反应5h,取反应液按实施例1方法检测(r)-2-溴代异戊酸乙酯的对映体过量值和转化率,结果见表1所示。结果显示,在35℃反应5h后,脂肪酶novozym435、lipozymetlim、lipozymermim、psim对底物2-溴代异戊酸乙酯两种构型都没有水解拆分活性,则以上四种商品脂肪酶对底物2-溴代异戊酸乙酯都没有对映体选择性,而当脂肪酶粗酶粉催化反应时,产物(r)-2-溴代异戊酸乙酯的ee值>99%,转化率为50.8%,气相色谱图3所示。
表1不同脂肪酶催化2-溴代异戊酸乙酯的水解拆分效果比较
实施例5反应时间对酶动力学水解拆分2-溴代异戊酸乙酯的影响
在ph7.0,0.2mm的na2hpo4/nah2po4缓冲溶液1ml中,加入终浓度30g/l的实施例2方法制备的脂肪酶粗酶粉,0.006g2-溴代异戊酸乙酯,于恒温混匀仪35℃,1000rpm条件下反应不同时间(3~6h),取反应液按实施例1方法检测(r)-2-溴代异戊酸乙酯的对映体过量值和转化率,结果见表2所示。
结果表明,反应5h后,产物(r)-2-溴代异戊酸乙酯的对映体过量值已达到最高,对映体过量值>99%,转化率为50.8%,当反应时间大于5h后,产物(r)-2-溴代异戊酸乙酯的对映体过量值逐渐在升高,转化率也在增大。
表2反应时间对酶催化反应的影响
实施例6反应温度对酶动力学水解拆分2-溴代异戊酸乙酯的影响
在ph7.0,0.2mm的na2hpo4/nah2po4缓冲溶液1ml中,加入终浓度30g/l的实施例2制备的脂肪酶粗酶粉,0.006g2-溴代异戊酸乙酯,于恒温混匀仪不同温度(20-45℃),1000rpm条件下反应5h,取反应液按实施例1方法检测(r)-2-溴代异戊酸乙酯的对映体过量值和转化率,结果见表3所示。
结果说明,在反应温度为35℃时,(r)-2-溴代异戊酸乙酯的对映体过量值最高,其ee值>99%。当反应温度高于35℃或者低于35℃时,(r)-2-溴代异戊酸乙酯的转化率和对映体过量值都会下降,说明温度对脂肪酶m5的光学选择性具有很大的影响。
表3反应温度对反应的影响
实施例7产物(r)-2-溴代异戊酸乙酯的分离提取
在50ml圆底烧瓶中加入20mlph7.0,0.2mmna2hpo4/nah2po4缓冲溶液,称取0.3g实施例2制备的脂肪酶粗酶粉,再加入终浓度5g/l的2-溴代异戊酸乙酯,用50mmnaoh进行流加滴定反应,控制反应ph维持在7.0,在磁力搅拌器35℃,600rpm条件下反应6h。反应结束后得到的反应液,用4mmhcl进行酸化至ph2.0,然后用等体积的乙酸乙酯萃取,分液漏斗分离出有机相,再经纯水洗涤两次,饱和nacl洗涤两次,干燥,旋蒸,得到最终产物,并称重,产物(r)-2-溴代异戊酸乙酯的质量收率达到96.4%。
序列表
<110>浙江工业大学
<120>一种脂肪酶在拆分外消旋2-溴代异戊酸乙酯中的应用
<160>2
<170>siposequencelisting1.0
<210>1
<211>368
<212>prt
<213>米曲霉(aspergillusoryzae)
<400>1
metlysileglnlysleuileleutyrlysphealaasngluleuthr
151015
alaserglyleuileproserlysalaleuthrcysleuasnglytyr
202530
alaileileaspleuasnserilehisarghisasnproserproglu
354045
asnleuseriletyrprotyrlysalalysseraspalaprotyrser
505560
ilealagluasnthrleuargalaglyilehisileproargserphe
65707580
serhislysargasplyslysileprovalleuleuvalproglythr
859095
alavalproalaalailethrphetyrpheasnpheglylysleuarg
100105110
argalaleuproglusergluleuvaltrpileaspleuproglnala
115120125
serleuaspaspileglnleuseralaglutyrvalalatyralaleu
130135140
asntyrvalseralaleuthrserserlysilealavalilesertrp
145150155160
serglnglyalaleuaspileglntrpalaleulystyrtrpproser
165170175
thrargglyvalvalasnasppheilealaileserproaspphehis
180185190
glythrilevallystrpleuvalcysproleuleuasnaspleuala
195200205
cysthrproseriletrpglnglnglytrpaspalaasnpheilegln
210215220
alaleuargserglnglyglyaspseralatyrvalprothrthrthr
225230235240
iletyrserserpheasplysilevalargprometserglygluasn
245250255
alaseralaargleuleuasptyrargglyvalglyvalserasnasn
260265270
hisleuglnthrilecysalaasnasnalaalaglyglyleutyrthr
275280285
hisgluglyvalleutyrasnproleualatrpalaleuthrvalasp
290295300
alaleuleuhisaspglyproserasnilethrargileaspthrgln
305310315320
lysilecysgluglnvalleuproprotyrleugluleuthraspmet
325330335
leuglythrglualaleuleuleuvalalaleualalysileleuthr
340345350
tyrserprolysvalserglygluproaspilealalystyralatyr
355360365
<210>2
<211>1107
<212>dna
<213>米曲霉(aspergillusoryzae)
<400>2
atgaaaatccagaaactgattttatataaatttgcaaacgagctcaccgcatcaggcctg60
ataccttcaaaggcactgacatgcctgaatggctacgcgatcattgacctcaattcgatt120
caccgtcacaacccatccccagaaaacttgagcatatacccatacaaagcaaagagcgat180
gcgccttactccattgcggaaaatactctccgggctggaattcacattcctagatcattc240
tcacacaaacgggacaagaaaataccggtgctcctggtaccaggaactgctgttcctgcg300
gccataaccttttatttcaactttggcaagttgaggagagccttacccgaaagtgagcta360
gtttggatcgatctccctcaggcctcgttggatgacattcaattgagcgctgaatatgtc420
gcctatgcgctcaattatgtttccgctttgacctcatctaagattgccgtgatttcttgg480
tcccaaggtgcactggatattcagtgggcactgaagtactggccatctacccggggcgtc540
gtcaacgacttcattgctatcagccccgacttccatggaacaatagtcaagtggctggta600
tgccctctattaaatgatttagcctgtactccttcgatttggcagcaagggtgggatgca660
aactttatacaggccttgcggagccaagggggagactctgcctatgtccccacgaccacc720
atttactcttcattcgacaagattgtgcgacccatgagtggggaaaatgcttctgctcgg780
ctactggactacaggggggtgggcgtttccaataaccatctacagaccatctgcgcaaat840
aatgccgctggtggcctctatacgcatgaaggcgtgttgtacaaccctcttgcatgggcc900
cttactgttgacgcactccttcacgatgggcctagcaatattacgcgaatcgatacccag960
aagatctgtgaacaagtacttccgccatatctcgaattaactgatatgctgggaaccgaa1020
gccctccttttagtagccctagcaaagattcttacatattccccgaaagtctccggtgag1080
cctgacattgcaaagtatgcatattaa1107
- 还没有人留言评论。精彩留言会获得点赞!