一种β-环糊精衍生物、其制备方法及制备超分子囊泡的方法与流程
本发明涉及一种β-环糊精衍生物、其制备方法及制备超分子囊泡的方法,属于化工原料合成及医药材料领域。
背景技术:
环糊精(cyclodextrin,cd)是由环糊精葡萄糖基转移酶作用于淀粉和麦芽寡聚糖等葡萄糖聚合物而形成的系列环状低聚糖,最早是由villiers于1891年在淀粉杆菌的淀粉消化液里发现的。环糊精是由d型吡喃葡萄糖通过α-1,4-糖苷键连接而成,根据吡喃葡萄糖单元的数目不同而分为不同的环糊精,如6个吡喃葡萄糖单元的环糊精被命名为α-环糊精,7个吡喃葡萄糖单元的环糊精被命名为β-环糊精以及8个吡喃葡萄糖单元的环糊精被命名为γ-环糊精等(童林荟.环糊精化学-基础与应用[m]:科学出版社,2001)。环糊精具有锥桶状的立体结构,腔外亲水,腔内疏水,因此可以包合水溶性差的客体分子,改善被包合客体分子的物理化学性质(j.szejtli,chemicalreviews,1998,98,1743-1754)。相比于锥桶空腔较小的α-环糊精和生产成本较高的γ-环糊精,β-环糊精以其适中的锥桶空腔大小、低廉的价格、良好的水溶性及生物相容性等优点而广泛地应用于食品、医药、化工及农业等领域。
但β-环糊精的疏水区域及催化活性等有限,β-环糊精的衍生化能够克服β-环糊精自身的缺陷,因此很多β-环糊精的衍生物被合成出来。如中国专利文献cn101195662a公开了一种6-(2-葡萄糖基胺基)-β-环糊精衍生物及其制备方法,以6-o-对甲苯磺酰基-β-环糊精、氨基葡萄糖盐酸盐为起始原料制备得到6-(2-葡萄糖基胺基)-β-环糊精,所得环糊精衍生物具有良好的水溶性和稳定性。但是,由于β-环糊精自身就是d型吡喃葡萄糖的环状衍生物,葡萄糖基胺基的引入,并不能够有效地改变β-环糊精的理化性质,6-(2-葡萄糖基胺基)-β-环糊精衍生物疏水区域依然有限,没有紫外吸收,不利于其的监测与后续应用,不具备抗癌活性,严重限制了其在药物载运领域的应用。因此,在β-环糊精骨架上接枝非葡萄糖基活性基团具有重要的理论意义和应用价值。而二茂铁是一种具有芳香性质的金属有机化合物,具有一定的抗癌活性(l.v.snegur,v.n.babin,a.a.simenel,y.s.nekrasov,l.a.ostrovskayaandn.s.sergeeva,russianchemicalbulletin,2010,59,2167-2178),将二茂铁通过化学键连接到β-环糊精上,有望改变β-环糊精的物理化学性质,拓展其应用范围。
囊泡是由双亲分子分散于水溶液时自发形成的具有封闭双层结构的有序组装体(d.e.discheranda.eisenberg,science,2002,297,967-973),在生物膜模拟、化学催化和药物载运等领域有着广泛的应用。β-环糊精疏水性的空腔可以通过疏水作用包合水溶性较差的客体分子,形成超分子双亲分子,从而进一步自组装形成结构有序的主客体超分子囊泡。基于β-环糊精的主客体超分子囊泡虽然可以有效地运载亲水性抗癌药物,但其对疏水性抗癌药物分子的运载能力却十分有限。
技术实现要素:
针对现有技术存在的不足,本发明提供一种β-环糊精衍生物及其制备方法。本发明通过化学键将二茂铁基团连接到β-环糊精上,反应条件温和,反应产率较高,反应路线适合大规模的工业化生产;所得β-环糊精衍生物疏水区域得到有效扩大,并且具备抗癌作用,同时具有了典型的紫外吸收,利于后续应用和监测,有利于应用于药物载运领域。
本发明还提供一种利用上述β-环糊精衍生物制备超分子囊泡的方法。所得囊泡的水合直径为130-170纳米,具有抗癌作用并易于被癌细胞吞噬,能够有效的运载亲水性和疏水性的药物,在药物载运方面有着巨大的潜在应用价值。
术语说明:
室温:是指25℃±5℃;
式ii化合物:单[6-对甲基苯磺酰基]-β-环糊精;
式iii化合物:单[6-脱氧-n-丁基胺基]-β-环糊精或单[6-脱氧-n-己基胺基]-β-环糊精;
式i化合物:单[6-脱氧-n-丁基胺基-n’-甲基二茂铁]-β-环糊精或者单[6-脱氧-n-己基胺基-n’-甲基二茂铁]-β-环糊精,即β-环糊精衍生物。
本发明化合物编号和结构式编号完全一致,具有相同的指代关系;以化合物结构式为依据。
本发明的技术方案如下:
一种β-环糊精衍生物,其特征在于,具有如下式i所示结构:
其中,式i所示结构中,n为2或3。
根据本发明优选的,所述β-环糊精衍生物是以式ii化合物为初始原料,经与1,4-丁二胺或1,6-己二胺反应,再与二茂铁甲醛反应,然后经还原制备得到。
上述β-环糊精衍生物的制备方法,包括步骤:
(1)于溶剂1中、催化剂三乙胺的存在下,式ii化合物和1,4-丁二胺或1,6-己二胺发生反应制备式iii化合物;
其中,式iii化合物结构式中,n为2或3;
(2)于溶剂2中、氮气保护下,式iii化合物和二茂铁甲醛发生避光反应;然后于氮气保护下,经硼氢化钠还原;最后分离纯化制备得到式i化合物。
根据本发明优选的,步骤(1)中,所述溶剂1为n-甲基吡咯烷酮、n,n-二甲基甲酰胺、n,n-二甲基乙酰胺或二甲亚砜;优选为n-甲基吡咯烷酮;所述式ii化合物的质量和溶剂1的体积比为0.01-0.1g/ml;优选的,所述式ii化合物的质量和溶剂1的体积比为0.05-0.07g/ml。
根据本发明优选的,步骤(1)中,所述催化剂三乙胺的质量是式ii化合物质量的25-30%。
根据本发明优选的,步骤(1)中,所述式ii化合物和1,4-丁二胺或1,6-己二胺的摩尔比为1:1-3;优选的,所述式ii化合物和1,4-丁二胺或1,6-己二胺的摩尔比为1:2。
根据本发明优选的,步骤(1)中,所述式ii化合物和1,4-丁二胺或1,6-己二胺的反应温度为60-80℃;优选的,所述式ii化合物和1,4-丁二胺或1,6-己二胺的反应温度为70℃。式ii化合物和1,4-丁二胺或1,6-己二胺的反应时间为8-12小时;优选的,式ii化合物和1,4-丁二胺或1,6-己二胺的反应时间为10小时。
根据本发明优选的,步骤(1)中,式ii化合物和1,4-丁二胺或1,6-己二胺反应后,所得反应液冷却至室温,然后倒入丙酮中,所得沉淀经丙酮洗涤制得式iii化合物粗产物,并直接用于步骤(2)。
根据本发明优选的,步骤(2)中,所述溶剂2为n-甲基吡咯烷酮、n,n-二甲基甲酰胺、n,n-二甲基乙酰胺或二甲亚砜;优选为n-甲基吡咯烷酮;所述式iii化合物的质量和溶剂2的体积比为0.05-0.3g/ml。
根据本发明优选的,步骤(2)中,所述式iii化合物和二茂铁甲醛的摩尔比为1:0.5-2;优选的,式iii化合物和二茂铁甲醛的摩尔比为1:1。
根据本发明优选的,步骤(2)中,所述式iii化合物和二茂铁甲醛的避光反应温度为50-70℃;优选的,所述式iii化合物和二茂铁甲醛的避光反应温度为60℃。避光反应时间为3-7小时;优选的,避光反应时间为5小时。
根据本发明优选的,步骤(2)中,所述硼氢化钠与式iii化合物的摩尔比为1-3:1;优选的,所述硼氢化钠与式iii化合物的摩尔比为2:1。
根据本发明优选的,步骤(2)中,所述还原反应温度为室温。还原反应时间为1-4小时;优选的,还原反应时间为2小时。
根据本发明优选的,步骤(2)中,所述还原反应完全后,用丙酮淬灭反应。
根据本发明优选的,步骤(2)中,所述分离纯化是使用硅胶色谱柱进行分离纯化;所用洗脱剂为异丙醇、水和30wt%氨水的混合溶液,所述异丙醇、水和30wt%氨水的体积比为5:3:2。
利用上述β-环糊精衍生物制备超分子囊泡的方法,包括步骤:
将β-环糊精衍生物和β-环糊精溶于三次蒸水中得到混合液;于20-30℃下,超声波混合20-50分钟,得到超分子囊泡。
根据本发明优选的,所述β-环糊精衍生物和β-环糊精的摩尔比为1:1。
对β-环糊精衍生物和β-环糊精的混合液进行紫外吸收测试,控制β-环糊精衍生物和β-环糊精的总浓度不变,变化混合液中β-环糊精衍生物和β-环糊精的摩尔比例,随着β-环糊精衍生物浓度的增大,β-环糊精衍生物和β-环糊精的混合液的紫外吸收逐渐增强,根据以上结果做出job’s曲线,发现β-环糊精衍生物和β-环糊精之间的包合摩尔比为1:1。
根据本发明优选的,所述混合液中β-环糊精衍生物的浓度为5×10-3-8×10-3mol/l。
根据本发明优选的,所述超声波混合温度为25±1℃,超声波混合时间为30分钟。
根据本发明优选的,所述超分子囊泡的平均粒径为130-170nm。
本发明β-环糊精衍生物的合成方程式如下:
其中,n为2或3。
本发明的技术特点及有益效果如下:
1、本发明以单[6-对甲基苯磺酰基]-β-环糊精和1,4-丁二胺或1,6-己二胺为原料合成单[6-脱氧-n-丁基胺基]-β-环糊精或单[6-脱氧-n-己基胺基]-β-环糊精,然后与二茂铁甲醛反应,经硼氢化钠还原得到单[6-脱氧-n-丁基胺基-n’-甲基二茂铁]-β-环糊精或者单[6-脱氧-n-己基胺基-n’-甲基二茂铁]-β-环糊精这两种全新的β-环糊精衍生物。本发明经两步反应将二茂铁基团通过化学键连接到β-环糊精上,制备方法简单、易于操作,反应条件温和;反应位点专一,副产物较少,反应产率较高,适合大规模的工业化生产。
2、本发明将二茂铁基团通过化学键连接到β-环糊精上,使β-环糊精衍生物疏水区域得到有效扩大,同时赋予β-环糊精衍生物抗癌作用,有利于应用于药物载运领域;并使所得β-环糊精衍生物具备紫外吸收特性(β-环糊精无紫外吸收特性),利于后续的监测和应用。所得β-环糊精衍生物结构中同时具有氨基和二茂铁基团,氨基对铜离子具有较好的刺激响应能力,而二茂铁基团对氧化剂具有较好的刺激响应能力。因而,其应用于载药具有敏感的刺激响应性,利于抗癌药物的主动靶向运输。
3、本发明所得β-环糊精衍生物可用于制备超分子囊泡,其作为客体分子可以有效地被主体分子β-环糊精包合形成超分子双亲分子,在一定条件下组装成主客体超分子囊泡。所得囊泡的水合直径为130-170纳米,使得该囊泡容易通过epr效应滞留在癌变组织部位,并且容易被癌细胞所吞噬;同时具有抗癌活性的二茂铁基团被包埋在了囊泡的壁层中,赋予囊泡一定的抗癌作用的同时扩大了疏水区域;囊泡中β-环糊精空腔以及壁层的疏水区域可以包合一些疏水性药物分子,囊泡的内腔可以载运一些亲水性的药物分子,从而实现对二茂铁、亲水性药物分子和疏水性药物分子的三重载运,大大的增大了药物载运能力。因此本发明所涉及的主客体超分子囊泡在药物载运方面有着巨大的潜在应用价值。另外,β-环糊精衍生物结构中同时具有氨基和二茂铁基团,氨基对铜离子具有较好的刺激响应能力,而二茂铁基团对氧化剂具有较好的刺激响应能力;因而,所得主客体超分子囊泡具有敏感的刺激响应性,利于抗癌药物的主动靶向运输。
附图说明
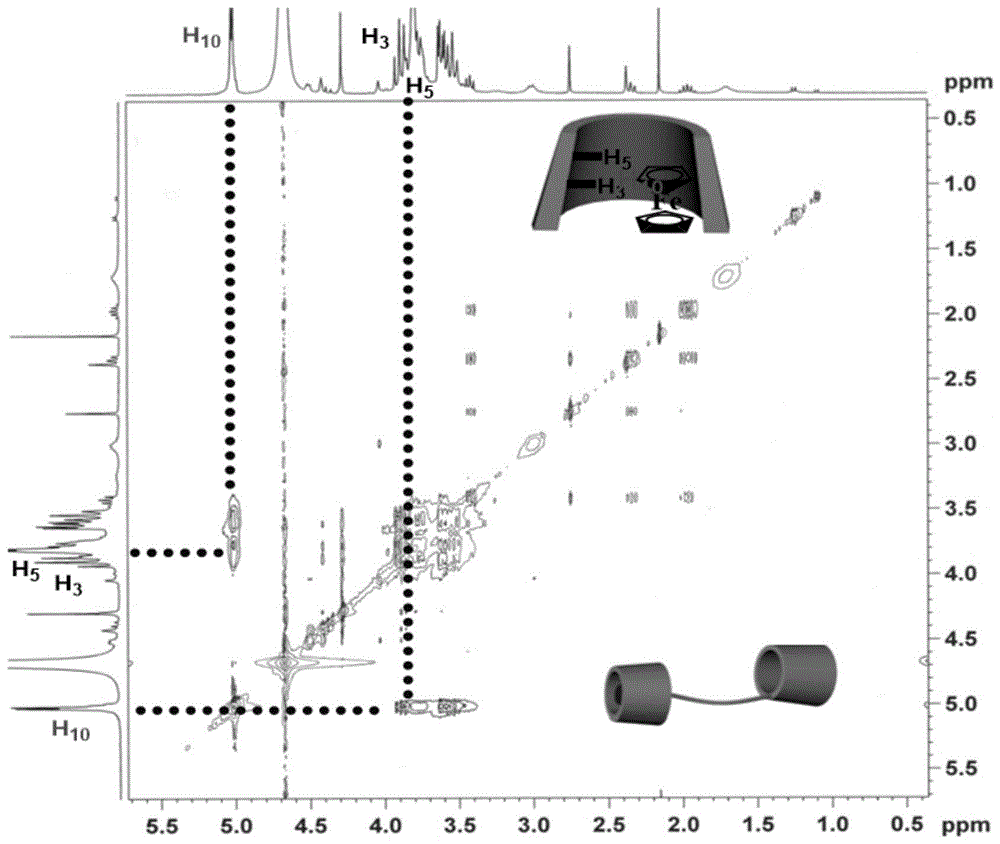
图1是本发明实施例1制备的超分子囊泡中单[6-脱氧-n-丁基胺基-n’-甲基二茂铁]-β-环糊精和β-环糊精之间的二维核磁(2dnmrrosey)谱图。
图2是本发明实施例1制备的超分子囊泡在水相中于不同放大倍数下的tem图像。
图3是本发明实施例1制备的超分子囊泡在水相中于不同放大倍数下的sem图像。
图4是本发明实施例1制备的超分子囊泡在水相中的动态水合直径图。
图5是本发明实施例2制备的超分子囊泡在水相中于不同放大倍数下的tem图像。
图6是本发明实施例2制备的超分子囊泡在水相中的动态水合直径图。
具体实施方式
下面结合具体实施例对本发明作进一步阐述,但是本发明并不仅限于以下实施例。
实施例中所述方法如无特别说明均为常规方法,所述试剂如无特殊说明均可市购获得。
实施例1
一种β-环糊精衍生物(单[6-脱氧-n-丁基胺基-n’-甲基二茂铁]-β-环糊精)的制备方法,包括步骤:
(1)室温下将单[6-对甲基苯磺酰基]-β-环糊精(ii,0.6445g,0.5mmol)加入到10毫升n-甲基吡咯烷酮中,搅拌至完全溶解,然后加入上述单[6-对甲基苯磺酰基]-β-环糊精2倍摩尔量的1,4-丁二胺(0.088g,1mmol),再滴加入0.25ml的三乙胺作催化剂,在70℃下反应10小时,tlc检测反应完全,冷却反应液至室温,将反应液倒入丙酮中,产生大量白色颗粒,抽滤并用丙酮洗涤滤饼3次,得到单[6-脱氧-n-丁基胺基]-β-环糊精(iii)粗产物;
(2)室温下将上述得到的单[6-脱氧-n-丁基胺基]-β-环糊精(iii,0.6025g,0.5mmol)溶于5毫升n-甲基吡咯烷酮中,然后加入0.107g(0.5mmol)的二茂铁甲醛,在60℃下,避光,氮气保护反应5小时,tlc检测反应完全;停止加热,反应冷却至室温,分3批在10分钟内向反应液中加入0.03783g(1mmol)的硼氢化钠,氮气保护下继续室温反应2小时,tlc检测反应完全,用1毫升的丙酮淬灭反应,得到单[6-脱氧-n-丁基胺基-n’-甲基二茂铁]-β-环糊精粗产物;将上述环糊精衍生物粗产物使用硅胶色谱柱分离纯化,洗脱剂为体积比为5:3:2的异丙醇、水和30wt%氨水的混合液,得到单[6-脱氧-n-丁基胺基-n’-甲基二茂铁]-β-环糊精,即β-环糊精衍生物。
本发明β-环糊精衍生物的产率为65%(以起始原料为基准的产率),为亮黄色粉末。
本发明所得产物的核磁数据如下:
1hnmr(300mhz,dmso-d6,300k,tms,δppm):5.97-5.61(m,9h,c5h5),4.92-4.81(m,4h,h1),4.27-4.17(m,3h,h1),3.94-3.37(m,28h,h3,h5,h6),3.36-3.20(m,14h,h2,h4),2.70-2.68(s,2h,ch2),2.31-2.15(m,2h,ch2),2.10-2.06(s,2h,ch2),2.02-1.74(m,2h,ch2),1.27-1.17(m,2h,ch2).13cnmr(75mhz,dmso-d6,300k,δppm):17.06,20.80,28.97,30.04,30.62,48.39,60.19,68.52,72.42,73.00,101.94,125.25,127.93.ft-ir(kbrpellet,υcm-1):3236.44(vn-h),2928.42(vc-h),1657.16(vc=c),618.49(δc=c).esi-ms:calcd.forc57h92n2o34fe2+,m/z=702.1850,foundm/z=702.2503。
利用上述所得β-环糊精衍生物制备超分子囊泡的方法,包括步骤:
将单[6-脱氧-n-丁基胺基-n’-甲基二茂铁]-β-环糊精和β-环糊精按照1:1摩尔比溶于三次蒸水中,制备成β-环糊精衍生物浓度为6×10-3mol/l的混合液;于25±1℃下,超声波混合30分钟,得到平均直径为150nm左右的超分子囊泡。
本发明制备的超分子囊泡中,单[6-脱氧-n-丁基胺基-n’-甲基二茂铁]-β-环糊精和β-环糊精之间的二维核磁(2dnmrrosey)谱图如图1所示,由图1可知,单[6-脱氧-n-丁基胺基-n’-甲基二茂铁]-β-环糊精中二茂铁基团上的h10与β-环糊精内腔的h3、h5之间具有明显的相关信号,说明β-环糊精包合了单[6-脱氧-n-丁基胺基-n’-甲基二茂铁]-β-环糊精中二茂铁基团,形成了超分子双亲分子。
本实施例制备的超分子囊泡在水相中于不同放大倍数下的tem、sem图像如图2和3所示,由图2和3可知,超分子囊泡呈球形,大小均一,平均直径在150nm左右,囊泡壁厚3.5nm左右,与单[6-脱氧-n-丁基胺基-n’-甲基二茂铁]-β-环糊精/β-环糊精包合物尺寸相当。
本实施例制备的超分子囊泡在水相中的动态水合直径图如图4所示,由图4可知超分子囊泡动态水合直径在150nm左右。
实施例2
一种β-环糊精衍生物(单[6-脱氧-n-己基胺基-n’-甲基二茂铁]-β-环糊精)的制备方法,包括步骤:
(1)室温下将单[6-对甲基苯磺酰基]-β-环糊精(ii,0.6445g,0.5mmol)加入到10毫升n-甲基吡咯烷酮中,搅拌至完全溶解,然后加入上述单[6-对甲基苯磺酰基]-β-环糊精2倍摩尔量的1,6-己二胺(0.116g,1mmol),再滴加入0.25ml的三乙胺作催化剂,在70℃下反应10小时,tlc检测反应完全,冷却反应液至室温,将反应液倒入丙酮中,产生大量白色颗粒,抽滤并用丙酮洗涤滤饼3次,得到单[6-脱氧-n-己基胺基]-β-环糊精(iii)粗产物;
(2)室温下将上述得到的单[6-脱氧-n-己基胺基]-β-环糊精(iii,0.6165g,0.5mmol)溶于5毫升n-甲基吡咯烷酮中,然后加入0.107g(0.5mmol)的二茂铁甲醛,在60℃下,避光,氮气保护反应5小时,tlc检测反应完全;停止加热,反应冷却至室温,分3批在10分钟内向反应液中加入0.03783g(1mmol)的硼氢化钠,氮气保护下继续室温反应2小时,tlc检测反应完全,用1毫升的丙酮淬灭反应,得到单[6-脱氧-n-己基胺基-n’-甲基二茂铁]-β-环糊精粗产物;将上述环糊精衍生物粗产物使用硅胶色谱柱分离纯化,洗脱剂为体积比为5:3:2的异丙醇、水和30wt%氨水的混合液,得到单[6-脱氧-n-己基胺基-n’-甲基二茂铁]-β-环糊精,即β-环糊精衍生物。
本发明β-环糊精衍生物的产率为68%(以起始原料为基准的产率),为亮黄色粉末。
本发明所得产物的核磁数据如下:
1hnmr(300mhz,dmso-d6,300k,tms,δppm):6.08-5.58(m,9h,c5h5),4.89-4.79(m,4h,h1),4.29-4.18(m,3h,h1),4.12-3.36(m,28h,h3,h5,h6),3.35-3.09(m,14h,h2,h4),3.02-2.56(m,4h,ch2),2.40-1.76(m,2h,ch2),1.73-0.84(m,8h,ch2).13cnmr(75mhz,dmso-d6,300k,δppm):17.58,20.78,21.22,25.94,29.41,30.49,31.09,49.01,60.41,62.36,69.04,73.68,73.60,82.08,102.43,125.93,128.38.ft-ir(kbrpellet,υcm-1):3248.80(vn-h),2938.66(vc-h),1662.28(vc=c),618.50(δc=c).esi-ms:calcd.forc59h96n2o34fe2+,m/z=716.1100,foundm/z=716.2684。
利用上述所得β-环糊精衍生物制备超分子囊泡的方法,包括步骤:
将单[6-脱氧-n-己基胺基-n’-甲基二茂铁]-β-环糊精和β-环糊精按照1:1摩尔比溶于三次蒸水中,制备成β-环糊精衍生物浓度为6×10-3的混合液;于25±1℃下,超声波混合30分钟,得到平均直径为160nm左右的超分子囊泡。
本实施例制备的超分子囊泡在水相中于不同放大倍数下的tem图像如图5所示,由图5可知,超分子囊泡呈球形,大小均一,平均直径在160nm左右。
本实施例制备的超分子囊泡在水相中的动态水合直径图如图6所示,由图6可知,超分子囊泡动态水合直径在160nm左右。
实施例3
一种β-环糊精衍生物(单[6-脱氧-n-丁基胺基-n’-甲基二茂铁]-β-环糊精)的制备方法,包括步骤:
(1)室温下将单[6-对甲基苯磺酰基]-β-环糊精(ii,0.6445g,0.5mmol)加入到10毫升n-甲基吡咯烷酮中,搅拌至完全溶解,然后加入上述单[6-对甲基苯磺酰基]-β-环糊精2倍摩尔量的1,4-丁二胺(0.088g,1mmol),再滴加入0.23ml的三乙胺作催化剂,在80℃下反应8小时,tlc检测反应完全,冷却反应液至室温,将反应液倒入丙酮中,产生大量白色颗粒,抽滤并用丙酮洗涤滤饼3次,得到单[6-脱氧-n-丁基胺基]-β-环糊精(iii)粗产物;
(2)室温下将上述得到的单[6-脱氧-n-丁基胺基]-β-环糊精(iii,0.6025g,0.5mmol)溶于3毫升n-甲基吡咯烷酮中,然后加入0.107g(0.5mmol)的二茂铁甲醛,在50℃下,避光,氮气保护反应7小时,tlc检测反应完全;停止加热,反应冷却至室温,分3批在10分钟内向反应液中加入0.03783g(1mmol)的硼氢化钠,氮气保护下继续室温反应3小时,tlc检测反应完全,用1毫升的丙酮淬灭反应,得到单[6-脱氧-n-丁基胺基-n’-甲基二茂铁]-β-环糊精粗产物;将上述环糊精衍生物粗产物使用硅胶色谱柱分离纯化,洗脱剂为体积比为5:3:2的异丙醇、水和30wt%氨水的混合液,得到单[6-脱氧-n-丁基胺基-n’-甲基二茂铁]-β-环糊精,即β-环糊精衍生物。
利用上述所得β-环糊精衍生物制备超分子囊泡的方法,包括步骤:
将单[6-脱氧-n-丁基胺基-n’-甲基二茂铁]-β-环糊精和β-环糊精按照1:1摩尔比溶于三次蒸水中,制备成β-环糊精衍生物浓度为5×10-3mol/l的混合液;于25±1℃下,超声波混合25分钟,得到超分子囊泡。
- 还没有人留言评论。精彩留言会获得点赞!