佐匹克隆半抗原、抗原、抗体、胶体金层析检测装置及其用途的制作方法
本发明涉及生物检测领域。更具体地,本发明涉及一种佐匹克隆半抗原、佐匹克隆抗原、佐匹克隆抗体以及包括上述抗原和抗体的胶体金层析检测装置及其用途。
背景技术:
随着现代社会竞争的日渐激烈,来自学习、生活、就业等压力也随之加大,焦虑和失眠成为困扰人们的常见问题。很多人不得不借助镇静安神类精神药物来维持正常的睡眠和生活,但是由于镇静催眠类药物,如佐匹克隆、艾司唑仑、巴比妥、地西泮等等,都属于二类精神药物,使用受到严格限制,于是具有镇静催眠功效的中药制剂以及保健食品可能成为患者的首选。但是不法分子为了突显产品疗效,在镇静安神类中成药、保健食品中非法添加佐匹克隆、艾司唑仑、巴比妥、地西泮化学成分的现象非常普遍。
佐匹克隆是新一代环吡咯酮类镇静催眠药,亦是第三代镇静催眠药的代表。目前,镇静安神类中成药、保健食品中非法添加佐匹克隆违禁化学药物的检测方法有液相色谱(lc)、高效液相色谱-串联质谱法(lc-ms/ms),以及薄层色谱法(tlc)、近红外光谱法(nir)、拉曼光谱法(ramanspectroscopy,rs)等。lc和lc-ms/ms检测具有精度高、分离效率高、选择性好、假阳性率低、重现性好等优点,但操作复杂、设备昂贵,对操作人员技术要求高,且不能立即显示结果等问题,不适用于快速的在线检测和监控。tlc、nir及rs,操作简单,分析速度快,但灵敏度差,多个成分之间经常会有干扰,专属性不好,且中成药及复杂食品基质容易出现假阳性的情况,一般需要运用专属性更高的方法予以进一步确认。
免疫学检测分析技术以其高灵敏、特异性高、快速、操作简便等优点在非法添加检测领域已被广泛应用比起仪器等检验方法有很多优势。综上,本领域亟需一种快速简便、灵敏度高、可检测镇静安神类保健食品或声称具有相应保健功效的食品、中成药中非法添加的佐匹克隆的快速检测方法。
技术实现要素:
针对相关技术中的问题,本发明提供了一种佐匹克隆胶体金层析检测装置,所述装置包括佐匹克隆抗原和佐匹克隆抗体,其能够特异性地、快速地检测出中成药或保健食品中非法添加的佐匹克隆,并且具有使用方便、灵敏度高的优点。
根据本发明的第一方面,本发明提供了一种佐匹克隆半抗原,所述佐匹克隆半抗原的结构式为:
根据本发明的第二方面,本发明提供了一种佐匹克隆抗原,所述佐匹克隆抗原包括本发明提供的佐匹克隆半抗原,以及与所述佐匹克隆半抗原偶联的载体蛋白。
在一个实施方案中,所述载体蛋白包括牛血清白蛋白、人血清白蛋白、鸡卵清白蛋白或血蓝蛋白。
根据本发明的第三方面,本发明提供了一种佐匹克隆抗体,所述佐匹克隆抗体为特异性针对本发明第二方面提供的佐匹克隆抗原的抗体。
在一个实施方案中,所述佐匹克隆抗体为佐匹克隆单克隆抗体或佐匹克隆多克隆抗体。
根据本发明的第四方面,本发明还提供了本发明第一方面的佐匹克隆半抗原、本发明第二方面的佐匹克隆抗原、本发明第三方面的佐匹克隆抗体在免疫学检测中的应用。
根据本发明的第五方面,本发明提供了一种佐匹克隆胶体金层析检测装置,包括试纸条和反应杯,其中,所述试纸条包括反应膜,所述反应膜上有检测线和质控线,并且其中,所述检测线包被有本发明第二方面的佐匹克隆抗原,并且其中,所述反应杯中含有胶体金标记的本发明第三方面的佐匹克隆抗体。
在一个实施方案中,所述质控线包被有特异性针对本发明第三方面的佐匹克隆抗体的第二抗体。
根据本发明的第六方面,本发明还提供了一种检测样品中佐匹克隆的方法,所述方法包括使用本发明第五方面的胶体金层析检测装置对样品中的佐匹克隆进行检测。
在一个实施方案中,所述样品为中成药或保健食品。
本发明的有益效果:本发明利用层析式免疫胶体金原理,通过试纸条中检测线与质控线之间的比色来半定量检测诸如中成药或保健食品等样品中非法添加的佐匹克隆的含量。该检测装置能够快速、准确地检测出诸如中成药或保健食品等样品中非法添加的佐匹克隆,能满足监管部门、检测机构现场监督执法的需要。
与现有技术相比,本发明具有敏度高、特异性强、成本低、操作简单、检测时间短、保质期长的优点。本发明可应用于诸如中成药或保健食品等样品中非法添加的佐匹克隆的快速检测。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
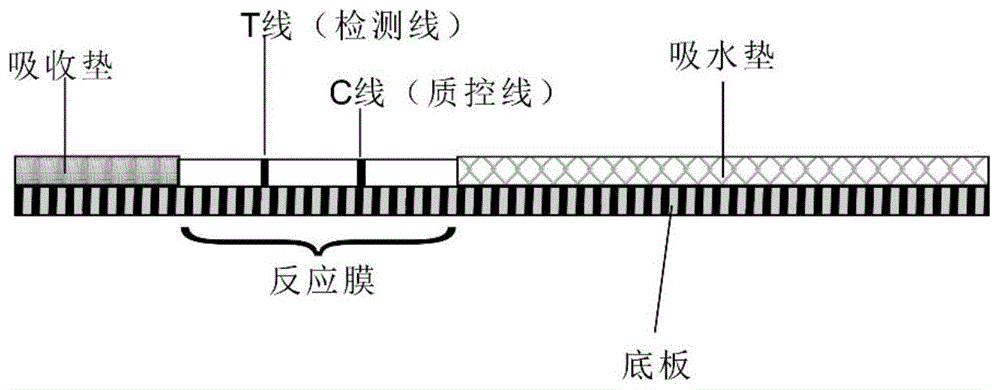
图1是根据本发明的实施方案的胶体金层析检测装置中的试纸条的剖面结构示意图。
图2是根据本发明的实施方案的胶体金层析检测装置中的微孔反应杯的示意图。
图3是根据本发明的实施方案的结果判定的示意图。
图4是根据本发明的实施方案的佐匹克隆半抗原的质谱图。
图5是根据本发明的实施方案的载体蛋白bsa、ova、佐匹克隆半抗原、相应的佐匹克隆抗原的吸收曲线。
具体实施方式
下面将结合本发明的实施方案和附图,对本发明进行清楚、完整地描述。显然,所描述的实施方案仅仅是本发明的一部分实施方案,而不是全部的实施方案。基于本发明中的实施方案,本领域普通技术人员所获得的所有其他实施方案,都属于本发明保护的范围。
根据本发明的第一方面,本发明提供了一种佐匹克隆半抗原,其中所述佐匹克隆半抗原的结构式为:
如本领域技术人员所理解的,所谓半抗原,是指这样的一类小分子物质:其单独存在时并不能诱导免疫应答,即不具备免疫原性,但当其与大分子蛋白质或非抗原性的多聚赖氨酸等载体交联或结合后可获得免疫原性,从而诱导免疫应答。这类小分子物质可与应答效应产物结合,具备抗原性,即免疫反应性,但是不具有免疫原性。
结合到本发明,容易理解,佐匹克隆半抗原针对佐匹克隆抗体(单抗隆抗体或多克隆抗体均可)具有免疫反应性,但是不具备免疫原性。换言之,佐匹克隆半抗原可以与其相对应的佐匹克隆抗体结合发生抗原-抗体反应;然而,在将该佐匹克隆半抗原接种到动物体内进行免疫时,不能单独刺激动物产生相应的抗体。
由于佐匹克隆作为半抗原,并不能产生良好的免疫反应性,因此在将其用作半抗原时需要对其进行修饰。但是需要注意的是,该修饰应尽可能地少,并且尽可能多地保留能与抗体结合的位点。
在本发明中,通过丁二酸酐修饰佐匹克隆中间体(cas:43200-81-3)来得到佐匹克隆半抗原分子,具体的制备过程如下实施例中详细描述的,合成路线如下式所示:
如上所述,佐匹克隆半抗原仅具有免疫反应性,而不具有免疫原性,并不能单独地刺激动物产生相应的抗体。因此,为了赋予佐匹克隆半抗原以免疫原性,需要将佐匹克隆半抗原与大分子蛋白质等载体偶联、结合或者交联在一起,由此产生既具有免疫反应性又具有免疫原性的佐匹克隆偶联抗原。半抗原与载体分子之间的偶联、结合或者交联方法是本领域已知的,例如本申请实施例部分所示例的方法。
因此,根据本发明的第二方面,本发明提供了一种佐匹克隆抗原,包含本发明第一方面提供的佐匹克隆半抗原,以及与所述佐匹克隆半抗原偶联的载体蛋白。
本发明所提及的术语“载体”是任何能够与半抗原偶联、结合或者交联并由此产生既具有免疫原性又具有免疫反应性的物质,包括例如大分子蛋白质或者非抗原性的多聚赖氨酸等。作为示例,可以使用的载体包括,但不限于,大分子蛋白质,例如牛血清白蛋白(bsa)、人血清白蛋白(hsa)、鸡卵清白蛋白(ova)、血蓝蛋白(klh)。
根据本发明的第三方面,提供了一种佐匹克隆抗体,该佐匹克隆抗体为特异性针对本发明第二方面提供的佐匹克隆抗原的抗体。
佐匹克隆抗体可以为单克隆抗体或者多克隆抗体。另外,可以采用本领域普通技术人员已知的方法来制备佐匹克隆抗体。例如,在佐匹克隆抗体为多克隆抗体的情况下,可以通过采用佐匹克隆抗原免疫接种哺乳动物例如小鼠、大鼠、兔、山羊、绵羊、灵长类动物(不包括人类)等、随后分离血清获得。在佐匹克隆抗体为单克隆抗体的情况下,可以通过制造和培养杂交瘤细胞并收集培养基获得单克隆抗体,或者可以将由此制备获得的杂交瘤细胞通过腹腔注射接种到哺乳动物例如小鼠、大鼠、兔、山羊、绵羊、灵长类动物(不包括人类)等的体内,在被接种动物的腹部明显膨大时收集腹水,由此获得单克隆抗体。
如本领域技术人员所能理解的,对于佐匹克隆抗体的来源,并没有特别的限制,其可以来源于任何哺乳动物,包括例如小鼠、大鼠、兔、山羊、绵羊、灵长类动物(不包括人类)等,但不限于此。在一个具体的实施方案中,佐匹克隆抗体为来源于小鼠、大鼠、兔、山羊、绵羊、灵长类动物(不包括人类)的多克隆或者单克隆抗体。
根据本发明的第四方面,提供了本发明第一方面的佐匹克隆半抗原、本发明第二方面的佐匹克隆抗原、本发明第三方面的佐匹克隆抗体在免疫学检测中的应用。
根据本发明的第五方面,提供了一种佐匹克隆胶体金层析检测装置,包括试纸条和反应杯,其中,试纸条包括反应膜,反应膜上有检测线和质控线,并且其中,检测线包被有本发明第二方面的佐匹克隆抗原,并且其中,所述反应杯中含有胶体金标记的本发明第三方面的佐匹克隆抗体(简称“金标抗体”)。
根据本发明的一些实施方案,试纸条还可以包括诸如底板、样品吸收垫和吸水垫的其他组件。在这种情况下,在底板上按顺序粘贴上样品吸收垫、反应膜、吸水垫。在本发明中,样品吸收垫可以为玻璃纤维棉、尼龙膜、聚偏二氟乙烯膜或聚醋膜;反应膜可以为硝酸纤维素膜、纯纤维素膜或羧化纤维素膜;吸水垫可以为吸水滤纸或滤油纸;底板可以为不吸水的韧性材料例如硬质塑胶条如pvc底板或不吸水硬纸条或其它硬质不吸水材料。
在本发明中,反应膜包含检测线和质控线。通常情况下,将检测线设置在靠近样品吸收垫一侧。检测线由佐匹克隆抗原(在本发明中即佐匹克隆半抗原-载体蛋白偶联物)在反应膜上进行线性点样制得。质控线可以通过将抗原或者抗体在反应膜上进行线性点样获得。
在本发明的一个实施方案中,质控线由本发明提供的佐匹克隆抗体的第二抗体点样获得。在胶体金标记的佐匹克隆抗体移动至质控线时,其会与形成该质控线的第二抗体发生结合反应,由此显现颜色。
如果质控线显色,则指示该检测系统成立,检测结果可用。相反,如果质控线不显色,则指示该检测系统不成立,检测结果不可用。
如上所述,反应杯中含有胶体金标记的本发明第三方面提供的佐匹克隆抗体,所述佐匹克隆抗体特异性地针对本发明第二方面的佐匹克隆抗原。
佐匹克隆抗体只要能够与佐匹克隆抗原发生抗原-抗体结合反应即可,而不管它是单克隆抗体还是多克隆抗体。然而,正如本领域技术人员可以理解的那样,从需要更高特异性的角度上考虑,单克隆抗体是更合适的。因此在本发明中,佐匹克隆抗体优选地为单克隆抗体。
在本发明中,质控线的点样制备可以根据胶体金标记的佐匹克隆抗体的类型来进行。具体地,若胶体金标记的佐匹克隆抗体为佐匹克隆单克隆抗体,则该质控线可以采用羊抗鼠抗抗体进行线性点样制得,若胶体金标记的佐匹克隆抗体为佐匹克隆多克隆抗体时,则该质控线可以采用羊抗兔抗抗体进行线性点样制得。
在本发明的一个实施方案中,本发明提供了一种佐匹克隆胶体金层析检测装置,包括试纸条和反应杯,如图1所示,试纸条包含底板以及在其上依次铺设的样品吸收垫、反应膜和吸水纸,该反应膜在样品吸收垫至吸水纸方向上包括检测线和质控线,检测线由佐匹克隆抗原制备获得;如图2所示,反应杯包含胶体金标记的佐匹克隆抗体,佐匹克隆抗体为特异性地针对佐匹克隆抗原的鼠源单克隆抗体,并且质控线为针对该佐匹克隆抗体的羊抗鼠抗抗体。
在本发明的一个实施方案中,可以通过下述制备方法来制备本发明的佐匹克隆胶体金层析检测装置:制备反应膜,采用本发明的佐匹克隆抗原在反应膜上进行线性点样制备检测线,并采用针对佐匹克隆抗体的羊抗鼠抗抗体通过线性点样制备质控线;在底板上沿同一方向依次搭接粘贴样品吸收垫、反应膜和吸水纸,由此组装成试纸条;将本发明的胶体金标记的佐匹克隆抗体加入微孔反应杯、冻干后,将微孔反应杯加上微孔塞。该制备方法中使用到的各成分或者组件如上文针对本发明的佐匹克隆胶体金层析检测装置所描述。
根据本发明的另一方面,本发明提供了一种检测样品中佐匹克隆的方法,该方法使用本发明提供的佐匹克隆胶体金层析检测装置进行检测。
在本发明中,该样品可以为任何疑似非法添加佐匹克隆的样品,其可以是中成药或保健食品。
根据本发明的一些实施方案,在采用本发明的方法检测样品中的佐匹克隆之前,可以根据样品的不同对其进行前处理,处理方法为本领域已知的用于检测的样品处理的一般方法,在此不对其进行特别限定。
在进一步的方案中,在对样品进行预处理之后,将其滴加至微孔反应杯中,混匀后,将试纸条插入微孔反应杯,待检样品溶液与微孔中的金标抗体结合后一起向反应膜扩散,若观察到质控线显现出紫红色条带,则指示该检测系统成立、可用。图3示出了根据本发明的一些实施例的采用本发明提供的方法检测佐匹克隆的判定结果,判断方法如下:
(1)若检测线(t线)不显色,或者与质控线(c线)相比显色更浅,则表明样品中含有佐匹克隆。因为待检样品液中含有佐匹克隆时,扩散过程中待检样品液中的佐匹克隆可与金标抗体相结合,进而完全封闭金标抗体上佐匹克隆的抗原结合点,阻止金标抗体与反应膜上的佐匹克隆抗原结合,t线不显色或t线颜色比c线颜色更浅,而抗抗体则可与金标抗体结合,c线显色。
(2)若检测线同质控线一样显现出紫红色条带,并且检测线的颜色深度与质控线的颜色深度相当或者更深,则表明样品不含佐匹克隆。因为待检样品液中不含佐匹克隆时,金标抗体上的抗原结合位点不能被封闭,进而金标抗体会与反应膜上的佐匹克隆抗原偶联结合,t线显色,同时抗抗体也可与金标抗体结合,c线亦显色,此时,t线颜色比c线颜色深或颜色相同。
(3)若反应膜上t线和c线均未显色,则试纸条失效。
本发明的有益效果:本发明利用层析式免疫胶体金原理,通过试纸条中检测线与质控线之间的比色来半定量检测中成药或保健食品中非法添加的佐匹克隆的含量,该检测装置能够快速、准确地检测出中成药或保健食品中非法添加的佐匹克隆,能满足监管部门、检测机构现场监督执法的需要。
与现有技术相比,本发明具有敏度高、特异性强、成本低、操作简单、检测时间短、保质期长的优点。本发明可应用于中成药或保健食品等中非法添加的佐匹克隆的快速检测。
下面结合附图和实施例对本发明进行更为具体和详细的描述。
实施例
实施例1.佐匹克隆半抗原的制备
通过丁二酸酐修饰佐匹克隆中间体(cas:43200-81-3)得到佐匹克隆半抗原分子的合成路线如下所示:
具体地,称取佐匹克隆中间体(cas:43200-81-3)1.31g,丁二酸酐1.0g,用无水吡啶完全溶解后,80℃搅拌反应过夜,薄层色谱(tlc)检测反应进程,待反应完全后,蒸干溶剂,加水溶解,用乙酸乙酯萃取2-3遍,合并有机相,蒸干后过柱纯化得白色固体h1,经ms鉴定为目标产物,见图4。
实施例2.佐匹克隆抗原的制备与鉴定
制备:取实施例1制备的佐匹克隆半抗原0.1mmol溶于2ml二甲基甲酰胺(dmf)中,搅拌加入0.2mmol二环己基碳二亚胺(dcc)和0.15mmoln-羟基琥珀酰亚胺(nhs)。4℃下磁力搅拌反应过夜,离心后上清液为a液,称取bsa140mg溶于10ml浓度为0.1mol/l的磷酸缓冲盐溶液(pbs)(ph=8.0)中。加入dmf1ml,搅拌溶解制备b液,磁力搅拌下,a液逐渐滴入b液中,4℃下反应12h。离心后,取上清液,4℃下用生理盐水透析3天,每天更换3次透析液。得到的全抗原以1mg/ml的浓度分装于0.5ml离心管中。冻存于-20℃冰箱中。同时还以同样的方式制备了以ova为载体蛋白的佐匹克隆抗原。
鉴定:将载体蛋白bsa、ova、佐匹克隆半抗原、相应的佐匹克隆抗原用ph=7.4的pbs配成0.5mg/ml的溶液,以0.01mol/lph=7.4pbs调零,用紫外分光光度计在波长200nm~800nm范围内扫描,得到载体蛋白bsa、ova、佐匹克隆半抗原、相应的佐匹克隆抗原-载体蛋白偶联物的吸收曲线。根据出现不同的吸收曲线,表明佐匹克隆半抗原与载体蛋白bsa、ova偶联成功,见图5。
实施例3.佐匹克隆抗体的制备
3.1动物免疫
利用实施例2得到的佐匹克隆免疫抗原,免疫4只6周龄balb/c小鼠,免疫剂量为200μg/只,加强免疫三次后,使其产生抗血清。
3.2细胞融合和克隆化
在无菌条件下,取免疫balb/c小鼠脾脏制备脾细胞,数量配比按脾细胞:骨髓瘤细胞(sp2/0)=91进行融合,经3次以上的克隆培养和检测,筛选得到稳定分泌抗佐匹克隆单克隆抗体的杂交瘤细胞株。
3.3细胞冻存和复苏
将杂交瘤细胞用冻存液制成5×106个/ml的细胞悬液,在液氮中长期保存。复苏时从液氮灌中取出冻存管,快速放入37℃温水浴中,并轻轻摇动使其尽快融化,离心去除冻存液后,移入细胞培养瓶内培养。
3.4单克隆抗体的制备与纯化
增量培养法:将杂交瘤细胞置于细胞培养基中,在37℃条件下进行培养,用辛酸-饱和硫酸铵法将得到的培养液进行纯化,得到单克隆抗体,-20℃保存。
该细胞培养基为向rpmi1640培养基中添加小牛血清和碳酸氢钠,使小牛血清在细胞培养基中的终浓度为20%(质量百分含量),使碳酸氢钠在细胞培养基中的终浓度为0.2%(质量百分含量);所述细胞培养基的ph为7.4。
实施例4.佐匹克隆胶体金层析检测装置的制备
4.1胶体金的制备
取1%氯金酸溶液1ml,加99ml超纯水成终浓度0.01%的氯金酸溶液,加热沸腾后,取1%柠檬酸三钠1.6ml一次性迅速加入煮沸的氯金酸溶液中,继续加热至溶液由淡黄色转为蓝黑色最终变为亮红色,颜色稳定后继续加热5min,室温冷却,补充失水至原体积。
4.2胶体金标记的单克隆抗体的制备
调节胶体金溶液ph值至8.0,用恒速搅拌器均匀搅拌,同时逐滴加入佐匹克隆的单克隆抗体,1h后加入抗体量相当的聚乙二醇(peg),充分反应30min后加入抗体量相当的bsa,加完后,继续搅拌30min。在9000rpm下离心30min获得均一性金标抗体沉淀,再加对硝基苯酚丁酸盐(pnpb)重悬备用。
4.3胶体金检测装置的制备:
制备硝酸纤维素膜:在该硝酸纤维素膜上将实施例2制备的佐匹克隆抗原进行线性点样,由此形成检测线;并将羊抗鼠抗抗体(以羊作为免疫动物,以实施例3制备的鼠源抗体为免疫原对无病原体羊进行免疫获得)进行线性点样,由此形成质控线。
制备试纸条:在pvc底板上,沿同一方向依次将样品吸收垫(玻璃纤维棉)、制备好的硝酸纤维素膜和吸水垫(吸水滤纸)依次搭接粘连,由此获得试纸条。
制备微孔反应杯:将所制备的胶体金标记的单克隆抗体加入至微孔反应杯中,冻干,由此形成所需的微孔反应杯。
佐匹克隆胶体金层析检测装置:将所得到的试纸条和所得到的微孔反应杯组合的一起,形成本发明的佐匹克隆胶体金层析检测装置。
实施例5.镇静安神类中成药及保健食品中佐匹克隆的检测方法
5.1样品前处理
取0.1g或0.1ml中成药或保健食品(硬胶囊、软胶囊、片剂、丸剂、散剂、水剂等剂型)待测物至含有0.1%醋酸溶液的提取瓶,拧紧瓶盖大力振摇约30秒;用pbs缓冲溶液稀释10倍,摇匀备用。
5.2用实施例4制备的佐匹克隆胶体金层析检测装置进行检测
取出胶体金层析检测装置中的微孔反应杯置于板架中;拧开试剂瓶的上盖,垂直滴入7~8滴(约100μl)稀释液于微孔反应杯;用塑料吸管上下抽吸1~3次混匀;将试纸条插入到微孔反应杯中,于20~40℃反应3分钟;从微孔反应杯中取出测试条,并进行结果判读。
5.3判读检测结果
阴性(-):若t线颜色比c线颜色深或颜色相同,表示样品中不含佐匹克隆化学成分或其残留量低于本产品的检出限。
阳性(+):若t线颜色比c线颜色浅,或只有c线显色(t线不显色),表示样品中含有佐匹克隆化学成分在本产品的检出限附近或高于本产品的检出限。
无效:t和c线均未显色,表明试纸条失效,建议更换试纸条重复测定。
实施例6.佐匹克隆胶体金层析检测装置的灵敏度
设置一系列的浓度梯度,佐匹克隆浓度分别为1.25、2.5、5、10、20μg/ml,用佐匹克隆胶体金层析检测装置进行测试,测试后使用仪器比较检测线与质控线颜色深浅。当佐匹克隆浓度为5μg/ml时,检测线颜色深度为质控线的90%以下,因此其灵敏度为5μg/ml。
选取5μg/ml平行实验5次,统计检测限颜色深度与质控线颜色深度的比例,其cv值小于15%。
实施例7.佐匹克隆胶体金层析检测装置的特异性
在阴性的液体样品中,分别加入佐匹克隆10μg/l、褪黑素10μg/l、巴比妥类药物(巴比妥10μg/l、苯巴比妥10μg/l、异戊巴比妥10μg/l、司可巴比妥10μg/l)、苯二氮卓类(地西泮10μg/l、艾司唑仑10μg/l、阿普唑仑10μg/l、奥沙西泮10μg/l、硝西泮10μg/l、三唑仑10μg/l、氯硝西泮10μg/l)。
实验结果发现,只有加入佐匹克隆的样品检出未阳性,而加入褪黑素、巴比妥类药物(巴比妥、苯巴比妥、异戊巴比妥、司可巴比妥)、苯二氮卓类(地西泮、艾司唑仑、阿普唑仑、奥沙西泮、硝西泮、三唑仑、氯硝西泮)的样品检出结果为阴性,说明本检测装置对佐匹克隆的特异性好,对其它类型镇静安神类药物无交叉反应。
实施例8.佐匹克隆胶体金层析检测装置的保质期测定
用三批常规生产的产品分别做保质期实验,放置于室内室温环境保持,每隔1个月取8个装置,用质控样本检测,分别做阴性,5μg/l,10μg/l和20μg/l样品,重复三次,观察数据变化,考察保质期时间。
阴性显色从13个月开始下降,在1年时间内产品品质无明显变化,因此确定保质期为1年。
以上仅为本发明的较佳实施方案而已,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!