铅离子核酸适配体及电化学传感器与制备方法与流程
本发明属于检测技术领域,涉及一种铅离子核酸适配体,以及基于该铅离子核酸适配体的电化学传感器,以及相应的制备方法与应用。
背景技术:
铅是一种地壳中常见的重金属,由于铅的长期大量开采使用和含铅废弃物的随意丢弃排放,环境中的铅污染问题越来越严重。铅作为一种不可降解的重金属污染物,可以与生物体以不同形式结合蓄积,然后通过食物链富集作用进入到人体当中并对包括肝脏、肾脏、骨骼、神经系统、心血管系统和生殖系统在内的各个器官和系统造成非可逆的损害。因此,分析和检测环境及食品中的铅含量对于环境保护和人体健康都具有重要意义。
环境和生物体中的铅多以铅离子(leadions,pb2+)及其化合物的形式存在,铅离子的检测方法种类繁多,不仅有主流的大型仪器检测法如原子发射光谱法、电感耦合等离子体质谱法,也有快速检测方法如免疫法、电化学阳极溶出伏安法以及生物传感器法等。电感耦合等离子体质谱法等大型仪器检测法尽管检测十分精准,但是也存在诸如仪器设备昂贵、基础设施较多以及需要专业人员操作等缺点,很难在现场快速检测领域中得到实际使用;而在快速检测方法当中,免疫法和电化学阳极溶出伏安法等在灵敏度、特异性以及检测限上都或多或少存在有一定的不足,所以目前也没有得到较好的发展。与以上方法相比,生物传感器法由于形式多样、特性优良、检测迅速以及成本低廉等特点获得了广泛关注和极大发展,是目前的一个研究热点。而在所有类型的生物传感器当中,以核酸适配体作为靶标物质识别分子,以电化学方式作为检测手段的生物传感器,不仅特异性好、灵敏度高、检测限低、分析速度快,而且操作简便、易于微型化和便携化。但到目前为止,使用基于特异性核酸适配体的电化学传感器检测铅离子的方法还未见报道。
技术实现要素:
本发明的第一个方面,提供了一种铅离子核酸适配体,该适配体具有亲和力高、特异性强、稳定性好、易于修饰等特点。
本发明所述的铅离子核酸适配体为长度33-35nt的单链dna(single-strandeddna,ssdna),且含有核酸序列cggatcggtatggatggtatt。
优选地,所述适配体的序列如seqidno:1-11所示。
进一步地,所述的适配体在其5’端修饰有多聚腺嘌呤核苷酸(polyadenine,polya)组装基团-aaaaa,即修饰后的核酸序列为:
aaaaagacgaccggatcggtatggatggtattgtcgtc(5’-3’)。
本发明的第二个方面,提供了一种基于核酸适配体的铅离子电化学传感器,该传感器以铅离子特异性核酸适配体为识别分子,特异性好,灵敏度高,有良好稳定性和重现性。
基于核酸适配体的铅离子电化学传感器以及配套检测方法,传感器以铅离子特异性核酸适配体为识别分子,以丝网印刷电极为载体,方法检测迅速,具有现场实时快速检测应用前景。
本发明所述的基于核酸适配体的铅离子电化学传感器含有所述的铅离子核酸适配体。
优选地,所述铅离子电化学传感器中所用的电极为丝网印刷电极,其中工作电极是直径4mm的金电极。
本发明的第三个方面提供了所述的铅离子电化学传感器的制备方法。
本发明所述的铅离子电化学传感器的制备方法,其特征在于,包括以下步骤:
s1.丝网印刷金电极电清洁预处理:将丝网印刷金电极片连接至电化学工作站,然后使电极片工作电极一端浸入硫酸溶液中,采用循环伏安法(cyclicvoltammetry,cv)对电极片进行电清洁扫描预处理,连续扫描4-6次直至扫描电流曲线基本稳定后使用超纯水冲洗,静置晾干备用,即得到预处理后的丝网印刷金电极,其中所述硫酸溶液为浓度为0.5m的硫酸溶液;
s2.核酸适配体溶液配制:核酸适配体干粉首先用核酸适配体组装液溶解成浓度为100μm的母液后于-20℃冰箱中保存,使用前再用体系缓冲溶液稀释到所需浓度。其中核酸适配体组装液为1mnacl溶液,体系缓冲溶液为ph7.4的20mmtris-hcl溶液;
s3.电极组装构建:滴加7-9μl一定浓度的核酸适配体溶液于丝网印刷金电极表面,确保液滴能够最大化地覆盖工作电极而不散开,然后将电极片放入塞有湿棉花的离心管中并于4℃冰箱中过夜组装;
s4.传感器电化学特性表征:电化学传感器完成组装后首先用超纯水清洗电极片,静置晾干后进行cv、差分脉冲伏安法(differentialpulsevoltammetry,dpv)和交流阻抗法(electrochemicalimpedancespectroscopy,eis)扫描,以验证电化学传感器组装成功。其中cv和dpv扫描所使用的电解液为5mmk3[fe(cn)6],含浓度为100mmkcl的溶液;eis扫描所使用的电解液为摩尔比1:1的5mmk3[fe(cn)6]/5mmk4[fe(cn)6],含浓度为100mmkcl的溶液。
本发明的第四个方面提供了根据所述的铅离子电化学传感器在检测铅离子方面的应用。
本发明所述的基于铅离子电化学传感器的铅离子检测方法,包括以下步骤:
s1.采用如权利要求4所述的铅离子电化学传感器对梯度浓度硝酸铅溶液进行检测,建立线性工作方程;
s2.将样品前处理后使用标准加标法对样品进行加标,加标后使用所述的铅离子电化学传感器检测样品中的铅离子,通过所建立的线性工作方程,计算相应的铅离子实际检出浓度,完成对加标样品中铅离子的定量检测。
根据本发明所述的铅离子检测方法的进一步特征,所述步骤s1中,将完成组装后的核酸适配体电化学传感器依次孵育检测梯度浓度的铅离子溶液,孵育完成后用超纯水缓慢冲洗并晾干,然后进行cv和dpv扫描分析,依次记录孵育检测各浓度铅离子溶液后的相关电流信号数据,分析数据及两者关系后建立线性工作方程;所述梯度浓度分别为0.1ng/ml、0.5ng/ml、1.0ng/ml、5.0ng/ml、10.0ng/ml、50.0ng/ml、100.0ng/ml、500.0ng/ml和1000.0ng/ml;所述电流信号数据是指dpv扫描峰电流强度值(peakcurrentintensity,ip),每个浓度铅离子溶液依次对应ipn,其中n=1,2……9;建立的线性工作方程以铅离子溶液的浓度对数值为横坐标,相应的dpv扫描峰电流强度变化值δipn值为纵坐标(n=1,2……9),工作方程具体为δip(μa)=9.645×logcpb2+(ng/ml)+13.36,其中cpb2+代表铅离子浓度,方法检测限达到0.03ng/ml(s/n=3)。
根据本发明所述的基于铅离子电化学传感器的铅离子检测方法的进一步特征,所述铅离子电化学传感器的核酸适配体组装浓度为10μm,组装时间为24h,铅离子的孵育时间为15min,孵育温度为30℃。
与现有的铅离子检测方法相比,本发明具有以下有益效果:
(1)本发明使用铅离子特异性核酸适配体对其进行识别检测,核酸适配体具有亲和力高、特异性好、合成成本低、性质稳定、易于修饰等优点,更适合用于重金属离子的检测。
(2)本发明使用的铅离子特异性核酸适配体在5’端修饰有-aaaaa组装基团,该组装基团可以在电极表面一次性完成组装和封闭,组装流程进一步简化;
(3)本发明中建立的核酸适配体电化学传感器检测铅离子方法,使用电化学方式进行表征检测,不仅检测范围广、灵敏度高、重现性好,检测限低至0.03ng/ml,而且检测非常迅速,dpv扫描分析仅需2min,可在2min时间内对铅离子实现电信号响应,与现场实时快速检测场景匹配度更高;
(4)本发明中建立的核酸适配体电化学传感器检测铅离子方法,操作方便、步骤简洁、无需标记,无需采用复杂的信号扩大方式即可达到较强的电信号值,除此以外,方法所使用的核酸适配体和丝网印刷电极片均成本较低、便于携带,可为包括食品安全在内的现场实时快速检测领域提供一种新的铅离子分析检测方法。
附图说明
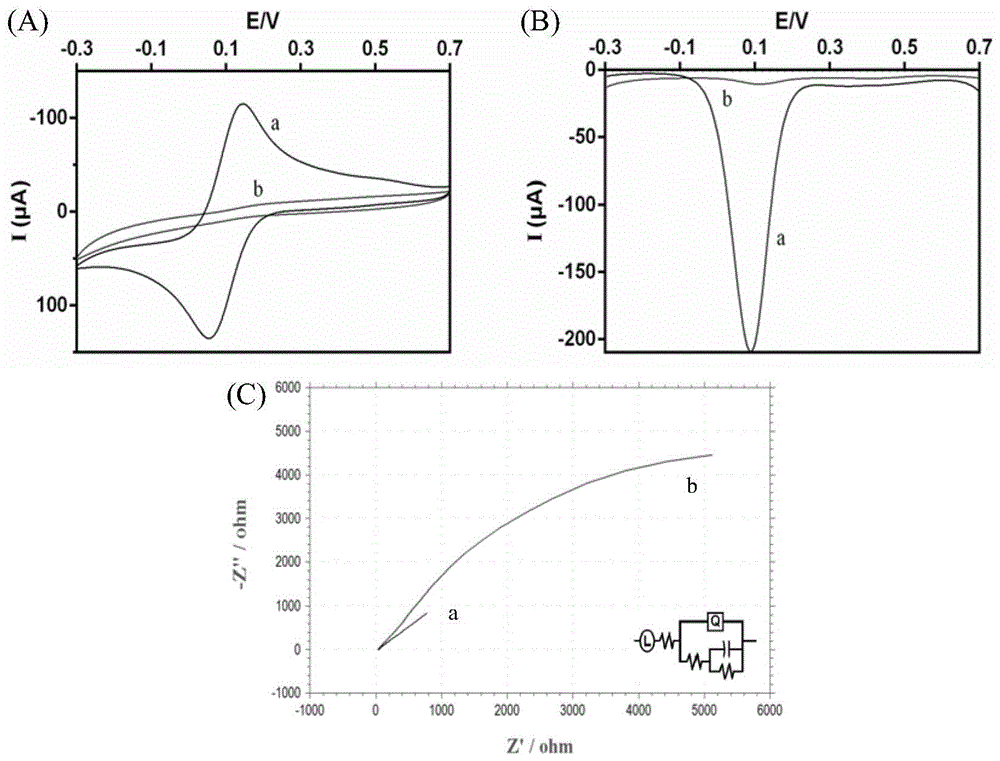
图1为本发明所述的铅离子核酸适配体电化学传感器在组装前后的cv扫描电流(图a)、dpv扫描电流(图b)和eis扫描表征电信号(图c);图中,(a)为组装前的裸金电极,(b)为组装后的核酸适配体。
图2为本发明所述的铅离子核酸适配体电化学传感器检测梯度浓度pb2+后的cv扫描电流(图a)、dpv扫描电流(图b)以及dpv峰电流强度值ip(图c);图中,a→j:组装完成后、0.1ng/ml、0.5ng/ml、1ng/ml、5ng/ml、10ng/ml、50ng/ml、100ng/ml、500ng/ml和1000ng/ml。
图3为基于核酸适配体电化学传感器的铅离子检测方法的线性工作方程曲线。
图4为核酸适配体电化学传感器孵育检测各离子后的(a)dpv扫描电流和(b)特异性评价结果;图中,a→l:组装完成后、铝离子(al3+)、银离子(ag+)、铅离子(cd2+)、钙离子(ca2+)、铜离子(cu2+)、钴离子(co2+)、铬离子(cr3+)、锰离子(mn2+)、钡离子(ba2+)、混合离子和铅离子。
具体实施方式
下面结合实施例对本发明作进一步的阐述,但并不对本发明的范围进行限制。
以下实施例中所使用的核酸适配体序列由上海生工生物工程有限公司合成,且经hplc纯化,所使用的丝网印刷金电极为瑞士万通公司dropsensc220bt型电极,所使用的电化学工作站为上海辰华chi660e型电化学工作站,所使用的电解液分别为5mmk3[fe(cn)6]溶液,含100mmkcl(电解液i)和5mmk3[fe(cn)6]/5mmk4[fe(cn)6]混合溶液(摩尔比1:1),含100mmkcl(电解液ii),所使用的铅离子溶液为硝酸铅pb(no3)2溶于ph7.4的20mmtris-hcl体系缓冲液后形成的母液及梯度稀释液。
实施例1:基于核酸适配体的铅离子电化学传感器构建
(1)丝网印刷金电极电清洁预处理:将丝网印刷金电极片连接至电化学工作站,然后将电极片工作电极一端浸入浓度为0.5m的硫酸溶液中,采用cv对电极片进行电清洁扫描预处理,cv扫描参数为扫描电压范围-0.3v-1.3v,扫描速度0.1v/s,扫描段数60,连续扫描4次共16圈至扫描电流曲线基本稳定后使用超纯水冲洗,静置晾干备用,得到预处理后的丝网印刷金电极;
(2)核酸适配体溶液配制:采用核酸适配体a1(序列号:seqidno:1)的干粉先用浓度为1m的nacl溶液溶解成浓度为100μm的母液后于-20℃冰箱中保存,使用前再用ph7.4的20mmtris-hcl体系缓冲液稀释到5μm;
(3)电极组装构建:滴加7μl浓度为5μm的核酸适配体a1溶液于丝网印刷金电极表面,确保液滴能够最大化地覆盖工作电极而不散开,然后将电极片放入塞有湿棉花的离心管中并于4℃冰箱中过夜组装;
(4)传感器电化学特性表征:电化学传感器完成组装后首先用超纯水清洗电极片,静置晾干后依次在电解液i和ii中进行cv、dpv和eis扫描,cv扫描参数设置为:扫描电压范围-0.3v-0.7v,扫描速度0.1v/s,扫描间隔1mv;dpv扫描表征参数设置为:扫描电压范围-0.3v-0.7v,电位增量4mv,脉冲幅度50mv,脉冲宽度0.05s,脉冲周期0.5s;eis扫描表征参数设置为:初始电压0.22v,高频区段频率105hz,低频区段频率1hz,脉冲宽度5mv,表征结果如图1所示,验证了电化学传感器组装成功。
实施例2:核酸适配体电化学传感器检测铅离子方法的建立
用于检测方法构建的核酸适配体电化学传感器的核酸适配体组装浓度为10μm,组装时间为24h,铅离子的孵育时间为15min,孵育温度为30℃。在该条件下,将所述的核酸适配体电化学传感器依次孵育检测梯度浓度为0.1ng/ml、0.5ng/ml、1.0ng/ml、5.0ng/ml、10.0ng/ml、50.0ng/ml、100.0ng/ml、500.0ng/ml和1000.0ng/ml的铅离子溶液,孵育完成后用超纯水缓慢冲洗并晾干,然后进行cv和dpv扫描分析,依次记录孵育检测各浓度铅离子溶液后的dpv扫描峰电流强度值ipn(n=1,2……9),结果如图2所示;然后减去组装后初始的dpv扫描峰电流强度值i0得到dpv扫描峰电流强度变化值δipn(n=1,2……9),以铅离子浓度的对数为横坐标,δip值为纵坐标,建立的线性工作方程为δip(μa)=9.645×logcpb2+(ng/ml)+13.36,其中cpb2+代表铅离子浓度,方法的线性工作方程如图3所示,其线性关系良好,r2为0.9931,检测限达到0.03ng/ml(s/n=3),完成了检测方法的建立。
实施例3:核酸适配体电化学传感器特异性评价
选取铅离子(cd2+)、钙离子(ca2+)、锰离子(mn2+)、钴离子(co2+)、铝离子(al3+)、铬离子(cr3+)、铜离子(cu2+)、钡离子(ba2+)和银离子(ag+)共9种离子作为干扰离子,在实施例2中所述的最佳检测条件下使用传感器分别对浓度为500ng/ml的干扰离子溶液及其混合离子溶液进行孵育检测。记录传感器孵育不同干扰离子后的dpv扫描ip值,计算其对应变化值δip并与铅离子浓度为5ng/ml时的δip值进行对比,结果如图4所示。从中可以发现,当铅离子浓度仅为5ng/ml时传感器即有明显的电信号响应,而当干扰离子浓度为铅离子浓度的100倍时传感器没有显示出明显的电信号响应,说明了传感器不会对其它重金属离子产生特异反应,传感器特异性较好,方法选择性高。
实施例4:实际加标样品中铅离子的定量检测
本实施例选取鱼肉样品、江水样品和自来水样品共3种样品进行检测,其中鱼肉样品的前处理方式为微波消解,消解定容后先用icp-ms检测溶液中是否含有铅离子,然后取1ml待分析溶液用超纯水稀释100倍,再以体积比1:1与ph7.4的20mmtris-hcl体系缓冲液进行混合,震荡混匀之后备用;江水和自来水样品的前处理方式为过0.22μm滤膜,然后用icp-ms检测是否含有铅离子,再取1ml待分析溶液,以体积比1:1与ph7.4的20mmtris-hcl体系缓冲液进行混合,震荡混匀之后备用。
在完成制样后,采用标准加标法分别向各样品中加入铅离子溶液使得铅离子加标浓度分别为1ng/ml、5ng/ml和50ng/ml,加标后使用传感器分别检测3种样品中的铅离子,通过实施例二中所建立的线性工作方程,计算相应的铅离子实际检出浓度以及检测回收率、相对标准偏差,完成对上述3种加标样品中铅离子的定量检测,并使用icp-ms对样品进行对比检测。检测结果如表1所示,3种样品的检测结果与icp-ms检测结果维持一致,所测样品的加标回收率在92.9%-109.0%之间,相对标准偏差在0.78%-3.29%之间。
表1.实际加标样品检测结果
实施例5:基于不同核酸适配体序列构建并检验电化学传感器的检测效果通过上述实施例1-4构建了基于原始核酸适配体序列a1(序列号:seqidno:1)的铅离子核酸适配体电化学传感器并验证了其对铅离子的检测效果。
进一步通过电化学实验检测结果表明,核酸适配体序列a1中间的cggatcggtatggatggtatt为核心序列,其两端可以与任意相互配对的核苷酸进行搭配形成如a2-a11(序列号:seqidno:2-11)所示的核酸适配体序列,在符合长度为33-35nt且二级结构为固定单一stem-loop的情况下均能对铅离子达到较好的检测灵敏度,具体检测结果如表2所示。
表2.铅离子核酸适配体及其检测灵敏度
尽管已在上文的实施例中对本发明作出了一般性说明和具体详细描述,但并不用于限定本发明。对于熟悉本技术领域的人员而言,凡是在本发明原理和技术方案基础上对其进行的修改、改进、组合和替代,均属于本发明要求的保护范围内。
sequencelisting
<110>暨南大学
<120>铅离子核酸适配体及电化学传感器与制备方法
<130>
<160>11
<170>patentinversion3.5
<210>1
<211>33
<212>dna
<213>人工序列
<400>1
gacgaccggatcggtatggatggtattgtcgtc33
<210>2
<211>33
<212>dna
<213>人工序列
<400>2
ggccttcggatcggtatggatggtattaaggcc33
<210>3
<211>35
<212>dna
<213>人工序列
<400>3
ggactatcggatcggtatggatggtattatagtcc35
<210>4
<211>33
<212>dna
<213>人工序列
<400>4
ctgagtcggatcggtatggatggtattactcag33
<210>5
<211>35
<212>dna
<213>人工序列
<400>5
cgttgcacggatcggtatggatggtatttgcaacg35
<210>6
<211>33
<212>dna
<213>人工序列
<400>6
agctagcggatcggtatggatggtattctagct33
<210>7
<211>33
<212>dna
<213>人工序列
<400>7
gtgcggcggatcggtatggatggtattccgcac33
<210>8
<211>33
<212>dna
<213>人工序列
<400>8
ccaattcggatcggtatggatggtattaattgg33
<210>9
<211>33
<212>dna
<213>人工序列
<400>9
cacggccggatcggtatggatggtattgccgtg33
<210>10
<211>35
<212>dna
<213>人工序列
<400>10
tcggacacggatcggtatggatggtatttgtccga35
<210>11
<211>33
<212>dna
<213>人工序列
<400>11
atgggccggatcggtatggatggtattgcccat33
- 还没有人留言评论。精彩留言会获得点赞!