一种由废锂电池正极活性材料浸出液合成二水草酸钴的方法与流程
本发明属于资源回收技术领域,特别涉及一种由废锂电池正极活性材料浸出液合成二水草酸钴的方法。
背景技术:
锂离子电池主要由外壳、正极(由正极活性材料通过粘结剂涂布于铝箔集流体组成)、负极(由负极活性材料通过粘结剂涂布于铜箔流体组成)、电解液和隔膜组成。正极活性材料主要是选择电化学势较高的、能可逆脱嵌锂离子的化合物,如层状结构的licoo2。天然钴资源少,其主要与其它金属以共生矿的形式存在于矿石中,且其含量仅占矿中金属含量的0.01~0.2%;而废锂电池中的钴含量远高于天然矿石中的含量,以钴酸锂电池为例,其中钴的含量达到15~20%。因此,对废锂电池正极活性材料中的钴元素进行回收和再利用具有可观的环境、经济和社会效益。
目前,废锂电池正极活性材料中钴元素的再生产品主要是二水草酸钴。常用的方法是将草酸或者是草酸铵加入到正极活性材料的浸出液中,通过调整溶液的ph值,反应得到二水草酸钴沉淀。但该工艺流程需要引入外加试剂草酸或草酸铵,流程也相对复杂。
技术实现要素:
有鉴于此,本发明的目的在于提供一种由废锂电池正极活性材料浸出液合成二水草酸钴的方法,本发明提供的方法无需引入外加试剂草酸或草酸铵,工艺流程简单。
为了实现上述发明的目的,本发明提供以下技术方案:
本发明提供了一种由废锂电池正极活性材料浸出液合成二水草酸钴的方法,包括以下步骤:
提供含钴废锂电池正极活性材料;
将所述含钴废锂电池正极活性材料和酒石酸的双氧水溶液混合,进行酸浸,得到浸出液;
将所述浸出液与双氧水混合后进行结晶反应,得到二水草酸钴。
优选的,所述含钴废锂电池正极活性材料的化学组成包括钴酸锂和/或镍钴锰酸锂。
优选的,提供所述废锂电池正极活性材料的方法包括以下步骤:
将含钴废锂电池进行拆解,得到正极片;
将所述正极片进行煅烧,得到所述含钴废锂电池正极活性材料。
优选的,所述煅烧的温度为450~800℃,时间为3~6h。
优选的,所述酒石酸的双氧水溶液中酒石酸的浓度为0.1~1.5mol/l;配制所述酒石酸的双氧水溶液的双氧水的质量分数≤30%。
优选的,所述酒石酸的双氧水溶液的体积与含钴废锂电池正极活性材料的质量的比为1l:(5~100)g。
优选的,所述酸浸的温度为25~80℃,时间为1~6h;所述酸浸在搅拌的条件下进行;所述搅拌的速率为100~400rpm。
优选的,所述结晶反应中,双氧水的质量分数≤30%;所述浸出液与双氧水的体积比为1:(1~10)。
优选的,所述结晶反应的温度为25~80℃,时间为1~120h。
本发明提供了一种由废锂电池正极活性材料浸出液合成二水草酸钴的方法,包括以下步骤:提供含钴废锂电池正极活性材料;将所述含钴废锂电池正极活性材料和酒石酸的双氧水溶液混合,进行酸浸,得到浸出液;将所述浸出液与双氧水混合后进行结晶反应,对结晶反应所得沉淀进行干燥,得到二水草酸钴。在本发明中,酒石酸作为浸出剂和络合剂,将含钴废锂电池正极活性材料中的钴提取出来,此时钴元素以co(iii)的形式与酒石酸的-cooh基团反应生成co(iii)-酒石酸络合物;h2o2具有极强的还原能力,将co(iii)-酒石酸络合物还原为co(ii)-酒石酸络合物,co(ii)-酒石酸络合物是一种弱的复合物,稳定常数很低,其极易解离形成二水草酸钴沉淀。本发明无需向浸出液中外加草酸或草酸铵药剂,即可原位形成二水草酸钴沉淀,试剂体系温和,操作简单。
本发明提供的方法无需向浸出液中外加草酸或草酸铵,即可得到二水草酸钴,试剂体系温和、无二次污染;实施例测试结果表明,所得二水草酸钴纯度≥98%,得率≥95%。
附图说明
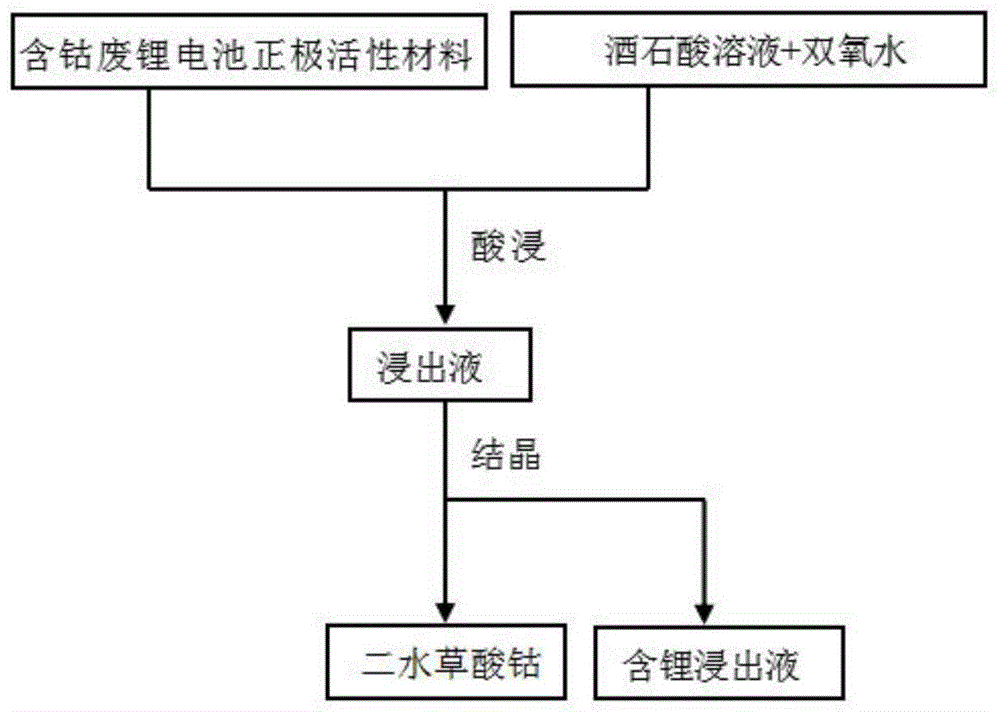
图1为本发明实施例提供的合成二水草酸钴方法的工艺流程图;
图2为实施例1所得浸出液与酒石酸溶液的紫外可见光谱图;
图3为实施例1所得二水草酸钴的xrd图;
图4为实施例1所得二水草酸钴的实物图。
具体实施方式
本发明提供了一种由废锂电池正极活性材料浸出液合成二水草酸钴的方法,包括以下步骤:
提供含钴废锂电池正极活性材料;
将所述含钴废锂电池正极活性材料和酒石酸的双氧水溶液混合,进行酸浸,得到浸出液;
将所述浸出液与双氧水混合后进行结晶反应得到二水草酸钴。
在本发明中,若无特殊说明,所述各组分均为本领域技术人员熟知的市售商品。
图1为本发明提供的由废锂电池正极活性材料浸出液合成二水草酸钴的方法的工艺流程图,下面结合图1,对本发明提供的方法进行具体说明。
本发明提供含钴废锂电池正极活性材料。
在本发明中,所述含钴废锂电池正极活性材料的化学组成优选包括钴酸锂(licoo2)和/或镍钴锰酸锂(licoxniymnzo2)。
在本发明中,提供所述废锂电池正极活性材料的方法优选包括以下步骤:
将含钴废锂电池进行拆解,得到正极片;
将所述正极片进行煅烧,得到所述含钴废锂电池正极活性材料。
本发明优选将含钴废锂电池进行拆解,得到正极片。本发明对所述含钴废锂电池没有特殊限定,采用本领域技术人员熟知的含钴废锂电池即可,具体的,如钴酸锂废电池和/或镍钴锰酸锂废电池,本发明对所述拆解没有特殊限定,采用本领域技术人员熟知的拆解工艺即可。在本发明中,所述正极片与正极集流体的分离方法优选为将含钴废锂电池的正极部分浸泡于有机溶剂中,以使正极集流体与正极片分离;所述有机溶剂优选为n-甲基吡咯烷酮。
得到正极片后,本发明优选将所述正极片进行煅烧,得到所述含钴废锂电池正极活性材料。在本发明中,所述煅烧的温度优选为450~800℃,更优选为500~750℃,最优选为700℃;时间优选为3~6h,更优选为4~5.5h,最优选为5h。在本发明中,所述煅烧的设备优选为马弗炉。
得到含钴废锂电池正极活性材料后,本发明将所述含钴废锂电池正极活性材料和酒石酸的双氧水溶液混合,进行酸浸,得到浸出液。
在本发明中,酒石酸的双氧水溶液优选为由酒石酸和双氧水配制得到;所述双氧水的质量分数优选≤30%,更优选为3~20%,进一步优选为5~10%。在本发明中,所述酒石酸的双氧水溶液中酒石酸的浓度优选为0.1~1.5mol/l,更优选为0.5~1.5mol/l,进一步优选为0.8~1.5mol/l。在本发明中,所述酒石酸的双氧水溶液的体积与含钴废锂电池正极活性材料的质量的比优选为1l:(5~100)g,更优选为1l:(5~50)g,进一步优选为1l:(5~30)g。
在本发明中,所述酸浸的温度优选为25~80℃,更优选为35~80℃,进一步优选为40~80℃;时间优选为1~6h,更优选为1.5~4h,进一步优选为1.5~3h。在本发明中,所述酸浸优选在搅拌的条件下进行;所述搅拌的速率优选为100~400rpm,更优选为100~300rpm,进一步优选为100~250rpm。
酸浸后,本发明优选将酸浸后所得固液混合体系进行固液分离,得到液相产物和固相产物。在本发明中,所述固液分离的方法优选为过滤,更优选为真空抽滤。本发明对所述真空抽滤没有特殊限定,采用本领域技术人员熟知的真空抽滤即可。固液分离后,本发明得到液相产物和固相产物;所述滤液即为浸出液;所述滤渣为未完全反应的含钴废锂电池正极活性材料和石墨组成的混合物(所述石墨来源于含钴废锂电池正极材料)。
得到浸出液后,本发明将所述浸出液与双氧水混合后进行结晶反应,得到二水草酸钴。
在本发明中,所述浸出液与双氧水的体积比优选为1:(1~10),更优选为1:(2~5)。在本发明中,所述双氧水的质量分数优选≤30%,更优选为3~30%,进一步优选为5~30%。
在本发明中,所述酸浸时,过氧化氢有利于使更多的钴离子从锂钴氧中释放出来;所述结晶反应时,过氧化氢有利于促进co(iii)转变成co(ii)。在本发明中,如果酸浸和结晶反应的体系均不含过氧化氢,不会有二水草酸钴生成;酸浸时无过氧化氢,浸出液中钴离子浓度会变偏低,虽然结晶反应中含过氧化氢,会生成二水草酸钴,但生成二水草酸钴的总量较少;酸浸中含过氧化氢,结晶反应中不含过氧化氢,会生成二水草酸钴,但二水草酸钴的生成速率非常慢。
在本发明中,所述结晶反应的温度优选为25~80℃,更优选为40~80℃,进一步优选为60~80℃;时间优选为1~120h,更优选为3~72h,进一步优选为3~48h。在本发明中,所述结晶优选在静置或搅拌的条件下进行;所述搅拌的速率优选为100~300rpm,更优选为150~250rpm。
以含钴废锂电池正极活性物质为钴酸锂为例,本发明所述由废锂电池正极活性材料浸出液合成二水草酸钴的方法中发生的总反应如式i所示反应:
2licoo2+2c4h6o6+4h2o2→2coc2o4·2h2o↓+c4h4o6li2+4h2o+o2↑式i。
反应主要是分两步进行,第一步,酒石酸和锂钴氧反应生成含有钴离子的溶液,过氧化氢促进更多的钴离子从锂钴氧中释放出来;第二步,将浸出液与过氧化氢混合,过氧化氢有利于使溶液中更多的co(iii)-酒石酸络合物还原成co(ii)-酒石酸络合物,由于co(ii)-酒石酸络合物不稳定,因此极易解离生成二水草酸钴。由于无其他沉淀物质生成,因此,本发明所得产品中二水草酸钴的纯度高(≥98%)。
结晶反应后,本发明优选还包括对结晶反应体系进行过滤;本发明对所述过滤没有特殊限定,采用本领域技术人员熟知的过滤即可,具体的,如真空抽滤。在本发明中,过滤所得滤渣即为结晶反应所得沉淀二水草酸钴。
过滤后,本发明优选还包括对所得滤渣进行干燥。在本发明中,所述干燥的温度优选为80~100℃,更优选为85~100℃,进一步优选为90~100℃;时间优选为8~12h,更优选为8~11h,进一步优选为8~10h。
在本发明中,所得二水草酸钴的纯度优选≥98%;得率优选≥95%,更优选为95~98%。说明:在本发明中,所述得率指的是浸出液中的钴元素转变成二水草酸钴的比例。
为了进一步说明本发明,下面结合实施例对本发明提供的一种由废锂电池正极活性材料浸出液合成二水草酸钴的方法进行详细地描述,但不能将它们理解为对本发明保护范围的限定。显然,所描述的实施例仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
实施例1
将钴酸锂废电池进行拆解,其中,正极部分置于n-甲基吡咯烷酮中,以使正极集流体与正极粉分离,得到正极粉;将所述正极粉于700℃煅烧5h,得到含钴废锂电池正极活性材料;
将2g所述含钴废锂电池正极活性材料、400ml浓度为0.8mol/l的酒石酸的双氧水溶液(采用质量分数为5%的双氧水配制得到)混合,在80℃、搅拌速率为100rpm条件下酸浸2h,对酸浸后的体系进行真空抽滤,所得滤液为浸出液,检测得到浸出液中钴离子质量浓度为4.24g/l;
将所述浸出液和质量分数为30%的双氧水按照体积比为2:1混合后,于60℃、搅拌速率为200rpm条件下进行结晶反应24h,对结晶反应后的体系进行真空抽滤,对真空抽滤后所得粉红色沉淀于100℃干燥8h,得到5g二水草酸钴。
对实施例1所得浸出液和酒石酸溶液进行紫外可见光分析,所得紫外可见光谱图见图2。由图2可见,本发明所得浸出液的紫外可见光谱图中呈现三个吸收峰,分别位于240nm、300nm和510nm处,对比酒石酸溶液的紫外可见光谱图可知,240nm处的吸收峰为酒石酸所产生,而510nm处的吸收峰为co(iii)-酒石酸络合物所产生,300nm左右的吸收峰为co(ii)-酒石酸络合物所产生。
对所得二水草酸钴产品进行x射线衍射测试,所得xrd图见图3。由图3可见,该谱图与二水草酸钴的标准谱图一致,没有杂峰,说明本实施例所得产品为高纯的二水草酸钴。
对所得二水草酸钴产品的实物进行观察,所得实物图见图4。由图4可见,本发明所得二水草酸钴为粉红色、结晶度良好的粉末。
对所得二水草酸钴进行测试,测得二水草酸钴纯度100%;二水草酸钴得率为95%。
实施例2
将钴酸锂废电池进行拆解,其中,正极部分置于n-甲基吡咯烷酮中,以使正极集流体与正极粉分离,得到正极粉;将所述正极粉于700℃下煅烧5h,得到含钴废锂电池正极活性材料;
将6g所述含钴废锂电池正极活性材料、250ml浓度为1.5mol/l的酒石酸的双氧水溶液(采用质量分数为10%的双氧水配制得到)混合,在40℃、搅拌速率为200rpm条件下酸浸2h,对酸浸后的体系进行真空抽滤,所得滤液为浸出液,检测得到浸出液中钴离子质量浓度为3.98g/l;
将所述浸出液和质量分数为30%的双氧水按照体积比为4:1混合后,于80℃、搅拌速率为200rpm条件下进行结晶反应6h,对结晶反应后的体系进行真空抽滤,对真空抽滤后所得粉红色沉淀于100℃干燥8h,得到2.96g二水草酸钴。
对所得二水草酸钴进行测试,测得二水草酸钴纯度100%;二水草酸钴得率为96%。
实施例3
将钴酸锂废电池进行拆解,其中,正极部分置于n-甲基吡咯烷酮中,以使正极集流体与正极粉分离,得到正极粉;将所述正极粉于700℃下煅烧5h,得到含钴废锂电池正极活性材料;
将5g所述含钴废锂电池正极活性材料、1000ml浓度为0.8mol/l的酒石酸的双氧水溶液(采用质量分数为10%的双氧水配制得到)混合,在80℃、搅拌速率为200rpm条件下酸浸1.5h,对酸浸后的体系进行真空抽滤,所得滤液为浸出液,检测得到浸出液中钴离子质量浓度为4.6g/l;
将所述浸出液和质量分数为30%的双氧水按照体积比为4:1混合后,于80℃、搅拌速率为200rpm条件下进行结晶反应10h,对结晶反应后的体系进行真空抽滤,对真空抽滤后所得粉红色沉淀于100℃干燥8h,得到13.97g二水草酸钴。
对所得二水草酸钴进行测试,测得二水草酸钴纯度100%;二水草酸钴得率为98%。
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!