一类人参三醇类化合物及其制备方法和医用用途
(td, j = 10.1, 5.0 hz, 1h, ch
‑
12), 1.98
‑
1.51 (m, 15h, panaxotriol
‑
h), 1.45 (s, 9h,
ꢀ‑
c(ch3)3), 1.41
‑
1.32 (m, 3h, panaxotriol
‑
h), 1.26 (s, 3h, panaxotriol
‑
ch3), 1.22 (s, 3h, panaxotriol
‑
ch3), 1.18 (s, 6h, panaxotriol
‑
ch3), 1.13
‑
1.11 (m, 2h, panaxotriol
‑
h), 1.06 (s, 6h, panaxotriol
‑
ch3), 1.00 (s, 1h, panaxotriol
‑
h), 0.96 (s, 3h, panaxotriol
‑
ch3), 0.90 (s, 3h, panaxotriol
‑
ch3), 0.87
‑
0.81 (m, 1h, panaxotriol
‑
h). 13
c
‑
nmr (cdcl3, 75 mhz, ppm): δ 170.18, 155.61, 82.06, 79.86, 77.24, 73.15, 69.72, 68.34, 61.10, 54.64, 50.99, 49.29, 48.76, 47.11, 42.66, 40.96, 38.99, 38.29, 36.41, 35.70, 33.01, 31.08, 30.72, 30.40, 29.68, 28.33 (3c), 27.15, 25.11, 23.37, 19.39, 17.23, 17.16, 17.01, 16.54, 16.23.实施例2药物组合物每片含100 mg 活性成分的1000片片剂配方:化合物ga11
‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑
100 g羟丙基纤维素
‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑
2 g小麦淀粉
‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑
10 g乳糖
‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑
100 g硬质酸镁
‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑
3 g滑石
‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑‑
3 g所用剂量应适应与疾病的性质和严重程度,给药途径以及患者的年龄和体重。日剂量在0.1 mg
‑
1.0 g之间变化,而且可以一次或数次给药。
13.通过以下试验进一步证明本发明化合物的医用用途:试验例1ga11对hif
‑
1的转录活性的影响为了检测化合物ga11对hif
‑
1的转录活性的影响,做了荧光素酶报告基因实验。在1%o2缺氧状态下,将pgl
‑
hre
‑
luc(在pgl
‑
3 promoter 质粒xhoi/kpni位点处插入6个拷贝的增强子的hre)、prl
‑
tk和相应空载体对照质粒转染人肝癌细胞hep3b。从实验结果(图2)中观察到给予化合物ga11后hif
‑
1的转录活性显著降低, 并且随着化合物ga11药物给予浓度的递增,hif
‑
1的转录活性被依次降低。
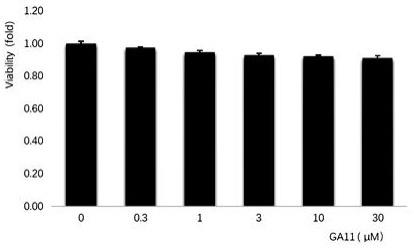
14.试验例2ga11对细胞毒性的影响采用mtt法分别测定化合物ga11对人肝癌细胞hep3b的毒性影响。0.3μm、1μm、3μm、10μm、30μm的化合物ga11处理hep3b细胞24h,然后加入mtt试剂孵育4h,检测结果如图2所示,处理药物组与未处理药物组对比,随着化合物ga11浓度的增加对hep3b细胞毒性无显著差异。初步评价,化合物ga11对hif
‑
1的转录活性的抑制并不是由于其本身对细胞产生毒性引起的。
15.结论:本发明可以制备抗肿瘤药物;或以人参三醇类衍生物为活性成分,同时含有一种
或多种药学上可接受的载体物质和/或辅剂制成药物学上的任何药物制剂。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1