一种氨基环己基类化合物的制备方法与流程
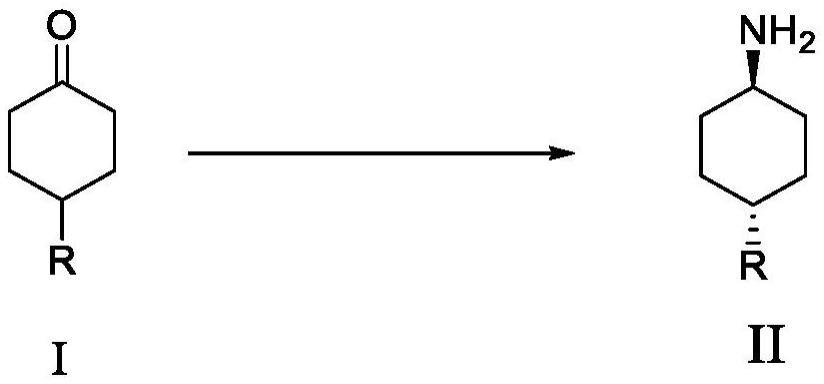
本发明属于化学合成领域,具体涉及一种氨基环己基类化合物的制备方法。
背景技术:
1、氨基环己基类化合物是一种重要的药物合成前体,在是多种处于临床阶段的创新化学药的重要砌块。此前的合成方法是,从对环己酮类化合物出发,经过化学催化形成顺式/反式混合的氨基环己基类化合物,再经过一次或多次重结晶,除去不需要的顺式构型。该法生产的步骤较多、收率较低(通常低于50%),反应是以钯、铂、铑、钌等不可回收的贵金属作为催化剂,成本较高,或者以镍等重金属作为催化剂,会对环境造成污染,且过程中需要在密闭反应装置中使用高压氢气,安全风险较高。
2、与化学法相比,酶催化法具备特异性好、纯度高、反应温和、成本低等特点,是一种替代上述化学方法的绿色新工艺。目前研究和应用较多的天然氨基转移酶(uniprot idf7j696;biotechnol lett,2003,25:1843-1846)(uniprot:f2xbu9;biotechnol bioeng,1999,65,206-211;)(uniprot id:q0c8g1;nat chem biol,2010,6:807-813.)(genbankaccession no.kj496414.1,appl microbiol biotechnol,2014,98(17):7399-7408)(uniprot id:q7nwg4,enzyme.microb.tech,.2007,.41:.628-637)。
3、化合物((1r,4r)-4-氨基甲酰基环己基)氨基甲酸叔丁酯是治疗恶性肿瘤的临床二期药物反式-4-氨基环己烷羧酸乙酯唯一的手性原料。目前这个原料是从昂贵的反-4-氨基环己酸盐酸盐(超过$1,000usd/kg)经过两步反应合成的。且水解过程中采用较多氯碱化工的产物,如氢氧化钾,氢氧化钠等,由于准备过程中氯废物的产生而对环境不友好。
技术实现思路
1、本发明所要解决的技术问题是为了克服现有合成氨基环己基类化合物的方法中存在的原子经济性较低、价格较高、选择性低、活性较差等问题,而提供了一种氨基环己基类化合物的制备方法。本发明合成氨基环己基类化合物的方法与现有技术完全不同;进一步地,本发明的合成方法催化剂用量低、选择性高;更进一步地,本发明的合成方法操作简单,还可以有较高的收率且产品的纯度高。
2、本发明通过以下技术方案来解决上述技术问题。
3、本发明提供了一种反式氨基环己基类化合物的制备方法,其包括如下步骤:在溶剂中,在氨基转移酶和磷酸吡哆醛的存在下,将如式i所示的环己基酮类化合物流加至反应体系中,与氨基供体进行如下所示的胺化反应,即得如式ii所示的反式氨基环己基类化合物;
4、
5、其中,r为-coor1或-cn;r1为h或c1~c6烷基;
6、所述的氨基转移酶为氨基酸序列如seq id no:1所示的来源于巨大芽孢杆菌(bacillus megaterium)的氨基转移酶和/或氨基转移酶的突变体;
7、所述的突变体的突变位点选自如seq id no:1所示的氨基酸序列的第3位、第4位、第5位、第7位、第8位、第9位、第15位、第19位、第21位、第25位、第28位、第29位、第32位、第33位、第37位、第47位、第48位、第51位、第56位、第58位、第61位、第67位、第69位、第76位、第77位、第80位、第84位、第86位、第88位、第94位、第108位、第110位、第113位、第119位、第120位、第121位、第122位、第123位、第124位、第125位、第126位、第131位、第135位、第136位、第140位、第145位、第147位、第148位、第150位、第151位、第152位、第155位、第156位、第159位、第167位、第172位、第173位、第175位、第179位、第185位、第186位、第193位、第198位、第199位、第201位、第202位、第206位、第208位、第209位、第210位、第214位、第225位、第229位、第230位、第231位、第235位、第236位、第238位、第239位、第241位、第242位、第243位、第245位、第249位、第251位、第257位、第260位、第261位、第262位、第270位、第272位、第273位、第274位、第277位、第287位、第292位、第295位、第296位、第297位、第299位、第306位、第307位、第308位、第314位、第315位、第318位、第319位、第322位、第326位、第328位、第329位、第332位、第333位、第337位、第350位、第356位、第358位、第360位、第374位、第376位、第379位、第386位第396位、第398位、第403位、第411位、第417位、第418位、第424位、第428位、第434位、第435位、第439位、第446位、第448位、第450位、第451位、第469位、第472位和第474位中的一个或多个。
8、在某一方案中,所述的制备方法中的某些条件的定义可如下所述,其他条件的定义可如其余任一方案所述(以下简称“在某一方案中”):所述的氨基转移酶突变体的突变位点还包括选自如seq id no:1所示的氨基酸序列的第59位、第60位、第144位、第161位、第164位、第169位、第174位、第240位、第244位、第327位、第330位、第331位、第373位、第387位、第410位、第436位、第437位和第442位中的一个或多个。
9、在某一方案中,所述的c1~c6烷基为c1~c4烷基,优选为甲基、乙基、正丙基、异丙基、正丁基、仲丁基、异丁基或叔丁基,更优选为乙基。
10、在某一方案中,r为-cooh、-coome、-cooet或-cn。
11、所述的流加为本领域进行此类反应的常规的流加方式。本发明中,所述的流加特别优选为通过蠕动泵或注射泵流加物料;通过电子监控系统,可以记录和显示流加速率和/或单位时间内流加物料量。
12、所述的如式i所示的环己基酮类化合物流加的速率为本领域进行此类反应的常规的流加速率。所述流加速率通常与反应规模相关,本发明中,所述流加速率特别优选为1-5ml/h,更优选为1.3ml/h、3ml/h或5ml/h。
13、所述的氨基供体为本领域进行此类反应的常规的氨基供体,本发明中,所述氨基供体特别优选为异丙胺、l-丙氨酸、dl-丙氨酸、l-赖氨酸、dl-赖氨酸、(s)-1-苯乙胺、(r)-1-苯乙胺、(rs)-1-苯乙胺、戊二胺、邻苯二甲胺、邻苯二甲胺盐酸盐、2-(4-硝基苯)乙胺、2-(4-硝基苯)乙胺盐酸盐中的一种或多种;更优选为异丙胺。
14、所述的氨基供体与所述的如式i所示的环己基酮类化合物的摩尔比为本领域进行此类反应的常规的摩尔比;本发明中,所述的氨基供体与所述的如式i所示的环己基酮类化合物的摩尔比特别优选为(0.8-5):1;更优选为1:1、2:1、3:1或4:1。
15、所述的氨基转移酶与所述的如式i所示的环己基酮类化合物的质量比为本领域进行此类反应的常规的质量比;本发明中,所述氨基转移酶与所述的如式i所示的环己基酮类化合物的质量比特别优选为0.025-0.25,更优选为0.25、0.2或0.1。
16、所述的磷酸吡哆醛与所述的氨基转移酶质量比为本领域进行此类反应的常规的质量比。本发明中,所述的磷酸吡哆醛与所述的氨基转移酶质量比特别优选为0.01-0.05;更优选为0.012或0.015。
17、所述的胺化反应的溶剂可为缓冲液,或缓冲液和本领域进行此类反应的常规的有机溶剂的混合物。本发明中,所述的胺化反应的溶剂特别优选为缓冲液。
18、所述的缓冲液为本领域进行此类反应的常规的缓冲液。本发明中,所述的缓冲液特别优选为磷酸盐缓冲液(pbs)、氨基丁三醇缓冲液、三乙醇胺缓冲液、碳酸氢钙-羧酸钙缓冲液和三羟甲基甲胺盐缓冲液中的一种或多种,更优选为磷酸盐缓冲液、三羟甲基甲胺盐缓冲液或三乙醇胺盐缓冲液,例如磷酸盐缓冲液。
19、所述缓冲液的浓度为本领域进行此类反应的常规的浓度,本发明中,所述的缓冲液的浓度特别优选为0.025-1mol/l,更优选为0.2mol/l。
20、所述的有机溶剂为本领域进行此类反应的常规的有机溶剂。本发明中,所述的有机溶剂特别优选为甲基叔丁基醚、异丙醚、四氢呋喃、2-甲基四氢呋喃、1,4-二氧六环、乙酸乙酯、二甲基亚砜、n,n-二甲基甲酰胺、甲醇、乙醇、异丙醇和正丁醇中的一种或多种。
21、当所述的胺化反应的溶剂为所述的缓冲液和所述的有机溶剂混合物时,所述的有机溶剂占反应总体积的比例为0~250ml/l。
22、所述的缓冲液与所述的如式i所示的环己基酮类化合物的体积质量比为本领域进行此类反应的常规的体积质量比;本发明中,所述的缓冲液与所述的如式i所示的环己基酮类化合物的体积质量比特别优选为5~100ml/g,更优选为6~10ml/g,例如:7ml/g、8ml/g、8.7ml/g或9ml/g。
23、所述的胺化反应的ph值为本领域进行此类反应的常规的ph值,本发明中,所述的胺化反应的ph值特别优选为6.0~9.0;更优选为7.0~9.0;例如7.0、7.5或8.0。
24、所述的胺化反应的反应温度为本领域进行此类反应的常规的反应温度,本发明中,所述的胺化反应的反应温度特别优选为10℃~60℃;更优选为47℃。
25、所述的胺化反应的反应时间为本领域进行此类反应的常规的反应时间,所述的胺化反应的反应时间同通常与反应规模相关,本发明中,特别优选为2~20h;更优选为4h。
26、所述的反式氨基环己基类化合物的制备方法,优选包括以下步骤:向所述的缓冲液、所述的氨基供体、所述的吡哆醛和所述的氨基转移酶的混合液中,流加所述的如式i所示的环己基酮类化合物,流加结束后在10℃~60℃下继续反应即可。
27、所述的胺化反应结束后,还可进一步包含后处理步骤。所述后处理步骤可为萃取、干燥、过滤和浓缩中的一种或多种,本发明中,特别优选萃取和/或减压浓缩。
28、所述的胺化反应结束后,所述的后处理步骤优选包括以下步骤:减压浓缩,向体系加入醚类溶剂,用碱调节ph≥10.5,取有机相,有机相干燥并除去醚类溶剂即可。
29、所述的醚类溶剂为本领域进行此类反应的常规醚类溶剂,优选为叔丁基甲醚。
30、所述的醚类溶剂的用量为本领域此类反应的常规用量,本发明中,所述的缓冲液与所述的醚类溶剂的体积比为(0.5:1)-(1.6:1),优选1.1:1、0.9:1或1.5:1。
31、所述的碱为本领域进行此类反应的常规碱,优选为氢氧化钠或氢氧化钾,例如氢氧化钾。
32、在某一方案中,所述的取有机相的方式可为离心。
33、在某一方案中,所述的除去醚类溶剂的方式为本领域进行此类反应的常规方式,优选为减压蒸馏,例如在压力为-0.09mpa下减压蒸馏。
34、在某一方案中,所述的突变体为如seq id no:1所示的氨基酸序列的:
35、第3位替换为:d、g、h、k、n、r、s、w或y;
36、和/或,第4位替换为:d、e、f、i、l、p、r、v或w;
37、和/或,第5位替换为:h、k、l、n或r;
38、和/或,第7位替换为:a、e、k、l、m、n、p、q或t;
39、和/或,第8位替换为:a、g、h、m、p、s、v或w;
40、和/或,第9位替换为:a、c、d、e、h、n、p或q;
41、和/或,第15位替换为:d、e、f、k、l、m、q、s、t、v、w或y;
42、和/或,第19位替换为:a、d、e、g、h、i、m、n、p、r、t、w或y;
43、和/或,第21位替换为:a、c、d、f、g、i、k、l、m、n、p、q、r、s或v;
44、和/或,第25位替换为:e、f、h、i、k、l、m、t、v或w;
45、和/或,第28位替换为:a、d、f、g、k、l、m、r、s、t或v;
46、和/或,第29位替换为:c、d、i、k、q或s;
47、和/或,第32位替换为:c、d、f、g、k、p或y;
48、和/或,第33位替换为:a、g、l、m、n、r或y;
49、和/或,第37位替换为:d、h、k、p、q、s、t、v、w或y;
50、和/或,第47位替换为:a、c、f、g、i、r、s、t、v或w;
51、和/或,第48位替换为:a、e、f、g、h、i、p、q、r、t、v或y;
52、和/或,第51位替换为:c、d、e、f、g、m、n、p、r、w或y;
53、和/或,第56位替换为:c、g、h、i、k、n、r、s或w;
54、和/或,第58位替换为:a、c、f、g、i、l、m、n、p、t或y;
55、和/或,第61位替换为:a、c、l、r、v或w;
56、和/或,第67位替换为:e、f、h、k、m、n、p或y;
57、和/或,第69位替换为:a、g、h、i、l、n、r、s或v;
58、和/或,第76位替换为:a、d、g、l、m、n、p、r、s、t或w;
59、和/或,第77位替换为:a、c、d、h、i、k、n、q、r或t;
60、和/或,第80位替换为:a、f、h、k、p、q、w或y;
61、和/或,第84位替换为:c、f、h、k、l、m、p、q、t、v、w或y;
62、和/或,第86位替换为:a、d、e、g、i、k、n、p、s、t、v、w或y;
63、和/或,第88位替换为:a、e、f、g、k、l、m、n、s、t或y;
64、和/或,第94位替换为:c、d、f、g、i、k、n、p、q、r、s或w;
65、和/或,第108位替换为:a、d、g、h、i、m、q或t;
66、和/或,第110位替换为:c、e、f、q、r或v;
67、和/或,第113位替换为:a、c、d、f、h、i、l、n、r或s;
68、和/或,第119位替换为:c、d、f、g、h、i、k、m、n、p、s或v;
69、和/或,第120位替换为:a、c、f、h、i、k、m、n、p或q;
70、和/或,第121位替换为:f、h、i、q、s、v、y、f或i;
71、和/或,第122位替换为:l、n、v或y;
72、和/或,第123位替换为:f、g、h、k、s或t;
73、和/或,第124位替换为:c、d、f、n、p或w;
74、和/或,第125位替换为:d、e、g、k、n、p、r、s或t;
75、和/或,第126位替换为:a、c、f、g、l、n、p、q或w;
76、和/或,第131位替换为:c、g、h、i、m、r、t、v或w;
77、和/或,第135位替换为:a、d、g、h、k、l、q、r、t或y;
78、和/或,第136位替换为:e、f、g、k、m、n、p、s、v或w;
79、和/或,第140位替换为:c、g、k、m、n、p、r或s;
80、和/或,第145位替换为:d、e、f、g、i、k、l、m、q、v、w或y;
81、和/或,第147位替换为:d、f、g、h、k、m、q、r、t、v、w或y;
82、和/或,第148位替换为:a、e、f、k、l、m、n、q、r、s、t或v;
83、和/或,第150位替换为:a、c、g、h、i、k、l、r、s、t或v;
84、和/或,第151位替换为:c、e、g、k、l、m、q、r、s或w、
85、和/或,第152位替换为:d、i、k、m、n、p、q、r、v或y、
86、和/或,第155位替换为:e、f、k、m、n、p、r、s、t、w或y、
87、和/或,第156位替换为:c、d、e、g、i、l、m、n、p、q、r或w、
88、和/或,第159位替换为:d、e、f、g、h、i、k、m、n、p、v或y、
89、和/或,第167位替换为:e、f、g、h、i、k、m、n、q、r、s、t或w;
90、和/或,第172位替换为:a、c、d、e、g、h、m、n、p、q、r、s、t、v或w;
91、和/或,第173位替换为:c、f、p、q、r或v;
92、和/或,第175位替换为:d、e、g、h、i、k、s、v、w或y;
93、和/或,第179位替换为:a、c、f、g、i、l、m、n、q、r或v;
94、和/或,第185位替换为:a、d、e、f、h、i、k、m、n、p、t、v或w;
95、和/或,第186位替换为:a、d、e、f、h、k、l、m、n、p、q或t;
96、和/或,第193位替换为:a、c、f、h、k、l、n、q、r、s、t或y;
97、和/或,第198位替换为:a、f、g、i、l、m、n、p、r、t、v或y;
98、和/或,第199位替换为:c、d、h、i、k、m、n、p、q、r或w;
99、和/或,第201位替换为:a、c、d、f、i、l、m、n、p、r、s或t;
100、和/或,第202位替换为:a、f、g、h、i、k、m、n、p、q、s或y;
101、和/或,第206位替换为:a、c、d、f、m、n、p、r、s、w或y;
102、和/或,第208位替换为:c、h、i、k、m、q、r或v;
103、和/或,第209位替换为:d、e、g、i、l、p、t、v、w或y;
104、和/或,第210位替换为:a、g、h、i、k、l、q、s或t;
105、和/或,第214位替换为:a、e、f、l、m、n、p、s、t或w;
106、和/或,第225位替换为:d、i、l、m、q、r、v或w;
107、和/或,第229位替换为:a、c、f、g、h、k、m、p或r;
108、和/或,第230位替换为:a、c、f、g、h、k、m、q、t、v或w;
109、和/或,第231位替换为:a、d、e、f、i、k、l、p、r或t;
110、和/或,第235位替换为:a、c、d、e、i、k、m、p、s或t;
111、和/或,第236位替换为:c、e、g、h、i、m、n、p、s、w或y;
112、和/或,第238位替换为:c、d、e、f、h、k或p;
113、和/或,第239位替换为:a、c、f、g、h、i、k、q、s、t、w或y;
114、和/或,第241位替换为:a、d、k、p、q、t或v;
115、和/或,第242位替换为:a、c、d、g、h、k、m、p、q、r、w或y;
116、和/或,第243位替换为:a、d、f、k、r、v、w或y;
117、和/或,第245位替换为:a、d、g、h、i、k、l、m、n、q、r、s、t或w;
118、和/或,第249位替换为:a、c、f、k、l、q、s、v或w;
119、和/或,第251位替换为:f、g、i、l、n、p、q、s、t、w或y;
120、和/或,第257位替换为:g、p、q或t;
121、和/或,第260位替换为:a、e、g、h、l、m、q、r、s、t、v或w;
122、和/或,第261位替换为:a、d、f、g、k、m、n、r、t、w或y;
123、和/或,第262位替换为:a、e、f、g、k、q、v或w;
124、和/或,第270位替换为:c、d、e、f、g、h、i、l、p、q、r、s或w;
125、和/或,第272位替换为:c、e、f、g、l、p、r、s、t或v;
126、和/或,第273位替换为:f、l、m、n、p、q、r、t、v、w或y;
127、和/或,第274位替换为:a、c、f、g、i、k、l、m、n、r、t或y;
128、和/或,第277位替换为:c、d、h、i、l、m、n、p、q或y;
129、和/或,第287位替换为:d、e、g、k、l、m、n、p、q或y;
130、和/或,第292位替换为:e、h、i、k、l、t、v、w或y;
131、和/或,第295位替换为:a、f、r、s、v或y;
132、和/或,第296位替换为:a、d、e、f、g、i、l、m、p、q、r或t;
133、和/或,第297位替换为:a、f、i、k、l、m、p、r、s或w;
134、和/或,第299位替换为:c、d、e、f、g、h、l、m、p、r或v;
135、和/或,第306位替换为:a、c、i、n、s或y;
136、和/或,第307位替换为:c、e、g、k、p、r、t或y;
137、和/或,第308位替换为:e、f、g、h、l、m、n、r、s或y;
138、和/或,第314位替换为:c、d、f、h、n、p、r、s、v或y;
139、和/或,第315位替换为:a、c、d、e、f、h、i、l、m、p、q、r或s、w或y;
140、和/或,第318位替换为:d、e、f、i、k、l、m、n、q、s、t或w;
141、和/或,第319位替换为:c、h、i、k、l、p、q、r或v;
142、和/或,第322位替换为:a、e、f、g、i、l、n、s或w;
143、和/或,第326位替换为:d、g、h、i、n、r、s、t或y;
144、和/或,第327位替换为:e、f、g、h、m、q、t或y;
145、和/或,第328位替换为:a、c、e、h、l、m、p、r或s;
146、和/或,第329位替换为:a、c、d、e、k、m、q、t或w;
147、和/或,第332位替换为:c、d、e、m、q、s、t、v或y;
148、和/或,第333位替换为:h、l、t或y;
149、和/或,第337位替换为:e、f、g、k、p、q、r、s、v或y;
150、和/或,第350位替换为:d、e、f、h、p、q、t、v或w;
151、和/或,第356位替换为:a、d、e、f、h、l、m、n、p、r、s或t;
152、和/或,第358位替换为:c、g、i、k、n、p、q、s、t或w;
153、和/或,第360位替换为:c、e、f、l、p、q、r、s或y;
154、和/或,第373位替换为:a、c、d、e、f、g、h、i、m、n、q、r、s、w或y;
155、和/或,第374位替换为:c、d、g、l、n、p、q、r、s、t、v、w或y;
156、和/或,第376位替换为:a、c、e、g、h、i、l、m、q、s、t、v或y;
157、和/或,第379位替换为:d、e、h、k、m、n、p、r、w或y;
158、和/或,第386位替换为:a、d、e、f、h、r、v或w;
159、和/或,第396位替换为:a、d、g、h、k、l、m、n、p、q、r、s或y;
160、和/或,第398位替换为:a、f、g、h、k、l、n、p、q或t;
161、和/或,第403位替换为:f、g、k、p、q、r、s、t、v、w或y;
162、和/或,第410位替换为:d、e、f、m、n、p、r或s;
163、和/或,第411位替换为:a、c、d、e、g、i、l、s、t或y;
164、和/或,第417位替换为:c、d、e、g、h、i、l、m、p或v;
165、和/或,第418位替换为:e、f、g、h、l、n、r、s、v、w或y;
166、和/或,第424位替换为:a、h、i、k、l、m、n、p、r或w;
167、和/或,第428位替换为:c、d、e、l、n、p、s、v、w或y;
168、和/或,第434位替换为:a、c、d、h、i、l、m、n、s或t;
169、和/或,第435位替换为:a、d、e、f、h、l、n、p、q、s、t、w或y;
170、和/或,第439位替换为:c、d、f、i、k、s、w或y;
171、和/或,第446位替换为:a、e、g、k、l、m、n、p、r或t;
172、和/或,第448位替换为:a、d、e、f、k、r、w或y;
173、和/或,第450位替换为:c、e、f、h、i、n、r、s或t;
174、和/或,第451位替换为:d、e、g、i、l或q;
175、和/或,第469位替换为:a、e、f、g、h、i、l、m或n;
176、和/或,第472位替换为:a、f、l、p、r、s、t或y;
177、和/或,第474位替换为:a、d、f、h、i、k、l、m、n、q、r、v或w。
178、在某优选一方案中,所述的突变体的还包括为如seq id no:1所示的氨基酸序列的:
179、和/或,第59位替换为:e、f、i、k、l、m、p、r、t、v或y;
180、和/或,第60位替换为:c、d、e、f、h、i、k、l、m、n、p、r、s、t、v、w或y;
181、和/或,第144位替换为:a、e、g、i、m、p、q、r、w或y;
182、和/或,第161位替换为:c、d、m或s;
183、和/或,第164位替换为:a、f、g、h、i、l、n、q、r、s、v或w;
184、和/或,第169位替换为:l;
185、和/或,第174位替换为:c、f、g、h、k、l、m、p、r、s、t、v、w或y;
186、和/或,第240位替换为:a、d、f、i、k、m、p、s、t或w;
187、和/或,第244位替换为:c、d、h、l、q、r、s、t、w或y;
188、和/或,第330位替换为:a、d、e、i、v或y;
189、和/或,第331位替换为:a、i、m、n、p、q、s、t或w;
190、和/或,第387位替换为:a、c、d、h、i、m、n、p、q、r、s、t、v、w或y;
191、和/或,第422位替换为:n;
192、和/或,第436位替换为:a、f、g、h、k、m、n、p、q、r、s或y;
193、和/或,第437位替换为:e、f、h、i、l、n、q、r、t、w或y;
194、和/或,第442位替换为:d、e、f、g、h、i、k、l、n、q、r、t、v或y。
195、在某一方案中,所述的突变体的突变位置和种类如表1所示:
196、表1
197、
198、
199、
200、
201、
202、
203、
204、
205、
206、
207、
208、
209、
210、本发明提供了一种如式iii所示的化合物的制备方法,其包括如下步骤:
211、步骤一:在溶剂中,在氨基转移酶和磷酸吡哆醛的存在下,将如式i所示的环己基酮类化合物与氨基供体进行如下所示的胺化反应,即得如式ii所示的反式氨基环己基类化合物;
212、
213、步骤二:在溶剂中,将步骤一得到的所述的如式ii所示的反式氨基环己基类化合物与氨基保护剂进行如下所示的氨基保护反应,得到如式iii所示的化合物即可;
214、
215、其中,r的定义同前所述,pg为氨基保护基。
216、步骤一中各反应参数和条件的定义可同前所述。
217、所述的步骤二中,所述的氨基保护基为本领域进行此类反应的常规的氨基保护基,本发明中,所述的氨基保护基特别优选为乙酰基、
218、所述的步骤二中,所述的氨基保护反应可在碱性条件下进行。所述的碱性条件可通过可产生碱性条件的添加剂得到。所述的添加剂为本领域常规的可产生碱性条件的添加剂,本发明中,所述的添加剂特别优选为二异丙基乙基胺、三乙胺、甲醇钠、甲醇锂、碳酸钾、碳酸钠、双三甲基硅基胺基锂、双三甲基硅基胺基钾、叔丁醇钠、叔丁醇钾、乙酸钠、醋酸锌和乙酸钾中的一种或多种。优选为二异丙基乙基胺和/或三乙胺。
219、所述的步骤二中,所述的溶剂为本领域进行此类反应的常规溶剂,本发明中,所述的溶剂特别优选为甲醇、乙醇、四氢呋喃、甲基四氢呋喃、二氧六环、n-甲基吡咯烷酮、二氯甲烷和甲基叔丁基醚中的一种或多种,更优选为二氯甲烷。
220、所述的步骤二中,所述的如式ii所示的反式氨基环己基类化合物与所述的添加剂的摩尔比为本领域进行此类反应的常规摩尔比,本发明中,所述的如式ii所示的反式氨基环己基类化合物与所述的添加剂的摩尔比特别优选为(0.1-1.5):1,更优选为(0.3-1):1,例如:0.3:1、0.4:1、0.8:1或1:1
221、所述的步骤二中,所述的溶剂与所述的如式ii所示的反式氨基环己基类化合物的体积质量比为本领域进行此类反应的常规体积质量比,本发明中,特别优选为5-100ml/g,更优选为10~25ml/g,例如:12ml/g、15ml/g或20ml/g。
222、所述的步骤二中,所述反应温度为本领域进行此类反应的常规反应温度,本发明中,特别优选为10-100℃,更优选为25℃。
223、所述的步骤二中,所述反应时间为本领域进行此类反应的常规反应时间,本发明中,特别优选为0.5-72小时。
224、所述的步骤二中,所述的氨基保护反应结束后,还可进一步包括如下后处理步骤:反应液用1m硫酸氢钠溶液洗涤两次;分液后取上层清液后减压浓缩。
225、本发明提供了一种如式iv所示的化合物的制备方法,其包括如下步骤:在溶剂中,在水解酶的存在下,如式iii所示的化合物进行如下所示的水解反应,得到如式iv所示的化合物即可;
226、
227、其中,r为-coor1或-cn;r1为c1~c6烷基;pg为氨基保护基;
228、所述的水解酶为来源于南极假丝酵母(candida antarctica)、皱褶假丝酵母(candida rugosa)、米黑根毛霉(rhizomucor miehei)或洋葱假单胞菌(pseudomonascepacia)的水解酶。
229、在某一方案中,所述的水解酶优选为对应于gen bank:z30645.1、gen bank:caa45957.1、uniprot:p19515或ncbi:wp_193100961.1的酶。
230、所述的c1~c6烷基定义同前所述。
231、所述的氨基保护基同前所述。
232、所述的水解反应的溶剂可为缓冲液,或缓冲液和本领域进行此类反应的常规的有机溶剂的混合物。本发明中,所述的水解反应的溶剂特别优选为缓冲液和有机溶剂的混合物。
233、所述的缓冲液为本领域进行此类反应的常规的缓冲液,本发明中,所述的缓冲液特别优选为磷酸盐缓冲液(pbs)、氨基丁三醇缓冲液、三乙醇胺缓冲液、碳酸氢钙-羧酸钙缓冲液和三羟甲基甲胺盐缓冲液中的一种或多种,更优选为磷酸盐缓冲液、三羟甲基甲胺盐缓冲液或三乙醇胺盐缓冲液,例如磷酸盐缓冲液。
234、所述的缓冲液的浓度为本领域进行此类反应的常规的浓度。本发明中,所述的缓冲液的浓度特别优选为0.025-1mol/l,更优选0.025mol/l、0.2mol/l或1mol/l。
235、所述的缓冲液的ph值为本领域进行此类反应的常规的ph值,本发明中,所述的缓冲液的ph值特别优选为5.0~9.0;更优选为6.0~8.0;例如6.5、7.0或7.5。
236、所述的有机溶剂为本领域进行此类反应的常规的有机溶剂。本发明中,所述的有机溶剂特别优选为甲基叔丁基醚、正庚烷、四氢呋喃、甲基四氢呋喃、乙腈、叔丁醇、正丁醇、甲苯和二甲基亚砜中的一种或多种;更优选为叔丁醇。
237、所述的缓冲液与所述的有机溶剂的体积比为本领域进行此类反应的常规的体积比。本发明中,所述的缓冲液和所述的有机溶剂的体积比特别优选为9:1-1:9,更优选为9:1、8:2、7:3、6:4、5:5、4:6、3:7、2:8或1:9。
238、所述的缓冲液与所述的如式iii所示的化合物的体积质量比为本领域进行此类反应的常规体积质量比。本发明中,所述的缓冲液与所述的如式iii所示的化合物的体积质量比特别优选为5-100ml/g,更优选为5-30ml/g;例如22ml/g、18ml/g、14ml/g或10ml/g。
239、所述的水解酶与所述的如式iii所示的化合物的质量比为本领域此类反应的常规体积质量比。本发明中,所述的水解酶与所述的如式iii所示的化合物的质量比特别优选为0.025-1.0,更优选为0.1~0.5,例如0.25~0.5。
240、所述的水解反应的反应温度为本领域进行此类反应的常规反应温度。本发明中,所述的水解反应的反应温度特别优选为10-50℃,更优选为30℃。
241、所述的水解反应的反应时间为本领域进行此类反应的常规反应时间。反应时间同通常与反应规模相关,本发明中,所述的水解反应的反应时间特别优选为0.5-48小时。
242、所述的水解反应结束后,还可进一步包含后处理步骤。所述后处理步骤可为萃取、干燥、过滤和浓缩中的一种或多种,本发明中,特别优选过滤。
243、所述的水解反应结束后,所述的后处理步骤优选包括以下步骤:反应液滤去水解酶,加酸调节ph5~6,析出固体,过滤得到所述的如式iv所示的化合物即可。
244、所述的酸为本领域进此类反应的常规的酸,本发明中,特别优选为柠檬酸。
245、本发明提供了一种如式iv所示的化合物的制备方法,其包括如下步骤:
246、步骤1.1:在溶剂中,将如式ii所示的反式氨基环己基类化合物与氨基保护试剂进行如下所示的氨基保护反应,得到如式iii所示的化合物即可;
247、
248、步骤1.2:在溶剂中,在水解酶的存在下,将步骤1.1得到的所述的如式iii所示的化合物进行如下所示的水解反应,得到所述的如式iv所示的化合物即可;
249、
250、其中,r为-coor1或-cn;r1为c1~c6烷基;pg为氨基保护基,所述氨基保护基同前所述;步骤1.1和步骤1.2各反应参数和条件的定义可同前所述。
251、本发明提供了一种如式iv所示的化合物的制备方法,其包括如下步骤:
252、步骤2.1:在溶剂中,在氨基转移酶和磷酸吡哆醛的存在下,将如式i所示的环己基酮类化合物与氨基供体进行如下所示的胺化反应,即得如式ii所示的反式氨基环己基类化合物;
253、
254、步骤2.2:在溶剂中,将步骤2.1得到的所述的如式ii所示的反式氨基环己基类化合物与氨基保护试剂进行如下所示的氨基保护反应,得到如式iii所示的化合物即可;
255、
256、步骤2.3:在溶剂中,在水解酶的存在下,将步骤2.2得到的所述的如式iii所示的化合物进行如下所示的水解反应,得到所述的如式iv所示的化合物即可;
257、
258、其中,r为-coor1或-cn;r1为c1~c6烷基;pg为氨基保护基,所述氨基保护基同前所述;步骤2.1、步骤2.2和步骤2.3各反应参数和条件的定义可同前所述。
259、本发明提供了一种如式v所示的化合物的制备方法,其包括如下步骤:在溶剂中,在水解酶的存在下,如式ii所示的化合物进行如下所示的水解反应,得到如式v所示的化合物即可;
260、
261、其中,r为-coor1或-cn;r1为c1~c6烷基。
262、所述水解反应的各反应参数和条件的定义可与如式iv所示的化合物的制备方法中的水解反应的各反应参数和条件的定义相同。
263、本发明提供了一种如式v所示的化合物的制备方法,其包括如下步骤:
264、步骤3.1:在溶剂中,在氨基转移酶和磷酸吡哆醛的存在下,将如式i所示的环己基酮类化合物与氨基供体进行如下所示的胺化反应,即得如式ii所示的反式氨基环己基类化合物;
265、
266、步骤3.2:在溶剂中,在水解酶的存在下,将步骤3.1得到的所述的如式ii所示的化合物进行如下所示的水解反应,得到如式v所示的化合物即可;
267、
268、其中,r为-coor1或-cn;r1为c1~c6烷基;步骤3.1各反应参数和条件的定义可同前所述。
269、步骤3.2中所述水解反应的各反应参数和条件的定义可与如式iv所示的化合物的制备方法中的水解反应可以的各反应参数和条件的定义相同。
270、在不违背本领域常识的基础上,上述各优选条件,可任意组合,即得本发明各较佳实例。
271、本发明所用试剂和原料均市售可得。
272、本发明的积极进步效果在于:本发明合成氨基环己基类化合物的方法与现有技术完全不同;进一步地,本发明的合成方法催化剂用量低、选择性高;更进一步地,本发明的合成方法操作简单,还可以有较高的收率且产品的纯度高;另外,经对环己酮甲酸乙酯合成如式iii所示的化合物,绕过了昂贵的物料,同时在水解过程中采用酶催化水解,避免了氯碱化工的产物的应用,原子经济性高,且路线更短,成本最低。
- 还没有人留言评论。精彩留言会获得点赞!