一种用于检测荚膜组织胞浆菌的特异引物对及其应用
1.本发明属于微生物菌检测技术领域,具体涉及一种用于检测荚膜组织胞浆菌的特异引物对及其应用。
背景技术:
2.荚膜组织胞浆菌(histoplasma capsulatum)是一种易引起免疫功能低下、患者深部感染的机会致病真菌,主要流行在美国中西部和拉丁美洲。由于其具有易导致患者肺部急、慢性感染,甚至引起播散性感染、治愈过程复杂且容易导致死亡等致病特征,该菌已被包括我国在内的多个国家列为生物危害程度3类的高致病性病原真菌(参见王牛牛,郑建铭,刘丽光,播散型组织胞浆菌病研究进展,微生物与感染,2020年12月25日,第15卷第6期:429-434页;潘炜华,我国组织胞浆菌病的流行特点及防治,皮肤科学通报,2017年l0月第34卷第5期;katia cristina dantas et al.comparison of diagnostic methods to detect histoplasma capsulatum in serum and blood samples from aids patients.plos one.2018;13(1):e0190408)。近年来,荚膜组织胞浆菌病在我国除了传统的输入型病例,也不断出现散发的本土病例;同时,ji wang、周莉等人在报道中发现,由于该病临床表现无特异性,病原学检测手段有限,临床病理涂片分析上极易与另一种病原真菌马尔尼菲篮状菌(talaromyces marneffei)混淆,导致错误诊断和治疗。因此急需找到一种针对荚膜组织胞浆菌检测与鉴定的方法(参见周莉,范松青,梁青春等,8例组织胞浆茵病临床特征分析并文献复习,中南大学学报(医学版),2016年第41卷第6期;ji wang et al.identification of histoplasma causing an unexplained disease cluster in matthews ridge,guyana.biosafety and health(2019)150
–
154)。
3.考虑到传统荚膜组织胞浆菌以培养为金标准进行病原菌的诊断,需要耗时3-4周,易错过最佳治疗时间,且在培养过程中具有一定实验室传播风险(参见g.s.de hoog,j.guarro,j.gen
é
,et al.atlas of clinical fungi[m].4th edition 2020);而利用病理涂片分析又容易与马尔尼菲篮状菌等其他病原菌混淆。因此,本领域技术人员需探索一种可以规避以上弊端,利用分子技术进行快速检测的技术方法,确保在安全的实验操作活动中,用最短时间给出明确的鉴定结果,有效保障荚膜组织胞浆菌病的临床快速检测鉴定。
[0004]
此前,国内已有少量关于荚膜组织胞浆菌特异性分子诊断引物设计的专利申请,例如“用于检测荚膜组织胞浆菌的lamp引物组、试剂盒及方法”(申请人为中国医学科学院北京协和医院、北京博奥晶典生物技术有限公司,专利申请号:202110457838.3,专利申请日:2021.07.23),该方法主要采用lamp方法,但lamp技术高度敏感,因此容易出现假阳性,在目前条件下的国内实验室都不易大面积推广;同时也是由于lamp的高敏感度,因此对引物设计要求极高,要求具备高度的特异性和灵敏性;但该专利中,发明人在阴性对照干扰排除方面的涉及菌种过少(3种真菌),未对临床其他常见病原真菌开展干扰排除的阴性扩增实验,尤其是易混淆的马尔尼菲篮状菌未纳入对照组中,一旦临床涂片或病理诊断中出现疑似感染,无法排除马尔尼菲篮状菌存在的可能性;同时上述专利中阳性荚膜组织胞浆菌
样本设置量偏少(1株),不能够确保实验设计中样本的覆盖广度。
技术实现要素:
[0005]
发明目的:本发明目的在于针对现有技术的不足,提供一种用于检测荚膜组织胞浆菌的特异引物对,利用常规pcr技术,快速精确实现荚膜组织胞浆菌的检测。所设计的引物对亦可优化用于荧光定量pcr,进行实时快速检测。本发明从分子检测扩增角度挖掘临床快速鉴定的分子靶标引物,以达到对荚膜组织胞浆菌临床疑似标本的精准、快速鉴定及与马尔尼菲篮状菌区分的能力,为荚膜组织胞浆菌病的临床检测及疾病预防控制提供有力手段。
[0006]
技术方案:本发明的目的通过下述技术方案实现:
[0007]
本发明提供了一种检测荚膜组织胞浆菌的特异性引物对,包括如下六组正向引物和反向引物:
[0008]
(1)第一组
[0009]
cp069117.1_s3857-f:tgcgatcctgttgtgtgaca
[0010]
cp069117.1_s3857-r:cgtcctatgccagcacactt;
[0011]
(2)第二组
[0012]
cp069117.1_s6964-f:gtcgagcatacgcctcactt
[0013]
cp069117.1_s6964-r:tatcgacgtccagttctcgc;
[0014]
(3)第三组
[0015]
cp069117.1_s7420-f:gagactccttgcctggatcg
[0016]
cp069117.1_s7420-r:ccgtccgtggctaagaatgt;
[0017]
(4)第四组
[0018]
cp069118.1_s4904-f:cacaatggagaggagcacca
[0019]
cp069118.1_s4904-r:gctgttgcgccattggttat;
[0020]
(5)第五组
[0021]
cp069118.1_s11573-f:tcggaattggaacgtcggtt
[0022]
cp069118.1_s11573-r:ggtacgatcattggccgtca;
[0023]
(6)第六组
[0024]
cp069118.1_s11966-f:ggcggtaagtcgttcaggac
[0025]
cp069118.1_s11966-r:tgtcaggcactccgattcag。
[0026]
上述6组特异性引物对均可实现对荚膜组织胞浆菌的检测。
[0027]
本发明还提供了上述特异性引物对在检测荚膜组织胞浆菌中的应用。
[0028]
进一步地,荚膜组织胞浆菌的检测方法,包括如下步骤:
[0029]
(1)提取待测样品中真菌的dna;
[0030]
(2)采用上述任意一组检测荚膜组织胞浆菌的特异性引物对,对步骤(1)获得的样品dna进行pcr扩增;
[0031]
(3)扩增后对pcr产物进行电泳条带检测分析。
[0032]
进一步地,上述pcr扩增的反应体系(20μl)如下:
[0033][0034]
上述反应体系中涉及的试剂均可从new england biolabs公司获得。
[0035]
进一步地,所述pcr反应程序为:
[0036]
(a)95℃预变性5min;
[0037]
(b)(95℃变性30s;55℃退火30s;72℃延伸45s)
×
35循环
[0038]
(c)72℃总延伸10min。
[0039]
本发明首先设计了特异性引物对,再分别采用各组特异性引物对对待测样品中的dna进行pcr扩增,以精确检测待测样品中荚膜组织胞浆菌。本发明检测方法具有检测快速、特异性强、操作便捷、检测准确的优点。本发明从分子检测扩增角度挖掘临床快速鉴定的分子靶标引物,以达到对荚膜组织胞浆菌临床疑似标本的精准、快速鉴定及与马尔尼菲篮状菌区分的能力,为荚膜组织胞浆菌病的临床检测及疾病预防控制提供有力手段。
附图说明
[0040]
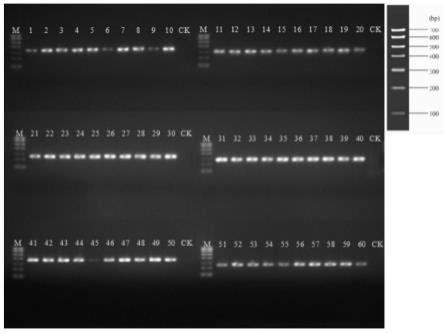
图1为10株不同进化支的荚膜组织胞浆菌利用设计的六组特异引物对扩增阳性的电泳图。
具体实施方式
[0041]
下面通过具体实施例对本发明技术方案进行详细说明,但是本发明的保护范围不局限于所述实施例。
[0042]
实施例1筛选荚膜组织胞浆菌的特异性靶基因位点,设计扩增引物
[0043]
1、基因组查找:在genebank网站(https://www.ncbi.nlm.nih.gov/)查询分析histoplasma capsulatum和talaromyces marneffei两个物种的所有基因组数据信息,如下:histoplasma capsulatum:基因组登录号:gca_000150115.1,gca_017310585.1,gca_017607465.1,gca_013420885.1,gca_000151005.2,gca_000151035.1,gca_000313325.1,gca_017355575.1,gca_017310615.1
[0044]
talaromyces marneffei:基因组登录号:gca_000001985.1,gca_003971505.1,gca_009556855.1,gca_009650675.1,gca_013122295.1,gca_006111635.1,gca_011320185.1,gca_000750115.1,gca_000227055.2。
[0045]
2、引物设计:
[0046]
(1)基于下载的基因组查找histoplasma capsulatum和talaromyces marneffei
物种内共有的基因组片段;
[0047]
(2)共有序列比对talaromyces marneffei的基因组,找到比对不上talaromyces marneffei的序列;
[0048]
(3)根据特有序列设计引物(保证扩增产物在150-280bp),然后引物比对talaromyces marneffei参考基因组,过滤掉可比对上的引物;
[0049]
(4)基于上述筛选剩余的引物,继续过滤掉含有三个连续的重复单碱基引物;
[0050]
(5)过滤掉产物含有小写atcg,和n的序列;
[0051]
(6)引物和产物比对histoplasma capsulatum基因组,入选只能在基因组上比对到一个片段的产物和引物。
[0052]
根据上述方法,初步设计获得10对特异引物,详细序列信息见表1:
[0053]
表1初步设计获得的10对特异引物
[0054][0055]
实施例2设计引物的pcr阳性扩增验证
[0056]
1、荚膜组织胞浆菌的总dna提取:利用实验室已有的10株荚膜组织胞浆菌,见表2:
[0057]
表2 10株荚膜组织胞浆菌来源
[0058][0059]
提取各株的总dna,提取方法为:
[0060]
(1)利用纯培养的菌株取1g菌体于含有研磨珠的研磨管内;
[0061]
(2)加入600μl裂解液(100mmol/l的tris-hcl、100mmol/l的edta、400mmol/l的nacl和2%sds),置于美国mp公司的fastprep-24高效破碎仪上剧烈研磨30s,将混悬液放入65℃水浴加热10min;
[0062]
(3)加入140μl饱和酚溶液(ph 4.5
±
0.2)混匀,10000r/min,离心10min;
[0063]
(4)取上清液加入400μl的异丙醇,10000r/min,离心2min;
[0064]
(5)弃上清后控干,加入300μl加热至65℃的双蒸水,吹吸混匀,加入150μl 3m醋酸钠溶液、300μl无水乙醇和5μl核糖核酸酶,混匀;
[0065]
(6)将混悬液转移至收集管内,10000r/min离心1min,弃废液,加入600μl清洗液对收集管内的dna离心清洗2次,空离心一次;
[0066]
(7)用5μl预热te缓冲液滴入收集管,静置后转移至新的1.5ml离心管内,10000r/min离心1min收集dna溶液。
[0067]
上述操作过程中涉及的试剂均来源于生工生物工程(上海)股份有限公司。
[0068]
2、pcr扩增验证:以提取的10株荚膜组织胞浆菌总dna作为模板对表1中10对引物
对一一开展pcr实验,进行第一轮验证筛查,pcr方法采用high-fidelity dna polymerases,20μl反应体系:
[0069][0070]
上述反应体系中涉及的试剂均可从new england biolabs公司获得。反应缓冲液采用reaction buffer pack(货号b9027s,浓度5
×
)。
[0071]
pcr仪:9700型
[0072]
pcr反应程序为:
[0073]
(a)95℃预变性5min;
[0074]
(b)(95℃变性30s;55℃退火30s;72℃延伸45s)
×
35循环
[0075]
(c)72℃总延伸10min。
[0076]
经pcr扩增后,对10个待测荚膜组织胞浆菌总dna产生300bp大小的单一显著条带的引物对有:cp069117.1_s3857-f&r、cp069117.1_s6964-f&r、cp069117.1_s7420-f&r、cp069117.1_s8505-f&r、cp069118.1_s4904-f&r、cp069118.1_s11573-f&r、cp069118.1_s11966-f&r和cp069120.1_s562-f&r。
[0077]
这8对引物对可以对荚膜组织胞浆菌进行特异序列的单一扩增,引物序列信息详见表1。
[0078]
实施例3从阳性扩增的引物中扩增筛选荚膜组织胞浆菌的种特异性引物
[0079]
为确保引物具备高度属特异性,只适用于荚膜组织胞浆菌,发明人设计了排除实验用于确认已对荚膜组织胞浆菌产生阳性扩增的引物不可扩增对其他种属的真菌及人源性基因片段产生阳性扩增。实验方法是以其他真菌/人的基因组dna为模板对上述8对引物对进行pcr验证,排除实验中产生阳性的扩增引物(对其他真菌/人的基因组dna产生pcr阳性被认定为产生非特异性扩增)。
[0080]
1、排除菌种的设计及dna提取
[0081]
将荚膜组织胞浆菌亲缘关系临近的种属以及临床易误诊、易混淆的相关病原真菌列为排除的真菌菌种。其中荚膜组织胞浆菌设计排除菌种为:烟曲霉、土曲霉、黄曲霉、白念珠菌、光滑念珠菌、近平滑念珠菌、热带念珠菌、球孢子菌、茄病镰刀菌、小孢根霉、尖端赛多孢、总状毛霉、不规则毛霉、淡紫拟青霉及马尔尼菲篮状菌这15种病原真菌,本团队从中国医学科学院病原微生物菌(毒)种保藏中心医学分中心保藏菌种中选取了上述排除菌种28株新鲜菌株,提取各自的总dna作为模板,提取方法同实施例2中的总dna提取方法。
[0082]
2、pcr扩增验证
[0083]
利用实施例2中8对引物分别对上述荚膜组织胞浆菌排除菌种的总dna模板进行扩增验证。pcr结果阴性认定为该引物具有荚膜组织胞浆菌种特异性,结果阳性认定为产生非特异性扩增;此轮筛选排除实验的pcr方法同实施例2中pcr扩增验证步骤所述方法。
[0084]
经验证后,在8对设计为荚膜组织胞浆菌检测引物对中有2对产生非特异性扩增产物的引物对(cp069117.1_s8505-f&r和cp069120.1_s562-f&r),最终确定荚膜组织胞浆菌种特异性引物对6对(cp069117.1_s3857-f&r、cp069117.1_s6964-f&r、cp069117.1_s7420-f&r、cp069118.1_s4904-f&r、cp069118.1_s11573-f&r和cp069118.1_s11966-f&r)。所有引物序列信息详见表1。
[0085]
3、人基因组阴性扩增验证
[0086]
考虑到设计的引物最终面向临床检验及鉴定,因此再次将上一步确认的6对荚膜组织胞浆菌的种特异性引物进行人基因组阴性扩增验证,以确认筛选引物对人源基因的pcr扩增应为阴性(人源基因来自临床健康人群体检血液),排除人源基因在临检过程中的干扰。其pcr扩增方法同实施例2中pcr扩增验证步骤所述方法。
[0087]
经人基因组pcr验证后,6对引物组对人源基因扩增均为阴性,适用于临床分子快速检测,引物序列信息详见表1。
[0088]
实施例4:六组引物对cp069117.1_s3857-f&r、cp069117.1_s6964-f&r、cp069117.1_s7420-f&r、cp069118.1_s4904-f&r、cp069118.1_s11573-f&r和cp069118.1_s11966-f&r验证荚膜组织胞浆菌的方法
[0089]
按照实施例2“设计引物的pcr阳性扩增验证”方法,对表2中1-10号不同进化支的荚膜组织胞浆菌的dna进行扩增验证。pcr产物采用2%琼脂糖凝胶电泳检测。电泳图结果详见图1。
[0090]
泳道1-10:引物对cp069117.1_s3857-f&r对表2中1-10号荚膜组织胞浆菌pcr扩增阳性条带,大小在300bp;
[0091]
泳道11-20:引物对cp069117.1_s6964-f&r对表2中1-10号荚膜组织胞浆菌pcr扩增阳性条带,大小在300bp;
[0092]
泳道21-30:引物对cp069117.1_s7420-f&r对表2中1-10号荚膜组织胞浆菌pcr扩增阳性条带,大小在300bp;
[0093]
泳道31-40:引物对cp069118.1_s4904-f&r对表2中1-10号荚膜组织胞浆菌pcr扩增阳性条带,大小在300bp;
[0094]
泳道41-50:引物对cp069118.1_s11573-f&r对表2中1-10号荚膜组织胞浆菌pcr扩增阳性条带,大小在300bp;
[0095]
泳道51-60:引物对cp069118.1_s11966-f&r对表2中1-10号荚膜组织胞浆菌pcr扩增阳性条带,大小在300bp。
[0096]
泳道1-10、11-20、21-30、31-40、41-50和51-60显示六对引物对对10株不同来源、不同进化支的荚膜组织胞浆菌特异性扩增结果均为阳性,可证明最终设计筛选的引物对(cp069117.1_s3857-f&r、cp069117.1_s6964-f&r、cp069117.1_s7420-f&r、cp069118.1_s4904-f&r、cp069118.1_s11573-f&r和cp069118.1_s11966-f&r)可有效地特异性扩增荚膜组织胞浆菌真菌。
[0097]
本发明是针对国内高致病性病原真菌荚膜组织胞浆菌开展的分子快速检测的特
异性引物筛选探索,可开发作为荚膜组织胞浆菌病快速检测的试剂盒,用于临床快速区分、诊断荚膜组织胞浆菌病的分子手段,为国内在上述病症中的临床分子诊断补充可靠的技术手段,同时也为该真菌病的疾病预防控制及进出口检疫提供精准快速的监测。
[0098]
如上所述,尽管参照特定的优选实施例已经表示和表述了本发明,但其不得解释为对本发明自身的限制。在不脱离所附权利要求定义的本发明的精神和范围前提下,可对其在形式上和细节上作出各种变化。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1