针对非洲猪瘟CD2v的抗体及其应用的制作方法
针对非洲猪瘟cd2v的抗体及其应用
技术领域
1.本发明属于生物医药领域,具体涉及针对非洲猪瘟cd2v的抗体及其应用。
背景技术:
2.非洲猪瘟(英文名称:infection with african swine fever,简称:asf)是由非洲猪瘟病毒(英文名称:african swine fever virus,简称:asfv)感染家猪和各种野猪(如非洲野猪、欧洲野猪等)而引起的一种急性、出血性、烈性传染病。世界动物卫生组织(oie)将其列为法定报告动物疫病,该病也是我国重点防范的一类动物疫情。其特征是发病过程短,急性感染死亡率高达100%,临床表现为发热,心跳加快,呼吸困难,部分咳嗽,眼、鼻有浆液性或粘液性脓性分泌物,皮肤发绀,淋巴结、肾、胃肠粘膜明显出血,非洲猪瘟临床症状与猪瘟症状相似,只能依靠实验室监测确诊。
3.asfv是一种核质双链dna大病毒,呈二十面体结构,外有囊膜包被,不同毒株基因组大小存在些许差异,长度介于170~190kb之间,有150多个主要开放阅读框,编码约200种蛋白质,其中存在许多与病毒复制、免疫逃逸、病毒传播等相关的蛋白,目前主要通过elisa和荧光pcr方法对病毒进行检测。
4.asfv基因编码的结构蛋白约有50种,包括囊膜蛋白cd2v、p30、p54,衣壳蛋白p72、p49,核壳蛋白多聚蛋白前体pp20和pp62,dna结合蛋白p10、pa104r。囊膜蛋白cd2v由ep402r基因编码,也称为pep402r,蛋白大小约45.3kd,因编码蛋白胞外区免疫球蛋白样结构域的氨基酸序列与宿主细胞的cd2非常相似,所以命名为cd2v。该蛋白是一种糖蛋白,能帮助asfv感染细胞与猪血液中的红细胞结合,促进病毒在宿主体内的扩散传播。cd2v在促进病毒复制与传播、病毒免疫逃逸等方面发挥着重要作用,是asfv疫苗研究的热点靶标。通过对cd2v进行生物信息学分析,发现序列中存在特异性抗原表位,具有作为抗原的潜力。
技术实现要素:
5.本公开提供了一种抗体或其抗原结合片段,其能够特异性结合cd2v蛋白,对cd2v具有高亲和力。另外,本公开还提供了制备和/或使用所述抗体或其抗原结合片段的方法。
6.产品
7.第一方面,本发明提供了一种抗体或其抗原结合片段,所述抗体或其抗原结合片段包含轻链cdr 1-3和重链cdr1-3,
8.其中,所述重链cdr1的氨基酸序列如seq id no.2所示,所述重链cdr2的氨基酸序列如seq id no.3所示,所述重链cdr3的氨基酸序列如seq idno.4所示,
9.所述轻链cdr1的氨基酸序列如seq id no.5所示,所述轻链cdr2的氨基酸序列如seq id no.6所示,以及所述轻链cdr3的氨基酸序列如seq idno.7所示。
10.在一些实施方案中,所述抗体包括单克隆抗体、嵌合抗体、人源化抗体、全人源抗体和双特异性抗体。
11.在一些实施方案中,所述抗原结合片段包括fab片段、fab’片段、f(ab)2片段、fv片
段和scfv。
12.在一些实施方案中,所述cd2v包括野生型cd2v或其突变体。
13.在一些实施方案中,所述抗体的重链可变区如sed id no.8所示。
14.在一些实施方案中,所述抗体的轻链可变区如sed id no.9所示。
15.在一些实施方案中,所述抗体还包括连接序列,所述连接可以是(ggggs)n、(gggs)n、(ssssg)n、(gsgsa)n和(ggsgg)n。具体地,“ggggs”是指氨基酸序列gly-gly-gly-gly-ser,“gggs”是指氨基酸序列gly-gly-gly-ser,“ssssg”是指氨基酸序列ser-ser-ser-ser-gly,“gsgsa”是指氨基酸序列gly-ser-gly-ser-ala,“ggsgg”是指氨基酸序列gly-gly-ser-gly-gly。所述n是大于等于1的整数。
16.优选地,所述抗体还包括恒定区。
17.优选地,所述恒定区包括任何来源的恒定区,更优选地,所述恒定区是人抗体的恒定区。
18.优选地,所述人抗体的恒定区包括人igg1、igg2、igg3或igg4的重链恒定区和κ或λ型轻链恒定区等。
19.如本发明所述“cd2v”、“cd2v蛋白”包括非洲猪瘟cd2v蛋白及其突变体,所述突变体相对于cd2v蛋白野生型有一个或多个突变。囊膜蛋白cd2v由ep402r基因编码,基因全长为1083bp,编码的蛋白大小为45.3kd,因此cd2v也被称为pep402r。
20.如本文中使用的,术语“特异性结合”是指,两分子间的非随机的结合反应,如本发明所提供的抗体和其所针对的cd2v蛋白之间的反应。
21.另一方面,本公开提供了一种分离的核酸分子,所述核酸分子编码前述抗体或其抗原结合片段。
22.优选地,所述核酸分子包括dna、rna或者dna和rna的杂交体,所述核酸分子可以是双链或单链的。
23.另一方面,本公开提供了一种载体,其包含前述编码抗体或其抗原结合片段的核酸分子。
24.如本文中所用,术语“载体”通常是指可在其中插入并表达编码蛋白质的多核苷酸的核酸媒介物。载体中携带的遗传物质成分可通过用载体转化、转导或转染宿主细胞而在宿主细胞中表达。
25.优选地,所述载体是表达载体。
26.优选地,所述载体包括细菌质粒载体、噬菌体载体、酵母质粒载体、腺病毒载体、逆转录病毒载体或慢病毒载体。
27.优选地,所述载体可以是商品化的成品载体,也可以是根据需要自行构建的载体,载体的构建方法是本领域所公知的。
28.在一些实施方案中,所述载体可包含多种控制表达的元件,包括启动子序列、转录起始序列、增强子序列、选择元件和报告基因。另外,载体还可包含复制起点,但不仅仅包括这些物质。
29.另一方面,本公开提供了一种细胞,所述细胞包含前述抗体或其抗原结合片段、核酸分子或载体中的一种或多种。
30.优选地,所述细胞可以是原核细胞,如细菌细胞;或是低等真核细胞,如酵母细胞;
或是高等真核细胞,如哺乳动物细胞。
31.如本发明所使用的,所述细胞可用于使核酸增殖和/或表达。所述细胞包括但不限于原核细胞,包括但不限于需氧、微量需氧、嗜二氧化碳、兼性、厌氧、革兰氏阴性和革兰氏阳性细菌细胞的菌株,例如以下菌株及其衍生型:大肠杆菌(escherichia coli)、枯草芽孢杆菌(bacillus subtilis)、地衣芽孢杆菌(bacillus licheniformis)、脆弱拟杆菌(bacteroides fragilis)、产气芽孢梭菌(clostridia perfringens)、困难梭状芽孢杆菌(clostridia difficile)、新月柄杆菌(caulobacter crescentus)、乳酸乳球菌(lactococcus lactis)、扭脱甲基杆菌(methylobacterium extorquens)、曼宁双球菌(neisseria meningirulls)、脑膜炎双球菌(neisseria meningitidis)、荧光假单胞菌(pseudomonas fluorescens)和鼠伤寒沙门氏菌(salmonella typhimurium);和真核细胞,包括但不限于酵母菌株,例如以下菌株及其衍生型:巴斯德毕赤酵母(pichia pastoris)、甲醇毕赤酵母(pichia methanolica)、安格斯毕赤酵母(pichia angusta)、粟酒裂殖酵母(schizosaccharomyces pombe)、啤酒酵母(saccharomyces cerevisiae)和解脂耶罗威亚酵母(yarrowia lipolytica);昆虫细胞和衍生自昆虫的细胞系,所述昆虫例如草地贪夜蛾(spodoptera frugiperda)、粉纹夜蛾(trichoplusia ni)、黑腹果蝇(drosophilamelanogaster)和烟草天蛾(manduca sexta)等;和哺乳动物细胞和衍生自哺乳动物细胞的细胞系,所述动物例如小鼠、大鼠、仓鼠、猪、牛、马、灵长类动物和人等。
32.示例性地,可应用于本发明的细胞包括但不限于:cho细胞、293细胞、cho-k1细胞、hek293细胞、caco2细胞、u2-os细胞、nih 3t3细胞、nso细胞、sp2细胞、cho-s细胞、dg44细胞、k-562细胞、u-937细胞、mrc5细胞、imr90细胞、jurkat细胞、hepg2细胞、hela细胞、ht-1080细胞、hct-116细胞、hu-h7细胞、huvec细胞、molt 4细胞等细胞系。
33.另一方面,本发明提供了一种检测cd2v蛋白的试剂盒,所述试剂盒中含有前述抗体或抗原结合片段、前述核酸分子、前述载体、前述宿主细胞中任意一种或多种。
34.优选地,所述试剂盒可包含其它材料,诸如细胞裂解液、稳定液、缓冲液、包装材料或使用说明书。
35.应用
36.另一方面,本发明提供了前述抗体或抗原结合片段、前述核酸分子、前述载体、前述宿主细胞、前述试剂盒中任意一种在检测cd2v蛋白中的应用。或者,在制备检测cd2v产品中的应用。
37.生产方法
38.另一方面,本公开提供了生产前述抗体或其抗原结合片段的方法,所述方法包括使其编码核酸表达。
39.更具体地,在能使核酸表达的环境中培养细胞,所述细胞中含有前述抗体或其抗原结合片段的编码核酸。
40.所述使编码核酸表达是通过本领域常规技术手段就可以实现的。
41.优选地,所述编码核酸是通过取决于细胞类型的方法转移到细胞中的。例如,对于原核细胞,通常利用氯化钙转染,而对于其他细胞宿主,可使用磷酸钙处理、电穿孔、脂质转染、基因枪法或基于病毒的转染。用于转化哺乳动物细胞的其他方法包括使用聚凝胺、原生质体融合、脂质体、电穿孔以及显微注射。
42.在一些实施方案中,所述方法任选地还包括收集、纯化所述抗体或其抗原结合片段的步骤。
43.优选地,所述收集、纯化可以是通过本领域常用的方法进行。例如,离心分离培养基和宿主细胞,高压匀浆破碎细胞、离心过滤去除细胞碎片,亲和层析纯化抗体。对于分离纯化所得的产物,可以使用本领域常用的方法进行纯度鉴定。例如,考马斯亮蓝法、凯氏定氮法、双缩脲法、lowry法、紫外吸收法、亲和层析、抗原抗体法、电泳分析(例如十二烷基磺酸钠聚丙烯酰胺凝胶电泳)、沉降分析、扩散分析、恒溶度法、蛋白质谱等。
44.检测方法
45.另一方面,本发明还提供了检测cd2v的方法,所述方法包括将待检测物质与以下任意一种接触:本发明所述抗体或其抗原结合片段、核酸分子、载体、细胞、试剂盒。
46.在一种实施方案中,所述方法是体外进行的。
47.在一种实施方案中,所述方法是非诊断目的的。
48.优选地,所述待测物包括可以为来自动物的样品,例如,牛、羊、猪、马、驴。
49.优选地,所述样品可以为鼻腔拭子、脓性鼻液、生殖道拭子、精液、呼吸道黏膜、部分扁桃体、肺、支气管淋巴结、动物胎儿、肝、肺、肾和胎盘子叶。
50.优选地,所述待测物包括还可以来源于养殖场的环境样品,例如,空气、水体、土壤、养殖场的设备等。
51.优选地,所述检测的方法可以与以下任意一种联合:酶联免疫吸附(elisa)、化学发光免疫检测、放射免疫检测、荧光免疫检测、免疫色谱法等检测方法。
52.本说明书中提及的所有出版物、专利和专利申请均通过引用并入本文,如同每个单独的出版物、专利或专利申请都被具体和单独地指出通过引用结合于此。其程度就如同每个单独出版物、专利或专利申请具体地和单独地表示为通过引用并入。
附图说明
53.图1是检测单克隆抗体5d8的电泳图。
54.图2是检测单克隆抗体5d8的hplc图。
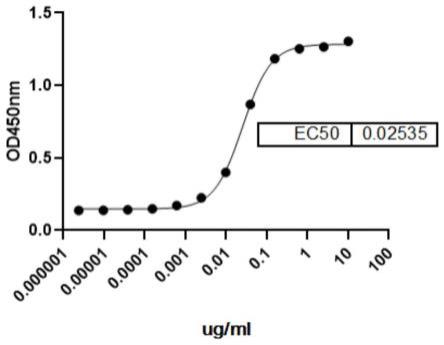
55.图3是elisa检测单克隆抗体5d8的结合活性图。
具体实施方式
56.下面结合实施例对本发明做进一步的说明,以下所述,仅是对本发明的较佳实施例而已,并非对本发明做其他形式的限制,任何熟悉本专业的技术人员可能利用上述揭示的技术内容加以变更为同等变化的等效实施例。凡是未脱离本发明方案内容,依据本发明的技术实质对以下实施例所做的任何简单修改或等同变化,均落在本发明的保护范围内。
57.实施例1、单克隆抗体的筛选
58.1、免疫原重组表达
59.合成非洲猪瘟cd2v蛋白序列,构建至pem5.1载体;抽提转染用质粒;转染至hek293细胞,培养细胞7天;收获上清,ni柱纯化,经过浓缩置换缓冲液,得到重组非洲猪瘟cd2v蛋白。
60.重组非洲猪瘟cd2v蛋白序列来源于uniprot,序列信息:niiiwstlnqtv flnnifti
ndtygglfwntyydnnrsnftycgiagnycsccghnislynttnncsliifpnnteifnrtyelvyldkkinytvkllksvdsptitynctnslitcknnngtnvniyliinntivndtngdilnyywngnnnftatcminntisslneteninctnpilkyqnylstgshhhhhh(seq id no.1所示)。
61.2、免疫
62.免疫小鼠,sp2/0融合,筛选亚克隆。
63.具体步骤:第一次用福氏完全佐剂,每只100μg,腹腔注射,总剂量0.5ml/只,间隔3周进行第二次免疫;第二次起用福氏不完全佐剂,剂量为50μg/0.5ml/只,间隔2周进行第三次免疫;第三次注射后10天准备细胞融合;取饲养细胞,可按105/孔使用,于融合前一天铺板105个/100μl/孔;取小鼠免疫脾细胞与准备好的骨髓瘤细胞用融合剂peg进行融合,铺入已经加入饲养细胞的96细胞培养板,100μl/孔。
64.3、杂交瘤细胞的筛选和克隆
65.通过elisa检测方法进行阳性孔筛选,铺重组表达cd2v蛋白过夜;洗板,加脱脂奶粉封闭,37℃,1h;洗板,加入100μl 96孔培养液上清,37℃,孵育1h;洗板,加入hrp标记羊抗鼠二抗,37℃,孵育30min;洗板,加入显色液,显色10min,加入终止液,读取od 450的数值;筛选高表达量细胞株进行亚克隆培养。
66.4、测序
67.收集细胞,采用trizol抽提总rna,用oligo(dt)20为引物,逆转录生成cdna。然后利用特异性引物pcr分别扩增其重、轻链可变区基因。pcr产物经电泳纯化后,通过ta克隆插入载体,进行转化,挑选阳性克隆送测序。
68.筛选到5d8克隆,测序结果如下:
[0069][0070]
实施例2、单克隆抗体5d8的理化性质检测
[0071]
单克隆抗体的表达和纯化,对筛选出的序列进行化学合成,并克隆至真核表达载体中。对质粒扩增提取。将编码抗体的质粒瞬时转染入哺乳动物细胞hek293。收集上清,利用亲和层析方法,纯化获得单克隆抗体。
[0072]
纯化后的抗体表达量是142mg/l。
[0073]
1、凝胶电泳检测单克隆抗体的纯度
[0074]
1)仪器设备
[0075][0076][0077]
2)主要试剂
[0078]
名称生产厂家规格货号1m tris-hcl缓冲液北京索莱宝科技有限公司60ml/瓶202009111.5m tris-hcl缓冲液北京索莱宝科技有限公司100ml/瓶2020091110%sds北京索莱宝科技有限公司10ml/瓶20200911faststaingene universal1000ml/瓶21da30%制胶液(29:1)北京索莱宝科技有限公司500ml/瓶20210414彩虹180广谱蛋白marker北京索莱宝科技有限公司250μl(50t)1202f021
[0079]
3)样品制备
[0080]
取20μl的样品与5μl的5
×
还原buffer混合均匀,在95℃中加热5min,冷却;取20μl的样品与5μl的5
×
非还原buffer混合均匀。
[0081]
4)电泳
[0082]
配置胶,加适量的电泳缓冲液,加样,进行电泳。
[0083]
5)染色与脱色
[0084]
电泳结束后,取凝胶放入适量考马斯亮蓝染色液中,室温染色1h或更长时间;倒出染色液,加入适量考马斯亮蓝染色脱色液,室温脱色4-24h。完成脱色后,用ddh2o浸泡,参照marker蛋白,与未染色凝胶对比,切下所需蛋白成分的凝胶,收集起来。然后把所要提纯的蛋白从凝胶中分离出来。
[0085]
6)结果
[0086]
结果如图1所示,从左至右条带分别是marker、还原条带;单克隆抗体的检测纯度均大于95%。
[0087]
2、hplc检测单克隆抗体的纯度
[0088]
1)仪器设备
[0089][0090][0091]
2)主要试剂
[0092]
名称生产厂家规格货号磷酸氢二钾三水国药集团化学试剂有限公司500g/瓶10017592
磷酸二氢钾国药集团化学试剂有限公司500g/瓶10017692氯化钾国药集团化学试剂有限公司500g/瓶10016392
[0093]
3)流动相配制
[0094]
将磷酸氢二钾三水、磷酸二氢钾和氯化钾加入到约900ml纯化水中,搅拌溶解,定容至1l,用ph计测量,确定其ph在6.2
±
0.1之间。0.22μm滤膜过滤,室温保存。
[0095]
4)样品制备
[0096]
系统适用性样品:mil62标准品用流动相稀释至2mg/ml
[0097]
供试品:待测样品用流动相稀释至2mg/ml。
[0098]
5)色谱条件
[0099][0100]
6)结果
[0101]
结果如图2所示,单克隆抗体的检测纯度均大于95%。
[0102]
实施例3、单克隆抗体的结合活性检测
[0103]
1、实验步骤
[0104]
1)包被:用包被液将抗原cd2v蛋白稀释成2μg/ml,混匀,加入96孔包被板,100μl/孔,封膜封闭,4℃过夜。
[0105]
2)洗板机洗涤3次,最后一次不能有液体残留在板子上,用吸水纸拍干板子表面的液体。
[0106]
3)封闭:加入5%奶粉(0.5g奶粉溶于10ml dpbs),300μl/孔,37℃孵育1h,按照步骤2)洗板3次。
[0107]
4)将抗体进行梯度稀释,100μl/孔,37℃反应1h,按照步骤2)洗板3次。
[0108]
5)加二抗:用dpbs按照1:2000稀释,加入96孔板,100μl/孔,37℃反应1h,按照步骤2)洗板3次。
[0109]
6)显色:加入tmb,100μl/孔,室温避光显色10min。
[0110]
7)终止:加入2n h2so4,100μl/孔。
[0111]
8)酶标仪测od 450,10min内检测。
[0112]
2、结果
[0113]
结果如图3所示,单克隆抗体5d8可以与抗原cd2v蛋白特异性结合,并且呈现浓度依赖性,ec50为0.02535μg/ml。
[0114]
上述实施例的说明只是用于理解本发明的方法及其核心思想。应当指出,对于本领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以对本发明进行若干改进和修饰,这些改进和修饰也将落入本发明权利要求的保护范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1