用于制备异氰酸酯基团封端的聚噁唑烷酮组合物的方法与流程
用于制备异氰酸酯基团封端的聚噁唑烷酮组合物的方法
1.本发明涉及用于制备异氰酸酯基团封端的聚噁唑烷酮组合物的方法,该方法包括使具有两个或更多个异氰酸酯基团的多异氰酸酯化合物与具有两个或更多个环氧基团的多环氧化物化合物在磷和
/
或锑催化剂的存在下共聚,其中多异氰酸酯化合物的异氰酸酯基团对多环氧化物化合物的环氧基团的摩尔比为大于
2:1
且小于
25:1
,并且其中该方法在不存在沸点
(
在1巴
(
绝对
))
高于
200℃
的溶剂的情况下进行
。
本发明还涉及所得的异氰酸酯基团封端的聚噁唑烷酮组合物和通过除去溶剂和
/
或未反应的多异氰酸酯化合物而制备异氰酸酯基团封端的聚噁唑烷酮的方法
。
2.噁唑烷酮是制药应用中广泛使用的结构基元并且环氧化物和异氰酸酯的环加成看起来是对于其方便的一锅法合成路线
。
昂贵的催化剂
、
反应性极性溶剂
、
长反应时间和低化学选择性在关于噁唑烷酮合成的早期报告中是常见的
(m.e.dyen
和
d.swern,chem.rev.,67,197,1967)。
由于这些缺点,需要用于生产噁唑烷酮的替代性方法,尤其是对于噁唑烷酮作为聚合物应用中的结构基元的应用
。
3.科学出版物
j.polym.sci.8(1970)2759-2773
公开了由各种双环氧化物和各种二异氰酸酯在碱金属卤化物催化剂的存在下制备的聚噁唑烷酮
。
在回流条件下,将等摩尔的双环氧化物和二异氰酸酯的溶液在1小时内滴加到含有溶解在
dmf
中的
licl
催化剂的反应器,并随后在回流条件下进行
12
至
23
小时的后反应,以完成反应
。
4.us 4,129,695 a
教导了由多异氰酸酯和多环氧化物制备的包含噁唑烷酮和碳二亚胺的聚合物,其中这些化合物可以是二异氰酸酯或二环氧化物,其中异氰酸酯基团的数目对环氧基团的数目的比为
1.1:1
和
20:1
,优选
1.2:1
和
10:1
,其中使用叔脂族
、
脂环族和芳族胺,例如三亚乙基二胺
(dabco)
作为用于噁唑烷酮形成的催化剂
。
5.在
flore
等人
(thermochmica acta(elsevier)
第
543
卷
(2012)
第
188
至
196
页
)
中公开了通过使
4-甲苯-2
,
4-二异氰酸酯与双酚a的二缩水甘油醚在三氟甲磺酸镱的存在下反应来制备异氰酸酯基团封端的聚噁唑烷酮,其中
4-甲苯-2
,
4-二异氰酸酯对双酚a的二缩水甘油醚的摩尔比为
2:1。
6.在
pelzer
等人
(european polymer journal 107(2018))
中,通过
4,4-亚甲基二苯基二异氰酸酯
(mdi)
与邻甲苯基缩水甘油醚
(ogce)
或双酚a二缩水甘油醚
(badge)
在各种四正丁基卤化铵的存在下的反应研究了噁唑烷酮的形成,其中使用1比3至至多3比1的
badge
与
mdi
摩尔比
。
然而,在
badge
对
mdi
的比为3比1下进行以形成环氧基封端的噁唑烷酮时,检测到显著量的副产物,即异氰脲酸酯
。
如果采用1比3的
badge
对
mdi
的摩尔比,则在所用的四正丁基卤化铵催化剂的存在下,无法形成异氰酸酯封端的噁唑烷酮
。
7.wo 2020/249472 a1
公开了用于制备异氰酸酯基团封端的聚噁唑烷酮的方法,该方法包括使具有两个或更多个异氰酸酯基团的多异氰酸酯化合物与具有两个或更多个环氧基团的多环氧化物化合物在催化剂
(c)
的存在下和在溶剂中共聚,其中在作为溶剂的邻二氯苯和环丁砜的混合物中,将
licl
或
libr
作为碱金属卤化物作为催化剂使用
。
8.在
us2017/081462 a1
中涉及用于选择性制备具有高活性的噁唑烷酮化合物的方法,该方法包括在作为催化剂的鎓盐存在下使异氰酸酯化合物与环氧化物反应的步骤,并
且涉及可通过所述方法得到的噁唑烷酮化合物
。
9.wo 86/06734a1
公开了通过使多环氧化物和多异氰酸酯反应以形成聚噁唑烷酮的方法,其中所述反应在催化量的有机碘化锑催化剂
(
如三苯基碘化锑
)
的存在下进行
。
该发明的目标是确定用于制备异氰酸酯基团封端的聚噁唑烷酮组合物和异氰酸酯基团封端的聚噁唑烷酮
(
预聚物
)
的简单方法,该组合物和预聚物具有限定的异氰酸酯当量重量,优选具有低多分散性组合用于进一步聚合应用
。
在该情况下,应显著地减少或有利地避免副反应,例如通过异氰脲酸酯或聚氨酯的形成
。
因此,与现有技术体系相比提高的噁唑烷酮对异氰酸酯
(
三聚体
)
的比是有益的
。
此外,该噁唑烷酮产物应具有与现有技术中所述的体系类似的低着色或优选甚至着色更少
。
这样的异氰酸酯基团封端的聚噁唑烷酮预聚物体系应对于进一步的聚合应用也是可熔化的
。
10.此外,高沸点溶剂的高量造成能量密集且耗时的脱除工艺,例如通过蒸馏,并且可不利地影响聚噁唑烷酮的后续挤出和注塑成型工艺,例如不想要的发泡
、
不合适的粘度和爆炸性气氛
。
因此,对于合成聚噁唑烷酮通常必需的溶剂应定量除去,例如通过蒸馏定量除去
。
11.令人惊讶地,已经发现可通过制备异氰酸酯基团封端的聚噁唑烷酮组合物的方法解决该问题,该方法包括使具有两个或更多个异氰酸酯基团的多异氰酸酯化合物
(a)
与具有两个或更多个环氧基团的多环氧化物化合物
(b)
在催化剂
(c)
的存在下和任选在溶剂
(d)
中共聚;
12.其中多异氰酸酯化合物
(a)
的异氰酸酯基团对多环氧化物化合物
(b)
的环氧基团的摩尔比大于
2:1
且小于
25:1
;
13.并且其中催化剂
(c)
由式(i)表示
14.[m(r1)(r2)(r3)(r4)]
+nyn-ꢀꢀꢀꢀ(i)[0015]
其中m是磷或锑,优选磷,
[0016]
其中
(r1)、(r2)、(r3)
和
(r4)
各自彼此独立地为含有1至
22
个碳原子的直链或支链烷基,其任选被一个或多个杂原子
、
含杂原子的取代基或其组合取代;含有3至
22
个碳原子的脂环族基团,其任选被一个或多个杂原子
、
含杂原子的取代基或其组合取代;
c1
至
c3
烷基桥接的含有3至
22
个碳原子的脂环族基团,其任选被一个或多个杂原子
、
含杂原子的取代基或其组合取代;或含有6至
18
个碳原子的芳基,其任选地被一个或多个含有1至
10
个碳原子的烷基
、
一个或多个含杂原子的取代基
、
一个或多个杂原子或其组合取代,
[0017]
其中y是卤离子
、
碳酸根
、
硝酸根
、
硫酸根或磷酸根阴离子,更优选卤离子或碳酸根,并且
[0018]
其中n是
1、2
或3的整数,
[0019]
并且其中该方法在不存在具有在1巴
(
绝对
)
高于
200℃
,优选高于
190℃
且更优选高于
180℃
的沸点的溶剂
(e)
的情况下进行
。
[0020]
如本文所用,术语“聚噁唑烷酮”意在表示在分子中含有至少两个噁唑烷酮基团的化合物
。
术语“异氰酸酯基团封端的”聚噁唑烷酮涉及聚噁唑烷酮化合物,其中多异氰酸酯化合物
(a)
的异氰酸酯基团对多环氧化物化合物
(b)
的环氧基团的摩尔比大于
2:1
,使得在根据本发明的聚噁唑烷酮化合物中不存在末端环氧基团
。
[0021]
如本文所用,术语“聚噁唑烷酮组合物”意在表示包含异氰酸酯基团封端的聚噁唑
烷酮和溶剂
(d)
和
/
或未反应的多异氰酸酯化合物
(a)(
如果存在溶剂
(d))
的组合物
。
[0022]
除非逻辑教导清楚地表明不能组合本发明的所有实施方案,否则可以组合这些实施方案
。
[0023]
在根据本发明的方法的一个实施方案中,共聚过程在
≥130℃
至
≤280℃
的反应温度进行,优选在
≥140℃
至
≤240℃
的温度进行,更优选在
≥155℃
至
≤210℃
的温度进行
。
如果设定温度低于
130℃
,则反应通常非常缓慢
。
在高于
280℃
的温度,不合意的副产物的量显著增加
。
[0024]
在根据本发明的方法的一个实施方案中,共聚过程以5分钟至
20
小时,优选以
10
分钟至
10
小时,并且更优选以
15
分钟至6小时的反应时间进行
。
[0025]
如本文所用,术语“多异氰酸酯化合物”意在表示具有两个或更多个异氰酸酯基团的化合物
。
[0026]
在根据本发明的方法的一个实施方案中,多异氰酸酯化合物
(a)
是脂族多异氰酸酯化合物
(a-1)
和
/
或芳族多异氰酸酯化合物
(a-2)
,优选脂族多异氰酸酯化合物
(a-1)。
[0027]
在根据本发明的方法的一个实施方案中,多异氰酸酯化合物
(a)
是可以各种方式得到的至少一种多异氰酸酯,所述方式例如通过在液相或气相中的光气化或通过无光气途径,例如通过热氨基甲酸酯裂解
。
[0028]
在根据本发明的方法的一个实施方案中,多异氰酸酯化合物
(a)
是选自具有脂族和
/
或芳族键合的异氰酸酯基团的
140g/mol
至
600g/mol
的分子量的多异氰酸酯中的至少一种化合物,实例是
1,4-丁烷二异氰酸酯
、1,5-戊烷二异氰酸酯
(
五亚甲基二异氰酸酯,
pdi)、1,6-己烷二异氰酸酯
(
六亚甲基二异氰酸酯,
hdi)、2-甲基-1,5-戊烷二异氰酸酯
、1,5-二异氰酸根合-2,2-二甲基戊烷
、2,2,4-或
2,4,4-三甲基-1,6-己烷二异氰酸酯
、1,8-辛烷二异氰酸酯
、1,10-癸烷二异氰酸酯
、1,12-十二烷二异氰酸酯
、1,3-和
1,4-环己烷二异氰酸酯
、1,3-和
1,4-双
(
异氰酸根合甲基
)
环己烷
、1-异氰酸根合-3,3,5-三甲基-5-异氰酸根合甲基环己烷
(
异佛尔酮二异氰酸酯,
ipdi)、2,4'-和
4,4'-二环己基甲烷二异氰酸酯
(h12-mdi)、4,4'-二异氰酸根合-2,2-二环己基丙烷
、1-异氰酸根合-1-甲基-4(3)
异氰酸根合甲基环己烷
、
双
(
异氰酸根合甲基
)
降冰片烷
、
或
、
或具有脲二酮
、
异氰脲酸酯
、
脲基甲酸酯
、
缩二脲
、
亚氨基噁二嗪二酮和
/
或噁二嗪三酮结构的任何多异氰酸酯,其通过简单的脂族二异氰酸酯
(
例如上述类型的那些
)
的改性来制备,例如描述在
j.prakt.chem.336(1994)185-200、de-a 1670666、de-a 1954093、de-a 2414413、de-a 2452532、de-a 2641380、de-a 3700209、de-a 3900053
和
de-a 3928503
中,或描述在
ep-a 0336205、ep-a 0339396
和
ep-a0798299
中,或通过至少两种此类多异氰酸酯的混合物,以及
1,3-和
1,4-双
(
异氰酸根合甲基
)
苯
(
苯二亚甲基二异氰酸酯,
xdi)、1,3-和
1,4-双
(2-异氰酸根合丙-2-基
)
苯
(
四甲基苯二亚甲基二异氰酸酯,
tmxdi)、1,3-双
(
异氰酸根合甲基
)-4-甲基苯
、1,3-双
(
异氰酸根合甲基
)-4-乙基苯
、1,3-双
(
异氰酸根合甲基
)-5-甲基苯
、1,3-双
(
异氰酸根合甲基
)-2,4,6-三甲基苯
、1,3-双
(
异氰酸根合甲基
)-4,5-二甲基苯
、1,4-双
(
异氰酸根合甲基
)-2,5-二甲基苯
、1,4-双
(
异氰酸根合甲基
)-2,3,5,6-四甲基苯
、1,3-双
(
异氰酸根合甲基
)-5-叔丁基苯
、1,3-双
(
异氰酸根合甲基
)-4-氯苯
、1,3-双
(
异氰酸根合甲基
)-4,5-二氯苯
、1,3-双
(
异氰酸根合甲基
)-2,4,5,6-四氯苯
、1,4-双
(
异氰酸根合甲基
)-2,3,5,6-四氯苯
、1,4-双
(
异氰酸根合甲基
)-2,3,5,6-四溴苯
、1,4-双
(2-异氰酸根合乙基
)
苯和
1,4-双
(
异氰酸根合甲基
)
萘
、1,2-、1,3-和
1,4-二异氰酸根合苯
(
亚苯基二异氰酸酯
)、2,4-和
2,6-二异氰酸根合甲苯
(
甲苯二异氰酸酯,
tdi)、2,3,5,6-四甲基-1,4-二异氰酸根合苯
、
异构体二乙基亚苯基二异氰酸酯
、
二异丙基亚苯基二异氰酸酯
、
二异十二烷基亚苯基二异氰酸酯和联苯二异氰酸酯
、3,3'-二甲氧基联苯-4,4'-二异氰酸酯
、2,2'-、2,4'-和
4,4'-二苯甲烷二异氰酸酯
(mdi)、3,3'-二甲基二苯甲烷-4,4'-二异氰酸酯
、4,4'-二苯乙烷二异氰酸酯
、1,5-萘二异氰酸酯
(ndi)、
二苯醚二异氰酸酯
、
乙二醇二苯醚二异氰酸酯
、
二乙二醇二苯醚二异氰酸酯
、1,3-丙二醇二苯醚二异氰酸酯
、
二苯甲酮二异氰酸酯
、
苯三异氰酸酯
、2,4,6-甲苯三异氰酸酯
、
三甲基苯三异氰酸酯
、
二苯甲烷-2,4,4'-三异氰酸酯
、3-甲基二苯甲烷-4,6,4'-三异氰酸酯
、
异构体萘三异氰酸酯和甲基萘二异氰酸酯
、
三苯甲烷三异氰酸酯
、2,4-二异氰酸根合-1-[(5-异氰酸根合-2-甲基苯基
)
甲基
]
苯
、4-甲基-二苯甲烷-3,5,2',4',6'-五异氰酸酯,以及被称为“聚合物-mdi”的二苯甲烷二异氰酸酯的多核同系物,以及可由单体
2,4-和
/
或
2,6-tdi
通过与多元醇反应和
/
或低聚
(
优选三聚
)
获得的具有氨基甲酸酯和
/
或异氰脲酸酯结构的多异氰酸酯,其可通过任何已知方法获得,例如描述在
de-a 870400、de-a 953012、de-a 1090196、ep-a0546399、cn 105218780、cn 103881050、cn 101717571、us 3183112、ep-a 0416338、ep-a 0751163、ep-a 1378529、ep-a 1378530、ep-a 2174967、jp 63260915
或
jp 56059828
中,或至少两种此类多异氰酸酯的混合物,以及带有芳族和脂族的异氰酸酯基团的那些多异氰酸酯化合物,例如描述在
de-a 1670667、ep-a 0078991、ep-a 0696606
和
ep-a 0807623
中的
2,4-和
/
或
2,6-tdi
与
hdi
的混合三聚体或脲基甲酸酯
。
[0029]
更优选多异氰酸酯化合物
(a)
是选自具有脂族和
/
或芳族键合的异氰酸酯基团的
140g/mol
至
600g/mol
的分子量的多异氰酸酯中的至少一种化合物,实例是
1,4-丁烷二异氰酸酯
、1,5-戊烷二异氰酸酯
(
五亚甲基二异氰酸酯,
pdi)、1,6-己烷二异氰酸酯
(
六亚甲基二异氰酸酯,
hdi)、1,5-二异氰酸根合-2,2-二甲基戊烷
、2,2,4-或
2,4,4-三甲基-1,6-己烷二异氰酸酯
、1,8-辛烷二异氰酸酯
、1,3-和
1,4-环己烷二异氰酸酯
、1,3-和
1,4-双
(
异氰酸根合甲基
)
环己烷
、1-异氰酸根合-3,3,5-三甲基-5-异氰酸根合甲基环己烷
(
异佛尔酮二异氰酸酯,
ipdi)、2,4'-和
4,4'-二环己基甲烷二异氰酸酯
(h12-mdi)、4,4'-二异氰酸根合-2,2-二环己基丙烷
、
或具有脲二酮
、
异氰脲酸酯
、
脲基甲酸酯
、
缩二脲
、
亚氨基噁二嗪二酮和
/
或噁二嗪三酮结构的任何多异氰酸酯,其通过简单的脂族二异氰酸酯
(
例如上述类型的那些
)
的改性来制备,例如描述在
j.prakt.chem.336(1994)185-200、de-a 1670666、de-a 1954093、de-a2414413、de-a 2452532、de-a 2641380、de-a 3700209、de-a3900053
和
de-a 3928503
中,或描述在
ep-a 0336205、ep-a 0339396
和
ep-a 0798299
中,以及
1,3-和
1,4-双
(
异氰酸根合甲基
)
苯
(
苯二亚甲基二异氰酸酯,
xdi)、1,3-和
1,4-双
(2-异氰酸根合丙-2-基
)
苯
(
四甲基苯二亚甲基二异氰酸酯,
tmxdi)、1,3-双
(
异氰酸根合甲基
)-4-甲基苯
、1,3-双
(
异氰酸根合甲基
)-4-乙基苯
、1,3-双
(
异氰酸根合甲基
)-5-甲基苯
、1,3-双
(
异氰酸根合甲基
)-2,4,6-三甲基苯
、1,3-双
(
异氰酸根合甲基
)-4,5-二甲基苯
、1,4-双
(
异氰酸根合甲基
)-2,5-二甲基苯
、1,4-双
(
异氰酸根合甲基
)-2,3,5,6-四甲基苯
、1,3-双
(
异氰酸根合甲基
)-5-叔丁基苯
、1,4-双
(2-异氰酸根合乙基
)
苯
、1,4-双
(
异氰酸根合甲基
)
萘
、1,2-、1,3-和
1,4-二异氰酸根合苯
(
亚苯基二异氰酸酯
)、2,4-和
2,6-二异氰酸根合甲苯
(
甲苯二异氰酸酯,
tdi)、2,3,5,6-四甲基-1,4-二异氰酸根合苯
、
二异丙基亚苯基二异氰酸酯
、
二异十二烷基亚苯基二异氰酸酯和联苯二异氰酸酯
、3,3'-二甲氧基联苯-4,4'-二异氰酸酯
、2,2'-、
2,4'-和
4,4'-二苯甲烷二异氰酸酯
(mdi)、3,3'-二甲基二苯甲烷-4,4'-二异氰酸酯
、4,4'-二苯乙烷二异氰酸酯
、1,5-萘二异氰酸酯
(ndi)、
二苯醚二异氰酸酯
、
乙二醇二苯醚二异氰酸酯
、1,3-丙二醇二苯醚二异氰酸酯
、
苯三异氰酸酯
、2,4,6-甲苯三异氰酸酯
、
三甲基苯三异氰酸酯
、3-甲基二苯甲烷-4,6,4'-三异氰酸酯
、
异构体萘三异氰酸酯和甲基萘二异氰酸酯
、
三苯甲烷三异氰酸酯
、2,4-二异氰酸根合-1-[(5-异氰酸根合-2-甲基苯基
)
甲基
]
苯以及被称为“聚合物-mdi”的二苯甲烷二异氰酸酯的多核同系物,以及可由单体
2,4-和
/
或
2,6-tdi
通过与多元醇反应和
/
或低聚
(
优选三聚
)
获得的具有氨基甲酸酯和
/
或异氰脲酸酯结构的多异氰酸酯,其可通过任何已知方法获得,例如描述在
de-a 870400、de-a 953012、de-a 1090196、ep-a 0546399、cn 105218780、cn 103881050、cn 101717571、us 3183112、ep-a 0416338、ep-a 0751163、ep-a 1378529、ep-a1378530、ep-a 2174967、jp 63260915
或
jp 56059828
中,以及带有芳族和脂族的异氰酸酯基团的那些多异氰酸酯化合物,例如描述在
de-a 1670667、ep-a 0078991、ep-a 0696606
和
ep-a 0807623
中的
2,4-和
/
或
2,6-tdi
与
hdi
的混合三聚体或脲基甲酸酯
。
[0030]
并且最优选多异氰酸酯化合物
(a)
是选自具有脂族和
/
或芳族键合的异氰酸酯基团的
140g/mol
至
600g/mol
的分子量的多异氰酸酯中的至少一种化合物,实例是
1,5-戊烷二异氰酸酯
(
五亚甲基二异氰酸酯,
pdi)、1,6-己烷二异氰酸酯
(
六亚甲基二异氰酸酯,
hdi)、1-异氰酸根合-3,3,5-三甲基-5-异氰酸根合甲基环己烷
(
异佛尔酮二异氰酸酯,
ipdi)、2,4'-和
4,4'-二环己基甲烷二异氰酸酯
(h12-mdi)
,以及
1,3-和
1,4-双
(
异氰酸根合甲基
)
苯
(
苯二亚甲基二异氰酸酯,
xdi)、1,3-和
1,4-双
(2-异氰酸根合丙-2-基
)
苯
(
四甲基苯二亚甲基二异氰酸酯,
tmxdi)、2,2'-、2,4'-和
4,4'-二苯甲烷二异氰酸酯
(mdi)、3,3'-二甲基二苯甲烷-4,4'-二异氰酸酯
、4,4'-二苯乙烷二异氰酸酯
、1,5-萘二异氰酸酯
(ndi)。
[0031]
也可以使用前述多异氰酸酯化合物
(a)
中的两种或更多种的混合物
。
[0032]
如本文所用,术语“脂族多异氰酸酯化合物”意在表示具有两个或更多个异氰酸酯基团和脂族部分并且可包含芳族部分的化合物
。
脂族多异氰酸酯化合物是指直链脂族或脂环族多异氰酸酯化合物
。
在脂族多异氰酸酯化合物内,异氰酸酯部分不直接与芳族部分键合
。
苯二亚甲基二异氰酸酯
(xdi)
是具有不直接键合到芳族部分的异氰酸酯部分的脂族多异氰酸酯的实例,其中该异氰酸酯基团通过亚甲基基团键合到苯基
。
在根据本发明的方法的一个优选实施方案中,多异氰酸酯化合物
(a)
是脂族的
(a-1)。
[0033]
在根据本发明的方法的一个实施方案中,脂族多异氰酸酯化合物
(a-1)
是选自具有脂族键合的异氰酸酯基团的
140g/mol
至
400g/mol
的分子量的多异氰酸酯中的至少一种化合物,实例是
1,4-丁烷二异氰酸酯
、1,5-戊烷二异氰酸酯
(
五亚甲基二异氰酸酯,
pdi)、1,6-己烷二异氰酸酯
(
六亚甲基二异氰酸酯,
hdi)、2-甲基-1,5-戊烷二异氰酸酯
、1,5-二异氰酸根合-2,2-二甲基戊烷
、2,2,4-或
2,4,4-三甲基-1,6-己烷二异氰酸酯
、1,8-辛烷二异氰酸酯
、1,10-癸烷二异氰酸酯
、1,12-十二烷二异氰酸酯
、1,3-和
1,4-环己烷二异氰酸酯
、1,3-和
1,4-双
(
异氰酸根合甲基
)
环己烷
、1-异氰酸根合-3,3,5-三甲基-5-异氰酸根合甲基环己烷
(
异佛尔酮二异氰酸酯,
ipdi)、2,4'-和
4,4'-二环己基甲烷二异氰酸酯
(h12-mdi)、4,4'-二异氰酸根合-2,2-二环己基丙烷
、1-异氰酸根合-1-甲基-4(3)
异氰酸根合甲基环己烷
、
双
(
异氰酸根合甲基
)
降冰片烷
、1,3-和
1,4-双
(
异氰酸根合甲基
)
苯
(
苯二亚甲基二异氰酸酯,
xdi)、1,3-和
1,4-双
(2-异氰酸根合丙-2-基
)
苯
(
四甲基苯二亚甲基二异氰酸酯,
tmxdi)、1,3-双
(
异氰酸根合甲基
)-4-甲基苯
、1,3-双
(
异氰酸根合甲基
)-4-乙基苯
、1,3-双
(
异氰酸根合甲基
)-5-甲基苯
、1,3-双
(
异氰酸根合甲基
)-2,4,6-三甲基苯
、1,3-双
(
异氰酸根合甲基
)-4,5-二甲基苯
、1,4-双
(
异氰酸根合甲基
)-2,5-二甲基苯
、1,4-双
(
异氰酸根合甲基
)-2,3,5,6-四甲基苯
、1,3-双
(
异氰酸根合甲基
)-5-叔丁基苯
、1,3-双
(
异氰酸根合甲基
)-4-氯苯
、1,3-双
(
异氰酸根合甲基
)-4,5-二氯苯
、1,3-双
(
异氰酸根合甲基
)-2,4,5,6-四氯苯
、1,4-双
(
异氰酸根合甲基
)-2,3,5,6-四氯苯
、1,4-双
(
异氰酸根合甲基
)-2,3,5,6-四溴苯
、1,4-双
(2-异氰酸根合乙基
)
苯和
1,4-双
(
异氰酸根合甲基
)
萘
、
或具有脲二酮
、
异氰脲酸酯
、
脲基甲酸酯
、
缩二脲
、
亚氨基噁二嗪二酮和
/
或噁二嗪三酮结构的任何多异氰酸酯,其通过简单的脂族二异氰酸酯
(
例如上述类型的那些
)
的改性来制备,例如描述在
j.prakt.chem.336(1994)185-200、de-a 1670666、de-a 1954093、de-a 2414413、de-a 2452532、de-a 2641380、de-a 3700209、de-a 3900053
和
de-a 3928503
中,或描述在
ep-a 0336205、ep-a 0339396
和
ep-a 0798299
中,或至少两种此类多异氰酸酯的混合物
。
[0034]
更优选脂族多异氰酸酯化合物
(a-1)
是选自具有脂族键合的异氰酸酯基团的
140g/mol
至
400g/mol
的分子量的多异氰酸酯中的至少一种化合物,实例是
1,4-丁烷二异氰酸酯
、1,5-戊烷二异氰酸酯
(
五亚甲基二异氰酸酯,
pdi)、1,6-己烷二异氰酸酯
(
六亚甲基二异氰酸酯,
hdi)、1,5-二异氰酸根合-2,2-二甲基戊烷
、2,2,4-或
2,4,4-三甲基-1,6-己烷二异氰酸酯
、1,8-辛烷二异氰酸酯
、1,3-和
1,4-环己烷二异氰酸酯
、1,3-和
1,4-双
(
异氰酸根合甲基
)
环己烷
、1-异氰酸根合-3,3,5-三甲基-5-异氰酸根合甲基环己烷
(
异佛尔酮二异氰酸酯,
ipdi)、2,4'-和
4,4'-二环己基甲烷二异氰酸酯
(h12-mdi)、4,4'-二异氰酸根合-2,2-二环己基丙烷
、1,3-和
1,4-双
(
异氰酸根合甲基
)
苯
(
苯二亚甲基二异氰酸酯,
xdi)、1,3-和
1,4-双
(2-异氰酸根合丙-2-基
)
苯
(
四甲基苯二亚甲基二异氰酸酯,
tmxdi)、1,3-双
(
异氰酸根合甲基
)-4-甲基苯
、1,3-双
(
异氰酸根合甲基
)-4-乙基苯
、1,3-双
(
异氰酸根合甲基
)-5-甲基苯
、1,3-双
(
异氰酸根合甲基
)-2,4,6-三甲基苯
、1,3-双
(
异氰酸根合甲基
)-4,5-二甲基苯
、1,4-双
(
异氰酸根合甲基
)-2,5-二甲基苯
、1,4-双
(
异氰酸根合甲基
)-2,3,5,6-四甲基苯
、1,3-双
(
异氰酸根合甲基
)-5-叔丁基苯
、1,3-双
(
异氰酸根合甲基
)-4-氯苯
、1,3-双
(
异氰酸根合甲基
)-4,5-二氯苯
、1,3-双
(
异氰酸根合甲基
)-2,4,5,6-四氯苯
、1,4-双
(
异氰酸根合甲基
)-2,3,5,6-四氯苯
、1,4-双
(
异氰酸根合甲基
)-2,3,5,6-四溴苯
、1,4-双
(2-异氰酸根合乙基
)
苯和
1,4-双
(
异氰酸根合甲基
)
萘
、
或具有脲二酮
、
异氰脲酸酯
、
脲基甲酸酯
、
缩二脲
、
亚氨基噁二嗪二酮和
/
或噁二嗪三酮结构的任何多异氰酸酯,其通过简单的脂族二异氰酸酯
(
例如上述类型的那些
)
的改性来制备,例如描述在
j.prakt.chem.336(1994)185-200、de-a 1670666、de-a 1954093、de-a 2414413、de-a 2452532、de-a 2641380、de-a 3700209、de-a 3900053
和
de-a 3928503
或
ep-a 0336205、ep-a 0339396
和
ep-a 0798299
中,或至少两种此类多异氰酸酯的混合物
。
[0035]
并且最优选脂族多异氰酸酯化合物
(a-1)
是一种或多种化合物并且选自
1,5-戊烷二异氰酸酯
(
五亚甲基二异氰酸酯,
pdi)、1,6-己烷二异氰酸酯
(
六亚甲基二异氰酸酯,
hdi)
和
1-异氰酸根合-3,3,5-三甲基-5-异氰酸根合甲基环己烷
(
异佛尔酮二异氰酸酯,
ipdi)。
[0036]
也可以使用前述脂族多异氰酸酯化合物
(a-1)
的两种或更多种的混合物
。
[0037]
如本文所用,术语“芳族多异氰酸酯化合物”意在表示具有两个或更多个异氰酸酯基团的化合物并且必须含有芳族基团,并可另外含有脂族部分
。
因此,术语“芳族多异氰酸
酯化合物”意在表示带有两个或更多个直接与芳族部分键合的异氰酸酯基团的化合物,例如
2,4-和
2,6-二异氰酸根合甲苯
(
甲苯二异氰酸酯,
tdi)
或
2,2'-、2,4'-和
4,4'-二苯甲烷二异氰酸酯
(mdi)。
在根据本发明的方法的一个次优选实施方案中,多异氰酸酯化合物
(a)
是芳族多异氰酸酯化合物
(a-2)
[0038]
在根据本发明的方法的一个优选实施方案中,芳族多异氰酸酯化合物
(a-2)
是选自
160g/mol
至
600g/mol
分子量的芳族二异氰酸酯和三异氰酸酯的至少一种化合物,例如
1,2-、1,3-和
1,4-二异氰酸根合苯
(
亚苯基二异氰酸酯
)、2,4-和
2,6-二异氰酸根合甲苯
(
甲苯二异氰酸酯,
tdi)、2,3,5,6-四甲基-1,4-二异氰酸根合苯
、
二异丙基亚苯基二异氰酸酯
、
二异十二烷基亚苯基二异氰酸酯和联苯二异氰酸酯
、3,3'-二甲氧基联苯-4,4'-二异氰酸酯
、2,2'-、2,4'-和
4,4'-二苯甲烷二异氰酸酯
(mdi)、3,3'-二甲基二苯甲烷-4,4'-二异氰酸酯
、4,4'-二苯乙烷二异氰酸酯
、1,5-萘二异氰酸酯
(ndi)、
二苯醚二异氰酸酯
、
乙二醇二苯醚二异氰酸酯
、1,3-丙二醇二苯醚二异氰酸酯
、
苯三异氰酸酯
、2,4,6-甲苯三异氰酸酯
、
三甲基苯三异氰酸酯
、3-甲基二苯甲烷-4,6,4'-三异氰酸酯
、
异构体萘三异氰酸酯和甲基萘二异氰酸酯
、
三苯甲烷三异氰酸酯
、2,4-二异氰酸根合-1-[(5-异氰酸根合-2-甲基苯基
)
甲基
]
苯以及被称为“聚合物-mdi”的二苯甲烷二异氰酸酯的多核同系物,以及可由单体
2,4-和
/
或
2,6-tdi
通过与多元醇反应和
/
或低聚
(
优选三聚
)
获得的具有氨基甲酸酯和
/
或异氰脲酸酯结构的多异氰酸酯,其可通过任何已知方法获得,例如描述在
de-a 870400、de-a 953012、de-a 1090196、ep-a0546399、cn 105218780、cn 103881050、cn 101717571、us 3183112、ep-a 0416338、ep-a 0751163、ep-a 1378529、ep-a 1378530、ep-a 2174967、jp 63260915
或
jp 56059828
中
。
[0039]
在根据本发明的方法的一个更优选实施方案中,芳族多异氰酸酯化合物
(a-2)
是选自
160g/mol
至
600g/mol
分子量的芳族二异氰酸酯和三异氰酸酯的至少一种化合物,例如
1,2-、1,3-和
1,4-二异氰酸根合苯
(
亚苯基二异氰酸酯
)、2,4-和
2,6-二异氰酸根合甲苯
(
甲苯二异氰酸酯,
tdi)、2,3,5,6-四甲基-1,4-二异氰酸根合苯
、
异构体二乙基亚苯基二异氰酸酯
、
二异丙基亚苯基二异氰酸酯
、
二异十二烷基亚苯基二异氰酸酯和联苯二异氰酸酯
、3,3'-二甲氧基联苯-4,4'-二异氰酸酯
、2,2'-、2,4'-和
4,4'-二苯甲烷二异氰酸酯
(mdi)、3,3'-二甲基二苯甲烷-4,4'-二异氰酸酯
、4,4'-二苯乙烷二异氰酸酯
、1,5-萘二异氰酸酯
(ndi)、
二苯醚二异氰酸酯
、
乙二醇二苯醚二异氰酸酯
、
二乙二醇二苯醚二异氰酸酯
、1,3-丙二醇二苯醚二异氰酸酯
、
二苯甲酮二异氰酸酯
、
苯三异氰酸酯
、2,4,6-甲苯三异氰酸酯
、
三甲基苯三异氰酸酯
、
二苯甲烷-2,4,4'-三异氰酸酯
、3-甲基二苯甲烷-4,6,4'-三异氰酸酯
、
异构体萘三异氰酸酯和甲基萘二异氰酸酯
、
三苯甲烷三异氰酸酯
、2,4-二异氰酸根合-1-[(5-异氰酸根合-2-甲基苯基
)
甲基
]
苯
、4-甲基-二苯甲烷-3,5,2',4',6'-五异氰酸酯,以及被称为“聚合物-mdi”的二苯甲烷二异氰酸酯的多核同系物,以及可由单体
2,4-和
/
或
2,6-tdi
通过与多元醇反应和
/
或低聚
(
优选三聚
)
获得的具有氨基甲酸酯和
/
或异氰脲酸酯结构的多异氰酸酯,其可通过任何已知方法获得,例如描述在
de-a 870400、de-a 953012、de-a 1090196、ep-a 0546399、cn 105218780、cn 103881050、cn 101717571、us 3183112、ep-a 0416338、ep-a 0751163、ep-a 1378529、ep-a 1378530、ep-a 2174967、jp 63260915
或
jp 56059828
中,或至少两种此类多异氰酸酯的混合物
。
[0040]
在根据本发明的方法的一个最优选实施方案中,芳族多异氰酸酯化合物
(a-2)
是
选自
2,2'-、2,4'-和
4,4'-二苯甲烷二异氰酸酯
(mdi)、3,3'-二甲基二苯甲烷-4,4'-二异氰酸酯
、4,4'-二苯乙烷二异氰酸酯
、1,5-萘二异氰酸酯
(ndi)
和
2,4-和
2,6-二异氰酸根合甲苯
(tdi)
的至少一种化合物
。
[0041]
也可以使用芳族多异氰酸酯化合物
(a-2)
中的两种或更多种的混合物
。
[0042]
如本文所用,术语“多环氧化物化合物”意在表示具有两个或更多个环氧基团的化合物
。
[0043]
在本发明的一个优选实施方案中,多环氧化物化合物
(b)
是脂族多环氧化物化合物
(b-1)
和
/
或芳多环氧化物化合物
(b-2)
,优选脂族多环氧化物化合物
(b-1)。
[0044]
在本发明的一个优选实施方案中,环氧化物化合物
(b)
是至少一种化合物,其选自间苯二酚二缩水甘油醚
、
新戊二醇二缩水甘油醚
、1,6-己二醇二缩水甘油醚
、1,4-丁二醇二缩水甘油醚
、
氢化双酚a二缩水甘油醚
、
双酚a二缩水甘油醚
、
双酚f二缩水甘油醚
、
双酚s二缩水甘油醚
、9,9-双
(4-缩水甘油基氧基苯基
)
芴
、
四溴双酚a二缩水甘油醚
、
四氯双酚a二缩水甘油醚
、
四甲基双酚a二缩水甘油醚
、
四甲基双酚f二缩水甘油醚
、
四甲基双酚s二缩水甘油醚
、
对苯二甲酸二缩水甘油酯
、
邻苯二甲酸二缩水甘油酯
、
偏苯三甲酸三缩水甘油酯
、1,4-环己烷二甲酸二缩水甘油酯
、
乙二醇二缩水甘油醚
、
聚乙二醇二缩水甘油醚
、
二乙二醇二缩水甘油醚
、
丙二醇二缩水甘油醚
、
二丙二醇二缩水甘油醚
、
聚丙二醇二缩水甘油醚
、
聚丁二烯二缩水甘油醚
、
聚丁二烯二环氧化物
、
甘油三缩水甘油醚
、
聚甘油多缩水甘油醚
(polyglycerol polyglycidyl ether)、
乙氧基化三羟甲基丙烷的多缩水甘油醚
、
聚四氢呋喃二醇二缩水甘油醚
、
季戊四醇
(pentaeritrol)
多缩水甘油醚
、
乙烯基环己烯二环氧化物
、
柠檬烯二环氧化物
、
双不饱和脂肪酸
c1-c18
烷基酯的二环氧化物
、
双不饱和乙氧基化脂肪醇的多环氧化物
、2-二羟基苯二缩水甘油醚
、1,4-二羟基苯二缩水甘油醚
、4,4'-(3,3,5-三甲基亚环己基
)
联苯基二缩水甘油醚
(4,4'-(3,3,5-trimethylcyclohexyliden)bisphenyl diglycidyl ether)
和间苯二甲酸二缩水甘油酯
、
四溴双酚a二缩水甘油醚
、
基于腰果酚的二缩水甘油醚
、
氢醌二缩水甘油醚
、4,4'-二羟基苯二缩水甘油醚
、
双-(4-羟基苯基
)-1,1-乙烷二缩水甘油醚
、
双-(4-羟基苯基
)-1,1-异丁烷二缩水甘油醚
、
双-(4-羟基苯基
)
醚二缩水甘油醚,以及前述组分的氯化和溴化种类
。
[0045]
经由具有由
2-40
个碳原子组成的脂族直链
、
脂族支链或脂环族部分的二-或多官能醇的环氧化衍生的脂族二-或多缩水甘油醚,例如乙二醇二缩水甘油醚
、
丙二醇二缩水甘油醚
、
异山梨醇二缩水甘油醚
、
辛二醇二缩水甘油醚
、
三羟甲基丙烷多缩水甘油醚
、
甘油聚乙烯三缩水甘油醚
、2-乙基己基二缩水甘油醚
。
[0046]
更优选多环氧化物化合物
(b)
选自新戊二醇二缩水甘油醚
、
氢化双酚a二缩水甘油醚
、1,4-环己烷二甲酸二缩水甘油酯
、
乙二醇二缩水甘油醚
、
聚乙二醇二缩水甘油醚
、
二乙二醇二缩水甘油醚
、
丙二醇二缩水甘油醚
、
二丙二醇二缩水甘油醚
、
聚丙二醇二缩水甘油醚
、
甘油三缩水甘油醚
、
聚甘油多缩水甘油醚
、
乙氧基化三羟甲基丙烷的多缩水甘油醚
、
聚四氢呋喃二醇二缩水甘油醚
、
季戊四醇多缩水甘油醚
、
乙烯基环己烯二环氧化物
、
双不饱和脂肪酸
c1-c18
烷基酯的二环氧化物
、
双不饱和乙氧基化脂肪醇的多环氧化物
、
经由具有由
2-40
个碳原子组成的脂族直链
、
脂族支链或脂环族部分的二-或多官能醇的环氧化衍生的脂族二-或多缩水甘油醚,例如乙二醇二缩水甘油醚
、
丙二醇二缩水甘油醚
、
异山梨醇二缩水甘油醚
、1,4-丁二醇二缩水甘油醚
、1,6-己二醇二缩水甘油醚
、
辛二醇二缩水甘油醚
、
三
羟甲基丙烷多缩水甘油醚
、
甘油聚乙烯三缩水甘油醚
、2-乙基己基二缩水甘油醚
、
异山梨醇二缩水甘油醚
、
双酚a二缩水甘油醚
、
双酚f二缩水甘油醚
、
双酚s二缩水甘油醚
。
[0047]
最优选多环氧化物化合物
(b)
选自乙二醇二缩水甘油醚
、
丁二醇二缩水甘油醚
、
己二醇二缩水甘油醚
、
三羟甲基丙烷三缩水甘油醚
、
甘油三缩水甘油醚
。
[0048]
也可以使用前述多环氧化物化合物
(b)
中的两种或更多种的混合物
。
[0049]
如本文所用,术语“脂族多环氧化物化合物”意在表示具有两个或更多个环氧基团以及脂族部分的化合物
。
脂族多环氧化物化合物是指芳脂族或脂环族多环氧化物化合物
。
[0050]
在本发明的一个优选实施方案中,多环氧化物化合物
(b)
是脂族多环氧化物化合物
(b-1)。
[0051]
在本发明的一个优选实施方案中,脂族多环氧化物化合物
(b-1)
是一种或多种化合物并且选自新戊二醇二缩水甘油醚
、
氢化双酚a二缩水甘油醚
、1,4-环己烷二甲酸二缩水甘油酯
、
乙二醇二缩水甘油醚
、
聚乙二醇二缩水甘油醚
、
二乙二醇二缩水甘油醚
、
丙二醇二缩水甘油醚
、
二丙二醇二缩水甘油醚
、
聚丙二醇二缩水甘油醚
、
甘油三缩水甘油醚
、
聚甘油多缩水甘油醚
、
乙氧基化三羟甲基丙烷的多缩水甘油醚
、
聚四氢呋喃二醇二缩水甘油醚
、
季戊四醇多缩水甘油醚
、
乙烯基环己烯二环氧化物
、
双不饱和脂肪酸
c1-c18
烷基酯的二环氧化物
、
双不饱和乙氧基化脂肪醇的多环氧化物
、
经由具有由
2-40
个碳原子组成的脂族直链
、
脂族支链或脂环族部分的二-或多官能醇的环氧化衍生的脂族二-或多缩水甘油醚,例如乙二醇二缩水甘油醚
、
丙二醇二缩水甘油醚
、1,4-丁二醇二缩水甘油醚
、1,6-己二醇二缩水甘油醚
、
辛二醇二缩水甘油醚
、
三羟甲基丙烷多缩水甘油醚
、
甘油聚乙烯三缩水甘油醚
、2-乙基己基二缩水甘油醚
、
异山梨醇二缩水甘油醚
。
[0052]
在本发明的一个更优选实施方案中,脂族多环氧化物化合物
(b-1)
是一种或多种化合物并且选自氢化双酚a二缩水甘油醚
、
聚乙二醇二缩水甘油醚
、
聚丙二醇二缩水甘油醚
、
甘油三缩水甘油醚
、
乙氧基化三羟甲基丙烷的多缩水甘油醚
、
聚四氢呋喃二醇二缩水甘油醚
、
季戊四醇多缩水甘油醚
、
双不饱和脂肪酸
c1-c18
烷基酯的二环氧化物
、
经由具有由
2-40
个碳原子组成的脂族直链
、
脂族支链或脂环族部分的二-或多官能醇的环氧化衍生的脂族二-或多缩水甘油醚,例如乙二醇二缩水甘油醚
、1,4-丁二醇二缩水甘油醚
、1,6-己二醇二缩水甘油醚
、
三羟甲基丙烷多缩水甘油醚
、
甘油聚乙烯三缩水甘油醚
、2-乙基己基二缩水甘油醚
、
异山梨醇二缩水甘油醚
。
[0053]
最优选脂族多环氧化物化合物
(b-1)
是一种或多种化合物并且选自乙二醇二缩水甘油醚
、
丁二醇二缩水甘油醚
、
己二醇二缩水甘油醚
、
三羟甲基丙烷三缩水甘油醚和甘油三缩水甘油醚
。
[0054]
也可以使用前述脂族多环氧化物化合物
(b-1)
中的两种或更多种的混合物
。
[0055]
本文中所用的术语“芳族多环氧化物化合物”意在表示具有两个或更多个环氧基团以及芳族部分的化合物
。
[0056]
在本发明的一个替代性优选实施方案中,多环氧化物化合物
(b)
是芳族多环氧化物
(b-2)。
[0057]
在本发明的一个优选实施方案中,芳族多环氧化物化合物
(b-2)
是一种或多种化合物并且选自间苯二酚二缩水甘油醚
、
双酚a二缩水甘油醚
、
双酚f二缩水甘油醚
、
双酚s二缩水甘油醚
、9,9-双
(4-缩水甘油基氧基苯基
)
芴
、
四溴双酚a二缩水甘油醚
、
四氯双酚a二缩
水甘油醚
、
四甲基双酚a二缩水甘油醚
、
四甲基双酚f二缩水甘油醚
、
四甲基双酚s二缩水甘油醚
、
对苯二甲酸二缩水甘油酯
、
邻苯二甲酸二缩水甘油酯
、
偏苯三甲酸三缩水甘油酯
、1,4-环己烷二甲酸二缩水甘油酯
、2-二羟基苯二缩水甘油醚
、1,4-二羟基苯二缩水甘油醚
、4,4'-(3,3,5-三甲基亚环己基
)
联苯基二缩水甘油醚
、
间苯二甲酸二缩水甘油酯
、
四溴双酚
a、
基于腰果酚的二缩水甘油醚
、
氢醌二缩水甘油醚
、4,4'-二羟基苯基二缩水甘油醚
、
双-(4-羟基苯基
)-1,1-乙烷二缩水甘油醚
、
双-(4-羟基苯基
)-1,1-异丁烷二缩水甘油醚
、
双-(4-羟基苯基
)
醚二缩水甘油醚,以及前述组分的氯化和溴化种类
。
[0058]
在本发明的一个更优选实施方案中,芳族多环氧化物化合物
(b-2)
是一种或多种化合物并且选自双酚a二缩水甘油醚
、
双酚f二缩水甘油醚
、
双酚s二缩水甘油醚
、
四甲基双酚a二缩水甘油醚
、
四甲基双酚f二缩水甘油醚
、
四甲基双酚s二缩水甘油醚
、
对苯二甲酸二缩水甘油酯
、
邻苯二甲酸二缩水甘油酯
、2-二羟基苯二缩水甘油醚
、1,4-二羟基苯二缩水甘油醚
、4,4'-(3,3,5-三甲基亚环己基
)
联苯基二缩水甘油醚
、
间苯二甲酸二缩水甘油酯
、
基于腰果酚的二缩水甘油醚
、
氢醌二缩水甘油醚
、4,4'-二羟基苯基二缩水甘油醚
、
双-(4-羟基苯基
)-1,1-乙烷二缩水甘油醚
、
双-(4-羟基苯基
)-1,1-异丁烷二缩水甘油醚
、
双-(4-羟基苯基
)
醚二缩水甘油醚
。
[0059]
在本发明的一个最优选实施方案中,芳族多环氧化物化合物
(b-2)
是一种或多种化合物并且选自双酚a二缩水甘油醚
、
双酚f二缩水甘油醚
、
双酚s二缩水甘油醚
、
四甲基双酚a二缩水甘油醚
、
四甲基双酚f二缩水甘油醚
、
四甲基双酚s二缩水甘油醚
、
对苯二甲酸二缩水甘油酯
、2-二羟基苯二缩水甘油醚
、1,4-二羟基苯二缩水甘油醚
、
间苯二甲酸二缩水甘油酯
。
[0060]
也可以使用前述芳族多环氧化物化合物
(b-2)
的两种或更多种的混合物
。
[0061]
在本发明的第一可选择的优选实施方案中,多异氰酸酯化合物
(a)
是脂族多异氰酸酯化合物
(a-1)
并且多环氧化物化合物
(b)
是脂族多环氧化物化合物
(b-1)。
[0062]
在本发明的第二可选择的次优选的实施方案中,多异氰酸酯化合物
(a)
是脂族多异氰酸酯化合物
(a-1)
并且多环氧化物化合物
(b)
是芳族多环氧化物化合物
(b-2)。
[0063]
在本发明的第三可选择的次优选的实施方案中,多异氰酸酯化合物
(a)
是芳族多异氰酸酯化合物
(a-2)
并且多环氧化物化合物
(b)
是脂族多环氧化物化合物
(b-1)。
[0064]
在本发明的第四可选择的次优选的实施方案中,多异氰酸酯化合物
(a)
是芳族多异氰酸酯化合物
(a-2)
并且多环氧化物化合物
(b)
是芳族多环氧化物化合物
(b-2)。
[0065]
也可以使用前述脂族多异氰酸酯
(a-1)、
芳族多异氰酸酯化合物
(a-2)、
脂族多环氧化合物
(b-1)
和
/
或芳族多环氧化合物
(b-2)
的一种或多种的混合物
。
[0066]
在本发明的一个优选实施方案中,多异氰酸酯化合物
(a)
的异氰酸酯基团对多环氧化物化合物
(b)
的环氧基团的摩尔比为
2.6:1
至
7.0:1
,优选
2.7:1
至
6.0:1
,更优选
2.8:1
至
5.5:1。
如果多异氰酸酯化合物
(a)
的异氰酸酯基团对多环氧化物化合物
(b)
的环氧基团的摩尔比低于
2.6:1
,则所得的包含异氰酸酯基团封端的聚噁唑烷酮的异氰酸酯基团封端的聚噁唑烷酮组合物的粘度显著提高
。
[0067]
在本发明的一个优选实施方案中,所述方法包括:
[0068]
a)
将溶剂
(d)
和催化剂
(c)
置于反应器中以提供混合物
(a)
[0069]
b)
将多异氰酸酯化合物
(a)
和多环氧化物化合物
(b)
置于第二容器中以提供混合
物
(b)
[0070]
c)
将混合物
(b)
加入混合物
(a)
以形成异氰酸酯基团封端的聚噁唑烷酮组合物
(c)。
[0071]
d)
任选从异氰酸酯基团封端的聚噁唑烷酮组合物
(c)
中除去溶剂
(d)
和
/
或未反应的多异氰酸酯化合物
(a)
,形成异氰酸酯基团封端的聚噁唑烷酮
(d)。
[0072]
在本发明的第一可选择优选实施方案中,所述方法包括以下步骤:
[0073]
i)
将多异氰酸酯化合物
(a)、
多环氧化物化合物
(b)、
催化剂
(c)
和任选的溶剂
(d)
混合,形成混合物(i);
[0074]
ii)
使混合物(i)共聚形成异氰酸酯基团封端的聚噁唑烷酮组合物
(ii)
[0075]
iii)
任选从异氰酸酯基团封端的聚噁唑烷酮组合物
(ii)
中除去溶剂
(d)
和
/
或未反应的多异氰酸酯化合物
(a)
,形成异氰酸酯基团封端的聚噁唑烷酮
(iii)。
[0076]
在本发明的第二可选择优选实施方案中,所述方法包括以下步骤:
[0077]
α
)
将多环氧化物化合物
(b)、
至少部分的催化剂
(c)
和任选的至少部分的溶剂
(d)
混合,形成混合物
(
α
)
;
[0078]
β
)
在共聚条件下将多异氰酸酯化合物
(a)
添加至混合物
(
α
)
,形成异氰酸酯基团封端的聚噁唑烷酮组合物
(
β
)
;
[0079]
γ
)
任选从异氰酸酯基团封端的聚噁唑烷酮组合物
(
β
)
中除去溶剂
(d)
和
/
或未反应的多异氰酸酯化合物
(a)
,形成异氰酸酯基团封端的聚噁唑烷酮
(
γ
)。
[0080]
在本发明的第三可选择的
、
次优选的实施方案中,所述方法包括以下步骤:
[0081]
(1)
将多异氰酸酯化合物
(a)
和至少部分的催化剂
(c)
和至少部分的溶剂
(d)
混合,形成混合物
(1)
;
[0082]
(2)
在共聚条件下将多环氧化物化合物
(b)
添加至混合物
(a)
形成异氰酸酯基团封端的聚噁唑烷酮组合物
(2)
;
[0083]
(3)
任选从异氰酸酯基团封端的聚噁唑烷酮组合物
(2)
中除去溶剂
(d)
和
/
或未反应的多异氰酸酯化合物
(a)
,形成异氰酸酯基团封端的聚噁唑烷酮
(3)。
[0084]
在本发明的一个优选实施方案中,催化剂
(c)
包括四烷基卤化鏻
、
四环烷基卤化鏻和四芳基卤化鏻或其组合,优选四芳基卤化鏻
。
[0085]
在本发明的一个更优选实施方案中,催化剂
(c)
是选自四苯基氯化鏻
、
四苯基溴化鏻
、
四苯基碘化鏻
、
双
(
三苯基膦
)
氯化亚铵
、
四苯基硝酸鏻
、
四苯基碳酸鏻,优选四苯基氯化鏻
、
四苯基溴化鏻和四苯基碘化鏻,且更优选四苯基氯化鏻和四苯基溴化鏻的至少一种化合物
。
[0086]
在根据本发明的方法的一个实施方案中,基于所用单体的理论质量
(
多异氰酸酯化合物和多环氧化物化合物
(b)
的质量的总和
)
计,催化剂
(c)
以
≥20ppm
至
≤25000ppm
的摩尔量,优选
≥50ppm
至
≤20000ppm
的摩尔量,更优选
≥100ppm
至
≤12000ppm
的摩尔量存在
。
[0087]
在本发明的一个实施方案中,使用溶剂
(d)。
[0088]
在本发明的一个实施方案中,二异氰酸酯化合物
(a)、
双环氧化物化合物
(b)
和催化剂
(c)
的总和相对于二异氰酸酯化合物
(a)、
双环氧化物化合物
(b)、
催化剂
(c)
和溶剂
(d)
的总和的计算质量比为
40
重量%至
100
重量%,优选
50
重量%至
90
重量%,更且优选
60
重量%至
80
重量%
。
[0089]
溶剂
(d)
按照一般定义被定义为溶解溶质
(
即化合物
(a)
和
/
或化合物
(b)
和
/
或化合物
(c))
但不与化合物
(a)、
化合物
(b)
和
/
或催化剂
(c)
,特别是多异氰酸酯化合物
(a)(
化学地
)
反应的物质
。
[0090]
根据本发明的合适溶剂
(d)
是非质子卤代芳族溶剂
、
高沸点非质子脂族杂环溶剂
、
卤代芳族或脂族杂环溶剂,其具有在1巴
(
绝对
)
等于或低于
200℃
,优选等于或低于
190℃
,并且更优选等于或低于
180℃
的沸点
。
[0091]
在本发明的一个优选实施方案中,共聚在溶剂
(d)
的存在下进行,其中溶剂
(d)
是一种或多种化合物并且选自氯苯
、
氯苯的不同异构体
、
二氯苯的不同异构体
、
二甲基甲酰胺
、n,n-二甲基乙酰胺
、
四氢呋喃
、
丙酮
、
甲基乙基酮
、1,2-二甲氧基乙烷
、1-甲氧基-2-(2-甲氧基乙氧基
)
乙烷
、
二噁烷的不同异构体,优选氯苯和邻二氯苯
。
[0092]
根据本发明的反应在不存在沸点
(
在1巴
(
绝对
))
高于
200℃
,优选高于
190℃
且更优选高于
180℃
的溶剂
(e)
的情况下进行
。
[0093]
这样的溶剂
(e)
包括例如环状碳酸酯
(
例如碳酸亚乙酯或碳酸亚丙酯
)、n-甲基吡咯烷酮
(nmp)
和环丁砜
。
不存在这类另外的溶剂
(e)
减少了这类高沸点溶剂的能量密集型且耗时的脱除工艺,例如蒸馏
。
[0094]
不存在另外的溶剂
(e)
是指
(e)
的溶剂量小于5重量%,优选4重量%,更优选2重量%
。
[0095]
本发明的另一方面是可通过根据本发明的方法获得的异氰酸酯基团封端的聚噁唑烷酮组合物
。
[0096]
在本发明的一个实施方案中,异氰酸酯基团封端的聚噁唑烷酮组合物具有小于
5000mpa
·s,优选
5mpa
·s至
2000mpa
·s,并且更优选
10mpa
·s至
1000mpa
·s的粘度,其中粘度经由来自
anton paar mcr 302
的锥
/
板流变仪测定
。
剪切速率
631
·
min-1
用于测定产物的粘度
。
粘度以单位
mpa
·s给出
。(
按照根据
din en iso 3219/a.3:1994
的程序
)。
如果没有另外指出,则所有测量均在
25℃
进行
。
[0097]
在本发明的一个实施方案中,异氰酸酯基团封端的聚噁唑烷酮组合物具有
50g/eq
至
10000g/eq
,优选
75g/eq
至
6000g/eq
,更优选
100g/eq
至
2000g/eq
的异氰酸酯当量重量
(iew)
,其中异氰酸酯当量重量根据
din en iso 11909:2007
经由滴定测定
。
[0098]
聚噁唑烷酮的异氰酸酯当量重量
(iew)
定义为含有1当量的异氰酸酯基团的物质的总质量
。
[0099]
在本发明的一个实施方案中,异氰酸酯基团封端的聚噁唑烷酮组合物具有高于
2.0:1
,优选
2.3:1
至
20.0:1
,更优选
2.8:1
至
10.0:1
的噁唑烷酮对异氰脲酸酯的比,其中噁唑烷酮-异氰脲酸酯比根据在实验部分内公开的红外测量方法测定
。
[0100]
在本发明的一个实施方案中,异氰酸酯基团封端的聚噁唑烷酮组合物具有小于
7.0
,优选
1.0
至
6.5
,更优选为
1.5
至
6.0
的
gardner
颜色指数,其中
gardner
颜色指数根据
din en iso 1557:1997
测定
。
[0101]
本发明的另一方面是用于制备异氰酸酯基团封端的聚噁唑烷酮
(
预聚物
)
的方法,其中从根据本发明的方法获得的异氰酸酯基团封端的聚噁唑烷酮组合物或可根据本发明的方法获得的异氰酸酯基团封端的聚噁唑烷酮组合物中除去溶剂
(d)
和
/
或未反应的多异氰酸酯化合物
(a)。
[0102]
在本发明的一个实施方案中,通过热处理方法,优选通过蒸馏和
/
或通过萃取,更优选通过薄膜蒸发除去未反应的多异氰酸酯化合物
(a)
和
/
或溶剂
(d)。
[0103]
为了在步骤
d)、
步骤
iii)、
步骤
γ
)
或步骤
(3)
中除去溶剂
(d)
和
/
或未反应的多异氰酸酯化合物
(a)
,可以应用适当的纯化方法,例如薄膜蒸发
。
除去溶剂
(d)
和
/
或未反应的多异氰酸酯化合物
(a)
对于将来的聚合应用是有益的,因为例如含卤素的溶剂和
/
或未反应的多异氰酸酯化合物
(a)
可干扰这些聚合反应并负面影响所得的聚合产物
。
此外,除去溶剂
(d)
和
/
或单体多异氰酸酯化合物
(a)
导致具有较低的健康风险的产物,因为有害的单体多异氰酸酯化合物
(a)
和溶剂
(d)
的量可显著降低
。
剩余的异氰酸酯基团封端的聚噁唑烷酮
(
预聚物
)
,例如异氰酸酯基团封端的聚噁唑烷酮
(d)、
异氰酸酯基团封端的聚噁唑烷酮
(
γ
)、
异氰酸酯基团封端的聚噁唑烷酮
(iii)
和异氰酸酯基团封端的聚噁唑烷酮
(3)
具有相对高的分子量,并且不期望表现出比无溶剂和具有低浓度的单体多异氰酸酯化合物的其它多异氰酸酯预聚物更高的风险
。
[0104]
本发明的另一方面是可根据本发明的方法获得的异氰酸酯基团封端的聚噁唑烷酮
。
[0105]
在本发明的一个实施方案中,异氰酸酯基团封端的聚噁唑烷酮具有
50g/eq
至
10000g/eq
,优选
75g/eq
至
6000g/eq
,更优选
100g/eq
至
2000g/eq
的异氰酸酯当量重量
(iew)
,其中异氰酸酯当量重量根据
din en iso 11909:2007
经由滴定测定
。
[0106]
聚噁唑烷酮的异氰酸酯当量重量
(iew)
定义为含有1当量的异氰酸酯基团的物质的总质量
。
[0107]
在本发明的一个实施方案中,异氰酸酯基团封端的聚噁唑烷酮的具有高于
2.0:1
,优选
2.3:1
至
20.0:1
,更优选
2.8:1
至
10.0:1
的噁唑烷酮对异氰脲酸酯的比,其中噁唑烷酮-异氰脲酸酯比根据在实验部分内公开的红外测量方法测定
。
[0108]
在本发明的一个实施方案中,异氰酸酯基团封端的聚噁唑烷酮具有小于
6.0
,优选
1.0
至
5.5
,更优选为
1.5
至
5.0
的
gardner
颜色指数,其中
gardner
颜色指数根据
din en iso 1557:1997
测定
。
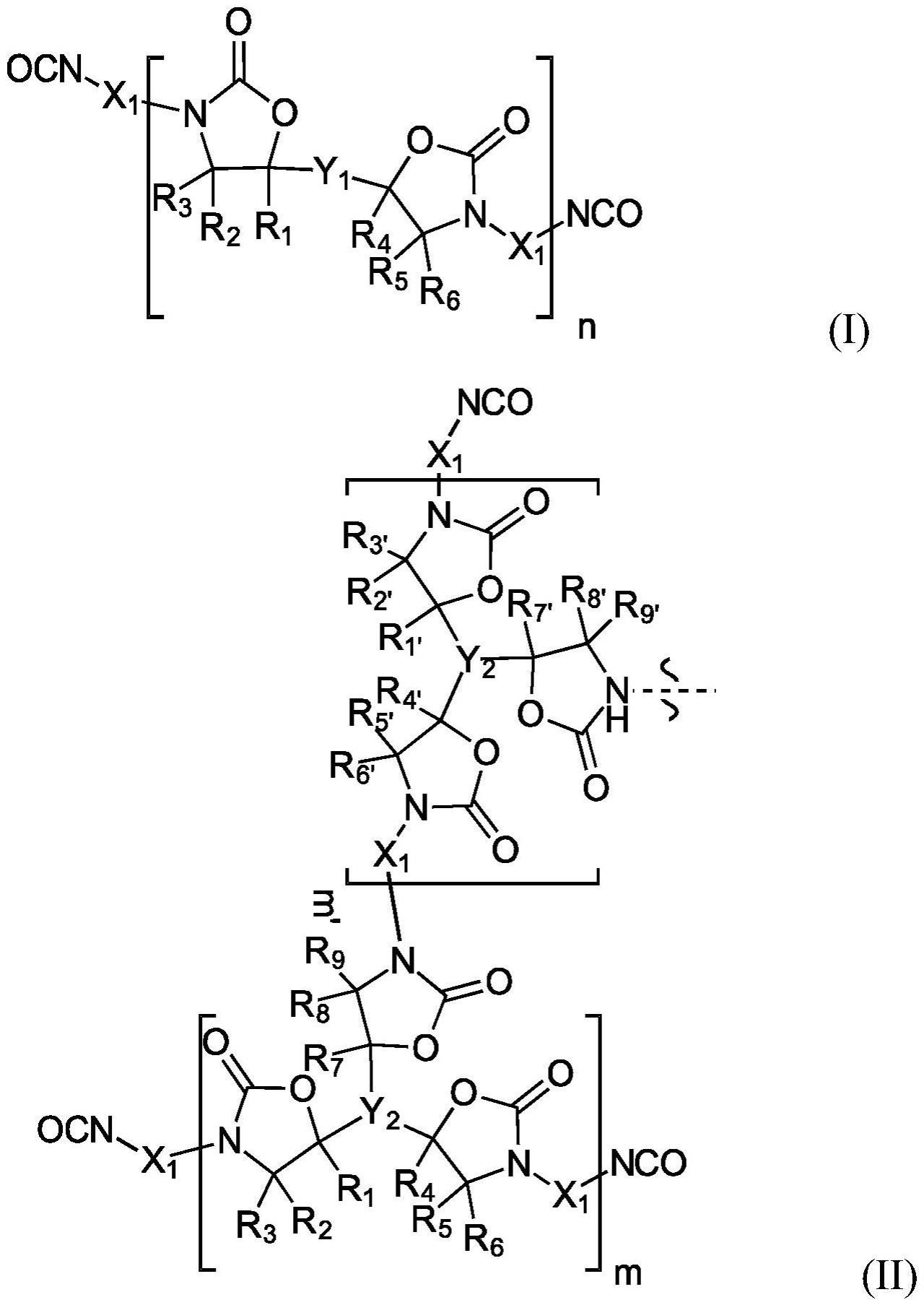
[0109]
本发明的另一方面是根据式
(i)、
式
(ii)
和
/
或式
(iii)
的异氰酸酯基团封端的聚噁唑烷酮
(
预聚物
)
[0110]
tetramethyl-m-or-p-xylylene)
;优选六亚甲基二异氰酸酯
、
五亚甲基二异氰酸酯或
5-(1-亚甲基-(1,3,3-三甲基环己烷
))。
[0114]
y1代表亚甲基
、
二亚甲基
、
三亚甲基
、
四亚甲基
、
五亚甲基
、
六亚甲基
、
七亚甲基
、
八亚甲基
、
多亚乙基
(polyethylene)、
聚乙二醇
(polyethyleneglycol)、1,2-亚环己基
、1,3-亚环己基
、1,4-亚环己基
、1,2-亚苯基
、1,3-亚苯基
、1,4-亚苯基
、1,2-亚甲苯基
、1,3-亚甲苯基
、1,4-亚甲苯基
、4,4'-亚甲基双
(4,1-亚苯基
)、4,4'-亚甲基双
(
环己烷-4,1-二基
)、4,4'-(
丙烷-2,2-二基
)
双
(4,1-亚苯基
)、
丙烷-2,2-二基-双
(
环己烷-4,1-二基
)
或
y1可以由通式
iv
表示,
[0115][0116]
其中
y'
表示亚甲基
、
二亚甲基
、
三亚甲基
、
四亚甲基
、
五亚甲基
、
六亚甲基
、
七亚甲基
、
八亚甲基
、
多亚乙基
、
聚乙二醇
、1,2-亚环己基
、1,3-亚环己基
、1,4-亚环己基
、1,2-亚苯基
、1,3-亚苯基
、1,4-亚苯基
、1,2-亚甲苯基
、1,3-亚甲苯基
、1,4-亚甲苯基
、4,4'-亚甲基双
(4,1-亚苯基
)、4,4'-亚甲基双
(
环己烷-4,1-二基
)、4,4'-(
丙烷-2,2-二基
)
双
(4,1-亚苯基
)、
丙烷-2,2-二基-双
(
环己烷-4,1-二基
)
或
4,4'-(3,3,5-三甲基亚环己基
)
双苯基,优选二亚甲基
、
四亚甲基或六亚甲基,最优选四亚甲基,
[0117]
y2可由式v表示
[0118][0119]
其中
y"
表示
1-(2,2-二亚甲基
)
丁烷
、1,2,3-丙烷
、1,3-(2,2-二亚甲基
)
丙烷
、
聚甲苯基多缩水甘油醚
、
酚醛清漆型缩水甘油醚,优选
1-(2,2-二亚甲基
)
丁烷
、1,2,3-丙烷或
1,3-(2,2-二亚甲基
)
丙烷
。
[0120]
所示出的分子结构
(ii)
和
(iii)
说明了整个预聚物支架的示例性部分
。
因此,与波浪线交叉的分散的键表示部分结构的延续
。
一方面,亚结构可由单个单体结构单元延续,另一方面,由类似于所描绘的部分结构的进一步
(
多维
)
的链延长延续
。
[0121]
r1、r1'、r2、r2'、r3、r3'、r4、r4'、r5、r5'、r6、r6'、r7、r7'、r8、r8'、r9、r9'
彼此独立地代表氢
、
氯
、
溴
、
氟
、
甲基
、
乙基
、
丙基
、
正丙基
、
异丙基
、
正丁基
、
异丁基
、2-丁基
、
叔丁基
、
己基
、
甲氧基
、
乙氧基
、
丁氧基
、
苯基
、
甲氧基苯基
、
氯苯基
、
溴苯基
、
硝基苯基
、
环丁基
、
环戊基
、
环己基
、
环庚基
。
[0122]
x1、y1、y2可以彼此相同或不同,
[0123]
r1、r1'、r2、r2'、r3、r3'、r4、r4'、r5、r5'、r6、r6'、r7、r7'、r8、r8'、r9、r9'
可以彼此相同或不同,并且
[0124]
m、n、m'、n'
是整数,其中
(m+n+m'+n')≥1
,优选
1≤(m+n+m'+n')≤100
,更优选
1≤(m+n+m'+n')≤50
,最优选
1≤(m+n+m'+n')≤30。
[0125]
在本发明的一个实施方案中,根据式
(i)、
式
(ii)
和
/
或式
(iii)
的异氰酸酯基团封端的聚噁唑烷酮具有
50g/eq
至
10000g/eq
,优选
75g/eq
至
6000g/eq
,更优选
100g/eq
至
2000g/eq
的异氰酸酯当量重量
(iew)
,其中异氰酸酯当量重量根据
din en iso 11909:2007
经由滴定测定
。
[0126]
根据式
(i)、
式
(ii)
和
/
或式
(iii)
的聚噁唑烷酮的异氰酸酯当量重量
(iew)
定义为含有1当量的异氰酸酯基团的物质的总质量
。
[0127]
在本发明的一个实施方案中,根据式
(i)、
式
(ii)
和
/
或式
(iii)
的异氰酸酯基团封端的聚噁唑烷酮具有高于
2.0:1
,优选
2.3:1
至
20.0:1
,更优选
2.8:1
至
10.0:1
的噁唑烷酮对异氰脲酸酯的比,其中噁唑烷酮-异氰脲酸酯比根据在实验部分内公开的红外测量方法测定
。
[0128]
在本发明的一个实施方案中,根据式
(i)、
式
(ii)
和
/
或式
(iii)
的异氰酸酯基团封端的聚噁唑烷酮具有小于
6.0
,优选
1.0
至
5.5
,更优选
1.5
至
5.0
的
gardner
颜色指数,其中
gardner
颜色指数根据
din en iso 1557:1997
测定
。
实施例
[0129]
将参考以下实施例进一步描述本发明,而不希望受它们限制
。
[0130]
二异氰酸酯化合物
(a)
[0131]
a-i
:异佛尔酮二异氰酸酯
(ipdi)
,
covestro
,
ag
,
germany。
[0132]
环氧化合物
(b)
[0133]
为了计算实验摩尔比,对于二环氧化物化合物假设化合物纯度为
100
%
。
为了计算,忽略了可能的杂质
(
例如醇类化合物
)。
[0134]
b-i
:
ipox rd3
丁二醇二缩水甘油醚
(bdde)
,
eew 130-145g/eq
;获自
ipox chemicals gmbh
,
germany。
[0135]
由于
ipox rd 3
提供了显著量的非理想结构的化合物
(bdde)
,基于下式计算用于计算环氧基团的有效摩尔量的校正因子f:
[0136][0137]
催化剂
(c)
[0138]
c-i
:
tppcl
四苯基氯化鏻,纯度
98
%,获自
sigma aldrich
[0139]
c-ii
:
tppbr
四苯基溴化鏻,纯度>
99
%,获自
sigma aldrich
[0140]
c-ii
:
tppi
四苯基碘化鏻,获自
merck schuchardt ohg
[0141]
c-iii
:
licl
氯化锂,获自
sigma aldrich
,具有>
99
%纯度
[0142]
c-iv
:
libr
溴化锂,纯度>
99.9
%,获自
acros organics
[0143]
c-v
:
yb(otf)3三
(
三氟甲磺酸
)
镱,
99.9
%,获自
acros organics
[0144]
c-vi
:
tbabr
四丁基溴化铵,>
99
%,获自
acros organics
[0145]
c-vii
:
emimcl
氯化
1-乙基-3-甲基咪唑鎓:>
97
%,通过
acros organics
获得
[0146]
c-viii
:
bmpcl
氯化
1-丁基-1-甲基哌啶鎓:
99
%,通过
iolitec ionic liquids technologies gmbh
获得
[0147]
c-ix
:
sb(ph)3三苯基锑
(iii)(
三苯锑
(iii))
:
99
%,获自
sigma aldrich
[0148]
c-x
:
i2碘:
》99.8
%,获自
sigma aldrich
[0149]
催化剂的浓度以与所用单体的理论质量相关的
ppm
给出
。
[0150]
溶剂
(d)
[0151]
d-i
:邻二氯苯
(o-dcb)
,纯度
99
%,无水,获自
sigma-aldrich,germany
[0152]
溶剂
(e)
[0153]
e-i
:环丁砜,纯度
≥99
%,无水,获自
sigma-aldrich,germany。
[0154]
o-dcb、ipdi、licl、libr、tppcl、tppbr、tppi、tbabr、emimcl、bmpcl
和
bdde
按原样使用,不经进一步纯化
。
环丁砜在
50℃
熔融并经分子筛干燥后使用
。
[0155]
聚噁唑烷酮预聚物的表征
[0156]
红外分析
(ir)
[0157]
在配备有金刚石探头的
bruker alpha-p ir
光谱仪上进行
ir
分析
。
使用软件
opus 6.5
进行数据处理
。
针对环境空气记录背景光谱
。
此后,将聚噁唑烷酮预聚物的少量样品
(
约
2mg)
施加到金刚石探头,并将在
4000
至
400cm-1
的范围内以
4cm-1
的分辨率获得的
24
个光谱取平均来记录
ir
光谱
。
[0158]
根据下式计算噁唑烷酮与异氰脲酸酯的峰高比:
[0159][0160]
对于噁唑烷酮使用
1749cm-1
处的峰的峰高,并且对于异氰脲酸酯使用
1680cm-1
处的峰的峰高
。
[0161]
颜色指数
[0162]
gardner
颜色指数通过使用购自
hach
的
lico 620
测定
。
因此,将异氰酸酯基团封端的聚噁唑烷酮组合物的样品装入比色皿中,随后按照
din en iso 1557:1997
对其进行分析
。
在颜色指数测量之前,将分离的异氰酸酯基团封端的聚噁唑烷酮预聚物溶解在
o-dcb(68
重量%固含量
)
中
。
[0163]
粘度测量
[0164]
粘度值经由来自
anton paar mcr 302
的锥
/
板流变仪测定
。
剪切速率
631
·
min-1
用于测定产物的粘度
。
粘度以单位
mpa
·s给出
。(
按照根据
din en iso 3219/a.3:1994
的程序
)。
如果没有另行指出,则所有测量均在
25℃
进行
。
[0165]
gpc
[0166]
在
40℃
在四氢呋喃
(thf
,流速为
1.0ml min-1
)
中进行
gpc
测量
。
柱组由4个连续柱
(2
×
pss,sdv 50a,5
μ
l
,和2×
pss,sdv 100a,5
μ
l)
组成
。
注入样品
(
浓度
2-3g l-1
,进样体积
100
μ
l)。agilent 1200
系列的
rid
检测器用于追踪柱出口处的浓度
。
使用
pss wingpc unity
软件包处理原始数据
。
使用已知分子量的聚苯乙烯作为参比来计算分子量分布
(
使用在
266da
至
66.000da
的区域中的
pss readycal kit)。
通过
gpc
测得的数均分子量在实施例中称为mn
(gpc)。
[0167]
反应器
[0168]
在配备有玻璃回流冷凝器
、
气体入口
(n2)、
注射泵
(
来自
syrdos
的
ip-syrdos2-hp-xlp)、
配备有温度探针的玻璃入口管
(
来自
ebro
的
gfx 460)
和顶置式
kpg
搅拌器
(
来自
ika
的
rw20)
的
250
毫升4颈圆底烧瓶中进行反应
。
该圆底烧瓶用来自
winkler
的加热套
(wm/bri/250
,最大加热功率为
120w)
加热,所述加热套与具有来自
ebro
的
rb 1691b-s
的温度探针连
接
。
[0169]
实施例
1(
对比
)
:在半间歇式程序中以
5.7:1
的异氰酸酯基团对环氧基团的摩尔比用
ipdi
作为化合物
(a-i)
和用
ipox rd 3
作为化合物
(b-i)
使用
licl(c-iii)
作为化合物
(c)
和包含作为化合物
(d-i)
的
o-dcb
与作为化合物
(e-i)
的环丁砜的溶剂混合物合成基于异氰酸酯封端的聚噁唑烷酮的组合物
。
[0170]
在如前所述的反应器中装入
licl(79.5mg
,
788ppm)(c-iii)。
随后添加环丁砜
(9.0ml)(e-i)
并搅拌
(400rpm)
混合物并用氮气
(
约
1ml/min)
吹扫
30
分钟
。
随后,将混合物加热至
175℃
,然后添加
o-dcb(d-i)(17ml)。
接着,在
30
分钟的时间范围内,使用注射泵以连续方式添加
ipox rd3(17.44g
,
0.066mol)(b-i)、ipdi(83.36g
,
0.375mol)(a-i)
和
o-dcb(11ml)(d-1)
的混合物
。
在单体的添加完成后,搅拌反应物并再加热
210
分钟,然后使反应混合物冷却至室温
。
[0171]
在反应过程中,取出反应混合物的样品并通过
ir
光谱法进行分析
。
通过观察到来自反应混合物的
ir
光谱中异氰酸酯带
(2260cm-1
)
不再变化来证实反应完全
。
[0172]
实施例
2(
对比
)
:在半间歇式程序中以
5.7:1
的异氰酸酯基团对环氧基团的摩尔比用
ipdi
作为化合物
(a-i)
和用
ipox rd 3
作为化合物
(b-i)
使用
licl(c-iii)
作为化合物
(c)
和包含作为化合物
(d-i)
的
o-dcb
的溶剂混合物合成基于异氰酸酯封端的聚噁唑烷酮的组合物
。
[0173]
在如前所述的反应器中装入
licl(79.5mg
,
788ppm)(c-iii)。
随后后添加
o-dcb(d-i)(25ml)
并搅拌
(400rpm)
混合物并用氮气
(
约
1ml/min)
吹扫
30
分钟
。
随后,将混合物加热至
175℃。
接着,在
30
分钟的时间范围内,使用注射泵以连续方式添加
ipox rd3(17.44g
,
0.066mol)(b-i)、ipdi(83.36g
,
0.375mol)(a-i)
和
o-dcb(11ml)(d-1)
的混合物
。
在单体的添加完成后,搅拌反应物并再加热
210
分钟,然后使反应混合物冷却至室温
。
[0174]
在反应过程中,取出反应混合物的样品并通过
ir
光谱法进行分析
。
通过观察到来自反应混合物的
ir
光谱中异氰酸酯带
(2260cm-1
)
不再变化来证实反应完全
。
[0175]
实施例
3(
对比
)
:在半间歇式程序中以
5.7:1
的异氰酸酯基团对环氧基团的摩尔比用
ipdi
作为化合物
(a-i)
和用
ipox rd 3
作为化合物
(b-i)
使用
tbabr(c-vi)
作为化合物
(c)
和包含作为化合物
(d-i)
的
o-dcb
的溶剂混合物合成基于异氰酸酯封端的聚噁唑烷酮的组合物
。
[0176]
在如前所述的反应器中装入
tbabr(604mg,5960ppm)(c-vi)。
随后添加
o-dcb(d-i)(25ml)
并搅拌
(400rpm)
混合物并用氮气
(
约
1ml/min)
吹扫
30
分钟
。
随后,将混合物加热至
175℃
,然后添加
o-dcb(d-i)(17ml)。
接着,在
30
分钟的时间范围内,使用注射泵以连续方式添加
ipox rd3(17.44g
,
0.066mol)(b-i)、ipdi(83.36g
,
0.375mol)(a-i)
和
o-dcb(11ml)(d-1)
的混合物
。
在单体的添加完成后,搅拌反应物并再加热
210
分钟,然后使反应混合物冷却至室温
。
[0177]
在反应过程中,取出反应混合物的样品并通过
ir
光谱法进行分析
。
通过观察到来自反应混合物的
ir
光谱中异氰酸酯带
(2260cm-1
)
不再变化来证实反应完全
。
[0178]
实施例
4(
对比
)
:在半间歇式程序中以
5.7:1
的异氰酸酯基团对环氧基团的摩尔比用
ipdi
作为化合物
(a-i)
和用
ipox rd 3
作为化合物
(b-i)
使用
tbabr(c-vi)
作为化合物
(c)
合成基于异氰酸酯封端的聚噁唑烷酮的组合物
。
[0179]
在如前所述的反应器中装入
tbabr(604mg,5960ppm)(c-vi)。
随后添加
ipdi(16.67g,0.075mol)
并搅拌
(400rpm)
混合物并用氮气
(
约
1ml/min)
吹扫
30
分钟
。
随后,将混合物加热至
175℃。
接着,在
30
分钟的时间范围内,使用注射泵以连续方式添加
ipox rd3(17.44g
,
0.066mol)(b-i)
和
ipdi(66.69g
,
0.30mol)(a-i)
的混合物
。
在单体的添加完成后,搅拌反应物并再加热
210
分钟,然后使反应混合物冷却至室温
。
[0180]
在反应过程中,取出反应混合物的样品并通过
ir
光谱法进行分析
。
通过观察到来自反应混合物的
ir
光谱中异氰酸酯带
(2260cm-1
)
不再变化来证实反应完全
。
[0181]
实施例
5(
对比
)
:在半间歇式程序中以
5.7:1
的异氰酸酯基团对环氧基团的摩尔比用
ipdi
作为化合物
(a-i)
和用
ipox rd 3
作为化合物
(b-i)
使用
emimcl(c-vii)
作为化合物
(c)
和包含作为化合物
(d-i)
的
o-dcb
的溶剂混合物合成基于异氰酸酯封端的聚噁唑烷酮的组合物
。
[0182]
在如前所述的反应器中装入
emimcl(275mg,2720ppm)(c-vii)。
随后添加
o-dcb(d-i)(25ml)
并搅拌
(400rpm)
混合物并用氮气
(
约
1ml/min)
吹扫
30
分钟
。
随后,将混合物加热至
175℃。
接着,在
30
分钟的时间范围内,使用注射泵以连续方式添加
ipox rd3(17.44g
,
0.066mol)(b-i)、ipdi(83.36g
,
0.375mol)(a-i)
和
o-dcb(11ml)(d-1)
的混合物
。
在单体的添加完成后,搅拌反应物并再加热
210
分钟,然后使反应混合物冷却至室温
。
[0183]
在反应过程中,取出反应混合物的样品并通过
ir
光谱法进行分析
。
通过观察到来自反应混合物的
ir
光谱中异氰酸酯带
(2260cm-1
)
不再变化来证实反应完全
。
[0184]
实施例
6(
对比
)
:在半间歇式程序中以
5.7:1
的异氰酸酯基团对环氧基团的摩尔比用
ipdi
作为化合物
(a-i)
和用
ipox rd 3
作为化合物
(b-i)
使用
bmpcl(c-viii)
作为化合物
(c)
和包含作为化合物
(d-i)
的
o-dcb
的溶剂混合物合成基于异氰酸酯封端的聚噁唑烷酮的组合物
。
[0185]
在如前所述的反应器中装入
bmpcl(348mg,3442ppm)(c-viii)。
随后添加
o-dcb(d-i)(25ml)
并搅拌
(400rpm)
混合物并用氮气
(
约
1ml/min)
吹扫
30
分钟
。
随后,将混合物加热至
175℃。
接着,在
30
分钟的时间范围内,使用注射泵以连续方式添加
ipox rd3(17.44g
,
0.066mol)(b-i)、ipdi(83.36g
,
0.375mol)(a-i)
和
o-dcb(11ml)(d-1)
的混合物
。
在单体的添加完成后,搅拌反应物并再加热
210
分钟,然后使反应混合物冷却至室温
。
[0186]
在反应过程中,取出反应混合物的样品并通过
ir
光谱法进行分析
。
通过观察到来自反应混合物的
ir
光谱中异氰酸酯带
(2260cm-1
)
不再变化来证实反应完全
。
[0187]
实施例
7(
对比
)
:在半间歇式程序中以
5.7:1
的异氰酸酯基团对环氧基团的摩尔比用
ipdi
作为化合物
(a-i)
和用
ipox rd 3
作为化合物
(b-i)
使用
libr(c-iv)
作为化合物
(c)
和包含作为化合物
(d-i)
的
o-dcb
与作为化合物
(e-i)
的环丁砜的溶剂混合物合成基于异氰酸酯封端的聚噁唑烷酮的组合物
。
[0188]
在如前所述的反应器中装入
libr(163mg,1613ppm)(c-iv)。
随后添加环丁砜
(9.0ml)(e-i)
并搅拌
(400rpm)
混合物并用氮气
(
约
1ml/min)
吹扫
30
分钟
。
随后,将混合物加热至
175℃
,然后添加
o-dcb(d-i)(17ml)。
接着,在
30
分钟的时间范围内,使用注射泵以连续方式添加
ipox rd3(17.44g
,
0.066mol)(b-i)、ipdi(83.36g
,
0.375mol)(a-i)
和
o-dcb(11ml)(d-1)
的混合物
。
在单体的添加完成后,搅拌反应物并再加热
210
分钟,然后使反应混合物冷却至室温
。
[0189]
在反应过程中,取出反应混合物的样品并通过
ir
光谱法进行分析
。
通过观察到来自反应混合物的
ir
光谱中异氰酸酯带
(2260cm-1
)
不再变化来证实反应完全
。
[0190]
实施例
8(
对比
)
:在半间歇式程序中以
5.7:1
的异氰酸酯基团对环氧基团的摩尔比用
ipdi
作为化合物
(a-i)
和用
ipox rd 3
作为化合物
(b-i)
使用
yb(otf)3(c-v)
作为化合物
(c)
和包含作为化合物
(d-i)
的
o-dcb
的溶剂混合物合成基于异氰酸酯封端的聚噁唑烷酮的组合物
。
[0191]
在如前所述的反应器中装入
yb(otf)3(1163mg,11406ppm)(c-v)。
随后添加
o-dcb(d-i)(25ml)
并搅拌
(400rpm)
混合物并用氮气
(
约
1ml/min)
吹扫
30
分钟
。
随后,将混合物加热至
175℃。
接着,在
30
分钟的时间范围内,使用注射泵以连续方式添加
ipox rd3(17.44g
,
0.066mol)(b-i)、ipdi(83.36g
,
0.375mol)(a-i)
和
o-dcb(11ml)(d-1)
的混合物
。
在单体的添加完成后,搅拌反应物并再加热
210
分钟,然后使反应混合物冷却至室温
。
[0192]
在反应过程中,取出反应混合物的样品并通过
ir
光谱法进行分析
。
通过观察到来自反应混合物的
ir
光谱中异氰酸酯带
(2260cm-1
)
不再变化来证实反应完全
。
[0193]
实施例9:在半间歇式程序中以
5.7:1
的异氰酸酯基团对环氧基团的摩尔比用
ipdi
作为化合物
(a-i)
和用
ipox rd 3
作为化合物
(b-i)
使用
tppcl(c-i)
作为化合物
(c)
和包含作为化合物
(d-i)
的
o-dcb
的溶剂混合物合成基于异氰酸酯封端的聚噁唑烷酮的组合物
。
[0194]
在如前所述的反应器中装入
tppcl(703mg,6924ppm)(c-i)。
随后添加
o-dcb(d-i)(25ml)
并搅拌
(400rpm)
混合物并用氮气
(
约
1ml/min)
吹扫
30
分钟
。
随后,将混合物加热至
175℃。
接着,在
30
分钟的时间范围内,使用注射泵以连续方式添加
ipox rd3(17.44g
,
0.066mol)(b-i)、ipdi(83.36g
,
0.375mol)(a-i)
和
o-dcb(11ml)(d-1)
的混合物
。
在单体的添加完成后,搅拌反应物并再加热
210
分钟,然后使反应混合物冷却至室温
。
[0195]
在反应过程中,取出反应混合物的样品并通过
ir
光谱法进行分析
。
通过观察到来自反应混合物的
ir
光谱中异氰酸酯带
(2260cm-1
)
不再变化来证实反应完全
。
[0196]
实施例
10
:在半间歇式程序中以
5.7:1
的异氰酸酯基团对环氧基团的摩尔比用
ipdi
作为化合物
(a-i)
和用
ipox rd 3
作为化合物
(b-i)
使用
tppbr(c-ii)
作为化合物
(c)
和包含作为化合物
(d-i)
的
o-dcb
的溶剂混合物合成基于异氰酸酯封端的聚噁唑烷酮的组合物
。
[0197]
在如前所述的反应器中装入
tppbr(786mg,7739ppm)(c-ii)。
随后添加
o-dcb(d-i)(25ml)
并搅拌
(400rpm)
混合物并用氮气
(
约
1ml/min)
吹扫
30
分钟
。
随后,将混合物加热至
175℃。
接着,在
30
分钟的时间范围内,使用注射泵以连续方式添加
ipox rd3(17.44g
,
0.066mol)(b-i)、ipdi(83.36g
,
0.375mol)(a-i)
和
o-dcb(11ml)(d-1)
的混合物
。
在单体的添加完成后,搅拌反应物并再加热
210
分钟,然后使反应混合物冷却至室温
。
[0198]
在反应过程中,取出反应混合物的样品并通过
ir
光谱法进行分析
。
通过观察到来自反应混合物的
ir
光谱中异氰酸酯带
(2260cm-1
)
不再变化来证实反应完全
。
[0199]
实施例
11
:在半间歇式程序中以
5.7:1
的异氰酸酯基团对环氧基团的摩尔比用
ipdi
作为化合物
(a-i)
和用
ipox rd 3
作为化合物
(b-i)
使用
tppi(c-iii)
作为化合物
(c)
和包含作为化合物
(d-i)
的
o-dcb
的溶剂混合物合成基于异氰酸酯封端的聚噁唑烷酮的组合物
。
[0200]
在如前所述的反应器中装入
tppi(874mg,8599ppm)(c-iii)。
随后添加
o-dcb(d-i)
(25ml)
并搅拌
(400rpm)
混合物并用氮气
(
约
1ml/min)
吹扫
30
分钟
。
随后,将混合物加热至
175℃。
接着,在
30
分钟的时间范围内,使用注射泵以连续方式添加
ipox rd3(17.44g
,
0.066mol)(b-i)、ipdi(83.36g
,
0.375mol)(a-i)
和
o-dcb(11ml)(d-1)
的混合物
。
在单体的添加完成后,搅拌反应物并再加热
210
分钟,然后使反应混合物冷却至室温
。
[0201]
在反应过程中,取出反应混合物的样品并通过
ir
光谱法进行分析
。
通过观察到来自反应混合物的
ir
光谱中异氰酸酯带
(2260cm-1
)
不再变化来证实反应完全
。
[0202]
实施例
12
:在半间歇式程序中以
4:1
的异氰酸酯基团对环氧基团的摩尔比用
ipdi
作为化合物
(a-i)
和用
ipox rd 3
作为化合物
(b-i)
使用
tppcl(c-i)
作为化合物
(c)
和包含作为化合物
(d-i)
的
o-dcb
的溶剂混合物合成基于异氰酸酯封端的聚噁唑烷酮的组合物
。
[0203]
在如前所述的反应器中装入
tppcl(703mg,6443ppm)(c-i)。
随后添加
o-dcb(d-i)(25ml)
并搅拌
(400rpm)
混合物并用氮气
(
约
1ml/min)
吹扫
30
分钟
。
随后,将混合物加热至
175℃。
接着,在
30
分钟的时间范围内,使用注射泵以连续方式添加
ipox rd3(25.03g
,
0.095mol)(b-i)、ipdi(83.36g
,
0.375mol)(a-i)
和
o-dcb(11ml)(d-1)
的混合物
。
在单体的添加完成后,搅拌反应物并再加热
210
分钟,然后使反应混合物冷却至室温
。
[0204]
在反应过程中,取出反应混合物的样品并通过
ir
光谱法进行分析
。
通过观察到来自反应混合物的
ir
光谱中异氰酸酯带
(2260cm-1
)
不再变化来证实反应完全
。
[0205]
实施例
13
:在半间歇式程序中以
3.3:1
的异氰酸酯基团与环氧基团的摩尔比用
ipdi
作为化合物
(a-i)
和用
ipox rd 3
作为化合物
(b-i)
使用
tppcl(c-i)
作为化合物
(c)
和包含作为化合物
(d-i)
的
o-dcb
的溶剂混合物合成基于异氰酸酯封端的聚噁唑烷酮的组合物
。
[0206]
在如前所述的反应器中装入
tppcl(703mg,6148ppm)(c-i)。
随后添加
o-dcb(d-i)(25ml)
并搅拌
(400rpm)
混合物并用氮气
(
约
1ml/min)
吹扫
30
分钟
。
随后,将混合物加热至
175℃。
接着,在
30
分钟的时间范围内,使用注射泵以连续方式添加
ipox rd3(30.26g
,
0.115mol)(b-i)、ipdi(83.36g
,
0.375mol)(a-i)
和
o-dcb(11ml)(d-1)
的混合物
。
在单体的添加完成后,搅拌反应物并再加热
210
分钟,然后使反应混合物冷却至室温
。
[0207]
在反应过程中,取出反应混合物的样品并通过
ir
光谱法进行分析
。
通过观察到来自反应混合物的
ir
光谱中异氰酸酯带
(2260cm-1
)
不再变化来证实反应完全
。
[0208]
实施例
14
:在半间歇式程序中以
2.2:1
的异氰酸酯基团对环氧基团的摩尔比用
ipdi
作为化合物
(a-i)
和用
ipox rd 3
作为化合物
(b-i)
使用
tppcl(c-i)
作为化合物
(c)
和包含作为化合物
(d-i)
的
o-dcb
的溶剂混合物合成基于异氰酸酯封端的聚噁唑烷酮的组合物
。
[0209]
在如前所述的反应器中装入
tppcl(703mg,5431ppm)(c-i)。
随后添加
o-dcb(d-i)(25ml)
并搅拌
(400rpm)
混合物并用氮气
(
约
1ml/min)
吹扫
30
分钟
。
随后,将混合物加热至
175℃。
接着,在
30
分钟的时间范围内,使用注射泵以连续方式添加
ipox rd3(45.35g
,
0.172mol)(b-i)、ipdi(83.36g
,
0.375mol)(a-i)
和
o-dcb(11ml)(d-1)
的混合物
。
在单体的添加完成后,搅拌反应物并再加热
210
分钟,然后使反应混合物冷却至室温
。
[0210]
在反应过程中,取出反应混合物的样品并通过
ir
光谱法进行分析
。
通过观察到来自反应混合物的
ir
光谱中异氰酸酯带
(2260cm-1
)
不再变化来证实反应完全
。
[0211]
实施例
15
:在半间歇式程序中以
8.7:1
的异氰酸酯基团对环氧基团的摩尔比用
ipdi
作为化合物
(a-i)
和用
ipox rd 3
作为化合物
(b-i)
使用
tppcl(c-i)
作为化合物
(c)
和包含作为化合物
(d-i)
的
o-dcb
的溶剂混合物合成基于异氰酸酯封端的聚噁唑烷酮的组合物
。
[0212]
在如前所述的反应器中装入
tppcl(703mg
,
7364ppm)(c-i)。
随后添加
o-dcb(d-i)(25ml)
并搅拌
(400rpm)
混合物并用氮气
(
约
1ml/min)
吹扫
30
分钟
。
随后,将混合物加热至
175℃。
接着,在
30
分钟的时间范围内,使用注射泵以连续方式添加
ipox rd3(11.38g
,
0.043mol)(b-i)、ipdi(83.36g
,
0.375mol)(a-i)
和
o-dcb(11ml)(d-1)
的混合物
。
在单体的添加完成后,搅拌反应物并再加热
210
分钟,然后使反应混合物冷却至室温
。
[0213]
在反应过程中,取出反应混合物的样品并通过
ir
光谱法进行分析
。
通过观察到来自反应混合物的
ir
光谱中异氰酸酯带
(2260cm-1
)
不再变化来证实反应完全
。
[0214]
实施例
16(
对比
)
:在半间歇式程序中以
36.3:1
的异氰酸酯基团与环氧基团的摩尔比用
ipdi
作为化合物
(a-i)
和用
ipox rd 3
作为化合物
(b-i)
使用
tppcl(c-i)
作为化合物
(c)
和包含作为化合物
(d-i)
的
o-dcb
的溶剂混合物合成基于异氰酸酯封端的聚噁唑烷酮的组合物
。
[0215]
在如前所述的反应器中装入
tppcl(703mg
,
8089ppm)(c-i)。
随后添加
o-dcb(d-i)(25ml)
并搅拌
(400rpm)
混合物并用氮气
(
约
1ml/min)
吹扫
30
分钟
。
随后,将混合物加热至
175℃。
接着,在
30
分钟的时间范围内,使用注射泵以连续方式添加
ipox rd3(2.73g
,
0.010mol)(b-i)、ipdi(83.36g
,
0.375mol)(a-i)
和
o-dcb(11ml)(d-1)
的混合物
。
在单体的添加完成后,搅拌反应物并再加热
210
分钟,然后使反应混合物冷却至室温
。
[0216]
在反应过程中,取出反应混合物的样品并通过
ir
光谱法进行分析
。
通过观察到来自反应混合物的
ir
光谱中异氰酸酯带
(2260cm-1
)
不再变化来证实反应完全
。
[0217]
实施例
17(
与实施例
09
一致
)
:在半间歇式程序中以
5.7:1
的异氰酸酯基团对环氧基团的摩尔比用
ipdi
作为化合物
(a-i)
和用
ipox rd 3
作为化合物
(b-i)
使用
tppcl(c-i)
作为化合物
(c)
和包含作为化合物
(d-i)
的
o-dcb
的溶剂混合物合成基于异氰酸酯封端的聚噁唑烷酮的组合物
。
经由薄膜蒸发从组合物中分离基于聚噁唑烷酮的预聚物
。
[0218]
在如前所述的反应器中装入
tppcl(703mg,6924ppm)(c-i)。
随后添加
o-dcb(d-i)(25ml)
并搅拌
(400rpm)
混合物并用氮气
(
约
1ml/min)
吹扫
30
分钟
。
随后,将混合物加热至
175℃。
接着,在
30
分钟的时间范围内,使用注射泵以连续方式添加
ipox rd3(17.44g
,
0.066mol)(b-i)、ipdi(83.36g
,
0.375mol)(a-i)
和
o-dcb(11ml)(d-1)
的混合物
。
在单体的添加完成后,搅拌反应物并再加热
210
分钟,然后使反应混合物冷却至室温
。
[0219]
在反应过程中,取出反应混合物的样品并通过
ir
光谱法进行分析
。
通过观察到来自反应混合物的
ir
光谱中异氰酸酯带
(2260cm-1
)
不再变化来证实反应完全
。
[0220]
通过除去未反应的单体和溶剂薄膜蒸发
(180℃
和
0.3mbar)
从组合物中分离基于异氰酸酯封端的聚噁唑烷酮的预聚物
。
[0221]
实施例
18(
对比
)
:在半间歇式程序中以
5.7:1
的异氰酸酯基团对环氧基团的摩尔比用
ipdi
作为化合物
(a-i)
和用
ipox rd 3
作为化合物
(b-i)
使用
sb(ph)3(c-ix)
与
i2(c-x)
的
1:2
摩尔混合物作为化合物
(c)
和包含作为化合物
(d-i)
的
o-dcb
的溶剂混合物合成基于异氰酸酯封端的聚噁唑烷酮的组合物
。
[0222]
在如前所述的反应器中装入
sb(ph)3(662mg
,
6460ppm)(c-ix)
和
i2(952mg
,
9294ppm)(c-x)。
随后添加
o-dcb(d-i)(25ml)
并搅拌
(400rpm)
混合物并用氮气
(
约
1ml/min)
吹扫
30
分钟
。
随后,将混合物加热至
175℃。
接着,在
30
分钟的时间范围内,使用注射泵以连续方式添加
ipox rd3(17.44g
,
0.066mol)(b-i)、ipdi(83.36g
,
0.375mol)(a-i)
和
o-dcb(11ml)(d-1)
的混合物
。
在单体的添加完成后,搅拌反应物并再加热
210
分钟,然后使反应混合物冷却至室温
。
[0223]
在反应过程中,取出反应混合物的样品并通过
ir
光谱法进行分析
。
通过观察到来自反应混合物的
ir
光谱中异氰酸酯带
(2260cm-1
)
不再变化来证实反应完全
。
[0224]
表1:比较实施例1至
18
的结果
。
[0225][0226]
对比
:
对比例
[0227]
a):
获得具有不溶性深色颗粒的多相反应混合物
。
[0228]
b):
在颜色数测量之前将预聚物溶解在
o-dcb(68
重量%固含量
)
中
。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1