与肿瘤相关抗原结合的多特异性抗体在治疗癌症时不引起或减少神经疼痛的制作方法
本发明涉及一种与肿瘤相关抗原结合的多特异性抗体,该抗体在治疗癌症时不引起或减少神经疼痛。
背景技术:
1、补体系统在先天性免疫反应和适应性免疫反应的相互作用中发挥着关键作用,从而达到破坏癌细胞的效果。有一种膜结合补体调节蛋白(mcrp),其包括例如cd55、cd46和cd59,它们在体内表达以实现对补体系统过度激活的抑制。然而,另一方面,mcrp也会过度调节补体系统,因此无法再破坏癌细胞。研究表明,在许多癌症类型中,mcrp可以作为恶性转化的生物标志物,因此在癌症治疗中应予以考虑。
2、肿瘤相关神经节苷脂gd2是免疫治疗的一个具有吸引力的靶点。虽然它在正常组织中的表达仅限于中枢神经系统和周围神经[1,2],但在神经母细胞瘤(nb)和大多数黑色素瘤病灶中可以强烈检测到[3,4]。此外,gd2还在肉瘤、神经胶质瘤以及约50-100%的小细胞肺癌(sclc)中被发现,在这些肿瘤中它与细胞增殖和侵袭活性的增强有关[5-7]。由于它在正常组织中表达有限,在神经母细胞瘤细胞上表达的gd2双唾液酸神经节苷脂原则上是mab治疗的极佳候选者。
3、许多在神经母细胞瘤中过表达的抗原在周围神经和/或其他神经组织中通常以较低水平存在[8-10]。因此,在开发抗gd2抗体时,一个重要的考虑因素为潜在的肿瘤外靶向毒性。由于抗gd2单克隆抗体与周围神经相互作用和补体系统的可能参与[15],会引起疼痛,需要连续输注麻醉药物进行镇痛[11-14]。
4、已获批准的抗体地努妥昔单抗(dinutuximab,17.5mg/m2/天),与gm-csf、il-2和ra联合使用时,具有显著的、相对可控的毒性特征。在关键性临床iii期试验(coganbl0032)中,该试验将地努妥昔单抗17.5mg/m2/天、gm-csf、il-2(3×106或4.5×106iu/m2/天)和ra与标准疗法(ra)进行了比较,接受地努妥昔单抗治疗的137名患者中,超过90%出现了与治疗相关的不良事件[16]。
5、与标准治疗组相比,接受地努妥昔单抗治疗的患者更常发生3级或4级毒性反应,包括疼痛(52%对6%)、过敏反应(25%对1%)、毛细血管渗漏综合征(23%对0%)和低血压(16%对0%)[12,26]。与地努妥昔单抗给药相关的疼痛通常是神经性的,最常影响腹部部位,并且最常发生在第1周期,在随后的周期中发生频率呈下降的趋势。
6、因此,人们越来越希望在肿瘤或癌症治疗过程中减轻或甚至消除神经疼痛。
7、发明和优选实施方案的详细描述
8、出于描述本发明和说明其优选实施方案的目的,包括以下讨论。
9、除非另有定义,否则本文中使用的所有技术术语和科学术语与本公开所属领域的普通技术人员所通常理解的含义相同。除非上下文另有明确指示,否则单数术语“一”、“一个”和“该”均包括复数指称。同样,“或”一词的本意也包括“和”,除非上下文另有明确说明。尽管与本文所述方法和材料类似或等效的方法和材料可用于本公开的实施或测试,但以下仍描述了合适的方法和材料。术语“包含”意为“包括”。本文提及的所有出版物、专利申请、专利和其他参考文献的全部内容均通过引用并入本文。如有冲突,以本说明书(包括术语解释)为准。另外,所述材料、方法和实施例仅为说明之用,并非旨在限定。
10、本发明涉及:
11、(1).一种完整的全igg双特异性抗体,其包含以下特性:
12、a)与t细胞结合;
13、b)与肿瘤细胞上的肿瘤相关抗原结合;
14、c)当抗体浓度小于500ng/ml时,无补体依赖性细胞毒性或仅有微弱的补体依赖性细胞毒性,从而避免神经疼痛。优选地,所述浓度是指受试者血液中抗体的浓度,和/或
15、所述双特异性抗体与肿瘤相关抗原的亲和力在kd=10-5-10-8m的范围内。
16、(2).(1)中所述的完整的双特异性抗体,其中双特异性抗体为针对每个靶向抗原的单价抗体。
17、(3).(1)或(2)中所述的完整的双特异性抗体,其中所述抗体为双特异性抗体,优选三功能双特异性抗体。
18、(4).优选地,(1)至(3)中任一项所述的完整的双特异性抗体,其中肿瘤相关抗原选自由肿瘤相关鞘脂和类鞘脂分子、神经节苷脂或葡糖鞘脂,例如gd2、gd3、gm1、gm2、gm3、岩藻糖基-gm1、globo-h、s1p、cer和gg3组成的组;优选地,肿瘤相关抗原为神经母细胞瘤相关抗原gd2。
19、(5).优选地,(1)至(4)中任一项所述的完整的双特异性抗体,其中所述完整的双特异性抗体通过t细胞表面抗原与t细胞结合,并且其中t细胞表面抗原选自由cd2、cd3、cd4、cd8、cd28、cd40l和cd44组成的组,优选地,t细胞表面抗原为cd3。
20、(6).优选地,(1)至(5)中任一项所述的完整的双特异性抗体,其中所述抗体包含fc部分,其中所述fc部分内的补体结合氨基酸通过取代、插入和缺失中的一种进行修饰。
21、(7).一种药物组合物,其包含(1)至(6)中任一项所述的完整的双特异性抗体。
22、(8).优选地,(7)中所述的药物组合物还包含药学上合适的载体。
23、(9).一种用作药物的完整的双特异性抗体,其中所述双特异性抗体为(1)至(8)中任一项所述的抗体。
24、(10).一种用于治疗神经母细胞瘤或肉瘤、黑色素瘤、神经胶质瘤、小细胞肺癌、乳腺癌、三阴性乳腺癌的完整的双特异性抗体,更优选用于治疗神经母细胞瘤、乳腺癌或三阴性乳腺癌,其中所述双特异性抗体为权利要求1至6中任一项所述的抗体。
25、(11).用于(9)或(10)的完整的双特异性抗体,其中所述抗体用于受试者,并且其中受试者为人,优选地,将所述抗体施用于所述受试者。
26、(12).用于(9)至(11)中任一项的完整的双特异性抗体,其中抗体可用作药物或用于治疗,但不会引起神经疼痛。
27、(13).优选地,用于(9)至(12)中任一项的完整的双特异性抗体,其中所述抗体与癌症干细胞或癌症干细胞样细胞结合。
28、(14).优选地,用于(9)至(13)中任一项的完整的双特异性抗体,其中所述抗体与乳腺癌干细胞或乳腺癌干细胞样细胞结合。
29、(15).优选地,用于(9)至(14)中任一项的完整的双特异性抗体,其中所述抗体与肿瘤、癌症、癌症干细胞或癌症干细胞样细胞表面表达的gd2结合。
30、(16).优选地,用于(9)至(15)中任一项的完整的双特异性抗体,其中所述双特异性抗体为抗gd2×抗cd3抗体。
31、(17).优选地,用于(9)至(16)中任一项的完整的双特异性抗体,其中所述完整的双特异性抗体以10μg/m2体表面积至10mg/m2体表面积以一次施用的量施用。
32、(18).优选地,用于(9)至(17)中任一项的完整的双特异性抗体,其中所述双特异性抗体在一个治疗周期施用2-12次,更优选在一个治疗周期施用4-10次,进一步更优选在一个治疗周期施用6-8次。
33、(19).优选地,用于(9)至(18)中任一项的完整的双特异性抗体,其中所述双特异性抗体通过静脉输注、腹腔内输注、肌肉注射、皮下注射或直接注射到肿瘤进行给药。
34、(20).用于(9)至(19)中任一项的完整的双特异性抗体,其中所述双特异性抗体的两次相邻给药的间隔为3-4天。
35、优选地,上述公开的完整的双特异性抗体为三功能双特异性抗体。
36、优选地,上述公开的完整的双特异性抗体可以是单价抗体、二价抗体、三价抗体、四价抗体或多价抗体。更优选地,所述抗体为三功能双特异性抗体。
37、优选地,上述公开的完整的双特异性抗体可以是单价抗体或二价抗体。所述单价结合特性可能与在抗体浓度小于100ng/ml时,更优选在抗体浓度小于500ng/ml时,无补体依赖性细胞毒性或仅有微弱的补体依赖性细胞毒性,以及更好地避免神经疼痛的效果相关。与所述单价抗体相比,二价抗体与肿瘤相关抗原具有相似的结合亲和力,这也与上述更好的预期效果有关。更优选地,所述抗体为三功能双特异性抗体。
38、优选地,本发明的单价双特异性抗体对抗原的亲和力比常规的二价抗体(例如常规的二价gd2特异性抗体)弱40-70倍,或对抗原的亲和力比常规的二价、三价、四价或多价抗体弱70-100倍。更优选地,所述抗体为三功能双特异性抗体。在这方面,术语“单价”是指与肿瘤相关抗原的结合。
39、在本发明中,术语“肿瘤细胞”是指任何能够不断分裂并形成实体瘤或使异常细胞充斥血液的细胞。优选地,在本发明中,肿瘤细胞可以来自上皮肿瘤、血液肿瘤或神经外胚层肿瘤。
40、本发明包括的肿瘤的实例包括但不限于肉瘤和癌,其包括纤维肉瘤、粘液肉瘤、脂肪肉瘤、软骨肉瘤、成骨肉瘤和其他肉瘤、滑膜瘤、间皮瘤、尤文氏瘤、平滑肌肉瘤、横纹肌肉瘤、结肠癌、淋巴恶性肿瘤、胰腺癌、乳腺癌(包括基底乳腺癌、导管癌和小叶乳腺癌以及三阴性乳腺癌和表达gd2的乳腺癌干细胞样细胞)、肺癌、卵巢癌、前列腺癌、肝细胞癌、鳞状细胞癌、基底细胞癌、腺癌、汗腺癌、甲状腺髓样癌、甲状腺乳头状癌、嗜铬细胞瘤、皮脂腺癌、乳头状癌、乳头状腺癌、髓样癌、支气管癌、肾细胞癌、肝癌、胆管癌、绒毛膜癌、肾母细胞瘤、宫颈癌、睾丸肿瘤、精原细胞瘤、膀胱癌和中枢神经系统肿瘤(例如神经胶质瘤、星形细胞瘤、髓母细胞瘤、颅咽管瘤、室管膜瘤、松果体瘤、血管母细胞瘤、听神经瘤、少突胶质细胞瘤、脑膜瘤、黑色素瘤、神经母细胞瘤和视网膜母细胞瘤)。其他例子包括上皮肿瘤、血液肿瘤、表达gd2的癌症干细胞和神经外胚层肿瘤。
41、优选地,本发明中的肿瘤为神经母细胞瘤。
42、优选地,在本发明中,所述肿瘤细胞来自上皮细胞、血液细胞、表达gd2的癌症干细胞或神经外胚层肿瘤。
43、在本发明中,“免疫细胞”包括t细胞和fc受体阳性细胞。在本发明中,“fc受体细胞”是指细胞表面存在fc受体的细胞。优选地,“fc受体阳性细胞”是指单核细胞、巨噬细胞、树突状细胞、自然杀伤细胞、中性粒细胞和嗜酸性细胞中的一种或多种。
44、在本发明中,所述完整的双特异性抗体能够形成所述抗体和所述肿瘤细胞的三维网络。在本发明的另一特别优选的实施方案中,所述抗体还能够与一个以上的肿瘤细胞和/或免疫细胞结合,以形成抗体、肿瘤细胞、任选的免疫细胞以及任选的其他肿瘤细胞的三维网络。
45、因此,本发明优选关注通过抗体特异性相互作用和涉及t细胞和/或fc受体阳性免疫细胞的免疫效应破坏所述肿瘤细胞来消除携带肿瘤相关抗原的肿瘤细胞。本发明优选地可从抗体能够交联抗原的能力中获益,在本示例中,所述抗原位于肿瘤细胞或其片段上。
46、优选地,本发明公开的抗体对肿瘤相关抗原表现出低亲和力至中等亲和力,更优选地kd值范围为10-5–10-8m。这种优选实施方案可以与在抗体浓度小于100ng/ml时,更优选在抗体浓度小于500ng/ml时,无补体依赖性细胞毒性或仅有微弱的补体依赖性细胞毒性,以及更好地避免神经疼痛的效果相关。更优选地,所述抗体为三功能双特异性抗体。
47、在本发明中,抗体与肿瘤相关抗原亲和力的测量方法与ruf等人在测量与gd2的结合力时所述的方法相同(journal of translational medicine,2012,10:219)。
48、优选地,本发明公开的抗体对gd2抗原表现出低亲和力至中等亲和力,更优选对gd2抗原表现出kd=10-5-10-8m范围内的亲和力。更优选地,所述抗体为三功能双特异性抗体。
49、优选地,本发明公开的抗体为单价抗体,对肿瘤相关抗原表现出低亲和力至中等亲和力,更优选地kd值范围为10-5–10-8m。这种优选实施方案可以与在抗体浓度小于100ng/ml时,更优选在抗体浓度小于500ng/ml时,无补体依赖性细胞毒性或仅有微弱的补体依赖性细胞毒性,以及更好地避免神经疼痛的效果相关。甚至更优选地,所述抗体为三功能双特异性抗体。在这方面,术语“单价”是指与肿瘤相关抗原的结合。
50、本文在本发明的限制范围内对完整的双特异性抗体进行了描述以及权利要求,并以抗cd3×抗gd2的双特异性抗体(ektomun)为例进行了说明。所述抗cd3×抗gd2双特异性抗体靶向肿瘤相关抗原gd2,此外还与t细胞表面抗原cd3结合,并通过其fc部分与fc受体阳性细胞结合。
51、本文在本发明的限制范围内对完整的双特异性抗体进行了描述以及权利要求,并以抗cd3×抗epcam的双特异性抗体(catumaxomab)为例进行了说明。所述抗cd3×抗epcam双特异性抗体靶向肿瘤相关抗原epcam,此外还与t细胞表面抗原cd3结合,并通过其fc部分与fc受体阳性细胞结合。
52、在示例中描述的具体实施方案应理解为示例性实施方案,它们为本发明的可行性提供了证据。提供了这一证据后,本领域技术人员将不可避免地具有将该概念扩展到本发明所涵盖的其他肿瘤和其他抗体的可能性,只要它们能够与所述肿瘤细胞以及任选的所述免疫细胞相互作用以提供三维网络。
53、本发明的抗体为双特异性抗体。然而,如果三特异性、四特异性和多特异性抗体也表现出相同的特性或效果,则所述双特异性抗体也可以指如本文所用的三特异性、四特异性和多特异性抗体。
54、本发明的抗体优选自三功能抗体。下文公开的三功能抗体是指三功能双特异性抗体。然而,如果三特异性、四特异性和多特异性抗体也表现出相同的特性或效果,则所述三功能抗体也可以指如本文所用的三功能三特异性、四特异性和多特异性抗体。
55、一般而言,双特异性抗体被定义为能够优选地通过其可变区与两种不同类型的抗原结合的抗体;三特异性抗体的特征在于优选地通过其可变区与三种不同类型的抗原结合;四特异性抗体的特征在于优选地通过其可变区与四种不同类型的抗原结合;多特异性抗体被定义为能够优选地通过其可变区与多种不同类型的抗原结合。作为一个具体的实施例,所述三功能双特异性抗体抗cd3×抗epcam被定义为一方面与肿瘤相关抗原epcam结合,另一方面与t细胞表面抗原cd3结合,且通过其fc部分与辅助细胞结合的抗体。作为另一具体的实施例,所述三功能双特异性抗体抗cd3×抗gd2被定义为一方面与肿瘤相关抗原gd2结合,另一方面与t细胞表面抗原cd3结合,且通过其fc部分与辅助细胞结合的抗体。
56、一般而言,上述二、三、四和多特异性抗体可以是单价抗体、二价抗体、三价抗体、四价抗体或多价抗体。
57、具有单价结合特性的抗体被定义为能与一种肿瘤相关抗原结合的抗体。二价单克隆抗体被定义为能够结合两种肿瘤相关抗原或一种肿瘤相关抗原和一种免疫细胞相关抗原的抗体。三价单克隆抗体被定义为能够结合三种不同肿瘤相关抗原,或两种肿瘤相关抗原和一种免疫细胞相关抗原,或一种肿瘤相关抗原和两种免疫细胞相关抗原的抗体。四价单克隆抗体被定义为能够结合四种不同的肿瘤相关抗原,或两种不同的肿瘤相关抗原(每种抗原均具有两个相同的抗原结合臂),或两/三种肿瘤相关抗原和一种免疫细胞相关抗原,或两种肿瘤相关抗原和两种免疫细胞相关抗原的抗体。多价单克隆抗体被定义为能够结合一种或多种肿瘤相关抗原和/或一种或多种免疫细胞相关抗原的抗体。术语“与肿瘤相关抗原结合”被定义为与肿瘤细胞上所述肿瘤相关抗原的表位结合。
58、kontermann re(ed.)springer heidelberg dordrecht london new york,pp.1-28(2011)一文总体描述了具有双特异性或三特异性(具有二价、三价和四价的三功能构型)的双功能或三功能抗体,这些抗体可以与一种肿瘤相关抗原以及白细胞(即免疫系统的细胞)的一种或多种表面抗原结合,这对于本专利申请是重要的。
59、·具有二价抗原结合特征的双特异性抗体构型:
60、例如,scfv(例如bite类)、db、scdb、dsdb、dart、dab2/vhh2)、旋钮入孔衍生物、seed-igg、heterofc-scfv、fab-scfv和crossmabs。
61、·具有三价抗原结合特征的双(三)特异性抗体构型:
62、例如:三联体、dnl-f(ab)3、scfv2-ch1/cl、dab3、fab-scfv2、igg-scfab
63、·具有四价抗原结合特征的双(三)特异性抗体构型:
64、例如igg-scfv、scfv-igg、scfv-fc、f(ab')2-scfv2、sdb-fc、scdb-ch3、db-fc、scfv2-h/l、dvd-ig、tandab、scfv-dhlx-scfv、dab2-igg、二合一mab、mab2、dab-igg、dab-fc-dab。
65、在以下参考文献中描述了根据本发明使用的其他抗体:
66、müller d and re kontermann.in:bispecific antibodies.kontermann re(ed.),springer heidelberg dordrecht london new york,pp.83-100(2011)
67、scfv(bite)
68、baeuerle pa,zugmaier g and d rüttinger.in:bispecificantibodies.kontermann re(ed.),springer heidelberg dordrecht london new york,pp.273-288(2011)
69、dvd-ig
70、tarcsa e,fraunhofer w,ghayur t,salfeld j and j gu.in:bispecificantibodies.kontermann re(ed.),springer heidelberg dordrecht london new york,pp.171-186(2011)
71、dnl-衍生物
72、chang c-h,rossi ea,sharkey rm,dm goldenberg.in:bispecificantibodies.kontermann re(ed.),springer heidelberg dordrecht london new york,pp.199-216(2011)
73、二合一抗体
74、koeing p and g fuh.in:bispecific antibodies.kontermann re(ed.),springer heidelberg dordrecht london new york,pp.187-198(2011)
75、crossmabs
76、schaefer等人.proc.natl.acad.sci.usa 108:11187(2011)
77、在本发明中,使用至少一种双特异性抗体,优选使用三功能双特异性抗体。优选地,可以将两种或多种具有不同特异性的所述双特异性抗体组合起来,用于介导肿瘤细胞与免疫细胞的结合。
78、优选地,本发明的双特异性抗体用于治疗癌症,其中所述抗体结合癌症干细胞或癌症干细胞样细胞。在这方面,“癌症干细胞”是指表现出与正常干细胞相关的特征的癌细胞,特别是能够产生特定癌症样本中发现的所有细胞类型。此外,“癌症干细胞样细胞”是指具有升高的肿瘤起始或癌症起始潜能的肿瘤或癌细胞亚群。更优选地,所述抗体为三功能双特异性抗体。
79、优选地,本发明的双特异性抗体用于治疗神经母细胞瘤、乳腺癌或三阴性乳腺癌。在这方面,三阴性乳腺癌是指雌激素受体、孕激素受体和her2蛋白过表达的检测结果均为阴性的癌症。更优选地,所述抗体为三功能双特异性抗体。
80、优选地,本发明中的双特异性抗体用于治疗乳腺癌或三阴性乳腺癌,其中所述抗体与乳腺癌干细胞或癌症干细胞样细胞结合。更优选地,所述抗体为三功能双特异性抗体。
81、优选地,gd2在上述癌症干细胞或癌症干细胞样细胞中表达。
82、优选地,gd2在上述乳腺癌干细胞或乳腺癌干细胞样细胞中表达。
83、优选地,本发明的双特异性抗体以10μg/m2体表面积至10mg/m2体表面积的剂量用于一次给药,或10μg/m2体表面积至800μg/m2体表面积的剂量用于一次给药,或10μg/m2体表面积至500μg/m2体表面积的剂量用于一次给药,或10μg/m2体表面积至200μg/m2体表面积的剂量用于一次给药,或10μg/m2体表面积至100μg/m2体表面积的剂量用于一次给药,或10μg/m2体表面积至50μg/m2体表面积的剂量用于一次给药,或800μg/m2体表面积至1mg/m2体表面积的剂量用于一次给药,或1mg/m2体表面积至2mg/m2体表面积的剂量用于一次给药,或2mg/m2体表面积至4mg/m2体表面积的剂量用于一次给药,或4mg/m2体表面积至6mg/m2体表面积的剂量用于一次给药,或6mg/m2体表面积至8mg/m2体表面积的剂量用于一次给药,或8mg/m2体表面积至10mg/m2的剂量用于一次给药。更优选地,所述抗体为三功能双特异性抗体。
84、在本发明中,通过在上述范围内使用所述双特异性抗体可以实现甚至更好的抗癌效果。
85、在本发明中,通过使用上述范围内的所述双特异性抗体,在抗体浓度小于100ng/ml时、更优选在抗体浓度小于500ng/ml时,可以实现无补体依赖性细胞毒性或仅有微量补体依赖性细胞毒性的更好效果,并且可以更好地避免神经疼痛。
86、优选地,患者血液中的抗体浓度应控制在小于100ng/ml的范围内,更优选在小于500ng/ml的范围内。甚至更优选地,所述抗体为三功能双特异性抗体。
87、优选地,患者血液中的抗体浓度控制在40ng/ml至80ng/ml、40ng/ml至120ng/ml、40ng/ml至160ng/ml、40ng/ml至200ng/ml、40ng/ml至240ng/ml、80ng/ml至240ng/ml、120ng/ml至240ng/ml、160ng/ml至240ng/ml、200ng/ml至240ng/ml、80ng/ml至200ng/ml或120ng/ml至160ng/ml的范围内。由于使用的抗体量较低,而且在患者血液中测得的抗体浓度也较低,减少量的抗体可能与靶细胞结合以启动补体级联反应,例如通过将c1q与细胞结合性抗体结合。更优选地,所述抗体为三功能双特异性抗体。
88、在本发明中,通过在上述范围内使用所述双特异性抗体可以实现甚至更好的抗癌效果。
89、在本发明中,通过使用上述范围内的所述双特异性抗体,在抗体浓度小于100ng/ml时、更优选在抗体浓度小于500ng/ml时,可以实现无补体依赖性细胞毒性或仅有微量补体依赖性细胞毒性的更好效果,并且可以更好地避免神经疼痛。这可能归因于这样的事实:所述范围会导致靶细胞上结合的抗体减少,从而不会启动补体级联反应。
90、优选地,在本发明使用的双特异性抗体中,所述双特异性抗体在一个治疗周期向患者施用2-12次,更优选地在一个治疗周期施用4-10次,进一步更优选地在一个治疗周期施用6-8次。所述抗体可以为三功能双特异性抗体。在这方面,可以在不引起副作用的情况下实现治疗效果。
91、优选地,所述双特异性抗体的两次相邻给药的间隔为3-4天。事实证明,所述间隔与改善的治疗效果有关。所述抗体可以为三功能双特异性抗体。在这方面,可以在不引起副作用的情况下实现治疗效果。
92、根据本发明,所述治疗在两个或多个治疗周期中进行。一个治疗周期被定义为一系列的后续给药。应当理解的是,本文所用的术语“治疗周期”还包括一系列后续用药(至少两次),其中两次后续用药之间的时间间隔优选为3-4天。这些后续用药形成一个治疗周期,该治疗周期与下一个治疗周期之间的间隔时间大大长于一个治疗周期内两次后续用药之间的时间间隔。
93、两个治疗周期彼此的时间间隔优选1-6个月、更优选1-3个月。
94、优选地,所述双特异性抗体对患者施用1-10个治疗周期,优选1-6个治疗周期,更优选1-4个治疗周期,甚至更优选2-4个治疗周期。
95、优选地,本发明公开的抗体包含经工程化的fc部分,其中fc部分内的补体结合氨基酸被删除,这可能与在抗体浓度小于1000ng/ml时,优选小于500ng/ml时,时无补体依赖性细胞毒性或仅有微量补体依赖性细胞毒性的更好效果,以及更好地避免神经疼痛相关。
96、本发明的双特异性抗体可通过选自由cd2、cd3、cd4、cd8、cd28、cd40l和cd44组成的组中的t细胞表面抗原与t细胞结合。这意味着,根据本发明使用的抗体优选包含能够识别并结合选自由cd2、cd3、cd4、cd8、cd28、cd40l和cd44组成的组中的t细胞表面抗原的表位的互补位。优选地,该特异性可促进t细胞的募集。
97、优选地,t细胞表面抗原为cd3。这意味着,根据本发明使用的抗体进一步优选包含能识别并结合cd3的表位的互补位。
98、卡妥索抗体(catumaxomab)为一种双特异性抗体的示例,通过其两个特异性结合位点结合epcam阳性肿瘤细胞和cd3阳性t细胞。卡妥索抗体还可通过其完整的可结晶片段(fc)区域的结合募集fcγri、iia和iii型阳性辅助细胞,从而产生三功能作用模式。除了卡妥索抗体在本发明中使用时的作用模式外,还描述了由双特异性三功能抗体诱导的肿瘤细胞破坏的几种机制。
99、zeidler等人[53],[54],[55]和riechelmann等人[36]在以下所列文献阐明,双特异性抗体biuii(卡妥索抗体的变体抗体)和卡妥索抗体在体外激活t细胞和辅助细胞,以及促进它们杀死肿瘤细胞。将该三功能抗体和外周血单核细胞(pbmcs)一起使用,结果表明辅助细胞的激活是抗肿瘤活性的重要贡献因素。t细胞和辅助细胞被激活后会产生细胞因子(白细胞介素[il]-1β、il-2、il-6、il-12、tnf-ɑ、干扰素-γ[ifn-γ]和趋化因子(c-c基序)配体18[ccl18])。值得注意的是,riechelmann等人证明,ifn-γ在5小时内达到峰值,tnf-ɑ在24小时内达到峰值。他们还证明了树突状细胞和nk细胞上激活标志物的上调。卡妥索抗体不与b淋巴细胞结合,而是刺激fcγr阳性辅助细胞通过直接吞噬作用消灭肿瘤细胞。
100、[53]zeidler r,mayer a,gires o,et al.tnf-alpha contributes to theanti-tumor activity of a bispecific,trifunctional antibody.anticancerres.2001;21(5):3499-3503.
101、[54]zeidler r,mysliwietz j,csanady m,et al.the fc-region of a newclass of intact bi-specific antibody mediates activation of accessory cellsand nk cells and induces direct phagocytosis of tumor cells.br j cancer.2000;83(2):261-266.
102、[55]zeidler r,reisbach g,wollenberg b,et al.simultaneous activationof t-cells and accessory cells by a new class of intact bi-specific antibodyresults in efficient tumor cell killing.j immunol 1999;163(3):1246-1252.
103、[36]riechelmann h,wiesneth m,schauwecker p,et al.adoptive therapy ofhead and neck squamous cell carcinoma with antibody coated immune cells:apilot clinical trial.cancer immunol immunother.2007;56(9):1397-1406.
104、[1]abbas ak,lichtman ah.general properties of cytokines.in:cellularand molecular immunology.5th edition.philadephia,pennsylvania:saunders,imprint of elsevier;2003:section iv.
105、在一个优选的实施方案中,本发明中使用的抗体为单克隆抗体。对于本文详细公开的双特异性抗体来说尤其如此。
106、具有相对明确的三维结构的蛋白质通常被称为蛋白质支架。这些蛋白质支架可用作设计人工工程抗体的试剂。这些支架通常包含一个或多个可进行特定或随机序列变异的区域,这种序列随机化通常是为了产生蛋白质文库,从中可以选择所需的抗体支架。这种支架在抗体设计领域尤其有用。
107、这些抗体支架为非免疫球蛋白蛋白,其在与例如肿瘤细胞和免疫细胞等的结合活性方面模拟单克隆抗体的特性。支架通常包括形成所述抗体支架结合面的环或结构域。这些抗体模拟物可用于设计能与几乎任何感兴趣的化合物结合的蛋白质。这种定向进化方法导致产生对感兴趣的抗原具有高亲和力的抗体样分子。此外,这些支架可用于展示特定的暴露环(例如,先前随机化并基于抗原结合选择的环),以直接引导与此类引入环结合的分子的进化。如何获得抗体样支架蛋白的方法是本领域已知的。下文介绍一种获得抗体样支架蛋白的可行方法。
108、第一种筛选方法可用于分离或鉴定随机或突变的感兴趣的蛋白质,包括(a)将感兴趣的化合物与候选蛋白相互接触,该候选蛋白为包括具有免疫球蛋白样折叠结构域的衍生非抗体蛋白,该非抗体蛋白通过具有突变的氨基酸序列而衍生自参考蛋白,其中该非抗体蛋白以至少为1μm的kd与未与参考蛋白紧密结合的化合物结合,其中接触是在允许化合物-蛋白复合物形成的条件下进行的;(b)从复合物中获得与该化合物结合的衍生蛋白。
109、第二种筛选方法用于分离或鉴定与感兴趣的肿瘤相关蛋白结合的化合物。该方法从非抗体蛋白开始,该非抗体蛋白包括具有免疫球蛋白样折叠的结构域,该非抗体蛋白通过具有突变的氨基酸序列而衍生自参考蛋白,其中该非抗体蛋白以至少为1μm的kd与未与参考蛋白紧密结合的化合物结合。然后将这种衍生物蛋白与候选化合物(肿瘤相关抗原或其表位)接触,其中接触是在允许化合物-蛋白复合物形成的条件下进行的,并从复合物中获得与衍生物蛋白结合的化合物。同样,该通用技术可用于任何蛋白质。
110、以下描述了获取与感兴趣化合物(肿瘤相关抗原或其表位)结合的非抗体蛋白的进一步方法。其中一种方法包括:(a)提供包括免疫球蛋白样折叠的非抗体支架蛋白,其中支架蛋白不与kd小于1μm的化合物结合;(b)产生非抗体支架蛋白的突变衍生物,从而产生突变蛋白文库;(c)将该蛋白文库与化合物接触;(d)从蛋白库中选择至少一种与化合物结合的衍生物蛋白,其kd至少为1μm;以及(e)任选地重复步骤(b)-(d),用上一步骤(d)的产物代替重复步骤(b)中的非抗体支架蛋白。同样,该通用技术可用于任何蛋白质。
111、如此产生的支架蛋白可以模拟上文和下文所公开的抗体的功能,既可以代替基于免疫球蛋白的抗体使用,也可以与之组合使用。
112、优选地,本发明的fc部分与补体因子的补体结合率很低或没有补体结合,这可能与抗体浓度小于1000ng/ml时,更优选抗体浓度小于500ng/ml时,无补体依赖性细胞毒性或仅有微弱的补体依赖性细胞毒性,以及更好地避免神经疼痛有关。
113、优选地,上述补体因子可以是fc受体或补体蛋白成分1q(c1q)。
114、一般而言,抗体可包括一个fc部分,该部分可通过i、ii和iii型fcγ受体与fc受体阳性细胞结合,所述fc部分可包括至少一个与所述i、ii和/或iii型fc受体结合的位点。
115、优选地,本发明中使用的抗体包含fc部分,其中所述fc蛋白中的补体结合氨基酸通过氨基酸的取代、插入或缺失中的一种或其组合进行修饰。在这方面,在抗体浓度小于100ng/ml时、更优选在抗体浓度小于500ng/ml时,可以实现无补体依赖性细胞毒性或仅有微量补体依赖性细胞毒性的更好效果,并且可以更好地避免神经疼痛。
116、优选地,上述fc部分的补体结合氨基酸包含ellggp基序(seq id no:1),更优选e233 l234 l235 g236 g237 p238基序、eflggp基序(seq id no:2),更优选e233f234 l235g236 g237 p238基序,或pvaggp基序(seq id no:3),更优选p233 v234a235 g236 g237p238基序。所述基序序列e233 l234 l235 g236 g237 p238、e233 f234l235 g236 g237p238和p233 v234 a235 g236 g237 p238由john d.issacs等人公开。(j immunol,1998,161,第3862-3869页),有关所述序列的基本信息请参阅john d.issacs等人的所述出版物。
117、优选地,上述fc部分的ellggp基序,更优选e233 l234 l235 g236 g237 p238基序,通过氨基酸的取代、插入或缺失中的一种或其组合进行修饰,其中包含所述fc部分的抗体优选为人igg1或igg3抗体。在这方面,在抗体浓度小于100ng/ml时、更优选在抗体浓度小于500ng/ml时,可以实现无补体依赖性细胞毒性或仅有微量补体依赖性细胞毒性的更好效果,并且可以更好地避免神经疼痛。
118、优选地,上述fc部分的eflggp基序,更优选上述fc部分的e233 f234 l235g236g237 p238基序,通过氨基酸的取代、插入或缺失中的一种或其组合进行修饰,其中包含所述fc部分的抗体优选为人igg4抗体。在这方面,在抗体浓度小于100ng/ml时、更优选在抗体浓度小于500ng/ml时,可以实现无补体依赖性细胞毒性或仅有微量补体依赖性细胞毒性的更好效果,并且可以更好地避免神经疼痛。
119、优选地,上述fc部分的pvaggp基序,更优选上述fc部分的p233 v234 a235g236g237 p238基序,通过氨基酸的取代、插入或缺失中的一种或其组合进行修饰,其中包含所述fc部分的抗体优选为人igg2抗体。在这方面,在抗体浓度小于100ng/ml时、更优选在抗体浓度小于500ng/ml时,可以实现无补体依赖性细胞毒性或仅有微量补体依赖性细胞毒性的更好效果,并且可以更好地避免神经疼痛。
120、优选地,包含上述修饰的fc部分的抗体为小鼠igg1-igg4或人igg1-igg4抗体。在这方面,在抗体浓度小于100ng/ml时、更优选在抗体浓度小于500ng/ml时,可以实现无补体依赖性细胞毒性或仅有微量补体依赖性细胞毒性的更好效果,并且可以更好地避免神经疼痛。
121、优选地,fc部分的上述seq id no:1或seq id no:2基序的ell或efl被取代修饰,更优选地,上述基序的e233 l234 l235或e233 f234 l235被取代修饰,其中被取代的基序优选为pva(seq id no:4),更优选地,被取代的基序为e233p l234v l235a或e233p f234vl235a。在这方面,在抗体浓度小于100ng/ml时、更优选在抗体浓度小于500ng/ml时,可以实现无补体依赖性细胞毒性或仅有微量补体依赖性细胞毒性的更好效果,并且可以更好地避免神经疼痛。
122、优选地,本发明使用的抗体包含fc部分,其显示出与c1q相当低的补体结合或无补体结合,这可能与抗体浓度小于100ng/ml时,更优选抗体浓度小于500ng/ml时,无补体依赖性细胞毒性或仅有微弱的补体依赖性细胞毒性的更好效果,以及更好地避免神经疼痛有关。
123、优选地,本发明中使用的抗体可包含p329位的取代或缺失,或邻近所述p329位的插入,这可能与在抗体浓度小于100ng/ml时,更优选抗体浓度小于500ng/ml时,无补体依赖性细胞毒性或仅有微弱的补体依赖性细胞毒性的更好效果,以及更好地避免神经疼痛有关。所述p329位由tilman schlothauer等人公开。(protein engineering,design&selection,2016,vol.29,no.10,page 457-466),有关所述p329的基本信息请参阅tilmanschlothauer等人的所述出版物。
124、优选地,本发明中使用的抗体可包含p329位的取代或缺失,或在邻近所述p329位进行插入,这可使抗体的fc部分显示出与c1q相当低的补体结合或无补体结合。
125、优选地,本发明中使用的抗体可包含p329a位或p329g位的取代,更优选p329g位,这可能与抗体浓度小于100ng/ml时,更优选抗体浓度小于500ng/ml时,无补体依赖性细胞毒性或仅有微弱的补体依赖性细胞毒性的更好效果,以及更好地避免神经疼痛有关。
126、优选地,本发明中使用的抗体可包含p329a位或p329g位的取代,更优选p329g位,这可使抗体的fc部分显示出与c1q相当低的补体结合或无补体结合。
127、优选地,所述p329位的取代或缺失,或在邻近所述p329位的所述插入,与上述ellggp、eflggp或pvaggp基序组合存在,更优选地,与上述e233 l234 l235 g236g237 p238基序、e233 f234 l235 g236 g237 p238基序或p233 v234 a235 g236 g237p238基序组合存在。
128、优选地,所述p329位的取代或缺失,或在邻近所述p329位的所述插入,与上述e233l234 l235或e233 f234 l235的取代组合存在。
129、优选地,所述p329位的取代或缺失,或在邻近所述p329位的所述插入,与上述l234a l235a的取代组合存在。
130、优选地,所述p329a位或p329g位的取代或缺失,更优选p329g,与ellggp、eflggp或pvaggp基序组合存在,更优选地,与上述e233 l234 l235 g236 g237 p238基序、e233 f234l235 g236 g237 p238基序或p233 v234 a235 g236 g237 p238基序组合存在。
131、优选地,所述p329a位或p329g位的取代,更优选p329g位,与上述e233 l234l235或e233 f234 l235的取代组合存在。
132、优选地,所述p329a位或p329g位的取代,更优选p329g位,与上述l234 l235的取代组合存在。
133、优选地,本发明公开的抗体为单价抗体,对肿瘤相关抗原表现出低亲和力至中等亲和力,更优选地kd值范围为10-5–10-8m,并包含具有上述公开的任何一种修饰的fc蛋白。该优选的实施方案可能与在抗体浓度小于100ng/ml时,更优选在抗体浓度小于500ng/ml时,无补体依赖性细胞毒性或仅有微弱的补体依赖性细胞毒性方面甚至更进一步改善的效果,以及更好地避免神经疼痛相关。
134、优选地,根据本发明使用的抗体能够与作为fc受体阳性的单核细胞、巨噬细胞、树突状细胞、自然杀伤细胞、中性粒细胞和/或嗜酸性粒细胞结合。
135、在本发明中,肿瘤相关抗原是指肿瘤细胞中产生并在肿瘤细胞表面表达的抗原物质。
136、优选地,双特异性抗体结合的肿瘤相关抗原选自由肿瘤相关鞘脂和类鞘脂分子、神经节苷脂或葡糖鞘脂,例如gd2、gd3、gm1、gm2、gm3、岩藻糖基-gm1、globo-h、s1p、cer和gg3组成的组;优选地,肿瘤相关抗原为神经母细胞瘤相关抗原gd2。
137、优选地,双特异性抗体结合的肿瘤相关抗原选自由肿瘤相关鞘脂和类鞘脂分子、神经节苷脂或葡糖鞘脂,例如gd2、gd3、gm1、gm2、gm3、岩藻糖基-gm1、globo-h、s1p、cer和gg3组成的组;优选地,肿瘤相关抗原为神经母细胞瘤相关抗原gd2。
138、优选地,双特异性抗体结合肿瘤相关鞘脂和类鞘脂分子(例如神经节苷脂),其在癌症治疗中不引起或减轻神经疼痛。
139、优选地,双特异性抗体结合肿瘤相关鞘脂和类鞘脂分子(如神经节苷脂),其在癌症治疗中不引起或减轻神经疼痛。
140、优选地,所述肿瘤相关抗原为神经母细胞瘤相关抗原gd2,其与在抗体浓度小于100ng/ml时,更优选在抗体浓度小于500ng/ml时,无补体依赖性细胞毒性或仅有微弱的补体依赖性细胞毒性的更好效果,以及更好地避免神经疼痛相关。这可能归因于本发明公开的抗体与gd2结合位点的单价结合。
141、优选地,本发明的双特异性抗体靶向一种t细胞表面抗原和一种肿瘤相关抗原,其中t细胞表面抗原可选自由cd2、cd3、cd4、cd8、cd28、cd40l和cd44组成的组,其可以与任何选自由肿瘤相关鞘脂和类鞘脂分子,神经节苷脂或葡糖鞘脂,例如gd2、gd3、gm1、gm2、gm3、岩藻糖基-gm1、globo-h、s1p、cer和gg3组成的组中的肿瘤相关抗原组合,优选地,肿瘤相关抗原为神经母细胞瘤相关抗原gd2。
142、优选地,本发明的双特异性抗体靶向一种t细胞表面抗原和一种肿瘤相关抗原,其中t细胞表面抗原可选自由cd2、cd3、cd4、cd8、cd28、cd40l和cd44组成的组,其可以与任何选自由肿瘤相关鞘脂和类鞘脂分子,神经节苷脂或葡糖鞘脂,例如gd2、gd3、gm1、gm2、gm3、岩藻糖基-gm1、globo-h、s1p、cer和gg3组成的组中的肿瘤相关抗原组合,优选地,所述肿瘤相关抗原为神经母细胞瘤相关抗原gd2。
143、优选地,本发明的双特异性抗体靶向一种t细胞表面抗原cd3和一种肿瘤相关抗原gd2。
144、优选的抗体为异源双特异性抗体,优选为单克隆抗体,可选自以下同种型抗体组合中的一种或多种:
145、·大鼠-igg2b/小鼠-igg2a、
146、·大鼠-igg2b/小鼠-igg2b、
147、·大鼠-igg2b/小鼠-igg3;
148、·大鼠-igg2b/人-igg1、
149、·大鼠-igg2b/人-igg2
150、·大鼠-igg2b/人-igg3[东方同种异型g3m(st)=与蛋白a结合],
151、大鼠-igg2b/人-igg4;
152、·大鼠-igg2b/大鼠-igg2c;
153、·小鼠-igg2a/人-igg3[高加索同种异型g3m(b+g)=与蛋白a无结合,以下标注为*]
154、·小鼠-igg2a/小鼠-[vh-ch1,vl-cl]-人-igg1-[铰链]-人-igg3*-[ch2-ch3]
155、·小鼠-igg2a/大鼠-[vh-ch1,vl-cl]-人-igg1-[铰链]-人-igg3*-[ch2-ch3]
156、·小鼠-igg2a/人-[vh-ch1,vl-cl]-人-igg1-[铰链]-人-igg3*-[ch2-ch3]
157、·小鼠-[vh-ch1,vl-cl]-人-igg1/大鼠-[vh-ch1,vl-cl]-人-igg1-[铰链]-人-igg3*-[ch2-ch3]
158、·小鼠-[vh-ch1,vl-cl]-人-igg4/大鼠-[vh-ch1,vl-cl]-人-igg4-[铰链]-人-igg4[ch2的n末端区域]-人-igg3*[ch2的c末端区域:>aa位点251]-人-igg3*[ch3]
159、·大鼠-igg2b/小鼠-[vh-ch1,vl-cl]-人-igg1-[铰链-ch2-ch3]
160、·大鼠-igg2b/小鼠-[vh-ch1,vl-cl]-人-igg2-[铰链-ch2-ch3]
161、·大鼠-igg2b/小鼠-[vh-ch1,vl-cl]-人-igg3-[铰链-ch2-ch3,东方同种异型]
162、·大鼠-igg2b/小鼠-[vh-ch1,vl-cl]-人-igg4-[铰链-ch2-ch3]
163、·人-igg1/人-[vh-ch1,vl-cl]-人-igg1-[铰链]-人-igg3*-[ch2-ch3]
164、·人-igg1/大鼠-[vh-ch1,vl-cl]-人-igg1-[铰链]-人-igg4[ch2的n末端区域]-人-igg3*[ch2的c末端区域:>aa位点251]-人-igg3*[ch3]
165、·人-igg1/小鼠-[vh-ch1,vl-cl]-人-igg1-[铰链]-人-igg4[ch2的n末端区域]-人-igg3*[ch2的c末端区域:>aa位点251]-人-igg3*[ch3]
166、·人-igg1/大鼠-[vh-ch1,vl-cl]-人-igg1-[铰链]-人-igg2[ch2的n末端区域]-人-igg3*[ch2的c末端区域:>aa位点251]-人-igg3*[ch3]
167、人-igg1/小鼠-[vh-ch1,vl-cl]-人-igg1-[铰链]-人-igg2[ch2的n末端区域]-人-igg3*[ch2的c末端区域:>aa位点251]-人-igg3*[ch3]
168、·人-igg1/大鼠-[vh-ch1,vl-cl]-人-igg1-[铰链]-人-igg3*-[ch2-ch3]
169、·人-igg1/小鼠-[vh-ch1,vl-cl]-人-igg1-[铰链]-人-igg3*-[ch2-ch3]
170、·人-igg2/人-[vh-ch1,vl-cl]-人-igg2-[铰链]-人-igg3*-[ch2-ch3]
171、·人-igg4/人-[vh-ch1,vl-cl]-人-igg4-[铰链]-人-igg3*-[ch2-ch3]
172、·人-igg4/人-[vh-ch1,vl-cl]-人-igg4-[铰链]-人-igg4[ch2的n末端区域]-人-igg3*[ch2的c末端区域:>aa位点251]-人-igg3*[ch3]
173、·小鼠-igg2b/大鼠-[vh-ch1,vl-cl]-人-igg1-[铰链]-人-igg3*-[ch2-ch3]
174、·小鼠-igg2b/人-[vh-ch1,vl-cl]-人-igg1-[铰链]-人-igg3*-[ch2-ch3]
175、·小鼠-igg2b/小鼠-[vh-ch1,vl-cl]-人-igg1-[铰链]-人-igg3*-[ch2-ch3]
176、在本发明的一个特别优选的实施方案中,使用的优选具有单价或二价结合特异性的双特异性抗体具有以下特性:
177、一种完整的全igg双特异性抗体,其包含以下特性:
178、a)与t细胞结合;
179、b)与肿瘤细胞上的肿瘤相关抗原结合;
180、c)通过其fc部分与fc受体阳性细胞结合、
181、d)在抗体浓度小于500ng/ml时,无补体依赖性细胞毒性或仅有微弱的补体依赖性细胞毒性,从而避免神经疼痛,其中所述双特异性抗体进一步选自具有以下同种型组合的抗体的组:
182、大鼠-igg2b/小鼠-igg2a、
183、大鼠-igg2b/小鼠-igg2b、
184、大鼠-igg2b/人-igg1、
185、小鼠-[vh-ch1;vl-cl]-人-igg1/大鼠-[vh-ch1,vl-cl]-人-igg1-[铰链]-人-igg3*-[ch2-ch3]
186、[*=高加索同种异型g3m(b+g)=不与蛋白a结合]。这种优选的抗体可能与在抗体浓度小于500ng/ml时,无补体依赖性细胞毒性或仅有微弱的补体依赖性细胞毒性的更好效果,以及更好地避免神经疼痛相关。这可能归因于本发明公开的抗体与gd2结合位点的单价结合。
187、特别优选的是一种抗体,优选靶向gd2和cd3的双特异性抗体和/或支架蛋白,其同种型组合为大鼠-igg2b/小鼠-igg2a。所述双特异性抗体的一个优选实施例为抗cd3×抗gd2抗体。优选地,所述抗体为单克隆抗体。
188、优选地,根据本发明的抗体为具有例如fv、fab、scfv或f(ab)2片段的单克隆、嵌合、重组、合成、半合成或化学修饰的完整的抗体。
189、本发明的方法中还可以使用人源的抗体、其衍生物或片段,或经过修饰以适用于人的抗体(即所谓的“人源化抗体”)(例如参见shalaby等人,j.exp.med.175(1992),217;mocikat等人,transplantation 57(1994),405)。
190、对于本领域技术人员来说,上述不同类型的抗体和抗体片段的制备是显而易见的。优选哺乳动物来源的单克隆抗体的制备,例如人、大鼠、小鼠、兔或山羊的单克隆抗体可采用常规方法,如和milstein(nature 256(1975),495)、harlow和lane(antibodies,a laboratory manual(1988),cold spring harbor)或galfré(meth.enzymol.73(1981),3)。
191、还可以根据本领域技术人员显而易见的技术,通过重组dna技术来制备所述抗体(参见kurucz等人,j.immunol.154(1995),4576;hollinger等人,proc.natl.acad.sci.usa90(1993),6444)。
192、制备具有两种不同特异性的抗体,即所谓的双特异性抗体,可以例如使用dna重组技术,也可以使用所谓的杂交瘤融合技术(例如,参见milstein等人,nature 305(1983),537)。这项技术包括融合杂交瘤细胞系,每个细胞系产生的抗体都具有一种所需的特异性,并鉴定和分离出具有两种特异性抗体的重组细胞系。
193、构成本发明基础的问题可以通过在优选的实施方案中使用双特异性抗体或三特异性抗体来克服,只要它们表现出如本文所述的特性和效果。本发明尤其以双特异性抗体的方式进行描述。然而,应当理解的是,本发明还涵盖以下表现出类似效果的三特异性抗体。尽管上文中术语“抗体”或“支架蛋白”可能指双特异性抗体,但是应当理解,它还可以涵盖以下表现出类似效果的三特异性抗体。
194、制备表现出三种特异性的抗体,即所谓的三特异性抗体,也适用于解决本发明的问题,例如,可以通过将具有额外特异性的第三抗原结合位点(例如以“单链可变片段”(scfv)的形式)偶联到双特异性抗体的一条igg重链来实现。此外,还可以使用重组技术,例如基于载体的蛋白质合成或寡核苷酸合成方法。
195、同样地,也可以用具有第三种特异性的scfv替换双特异性抗体中一种特异性重链的ch2-ch3区域,从而制备三特异性f(ab)2构建体,而具有另一种特异性的重链的ch2-ch3区域可以例如通过在编码基因中插入终止密码子(在“铰链”5区域的末端)等同源重组的方法去除。
196、还可以制备三特异性scfv构建体,其中代表三种不同的特异性的三个vh-vl区域串联排列。
197、完整的双特异性抗体由两个抗体半分子(每个半分子都有一条h免疫球蛋白链和一条l免疫球蛋白链)组成,每个抗体半分子都代表一种特异性,此外,与普通抗体一样具有执行众所周知的效应功能的fc部分。完整的双特异性抗体优选使用quadroma技术来制备。专利文献de-a-44 19 399举例说明了这种制备方法。为了完整公开,该文件关于双特异性抗体的定义也通过引用整体并入本文。应当理解,其他制备方法也是有用的,只要它们能根据上述定义制备出本发明所需的完整的双特异性抗体。
198、例如,使用新开发的制备方法可以生产出足量的完整的双特异性抗体(lindhofer等人,j.immunology,155:219(1995))。在乳腺癌细胞上,靶向两种不同肿瘤相关抗原(例如c-erb-b2、epcam,如ga-733-2=c215)的两种双特异性抗体的组合可最大限度地降低仅表达其中一种抗原的肿瘤细胞未被识别的风险。
199、附图
200、图1利用流式细胞术分析fadu和kato iii细胞mcrp的表达。fadu细胞和kato iii细胞分别用靶向mcrp(cd46、cd55和cd59)的fitc偶联抗体或同种型对照抗体进行染色。直方图显示了通过流式细胞术测量的fitc荧光强度。
201、图2对源于31.08.05的供体i的卡妥索抗体介导的补体依赖性细胞毒性分析。将kato iii细胞与50ng/ml、500ng/ml或1μg/ml的卡妥索抗体在10%常规血清(人血清)、10%灭活血清或无血清的条件下孵育。肿瘤细胞存活率表示为未含卡妥索抗体的对照组的百分比。“w/o”代表“无”。
202、图3对源于31.08.05的供体ii的卡妥索抗体介导的补体依赖性细胞毒性分析。kato iii细胞与50ng/ml、500ng/ml或1μg/ml的卡妥索抗体在10%常规血清(人血清)、10%灭活血清或无血清的条件下孵育。肿瘤细胞存活率表示为未含卡妥索抗体的对照组的百分比。“w/o”代表“无”。
203、图4对源于24.08.05的供体iii的卡妥索抗体介导的补体依赖性细胞毒性分析。kato iii细胞与50ng/ml、500ng/ml或1μg/ml的卡妥索抗体在10%常规血清(人血清)、10%灭活血清或无血清的条件下孵育。肿瘤细胞存活率表示为未含卡妥索抗体的对照组的百分比。“w/o”代表“无”。
204、图5对源于20.07.05的供体iv的卡妥索抗体介导的补体依赖性细胞毒性分析。kato iii细胞与50ng/ml、500ng/ml或1μg/ml的卡妥索抗体在10%常规血清(人血清)、10%灭活血清或无血清的条件下孵育。肿瘤细胞存活率表示为未含卡妥索抗体的对照组的百分比。“w/o”代表“无”。
205、图6对源于20.07.05的供体iv的卡妥索抗体介导的补体依赖性细胞毒性分析。fadu细胞与50ng/ml、500ng/ml或1μg/ml的卡妥索抗体在10%常规血清(人血清)、10%灭活血清或无血清的条件下孵育。肿瘤细胞存活率表示为未含卡妥索抗体的对照组的百分比。“w/o”代表“无”。
206、图7对源于31.08.05的供体i的ho-3介导的补体依赖性细胞毒性分析。kato iii细胞与50ng/ml、500ng/ml或1μg/ml的卡妥索抗体和10%常规血清(人血清)、10%灭活血清或无血清的条件下孵育。肿瘤细胞存活率表示为未含ho-3的对照组的百分比。
207、“w/o”代表“无”。
208、图8对源于31.08.05的供体ii的ho-3介导的补体依赖性细胞毒性分析。kato iii细胞与50ng/ml、500ng/ml或1μg/ml的卡妥索抗体在10%常规血清(人血清)、10%灭活血清或无血清的条件下孵育。肿瘤细胞存活率表示为未含ho-3的对照组的百分比。
209、“w/o”代表“无”。
210、图9对源于24.08.05的供体iii的ho-3介导的补体依赖性细胞毒性分析。kato iii细胞与50ng/ml、500ng/ml或1μg/ml的卡妥索抗体在10%常规血清(人血清)、10%灭活血清或无血清的条件下孵育。肿瘤细胞存活率表示为未含ho-3的对照组的百分比。“w/o”代表“无”。
211、图10一名患有骨转移的iv级神经母细胞瘤患者1接受了两个周期剂量递增的双特异性抗体ektomun治疗。药代动力学分析表明,患者1和另一名患者2的剂量与循环抗体量的增加呈线性关系。(a)患者1的第一个治疗周期;(b)患者1的第二个治疗周期;(c)患者2的第一个治疗周期。
212、以下描述了用于实施本发明的一个具体实施例。本领域普通技术人员采用这种方法必然会获得所要求保护的益处。可以根据该实施例,在不偏离本发明的情况下进行各种修改。以下实施例仅用于说明上述公开内容,不应被视为对本发明范围的限制。
213、实施例
214、实施例1
215、为了比较亲本抗-epcam抗体ho-3(同种型为小鼠igg2a)与双特异性抗体--卡妥索抗体(抗-epcam×抗-cd3,同种型组合为小鼠igg2a×大鼠igg2b)的补体结合活性,进行实验以评估补体介导的细胞毒性,作为ektomun和其相关亲本抗体me361的模型系统,它们具有相同的fc区,因此拥有相同的补体结合特性。此外,卡妥索抗体和ektomun抗体的cd3结合臂完全相同。
216、首先,作为前提条件,利用流式细胞术测量了肿瘤靶细胞系kato iii和fadu表面膜结合补体调节蛋白(mcrp)的表达(图1)。
217、膜结合补体调节蛋白(mcrps),例如cd46、cd55和cd59,在全身表达,以防止补体系统的过度激活。然而,这些mcrp就像一把双刃剑,因为它们也会过度调节补体系统,使其不再有效地消除癌细胞(参见geller a and yan j(2019)the role of membrane boundcomplement regulatory proteins in tumor development and cancerimmunotherapy.front.immunol.10:1074.doi:10.3389/fimmu.2019.01074)一文。
218、为了更好地理解后续实验中测量的受测试抗体的补体依赖性细胞毒性,评估了mcrp的表达。
219、其次,用katoiii和4种不同的补体供体,以及用fadu和一种补体供体,分析了卡妥索抗体的补体依赖性细胞毒性(图2-6)。
220、还基于上述类似的方法评估了亲本抗-epcam抗体ho-3介导的补体依赖性细胞毒性(图7-9)。
221、实施例2
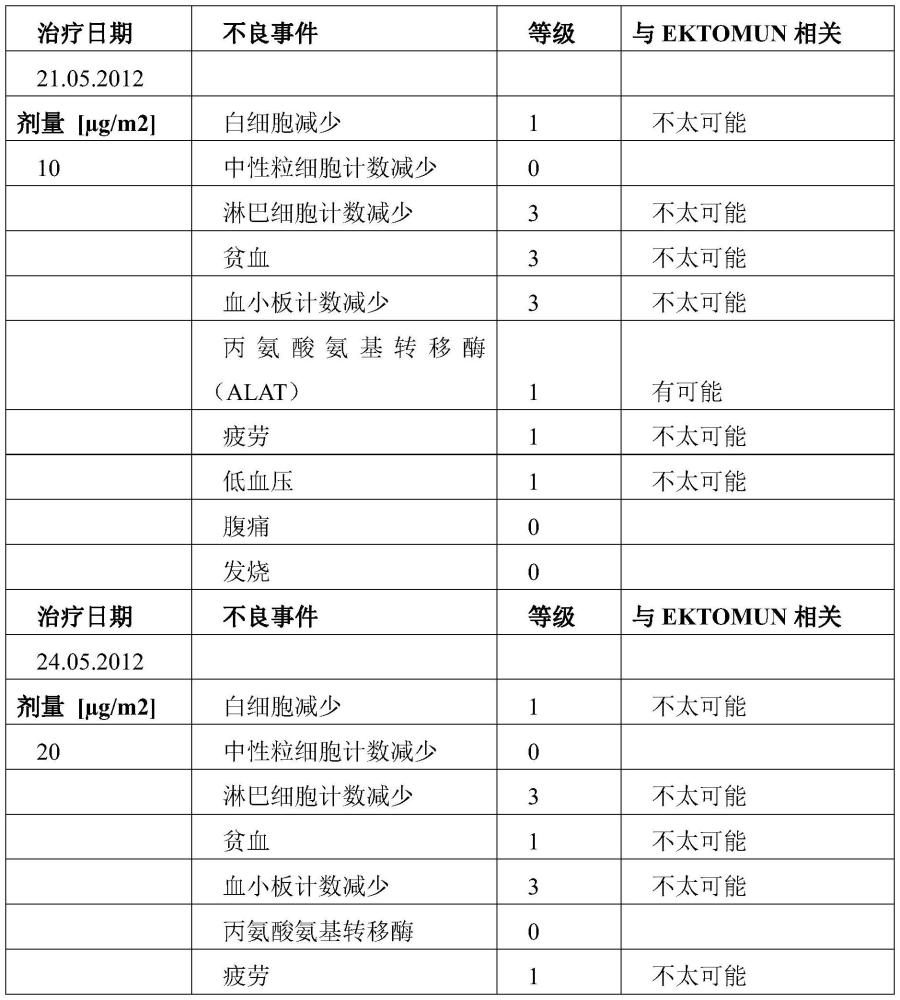
222、使用双特异性抗体ektomun(抗gd2 x抗cd3)对指定的神经母细胞瘤患者进行的治疗不会引起神经疼痛。一名患有骨转移的iv级神经母细胞瘤患者1接受了两个周期的剂量递增的bsab ektomun治疗(图10a-b)药代动力学分析表明,患者1和患者2的剂量与循环抗体量的增加呈线性关系(图10a-c)。对于患者1,第一个治疗周期的所有不良事件均被详细记录(见下文表1-3)。预期的与抗体相关的不良事件为发热、寒战和流感样症状。然而,没有观察到抗体相关的神经疼痛。从个人交流中得知,在第二个治疗周期期间和之后也没有出现神经疼痛。
223、使用ektomun(静脉注射)治疗神经母细胞瘤患者的毒性评估
224、表1:
225、
226、
227、
228、表2:
229、
230、
231、表3:
232、
233、
234、总结和结论
235、补体依赖性细胞毒性试验结果表明,亲本抗-epcam抗体ho-3对肿瘤细胞的破坏显著优于卡妥索双特异性抗体。尽管ho-3在所有抗体浓度下(甚至在500ng/ml时)均表现出补体依赖性细胞毒性,卡妥所抗体在小于500ng/ml的抗体浓度下无法重复地和定量地裂解细胞。
236、造成这一现象的原因可能是双特异性抗体与肿瘤相关抗原的单价结合。二价结合抗体能以更高的亲和力与肿瘤靶点结合,因此即使抗体浓度较低,也能介导有效的补体依赖性肿瘤细胞裂解。
237、本发明公开的双特异性抗体具有以下特征,其可进一步与减少或减轻与补体结合相关的神经疼痛至不重要或不存在的水平相关:本发明公开的抗体,优选为结合gd2的抗体,对肿瘤相关抗原表现出低亲和力至中等亲和力,优选地kd值范围为10-5–10-8m,因此靶细胞(例如gd2阳性肿瘤)或健康组织的调理作用只能由参与的fc-γ受体阳性细胞或t细胞介导,这些细胞可以将结合的抗体(例如抗-gd2抗体或抗-gd2×抗-cd3双特异性抗体)的亲和力提高到足够的结合的水平。
238、在本发明公开的抗体中,低补体结合的原因可能是由于单价结合至肿瘤相关抗原(如gd2)的亲和力较低。也就是说,本发明公开的抗体首先与t细胞结合,然后才能通过调理的t细胞上例如数百个trak分子的增加的亲和力与肿瘤细胞(例如在ektomun的情况下为gd2阳性肿瘤细胞)结合并破坏它们,在此过程中补体可能不会发挥作用,因为t细胞表面表达了许多抑制补体的抗原。
239、背景部分的参考文献
240、1.zhang s,cordon-cardo c,zhang hs,reuter ve,adluri s,hamilton wb,lloyd ko,livingston po:selection of tumor antigens as targets for immuneattack using immunohistochemistry:i:focus on gangliosides.int j cancer 1997,73:42–49.
241、2.svennerholm l,bostrom k,fredman p,jungbjer b,lekman a,mansson je,rynmark bm:gangliosides and allied glycosphingolipids in human peripheralnerve and spinal cord.biochim biophys acta 1994,1214:115–123.
242、3.hamilton wb,helling f,lloyd ko,livingston po:ganglioside expressionon human malignant melanoma assessed by quantitative immune thinlayerchromatography.int j cancer1993,53:566–573.
243、4.mujoo k,cheresh da,yang hm,reisfeld ra:disialoganglioside gd2 onhuman neuroblastoma cells:target antigen for monoclonal antibodymediatedcytolysis and suppression of tumor growth.cancer res 1987,47:1098–1104.
244、5.grant sc,kostakoglu l,chris mg,yeh sdj,larson sm,finn rd,oettgenhf,cheung nkv:targeting of small cell lung cancer using the anti-gd2ganglioside monoclonal antibody 3f8:a pilot trial.eur j nucl med 1996,23:145–149.
245、6.yoshida s,fukumoto s,kawaguchi h,sato s,ueda r,furukawa k:ganglioside g(d2)in small cell lung cancer cell lines:enhancement of cellproliferation and mediation of apoptosis.cancer res 2001,61:4244–4252.
246、7.cheresh da,rosenberg j,mujoo k,hirschowitz l,reisfeld ra:biosynthesis and expression of the disialoganglioside gd2,a relevant targetantigen on small cell lung carcinoma for monoclonal antibody-mediatedcytolysis.cancer res 1986,46:5112–5118.
247、8.lammie g,cheung n,gerald w,rosenblum m,cordoncardo c.ganglioside gdexpression in the human nervous-system and in neuroblastomas-animmunohistochemical study.int j oncol.(1993)3:909–15.doi:10.3892/ijo.3.5.909
248、9.schulz g,cheresh da,varki nm,yu a,staffileno lk,reisfeldra.detection of ganglioside gd2 in tumor tissues and sera of neuroblastomapatients.cancer res.(1984)44(12pt 1):5914–20.
249、10.svennerholm l,bostrom k,fredman p,jungbjer b,lekman a,mansson je,et al.gangliosides and allied glycosphingolipids in human peripheral nerveand spinal cord.biochim biophys acta(1994)1214:115–23.doi:10.1016/0005-2760(94)90034-5
250、11.mody r,naranjo a,van ryn c,yu al,london wb,shulkin bl,etal.irinotecan-temozolomide with temsirolimus or dinutuximab in children withrefractory or relapsed neuroblastoma(cog anbl1221):an open-label,randomised,phase 2 trial.lancet oncol.(2017)18:946–57.doi:10.1016/s1470-2045(17)30355-8
251、12.navid f,sondel pm,barfield r,shulkin bl,kaufman ra,allay ja,etal.phase i trial of a novel anti-gd2 monoclonal antibody,hu14.18k322a,designed to decrease toxicity in children with refractory or recurrentneuroblastoma.j clin oncol.(2014)32:1445–52.doi:10.1200/jco.2013.50.4423
252、13.kushner bh,kramer k,modak s,cheung nk.successful multifold doseescalation of anti-gd2 monoclonal antibody 3f8 in patients withneuroblastoma:a phase i study.j clin oncol.(2011)29:1168–74.doi:10.1200/jco.2010.28.3317
253、14.osenga kl,hank ja,albertini mr,gan j,sternberg ag,eickhoff j,etal.a phase i clinical trial of the hu14.18-il2(emd 273063)as a treatment forchildren with refractory or recurrent neuroblastoma and melanoma:a study ofthe children's oncology group.clin cancer res.(2006)12:1750–9.doi:10.1158/1078-0432.ccr-05-2000
254、15.isaacs jd,greenwood j,waldmann h.therapy with monoclonalantibodies.ii.the contribution of fc gamma receptor binding and the influenceof c(h)1 and c(h)3 domains on in vivo effector function.j immunol.(1998)161:3862–9.
255、16.yu al,gilman al,ozkaynak mf,et al.anti-gd2 antibody with gm-csf,interleukin-2,and isotretinoin for neuroblastoma.(n engl j med.2010;363:1324-1334).
技术实现思路
- 还没有人留言评论。精彩留言会获得点赞!