针对CD40和CD137的多特异性抗体的制作方法
本发明涉及与cd40和cd137结合的多特异性抗体,以及此类多特异性抗体的用途,特别是用于治疗癌症的用途。
背景技术:
1、cd40是肿瘤坏死因子(tnf)受体(tnfr)家族的成员,并且已知为在多种细胞类型上发现的共刺激蛋白。cd40由抗原呈递细胞(apc)(包括树突状细胞(dc)、b细胞和巨噬细胞)组成型表达。它也可以由内皮细胞、血小板、平滑肌细胞、成纤维细胞和上皮细胞表达。与其在正常细胞上的广泛表达一致,cd40也在多种肿瘤细胞上表达。
2、在mhc ii类分子的背景中将肽抗原呈递至抗原特异性cd4+t细胞,连同共刺激信号(来自cd80和/或cd86),导致cd4+t细胞的活化以及dc许可因子cd40配体(cd40l)和淋巴毒素-α1β2(ltα1β2)的上调。cd40l和ltα1β2在活化的抗原特异性cd4+t细胞上的表达通过cd40和ltβ受体(ltβr)诱导信号传导,并且这许可dc诱导cd8+t细胞应答。cd40信号传导导致白细胞介素-12(il-12)的产生和cd70、cd86、4-1bb配体(4-1bbl)、ox40配体(ox40l)和gitr配体(gitrl)的上调,而ltβr信号传导导致i型干扰素(ifn)的产生。控制核因子kappab(nf-kb)的活性的信号传导系统对几乎所有tnfr超家族成员都响应。病原体相关分子模式(pamp)和损伤相关分子模式(damp)也有助于这些事件。通过mhc i类限制性肽引发cd8+t细胞导致cd27、4-1bb、ox40和糖皮质激素诱导的tnfr相关蛋白(gitr)的上调。通过其同源tnf超家族配体与il-12和i型ifn组合刺激cd8+t细胞上的这些受体,导致强大的cd8+t细胞活化、增殖和效应功能,以及cd8+t细胞记忆的形成和维持。cd40抗体可以发挥不同的作用,通过诱导抗体依赖性细胞介导的细胞毒性(adcc)、补体依赖性细胞毒性(cdc)或抗体依赖性细胞介导的吞噬作用(adcp)来杀伤表达cd40的肿瘤细胞,诱导细胞信号传导以诱导直接细胞凋亡或生长停滞,并且不依赖于肿瘤细胞上的cd40表达通过许可apc刺激抗癌免疫反应。与cd40结合的抗体可以触发apc上的cd40以引发效应细胞毒性t淋巴细胞(ctl)并诱导这些细胞释放il-2,并间接活化nk细胞。刺激cd40的抗体已在现有技术中公开,包括cp-870,893,人igg2抗体(wo 2003/040170);达西珠单抗(dacetuzumab),一种人源化igg1抗体(wo2000/075348)和chi lob 7/4,一种嵌合igg1抗体(us2009/0074711)。此外,已经公开了拮抗性cd40抗体鲁卡妥姆单抗(lucatumumab),一种人igg1抗体(wo 2002/028481)。
3、cd137(4-1bb)也是tnfr家族的成员。cd137是cd8+和cd4+t细胞、调节性t细胞(treg)、自然杀伤t细胞(nk(t)细胞)、b细胞和嗜中性粒细胞上的共刺激分子。在t细胞上,cd137不是组成型表达,而是在t细胞受体(tcr)激活后诱导(例如,在肿瘤浸润淋巴细胞(til)上(gros et al.,j.clin invest2014;124(5):2246-59))。经由其天然配体4-1bbl或激动剂抗体的刺激导致使用traf-2和traf-1作为衔接物的信号传导。通过cd137的早期信号传导涉及k-63多泛素化反应,其最终导致核因子(nf)-kb和丝裂原激活蛋白(map)-激酶途径的激活。信号传导导致增加的t细胞共刺激、增殖、细胞因子产生、成熟和延长的cd8+t细胞存活。已显示针对cd137的激动性抗体在各种临床前模型中促进t细胞的抗肿瘤控制(murillo et al.,clin cancer res2008;14(21):6895-906)。刺激cd137的抗体可以诱导t细胞的存活和增殖,从而增强抗肿瘤免疫应答。刺激cd137的抗体已在现有技术中公开,包括乌瑞芦单抗(urelumab),一种人igg4抗体(au2004279877)和乌托鲁单抗(utomilumab),一种人igg2抗体(fisher et al.2012cancer immunol.immunother.61:1721-1733)。
4、westwood ja,et al.,leukemia research 38(2014),948-954公开了“在小鼠myc驱动的血液癌症中的联合抗cd137和抗cd40抗体治疗(combination anti-cd137 andanti-cd40抗体therapy in murine myc-driven hematological cancers)”。
5、us20090074711公开了“使用嵌合激动性抗人cd40抗体的人体治疗(hunmantherapies using chimeric agonistic anti-human cd40 antibody)”。
6、然而,尽管本领域有这些和其他进步,但仍需要可以结合cd40和cd137两者的多特异性抗体,同时结合表达cd40的apc和表达cd137的t细胞,从而使这些细胞类型紧密接触。这继而可以导致两种细胞类型的活化和抗肿瘤免疫的有效诱导。
技术实现思路
1、本发明人已经鉴定了可以结合cd40和cd137两者并引起t细胞和apc活化的多特异性抗体。
2、因此,一方面,本发明涉及多特异性抗体,其包含
3、(i)与人cd40结合的第一抗原结合区,和(ii)与人cd137结合的第二抗原结合区。
4、在一些实施方案中,本发明涉及此类多特异性抗体,其中第一抗原结合区包含重链和轻链可变区cdr1、cdr2和cdr3,其包含特定氨基酸序列(任选地具有突变),或与包含此类特定氨基酸序列的抗体竞争或具有包含此类特定氨基酸序列的抗体的特异性的抗体的氨基酸序列。在具体的实施方案中,第一抗原结合区包含重链和轻链可变序列,其包含抗cd40抗体001的cdr1、cdr2和cdr3,或与此类抗体竞争或具有此类抗体的特异性。
5、在一些实施方案中,本发明涉及此类多特异性抗体,其中第二抗原结合区包含重链和轻链可变序列,其中cdr1、cdr2和cdr3包含特定氨基酸序列或提供特定氨基酸序列,任选地具有突变,或者包含与包含此类特定氨基酸序列的抗体竞争或具有包含此类特定氨基酸序列的抗体的特异性的抗体的氨基酸序列。在具体的实施方案中,第二抗原结合区包含重链和轻链可变序列,其包含抗cd137抗体001、002、003、004、005、006、007、008、009、010、011或012的cdr1、cdr2和cdr3,或与任意此类抗体竞争或具有任意此类抗体的特异性。
6、本发明进一步涉及以下实施方案:
7、1.多特异性抗体,其包含
8、(i)与人cd40结合的第一抗原结合区,其中所述第一抗原结合区包含选自下组的重链和轻链可变区cdr1、cdr2和cdr3:
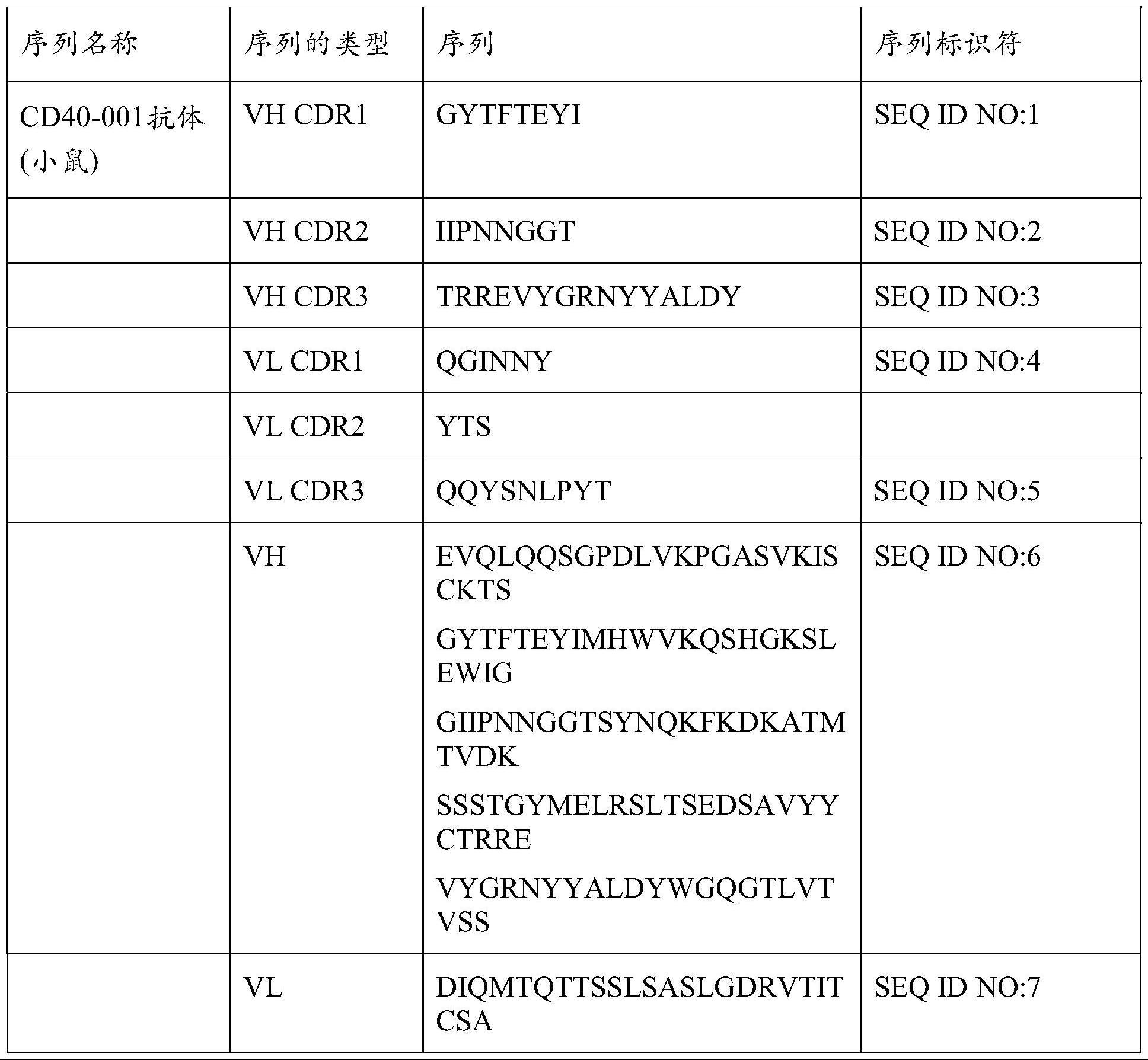
9、a)分别具有seq id no:1、2和3所示的氨基酸序列的重链可变区cdr1、cdr2和cdr3,以及分别具有seq id no:4、yts和5所示的氨基酸序列的轻链可变区cdr1、cdr2和cdr3;
10、b)具有总共一至十二个突变的根据a)的重链和轻链可变区cdr1、cdr2和cdr3;和
11、c)抗体的重链和轻链可变区cdr1、cdr2和cdr3,所述抗体(i)与包含根据a)或b)的重链和轻链可变区cdr1、cdr2和cdr3的抗体竞争与人cd40结合和/或(ii)具有包含根据a)或b)的重链和轻链可变区cdr1、cdr2和cdr3的抗体对cd40的特异性,
12、和
13、(ii)与人cd137结合的第二抗原结合区。
14、2.根据实施方案1的多特异性抗体,其中所述第一抗原结合区包含第一重链可变(vh)序列和第一轻链可变(vl)序列,所述第二抗原结合区包含第二vh序列和第二vl序列,并且所述第一和第二vh和vl序列各自包含三个cdr序列,分别是cdr1、cdr2和cdr3,以及四个框架序列,分别是fr1、fr2、fr3和fr4。
15、3.根据前述实施方案中任一项的多特异性抗体,其中所述第一抗原结合区包含分别具有seq id no:1、2和3所示的序列的重链可变区cdr1、cdr2和cdr3,以及分别具有seqid no:4、yts和5所示的序列的轻链可变区cdr1、cdr2和cdr3。
16、4.根据实施方案2-3中任一项的多特异性抗体,其中所述第一抗原结合区的vh序列包含与seq id no:117和6的至少一个具有至少70%、至少75%、至少80%、至少85%、至少90%、至少95%、至少97%、至少99%或100%同一性的氨基酸序列。
17、5.根据实施方案2-4中任一项的多特异性抗体,其中所述第一抗原结合区的vl序列包含与seq id no:121和7的至少一个具有至少70%、至少75%、至少80%、至少85%、至少90%、至少95%、至少97%、至少99%或100%同一性的氨基酸序列。
18、6.根据实施方案2-5中任一项的多特异性抗体,其中所述第一抗原结合区的vh序列包含与seq id no:117具有至少70%、至少75%、至少80%、至少85%、至少90%、至少95%、至少97%、至少99%或100%同一性的氨基酸序列;并且其中所述第一抗原结合区的vl序列包含与seq id no:121具有至少70%、至少75%、至少80%、至少85%、至少90%、至少95%、至少97%、至少99%或100%同一性的氨基酸序列。
19、7.根据前述实施方案中任一项的多特异性抗体,其中所述第二抗原结合区与猕猴(cynomolgus)cd137结合。
20、8.根据前述实施方案中任一项的多特异性抗体,其中所述第二抗原结合区与人cd137(seq id no:92)结合的程度高于其与突变体人cd137(seq id no:93)结合的程度。
21、9.根据实施方案1-7中任一项的多特异性抗体,其中所述第二抗原结合区与人cd137(seq id no:92)结合的程度高于其与突变体人cd137(seq id no:94)结合的程度。
22、10.根据前述实施方案中任一项的多特异性抗体,其中所述第二抗原结合区与人cd137(seq id no:92)结合的程度与其与突变体人cd137(seq id no:95)结合的程度相同。
23、11.根据实施方案8-10中任一项的多特异性抗体,其中通过如下测定与所述人cd137(seq id no:92)和所述突变体人cd137(分别为seq id no:93、94和95)的结合:使用人cd137和不同物种的cd137作为参照构建体,制备衍生自人cd137的改组构建体(shuffleconstruct),用来自不同物种的cd137的相应结构域取代所述人cd137的蛋白质结构域;分别用编码所述参照构建体或所述改组构建体的质粒转导细胞,并且通过流式细胞术测量所述抗体与每种这些cd137构建体的结合。
24、12.根据实施方案1-8和10-11中任一项的多特异性抗体,其中所述第二抗原结合区包含选自下组的重链和轻链可变区cdr1、cdr2和cdr3:
25、a)分别具有seq id no:64、65和66所示的序列的重链可变区cdr1、cdr2和cdr3,以及分别具有seq id no:67、gas和68所示的序列的轻链可变区cdr1、cdr2和cdr3,和
26、b)具有总共一至十二个突变的根据a)的重链和轻链可变区cdr1、cdr2和cdr3,
27、c)抗体的重链和轻链可变区cdr1、cdr2和cdr3,所述抗体(i)与包含根据a)或b)的重链和轻链可变区cdr1、cdr2和cdr3的抗体竞争与人cd137结合和/或(ii)具有包含根据a)或b)的重链和轻链可变区cdr1、cdr2和cdr3的抗体对cd137的特异性。
28、13.根据实施方案1-8和10-12中任一项的多特异性抗体,其中所述第二抗原结合区的vh序列包含与seq id no:123和69的至少一个具有至少70%、至少75%、至少80%、至少85%、至少90%、至少95%、至少97%、至少99%或100%同一性的氨基酸序列。
29、14.根据实施方案1-8和10-13中任一项的多特异性抗体,其中所述第二抗原结合区的vl序列包含与seq id no:127和70的至少一个具有至少70%、至少75%、至少80%、至少85%、至少90%、至少95%、至少97%、至少99%或100%同一性的氨基酸序列。
30、15.根据实施方案1-8和10-14中任一项的多特异性抗体,其中所述第二抗原结合区的所述vh和所述vl序列分别包含与seq id no:123和seq id no:127具有至少70%、至少75%、至少80%、至少85%、至少90%、至少95%、至少97%、至少99%或100%同一性的氨基酸序列。
31、16.根据实施方案1-7和9-11中任一项的多特异性抗体,其中所述第二抗原结合区包含选自下组的重链和轻链可变区cdr1、cdr2和cdr3:
32、a)分别具有seq id no:36、37和38所示的序列的重链可变区cdr1、cdr2和cdr3,以及分别具有seq id no:39、sas和40所示的序列的轻链可变区cdr1、cdr2和cdr3,和
33、b)具有总共一至十二个突变的根据a)的重链和轻链可变区cdr1、cdr2和cdr3,
34、c)抗体的重链和轻链可变区cdr1、cdr2和cdr3,所述抗体(i)与包含根据a)或b)的重链和轻链可变区cdr1、cdr2和cdr3的抗体竞争与人cd137结合和/或(ii)具有包含根据a)或b)的重链和轻链可变区cdr1、cdr2和cdr3的抗体对cd137的特异性。
35、17.根据实施方案1-7、9-11和16中任一项的多特异性抗体,其中所述第二抗原结合区的vh序列包含与seq id no:41具有至少70%、至少75%、至少80%、至少85%、至少90%、至少95%、至少97%或至少99%同一性的氨基酸序列。
36、18.根据实施方案1-7、9-11和16-17中任一项的多特异性抗体,其中所述第二抗原结合区的vl序列包含与seq id no:42具有至少70%、至少75%、至少80%、至少85%、至少90%、至少95%、至少97%或至少99%同一性的氨基酸序列。
37、19.根据实施方案1-7、9-11和16-18中任一项的多特异性抗体,其中所述第二抗原结合区的所述vh和所述vl序列分别包含与seq id no:41和seq id no:42具有至少70%、至少75%、至少80%、至少85%、至少90%、至少95%、至少97%或至少99%同一性的氨基酸序列。
38、20.根据实施方案4-19中任一项的多特异性抗体,其中所述第一抗原结合区包含分别具有seq id no:1、2和3所示的氨基酸序列的重链可变区cdr1、cdr2和cdr3,以及分别具有seq id no:4、yts和5所示的氨基酸序列的轻链可变区cdr1、cdr2和cdr3;并且所述第二抗原结合区包含
39、a)分别具有seq id no:64、65和66所示的序列的重链可变区cdr1、cdr2和cdr3,以及分别具有seq id no:67、gas和68所示的序列的轻链可变区cdr1、cdr2和cdr3,或
40、b)分别具有seq id no:36、37和38所示的序列的重链可变区cdr1、cdr2和cdr3,以及分别具有seq id no:39、sas和40所示的序列的轻链可变区cdr1、cdr2和cdr3。
41、21.根据实施方案4-20中任一项的多特异性抗体,其中所述第一和/或第二抗原结合区的vh和vl序列的各自的fr1、fr2、fr3和fr4框架序列与所述vh和vl序列的各自的fr1、fr2、fr3和fr4框架序列具有至少70%、至少75%、至少80%、至少85%、至少90%、至少95%、至少97%或至少99%氨基酸序列同一性。
42、22.根据前述实施方案中任一项的多特异性抗体,其中所述抗体包含(i)包含所述第一抗原结合区的第一结合臂,和(ii)包含所述第二抗原结合区的第二结合臂。
43、23.根据实施方案22的多特异性抗体,其中所述第一结合臂包含第一重链恒定序列,并且所述第二结合臂包含第二重链恒定序列。
44、24.根据实施方案22-23中任一项的多特异性抗体,其中(i)所述第一结合臂包括包含第一重链可变(vh)序列和第一重链恒定(ch)序列的第一重链,和包含第一轻链可变(vl)序列的第一轻链,以及(ii)所述第二结合臂包括包含第二重链可变(vh)序列和第二重链恒定(ch)序列的第二重链,和包含第二轻链可变(vl)序列的第二轻链。
45、25.根据实施方案24的多特异性抗体,其中所述第一轻链进一步包含第一轻链恒定(cl)序列,并且所述第二轻链进一步包含第二轻链恒定(cl)序列。
46、26.根据前述实施方案中任一项的多特异性抗体,其中所述第一抗原结合区衍生自小鼠抗体。
47、27.根据前述实施方案中任一项的多特异性抗体,其中所述第一抗原结合区衍生自人源化抗体。
48、28.根据实施方案22-27中任一项的多特异性抗体,其中所述第一结合臂衍生自全长抗体。
49、29.根据实施方案22-28中任一项的多特异性抗体,其中所述第一结合臂衍生自全长igg1,λ(lambda)或igg1,κ(kappa)抗体。
50、30.根据前述实施方案中任一项的多特异性抗体,其中所述第二抗原结合区衍生自兔抗体。
51、31.根据前述实施方案中任一项的多特异性抗体,其中所述第二抗原结合区衍生自人源化抗体。
52、32.根据实施方案22-31中任一项的多特异性抗体,其中所述第二结合臂衍生自全长抗体。
53、33.根据实施方案22-32中任一项的多特异性抗体,其中所述第二结合臂衍生自全长igg1,λ(lambda)或igg1,κ(kappa)抗体。
54、34.根据前述实施方案中任一项的多特异性抗体,其中所述第一和第二抗原结合区的每一个衍生自人源化抗体。
55、35.根据实施方案22-34中任一项的多特异性抗体,其中所述第一和第二结合臂的每一个衍生自全长抗体。
56、36.根据实施方案22-35中任一项的多特异性抗体,其中所述第一和第二结合臂的每一个衍生自全长igg1,λ(lambda)或igg1,κ(kappa)抗体。
57、37.根据实施方案22-36中任一项的多特异性抗体,其中所述第一和所述第二重链是igg同种型的,具有选自下组的亚类:igg1、igg2、igg3和igg4。
58、38.根据实施方案24-37中任一项的多特异性抗体,其中所述第一和第二重链的每一个包含至少铰链区、ch2和ch3区。
59、39.根据实施方案38的多特异性抗体,其中所述第一和第二重链的ch3区包含不对称突变。
60、40.根据实施方案24-39中任一项的多特异性抗体,其中在所述第一重链中,在对应于选自下组的位置的位置中的至少一个氨基酸已经被取代:根据eu编号的人igg1重链中t366、l368、k370、d399、f405、y407和k409,并且在所述第二重链中,在对应于选自下组的位置的位置中的至少一个氨基酸已经被取代:根据eu编号的人igg1重链中t366、l368、k370、d399、f405、y407和k409,并且其中所述第一和所述第二重链不在相同的位置中被取代。
61、41.根据实施方案40的多特异性抗体,其中(i)在所述第一重链中对应于根据eu编号的人igg1重链中的f405的位置中的氨基酸是l,并且在所述第二重链中对应于根据eu编号的人igg1重链中的k409的位置中的氨基酸是r,或(ii)在所述第一重链中对应于根据eu编号的人igg1重链中的k409的位置中的氨基酸是r,并且在所述第二重链中对应于根据eu编号的人igg1重链中的f405的位置中的氨基酸是l。
62、42.根据前述实施方案中任一项的多特异性抗体,其中所述抗体包含第一和第二重链,并且其中与包含相同第一和第二抗原结合区和两条包含人igg1铰链、ch2和ch3区的重链的多特异性抗体相比,所述抗体在更小程度上诱导fc介导的效应功能。
63、43.根据实施方案42的多特异性抗体,其中修饰所述第一和第二重链,使得与除了包含未修饰的第一和第二重链外相同的多特异性抗体相比,所述多特异性抗体更较小程度上诱导fc介导的效应功能。
64、44.根据实施方案42-43中任一项所述的多特异性抗体,其中通过与fcγ受体结合、与c1q结合或诱导fc介导的fcr的交联来测量所述fc介导的效应功能。
65、45.根据实施方案44的多特异性抗体,其中通过与c1q结合来测量所述fc介导的效应功能。
66、46.根据实施方案45的多特异性抗体,并且其中已修饰所述第一和第二重链和轻链恒定序列,使得与野生型双特异性抗体相比,c1q与所述多特异性抗体的结合降低至少70%、至少80%、至少90%、至少95%、至少97%或100%,其中通过elisa测定c1q结合。
67、47.根据前述实施方案中任一项的多特异性抗体,其中所述抗体包含第一和第二重链,其中在所述第一和第二重链的至少一个中,在对应于根据eu编号的人igg1重链中的位置l234、l235、d265、n297和p331的位置中一个或多个氨基酸分别不是l、l、d、n和p。
68、48.根据实施方案47的多特异性抗体,其中在所述第一和第二重链中,对应于根据eu编号的人igg1重链中的位置l234和l235的位置分别是f和e。
69、49.根据实施方案48的多特异性抗体,其中所述第一和第二重链中,对应于根据eu编号的人igg1重链中的位置l234、l235和d265的位置分别是f、e和a。
70、50.根据实施方案49的多特异性抗体,其中所述第一重链和所述第二重链两者的对应于根据eu编号的人igg1重链中的位置l234、l235和d265的位置分别是f、e和a,并且其中(i)所述第一重链的对应于根据eu编号的人igg1重链中的f405的位置是l,并且所述第二重链的对应于根据eu编号的人igg1重链中的k409的位置是r,或(ii)所述第一重链的对应于根据eu编号的人igg1重链中的k409的位置是r,并且所述第二重链的对应于根据eu编号的人igg1重链中的f405的位置是l。
71、51.根据实施方案48的多特异性抗体,其中所述第一重链和所述第二重链两者的对应于根据eu编号的人igg1重链中的位置l234和l235的位置分别是f和e,并且其中(i)所述第一重链的对应于根据eu编号的人igg1重链中的f405的位置是l,并且所述第二重链的对应于根据eu编号的人igg1重链中的k409的位置是r,或(ii)所述第一重链的对应于根据eu编号的人igg1重链中的k409的位置是r,并且所述第二重链的对应于根据eu编号的人igg1重链中的f405的位置是l。
72、52.根据前述实施方案中任一项的多特异性抗体,其中所述抗体能够交联表达人cd40的第一细胞和表达人cd137的第二细胞。
73、53.根据实施方案52的多特异性抗体,其中通过使用表达人cd40的第一细胞系和表达人cd137的第二细胞系的测定法测定所述交联,并且其中所述第一或所述第二细胞系包含在nf-κb活化后导致产生可测量的报告物的报告结构。
74、54.根据前述实施方案中任一项的多特异性抗体,其中所述抗体诱导和/或增强t细胞的增殖。
75、55.根据实施方案54的多特异性抗体,其中所述t细胞是cd4+t细胞和/或cd8+t细胞。
76、56.根据实施方案54-55中任一项的多特异性抗体,其中通过pbmc池中t细胞的次优活化来测定所述t细胞的增殖的诱导或增强。
77、57.根据实施方案56的多特异性抗体,其中通过滴定添加到pbmc池中的抗cd3抗体的浓度,测量t细胞增殖和选择导致低t细胞增殖但允许t细胞增殖的进一步增强的抗cd3抗体浓度来测定次优活化。
78、58.根据实施方案54-55中任一项的多特异性抗体,其中通过将表达特异性t细胞受体(tcr)的t细胞与在主要组织相容性复合体上呈递相应抗原的树突状细胞(dc)共培养来测量t细胞的增殖,所述主要组织相容性复合体被所述tcr识别。
79、59.根据实施方案54-55中任一项的多特异性抗体,其中所述t细胞是肿瘤浸润淋巴细胞(til),并且通过将人肿瘤样品与白细胞介素-2(il-2)和所述抗体温育,以及在温育约10至约14天的时间后回收并计数til来测定所述til的增殖的诱导和增强。
80、60.根据实施方案59的多特异性抗体,其中所述人肿瘤是黑色素瘤或非小细胞肺癌(nsclc)肿瘤。
81、61.根据实施方案54-60中任一项的多特异性抗体,其中与包含根据实施方案1-2中任一项的第二抗原结合区,但其中所述第一抗原结合区包含分别具有seq id no:99、100和101所示的序列的重链可变区cdr1、cdr2和cdr3,以及分别具有seq id no:102、gvs和103所示的序列的轻链可变区cdr1、cdr2和cdr3的双特异性抗体相比,所述抗体诱导或增强t细胞的更多增殖。
82、62.根据前述实施方案中任一项的抗体,其中所述抗体是双特异性抗体。
83、63.编码实施方案1-62的一个或多个氨基酸序列的核酸。
84、64.编码如实施方案1-62中任一项所定义的多特异性抗体的核酸。
85、65.包含根据实施方案63-64中任一项的核酸的表达载体。
86、66.包含根据实施方案63或64中任一项的核酸,或实施方案65的表达载体的宿主细胞。
87、67.根据实施方案66的宿主细胞,其中所述宿主细胞是重组真核、重组原核或重组微生物宿主细胞。
88、68.包含根据实施方案1-62中任一项的多特异性抗体、根据实施方案63和64中任一项的核酸、根据实施方案65的表达载体或根据实施方案66和67中任一项的宿主细胞的组合物。
89、69.根据实施方案68的组合物,其是药物组合物。
90、70.根据实施方案69的药物组合物,其进一步包含药学上可接受的载体。
91、71.根据实施方案1-62中任一项的多特异性抗体、根据实施方案63或64的核酸、根据实施方案65的表达载体、根据实施方案66或67的宿主细胞、根据实施方案68的组合物,或根据实施方案69或70的药物组合物,其用作药物。
92、72.根据实施方案1-62中任一项的多特异性抗体、根据实施方案63或64的核酸、根据实施方案65的表达载体、根据实施方案66或67的宿主细胞、根据实施方案68的组合物,或根据实施方案69或70的药物组合物,其用于治疗疾病。
93、73.根据实施方案72使用的多特异性抗体、核酸、表达载体、宿主细胞或组合物,其中所述疾病是传染病。
94、74.根据实施方案72使用的多特异性抗体、核酸、表达载体、宿主细胞或组合物,其中所述疾病是癌症。
95、75.根据实施方案74使用的多特异性抗体、核酸、表达载体、宿主细胞或组合物,其中所述癌症选自下组:黑色素瘤、肺癌、乳腺癌、结肠癌、肾癌、宫颈癌和前列腺癌,例如非小细胞肺癌(nsclc)或黑色素瘤。
96、76.治疗疾病的方法,所述方法包括向有此需要的受试者施用根据实施方案1-62中任一项的多特异性抗体、根据实施方案63或64的核酸、根据实施方案65的表达载体、根据实施方案66或67的宿主细胞、根据实施方案68的组合物,或根据实施方案69或70的药物组合物。
97、77.根据实施方案1-62中任一项的多特异性抗体、根据实施方案63或64的核酸、根据实施方案65的表达载体、根据实施方案66或67的宿主细胞、根据实施方案68的组合物,或根据实施方案69或70的药物组合物用于制备药物的用途。
98、78.根据实施方案71-77中任一项的方法或用途,其中所述方法或用途是与一种或多种其他治疗剂,例如化学治疗剂组合使用。
99、79.用于生产根据实施方案62的双特异性抗体的方法,所述方法包括以下步骤:
100、a)提供包含fc区的第一抗体,所述fc区包含第一ch3区;
101、b)提供包含第二fc区的第二抗体,所述fc区包含第二ch3区,
102、其中所述第一抗体是包含两个根据实施方案1-62中任一项的第一抗原结合区的cd40抗体,并且所述第二抗体是包含两个根据实施方案1-62中任一项的第二抗原结合区的cd137抗体,或反之亦然;以及其中所述第一和第二ch3区的序列是不同的并且使得所述第一和第二ch3区之间的异源二聚体相互作用强于所述第一和第二ch3区的同源二聚体相互作用的每一个;
103、c)在还原条件下将所述第一抗体与所述第二抗体一起温育;和
104、d)获得所述双特异性cd40xcd137抗体。
105、80.用于检测样品中表达cd40和cd137的细胞之间的交联是否发生的方法,所述样品获得自施用根据实施方案1-62中任一项的多特异性抗体后的患者,例如血液样品、淋巴结样品或骨髓样品,所述方法包括以下步骤:
106、(i)在允许所述多特异性抗体与表达cd40和cd137的细胞之间形成复合物的条件下使所述样品与根据实施方案1-62中任一项的多特异性抗体接触;和
107、(ii)分析是否已形成复合物。
108、81.用于在获得自患者的样品,例如血液样品、淋巴结样品或骨髓样品中检测表达cd40和cd137的细胞之间的交联的试剂盒,所述试剂盒包含
109、i)根据实施方案1-62中任一项的多特异性抗体;和
110、ii)使用所述试剂盒的说明书。
111、82.与如实施方案1-62中任一项所定义的第二或第一和第二抗原结合区结合的抗独特型抗体。
112、以下进一步详细描述这些和其他方面和实施方案,包括编码此类多特异性抗体的氨基酸序列的核酸;包含此类核酸的表达载体;包含此类核酸或表达载体的宿主细胞;包含此类多特异性抗体的组合物;用于治疗癌症或其他疾病的此类组合物;用于生产此类多特异性抗体的方法;以及基于此类多特异性抗体的诊断方法和试剂盒。
- 还没有人留言评论。精彩留言会获得点赞!