抑制TUBB2基因表达的干扰RNA及其应用的制作方法
本发明涉及分子生物学与生物医药,具体涉及一种有效抑制tubb2表达的干扰rna,特别是sirna,及其应用。
背景技术:
1、微管蛋白是构成真核细胞骨架的重要部分,广泛存在于活细胞的微管中。微管是组成真核细胞骨架的基本元素,主要由微管蛋白α和β聚合而成。在正常情况下,微管和微管蛋白二聚体之间存在动态平衡。微管在细胞支持和细胞运动中起着至关重要的作用,可以帮助细胞抵抗压缩力,使其能够保持其预期的形状和结构;此外,微管对于细胞运动、有丝分裂期间的染色体分离以及细胞器的细胞内运输等过程同样至关重要。
2、在人类中,微管蛋白有五个亚组:α-微管蛋白、β-微管蛋白、γ-微管蛋白、δ和ε-微管蛋白以及ζ-微管蛋白。β-微管蛋白特别令人感兴趣,因为它形成了一种仅在神经元中表达的微管。此外,所有与人微管蛋白结合的药物也与β-微管蛋白结合,使其成为一种治疗靶点。
3、抗有丝分裂化疗药物以微管蛋白为靶点,微管蛋白是有丝分裂纺锤体中的主要蛋白质,微管蛋白亚型组成被认为是肿瘤进展诊断和细胞对化疗反应的决定因素。这意味着正常组织和肿瘤组织的亚型组成是不同的,为肿瘤的化疗药物的开发提供了理论基础。目前常见的抗微管蛋白药物有长春碱、紫杉醇等。其中,紫杉醇可使微管与微管蛋白二聚体之间失去动态平衡,诱导和促进微管蛋白聚合,防止解聚,稳定微管。长春碱主要抑制微管蛋白的聚合,而妨碍纺锤体微管的形成,使核分裂停止于中期;也可引起核崩溃,呈空泡式固缩;作用于细胞膜,干扰细胞膜对氨基酸的运转,使蛋白质的合成受抑制;可通过抑制rna聚合酶的活力而抑制rna的合成,将细胞杀灭于g1期。这些作用导致细胞在进行有丝分裂时不能形成纺锤体和纺锤丝,抑制了细胞分裂和增殖,从而发挥抗肿瘤作用。因此,通过抑制或促进微管蛋白聚合,干扰微管的平衡,从而影响细胞的有丝分裂,抑制细胞增殖。
4、β2微管蛋白存在于细胞核,也可以非微管形式存在,可以显著影响细胞的行为。β2微管蛋白参与了几种类型肿瘤的发生发展,如神经上皮瘤和脑肿瘤、结肠癌和前列腺癌。在侵袭性转移瘤中,发现了位于细胞核的β2微管蛋白,暗示其可以与抗微管药紫杉醇和长春碱相互作用。细胞质中没有被装配到微管中的β2微管蛋白可以与电压依赖性阴离子通道(vdac)相互作用,为肌肉细胞提供能量。研究发现,β2微管蛋白的过表达与结肠直肠癌患者较短的预期寿命相关。β2微管蛋白定位于细胞核的肿瘤患者的预期寿命甚至更短。
5、因此,本技术筛选出抑制活性较高的干扰rna序列,有望制备成rna药物,用于治疗肿瘤。另外,sirna分子较大,带有大量负电荷,很难通过同样带负电荷的细胞膜。因此寻找合适的递送系统是开发sirna药物过程中重要的一部分,本技术提供了脂质纳米颗粒(lipid nanoparticles,lnp)和抗体偶联sirna(antibody–sirna conjugates,arc)两种可行的递送方式。
技术实现思路
1、本发明的第一方面,提供了一种靶向微管蛋白β2(tubb2)基因的干扰rna。
2、所述的干扰rna抑制tubb2的表达。
3、所述干扰rna的靶位点序列包含seq id no:1-13中的任一个或两个以上所示的核苷酸序列。优选的,所述干扰rna的靶位点序列如seq id no:1-13中的任一个核苷酸序列所示。
4、优选的,所述干扰rna的靶位点序列包含seq id no:1-10或12中的任一个或两个以上所示的核苷酸序列。优选的,所述干扰rna的靶位点序列如seq id no:1-10或12中的任一个核苷酸序列所示。
5、进一步优选的,所述干扰rna的靶位点序列包含seq id no:1-3或5-6或8-10中的任一个或两个以上所示的核苷酸序列。优选的,所述干扰rna的靶位点序列如seq id no:1-3或5-6或8-10中的任一个核苷酸序列所示。
6、在本发明的一个具体实施方式中,所述干扰rna的靶位点序列包含seq id no:2、8和/或10。所述的干扰rna包含sirna、dsrna、shrna、airna或mirna中一种或两种以上的组合。
7、在本发明的一个具体实施方式中,所述的干扰rna为sirna。
8、所述干扰rna的长度为17-25nt,优选19-21nt,例如17、18、19、20、21、22、23、24、25nt。
9、所述干扰rna还包括悬挂碱基,以增加干扰rna稳定性和活性。
10、优选的,所述的干扰rna包含1-10个悬挂碱基。进一步优选2-4个悬挂碱基。例如1、2、3、4、5、6、7、8、9、10个悬挂碱基。
11、所述的悬挂碱基位于所述的干扰rna的正义链和/或反义链的3’末端。
12、所述的悬挂碱基为脱氧核苷;优选的,悬挂碱基可以为n个相同或不同的脱氧核苷(例如脱氧胸苷(dt)、脱氧胞苷(dc)、脱氧尿苷(du)等),n为1-10的整数(例如1、2、3、4、5、6、7、8、9、10)。
13、在本发明的一个具体实施方式中,所述的干扰rna的正义链和/或反义链的末端设有2个相同的悬挂碱基。
14、在本发明的一个具体实施方式中,所述的干扰rna的正义链和/或反义链的末端设有2个不同的悬挂碱基。
15、在本发明的一个具体实施方式中,所述的悬挂碱基为dtdt、dtdc或dudu。
16、在本发明的一个具体实施方式中,所述的干扰rna包含正义链和/或反义链。
17、优选的,所述的正义链和反义链互补配对。
18、优选的,所述的正义链包含seq id no:14-26中的任一个或两个以上所示的核苷酸序列。进一步优选的,所述的正义链如seq id no:14-26中的任一个核苷酸序列所示。进一步优选的,所述的正义链包含seq id no:14-23或25中的任一个或两个以上所示的核苷酸序列。更进一步优选的,所述的正义链包含seq id no:14-16或18-19或21-23中的任一个或两个以上所示的核苷酸序列。
19、在本发明的一个具体实施方式中,所述的正义链包含seq id no:15、21和/23。
20、优选的,所述的反义链包含seq id no:27-39中的任一个或两个以上所示的核苷酸序列。进一步优选的,所述的反义链如seq id no:27-39中的任一个核苷酸序列所示。进一步优选的,所述的反义链包含seq id no:27-36或38中的任一个或两个以上所示的核苷酸序列。更进一步优选的,所述的反义链包含seq id no:27-29或31-32或34-36中的任一个或两个以上所示的核苷酸序列。
21、在本发明的一个具体实施方式中,所述的反义链包含seq id no:28、34和/或36。
22、在本发明的一个具体实施方式中,所述的干扰rna中还可以包含至少一个修饰。修饰的干扰rna具有比相应未修饰的干扰rna更佳的性质,如更高的稳定性,更低的免疫刺激性等。
23、所述的修饰包括在碱基、糖环和/或磷酸盐的化学结构上进行的修饰。
24、优选的,碱基的修饰包括但不限于5位嘧啶修饰、8位嘌呤修饰和/或5-溴尿嘧啶取代。
25、优选的,所述的糖环的修饰包括但不限于2'-oh被h、oz、z、halo、sh、sz、nh2、nhz、nz2或cn等基团取代,其中z为烷基基团。
26、所述的烷基基团代表直链或支链的且不含不饱和键的烃基,且该烃基以单键与分子其它部分连接。典型的烷基基团含有1至20(例如1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20)个碳原子,例如甲基、乙基、正丙基、异丙基、正丁基、仲丁基、异丁基、叔丁基、正戊基、异戊基、新戊基、叔戊基、正己基、异己基、正庚基、异庚基、正辛基、壬基、癸基、十一烷基、1-甲基十一烷基、十二烷基、十三烷基、十四烷基、十五烷基、十六烷基、十七烷基、十八烷基、十九烷基及二十烷基等。
27、优选的,所述的磷酸骨架修饰包括但不限于硫代磷酸修饰。
28、优选的,所述的修饰还包括具有肌苷、辫苷、黄嘌呤、2'-甲基核糖、非天然磷酸二酯键(如甲基膦酸酯、硫代膦酸酯)和/或肽的核苷酸。
29、在本发明的一个具体实施方式中,所述的修饰可以为甲基化、氟化、硫代磷酸化、假尿嘧啶等。
30、所述的修饰可以发生在序列的任一位置,例如可以为部分位置修饰或全部修饰。
31、同一条序列可以为相同或不同修饰类型的部分位置修饰,也可以相同或不同修饰类型的全部位置修饰。
32、在本发明的一个具体实施方式中,所述的干扰rna包含如下靶位点序列、正义链和反义链序列组合中的一种或两种以上的组合:
33、a)seq id no:1,seq id no:14,seq id no:27;
34、b)seq id no:2,seq id no:15,seq id no:28;
35、c)seq id no:3,seq id no:16,seq id no:29;
36、d)seq id no:5,seq id no:18,seq id no:31;
37、e)seq id no:6,seq id no:19,seq id no:32;
38、f)seq id no:8,seq id no:21,seq id no:34;
39、g)seq id no:9,seq id no:22,seq id no:35;
40、h)seq id no:10,seq id no:23,seq id no:36;
41、i)seq id no:8,seq id no:56,seq id no:60;
42、j)seq id no:8,seq id no:57,seq id no:61;
43、k)seq id no:10,seq id no:58,seq id no:62;
44、l)seq id no:10,seq id no:59,seq id no:63。
45、优选的,所述的干扰rna包含b)组、f)组和/或h)组。
46、在本发明的一个具体实施方式中,所述的干扰rna包含表1或表15所示的核酸序列中的一种或两种以上。
47、所述的干扰rna可以采用现有技术任意方法制备获得,例如化学合成等。
48、本发明的第二方面,提供了一种递送系统,所述的递送系统包含上述的干扰rna。
49、优选的,所述的递交系统还包括载体。
50、优选的,所述的载体可以采用任何适于将本发明上述干扰rna递送于靶组织或靶细胞等的载体,如现有技术(例如陈中华,朱德生,李军,黄展勤.“非病毒sirna载体研究进展”.中国药理学通报.2015,31(7):910-4;王锐,曲炳楠,杨婧.“载sirna的纳米制剂研究进展”.中国药房.2017,28(31):4452-4455)中公开的载体。
51、在本发明的一个具体实施方式中,所述的载体为病毒载体,优选的,所述的病毒载体包括但不限于慢病毒载体、逆转录病毒载体、腺病毒载体、腺相关病毒载体、痘病毒载体或疱疹病毒载体等中的一种或两种以上。
52、在本发明的一个具体实施方式中,所述的载体为非病毒载体,优选的,所述的非病毒载体包括但不限于脂质体、脂质纳米颗粒(lnp)、聚合物、多肽、抗体、适配体或n-乙酰半乳糖胺(galnac)中的任一种或两种以上的组合;进一步优选的,所述的非病毒载体包括脂质纳米颗粒(lnp)。其中,所述的干扰rna与非病毒载体的重量比可以为1:1-50中的任一数值(例如1:1、1:5、1:6、1:7、1:8、1:9、1:10、1:15、1:20、1:25、1:30、1:35、1:40、1:45、1:50),优选为1:1-10中的任一数值。
53、优选的,上述脂质纳米颗粒/脂质体包括:阳离子脂质、中性脂质、聚乙二醇脂质、甾族脂质或阴离子脂质中的一种或两种以上组合。
54、进一步优选的,所述阳离子脂质包括:十八酰胺(sa)、溴化月桂基三甲基铵、溴化十六烷基三甲基铵、溴化肉豆蔻基三甲基铵、溴化二甲基二-十八铵(ddab)、[(4-羟基丁基)氮杂二烷基]双(己烷-6,1-二基)双(2-己基癸酸酯)(alc-0315)、1,2-二油酰基氧基-3-(三甲基铵基)丙烷(dotap)、1,2-二-(9z-十八烯酰基)-3-三甲基铵-丙烷和1,2-二-十六酰基-3-三甲基铵-丙烷、3β-[n-(n',n'-二甲基氨基乙烷)-氨基甲酰基]胆固醇(dc胆固醇)、二甲基二十八烷基铵(dda)、1,2-二肉豆蔻酰基-3-三甲基铵丙烷(dmtap)、二棕榈酰(c16:0)三甲基铵丙烷(dptap)、二硬脂酰基三甲基铵丙烷(dstap)、n-[1-(2,3-二烯丙氧基)丙基]-n,n,n-三甲基氯化铵(dotma)、n,n-二油酰基-n,n-二甲基氯化铵(dodac)、1,2-二油酰基-sn-丙三氧基-3-乙基磷酸胆碱(doepc)、1,2-二油酰基-3-二甲基铵丙烷(dodap)、1,2-二亚油基氧基-3-二甲基氨基丙烷(dlindma)、1,2-二-十四酰基-3-二甲基铵-丙烷、1,2-二-十六酰基-3-二甲基铵-丙烷和1,2-二-十八酰基-3-二甲基铵-丙烷、1,2-二油酰基-c-(4'-三甲基铵)-丁酰基-sn-甘油(dotb)、二-十八酰胺-丙氨酰基精胺、saint-2、聚阳离子脂质2,3-二油酰基氧基-n-[2(精胺-羧酰氨基)乙基]-n,n-二甲基-1-丙铵三氟乙酸盐(dospa)、
55、
56、中的一种或两种以上的组合。
57、优选的,所述阳离子脂质为类固醇-阳离子脂质化合物,
58、所述化合物的结构为:
59、
60、
61、中的一种或两种以上。
62、进一步优选的,所述中性脂质包括:1,2-二硬脂酰-sn-甘油-3-磷酸胆碱(dspc)、1,2-二棕榈酰-sn-甘油-3-磷酸胆碱(dppc)、1,2-二油酰-sn-甘油-3-磷酸乙醇胺(dope)、1,2-二棕榈酰-sn-甘油-3-磷酸乙醇胺(dppe)、1,2-二肉豆蔻酰-sn-甘油-3-磷酸乙醇胺(dmpe)、2-二油酰基-sn-甘油-3-磷酸-(1'-rac-甘油)(dopg)、油酰磷脂酰胆碱(popc)、1-棕榈酰基-2-油酰基磷脂酰乙醇胺(pope)或二硬脂酰磷脂酰乙醇胺(dspe)中的一种或两种以上的组合。
63、进一步优选的,所述聚乙二醇脂质包括:2-[(聚乙二醇)-2000]-n,n-二十四烷基乙酰胺(alc-0159)、1,2-二肉豆蔻酰基-sn-甘油甲氧基聚乙二醇(peg-dmg)、1,2-二硬脂酰基-sn-甘油基-3-磷酸乙醇胺-n-[氨基(聚乙二醇)](peg-dspe)、peg-二甾醇基甘油(peg-dsg)、peg-二棕榈油基、peg-二油基、peg-二硬脂基、peg-二酰基甘油酰胺(peg-dag)、peg-二棕榈酰基磷脂酰乙醇胺(peg-dppe)或peg-1,2-二肉豆蔻酰基氧基丙基-3-胺(peg-c-dma)、
64、
65、等中的一种或两种以上的组合;
66、其中,n选自20-300的整数,例如20、30、50、80、100、150、200、250、300等。
67、优选的,所述聚乙二醇脂质为单一分子量的聚乙二醇脂质,优选的,所述的聚乙二醇脂质包括:
68、
69、进一步优选的,所述阴离子脂质体包括:二油酰磷脂酰甘油和/或二油酰磷脂酰乙醇胺等。
70、进一步优选的,所述的甾族脂质包括:燕麦甾醇、β-谷甾醇、菜子甾醇、麦角骨化醇、菜油甾醇、胆甾烷醇、胆固醇、粪甾醇、脱氢胆固醇、链甾醇、二氢麦角骨化醇、二氢胆固醇、二氢麦角甾醇、黑海甾醇、表胆甾醇、麦角甾醇、岩藻甾醇、六氢光甾醇、羟基胆固醇、羊毛甾醇、光甾醇、海藻甾醇、谷甾烷醇、谷甾醇、豆甾烷醇、豆甾醇、胆酸、甘氨胆酸、牛磺胆酸、脱氧胆酸或石胆酸中的一种或两种以上的组合。
71、优选的,上述聚合物可以为合成型聚合物(如聚乙烯亚胺、环糊精等)或天然型聚合物(如壳聚糖、端胶原等)或其混合物。
72、优选的,上述多肽可以为细胞穿透肽(cpp)(如鱼精蛋白、tat肽、transportan肽、penetratin肽、寡聚精氨酸肽等)。
73、优选的,上述抗体可以为单链抗体(如scfv-tp、scfv-9r等)。
74、本技术的递送系统还可以包裹各种对人体有益的成分,将其直接递送到细胞内发挥作用,可以更快更好地产生预期效果。
75、本发明的第三方面,提供了一种细胞,所述的细胞中包含上述的干扰rna或上述的递送系统。
76、所述的细胞中tubb2的表达量被抑制。
77、所述的细胞可以为肿瘤细胞。
78、本发明的第四方面,提供了一种细胞的制备方法,所述的制备方法包括将上述的干扰rna或上述的递送系统导入到细胞中。
79、本发明的第五方面,提供了一种脂质纳米颗粒,所述的脂质纳米颗粒包含上述的干扰rna。
80、优选的,所述的脂质纳米颗粒还包含聚乙二醇脂质化合物、阳离子脂质、甾族脂质或中性脂质中的一种或两种以上。
81、其中,聚乙二醇脂质化合物、阳离子脂质、甾族脂质及中性脂质的限定同本技术第二方面。
82、在本发明的一个具体实施方式中,所述的脂质纳米颗粒包含上述的干扰rna以及聚乙二醇脂质化合物、阳离子脂质(不包括类固醇-阳离子脂质化合物)、甾族脂质和中性脂质。
83、优选的,所述的脂质纳米颗粒中,聚乙二醇脂质化合物、阳离子脂质、甾族脂质和中性脂质的摩尔比为(0.5-5):(30-55):(30-55):(5-20),例如(0.5、1、2、3、4、5):(30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55):(30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55):(5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20)。优选的,聚乙二醇脂质化合物、阳离子脂质、甾族脂质和中性脂质的摩尔比为(1-5):(35-50):(40-50):(8-15)。
84、在本发明的一个具体实施方式中,所述的脂质纳米颗粒包含上述的干扰rna以及类固醇-阳离子脂质化合物、第二脂质和聚乙二醇脂质。其中,所述的第二脂质选自:中性脂质、两性离子脂质或阴离子脂质。
85、优选的,所述的脂质纳米颗粒中,所述类固醇-阳离子脂质:第二脂质:聚乙二醇脂质摩尔比为(10-30):(60-80):(10-25),例如(10、15、20、25、30):(60、65、70、75、80):(10、15、20、25),优选(20-30):(60-70):(10-20)。
86、本技术的脂质纳米颗粒还可以包裹各种对人体有益的成分,将其直接递送到细胞内发挥作用,可以更快更好地产生预期效果。
87、所述的脂质纳米颗粒可以采用本领域常规的脂质纳米颗粒制备方法制备得到,例如高压乳匀法、乳化沉淀法、超声分散法等。
88、本发明的第六方面,提供了一种药物或试剂盒,所述的药物或试剂盒包含上述的干扰rna、上述的递送系统、上述的脂质纳米颗粒或上述的细胞。
89、所述的药物还包括药学上可接受的辅料。
90、优选的,所述的药学上可接受的辅料包括但不限于载体、稀释剂、粘合剂、润滑剂、润湿剂等等。
91、优选的,所述的药物的给药方式包括但不限于口服、肠给药、皮下注射、肌肉注射、静脉注射、鼻腔给药、透皮给药、结膜下给药、眼球内给药、眼眶给药、眼球后给药、视网膜给药、脉络膜给药、鞘内注射等等。
92、优选的,所述的药物的剂型包括但不限于片剂、胶囊、丸剂、注射剂、吸入剂、含片、栓剂、乳剂、微乳剂、亚微乳剂、纳米颗粒、凝胶剂、粉剂、悬乳液、乳膏剂、胶冻剂、喷雾剂等等。所述药物的各种剂型可以按照药学领域的常规生产方法制备。
93、优选的,所述的药物中上述的干扰rna、上述的递送系统或上述的细胞的质量含量可以为1%-100%,例如1%、2%、3%、4%、5%、6%、7%、8%、9%、10%、15%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%、96%、97%、98%、99%、99.5%、100%。
94、本发明的第七方面,提供了一种抗体-核酸偶联药物,所述的抗体-核酸偶联药物中包含上述的干扰rna或上述的递送系统或上述的脂质纳米颗粒。
95、所述的抗体-核酸偶联药物中包含一个或多个干扰rna,以及抗体。
96、所述的抗体-核酸偶联药物中抗体与核酸可以直接相连或通过连接基团或连接肽相连。
97、所述的抗体-核酸偶联药物的通式(i)为:
98、
99、其中,r为上述的干扰rna;
100、x1为1-144的整数;优选的,x1为1-9的整数;更优选的,x1为1-3的整数;
101、x2为1-8的整数;优选的,x2为1-2的整数;
102、ab为抗体、蛋白质、多肽;
103、l为连接ab与r之间的连接单元。
104、优选的,所述l部分具有通式(ⅱ)结构:
105、
106、其中,
107、式ⅱ中x3选自1-12的整数;优选为1-3;
108、式ⅱ中x4选自1-12的整数;优选为1-3;
109、p1、p2相同或不同的聚乙二醇残基;
110、l1为连接ab与p1之间的连接单元;
111、l2为连接p2与r之间的连接单元;
112、a1为连接p1与p2之间的连接单元;
113、优选的,所述p1、p2独立地选自直链、y型、多分支的聚乙二醇残基;
114、优选的,当所述p1、p2为单一分子量聚乙二醇,分子量为88-4400da,更优选的,所述p1、p2分子量为176-1056da;
115、优选的,当所述p1、p2为非单一分子量聚乙二醇,分子量为1000da-40kda;
116、更优选的,所述p1、p2分子量为2000da-10kda。
117、优选的,所述l1为连接基团,选自直链或支链的c1-12亚烷基、c6-12亚芳基、c3-12环亚烷基、-s-、-s-s-、中的一种或者两种以上基团的组合;
118、所述直链或支链的c1-12链亚烷基、c6-12的亚芳基或c3-12环亚烷基上的任意的h原子被-h、-f、-cl、-br、-i、-o-、-s-、-so2、-no2、c1-12链烷基、c3-12环烷基、c6-12芳烷基、取代或未取代的杂环基或取代或未取代的杂环基烷基、中的一种或者两种以上基团组成的组取代;
119、优选的,所述l2为连接基团,选自直链或支链的c1-12亚烷基、c6-12亚芳基、c3-12环亚烷基、-s-、-o-、-s-s-、中的一种或者两种以上基团的组合;
120、所述直链或支链的c1-12链亚烷基、c6-12的亚芳基或c3-12环亚烷基上的任意的h原子被-h、-f、-cl、-br、-i、-o-、-s-、-so2、-no2、c1-12链烷基、c3-12环烷基、c6-12芳烷基、取代或未取代的杂环基或取代或未取代的杂环基烷基、中一种或者以上基团组成的组取代;
121、优选的,所述l1为酰胺键、腙键以及巯基-马来酰亚胺键;
122、更优选的,所述l1为酰胺键;
123、优选的,所述l2为二硫键以及巯基-马来酰亚胺键;
124、更优选的,所述l2为二硫键。
125、优选的,所述a1为连接p1与p2之间的连接基团,选自直链或支链的c1-12亚烷基、c6-12亚芳基、c3-12环亚烷基、-s-、-o-、-s-s-、中的一种或者两种以上基团的组合;
126、所述直链或支链的c1-12链亚烷基、c6-12的亚芳基或c3-12环亚烷基上的任意的h原子被-h、-f、-cl、-br、-i、-o-、-s-、-so2、-no2、c1-12链烷基、c3-12环烷基、c6-12芳烷基、取代或未取代的杂环基或取代或未取代的杂环基烷基、中一种或者两种以上基团组成的组取代。
127、进一步优选的,所述的抗体-核酸偶联药物的通式(iv):
128、
129、所述l1为连接基团,选自直链或支链的c1-12亚烷基、c6-12亚芳基、c3-12环亚烷基、-s-、-o-、-s-s-、中的一种或者两种以上基团的组合;
130、优选的,p1为相同或不同的聚乙二醇残基;
131、优选的,当所述p1为单一分子量聚乙二醇,分子量为88-4400da,更优选的,所述p1分子量为176-1056da;
132、优选的,当所述p1为非单一分子量聚乙二醇,分子量为1000da-40kda;更优选的,所述p1分子量为2000da-10kda。
133、所述l2为连接基团,选自直链或支链的c1-12亚烷基、c6-12亚芳基、c3-12环亚烷基、-s-、-o-、-s-s、中的一种或者两种以上基团的组合;
134、x1为1-144的整数;优选的,x1为1-9的整数;更优选的,x1为1-3的整数;
135、x2为1-8的整数;优选的,x2为1-2的整数。
136、在本发明的一个具体实施方式中,所述的抗体-核酸偶联药物具有如下结构:
137、
138、所述n1选自4-100的整数,优选为4-24;n1可以为定值也可以为均值。
139、在本发明的一个具体实施方式中,所述的抗体-核酸偶联药物具有如下结构:
140、
141、所述n1、n2独立地选自4-100的整数,优选为4-24。n1、n2可以为定值也可以为均值。
142、优选的,所述的ab选自单克隆抗体、多克隆抗体、抗体片段、抗体融合片段。
143、所述的抗体可以为单域抗体或单链抗体。
144、进一步优选的,ab为单克隆抗体;更优选的,所述单克隆抗体对癌症、恶性细胞、感染性生物或自身免疫性疾病相关的抗原或其表位是反应性的。
145、在本发明的一个具体实施方式中,所述ab选自:抗her2抗体、抗egfr抗体、抗pmsa抗体、抗vegfr抗体、抗cd30抗体、抗cd22抗体、抗cd56抗体、抗cd29抗体、抗gpnmb抗体、抗cd138抗体、抗cd74抗体、抗enpp3抗体、抗nectin-4抗体、抗egfrⅷ抗体、抗slc44a4抗体、抗间皮素抗体、抗et8r抗体、抗cd37抗体、抗ceacam5抗体、抗cd70抗体、抗muc16抗体、抗cd79b抗体、抗muc16抗体、抗muc1抗体、抗cd3抗体、抗cd28抗体、抗cd38抗体、抗cd19抗体、抗pd-l1抗体、抗4-1bb抗体等。
146、本发明的第八方面,提供了一种上述的干扰rna、上述的递送系统、上述的细胞、上述的药物或试剂盒、上述的脂质纳米颗粒或上述的抗体-核酸偶联药物的应用,所述的应用包括:
147、a)在制备治疗和/或预防tubb2表达增加或细胞过度增殖相关疾病的药物中的应用;
148、b)在抑制tubb2表达中的应用;
149、c)在治疗和/或预防tubb2表达增加或细胞过度增殖相关疾病中的应用。
150、优选的,所述治疗使用的干扰rna、上述的递送系统、上述的细胞、上述的药物或试剂盒、上述的脂质纳米颗粒或上述的抗体-核酸偶联药物的工作浓度为0.01-1000nm,例如0.01、1、2、3、4、5、6、7、8、9、10、15、20、25、30、35、40、45、50、55、60、65、70、75、80、85、90、95、100、200、300、400、500、600、700、800、900或1000nm。
151、优选的,tubb2表达增加或细胞过度增殖相关疾病包括肿瘤。进一步优选的,所述的肿瘤包括消化道肿瘤(口腔癌、舌癌、食管癌、胃癌、肝癌、胰腺癌、结肠直肠癌等)、神经系统肿瘤(胶质瘤(例如神经胶质瘤)、神经上皮瘤、神经鞘瘤、星形细胞瘤、神经纤维瘤(例如神经纤维肉瘤)、室管膜瘤、成神经管细胞瘤、脑膜瘤、脑转移瘤等)、呼吸道肿瘤(鼻咽癌、喉癌、支气管癌、肺癌等)、泌尿生殖系统肿瘤(前列腺癌、肾脏肿瘤、膀胱癌、乳腺癌、宫颈癌、卵巢癌、胎盘绒毛癌、尿路系统肿瘤、精囊腺肿瘤、睾丸及睾丸旁组织肿瘤、阴茎肿瘤、阴道癌、外阴癌、子宫癌、子宫内膜癌等)、血液淋巴系统肿瘤(白血病(例如慢性粒细胞白血病、急性髓系白血病、慢性淋巴细胞白血病、骨髓增生异常综合征、慢性骨髓细胞性白血病、急性淋巴细胞白血病等)、多发性骨髓瘤、间皮瘤、骨髓瘤、淋巴瘤(例如非霍奇金淋巴瘤、霍奇金淋巴瘤、皮肤t细胞淋巴瘤)、皮肤系统肿瘤(如皮肤癌、表皮样癌、黑色素瘤、基底细胞癌、鳞状细胞癌、paget病、卡波西肉瘤、merkel细胞癌、不典型纤维黄瘤、附属器肿瘤、皮肤t细胞淋巴瘤(蕈状肉芽肿)等)等以及横纹肌肉瘤、头颈部癌等。
152、进一步优选的,所述的肿瘤选自泌尿生殖系统肿瘤和/或皮肤系统肿瘤。
153、在本发明的一个具体实施方式中,所述的肿瘤选自前列腺癌、乳腺癌或黑色素瘤。
154、本发明的第九方面,提供了一种抑制tubb2表达的方法,所述的方法包括加入上述的干扰rna、上述的递送系统、上述的细胞、上述的脂质纳米颗粒、上述的药物或试剂盒或上述的抗体-核酸偶联药物。
155、优选的,所述的方法抑制细胞中tubb2表达,所述的细胞为肿瘤细胞。
156、优选的,所述的方法包括将上述干扰rna递送入细胞中。所述的递送使用上述的递送系统。
157、本发明的第十方面,提供了一种治疗tubb2表达增加或细胞过度增殖相关疾病的方法,所述的方法包括向受试者施加治疗有效量的上述的干扰rna、上述的递送系统、上述的脂质纳米颗粒、上述的细胞、上述的药物或试剂盒或上述的抗体-核酸偶联药物。
158、优选的,tubb2表达增加或细胞过度增殖相关疾病包括肿瘤。进一步优选的,
159、所述的肿瘤包括消化道肿瘤(口腔癌、舌癌、食管癌、胃癌、肝癌、胰腺癌、结肠直肠癌等)、神经系统肿瘤(胶质瘤(例如神经胶质瘤)、神经上皮瘤、神经鞘瘤、星形细胞瘤、神经纤维瘤(例如神经纤维肉瘤)、室管膜瘤、成神经管细胞瘤、脑膜瘤、脑转移瘤等)、呼吸道肿瘤(鼻咽癌、喉癌、支气管癌、肺癌等)、泌尿生殖系统肿瘤(前列腺癌、肾脏肿瘤、膀胱癌、乳腺癌、宫颈癌、卵巢癌、胎盘绒毛癌、尿路系统肿瘤、精囊腺肿瘤、睾丸及睾丸旁组织肿瘤、阴茎肿瘤、外阴癌、阴道癌、子宫癌、子宫内膜癌等)、血液淋巴系统肿瘤(白血病(例如慢性粒细胞白血病、急性髓系白血病、慢性淋巴细胞白血病、骨髓增生异常综合征、慢性骨髓细胞性白血病、急性淋巴细胞白血病等)、多发性骨髓瘤、间皮瘤、骨髓瘤、淋巴瘤(例如非霍奇金淋巴瘤、霍奇金淋巴瘤、皮肤t细胞淋巴瘤)、皮肤系统肿瘤(如皮肤癌、表皮样癌、黑色素瘤、基底细胞癌、鳞状细胞癌、paget病、卡波西肉瘤、merkel细胞癌、不典型纤维黄瘤、附属器肿瘤、皮肤t细胞淋巴瘤(蕈状肉芽肿)等)等以及横纹肌肉瘤、头颈部癌等。
160、本发明的第十一方面,提供了一种治疗肿瘤的方法,所述的方法包括向受试者施加治疗有效量的上述的干扰rna、上述的递送系统、上述的细胞、上述的脂质纳米颗粒、上述的药物或试剂盒或上述的抗体-核酸偶联药物。
161、优选的,所述的肿瘤包括消化道肿瘤(口腔癌、舌癌、食管癌、胃癌、肝癌、胰腺癌、结肠直肠癌等)、神经系统肿瘤(胶质瘤(例如神经胶质瘤)、神经上皮瘤、神经鞘瘤、星形细胞瘤、神经纤维瘤(例如神经纤维肉瘤)、室管膜瘤、成神经管细胞瘤、脑膜瘤、脑转移瘤等)、呼吸道肿瘤(鼻咽癌、喉癌、支气管癌、肺癌等)、泌尿生殖系统肿瘤(前列腺癌、肾脏肿瘤、膀胱癌、乳腺癌、宫颈癌、卵巢癌、胎盘绒毛癌、尿路系统肿瘤、精囊腺肿瘤、睾丸及睾丸旁组织肿瘤、阴茎肿瘤、外阴癌、阴道癌、子宫癌、子宫内膜癌等)、血液淋巴系统肿瘤(白血病(例如慢性粒细胞白血病、急性髓系白血病、慢性淋巴细胞白血病、骨髓增生异常综合征、慢性骨髓细胞性白血病、急性淋巴细胞白血病等)、多发性骨髓瘤、间皮瘤、骨髓瘤、淋巴瘤(例如非霍奇金淋巴瘤、霍奇金淋巴瘤、皮肤t细胞淋巴瘤)、皮肤系统肿瘤(如皮肤癌、表皮样癌、黑色素瘤、基底细胞癌、鳞状细胞癌、paget病、卡波西肉瘤、merkel细胞癌、不典型纤维黄瘤、附属器肿瘤、皮肤t细胞淋巴瘤(蕈状肉芽肿)等)等以及横纹肌肉瘤、头颈部癌等。
162、进一步优选的,所述的肿瘤选自泌尿生殖系统肿瘤和/或皮肤系统肿瘤。
163、在本发明的一个具体实施方式中,所述的肿瘤选自前列腺癌、乳腺癌或黑色素瘤。
164、本发明的第十二方面,提供了一种抑制细胞过度增殖的方法,所述的方法包括向受试者施加治疗有效量的上述的干扰rna、上述的递送系统、上述的细胞、上述的脂质纳米颗粒、上述的药物或试剂盒或上述的抗体-核酸偶联药物。
165、本发明的第十三方面,提供了一种抗有丝分裂的方法,所述的方法包括向受试者施加治疗有效量的上述的干扰rna、上述的递送系统、上述的细胞、上述的脂质纳米颗粒、上述的药物或试剂盒或上述的抗体-核酸偶联药物。
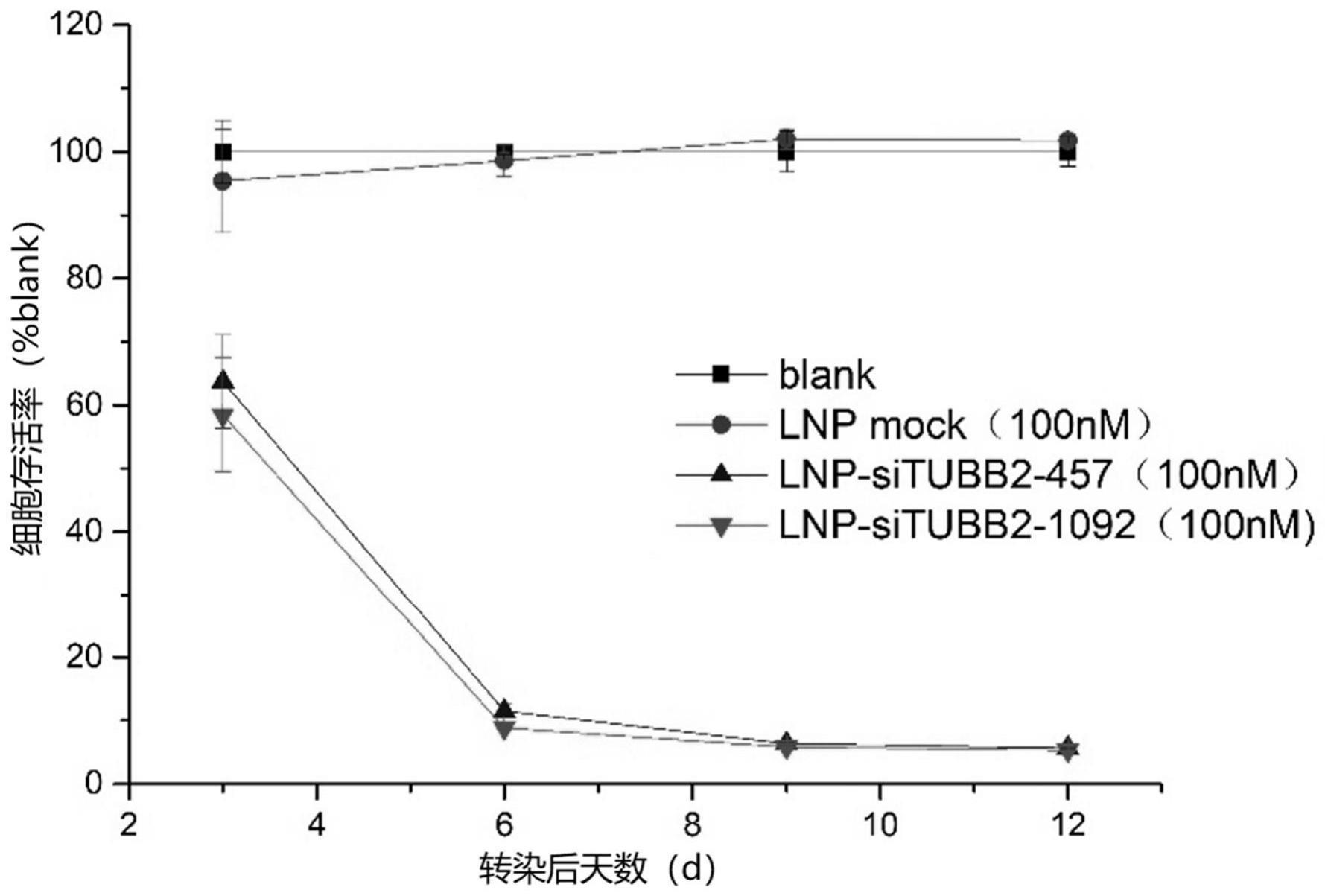
166、本技术筛选出的tubb2 sirna序列,可以用于细胞增殖旺盛相关疾病(如各种肿瘤等)的治疗,有强大的开发潜力。并经实验证实,可显著抑制多种细胞(如a375、mda-mb-231-gfp、pc-3、skov-3、hct116等细胞)中tubb2的mrna表达水平。因此,有望用于与微管蛋白表达增加相关的疾病,如各种恶性肿瘤等疾病状态,通过抑制微管蛋白β2的表达,阻断或降低细胞的增殖,实现减缓疾病进展和改善疾病转归的目的。
167、本发明所述的“干扰rna”,包括单链rna(例如,成熟mirna)或双链rna(例如,sirna、shrna、airna或前体mirna),当干扰rna与靶基因或序列处于同一细胞中时,能够降低或抑制靶基因或序列的表达(例如,通过介导降解和/或抑制与干扰rna序列互补的mrna的翻译)。
168、其中,sirna为小干扰rna,其分子的每条链包含长度为约15nt至约60nt的核苷酸(例如,长度为约15-60、15-50、15-40、15-30、15-25、或19-25nt的核苷酸,或者长度为15、16、17、18、19、20、21、22、23、24、或25nt的核苷酸)。在一个具体实施方式中,sirna可以是化学合成的。本发明的sirna分子能够在体外和/或体内沉默靶序列的表达。在一些实施方式中,sirna可以不含有修饰的核苷酸;在其他实施方式中,sirna包含至少一个修饰的核苷酸,例如sirna在双链区中包含一个、两个、三个、四个、五个、六个、七个、八个、九个、十个或更多个修饰的核苷酸。shrna为小发夹rna或短发夹rna,包括产生紧密发夹转角(hairpinturn)的短rna序列,所述发夹转角可以用于通过rna干扰来沉默基因表达,shrna发夹结构可由细胞机器裂解为sirna。mirna(微rna)是长度约21-23个核苷酸的调节基因表达的单链rna分子。
169、本发明所述的“抑制靶基因的表达”是指本发明的干扰rna(例如,sirna)沉默、降低或抑制靶基因(例如tubb2基因)表达的能力。
170、本发明所述的“包含”或“包括”为开放式写法,含有所描述的指定成分或步骤,以及不会实质上影响的其他指定成分或步骤。当用于描述蛋白质或核酸的序列时,所述蛋白质或核酸可以是由所述序列组成,或者在所述蛋白质或核酸的一端或两端可以具有额外的氨基酸或核苷酸,但仍然具有与原序列相同或相似的活性。
171、本发明所述的“肿瘤”可以是任何不良的细胞增殖(或本身表现为不良细胞增殖的任何疾病)、赘生物,或不良细胞增殖、赘生物或肿瘤的倾向性或风险增加。其可以是良性或恶性的,也可以是原发性或继发性(转移性)。赘生物可以是细胞的任何异常生长或增殖,并且可以位于任何组织中。组织的实例包括肾上腺、肾上腺髓质、肛门、阑尾、膀胱、血液、骨、骨髓、脑、乳腺、盲肠、中枢神经系统(包括或排除大脑)、小脑、子宫颈、结肠、十二指肠、子宫内膜、胆囊、食道、神经胶质细胞、心脏、回肠、空肠、肾、泪腺、喉、肝、肺、淋巴、淋巴结、上颌骨、纵隔、肠系膜、子宫肌层、鼻咽、网膜、口腔、卵巢、胰腺、腮腺、周围神经系统、腹膜、胸膜、前列腺、唾液腺、结肠、皮肤、软组织、脾、胃、睾丸、胸腺、甲状腺、舌、扁桃体、气管、子宫、外阴、直肠。进一步优选的,所述的肿瘤包括消化道肿瘤(口腔癌、舌癌、食管癌、胃癌、肝癌、胰腺癌、结肠直肠癌等)、神经系统肿瘤(胶质瘤(例如神经胶质瘤)、神经上皮瘤、神经鞘瘤、星形细胞瘤、神经纤维瘤(例如神经纤维肉瘤)、室管膜瘤、成神经管细胞瘤、脑膜瘤、脑转移瘤等)、呼吸道肿瘤(鼻咽癌、喉癌、支气管癌、肺癌等)、泌尿系统肿瘤(如肾细胞癌、膀胱癌等)、生殖系统肿瘤(前列腺癌、睾丸癌、乳腺癌、宫颈癌、卵巢癌、胎盘绒毛癌等)、血液淋巴系统肿瘤(多发性骨髓瘤、间皮瘤、骨髓瘤、淋巴瘤(例如非霍奇金淋巴瘤、霍奇金淋巴瘤、皮肤t细胞淋巴瘤)、白血病(例如慢性粒细胞白血病、急性髓系白血病、慢性淋巴细胞白血病、骨髓增生异常综合征等)、胸腺癌等)、皮肤系统肿瘤(如皮肤癌、表皮样癌、黑色素瘤等)等以及横纹肌肉瘤、头颈部癌等。
172、本发明所述的“受试者”可以为人或非人哺乳动物,所述的非人哺乳动物可以为野生动物、动物园动物、经济动物、宠物、实验动物等等。优选的,所述的非人哺乳动物包括但不限于猪、牛、羊、马、驴、狐、貉、貂、骆驼、狗、猫、兔、鼠(例如大鼠、小鼠、豚鼠、仓鼠、沙鼠、南美洲栗鼠、松鼠)或猴等等。
173、本发明所述的“治疗”表示在疾病已开始发展后减缓、中断、阻止、控制、停止、减轻、或逆转一种体征、症状、失调、病症、或疾病的进展或严重性,但不一定涉及所有疾病相关体征、症状、病症、或失调的完全消除。
174、本发明所述的“预防”表示为了阻止或延迟疾病或病症或症状在机体内的发生而实施的方式。
175、本发明所述“有效量”是指在以单个或多个剂量给予至受试者或其细胞或器官之后提供所希望的效果(例如治疗、预防或抑制tubb2表达)的本发明的产品的量或剂量。
176、本发明所述“脂质”是指一组有机化合物,其包括但不限于脂肪酸的酯,并且通常以难溶于水但可溶于许多有机溶剂为特征。
177、本发明所述“阳离子脂质”是指能够带正电的脂质分子。
178、本发明所述“中性脂质”术语是指不带电荷的、非磷酸甘油酯的脂质分子。
179、本发明所述“聚乙二醇脂质”是指包含脂质部分和聚乙二醇部分的分子。
180、本发明所述“脂质纳米颗粒”是指具有至少一个纳米量级尺寸的颗粒,其包含至少一种脂质。
181、本发明所述“递送系统”是指调控生物活性成分在空间、时间及剂量在生物体内分布的制剂或组合物。
- 还没有人留言评论。精彩留言会获得点赞!