一种基于CRISPR-Cas12a的BVDV特异crRNA及其相关试剂盒与检测方法
本发明属于病毒检测,具体涉及一种bvdv特异crrna及其相关试剂盒与检测方法。
背景技术:
1、牛病毒性腹泻(bvd)是由牛病毒性腹泻病毒(bvdv)引起的一种在世界范围内广泛流行的传染病。牛感染bvdv后轻则出现腹泻、发热症状,重则直接死亡,导致奶牛产奶量下降、育肥牛产肉质量降低及种用牛繁殖能力下降;孕畜感染则会发生流产,产出死胎或畸形胎。此外,如母畜在妊娠期40-120天感染,bvdv可通过胎盘传播至胎儿,若胎儿幸存则会成为持续感染(pi)牛,其分泌物和排泄物中存在大量病毒,是bvdv的主要传染源之一。
2、bvdv是单股正链rna病毒,属于黄病毒科瘟病毒属成员,病毒粒子有囊膜,具有耐高温、存活期长等特点。bvdv基因组全长为12.3 kb左右,由5'非编码区(5'utr),3'非编码区(3'utr)和开放阅读框(orf)组成,其中,最保守序列为5'utr。在所有的基因组区域中,5'utr、npro和e2基因被广泛地用于序列比对、基因分型和系统发育分析。据此,bvdv被分为三种主要基因型,即bvdv-1、bvdv-2和bvdv-3。又根据5'utr,bvdv-1被分为21个基因亚型(bvdv-1a至bvdv-1u),bvdv-2被分为4个亚型(bvdv-2a至bvdv-2d)。
3、因此,建立可用于现场的bvdv快速精确检测方法尤为重要,尤其是对精准剔除牛群中pi牛更为重要。
4、目前,bvdv的检测方法主要分为血清学检测方法、病毒抗原检测、经典病毒分离培养和病毒核酸检测。其中,普通pcr和qrt-pcr检测是最常用的病原体核酸检测技术;pi牛的筛选方法主要依赖于erns蛋白的捕获elisa和qrt-pcr检测。然而,这些检测方法均存在耗时长、假阳性率高、需要昂贵的仪器或专业的技术人员等缺点,并且无法实现现地快速检测。近几年迅速发展的环介导等温扩增(lamp)分析检测具有高灵敏的特点,但依然存在耗时较长,程序繁琐等缺点(maan s, maan n, batra k, kumar a, gupta a, rao p,hemadri d, reddy y, guimera m, belaganahalli m, mertens p. 2016. reversetranscription loop-mediated isothermal amplification assays for rapididentification of eastern and western strains of bluetongue virus in india.journal of virological methods, 234, 65-74. doi,10.1016/j.jviromet.2016.04.002.);逆转录-重组酶-聚合酶扩增的侧流试纸快速目视检测(rt-rpa lfd)方法可获得可视化结果,但其敏感性和特异性难以保证(yang s, wang q, tanb, shi p, qiao l, li z, liu k, cao z, zhang s, sun f. 2022. a lateral flowdipstick combined with reverse transcription recombinase polymeraseamplification for rapid and visual detection of the bvdv and bpiv3. journalof virological methods, 299, 114343. doi,10.1016/j.jviromet.2021.114343.)。
5、基于crispr技术的核酸检测方法因其特异性好、敏感性高、简单、易于现场实施而得到广泛应用。目前现有技术已建立了基于cas13a的基因3型bvdv和bvdv nadl毒株的检测方法,例如,申请号为cn202310728497.8,发明名称为一种用于检测牛病毒性腹泻病毒3型的试剂盒与检测方法及申请号为cn202010905632.8,发明名称为基于crispr-cas13a的牛病毒性腹泻病毒的检测方法的专利,然而上述方法检测只能针对特定毒株进行检测,具有检测局限性,且敏感性偏低。与cas13a具有切割单链rna的活性不同,cas12a具有切割双链dna片段活性,当cas12-crrna-靶标dna序列三元复合物形成时,cas12蛋白表现出反式切割活性。通过将cas12蛋白与预扩增步骤相结合,可开发更灵敏的核酸检测生物传感器平台。
6、因此,开发一种基于crispr-cas12a的快速、灵敏度高、特异强,不依赖实验室精密仪器,且可在1小时内得到可视化检测结果的bvdv现地检测方法具有重要应用前景及实践意义。
技术实现思路
1、本发明公开了一种基于crispr-cas12a的bvdv特异crrna及其相关试剂盒与检测方法,解决了现有的bvdv检测方法耗时长、假阳性率高、需要昂贵仪器或专业技术人员、无法实现现场实时检测的技术问题。
2、本发明的技术方案如下:
3、一种基于crispr-cas12a的bvdv特异crrna,所述bvdv特异crrna为seq id no.1~seq id no.6任一所示crrna或seq id no.1~seq id no.6所示任意两种以上crrna混合。
4、进一步的,所述bvdv特异crrna为seq id no.1、seq id no.3、seq id no.4和seqid no.5所示的crrna等比例混合。
5、一种基于crispr-cas12a的检测不同亚型bvdv的试剂,所述基于crispr-cas12a的检测不同亚型bvdv的试剂包括上述bvdv特异crrna。
6、上述bvdv特异crrna在制备检测bvdv的试剂盒中的应用。
7、上述试剂在制备检测bvdv的试剂盒中的应用。
8、一种基于crispr-cas12a的检测不同亚型bvdv的试剂盒,所述试剂盒包括上述bvdv特异crrna,bvdv 5'utr基因等温扩增试剂、crispr-cas12a蛋白酶,ssdna报告系统,核酸酶抑制剂和nebuffer 3.1。
9、进一步的,所述bvdv 5'utr基因等温扩增试剂包括等温扩增引物对,所述等温扩增引物对的上游引物为如seq id no.13所示的核苷酸序列,下游引物为如seq id no.17所示的核苷酸序列。
10、进一步的,所述ssdna报告系统为5'端fam标记、3'端bhq1标记的单链核苷酸序列。
11、所述试剂盒在非疾病诊断目的的bvdv可视化检测中的应用。
12、一种可视化检测bvdv的方法,采用上述试剂盒进行检测,包括如下步骤:
13、s1、取待测样品,利用核酸释放剂释放样品中的核酸;
14、s2、将s1获得的核酸和上述等温扩增引物对加入到逆转录-重组酶聚合酶扩增体系中进行扩增,获得特异性产物;
15、s3、将s2获得的特异性产物加入crispr-cas12a检测体系中,对特异性产物进行识别切割;
16、s4、利用荧光酶标仪或荧光灯肉眼直接检测判读待测样品中是否存在bvdv特异性核酸。
17、本发明通过序列比对和筛选,获得了6种bvdv特异crrna,并且通过对6种bvdv特异crrna及由其组成的混合物的筛选发现crrna混合物1在crispr反应中可检测目前流行bvdv亚型的所有毒株。
18、本发明通过序列比对和筛选,设计的rt-era引物可特异性扩增靶标序列,产物可用于下游crispr反应。
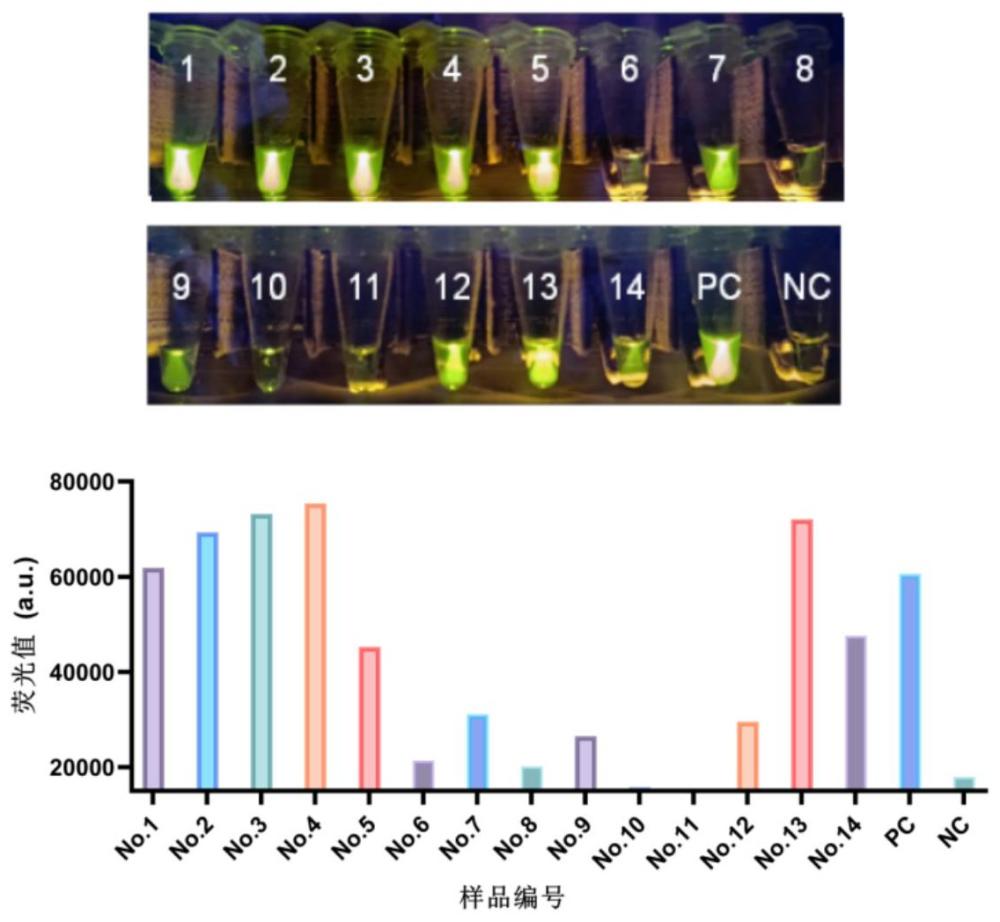
19、本发明将逆转录-重组酶聚合酶扩增(rt-era)技术与crispr-cas12a系统相结合,建立了一种快速、灵敏高、特异性强的bvdv结果可视的检测方法,用于bvdv的快速现场诊断。本发明所述的检测方法能够在45分钟内检测低至20个拷贝载量的病毒,并且不与其他共感染病原体发生交叉反应,包括牛轮状病毒(brv)、牛冠状病毒(bcov)、牛副流感病毒3型(bpiv-3)、传染性牛鼻气管炎病毒(ibrv)和牛呼吸道合胞病毒(brsv)。本发明所述的检测方法可以识别当前流行的所有已知的bvdv-1和bvdv-2亚型。本发明中对112个临床样本进行了检测,本发明所述检测方法与rna提取样本的定量pcr(qpcr)结果一致,对无提取bvdv样本的敏感性更高。现地样品检测的核酸阳性率为14.3%,与qpcr相符,并且可以不依赖实验室精密仪器得到可视的检测结果,适用于基层bvdv的筛检工作。
20、本发明所述的试剂盒及检测方法快速、灵敏度高、特异强,不依赖实验室精密仪器,且可得到可视化检测结果,具有重要应用前景及实践意义。
- 还没有人留言评论。精彩留言会获得点赞!