一种孔径可调的核壳固定相的制备方法与流程
本发明属于分析化学的色谱分析领域,具体涉及一种孔径可调的大孔核壳固定相的制备。
背景技术:
核壳颗粒的制备技术最早由horvath[horvath,c.g.;preiss,b.a.;lipsky,s.r.anal.chem.1967,39,1422-1428]和kirkland[kirkland,j.j.anal.chem.1969,41,218-220]两人提出。最初的核壳颗粒的粒径为50μm左右,表面覆盖了一层厚度约1μm的壳层。这种颗粒的最大缺点是柱容量偏低。10年前,kirkland制备出了新一代的核壳颗粒,其商品名称为halo[destefano,j.j.;langlois,t.j.;kirkland,j.j.j.chromatogr.sci.2008,46,254-260]。该颗粒粒径为2.7μm,壳层厚度则约为0.5μm。对比传统的核壳颗粒,其柱容明显增加。更为突出的是,该类型颗粒由于具有较短的传质距离和更为均一的颗粒粒径分布,因而取得了极高的分离柱效。填充新一代核壳颗粒的分离柱的柱效约为填充了同样粒径的多孔颗粒柱的1倍。因而,发展更多方法制备新型核壳颗粒成为了目前色谱固定相制备领域最受关注的研究课题。
通常,核壳颗粒采用层层组装法制备。采用该方法制备核壳颗粒的最大缺点是工艺复杂且耗时。根据报道,制备厚度为0.5μm的壳层需要40-50步制备工序。为了克服这个缺点,chen等人开发了一种凝聚法制备核壳颗粒的方法。该法仅需2-3步即可获得多孔壳层[chen,w.;jiang,k.;mack,a.;sachok,b.;zhu,x.;barber,w.e.;wang,x.j.chromatogr.a2015,1414,147-57]。该方法的主要缺点是制备过程中会生成小颗粒及出现颗粒团聚现象,因而需要额外的颗粒筛分过程。
颗粒孔径大小是影响色谱分离效率的一个重要指标。颗粒孔径过小,样品分子无法进入孔道内部与固定相作用,因而分离效率低。目前市售的核壳颗粒的孔径多为9-12nm。这个孔径大小可以对小分子化合物实现高效的分离,但对分离蛋白质,特别是生物大分子,这个孔径偏小。然而,目前报道的几种制备核壳颗粒的主要方法均无法实现对壳层孔径进行简单有效的调控,需要采用后处理方法对制备得到的核壳颗粒进行扩孔。目前,商品颗粒主要采用碱腐蚀的方法来增大孔径,该方法虽然可以实现颗粒孔径提高到20nm以上,但该法在操作过程中会导致部分颗粒出现粘连,很容易出现颗粒团聚,造成柱效的下降。此外,碱溶解法也会导致壳层机械强度下降。因此,开发新的简单的孔径控制方法对提升核壳颗粒的分析范围至关重要。
技术实现要素:
为了解决现有技术无法有效控制颗粒孔径、层层组装法工艺复杂、碱溶解法扩孔导致颗粒粘连及柱效和机械强度下降的技术问题,本专利提供了一种基于两相法、自由调控颗粒孔径和一步反应的孔径可调的核壳固定相的制备方法。
为解决上述技术问题,本发明提供一种孔径可调的核壳固定相的制备方法,其特征在于包括下列具体步骤:
(1)将sio2无孔颗粒、十六烷基三甲基溴化铵(ctab)、尿素和异丙醇按质量比5:5:3:3.6混合,然后加入30倍sio2无孔颗粒质量的水中,室温下搅拌0.5h。
(2)量取与步骤(1)中水同体积的有机溶剂,再按有机溶剂和正硅酸四乙酯体积30:1的比例将正硅酸四乙酯加入有机溶剂中,将此混合液搅拌状态下加入步骤(1)的溶液中,搅拌速度控制在200rpm,保持搅拌状态,70℃下反应16h。
(3)将所得颗粒用乙醇溶液和水分别离心清洗。接着将颗粒放入100℃烘箱干燥5h,然后放入马弗炉中于550℃下煅烧4h。
优选的,所述有机溶剂为苯、甲苯、混二甲苯、均三甲苯、环己烷、十三烷,n,n-二甲基苯胺或其它不溶解于水且相对极性大小小于0.2的有机溶剂。
优选的,所述孔径可调的核壳固定相的孔径为3-37nm。
优选的,1所述孔径可调的核壳固定相的制备方法,包括下列步骤:
(1)将0.5gsio2无孔颗粒,0.5g十六烷基三甲基溴化铵(ctab),0.3g尿素,0.46ml异丙醇加入15mlh2o中,室温下搅拌0.5h。
(2)将15ml苯和0.5ml正硅酸四乙酯在搅拌下加入步骤(1)溶液中,搅拌速度控制在200rpm,保持搅拌状态,在70℃下反应16h。
(3)将所得颗粒用乙醇溶液和水分别离心清洗。接着将颗粒放入100℃烘箱干燥5h,然后放入马弗炉中于550℃下煅烧4h。
本发明还提供一种利用上述方法所制备的孔径可调的核壳固定相,通过下列步骤制备而成:
(1)将sio2无孔颗粒、十六烷基三甲基溴化铵(ctab)、尿素和异丙醇按质量比5:5:3:3.6混合,然后加入30倍sio2无孔颗粒质量的水中,室温下搅拌0.5h。
(2)量取与步骤(1)中水同体积的有机溶剂,再按有机溶剂和正硅酸四乙酯体积30:1的比例将正硅酸四乙酯加入有机溶剂中,将此混合液搅拌状态下加入步骤(1)的溶液中,搅拌速度控制在200rpm,保持搅拌状态,70℃下反应16h。
(3)将所得颗粒用乙醇溶液和水分别离心清洗。接着将颗粒放入100℃烘箱干燥5h,然后放入马弗炉中于550℃下煅烧4h。
与现有技术相比,本发明取得的有益效果为:(1)本发明基于两相法,通过一步反应,改变了传统核壳固定相采用后处理法扩孔的方法,直接在核壳固定相的制备过程中,对于相对极性小于0.2的有机溶剂,只要通过选择不同相对极性的有机溶剂作为油相,就可实现对颗粒孔径的有效调控。(2)通过选择不同相对极性的有机溶剂作为油相,一步法可控合成孔径大小可调(3-37nm)的核壳固定相,大大节省了工艺步骤,采用液相色谱分析法实现了对中性和碱性样品、多肽和小分子量的蛋白质、以及大分子量蛋白质的有效分离,该发明具有广泛的应用价值。
附图说明
图1是实施例1所制得的核壳固定相的tem照片。
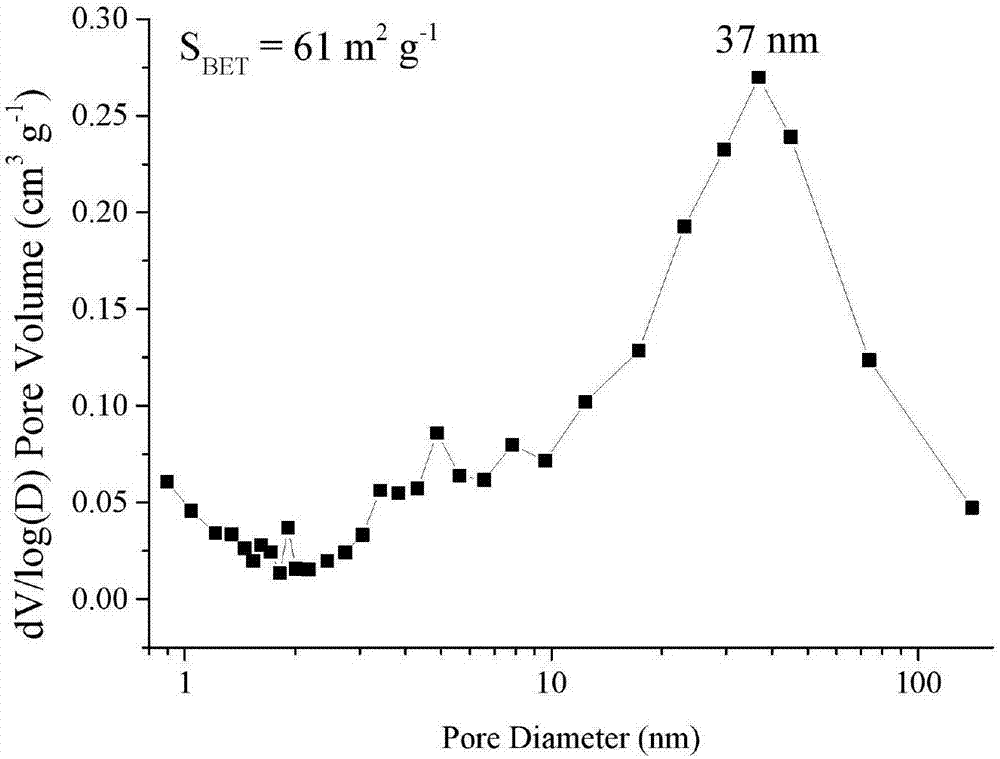
图2是实施例1所制得的核壳固定相的孔径分布图。
图3是实施例1所制得的核壳固定相分离一组中性和碱性样品的色谱图。
图4是实施例1所制得的核壳固定相分离一组多肽和小分子量蛋白质的色谱图。
图5是实施例1所制得的核壳固定相分离一组大分子量蛋白质的色谱图。
图6是实施例1所制得的核壳固定相经70mpa高压处理后的颗粒的sem照片。
图7是实施例2所制得的核壳固定相的tem照片。
图8是实施例2所制得的核壳固定相的孔径分布图。
图9是实施例3所制得的核壳固定相的tem照片。
图10是实施例3所制得的核壳固定相的孔径分布图。
图11是实施例4所制得的核壳固定相的tem照片。
图12是实施例4所制得的核壳固定相的孔径分布图。
图13是实施例5所制得的核壳固定相的tem照片。
图14是实施例5所制得的核壳固定相的孔径分布图。
图15是实施例6所制得的核壳固定相的tem照片。
图16是实施例6所制得的核壳固定相的孔径分布图。
图17是实施例7所制得的核壳固定相的tem照片。
图18是实施例7所制得的核壳固定相的孔径分布图。
图19是实施例8所制得的核壳固定相的tem照片。
图20是实施例8所制得的核壳固定相的孔径分布图。
具体实施方式
下面结合具体实施例对本发明的技术方案作进一步具体说明。
实施例1
孔径可调的核壳固定相的制备方法:将0.5gsio2无孔颗粒,0.5g十六烷基三甲基溴化铵(ctab),0.3g尿素,0.46ml异丙醇加入15mlh2o中,室温下搅拌0.5h。之后,将15ml有机溶剂苯(相对极性0.111)和0.5ml正硅酸四乙酯在搅拌下加入上述溶液中,溶液的搅拌速度控制在200rpm,保持搅拌状态,在70℃下反应16h。反应结束后将所得颗粒用乙醇溶液和水分别离心清洗。接着将颗粒放入100℃烘箱干燥5h,然后放入马弗炉中于550℃下煅烧4h。
将煅烧后的产品采用tem测试其结构,采用氮气吸附法测试其孔径和比表面积。图1为制备得到的核壳固定相的tem照片。从图中可以看到制备得到的颗粒具有明显的核壳结构,修饰获得的壳层具有特殊的放射状结构,壳层厚度约200nm。图2为制备得到的核壳固定相氮气吸附法测定结果。测得孔径d=37nm,比表面积s=61m2g-1。
将制备得到的核壳固定相衍生c18,再采用匀浆法将核壳固定相填充入内径4.6mm,长度为10cm的不锈钢管柱中。采用液相色谱分离模式分离一组中性和碱性样品,分离结果如图3,分离条件为:流速,1.0mlmin-1;流动相,acn/h2o=55/45(v/v);进样量,1μl;检测波长254nm;分离温度,25℃。出峰顺序及相应色谱柱效1.茶碱(27163塔板数m-1),2.尼泊金甲酯(44056塔板数m-1),3.尼泊金乙酯(55671塔板数m-1),4.邻硝基苯胺(57391塔板数m-1),5.尼泊金丙酯(65420塔板数m-1),6.尼泊金丁酯(88179塔板数m-1),7.溴苯(188373塔板数m-1),8.邻二氯苯(204890塔板数m-1),9.萘(146116塔板数m-1),10.间二氯苯(207600塔板数m-1),11.对二氯苯(219633塔板数m-1),12.联苯(243074塔板数m-1),13.二甲基萘(245923塔板数m-1),14.芴(264531塔板数m-1)。该色谱柱柱效远高于普通全多孔颗粒填充柱的柱效,也高于采用层层组装法获得的核壳颗粒的柱效,这表明特殊的放射状壳层结构可以显著的提高色谱分离柱效。
将制所得核壳固定相衍生c18,再采用匀浆法将核壳固定相填充入内径4.6mm,长度为10cm的不锈钢管柱中,采用液相色谱分离模式分离一组多肽和小分子量的蛋白质,分离结果如图4,分离条件为:流速,1.0mlmin-1;流动相a,10%acn-0.1%三氟乙酸;流动相b,acn/h2o/三氟乙酸=70/30/0.1(v/v);梯度分离,5min内从25%b升至60%b;进样量,1μl;检测波长220nm;分离温度,30℃。出峰顺序1.甲硫啡肽(111450理论塔板数m-1),2.牛胰岛素(144979理论塔板数m-1)),3.细胞色素c(183334理论塔板数m-1)),4.溶菌酶(197037理论塔板数m-1))。以上分离结果表明具有大孔结构的核壳固定相对于多肽和小分子量的蛋白质这一类分子量不是很大的样品仍然具有极高的分离柱效。
为了进一步考察所制得核壳固定相对大分子物质的分离效果,将所制得的核壳固定相衍生c18,再采用匀浆法将核壳固定相填充入内径4.6mm,长度为10cm的不锈钢管柱中,采用液相色谱分离模式对一组大分子量的蛋白质进行分离,分离结果如图5,分离条件:流速,1.0mlmin-1;流动相a,10%acn-0.1%三氟乙酸;流动相b,acn/h2o/三氟乙酸=75/25/0.1(v/v);梯度分离,8min内从36%b升至60%b;进样量,1μl;检测波长280nm;分离温度,30℃。出峰顺序1.α-糜蛋白酶(25kda),2.过氧化氢酶(60kda),3.烯醇酶(47kda),4.碳酸酐酶(29kda),5.淀粉酶(200kda)。从图中可以看到,所有5种大分子量的蛋白质均可在7min内实现快速基线分离,充分证明了具有大孔结构的核壳固定相的超高分离能力。
将采用本实施例制备得到的核壳固定相衍生c18,再采用匀浆法将核壳固定相填充入内径4.6mm,长度为10cm的不锈钢管柱中,填充压力为70mpa。填充后取少量核壳固定相采用扫描电镜观察(图6),未发现壳层破损及脱落现象,说明采用该方法制备得到的核壳固定相具有良好的机械稳定性。
实施例2
采用n,n-二甲基苯胺(相对极性0.179)作为有机溶剂,其他制备步骤同实施例1的孔径可调的核壳固定相的制备方法。将制得的产品采用tem测试其结构,采用氮气吸附法测试其孔径和比表面积。图7为制备得到的核壳固定相的tem照片。图8为所制得的核壳固定相的氮气吸附法测定结果,测得孔径d=3nm,比表面积s=157m2g-1。
实施例3
采用十三烷(相对极性0.005)作为有机溶剂,其他制备步骤同实施例1孔径可调的核壳固定相的制备方法。将制得的产品采用tem测试其结构,采用氮气吸附法测试其孔径和比表面积。图9为制备得到的核壳固定相的tem照片。从图中可以看到制备得到的颗粒具有明显的核壳结构,修饰获得的壳层具有特殊的放射状结构,壳层厚度约200nm。图10为核壳固定相氮气吸附法测定结果。测得孔径d=5.5nm,比表面积s=140m2g-1。
实施例4
采用环己烷(相对极性0.006)作为有机溶剂,其他制备步骤同实施例1孔径可调的核壳固定相的制备方法。将制得的颗粒采用tem测试其结构,采用氮气吸附法测试其孔径和比表面积。图11为制备得到的核壳固定相的tem照片。从图中可以看到制备得到的颗粒具有明显的核壳结构,修饰获得的壳层具有特殊的放射状结构,壳层厚度约160nm。图12为制备得到的核壳固定相的氮气吸附法测定结果。测得孔径d=7.1nm,比表面积s=121m2g-1。
实施例5
采用混二甲苯(相对极性0.070)作为有机溶剂,其他制备步骤同实施例1孔径可调的核壳固定相的制备方法。将制得的颗粒采用tem测试其结构,采用氮气吸附法测试其孔径和比表面积。图13为制备得到的核壳固定相的tem照片。从图中可以看到制备得到的颗粒具有明显的核壳结构,修饰获得的壳层具有特殊的放射状结构,壳层厚度约150nm。图14为制备得到的核壳固定相的氮气吸附法测定结果,测得孔径d=18nm,比表面积s=95m2g-1。
实施例6
采用对二甲苯(相对极性0.074)作为有机溶剂,其他制备步骤同实施例1孔径可调的核壳固定相的制备方法。将制得的颗粒采用tem测试其结构,采用氮气吸附法测试其孔径和比表面积。图15为制备得到的核壳固定相的tem照片。从图中可以看到制备得到的颗粒具有明显的核壳结构,修饰获得的壳层具有特殊的放射状结构,壳层厚度约200nm。图16为制备得到的核壳固定相的氮气吸附法测定结果。测得孔径d=20nm,比表面积s=85m2g-1。
实施例7
采用均三甲苯(相对极性0.091)作为有机溶剂,其他制备步骤同实施例1孔径可调的核壳固定相的制备方法。将制得的颗粒采用tem测试其结构,采用氮气吸附法测试其孔径和比表面积。图17为制备得到的核壳固定相的tem照片。从图中可以看到制备得到的颗粒具有明显的核壳结构,修饰获得的壳层具有特殊的放射状结构,壳层厚度约220nm。图18为制备得到的核壳固定相的氮气吸附法测定结果,测得孔径d=23nm,比表面积s=107m2g-1。
实施例8
采用甲苯(相对极性0.099)作为有机溶剂,其他制备步骤同实施例1孔径可调的核壳固定相的制备方法。将制得的颗粒采用tem测试其结构,采用氮气吸附法测试其孔径和比表面积。图19为制备得到的核壳固定相的tem照片。从图中可以看到制备得到的颗粒具有明显的核壳结构,修饰获得的壳层具有特殊的放射状结构,壳层厚度约300nm。图20为制备得到的核壳固定相的氮气吸附法测定结果,测得孔径d=30nm,比表面积s=140m2g-1。
实际上,本发明中油相的选择不仅限于以上实施例中用到的苯、甲苯、混二甲苯、均三甲苯、环己烷、十三烷和n,n-二甲基苯胺,其它不溶解于水且相对极性大小小于0.2的有机溶剂均适用于本技术方案。
上述实施例所制备的孔径可调的核壳固定相孔径可调、机械强度好、制备工艺简单、孔径范围宽,能够采用液相色谱分析法,实现对中性和碱性样品、多肽和小分子量的蛋白质、以及大分子量蛋白质等多种分子有效分离,具有潜在的应用价值,是一种理想的核壳固定相。
最后所应说明的是,以上具体实施方式仅用以说明本发明的技术方案而非限制,尽管参照较佳实施例对本发明进行了详细说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本发明技术方案的精神和范围,其均应涵盖在本发明的权利要求范围当中。
- 还没有人留言评论。精彩留言会获得点赞!