具有可控气氛的酶标仪及相应方法与流程
技术领域
本发明涉及一种酶标仪,所述酶标仪包括至少一个测量装置和一保持装置。所述至少一个测量装置用于检测插于所述酶标仪中的微孔板的孔内的样品所射出的光和/或插于所述酶标仪中的微孔板的孔内的被光穿透的样品所影响的光。所述保持装置用于容纳至少一个微孔板和相对于所述至少一个测量装置定位所述一或多个微孔板的包含样品的孔。本发明还涉及所述酶标仪的相应方法和特定用途。
背景技术:
很多年来,现有技术所知的一般酶标仪的原理是测量用试剂处理过的样品的发光和/或荧光。发光或荧光通常是指来自样品的光发射,其中发光是由在样品中化学反应过程引起的,荧光是由激发光的辐射引起的。这样的酶标仪用于观测加入了试剂的样品中的反应或者检测能够发出荧光的样品组分。
用于触发发光反应的已知酶标仪包括注射装置,其用于将试剂加入到插于所述酶标仪的一或多个微孔板的孔内的样品中。还知道酶标仪包括照明装置,用于照射或透照在所述酶标仪的一或多个微孔板的孔内的样品。这样的酶标仪用于测量样品中被激发的荧光或由样品所影响的透光率(吸光度)的减少程度。
技术实现要素:
本发明的目的是提供一种酶标仪,在酶标仪中测量活细胞的相应方法,以及所述酶标仪的用途,所述酶标仪可观测样品中的反应和/或在至少近似生理状态下检测特定的样品组分。
根据本发明公开的第一方面所涉及的酶标仪,可实现本发明的所述目的。所述酶标仪包括:
a)至少一个测量装置,所述测量装置选自包括以下测量装置的组:
a1)第一测量装置,所述第一测量装置设计成测量用在或插于酶标仪中的微孔板的孔内的样品的吸光度,
a2)第二测量装置,所述第二测量装置设计成测量用在或插于酶标仪中的微孔板的孔内的被光照射的样品的荧光,
a3)第三测量装置,所述第三测量装置设计成测量用在或插于酶标仪中的微孔板的孔内的样品的发光;
b)保持装置,所述保持装置用于容纳至少一个微孔板,并且相对于至少一个测量装置来定位这个或这些微孔板的包含样品的孔;
c)控制单元,所述控制单元控制用在或插于酶标仪中的微孔板的包含样品的孔周围的气氛的温度。
替换地,所述酶标仪还包括:
d1)分隔板,所述分隔板将酶标仪的外壳的内部空间分隔成器具隔室和样品隔室,并且包括至少一个开口,所述分隔板设计成使得用在酶标仪中的微孔板的孔内的样品所射出的光或所影响的光能够穿过所述开口从样品隔室进入器具隔室;或者
d2)内部壳体,所述内部壳体设于酶标仪的外壳内,保持装置设于内部壳体内,内部壳体将酶标仪的外壳的内部空间分隔成器具隔室和包围保持装置的样品隔室,内部壳体包括至少一个开口,所述开口设计成使得用在酶标仪中的微孔板的孔内的样品所射出的光或所影响的光能够穿过所述开口从样品隔室进入器具隔室。
对于分隔板和内部壳体,这两个替换的分区装置的主要功能是一样的,即将样品隔室与器具隔室分隔开,以使在样品隔室内的样品只有当想要的时候才受器具影响。
在所述外壳的内部空间中,所述酶标仪设计成通过分隔板或内部壳体将样品隔室与器具隔室分隔成大体不透光和大体不透气。为此,开口可能包括相应的防护装置。替换地或除此之外,可设置沿开口四周延伸的防护装置。在本发明的实施例中,防护装置可设计成所述防护装置主要影响光大体上穿过开口,即使得用在酶标仪中的微孔板的孔内的样品所射出的光或所影响的光可穿过开口从样品隔室进入器具隔室,而尽可能完全阻挡其它光(不是样品所射出的光或所影响的光)穿过开口。
在样品隔室内设置有运动装置,所述运动装置用于混合和/或循环出现在样品隔室内的气体和/或流入样品隔室内的气体。
运动装置可包括以下器件中的至少一个器件:吹风机、包括一或多个挡板的器件、包括一或多个桨的搅拌器、或者结构化喷嘴系统。由此,包括一或多个挡板的器件可设于样品隔室的气体入口附近。包括一或多个桨的搅拌器可设置在保持装置附近。结构化喷嘴系统可包括多个入口喷嘴,这些入口喷嘴大体均匀地分布在样品隔室内,以致于在气体穿过入口喷嘴流入样品隔室的过程中,样品隔室内的气氛大体均匀地移动和混合。入口喷嘴可设置成沿气体入口管道优选为等距地分布。气体入口管道可藏于整体上大致平行于样品隔室的壁表面(诸如顶壁表面或底壁表面)配置的装置内。所述装置可包括大体S形的装置、多个大体S形的装置和/或大体螺旋状的装置。替换地或除此之外,气体入口管道可分成两个或多个气体入口子管道,或以至少分叉成一段或多段,形成两个或多个气体入口子管道。
控制单元可包括计算机(诸如存储有相应的软件的计算机),其中所述计算机可连接至酶标仪的中央计算机或集成在酶标仪的中央计算机内。替换地,控制单元可包括具有相应的软件的计算机,其中所述计算机可连接至酶标仪的中央计算机且设置在分离的外壳内。
控制单元可设计成控制包括达到4种、5种、6种或更多种不同气体的气氛的组成。为实现这一目的,控制单元可包括气体传感器,用于测量样品隔室内的不同气体,即控制用在所述酶标仪中的微孔板的包含样品的孔周围的气氛的组成。不受此约束,酶标仪可包括气体入口(特别是不具有气体传感器的气体入口),所述入口可被控制单元致动且允许气体进入样品隔室。
所述不同气体中的至少一种气体可选自包括氮气(N2)、二氧化碳(CO2)、氧气(O2)、一氧化碳(CO)、硫化氢(H2S)和二氧化硫(SO2)的组。
控制单元优选地包括:O2传感器,用于测量和控制用在所述酶标仪中的微孔板的包含样品的孔周围的气氛中的氧气含量;以及CO2传感器,用于测量和控制用在所述酶标仪中的微孔板的包含样品的孔周围的气氛中的二氧化碳含量。
不受此约束和/或更进一步地,控制单元设计成控制所述气氛的湿度和温度。为实现这一目的,控制单元可包括在样品隔室内的用于测量气氛的湿度的湿度传感器和用于测量气氛的温度的温度传感器。
不受此约束和/或更进一步地,控制单元可包括用于冷却样品隔室的冷却装置和/或用于加热样品隔室的加热装置。优选地,加热装置安装在分隔板或内部壳体上且与样品隔室内的气氛为热交换连通,而冷却装置安装在样品隔室的底部且与样品隔室内的气氛为热交换连通。加热装置可安装在设于分隔板的样品隔室侧或内部壳体的内部空间侧的板上。优选地,所述板以不导热的方式与分隔板或内部壳体连接。通过布置这些加热装置和冷却装置,避免了微孔板上的、或者微孔板的孔附近、孔上和/或孔内的湿气或水凝结。这里所公开的冷却装置或加热装置同样适用于具有分隔板或内部壳体的酶标仪的设计。
在酶标仪内可配置分离的通风装置,其可设于器具隔室内。通风装置用于冷却光源(诸如灯)和/或其它会产生热量的装置。通风装置的致动和运行可独立于设于样品隔室内的加热装置或冷却装置。
在酶标仪中,第一测量装置、第二测量装置和/或第三测量装置可分别包括具有光入射点和光出射点的光引导件和配置成用于测量从所述出射点射出的光的光检测器。光进入第一测量装置的第一接收点、光进入第二测量装置的第二接收点和光进入第三测量装置的第三接收点分别设于样品隔室内。
在本文中,术语光引导件应当理解为光纤、光纤束或镜系统。做成光纤、光纤束或镜系统的光引导件包括光入射点、光出射点和光引导通道,光引导通道从入射点延伸至出射点,光引导件引导光沿光引导通道传输。
在酶标仪中,第一、第二和/或第三测量装置的相应的光引导件可做成光纤或光纤束。替换地,相应的光引导件可做成镜系统。也可采用光纤和镜的组合来照射样品以及探测来自样品的光。第一、第二和/或第三测量装置的相应的光检测器可设于样品隔室或器具隔室内。
在酶标仪中,第一测量装置的第一光检测器和/或第三测量装置的第三光检测器可设于样品隔室内。在酶标仪中,第二测量装置的第二光检测器设计成用于测量孔内的荧光,它可设于器具隔室内。
酶标仪可包括至少一个照明装置,所述照明装置设计成光透照或照射于酶标仪中的微孔板的孔内的样品。照明装置包括光源和光引导件,所述光引导件用于将由所述光源产生的至少一部分光引导进入用于酶标仪中的微孔板的孔内或引导至设于孔内的样品中。
可配置第一、第二和/或第三照明装置,分别用于相应的第一、第二和/或第三测量装置。然而,还可以为第一和第二测量装置、第二和第三测量装置、第一和第三测量装置或者第一、第二和第三测量装置配置一共用的照明装置。
照明装置的光源可选自包括激光、频闪灯、LED(发光二极管)和激光二极管的组。
在酶标仪的特定用途中,重要的是检测作为微孔板的孔内的样品的细胞培养体的生长或转化的动力学。通过测量或检测特别是细胞培养体(样品)的吸光度、荧光和/或发光(优选为细胞培养体(样品)的发光)随时间的变化来测量或检测这些动力学。
对于测量或检测进行得较快的动力学,有必要,特别优选地,使照明装置的光源产生较短的光脉冲。因此,脉冲激光、频闪灯、以脉冲模式运作的LED(发光二极管)、和/或以脉冲模式运作的激光二极管适于用作实现这个目的光源。
在酶标仪中可配置不能被主动冷却的频闪灯作为光源。所述频闪灯可设于器具隔室内。而且,可通过光引导件将由所述光源产生的光引导至配置在酶标仪中的微孔板的孔内的样品,从而照射和/或透照样品。
酶标仪可包括第一照明装置,其设计成光透照过在酶标仪中的微孔板的孔内的样品,并且设于器具隔室内。因此,第一测量装置可设于样品隔室内。第二测量装置可设于器具隔室内。第三测量装置可设于样品隔室内或器具隔室内。所以光进入第一测量装置的第一接收点、光进入第二测量装置的第二接收点和光进入第三测量装置的第三接收点分别设于样品隔室内。
酶标仪可包括第一照明装置,其设计成光透照过用在酶标仪中的微孔板的孔内的样品。因此,第一照明装置的出射点可设于样品隔室内。酶标仪还可包括设于器具隔室内的第二照明装置,其设计成光照射于酶标仪中的微孔板的孔内的样品。所以第二照明装置的出射点可设于样品隔室内。第二照明装置可选自包括激光、频闪灯、LED(发光二极管)和激光二极管的组。
第一、第二和/或第三测量装置可包括第一、第二和/或第三光学系统,其中这些光学系统中的至少一个光学系统和/或所使用的(所插入的)微孔板被设计成能够沿笛卡尔坐标系统的Z轴方向相对于彼此移动。因此,所使用的(所插入的)微孔板可设计成能够沿Z轴方向移动。替换地或除此之外,第一、第二和/或第三光学系统可设计成能够沿Z轴方向移动。优选地,可设计第一、第二和/或第三光学系统,以致于第一、第二和/或第三光学系统能够往下移以使其一部分穿过分隔板内的或者内部壳体的壁(诸如顶壁)内的至少一个开口而进入样品隔室内。
在酶标仪中测量活细胞的相应方法(如下所述)和/或在酶标仪的用途中(如下所述),可以诸如使用注射装置将试剂加入至微孔板的至少一个孔内的至少一个样品中,并且触发化学反应。触发化学反应可能伴随样品发生发光反应,或者改变样品的发光性质、改变荧光性和/或改变吸光度。例如,通过使用至少一个测量装置,诸如通过观测(测量或检测)样品的发光和/或荧光和/或吸光度,可检测到这些现象。
对于添加试剂,酶标仪可包括相应的注射装置,其设计成将试剂加入至用在酶标仪中的微孔板的孔内的样品中。注射装置可分配试剂,所述试剂可触发刚好位于第三测量装置的光轴上的孔内发生化学反应或者伴随触发化学反应而来的发光反应。可以在添加试剂的同时(诸如通过观测发光反应)对化学反应进行观测(测量或检测),其中添加试剂与发生化学反应之间有一段时间间隔。替换地或除此之外,可以在不添加试剂的其它孔内,诸如通过观测发光反应对化学反应进行观测(测量或检测)。特别地,所述观测(测量或检测)可在将试剂加入孔内的同时执行,其中添加试剂与发生化学反应之间有一段时间间隔。
优选地,将试剂加入至孔内的样品中,同时观察与所述孔隔开的另一孔(诸如相邻的孔)内的化学反应。从这个意义上说,可以按顺序将试剂加入至微孔板的每一孔内的样品中,并且同时通过观察(测量或检测)与所述孔隔开的另一孔(诸如相邻的孔)内的样品的发光和/或荧光和/或吸光度来观测所述另一孔内的化学反应。通过所述步骤,可以一个接一个地“刺激”微孔板的孔(即将试剂加入孔的样品中),并且观察(测量或检测)一段时间后由所述刺激引起的化学反应。延迟的时间长短由以下两者确定:隔开的相应孔(诸如相应的相邻孔)之间的几何偏移(即在X-Y平面内的横向距离);以及微孔板和用于观察化学反应的测量装置(更精确地:所述测量装置的光轴)之间特别是在与微孔板的平面平行的平面内相对于彼此移动的速度。
根据本发明第二方面所公开的特征,可实现本发明的所述目的。因此,本发明还提供一种在酶标仪中测量活细胞的方法,所述酶标仪包括包围内部空间的外壳。所述方法包括以下步骤:
a)提供样品隔室,所述样品隔室与器件隔室被隔开,在所述样品隔室内设有用于容纳至少一个微孔板的保持装置,
a1)其中分隔板设于所述外壳内以将所述外壳的内部空间分隔成所述样品隔室和所述器具隔室;或者
a2)其中在所述外壳内配置内部壳体,所述保持装置设于所述内部壳体内;以及
其中,所述分隔板或所述内部壳体具有至少一个开口,所述开口设计成使得用在或插于所述酶标仪中的微孔板的孔内的样品所射出的光或所影响的光能够穿过所述开口从所述样品隔室进入所述器具隔室;
b)在所述酶标仪的保持装置内放置至少一个包括包含样品的孔的微孔板;
c)相对于所述酶标仪的至少一个测量装置来定位这个或这些微孔板的包含样品的孔;
d)控制在所述样品隔室内的气氛的温度;以及
e)使用至少一个测量装置来检测光,所述光是
-用在或插于所述酶标仪中的微孔板的孔内的样品所射出的光,和/或
-用在或插于所述酶标仪中的微孔板的孔内的被光透照的样品所影响的光。
可以改变所述方法的步骤的顺序,特别是步骤b)至e)的顺序。因此,例如步骤d)可在步骤c)或步骤b)之前执行,和/或步骤e)可在步骤c)或步骤d)之前执行。
所述方法还可包括以下步骤中的至少一个或多个步骤:
f)测量用在所述酶标仪中的微孔板的孔内的被光透照的样品所影响的光,以测量所述样品的吸光度;
g)测量用在所述酶标仪中的微孔板的孔内的被光照射的样品所射出的光,以测量所述样品的荧光;以及
h)测量用在所述酶标仪中的微孔板的孔内的被光照射的样品所射出的光,以测量所述样品的发光。
在样品隔室内调整限定的气氛,并且基于上述的步骤d)中所调整的气氛分别执行前述的步骤f)、g)和h)中的至少一个或多个步骤。
在所述方法中,通过设于样品隔室内的运动装置来混合和/或循环流入样品隔室内的气体和/或存在于样品隔室内的气体。
在所述方法中,通过控制单元来控制在样品隔室内的气氛的组成。因此,可允许气体通过气体入口进入样品隔室内,这由控制单元致动。在所述方法中,可控制样品隔室内气氛的不同气体中至少一种特定的气体的比例,其中所述特定的气体选自包括氮气(N2)、二氧化碳(CO2)、氧气(O2)、一氧化碳(CO)、硫化氢(H2S)和二氧化硫(SO2)的组。在所述方法中,可通过控制单元来控制在样品隔室内的气氛的湿度和/或温度。在所述方法中,在样品隔室内通过通风装置来进行通风。
在测量活细胞的方法中和/或在酶标仪的用途(如下所述)中,通过注射装置将试剂加入至微孔板的至少一个孔内的至少一个样品中。继而导致化学反应,所述化学反应能够被所述测量装置中至少之一检测。特别地,伴随着化学反应,样品中会发生发光反应,或者样品的发光性质、荧光和/或吸光度会改变。例如,可将试剂加入刚好位于第三测量装置的光轴上的孔内,则会导致孔内发生化学反应。
可在将试剂加入孔内的同时,诸如通过观察同一个孔内发生的发光反应来对所述孔内的化学反应进行观察(测量或检测),其中添加试剂与发生化学反应之间有一段时间间隔。替换地或除此之外,还可诸如通过观察与当前试剂所加入的孔不同的另一孔内发生的发光反应来对所述另一孔内的化学反应进行观察(测量或检测)。具体地,这可在将试剂加入孔的同时进行,其中添加试剂与发生化学反应之间有一段时间间隔。
如上所述,优选地,将试剂加入孔内的样品中,同时观测与所述孔相隔开的另一孔(诸如相邻的孔)内的化学反应。
通过观察(测量或检测)装在微孔板的孔内的样品或细胞培养体的生长动力学或改变,可观察或识别由于加入试剂或细胞培养体而引发样品(诸如细胞培养体)中发生的化学反应。在所述方法中,可通过照明装置将光透照于用在或插于酶标仪中的微孔板的孔内的样品,和/或通过照明装置将光照射于孔内的样品。
还可通过第二照明装置将光照射于用在酶标仪的微孔板的孔内的样品。第二照明装置可设于器具隔室中。优选地,第二照明装置选自包括激光、频闪灯、LED(发光二极管)和激光二极管的组。在所述方法中,可通过设于样品隔室或器具隔室内的测量装置分别测量样品的吸光度和/或荧光和/或发光。特别地,可通过设于样品隔室内的第一测量装置测量样品的吸光度,和/或通过设于器具隔室内的第二测量装置测量样品的荧光。另外,通过设于样品隔室或器具隔室内的第三测量装置测量样品的发光。
在实施所述方法的酶标仪中,控制单元可包括O2传感器和/或CO2传感器,用于控制用在(插于)所述酶标仪中的微孔板的包含样品的孔周围的气氛中的氧气含量和/或二氧化碳含量。因此,在对微需氧微生物、选择性厌氧微生物、专性厌氧微生物、真菌细胞或真核细胞进行测量的过程中,通过选择性地引入二氧化碳和/或氮气,可使所述气氛中的氧气浓度和/或二氧化碳浓度保持在限定的值。
在如上所述的方法中,以下步骤是可行的:
d1)当控制在样品隔室内的气氛的组成时,通过将诸如氮气或惰性气体的化学非活性气体引入样品隔室内来降低在所述气氛中已经存在的气体诸如氧气(O2)或二氧化碳(CO2)的浓度(特别地,藉此使包括所述已经存在的气体的所述气氛“稀释”或部分排出),并且用对应于已经存在的气体的传感器,诸如O2传感器和/或CO2传感器,来测量所述已经存在的气体的浓度;或者
d2)当控制在样品隔室内的气氛的组成时,可以引入所述气氛中已经存在的气体,诸如氧气(O2)或二氧化碳(CO2),而使该气体在样品隔室内的浓度增加(特别地,藉此选择性地增加所述气体的浓度),并且用对应于该气体的传感器来测量所述气体的浓度;或者
d3)当控制在样品隔室内的气氛的组成时,可以引入所述气氛中还未存在或已经存在的气体,诸如硫化氢(H2S)或一氧化碳(CO),而使该气体在样品隔室内的浓度增加(特别地,藉此选择性地增加所述气体的浓度),并且用对应于该气体的传感器来测量所述气体的浓度。
根据本发明第三方面的上述的酶标仪的用途或根据本发明的上述方法,可实现本发明的上述目的。这些用途涉及在酶标仪中测量活细胞,其中活细胞选自包括微需氧微生物、选择性厌氧微生物、专性厌氧微生物、真菌细胞和真核细胞的组。
所附的相应从属权利要求描述了本发明的其它特征。
所述酶标仪的用途优选用于在限定的O2浓度下测量微需氧微生物或兼性厌氧微生物。在酶标仪中测量活细胞的方法中也优选用于选自包括微需氧微生物、兼性厌氧微生物、强制性厌氧微生物、真菌细胞和真核细胞的组的活细胞。根据ANSI-SBS Standard 2004标准的多孔板或微量滴定板被用作微孔板,所述微孔板例如可包括6、12、24、48、96、384或1536个孔。
根据本发明的酶标仪具有以下优点:
—装有待测量样品的微孔板不需要一直在培养室和测量装置之间来回转移。因此可略去这样的转移,在这样的转移过程中,细胞或细胞培养体会接触周围环境的空气,所述周围环境的空气会影响细胞或细胞培养体,以致于使得到的测量结果发生偏差。
—发光和/或荧光和/或吸光度的测量全自动化,在使根据本发明的酶标仪通电之后,不再需要操作员在场。
—与不具备荧光测量的传统培养室(诸如CO2培养室)相比,根据本发明的酶标仪可进行长时间的测量,从而避免了所谓的“夜视窗”的发生,那时检测不到任何数据。
—在微孔板的孔上方的气氛中或在微孔板的孔周围环境中控制O2和/或CO2的浓度,能够在限定的O2和/或CO2浓度下测量微需氧微生物、兼性厌氧微生物、强制性厌氧微生物、真菌细胞或真核细胞。
附图说明
现在将结合以下附图来对根据本发明的酶标仪和根据本发明的酶标仪的用途进行说明,这些附图示出了优选的示例性实施例,但并不限制本发明的范围,其中:
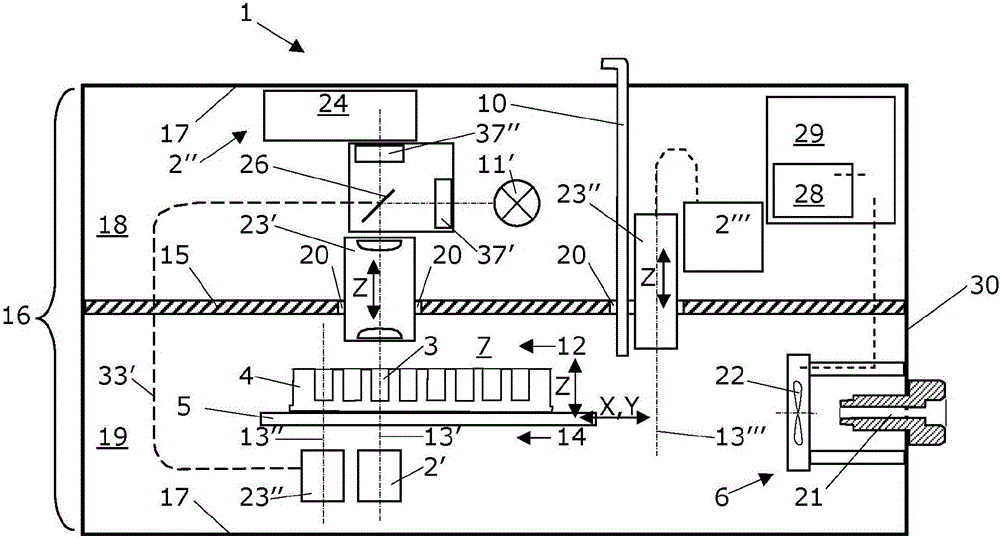
图1所示为根据本发明的第一优选实施例的酶标仪高度图解的垂直方向剖视图,所述酶标仪包括外壳的内部空间,所述内部空间通过分隔板被分隔成器具隔室和样品隔室;
图2所示为根据本发明的第二优选实施例的酶标仪高度图解的垂直方向剖视图,所述酶标仪包括外壳的内部空间,所述内部空间通过分隔板被分隔成器具隔室和样品隔室;
图3所示为根据本发明的第三优选实施例的酶标仪高度图解的垂直方向剖视图,所述酶标仪包括外壳的内部空间,所述内部空间通过分隔板被分隔成器具隔室和样品隔室;
图4所示为位于根据本发明的酶标仪的后壁的内部的O2传感器、CO2传感器、风扇和气体入口的示例性布置;
图5所示为使用根据本发明的酶标仪分别在有和没有CO2对照的情况下获得的真核肿瘤细胞在含血清的培养体(MWS)中的生长曲线;以及
图6所示为使用根据本发明的酶标仪分别在有和没有CO2对照的情况下获得的真核肿瘤细胞在不含血清的培养体(MWOS)中的生长曲线。
具体实施方式
图1所示为根据本发明的第一优选实施例的酶标仪1高度图解的垂直方向剖视图,所述酶标仪1包括外壳17,所述外壳17的内部空间16通过分隔板15被分隔成器具隔室18和样品隔室19。所述酶标仪1包括至少一个测量装置2′、2″、2″′。
图1示出了根据酶标仪1的第一种变型的第一测量装置2′,通过所述第一测量装置2′可测量用在所述酶标仪1的微孔板4的孔3内的被光透照的样品所影响的光(因而测量样品的吸光度)。所述第一测量装置2′优选地设于酶标仪1的样品隔室19内,而用于透照微孔板4的孔3内的样品的第一照明装置11′优选地设于酶标仪1的器具隔室18内。因此,检测用在所述酶标仪1的微孔板4的孔3内的样品所影响的光的第一测量装置2′沿第一光轴13′的方向安置在插于所述酶标仪1的微孔板4的第二侧14(即底侧)。因此,用于透照样品的第一照明装置11′沿第一光轴13′的方向安置在插于所述酶标仪1的微孔板4的第一侧12(即顶侧)。在这种情况下,第一照明装置11′经第一光纤光路33′分配给第一光轴13′。第一照明装置11′包括第一光纤滑块34′,第一波长选择单色仪35′和频闪灯36。因此,通过位于第一光轴13′方向上的第一光纤线路33′和对着样品的第一光学系统23′来引导频闪灯36的光以用于透照样品。所述第一光学系统23′设置成沿笛卡尔坐标系统的Z轴方向(参见双箭头Z)可调节其高度。在这种情况下,在第一照明装置11′和第一测量装置2′之间,但优选地在样品隔室19内,设置保持装置5,以容纳至少一个微孔板4并且相对于第一测量装置2′因而也相对于第一光轴13′来定位这个或这些微孔板4的孔3。
图1示出了根据本发明的酶标仪1的第二种变型的第二测量装置2″,通过所述第二测量装置2″可相对于第二光轴13″测量用在所述酶标仪1的微孔板4的孔3内的样品所射出的光(因而测量样品的荧光)。所述第二测量装置2″包括光电倍增管(PMT)24,第二波长选择单色仪35″和第二光纤滑块34″。为了进行所述荧光测量,酶标仪1的第一照明装置11′用于照射(激发)微孔板4的孔3内的样品。在这种情况下,第一照明装置11′经第二光纤光路33″和第二光学系统23″分配给第二光轴13″。所述第二光学系统23″设置成沿笛卡尔坐标系统的Z轴方向(参见双箭头Z)可调节其高度。结果,通过通往第二光轴13″方向的第二光纤线路33″来引导频闪灯36的光以用于照射样品。
有两种不同的布置可以用于检测样品所发出的荧光:
—在所谓的“顶部检测(top reading)”中,所用的第二光学系统23″置于微孔板4的上方,第二光学系统23″通过第二光纤光路33″与第二光纤滑块34″连接,从而光电倍增管(PMT)24可用于检测微孔板4的每一孔3内的样品的荧光。
—在所谓的“底部检测(bottom reading)”中,第三光学系统23″′置于微孔板4的下方,且通过第三光纤光路33″′与第一光纤滑块34′和第二光纤滑块34″连接,从而所述照明装置11′和所述测量装置2″可用于激发和检测微孔板4的每一孔3内的样品的荧光。
在这种情况下,优选地相对于第一或第二测量装置2′、2″在样品隔室19内于第一照明装置11′的下方安置保持装置5,以容纳至少一个微孔板4和定位这个或这些微孔板4的包含样品的孔3,其中所述第一照明装置11′优选地容纳在器具隔室18内。
图1示出了根据本发明的酶标仪1的第三种变型的第三测量装置2″′,通过所述第三测量装置2″′可测量用在所述酶标仪1的微孔板4的孔3内的样品所射出的光(即测量样品的发光)。第三测量装置2″′用于发光测量,该测量装置优选地相对于第三光轴13″′设于酶标仪1的器具隔室18内。公知的普通注射装置10优选地可伸到酶标仪1的样品隔室19内,以触发化学反应,并伴随发生发光反应或改变微孔板4的孔3内的样品内或样品上的发光性质和/或荧光和/或吸光度。所述注射装置10优选地配置和设置成当微孔板4的孔3位于第三光轴13″′上,因而精确地位于第三测量装置2″′的上方时,所述注射装置10将触发诸如发光反应的化学反应的试剂加入孔3内。
酶标仪1的优选实施例可设计成将试剂加入孔3内的样品中,同时观察与所述孔相隔开的另一孔(诸如相邻的孔)内的化学反应。在这方面,可以将试剂按顺序加入至微孔板4的每一孔3内,同时通过观察(测量或检测)与所述孔相隔开的另一孔(诸如相邻的孔)内的样品的发光和/或荧光和/或吸光度,来观测所述另一孔内的化学反应。通过所述步骤,可以逐个“刺激”微孔板4的孔(即将试剂加入孔内的样品中),并且观察(测量或检测)一段时间后由所述刺激引发的化学反应。所述延迟的时间段由以下参数确定:相关的孔3(相隔开的孔,诸如相邻的孔)之间的几何偏移(即在X-Y平面内的横向距离),以及微孔板4和用于观测化学反应的测量装置2′、2″、2″′(或所述测量装置的光轴13′、13″、13″′)之间相对于彼此移动的速度,特别是与X-Y平面平行的平面内的速度。
也可以想到在如图2和3所示的酶标仪的实施例中使用相应的注射装置10,在上文与注射装置10及其功能或应用相关的内容中已经对此作了描述,适用于图2和3中的实施例。
第三测量装置2″′优选地包括第四光学系统23″″,其沿笛卡尔坐标系统的Z轴方向(参见双箭头Z)可移动地安置。特别优选地,第一、第二、第三和第四光学系统23′、23″、23″′和23″″设置成可调低它们的位置以使它们的一部分穿过分隔板15的相应开口20进入样品隔室19内。
分离的控制单元6′位于根据本发明的酶标仪1的外壳17上,O2传感器8、CO2传感器9、风扇22和气体入口21配置在根据本发明的酶标仪1的外壳17的后壁30的内部(参见图4)。酶标仪1的控制单元6优选地包括O2传感器8,用于测量和控制样品隔室19内的气氛7(即插于所述酶标仪1中的微孔板的包含样品的孔3周围的气氛7)中的氧气含量。替换地或者除了所述O2传感器8之外,酶标仪1的控制单元6特别优选地包括CO2传感器9,用于测量和控制插于所述酶标仪1中的一或多个微孔板4的包含样品的孔3周围的气氛7中的二氧化碳含量。因此,控制单元6的一部分设于酶标仪1的外壳17内,另一部分设于酶标仪1的外壳17之外且通过电接头27和气体管道38连接至或能够连接至酶标仪1。分离的控制单元6′直接与必要的待用气体压力缸连接。所需气体连接的相应的阀门和节流阀安装于分离的控制单元6′内(未示出)。替换地,还可以使用安装在气体压力缸上的定位器和节流阀,其中这些阀门优选地选用电控制的(正常状态为闭合的那种类型)电磁阀。图1中没有示出用于分离的控制单元6′和酶标仪1的其它控制元件、显示元件和电源。
图2所示为根据本发明的第二优选实施例的酶标仪1高度图解的垂直方向剖视图,所述酶标仪1包括外壳17,所述外壳17的内部空间16通过分隔板15被分隔成器具隔室18和样品隔室19。所述酶标仪1包括至少一个测量装置2′、2″、2″′。
图2示出了根据本发明的酶标仪1的第一种变型的第一测量装置2′,通过所述第一测量装置2′可测量用在所述酶标仪1的微孔板4的孔3内的被光透照的样品所影响的光(因而测量样品的吸光度)。所述第一测量装置2′优选地设于酶标仪1的样品隔室19内,而用于透照微孔板4的孔3内的样品的第一照明装置11′优选地设于酶标仪1的器具隔室18内。因此,检测用在所述酶标仪1的微孔板4的孔3内的样品所影响的光的第一测量装置2′沿第一光轴13′的方向安置在插于所述酶标仪1的微孔板4的第二侧14(即底侧)。因此,用于透照样品的第一照明装置11′沿第一光轴13′的方向安置在插于所述酶标仪1的微孔板4的第一侧12(即顶侧)。在这种情况下,第一照明装置11′经部分透光(诸如50%透光)的镜26或二向色镜分配给第一光轴13′。第一照明装置11′包括第一波长选择滤波器37′和频闪灯36。因此,通过位于第一光轴13′方向上的部分透明的镜26和对着样品的第一光学系统23′来引导频闪灯36的光以用于透照样品。所述第一光学系统23′设置成沿笛卡尔坐标系统的Z轴方向(参见双箭头Z)可调节其高度。在这种情况下,在第一照明装置11′和第一测量装置2′之间,但优选地在样品隔室19内,设置保持装置5,以容纳至少一个微孔板4并且相对于第一测量装置2′因而也相对于第一光轴13′来定位这个或这些微孔板4的孔3。
图2示出了根据本发明的酶标仪1的第二种变型的第二测量装置2″,通过所述第二测量装置2″可相对于第一光轴13′或第二光轴13″测量用于所述酶标仪1的微孔板4的孔3内的样品所射出的光(因而测量样品的荧光)。所述第二测量装置2″包括光电倍增管(PMT)24,第二波长选择滤波器37″。为了进行所述荧光测量,酶标仪1的第一照明装置11′再次用于照射(激发)微孔板4的孔3内的样品。在这种情况下,第一照明装置11′经部分透光(诸如50%透光)的镜26或二向色镜和第一光学系统23′分配给第二光轴13″。
有两种不同的布置可以用于检测样品所发出的荧光性:
—在所谓的“底部检测”中,第二光学系统23″位于微孔板4的下方,且通过第一光纤光路33′与部分透光的镜26和第二滤波器37″连接,从而光电倍增管(PMT)24可用于检测微孔板4的每一孔3内的样品的荧光。
—在所谓的“顶部检测”中,所用的第一光学系统23′位于微孔板4的上方,第一光学系统23′通过部分透光的镜26连接至第二滤波器37″,从而同一光电倍增管(PMT)24可用于检测微孔板4的每一孔3内的样品的荧光。
在这种情况下,优选地相对于第一或第二测量装置2′、2″在样品隔室19内位于第一照明装置11′的下方安置保持装置5,以容纳至少一个微孔板4和定位这个或这些微孔板4的包含样品的孔3,其中所述第一照明装置11′优选地封装在器具隔室18内。
图2示出了根据本发明的酶标仪1的第三种变型的第三测量装置2″′,通过所述第三测量装置2″′可测量用于所述酶标仪1的微孔板4的孔3内的样品所射出的光(即测量样品的发光)。第三测量装置2″′用于发光测量,该测量装置优选地相对于第三光轴13″′设于酶标仪1的器具隔室18内。公知的普通注射装置10优选地可伸到酶标仪1的样品隔室19内,以触发化学反应,并伴随发生发光反应或改变微孔板4的孔3内的样品内或样品上的发光性质和/或荧光和/或吸光度。所述注射装置10优选地配置和设置成当微孔板4的孔3位于第三光轴13″′上,因而精确地位于第三测量装置2″′的上方时,所述注射装置10将触发诸如发光反应的化学反应的试剂加入孔3内。第三测量装置2″′优选地包括第三光学系统23″′,其沿笛卡尔坐标系统的Z轴方向(参见双箭头Z)可移动地安置。特别优选地,第一和第二光学系统23′、23″设置成可调低它们的位置以使它们的一部分穿过分隔板15内的相应开口20进入样品隔室19内。
优选地,根据本发明的酶标仪1的前述的所有变型都可使用同一个控制单元6。
图3所示为根据本发明的第三优选实施例的酶标仪1高度图解的垂直方向剖视图,所述酶标仪1包括外壳17,所述外壳17的内部空间16通过内部壳体39被分隔成器具隔室18和样品隔室19。所述酶标仪1包括用于探测光的至少一个测量装置2′、2″、2″′。内部壳体39包括开口20,所述开口20设计成使得用于酶标仪1的微孔板4的孔3内的样品所射出的光或所影响的光可穿过开口20从样品隔室19进入器具隔室18。
图3示出了根据本发明的酶标仪1的第一种变型的第一测量装置2′,通过所述第一测量装置2′可测量用在所述酶标仪1的微孔板4的孔3内的被光透照的样品所影响的光(因而测量样品的吸光度)。所述第一测量装置2′优选地设于酶标仪1的器具隔室18内,而用于透照微孔板4的孔3内的样品的第一照明装置11′优选地设于酶标仪1的样品隔室内。因此,检测用在所述酶标仪1的微孔板4的孔3内的样品所影响的光的第一测量装置2′沿第一光轴13′的方向安置在插于所述酶标仪1的微孔板4的第一侧12(即顶侧)。因此,用于透照样品的第一照明装置11′沿第一光轴13′的方向安置在插于所述酶标仪1的微孔板4的第二侧14(即底侧)。第一测量装置2′优选地包括镜25,其用于使从样品发出的光偏转至光电倍增管(PMT)24的方向。替换地,从样品发出的光由PMT 24中的光纤(未示出)供给。类似地,第一照明装置11′可选用灯,设置于第一光轴13′上。替换地,通过位于第一光轴13′方向上的镜或光纤(均未示出)可引导光以用于透照样品。在这种情况下,优选地在第一照明装置11′和第一测量装置2′之间,但优选地在样品隔室19内,设置保持装置5,以容纳至少一个微孔板4并且定位这个或这些微孔板4的包含样品的孔3。
图3示出了根据本发明的酶标仪1的第二种变型的第二测量装置2″,通过所述第二测量装置2″可测量用在所述酶标仪1的微孔板4的孔3内的样品所射出的光(因而测量样品的荧光)。为了进行所述荧光测量,再次使用酶标仪1的第一测量装置2′,在这种情况下,所述第一测量装置2′与所述第二测量装置2″相同。第二照明装置11″(优选为激光、频闪灯或激光二极管)被用作光源,以提供照射微孔板4的孔3内的样品所需的激发光。所述第二照明装置11″优选地设于酶标仪1的外壳空间18内。因此,检测插于酶标仪1的微孔板4的孔3内的样品所射出的光的第一测量装置2′和第二测量装置2″均设于插于所述酶标仪1中的微孔板4的同一侧12(因而为顶侧)。第二照明装置11″优选地包括部分透光(诸如50%透光)的镜26或二向色镜,以将激发光偏转至第一光轴13′的方向继而偏转至样品上或样品内。在这种情况下,优选地相对于第一测量装置2′在样品隔室19内位于第二照明装置11″和第一测量装置2′(这两者优选地容纳在器具隔室18内)的下方安置保持装置5,以容纳至少一个微孔板4和定位这个或这些微孔板4的包含样品的孔3。
图3示出了根据本发明的酶标仪1的第三种变型的第三测量装置2″′,通过所述第三测量装置2″′可测量用在所述酶标仪1的微孔板4的孔3内的样品所射出的光(即测量样品的发光)。第三测量装置2″′用于发光测量,所述第三测量装置优选地相对于第二光轴13″设于酶标仪1的样品隔室19内。公知的普通注射装置10优选地设于酶标仪1的样品隔室19内,以触发化学反应,并伴随发生发光反应或改变微孔板4的孔3内的样品内或样品上的发光性质和/或荧光和/或吸光度。例如,所述注射装置10被配置和设置成当微孔板4的孔3位于第二光轴13″上,因而精确地位于第三测量装置2″′的上方时,所述注射装置10将触发诸如发光反应的化学反应的试剂加入孔3内。在这种情况下,优选地相对于第一测量装置2′在样品隔室19内位于注射装置10的下方且位于第三测量装置2″′的上方安置保持装置5,以容纳至少一个微孔板4和定位这个或这些微孔板4的包含样品的孔3。第一测量装置2′优选地包括第一光学系统23′,其沿笛卡尔坐标系统的Z轴方向可移动地安置。根据如图3所示的第一实施例,特别优选地,第一光学系统23′设置成可调低它的位置以使它的一部分穿过内部壳体39内的相应开口20进入样品隔室19内。
微孔板4或保持装置5可相对于第一、第二和/或第三测量装置2′、2″、2″′的相应的第一、第二和/或第三光学系统23′、23″、23″′沿笛卡尔坐标系统的Z轴方向(参见图2和3中的双箭头Z)移动。微孔板4或保持装置5(参见双箭头X、Y)、和/或第一、第二和/或第三测量装置2′、2″、2″′或者它们相应的第一、第二和/或第三光学系统23′、23″、23″′还可设计成能够沿笛卡尔坐标系统的X轴和/或Y轴方向移动。这适用于根据本发明的酶标仪1的如附图所示的所有实施例和变性以及可能的改型。
根据本发明的酶标仪1的所有实施例和变型的特征在于,所述酶标仪1包括控制单元6,用于控制插于所述酶标仪1中的微孔板4的包含样品的孔3周围的气氛7的组成。此外,保持装置5优选地沿笛卡尔坐标系统的X轴和Y轴方向可移动地安置(参见图1至3中的双箭头X、Y)。
图4所示为位于根据本发明的酶标仪1的外壳17的后壁30的内部的O2传感器8、CO2传感器9、风扇22和气体入口21的示例性布置。酶标仪1的控制单元6优选地包括O2传感器8,用于测量和控制插于所述酶标仪1中的微孔板4的包含样品的孔3周围的气氛7中的氧气含量。替换地或除了所述O2传感器8之外,酶标仪1的控制单元6特别优选地包括CO2传感器9,用于测量和控制插于所述酶标仪1中的一或多个微孔板4的包含样品的孔3周围的气氛7中的二氧化碳含量。所述控制单元6可部分地设于酶标仪1的外壳17之外,并且诸如通过电接头27和气体管线(未示出)连接至或能够连接至酶标仪1(未示出)。但是还可以将控制单元6完全集成在酶标仪1中且容纳于普通的外壳17内(参见图2和3)。在这种情况下,酶标仪1可直接与必要的待用气体压力缸连接(参见图2和3)。优选地,可在酶标仪1的外壳17上安装相应的阀门和节流阀(未示出)。替换地,也可在气体压力缸上安装阀门和节流阀,这些阀门优选地选用电控制的(正常状态为闭合的那种类型)电磁阀(未示出)。
控制单元优选地包括具有相应软件的计算机28。在此情况下,计算机28可连接至酶标仪1的中央计算机29(参见图1)(例如将计算机28安装在分离的外壳17′中),或者集成在酶标仪1的所述中央计算机29内(未示出)。
优选地,在压力缸内装载用于置换周围空气的氮气(N2)和/或二氧化碳(CO2),这些压力缸采用公知的普通控制阀和节流阀来设定这些气体所需的进给压力。替换地,还可从其它来源(诸如从自身管线)得到这些工艺气体。除了氮气和二氧化碳之外,还可使用其它气体来产生样品隔室内流通的气氛中限定的百分比(与样品隔室19内的相应的气体检测器结合使用)。通过观察可能适用的安全措施,还可将其它气体(例如稀有气体或惰性气体如氩气,或者活性气体或有毒气体(如氧气、一氧化碳、硫化氢或二氧化硫)通过气体入口21引入酶标仪1的样品隔室19内并到达插于所述酶标仪1的微孔板4的孔3的区域,以产生具有特定的气体组成的气氛。优选地,控制单元6配备有足够的气体管线和控制阀,以得到由几种气体组分构成的更为复杂的气体组成。
关于合适的CO2传感器,目前所使用的CO2传感器是瑞典代尔斯布SE-820 60的SenseAir AB制造的CO2ICB,产品编号为033-9-0001。关于合适的O2传感器,目前所使用的O2传感器是瑞士苏黎世CH-8052的Pewatron AG制造的Pewatron FCX-MEP2-F-CH氧气模块。
控制单元6与O2传感器联用,可控制插于所述酶标仪1中的一或多个微孔板4的包含样品的孔3周围的气氛7中的氧气含量,因此酶标仪1可用于在限定的O2浓度下测量微需氧微生物或兼性厌氧微生物。因此也可在限定的O2浓度下测量厌氧微生物或真核细胞。
控制单元6与CO2传感器联用,可控制插于所述酶标仪1中的一或多个微孔板4的包含样品的孔3周围的气氛7中的二氧化碳含量,因此所述酶标仪1可用于在限定的CO2浓度下测量活细胞培养体。
按照本发明,细胞培养体、与所述细胞培养体分离或其它方式获得的生物细胞聚集体、或个别细胞都称为细胞,这些细胞包括微生物、真菌细胞、动物细胞和植物真核细胞。
如图1至4所示的根据本发明的酶标仪1的各个元件和控制单元6的任何组合应该属于本发明的范围。
利用本发明的第一实施例的酶标仪1(参见图1)检测了5%CO2调节的真核肿瘤细胞。GFP-转染A431细胞用于测定荧光。简写“GFP”表示的是大家公知的“绿色荧光蛋白”,其最大的激发波长介于396nm和475nm之间,最大发射波长是508nm。为了记录这些细胞在72小时内相应的生长曲线,将这些细胞悬浮在含10%血清的培养体(MWS)中或不含血清的培养体(MWOS)中。
含血清的培养体(MWS)包括以下成分:具有4.5g/l葡萄糖的杜氏培养液(包含酚红的DMEM),补入了10mMHEPES(赫佩斯)缓冲液、2mM L-谷氨酰胺、1mM丙酮酸钠、100U/ml盘尼西林、0.1mg/ml链霉素和5%(v/v)胎牛血清(FBS)。培养体的所有成分均从奥地利林兹的PAA laboratories获得。
不含血清的培养体(MWOS)除了不含胎牛血清(FBS)之外,含有上述相同的成分。
所采用的微孔板4是具有无菌涂层的Greiner Standard Cell Culture MTP96Well(无菌的培养组织板上的Greiner 96孔具有黑色的、扁平的和干净的底部)。所述微孔板4中的48个孔3分别装有2500A431GFP细胞和10%的血清(样品类型A,参见图5)。所述微孔板4中的其它48个孔分别装有2500A431GFP细胞,但不含血清(样品类型B,参见图6)。使用这2个样品类型A和B来进行两个测试系列:
第一测试系列包括使用CO2传感器(Typ CO2ICB,产品编号:033-9-0001)测量样品隔室19内的CO2浓度,通过具有集成的电子控制系统的控制单元6使CO2浓度保持在5%。这可通过以下方式实现:首先根据本发明的酶标仪1中的样品隔室19和器具隔室18内的气氛的气体组成与周围环境空气的气体组成相同,即气氛最初的气体组成近似对应于标准大气,其具有以下组成:20.93%的氧气、78.10%的氮气、0.93%的氩气、0.03%的二氧化碳以及0.01%的氢气、氖气、氦气、氪气和氙气。在将微孔板4定位在酶标仪1的保持装置5之后,关闭酶标仪1的外壳17,并且将CO2气体通过气体入口21引入样品隔室19内,直到CO2气体的浓度达到5%。在测量过程中CO2气体的浓度一直保持在5%,可根据需要(一旦CO2传感器检测到二氧化碳浓度不足时)将CO2气体引入样品隔室19内。样品隔室19内的气体混合物通过风扇22不断地循环。在任何情况下都使温度恒定保持在37℃。
第二测试系列包括:不将任何额外的CO2引入样品隔室19内,使样品一直接触周围环境的空气。在任何情况下都使温度恒定保持在37℃。
通过第一照明装置11′分别激发(每一孔3内的)每一样品的荧光,所述第一照明装置11′设于微孔板4的下方(激发波长为485nm;检测荧光的波长为535nm)且通过第二光学系统23″被引导至光电倍增管24以进行检测。分别测量各个样品在不同时间的荧光。在酶标仪1的中央计算机29中分别处理由光电倍增管24检测到的每一孔内的荧光的强度,然后显示在曲线图中(参见图5和6)。
图5所示为使用根据本发明的酶标仪1分别在有CO2对照和没有CO2对照的情况下所获得的真核肿瘤细胞在含10%血清的培养体(MWS)中的生长曲线。附图标记31表示CO2浓度一直保持在5%的样品,而附图标记32表示接触正常的环境空气的样品。图5近似地示出了在最初的35小时内细胞的行为,其中CO2浓度一直保持在5%的样品31的细胞生存力一直稍微低于接触正常的环境空气的样品32的细胞生存力,细胞生存力是根据相应的GFP-信号(即根据荧光强度)测到的。在大约35小时之后,接触正常的环境空气的样品32的细胞生长急剧地减慢。在大约60小时后,样品32的细胞生长达到约为450%的最大值,然后开始减慢,在测量结束(即在75小时)时细胞生长降低至初始值的400%以下。与样品32相比,CO2浓度一直保持在5%的样品31的细胞生存力在35小时测量期之后实质地线性地增加,直到测量结束(即在75小时)时达到大约初始值的900%。
图6所示为使用根据本发明的酶标仪1分别在有CO2对照和没有CO2对照的情况下所获得的真核肿瘤细胞在不含10%血清的培养体(MWOS)中的生长曲线。附图标记31表示CO2浓度一直保持在5%的样品,而附图标记32表示接触正常的环境空气的样品。图6近似地示出了在最初的35小时内细胞的行为,其中CO2浓度一直保持在5%的样品31的细胞生存力一直稍微低于接触正常的环境空气的样品32的细胞生存力,细胞生存力是根据相应的GFP-信号(即根据荧光强度)测到的。在大约35小时之后,接触正常的环境空气的样品32的细胞生长达到200%的最大值,直到测量结束(即在75小时)时降低至大约初始值的100%。与样品32相比,CO2浓度一直保持在5%的样品31的细胞生存力在35小时测量期之后保持等量地增加,直到测量结束(即在75小时)时达到大约初始值的300%。
图示的结果表明细胞在CO2浓度一直保持在5%的条件下所表现的生存力比接触正常的环境空气的细胞的生存力高很多。所述高的细胞生存力在培养40小时之后特别明显。额外添加的10%的血清在最初的35小时内使细胞生存力增加大约2倍,而在75小时之后甚至增加至大约3倍。
通过本发明可进行这样的不间断的长期研究,而不像传统的CO2培养器没有将荧光测量功能整合在一起,其在夜晚有大约14个小时的空窗,那时不能收集任何数据。
现有技术中还没有公开这样的酶标仪,其包括传感器和控制单元,用于控制用在所述酶标仪中的微孔板的包含样品的孔上方的或孔的周围环境中的气氛的组成。
虽然已公布的德国申请DE 10 2005 033 927 A1公开了一种照明装置,用于在倒置显微镜的亮视场中传输对比光以观测活细胞,但所述照明装置集成在倒置显微镜的气密、防光的紧凑培养器内,以按顺序照射做成微量滴定板的样品保持装置内的每一个孔,并且同时在较长的时间内保证样品容积的热稳定性和尽可能少的热损失。所述照明装置被固定在培养器的上部且位于投影透镜的上方。插入的微量滴定板、培养皿或其它类似的元件可相对于培养器底部的显微镜载物台上方的投影透镜移动。培养器包括第一容室,所述容室被第二外部容室完全包围,所以第一容室与周围环境热隔绝。包含样品的微量滴定板设于所述内部容室内,通过控制装置来控制所述内部容室的中温度、气体湿度和CO2含量。所述已公布的德国申请DE 10 2005 033 927 A1专有地涉及倒置显微镜,其配置和用途与酶标仪很不相同,酶标仪不包括任何成像功能且对每个孔的测量时间短得多。在所述德国申请的公布文本中并未提及酶标仪,特别是没有提及O2传感器。
从专利EP 1 575 706 B1中还可知道用于观察微量滴定板内的样品的气候室。向所述气候室引入可调的培养基,它为具有限定的气体湿度和/或温度的空气。可引入限定的CO2气体,并且在载有微量滴定板的样品保持器附近配置温度传感器、湿度传感器和/或气体传感器。在所述专利的公布文本中并未提及酶标仪,特别是没有提及O2传感器。
因此,根据现有技术,本发明的酶标仪1和控制单元6对于本领域的技术人员来说并不是显而易见,其中所述控制单元6用于控制用在所述酶标仪1中的微孔板4的包含样品的孔3上方的或孔3周围环境内的气氛7的组成。
根据本发明的酶标仪1和控制单元6的其它优选的应用涉及例如用于检查O2的部分压力对微生物(诸如深红红螺菌(Rhodospirillum rubrum)[Biedermann等,1967,“Archiv fur Mikrobiologie”(Archive for Microbiology)56,133-147])的生长的影响,以及检查微需氧海藻酸盐的生产,其中优选地将O2的浓度设定为2.5-5%(优选为2.5%)[wael sabra 1999:Microaerophilic alginate production with Azotobacter vinelandii;Dissertation at the Common Scientific Faculty of the Braunschweig University of Technology]。
采用相同的附图标记来表示附图中示出的酶标仪1的相同的或相应的特征,这也适用于本说明书中没有特别说明的地方。另外,附图中所示的实施例的特征之间的任意组合或者这些特征的等效技术特征应当属于在本文中公开的本发明的范围。
附图标记列表
1 酶标仪
2′ 第一测量装置
2″ 第二测量装置
2″′ 第三测量装置
3 孔
4 微孔板
5 保持装置
6 控制单元
6′ 分离的控制单元
7 气氛
8 O2传感器
9 CO2传感器
10 注射装置
11′ 第一照明装置
11″ 第二照明装置
12 所插入的微孔板的第一侧
13′ 第一光轴
13″ 第二光轴
13″′ 第三光轴
14 所插入的微孔板的第二侧
15 分隔板
16 内部空间
17 所述检测仪的外壳
17′ 分离的外壳
18 器具隔室
19 样品隔室
20 开口
21 气体入口
22 风扇
23′ 第一光学系统
23″ 第二光学系统
23″′ 第三光学系统
24 PMT光电倍增管
25 镜
26 部分透照镜
27 电接头
28 计算机
29 酶标仪的中央计算机
30 后壁
31 有CO2对照的细胞的生长曲线
32 没有CO2对照的细胞的生长曲线
33′ 第一光纤光路
33″ 第二光纤光路
33″′ 第三光纤光路
34′ 第一光纤滑块
34″ 第二光纤滑块
35′ 第一单色仪
35″ 第二单色仪
36 频闪灯
37′ 第一过滤器
37″ 第二过滤器
38 气体管道
39 内部壳体
- 还没有人留言评论。精彩留言会获得点赞!