一种IVIG中IgGFab片段和Fc片段唾液酸含量的测定方法与流程
本发明属于生物医药检测技术领域,具体涉及一种ivig中iggfab片段和fc片段唾液酸含量的测定方法。
背景技术:
静注人免疫球蛋白ph4(intravenousimmunoglobulins,ivig),是一种重要的人血浆蛋白制品,主要成分是免疫球蛋白igg。
唾液酸(sialicacid)是一类天然的碳水化合物,通常以低聚糖、糖脂或糖蛋白的形式存在,为9-碳单糖的衍生物。是一种能使唾液产生光滑感觉的负电荷离子。它不仅具有"诱导"入侵病菌的作用,目前认知是神经节苷脂的传递递质,并且是大脑的组成部分。唾液酸可以阻止病菌入侵,同时也是流感病毒的受体,是流感病毒结合在黏液细胞中的结合位点。唾液酸修饰的浓度对生物大分子发挥功能有着非常重要的影响,获得对唾液酸进行准确快速的定量分析方法对于药物的临床使用、质量检测等方面具有重要的应用价值。
igg作为一种糖蛋白,其中唾液酸位于其fab段和fc段n-端糖链终端。fab段即抗原结合片段(fragmentantigenbinding,fab),相当于抗体分子的两个臂,由一条完整的轻链和重链的vh和ch1结构域组成;与异物蛋白结合。fc段即可结晶片段(fragmentcrystallizable,fc),相当于igg的ch2和ch3结构域。与吞噬细胞结合。igg在酶的作用下可降解为fab片段和fc片段。
ivig中iggfc片段唾液酸化程度会影响其与fc受体系统的结合,对ivig发挥抗炎疗效至关重要,ivig中iggfc片段唾液酸含量的多少是其治疗各种炎症疾病的重要指标。而fab段的唾液酸化程度会影响抗原抗体的结合,影响ivig在治疗免疫缺陷疾病时的效果。目前对唾液酸含量的检测,多限于样品或生物制品总唾液酸含量的检测,尚无专门针对fab片段和fc片段分开进行检测,而这两者的唾液酸含量的差异在临床使用中有不同的意义。
根据目前药典相关规定及已发表的分光光度法,hplc方法精确、灵敏度更高。但目前尚无文献报道hplc-荧光法应用于ivig制品中唾液酸含量的检测。因此,有必要建立一种用于测定ivig中iggfab片段和fc片段唾液酸含量的方法。
技术实现要素:
为了解决以上技术问题,本发明提供一种ivig中iggfab片段和fc片段唾液酸含量的测定方法,能够测定ivig制品iggfab片段和fc片段唾液酸含量,方法简单,精确、灵敏度高,重复性和准确性高。
解决以上技术问题的一种ivig中iggfab片段和fc片段唾液酸含量的测定方法,所述测定方法为经过双链fc片段的纯化步骤、ivig去除糖类保护剂处理步骤、唾液酸解离步骤、荧光衍生步骤、高效液相色谱检测和标准曲线的绘制步骤,即得唾液酸总含量和fc片段的唾液酸含量;其中,fab段唾液酸含量为=(ivig中的唾液酸总含量×ivig分子量-fc片段的唾液酸含量×fc片段分子量)/fab片段分子量,式中ivig分子量为150,000da,fc片段分子量为55,000da,fab片段分子量为95,000da。
糖类保护剂是指单糖如葡萄糖,双糖如蔗糖、海藻糖、乳糖,聚糖有葡聚糖等,都具有大量的自由羟基。
本发明中一种ivig中iggfab片段和fc片段唾液酸含量的测定方法,包括以下具体步骤:
步骤一:待测样品预处理:
(1)双链fc片段的纯化:取ivig,酶切、蛋白g层析和分子筛层析后得到双链fc片段;其中层析得到的双链fc片段溶液经测定蛋白浓度后,稀释或浓缩,获得蛋白浓度为0.5~4mg/ml的溶液待测;分子筛的作用是将fc从酶切且经过proteing层析后的产物中纯化出来。
(2)ivig去除糖类保护剂处理;取ivig,分子筛层析去除糖类保护剂;
将待检测的ivig上样于分子筛,去除糖类组分,层析得到的溶液经测定蛋白浓度后,稀释或浓缩,获得蛋白浓度为0.5~4mg/ml的溶液待测;分子筛的作用是将ivig中的igg与糖类保护剂分开。
本发明中检测的样本ivig,其成分中含有大量麦芽糖、蔗糖等糖类物质作为ivig储存的保护剂和稳定剂,而且唾液酸也是一种糖类衍生物。现在唾液酸含量检测方法中不论是色谱法还是分光光度方法,均基于发色物质或荧光物质与糖类的反应,样本中所含有的糖类物质即便是很少的残留也影响着测定准确性高低。本发明中检测方法首先采取分子筛层析去除样品中的糖类物质,去除干扰,提高检测准确性。
再将去除糖类保护剂后的ivig和纯化后的双链fc片段分别进行步骤二至步骤五处理,得ivig中的唾液酸总含量和fc片段的唾液酸含量;
步骤二:唾液酸解离:用酸性溶剂将待测样品的唾液酸解离下来;
步骤三:荧光衍生,将苯甲酸二甲基氨基乙酯(dmb)衍生液加入步骤二中,50℃金属浴避光反应2.5h;单独的唾液酸是无法被很好地被高效液相色谱(hplc)仪检测到,需要加入与唾液酸(糖类物质)反应的荧光衍生剂反应后,再上hplc检测。
步骤四:高效液相色谱检测和标准曲线的绘制:用高效液相色谱仪进行检测,再以标准曲线样品梯度浓度为横坐标,标准曲线样品经高效液相色谱检测的衍生峰面积为纵坐标,采用线性方程绘制标准曲线;
步骤五:唾液酸含量的计算:
将待测样品的经高效液相色谱检测的衍生峰面积代入标准曲线,计算样品中每毫升溶液唾液酸含量,将计算的结果除以样品溶液的蛋白浓度,即得到每mg样品中唾液酸的含量;
其中,fab段唾液酸含量为=(ivig中的唾液酸总含量×ivig分子量-fc片段的唾液酸含量×fc片段分子量)/fab片段分子量;式中,ivig分子量为150,000da,fc片段分子量为55,000da,fab片段分子量为95,000da。
所述步骤一中酶切条件为在ivig中加入edta-na2,l-半胱氨酸盐酸盐和木瓜蛋白酶,37℃,4h,edta-na2,l-半胱氨酸盐酸盐和木瓜蛋白酶用量比为1:5:20。
所述步骤一中第(1)步中分子筛层析为将蛋白g层析柱层析后收集的含fc片段的组分,上样于分离范围包含5000da-300000da的分子筛,将样品中的各组分按照分子量分离开来,收集分子量为50000da的蛋白,即为完整的双链fc片段。
所述步骤一中待测样品溶液蛋白浓度为0.5~4mg/ml,优化浓度为0.5~2mg/ml,更优化浓度为0.5mg/ml。
所述唾液酸解离步骤为取300μl的1mg/ml待测样品加入100μl0.1m三氟乙酸,金属浴80℃,1h,产物经0.22μm滤膜过滤。
所述高效液相色谱仪中色谱柱:waterssymmetryc18液相色谱柱4.6×2505μm,柱温30℃,荧光检测器激发波长373nm,发射波长448nm,流动相为甲醇、乙腈主超纯水,其中甲醇:乙腈:超纯水=7:8:85,流速为0.9ml/min。
所述标准曲线的绘制中1mg唾液酸标准品加10ml水配制成0.1mg/ml的唾液酸标准溶液,加水分别稀释至5、10、20、30、40ug/ml,取300μl各浓度标准品溶液,分别加入50μldmb衍生液,50℃金属浴避光反应2.5h,20μl进样检测。
本发明测定ivig制品iggfab片段和fc片段唾液酸含量,方法简单,精确、灵敏度高,重复性和准确性高。
附图说明
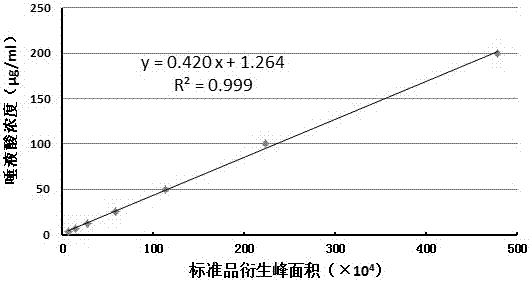
图1为本发明中试验一的唾液酸含量检测标准曲线
图2为本发明中试验二的唾液酸含量检测标准曲线
图3-图9为本发明中试验一中的色谱图
具体实施方式
下面结合具体实施方式对本发明作进一步的详细描述。
实施例1
一种ivig中iggfab片段和fc片段唾液酸含量的测定方法,包括以下具体步骤:
步骤一:待测样品预处理:
(1)双链fc片段的纯化:取ivig,酶切、蛋白g层析和分子筛层析后得到双链fc片段;其中层析得到的双链fc片段溶液经测定蛋白浓度后,稀释或浓缩,获得蛋白浓度为0.5~4mg/ml的溶液待测;分子筛有两个作用,在实验之初,对igg脱盐;或将fc从酶切且经过proteing层析后的产物中纯化出来。
分子筛层析为将蛋白g层析柱层析后收集的含fc片段的组分,上样于分离范围包含5000da-300000da的分子筛,将样品中的各组分按照分子量分离开来,收集分子量为50000da的蛋白,即为完整的双链fc片段。
待测样品溶液蛋白浓度为0.5~4mg/ml,优化浓度为0.5~2mg/ml,更优化浓度为0.5mg/ml。
(2)ivig去除糖类保护剂处理;取ivig,分子筛层析去除糖类保护剂;
将待检测的ivig上样于分子筛,去除糖类组分,层析得到的溶液经测定蛋白浓度后,稀释或浓缩,获得蛋白浓度为0.5~4mg/ml的溶液待测;
本发明中检测的样本ivig,其成分中含有大量麦芽糖、蔗糖等糖类物质,而且唾液酸也是一种糖类衍生物。现在唾液酸含量检测方法中不论是色谱法还是分光光度方法,均基于发色物质或荧光物质与糖类的反应,样本中所含有的糖类物质即便是很少的残留也影响着测定准确性高低。本发明中检测方法首先采取分子筛层析去除样品中的糖类物质,去除干扰,提高检测准确性。
再将去除糖类保护剂后的ivig和纯化后的双链fc片段分别进行步骤二至步骤五处理,得ivig中的唾液酸总含量和fc片段的唾液酸含量;
步骤二:唾液酸解离:用酸性溶剂将待测样品的唾液酸解离下来;唾液酸解离步骤为取300μl的1mg/ml待测样品加入100μl0.1m三氟乙酸,金属浴80℃,1h,产物经0.22μm滤膜过滤。
步骤三:荧光衍生,将dmb衍生液加入步骤二中,50℃金属浴避光反应2.5h;单独的唾液酸是无法被很好地被hplc检测到,需要加入与唾液酸(糖类物质)反应的荧光衍生剂反应后,再上hplc检测。
步骤四:高效液相色谱检测和标准曲线的绘制:用高效液相色谱仪进行检测,再以标准曲线样品梯度浓度为横坐标,标准曲线样品经高效液相色谱检测的衍生峰面积为纵坐标,采用线性方程绘制标准曲线;
高效液相色谱仪中色谱柱:waterssymmetryc18液相色谱柱4.6×2505μm,柱温30℃,荧光检测器激发波长373nm,发射波长448nm,流动相为甲醇、乙腈主超纯水,其中甲醇:乙腈:超纯水=7:8:85,流速为0.9ml/min。
标准曲线的绘制中1mg唾液酸标准品加10ml水配制成0.1mg/ml的唾液酸标准溶液,加水分别稀释至5、10、20、30、40μg/ml,取300μl各浓度标准品溶液,分别加入50μldmb衍生液,50℃金属浴避光反应2.5h,20μl进样检测。
步骤五:唾液酸含量的计算:
将待测样品的经高效液相色谱检测的衍生峰面积代入标准曲线,计算样品中每毫升溶液唾液酸含量,将计算的结果除以样品溶液的蛋白浓度,即得到每mg样品中唾液酸的含量;
其中,fab段唾液酸含量为=(ivig中的唾液酸总含量×ivig分子量-fc片段的唾液酸含量×fc片段分子量)/fab片段分子量;式中,ivig分子量为150,000da,fc片段分子量为55,000da,fab片段分子量为95,000da。实施例2
一种ivig制品iggfab片段和fc段唾液酸含量的测定方法,包括以下步骤:
(1)fc片段的纯化
a酶切:
取ivig1ml,加入edta-na2,l-半胱氨酸盐酸盐和木瓜蛋白酶,酶切,37℃,4h。
b层析纯化:
a、蛋白g层析
将酶切产物过滤后上样于蛋白g(proteing)层析柱层析,收集酶切产物中含有fc片段的组分。
蛋白g层析步骤:
①冲液配制:
结合缓冲液:20mm磷酸纳,ph7.0。洗脱缓冲液:100mm甘氨酸,ph2.7中和缓冲液:1mtris-hcl,ph9.0。
②样品上样前处理
样品加入2倍体积结合缓冲液,充分混匀,放置过夜。上样前一次性0.22um滤器过滤。
③柱平衡
先用5倍柱体积的蒸馏水洗柱,再用5倍体积结合缓冲液洗柱,流速均为1ml/min,至电导、紫外吸收紫外检测器在280nm波长检测等基线稳定。
④上样
样品泵s2管路进样,1ml/min。进样体积约20ml。
⑤洗涤
用5-10倍柱体积的结合缓冲液平衡分离柱,直到基线,即所有未结合物质都被冲洗出柱子(紫外检测器在280nm波长检测)。
⑥洗脱与样品收集
用10倍柱体积的洗脱缓冲液进行洗脱。收集洗脱峰,收集后立即用中和缓冲液(0.06ml~0.2ml1mtris-hcl)中和至中性。
b、分子筛层析
将蛋白g层析柱层析后收集的所有含fc片段的组分(包括双链fc、未酶切的ivig,以及部分含铰链区的单链fc),上样于分离范围包含5000da-300000da的分子筛,将样品中的各组分按照分子量分离开来,收集分子量为50000da的蛋白,即为完整的双链fc片段。
分子筛层析步骤:
①柱平衡
用2倍柱体积超纯水冲洗hiprep26/60sephacryls-200highresolution预装柱后,用2倍柱体积0.9%生理盐水平衡。
②样品处理与上样
浓缩样品,至浓度10mg/ml或以上。进样体积5ml,流速1.3ml/min。
③层析
生理盐水1.3ml/min洗涤,约3个小时直至所有组分的峰全部出完。
④峰收集
在约90-120min之间,出现第二个样品峰,此峰的主要成分即我们所需要的fc片段的峰。
(2)唾液酸含量检测
a待测样品前处理:
待测样品为ivig和纯化的双链fc片段;
将ivig上样于能够分子筛,去除其中含有的糖类组分;
将去除糖类保护剂的ivig和双链fc片段经稀释或超滤浓缩,获得浓度为0.5mg/ml的蛋白样品。
b唾液酸解离:
利用酸性条件(tfa,盐酸,醋酸)将ivig或双链fc片段上的唾液酸解离下来。
取300μl蛋白样品(1mg/ml)加入100μl0.1m三氟乙酸(7.45ml三氟乙酸加水至100ml),金属浴80℃,1h,产物经0.22μm滤膜过滤。
c荧光衍生
取上一步反应产物,加入dmb衍生液,50℃金属浴避光反应2.5h,20μl进样检测。
d高效液相色谱检测:
色谱柱:waterssymmetryc18液相色谱柱4.6×2505μm;柱温30℃;荧光检测器激发波长373nm,发射波长448nm;流动相为甲醇:乙腈:超纯水=(7:8:85);流速为0.9ml/min;
e标准曲线的绘制:
1mg唾液酸标准品加10ml水配制成0.1mg/ml的唾液酸标准溶液。加水分别稀释至5、10、20、30、40ug/ml。取300μl各浓度标准品溶液,分别加入50μldmb衍生液,50℃金属浴避光反应2.5h,20μl进样检测。
以标准曲线样品梯度浓度为横坐标,标准曲线样品经高效液相色谱检测的衍生峰面积为纵坐标,采用线性方程绘制标准曲线。
f唾液酸含量的计算:
将待测样品的经高效液相色谱检测的衍生峰面积代入标准曲线,计算样品中唾液酸含量。
其中ivig中的唾液酸总含量和fc片段的唾液酸含量经以上计算直接得出;fab段唾液酸含量为ivig中的唾液酸总含量减去fc片段的唾液酸含量得到。
试验一:比较是否去除糖类保护剂对样品测定结果的影响
设试验组和对照组,其它步骤相同,试验组有去除糖类保护剂步骤,制品溶液为a1和b1;对照组没有去除糖类保护剂步骤,制品溶液为a2和b2;具体步骤如下:
(1)待测样品制备:
以市售的a、b两个公司的ivig制品为检测样品,分别经层析去除保护剂的处理和不经去除糖类保护剂的处理后,用本发明所述方法绘制标注曲线并检测其ivig唾液酸总含量。
试验组中去除糖类保护剂的ivig样品制备
设置流速1ml/min,用2倍柱体积超纯水冲洗hiprep26/60sephacryls-200highresolution预装柱后,用2倍柱体积生理盐水平衡;取市售的a公司的ivig制品2ml上样于层析柱层析,收集分子量为150,000da(的蛋白液;经测定蛋白浓度后,利用生理盐水对其稀释,获得蛋白浓度为0.5~4mg/ml的溶液a1;
重复以上步骤,对b公司静注人免疫球蛋白进行处理,获得蛋白浓度为0.5~4mg/ml的溶液b1,待测。
对照组中不去除糖类保护剂的ivig样品制备
利用生理盐水将a、b公司ivig制品稀释至0.5~4mg/ml,分别获得蛋白溶液a2、b2,待测。
(2)唾液酸含量检测
a唾液酸解离:
取300μl蛋白样品加入100μl0.1m三氟乙酸,金属浴80℃,1h。
b荧光衍生:
取上一步反应产物,加入dmb衍生液,50℃金属浴避光反应2.5h。
c高效液相色谱检测:
选择色谱柱:waterssymmetryc18液相色谱柱;柱温30℃;荧光检测器激发波长373nm,发射波长448nm;流动相为甲醇:乙腈:超纯水=(7:8:85);设置流速为0.9ml/min,上样体积10μl,将待测样品进样于色谱柱进行检测,并计算进样10~14min出现的最大衍生峰的面积。
d标准曲线的绘制:
以n-乙酰神经氨酸作为标准品,用生理盐水将其溶解并稀释至浓度梯度:0、6.25、12.5、25、50、100、200μg/ml。以不同浓度标准品为样品,重复步骤“b”、“c”,获得各浓度标准品在进样10~14min时出现的最大衍生峰的面积。不同标准品高效液相色谱图如图3-9所示,目标峰明显,易于判断。
目标衍生峰全部在12.3分钟出现,对不同浓度标准品检测实验中标准品浓度、色谱峰的出峰时间、峰面积相关对应数据整理见表1:
表1:标准品(标准曲线)色谱数据
(注:编号a到g,分别一一对应于图3到图9,试验一中以下相同)。
以标准曲线样品浓度为纵坐标,标准曲线样品经高效液相色谱检测的衍生峰面积为横坐标,采用线性方程绘制标准曲线,并获得曲线方程,如图1所示,能够拟合得到较好的直线方程,相关系数的平方(r2)大于0.99。
e唾液酸含量的计算:
将待测样品的经高效液相色谱检测的衍生峰面积代入标准曲线,计算样品中每毫升溶液唾液酸含量,将计算的结果除以样品溶液的蛋白浓度,即得到每mg蛋白上唾液酸的含量。
f重复实验
重复以上方法,对制待测样品进行重复试验,结果求均值如下表2:
表2
从结果能够看出,试验组a1、b1小于对照组a2、b2,其原因为:本发明中检测的样本ivig,其成分中含有大量麦芽糖、蔗糖等糖类物质,而且唾液酸也是一种糖类衍生物。色谱法进行唾液酸含量检测方法时基于发色物质或荧光物质与糖类的反应,因为对照组a2、b2并未去除保护剂中含有的糖类,能与dmb发生衍生,导致测定结果偏大,不准确。试验组样品a1、b1是将ivig制品a、b经过分子筛层析后获得的不含糖类保护剂的蛋白样品,去除了影响检测的因素,使结果更准确。因此,本发明中在检测ivig制品的唾液酸含量前对ivig进行分子筛层析处理是需要和取得了好的效果。
试验二
以市售的c、d、e、f四个公司的ivig制品为检测样品,用本发明所述方法进行检测。
(1)fc片段的纯化
a酶切:
取市售的c公司的ivig制品1ml,分别加入100μgedta-na2,500μgl-半胱氨酸盐酸盐和2mg木瓜蛋白酶,酶切,37℃,4h。
b层析纯化:
(1)蛋白g层析
①缓冲液配制:
结合缓冲液:20mm磷酸纳,ph7.0。洗脱缓冲液:100mm甘氨酸,ph2.7,中和缓冲液:1mtris-hcl,ph9.0
②层析
设置流速1ml/min,先用5倍柱体积的蒸馏水洗涤蛋白g层析柱,再用5倍体积结合缓冲液洗柱;取步骤“a”中获得的酶切产物加入2倍体积结合缓冲液,充分混匀后上样于层析柱,再经5倍柱体积的结合缓冲液平衡层析柱后,用10倍柱体积的洗脱缓冲液进行洗脱,收集洗脱液,并用中和缓冲液调节其ph至中性。
(2)分子筛层析
设置流速1ml/min,用2倍柱体积超纯水冲洗hiprep26/60sephacryls-200highresolution预装柱后,用2倍柱体积生理盐水平衡;取步骤“a”中获得的酶切产物上样于层析柱层析,收集分子量为50000~60000da的蛋白液。
(3)层析得到的溶液经测定蛋白浓度后,利用蛋白超滤离心管浓缩,获得蛋白浓度为0.5~4mg/ml的溶液;
c重复以上步骤,纯化b、c、d三个公司fc片段,待测。
(2)ivig的层析处理
设置流速1ml/min,用2倍柱体积超纯水冲洗hiprep26/60sephacryls-200highresolution预装柱后,用2倍柱体积生理盐水平衡;取市售的a公司的ivig制品2ml上样于层析柱层析,收集分子量为150000da的蛋白液;经测定蛋白浓度后,利用生理盐水对其稀释,获得蛋白浓度为0.5~4mg/ml的溶液;
重复以上步骤,对d、e、f三个公司静注人免疫球蛋白进行处理,待测。
(3)唾液酸含量检测
a唾液酸解离:
取300μl蛋白样品加入100μl0.1m三氟乙酸,金属浴80℃,1h。
b荧光衍生:
取上一步反应产物,加入dmb衍生液,50℃金属浴避光反应2.5h。
c高效液相色谱检测:
选择色谱柱:waterssymmetryc18液相色谱柱;柱温30℃;荧光检测器激发波长373nm,发射波长448nm;流动相为甲醇:乙腈:超纯水=(7:8:85);设置流速为0.9ml/min,上样体积10μl,将待测样品进样于色谱柱进行检测,并计算进样10~14min出现的最大衍生峰的面积。
d标准曲线的绘制:
以n-乙酰神经氨酸作为标准品,用生理盐水将其溶解并稀释至浓度梯度:3.125、6.25、12.5、25、50、100、200μg/ml。以不同浓度标准品为样品,重复步骤“b”、“c”,获得各浓度标准品在进样10~14min时出现的最大衍生峰的面积。
以标准曲线样品浓度为纵坐标,标准曲线样品经高效液相色谱检测的衍生峰面积为横坐标,采用线性方程绘制标准曲线,并获得曲线方程,如图2所示:
e唾液酸含量的计算:
将待测样品的经高效液相色谱检测的衍生峰面积代入标准曲线,计算样品中每毫升溶液唾液酸含量,将计算的结果除以样品溶液的蛋白浓度,即得到每mg蛋白上唾液酸的含量。
其中ivig中的唾液酸总含量和fc片段的唾液酸含量经以上计算直接得出;fab段唾液酸含量为:
(ivig中的唾液酸总含量×ivig分子量-fc片段的唾液酸含量×fc片段分子量)/fab片段分子量
其中,ivig分子量为150,000da,fc片段分子量为55,000da,fab片段分子量为95,000da。
f重复实验
重复以上方法,共计对制待测样品进行3次重复试验,结果统计如下表3:
表3
从以上可以得出,本发明中的检测方法准确,且重复性高。
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!