一种尿液羟基多环芳烃的快速检测方法与流程
本发明涉及一种快速检测方法,特别涉及一种尿液羟基多环芳烃的快速检测方法。
背景技术:
尿中OH-PAHs是致癌性环境有机污染物PAHs的重要生物标志物,在人体对PAHs暴露及健康风险评价研究(如PAHs分子流行病学研究)中意义重大。
尿中OH-PAHs的检测流程主要包括样品前处理和仪器分析两部分。其中,样品前处理过程能够直接影响整个分析方法的灵敏度/检测限、重现性和分析速度。目前,文献报道尿中OH-PAHs的前处理技术主要包括:固相萃取(Solid phase extraction,SPE)、固相微萃取(Solid-phase microextraction,SPME)、液液萃取(Liquid-liquid extraction,LLE)、液液微萃取(Liquid-liquid microextraction,LLME)、免疫亲和萃取(Immunosorbent extraction)等。固相萃(SPE)虽然能基本满足检测的需要,但是前处理方式耗时长,有机溶剂使用量大,需要特定的实验设备且对操作者有较高的技术要求,难以满足大量样品的分析工作,无法实现对OH-PAHs的临床常规检测。
2006年,Assidi[1]提出了用液液分散萃取(DLLME)的方法来提取水溶液中的微量有机化合物,此方法操作简单、快速,需要的萃取溶剂少,且能提供很好的回收率,但不能用于尿液样品等复杂基质中有机化合物的萃取。2008年,Leong[2]等人对DLLME方法进行改进,他结合了固体悬浮有机液滴(SFO)的方法,使用密度小于水的低毒性有机溶剂作为萃取剂。悬浮有机液滴置于低温下凝固后,很容易被收集,弥补了传统DLLME方法的不足,此方法也被广泛应用于尿液、血液以及环境样品中极性和非极性物质的提取,但相关方法尚未实现对OH-PAHs的提取[3,4]。2012年,Wang用液液分散萃取的方法萃取了沉积物中8种OH-PAHs,使用氯苯作为萃取剂[5]。相关方法有望用于提取尿液中的OH-PAHs,但氯苯毒性较大,不利于操作者与环境安全。
参考文献:
1.Rezaee M,Assadi Y,Milani Hosseini MR,Aghaee E,Ahmadi F and Berijani S:Determination of organic compounds in water using dispersive liquid-liquid microextraction.J Chromatogr A.1116:1-9,2006.
2.Leong MI and Huang SD:Dispersive liquid-liquid microextraction method based on solidification of floating organic drop combined with gas chromatography with electron-capture or mass spectrometry detection.J Chromatogr A.1211:8-12,2008.
3.Ahmadi-Jouibari T,Fattahi N and Shamsipur M:Rapid extraction and determination of amphetamines in human urine samples using dispersive liquid-liquid microextraction and solidification of floating organic drop followed by high performance liquid chromatography.J Pharm Biomed Anal.94:145-51.
4.Chen B and Huang Y:Dispersive liquid-phase microextraction with solidification of floating organic droplet coupled with high-performance liquid chromatography for the determination of Sudan dyes in foodstuffs and water samples.J Agric Food Chem.62:5818-26.
5.Wang X,Lin L,Luan T,Yang L and Tam NF:Determination of hydroxylated metabolites of polycyclic aromatic hydrocarbons in sediment samples by combining subcritical water extraction and dispersive liquid-liquid microextraction with derivatization.Anal Chim Acta.753:57-63。
技术实现要素:
本发明的目的在于提供一种尿液羟基多环芳烃的快速检测方法,该方法同时还极为绿色环保,同时也是一种高通量的检测方法。
本发明所采取的技术方案是:
一种尿液羟基多环芳烃的快速检测方法,包括如下步骤:
1)尿样预处理:将尿样离心并对上清进行酶解处理使OH-PAHs游离,得到预处理的尿样;
2)萃取:在预处理的尿样中加入混合均匀的分散剂丙酮和萃取剂正十一醇,混匀后分层,正十一醇层悬浮于表面;
3)将样品冷却至正十一醇层凝固,取出凝固的正十一醇层溶解于有机溶剂中,进行色谱分析。
优选的,丙酮和正十一醇的体积混合比为20:(1~4),更佳为20:(1~3)。
优选的,丙酮和正十一醇混合液与尿样的体积混合比为1:(5~40),进一步的,丙酮和正十一醇的体积混合比为20:(1~3)。
优选的,酶解处理的操作如下:
1)在尿样上清加入pH缓冲剂并调节上清的pH至酶的最适pH;
2)加入适量葡糖甘酸酶/硫酸酯酶,混匀后振荡至酶解完全。
优选的,酶解处理时使用的pH缓冲剂为醋酸-醋酸钠缓冲体系,反应体系的pH为5~6。
优选的,萃取前,将预处理的尿样的pH调节至4~6。
优选的,萃取前,将预处理的尿样的离子质量浓度调节至15~25%。
本发明的有益效果是:
与现有技术相比,发明采用分散液液萃取-上浮液滴固化法快速富集,高效液相色谱-荧光检测方法,快速有效地检测尿液中的OH-PAHs,其中前处理过程采用微量的有机溶剂(400μL丙酮和40μL正十一醇)进行快速注射提取,处理过程仅需15分钟即可完成;使用溶剂量是传统固相萃取的1/30,处理时间仅为传统方法的1/16,大大降低了流行病学上大量样本的处理成本和分析时间,同时也更为绿色环保,有利于保护对分析操作人员的身体健康。
附图说明
图1是尿液pH值对6种加标OH-PAHs回收率的影响;
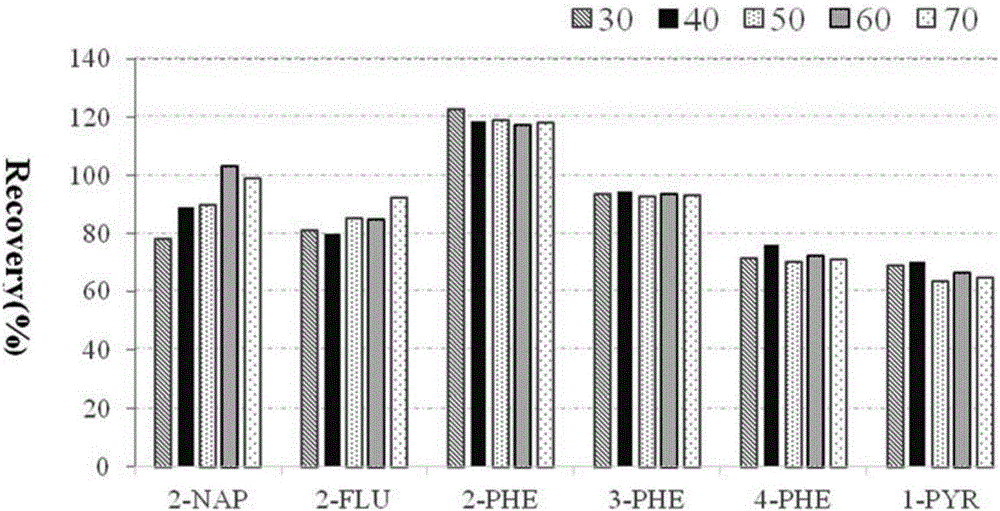
图2是萃取剂(正十一醇)的体积对回收率的影响;
图3是分散剂的选择对回收率的影响;
图4是分散剂的体积对回收率的影响;
图5是盐的添加量对回收率的影响。
具体实施方式
一种尿液羟基多环芳烃的快速检测方法,包括如下步骤:
1)尿样预处理:将尿样离心并对上清进行酶解处理使OH-PAHs游离,得到预处理的尿样;
2)萃取:在预处理的尿样中加入混合均匀的分散剂丙酮和萃取剂正十一醇,混匀后分层,正十一醇层悬浮于表面;
3)将样品冷却至正十一醇层凝固,取出凝固的正十一醇层溶解于有机溶剂中,进行色谱分析。
优选的,丙酮和正十一醇的体积混合比为20:(1~4),更佳为20:(1~3)。
优选的,丙酮和正十一醇混合液与尿样的体积混合比为1:(5~40),进一步的,丙酮和正十一醇的体积混合比为20:(1~3)。
优选的,酶解处理的操作如下:
1)在尿样上清加入pH缓冲剂并调节上清的pH至酶的最适pH;
2)加入适量葡糖甘酸酶/硫酸酯酶,混匀后振荡至酶解完全。
优选的,酶解处理时使用的pH缓冲剂为醋酸-醋酸钠缓冲体系,反应体系的pH为5~6。
调节尿液的pH值,增加或减少尿液中质子的总量,可有利于OH-PAHs的萃取。优选的,萃取前,将预处理的尿样的pH调节至4~6。
在尿液中添加盐溶液增加尿液中的离子强度,有利于OH-PAHs以分子形式存在于尿液中,易于萃取。优选的,萃取前,将预处理的尿样的离子质量浓度调节至15~25%。
下面结合实验,进一步说明本发明的技术方案。
目标物标准溶液的配制
购于Cambridge Isotope Laboratories的单标浓度均为50mg/L,作为储备液;OH-PAHs标准混合使用液:量取OH-PAHs各单体的标准储备液于10mL容量瓶中,用甲醇稀释定容,得到OH-PAHs浓度为5mg/L的混合标准使用液。稀释混标得到浓度分别为10、50、250μg/L,作为加标尿样的浓度。标样密封于-20℃冰箱避光保存。
样品预处理
1)样品离心:取出冷藏样品放至室温后,取多于5mL的尿样,3000r/min离心后,取上层清液;
2)样品的酶解:准确量取5mL尿样(离心后的上层清液)于具塞刻度离心管中,加回收率指示物使用溶液10μL,混匀后加0.5mL盐酸和1.5mL醋酸钠和醋酸的缓冲溶液,调节pH值为5.5,加20μL葡糖甘酸酶/硫酸酯酶,混匀后置于恒温振荡箱中反应16h,恒温37℃,振荡箱振荡速度100r/min。
样品的萃取
1)取上述酶解好的尿样5ml,分别加入不同比例混合均匀的分散剂和萃取剂正十一醇,之后用注射器吸取混合均匀的分散剂和萃取剂,快速注入尿样中,混匀进行萃取;
2)萃取完成后离心,使正十一醇悬浮于表面,将样品冷冻至正十一醇凝固;
3)取出凝固的正十一醇,用甲醇溶解,过0.2μm的尼龙膜去除颗粒物后进行色谱分析。
下面基于上述样品的萃取处理流程,改变其中的部分条件,确定不同萃取条件对OH-PAHs回收率的影响。
pH对加标化合物回收率的影响
在加标(6种OH-PAHs)浓度为50μg/L的尿样中,调节尿液的pH值分别为2、3、4、5、6、7、8和9,添加2.0g的NaCl调节盐溶液浓度,取400μL丙酮与40μL的正十一醇混合,萃取时间为5min,比较加标化合物的回收率。实验结果如图1所示,从图中可以看出,pH 3~6时,6种OH-PAHs均具有较好的回收率,pH为5时最佳。
萃取剂同量对加标化合物回收率的影响
在加标(6种OH-PAHs)浓度为50μg/L的尿样中,调节尿液的pH值为5,添加2g NaCl调节盐溶液浓度,取分散剂为400μL丙酮分别与30、40、50、60和70μL体积的萃取剂(正十一醇)混合,萃取时间为5min,比较加标化合物的回收率。实验结果如图2所示,从图中可以看出,正十一醇的添加量对6种OH-PAHs的回收率有一定的影响,添加量在30~70μL时均具有较好的回收率,特别是其用量为40μL时,具有最佳的综合回收率。
分散剂对回收率的影响
在加标(6种OH-PAHs)浓度为50μg/L的尿样中,调节尿液的pH值为5,添加2g NaCl调节盐溶液浓度,取分散剂的体积为400μL,三种溶剂(甲醇、乙腈和丙酮)分别与40μL的正十一醇混合,萃取时间为5min,比较加标化合物的回收率。实验结果如图3所示,从图中可以看出,当分散剂为丙酮时,能使6种OH-PAHs均获得良好的回收率。
分散剂体积对回收率的影响
在加标(6种OH-PAHs)浓度为50μg/L的尿样中,调节尿液的pH值为5,添加2g NaCl调节盐溶液浓度,取分散剂丙酮的体积分别为200、300、400、500和600μL,分别与40μL的正十一醇混合,萃取时间为5min,比较加标化合物的回收率。实验结果如图4所示,从图中可以看出,丙酮的用量在200~400μL时,6种OH-PAHs的回收率均可以接受,综合考虑,丙酮的体积为400μL时,6种OH-PAHs的回收率最佳。
盐溶液的量对回收率的影响
在加标(6种OH-PAHs)浓度为50μg/L的尿样中,调节尿液的pH值为5,分别添加0.5、1.0、1.5和2.0g的NaCl调节盐溶液浓度,取400μL丙酮与40μL的正十一醇混合,萃取时间为5min,比较加标化合物的回收率。实验结果如图4所示,从图中可以看出,盐的添加量在1~2g时,6种OH-PAHs的回收率均可以接受,盐的添加量为2时,6种OH-PAHs可以获得最佳的回收率。
萃取时间对回收率的影响
在加标(6种OH-PAHs)浓度为50μg/L的尿样中,调节尿液的pH值为5,添加2.0g的NaCl调节盐溶液浓度,取400μL丙酮与40μL的正十一醇混合,萃取时间分别为2、5、10和20min,比较加标化合物的回收率。发现随着萃取时间的增加,化合物的回收率几乎没变化,因此认为分散液液萃取过程非常快速,为了达到充分的萃取,最终选择萃取时间为5min。
综上,为获得最佳的萃取效果,选择的萃取条件为:每5ml酶解处理后的尿样,调节尿液的pH值为5,添加2.0g的NaCl调节盐溶液浓度,取400μL丙酮与40μL的正十一醇混合,萃取时间为5min。
采用上述优化的萃取条件,将处理得到的固化正十一醇取出,溶于400μL甲醇中,过0.2μm的尼龙膜去除颗粒物,进液相色谱检测分析。
液相色谱及检测器条件
色谱柱:Agilent ZORBAX SB-C18柱子,内径4.6mm,长250mm,不锈钢柱。柱填充:C18键合多孔硅胶,粒径5μm;柱温:25℃;流动相梯度淋洗比例和流速见表1;检测波长见表2;进样量:20μL。
表1流动相比例及流速
表2紫外光检测参数
以甲醇为溶剂将下述目标物标样配置得到不同的浓度梯度(共7个检测点),绘制标准曲线并检测计算其线性范围。当线性系数(R2)>0.999时,表明线性较好,可由此进行定量计算。其中,RSD为同一浓度3次检测的标准偏差,LOD为最低检测浓度,LOQ为最低定量浓度,浓缩倍数为尿液处理后体积较原始样本体积的缩小倍数。实验结果如表3所示。
表3 DLLME-SFO方法分析人体尿液的分析特征
将相应标准品按如下加标浓度分别加入尿液样本中,经样本处理与萃取后,计算相应目标物的回收率。实验结果如表4所示。
表4各种加标浓度下的回收率
在上述优化的萃取条件下,采用高效液相色谱荧光检测器检测,6种羟基多环芳烃的富集倍数可达到52~65倍;各化合物的回收率达到70.4%~129%;方法检出限(S/N=3)在0.5~1.0μg/L。
- 还没有人留言评论。精彩留言会获得点赞!