基于微滴和纳米荧光探针的胞内蛋白检测方法与流程
本发明涉及一种胞内蛋白检测方法,特别涉及一种基于微滴和纳米荧光探针的胞内蛋白检测方法。
背景技术:
在单细胞水平上分析细胞内部组分是当前生物医学研究的迫切需求,随着单细胞测序、单细胞转录组等技术的不断发展,人类从DNA、RNA的水平深入了解细胞群体异质性。在蛋白质检测方面,免疫荧光染色和流式细胞术是最常用的单细胞胞内蛋白检测方法。但免疫荧光染色和流式细胞术检测时,需要对细胞进行固定,打孔,以便使细胞膜变得可渗透,然后孵育抗体,标记待检测靶蛋白。这种方法步骤繁琐,操作时间长,而且对固定、打孔步骤所用的试剂浓度和反应时间要求较高,固定不完全或打孔时间过长会导致细胞破裂,打孔时间过短则会导致抗体无法充分进入细胞同胞内蛋白结合,影响胞内蛋白检测的准确性。此外现有的固定方法如醛固定术等尽管可以保存细胞的形态,但是许多抗原位点也被固定方法破坏,影响蛋白检测的灵敏度和准确度。因此亟需一种快速、灵敏、稳定的单细胞胞内蛋白检测方法。
技术实现要素:
针对现有技术中存在的技术问题,本案提供一种基于微滴和纳米荧光探针的胞内蛋白检测方法。
微流控技术是在微米级结构中操控纳升至皮升体积流体的科学技术,由于微结构的尺寸与细胞在同一尺度,而且在微流控芯片上进行生化反应具有试剂和样品量少、快速实时、大量样本平行处理、防止样品交叉污染等诸多优点,微流控技术已成为单细胞分析的有力工具。
数字微滴技术利用微流控芯片中流体的剪切力得到微小体积(1fl-102nl)的微滴,微滴间无交叉污染,微滴可快速连续产生,可在几分钟内完成数万个微滴的生成与检测,而且芯片设计加工相对简单,已被用于细胞的高通量快速分选、蛋白、核酸检测等领域。
纳米材料尺寸分布特殊,具有表面效应、小尺寸效应以及宏观量子隧道效应,从而表现出一系列独特的电学、光学、磁学性能,将纳米材料用于生物分子标记,可显著提高检测的灵敏度。将纳米颗粒同荧光探针结合的纳米荧光探针技术已被用于单细胞RNA检测。但该技术依赖胞吞作用,无法快速准确测定细胞核酸的即时含量。因此,将数字微滴技术同纳米荧光探针技术相结合,可以在单个微滴内实现单个细胞的快速捕获、裂解、探针结合和检测,避免了细胞固定、打孔等繁琐步骤,将显著提高检测速度和检测通量,实现单细胞胞内蛋白的快速、灵敏探测。
本案通过以下技术方案实现:
一种基于微滴和纳米荧光探针的胞内蛋白检测方法,其包括:
1)制备纳米荧光探针复合物;
2)将待测细胞悬液加入到微流控芯片的第一样品孔,将所述纳米荧光探针复合物和细胞裂解液加入到所述微流控芯片的第二样品孔,将流动相加至所述微流控芯片的流动相孔,驱动待测细胞悬液、纳米荧光探针复合物、细胞裂解液和流动相进入所述微流控芯片的微流控管道,并在流体剪切力作用下生成油包水微滴,待测细胞悬液中的细胞、纳米荧光探针复合物和细胞裂解液均被包裹在微滴中;
3)在37℃孵育20-60min,使微滴中的细胞裂解后释放出胞内蛋白并与纳米荧光探针复合物结合;
4)采用数字PCR系统或荧光拍照检测微滴的荧光强度,从而测出胞内蛋白的含量。
优选的是,所述的基于微滴和纳米荧光探针的胞内蛋白检测方法,其中,所述纳米荧光探针复合物包括有:纳米金颗粒、与靶蛋白产生特异性结合的靶向识别DNA链、以及与该靶向识别DNA链杂交互补的荧光探针链。
优选的是,所述的基于微滴和纳米荧光探针的胞内蛋白检测方法,其中,所述纳米金颗粒表面经巯基化处理。
优选的是,所述的基于微滴和纳米荧光探针的胞内蛋白检测方法,其中,所述纳米金颗粒的粒径为5-30nm。
优选的是,所述的基于微滴和纳米荧光探针的胞内蛋白检测方法,其中,所述流动相选自氟化油、石蜡油、矿物油或其组合。
优选的是,所述的基于微滴和纳米荧光探针的胞内蛋白检测方法,其中,所述待测细胞悬液中还添加有Percoll分离液或Ficoll分离液。
优选的是,所述的基于微滴和纳米荧光探针的胞内蛋白检测方法,其中,每个微滴中的细胞数量不超过1个。
本发明的有益效果是:
1、本发明将数字微滴技术同纳米荧光探针相结合,通过将单个细胞和纳米荧光探针检测探针包裹在单个微滴中,细胞在微滴内破裂后释放出胞内蛋白,进而同纳米荧光探针探针结合,从而检测出单细胞胞内蛋白含量。
2、本发明无需常规流式细胞术和免疫荧光检测方法中的固定、打孔破膜,避免了抗原结合位点损失,简化了操作步骤、提高了检测灵敏度。
附图说明
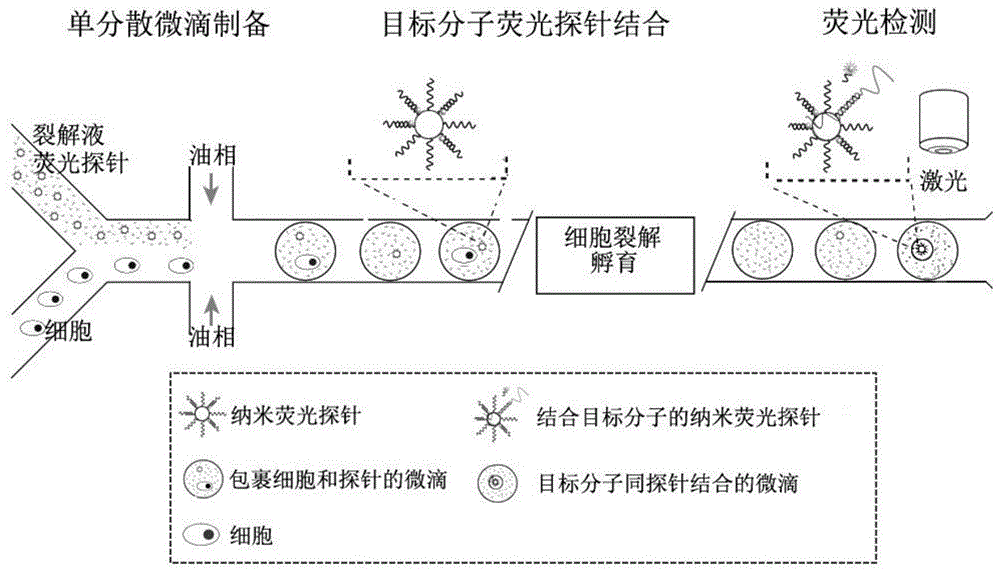
图1为本案胞内蛋白检测方法的检测原理示意图。
图2为本案实施例3的荧光发射光谱图。
具体实施方式
下面结合附图对本发明做进一步的详细说明,以令本领域技术人员参照说明书文字能够据以实施。
本案列出一实施例的基于微滴和纳米荧光探针的胞内蛋白检测方法,其包括:
1)制备纳米荧光探针复合物;
2)将待测细胞悬液加入到微流控芯片的第一样品孔,将所述纳米荧光探针复合物和细胞裂解液加入到所述微流控芯片的第二样品孔,将流动相加至所述微流控芯片的流动相孔,驱动待测细胞悬液、纳米荧光探针复合物、细胞裂解液和流动相进入所述微流控芯片的微流控管道,并在流体剪切力作用下生成油包水微滴,待测细胞悬液中的细胞、纳米荧光探针复合物和细胞裂解液均被包裹在微滴中;
3)在37℃孵育20-60min,使微滴中的细胞裂解后释放出胞内蛋白并与纳米荧光探针复合物结合;
4)采用数字PCR系统或荧光拍照检测微滴的荧光强度,从而测出胞内蛋白的含量。
其中,纳米荧光探针复合物包括有:纳米金颗粒、与靶蛋白产生特异性结合的靶向识别DNA链、以及与该靶向识别DNA链杂交互补的荧光探针链。
其中,纳米金颗粒表面优选经巯基化处理。
其中,纳米金颗粒的粒径优选为5-30nm。
其中,流动相选自氟化油、石蜡油、矿物油或其组合。
其中,待测细胞悬液中还可优选添加有Percoll分离液或Ficoll分离液。
其中,每个微滴中的细胞数量不超过1个。
当待测细胞中不含靶蛋白时,靶向识别DNA链同探针链结合,探针链所标记的荧光被淬灭。当待测细胞中含有靶蛋白时,靶向识别DNA链同靶蛋白结合,荧光探针链被释放到溶液中,在激光激发下发出荧光。油包水微滴,油相选用氟化油、石蜡油或矿物油,水相为待测细胞悬液或纳米荧光探针溶液中的水。油相溶液和水相溶液通过注射泵进入微流控管道并剪切形成油包水微滴。控制油相溶液和水相溶液的进样速度,可以保证每个微滴中仅含有1个细胞或不含细胞。细胞包裹于微滴后在细胞裂解液作用下破裂释放出胞内蛋白,释放出的胞内蛋白同纳米荧光探针复合物结合,释放出荧光探针链,在激光激发作用下发出荧光。
实施例1
纳米荧光探针复合物制备
24μL的10mM巯基化单链DNA溶液与1200μL的5nm金纳米粒子或者600μL的10nm金纳米粒子溶液混合,然后加10mM pH7.0的磷酸盐缓冲液,使得与5nm金纳米粒子溶液混合的单链DNA的最终浓度为80nM,或与10nm金纳米粒子溶液混合的单链DNA的最终浓度为160nM。静置24h,加NaCl溶液使最终浓度为0.1M,继续反应40h,离心去除过量的巯基化DNA,用0.1M NaCl和10mM磷酸盐缓冲液清洗沉淀,然后将沉淀用0.1M PBS重悬。
加入3-巯基-1-丙醇使最终浓度为3μM,24h后离心处理,然后将沉淀重悬于缓冲液A(缓冲液A:20mM Tris-HCl,140mM NaCl,5mM KCl,1mM MgCl2,溶液pH 7.4)。
实施例2
微滴制备与胞内蛋白探针结合
利用微流控芯片的流体剪切作用制备油包水微滴,微流控芯片包含3个进样孔和一个出孔,3个进样孔分别加入待测细胞悬液、与纳米荧光探针复合物+细胞裂解液和流动相,其中流动相选用氟化油,细胞裂解液成分选用1%Tritionx X-100,调节细胞悬液浓度至5×105-2×106个/mL之间,出孔连接负压系统,打开负压系统,调节压力至20-40kPa,细胞悬液和纳米荧光探针复合物及流动相在负压作用下流过微流控芯片管道十字交叉节点,在流体剪切作用下生成。通过调节细胞悬液浓度和负压系统压力,来使单个微滴内细胞数目不超过1个。
微滴制备完成后,转移至PCR反应管中,37度孵育20-60min,细胞在细胞裂解液作用下裂解,胞内蛋白释放,然后与纳米荧光探针复合物结合反应,释放出荧光标记探针。
实施例3
基于微滴和纳米荧光探针的检测p53突变蛋白检测
p53基因是一种抑癌基因,定位于人类染色体17p13.1,编码393个氨基酸组成的53kD的核内磷酸化蛋白,被称为p53蛋白。p53基因是细胞生长周期中的负调节因子,与细胞周期的调控、DNA修复、细胞分化、细胞凋亡等重要的生物学功能有关。p53基因分为野生型和突变型两种,突变型p53蛋白稳定性增加,半衰期延长,p53基因的突变(缺失)是人类肿瘤的常见事件,与肿瘤的发生、发展有关。一般认为p53过表达与肿瘤的转移、复发及不良预后相关。因此定量检测细胞中p53突变蛋白含量对肿瘤诊断和治疗具有重要意义。
取人肺肿瘤细胞,调节细胞悬液浓度至106个/mL,加10μL至微流控芯片样品孔中,具体操作方法同实施例2;所用靶向识别DNA链为:5’-ATTAGCGCATTTTAACATAGGGTGC-AAAAA-Propylthiol-3’;所用荧光探针链为:3’-TAAAATTGTATCCCACG-T-Cy5-5’。
图2列出了实施例3的荧光发射光谱图。曲线1和曲线2分别是未结合目标分子和结合非特异性分子的荧光探针发射光谱,曲线3是结合目标分子的发射光谱。未结合目标分子的荧光探针和非特异性吸附的对照探针荧光都比较弱,和目标分子结合后荧光强度明显变强,说明本案方法可用于目标分子的特异性检测。
尽管本发明的实施方案已公开如上,但其并不仅仅限于说明书和实施方式中所列运用,它完全可以被适用于各种适合本发明的领域,对于熟悉本领域的人员而言,可容易地实现另外的修改,因此在不背离权利要求及等同范围所限定的一般概念下,本发明并不限于特定的细节和这里示出与描述的图例。
实施例3中的靶向识别DNA链为:5’-ATTAGCGCATTTTAACATAGGGTGC-AAAAA-Propylthiol-3’;
荧光探针链为:3’-TAAAATTGTATCCCACG-T-Cy5-5’。
- 还没有人留言评论。精彩留言会获得点赞!