收入重症监护病房的患者发生播散性感染的风险预测的制作方法
本发明涉及感染性疾病领域。更具体而言,本发明涉及一种通过使用凝溶胶蛋白作为生物标志预测收入重症监护的患者发生播散性感染或者脓毒性综合征的风险的方法。
脓毒性综合征,是对感染的全身反应,也称作播散性感染,是在重症监护中导致死亡的主要原因之一。事实上,在重症监护治疗的患者是易受攻击的患者,其具有或者可能具有一或多种直接影响其预后生存的急性内脏功能障碍。可导致患者收入重症监护的原因多种多样:休克状态、多发性创伤、昏迷、急性器官功能不全、由于慢性疾病所致呼吸困难、出血、中毒、重度感染、大面积烧伤、大手术的术后期等。通常地,需要重症监护的患者患有器官衰竭如血流动力学不稳定(低血压/高血压)、呼吸窘迫、急性肾功能不全、重度心律失常、神经学病症(颅脑创伤、休克、昏迷)等。这些病症的组合称作多脏器衰竭。事实上,由于大多数器官系统是彼此联系的,因此这些衰竭之一经常导致另一衰竭。
呆在重症监护需要持续监测生命机能,及在适当情况中使用补充方法(输入血液制剂、血管充盈、机械通气、儿茶酚胺、血液透析、体外循环等)。重症监护的最终目标是恢复体内稳态。
结果,收入重症监护的患者处于细菌、病毒、真菌或者寄生物源的医院感染的风险中。
医院感染定义为在医院内的感染,也就是说当患者进入医院(在这种情况中是收入重症监护室)时不存在,在收入之后至少48小时爆发的感染。医院感染可影响机体的任何部分,但是在重症监护内最常见的是与机械通气相关的肺炎、创伤或手术后的腹内感染、尿道感染(或者uti)及与血管内装置相关的菌血症(vincentjl,lancet,2003;eggimanp,chest,2001)。
由于一些内源性风险因素的有害聚集:患者暴露于介入治疗(人工通气、留置导尿、导管插入)、患者严重程度(以及相关的合并症)和治疗方法(多次输血、镇静),医院感染在重症监护室内的发病率明显高于在医院其它部门观测到的发病率。然而,尽管所有卫生和监测措施(外源风险)落实到位并考虑到这些外源风险因素,但是历年以来医院感染的发生率仍保持稳定或者略微降低。
医院感染易于导致播散性感染或者脓毒性综合征,其可使简单的脓毒症进展为重度脓毒症或者甚至进展为脓毒性休克。
这三种临床综合征(脓毒症、重度脓毒症和脓毒性休克)在1992年由专家小组定义为严重程度逐步增加(r.c.boneetal.,1992):
-脓毒症是与感染相关的全身性炎症反应,
-重度脓毒症是伴随至少一个器官功能障碍的脓毒症,
-脓毒性休克是重度脓毒症联合持续性低血压,且可被限定为:
ο存在经鉴定的感染部位,
ο普遍的炎症反应,表现为至少三个如下病征:a)体温高于38℃或者低于36℃,b)心率高于90次/分钟,c)呼吸频率高于20次/分钟,d)白细胞数高于12,000/mm3或者低于4000/mm3,
ο尽管经过足够充盈和血管加压处理仍持续低血压。
在那些一收入并在不存在播散性感染的任何症状时就鉴别最可能处于播散性感染风险的那些患者使得可尽快地实施策略以限制其发生这种感染的风险。例如,可给予预防性抗生素治疗(puisieuxfetal.,1993;jensenjuetal.,2011)或者预防性治疗(k.asehnouneetal.,2014)或者靶向免疫治疗(chahinaetal.,2015;aliymetal.,2014),或者更简单地可限制病原体的进入点(即尽快地撤下导管等)。这些措施可更好地治疗患者,使得:
·在重症监护和医院的住院时间长度缩短,这样可降低相关的费用(lambertmlscetal.,2011);
·减少脓毒性并发症;及
·降低死亡率。
因此迫切需要找到多年来尚未符合要求的能在收入重症监护及尚无播散性感染的临床症状的患者中进行预测的正确工具,所述患者最可能处于发生播散性感染的风险中,并因此可在其一收入时就根据其发生这种类型感染的风险对其进行分层。
令人惊奇地,本申请人证实通过分析源自收入重症监护的患者的生物样品中凝溶胶蛋白的剂量可进行这种预测。事实上,本申请人示出处于发生这种播散性感染高风险中的患者具有显著降低的凝溶胶蛋白水平。因此,本发明表现出在对抗播散性感染发生的领域中向前迈出了重要一步,播散性感染是导致收入重症监护的情况下处于风险中的患者死亡率的主要原因之一,所述患者当其收入时尚未呈现播散性感染的症状。
因此,本发明第一主题是预测收入重症监护的尚无播散性感染的临床症状的患者发生这种感染的风险的方法,所述方法包括如下步骤或由如下步骤组成:
-在收入重症监护当天和之后48小时之间确定来自所述患者生物样品中的凝溶胶蛋白的第一剂量g1,所述第一剂量源自t1时间获取的第一样品,
-在第一次取样后2-3天确定来自所述患者生物样品中的凝溶胶蛋白的第二剂量g2,所述第二剂量源自t2时间获取的第二样品,
-计算凝溶胶蛋白的剂量g2与凝溶胶蛋白的剂量g1之间的差异,给出δ值,
-将在前一步骤中获得的δ值与在收入重症监护的两群患者中预先确定的阈值s进行比较,所述两群患者中的一群未发生播散性感染,另一群已经发生这种感染,
·δ值低于所述阈值s意味着收入重症监护的患者是处于发生播散性感染高风险的患者,及
·δ值高于所述阈值s意味着收入重症监护的患者不是处于发生播散性感染高风险的患者。
本申请人因此出人意料地示出可使用凝溶胶蛋白作为标志物,在收入重症监护的患者中预测发生播散性感染的风险。
根据本发明,收入重症监护的患者是具有或者可能具有一些急性、直接危及生命的内脏功能失常的患者,需要使用补充方法。这些患者是例如多发性创伤患者,指的是重度烧伤患者、患有胰腺炎或者其它急性呼吸综合征的患者。这些患者因此特别易于医院感染,可进展为播散性感染。
根据本发明,播散性感染是一种非局限性感染,广泛分布于机体内,由如细菌、真菌、病毒或者寄生物等病原体导致。这种感染也称作脓毒性综合征。
预测发生播散性感染的风险意味着在收入重症监护时鉴别尚无播散性感染症状的患者,即没有这种播散性感染的任何临床表现的患者,该患者在收入重症监护之后几天内、在已经收入之后平均5天将发生这种感染。换句话说,预测发生播散性感染的风险意味着在收入重症监护时尚无播散性感染症状的患者中确定这种风险。最可能发生播散性感染风险的患者被称作高风险患者,对这种患者应尽快地实施限制发生这种感染风险的策略。对于这些高风险患者,使用凝溶胶蛋白可预测播散性感染的发生。换句话说,高风险患者是发生播散性感染的可能性为至少75%的患者。
在本发明的情况中,感染是早期感染,即将在患者收入重症监护之后5天内发生。
本发明中用于预测发生播散性感染风险的标志物是凝溶胶蛋白。这是分子量在82-84kda之间的蛋白质(swissprotno.p06396),是胞质蛋白,包含在高浓度钙离子存在的条件下能结合肌动蛋白单体或者肌动蛋白纤丝的6个结构域(g1-g6)。这种结合可由ph、磷酸肌醇、溶血磷脂酸和高钙浓度调节。肌动蛋白单体结合位点存在于g1结构域中,也存在于g4-6区段中,而结合肌动蛋白纤丝的高亲和性位点在g2-3区段中。凝溶胶蛋白随后在组织损伤处发挥修复作用。该蛋白质有4种已知同种型,其中主要的是同种型1(swissprotno.p06396-1),其是分泌血浆形式的蛋白质。胞质同种型2(swissprotno.p06396-2)与同种型1的不同之处是缺失前51个氨基酸。胞质同种型3和4(swissprotno.p06396-3和p06396-4)与同种型1的不同之处是前48个氨基酸序列的修饰。
在本发明的情况中,凝溶胶蛋白的所有同种型均可用作标志物以预测收入重症监护的患者发生播散性感染的风险。根据一个实施方案,分析的同种型是同种型1。
已知凝溶胶蛋白参与许多病理,特别是参与不同类型的癌症、某些炎症和感染性情况、心肺疾病、阿尔茨海默病或者衰老。
在科学文献中已经将这种蛋白质描述为是一种标志物:
-用于诊断脓毒性综合征,即鉴别已经患有脓毒性综合征及具有感染的临床症状的患者(leeetal.,2008),将严重程度和死亡率预测联系起来(xianhuietal.,2014),
-或者用于在脓毒性患者中的脓毒性综合征进展的预后,即估计已经认定为具有播散性感染的患者中这种负面的进展(wangetal.,2008),
-或者用于预测脓毒性患者的死亡率,即估计已经认定为具有播散性感染的患者的死亡率风险(wangetal.,2008)。
然而,尚无关于凝溶胶蛋白预测处于易受感染风险中的患者如收入重症监护的尚无播散性感染临床表现的患者发生播散性感染风险的描述。
预测在收入重症监护的患者中发生播散性感染的风险是通过确定所述患者的生物样品中凝溶胶蛋白的剂量而实施的。
通常,术语“样品”是指用于分析目的的取自一或多个实体的一部分或一定量,更具体而言是小部分或者少量。这种样品可任选经历预处理,例如包括混合和稀释步骤。
在本发明的方法的情况中,样品是源自希望确定发生播散性感染风险的患者的生物样品。具体来说,这种生物样品选自易含有凝溶胶蛋白的那些样品。
根据本发明的生物样品可是不同性质的。具体来说,这种样品是生物流体,例如选自血液、全血(如通过静脉途径收集,即含有白细胞和红细胞、血小板和血浆)、血清、血浆、支气管肺泡灌洗液、脑脊液和尿液。优选地,源自患者的生物样品是全血、血浆、血清或者任何衍生物样品。
“凝溶胶蛋白剂量”是指所述生物样品中凝溶胶蛋白的量。有时其不是作为所述方法的最终结果给出的剂量,而是通过将该剂量除以测量的样品体积计算的凝溶胶蛋白的浓度。对于本发明的目的,凝溶胶蛋白的剂量或者浓度均称作“剂量”
生物样品中凝溶胶蛋白的剂量可根据本领域技术人员熟知的用于确定生物样品中分析物的量或者剂量的技术确定。例如,可提及的技术是免疫测定如elisa(酶联免疫吸附测定)、elfa(酶联荧光测定)和ria(放射性免疫测定)及质谱分析测定,其组成了本发明的实施方案。
免疫测定是本领域技术人员熟知的方法,广泛用于生物样品分析领域。这种方法可检测样品中的分析物,特别是蛋白质(抗原/抗体)、肽和半抗原形式,如类固醇或者维生素,涉及待检测的分析物(在本发明中是凝溶胶蛋白)和该分析物的一或多个结合配偶体之间的免疫学反应。这些免疫测定方法基于测量,使得可以量化在生物样品分析期间发出的信号。检测的信号的量通常与测量的分析物的量或者剂量成比例(例如在夹心测定期间)或者与测量的分析物的量或者剂量成反比(例如竞争性测定)。当然,例如在“免疫测定”中的术语“免疫”在本申请中不被认为是严格地指代结合配偶体是免疫学配偶体,如抗体。事实上,在结合配偶体(也称作配体)不是免疫学配偶体而是例如希望检测的分析物的受体时,本领域技术人员也广泛使用该术语。因此,已知elisa测定(酶联免疫吸附测定)使用非免疫学结合配偶体,更通常称作“配体结合测定”,即便首字母缩写的elisa中也包括术语“免疫”。为了清楚性的目的,本申请人在整个申请中对于使用结合配偶体的任何测定均使用术语“免疫”,即使当其不是免疫学配偶体时。
作为凝溶胶蛋白的结合配偶体,可提及的是抗体、抗体部分、nanofitin、适体(ochsneru.a.etal.,2014)或者已知与研究的凝溶胶蛋白相互作用的任何其它分子,如脂多糖(buckir.etal.,2005)。
结合配偶体抗体是例如多克隆抗体或者单克隆抗体,本领域技术人员熟知这些抗体的产生。这种抗体可商购,例如以下多克隆抗体:抗凝溶胶蛋白血浆山羊多克隆抗体(anti-gelsolinplasmagoatpolyclonalantibody)、abcam、抗凝溶胶蛋白多克隆抗体(anti-gelsolinpolyclonalantibody)sheep1、thermopierceanbop0000269032,以及以下单克隆抗体:单克隆抗凝溶胶蛋白1(monoclonalanti-gelsolin1),bosterbiologicaltechnologyanbop0000215379。
可提及的抗体片段例如是fab、fab'、f(ab')2片段,及scfv(单链可变片段)和dsfv(双链可变片段)链。这些功能性片段可特别通过遗传工程获得。
包含确定凝溶胶蛋白剂量的免疫测定是本领域技术人员熟知的定量测定,优选采用凝溶胶蛋白的两个结合配偶体。这两个配偶体之一可以与标记偶联形成缀合物或者示踪物。另一结合配偶体可以捕获在固体支持物上。后者可以称作捕获配偶体,前者称作检测配偶体。
如上所示,在免疫测定期间所测量的发出的信号与生物样品中的凝溶胶蛋白的量或者剂量成比例。
为了使获得的信号与生物样品中的剂量或者浓度相关联,可以适当地使用从标准范围预先建立的数学模型。这个标准范围预先以已知方式获得。简而言之,获得标准范围包括测量通过增加的已知量或浓度的凝溶胶蛋白产生的信号,绘制给出信号与剂量或浓度之间函数关系的曲线,找到尽可能接近地代表这种关系的数学模型。所述数学模型用于通过外推确定检测的生物样品中包含的凝溶胶蛋白的未知剂量或者浓度。
用于形成缀合物的标记特别是指含有与结合配偶体的基团反应的基团的任何分子,其不用化学修饰而直接包含该基团或者在经化学修饰之后包含该基团,该分子能直接或者间接产生可检测信号。这些直接检测标记的非限制性列表由以下组成:
·酶,其通过例如比色法、荧光、发光产生可检测信号,例如辣根过氧化物酶、碱性磷酸酶、β-半乳糖苷酶、葡萄糖-6-磷酸脱氢酶,
·发色团,如荧光、发光或者生色化合物,
·放射性分子,如32p、35s或者125i,
·荧光分子,如alexa或者藻蓝蛋白,及
·电化学发光盐,如基于吖啶或者钌的有机金属衍生物。
也可以使用间接检测系统,例如能与抗配体反应的配体。随后所述配体相当于标记与结合配偶体形成缀合物。
配体/抗配体对为本领域技术人员熟知,例如如下对:生物素/链霉抗生物素蛋白、半抗原/抗体、抗原/抗体、肽/抗体、糖/凝集素、多核苷酸/与该多核苷酸互补的序列。
接着,抗配体可以通过上述直接检测标记直接检测,或者可通过另一配体/抗配体对检测到自身等。
在某些条件下,这些间接检测系统可导致信号的放大。信号放大技术为本领域技术人员熟知,可参考本申请人之一先前的专利申请fr2781802或wo95/08000。
根据使用的标记的类型,本领域技术人员加入通过任何类型合适的测量装置可以检测的能够可视化标记或者信号发射的试剂,所述测量装置是例如分光光度计、分光荧光计、光密度计或者高清相机。
免疫测定还可包括本领域技术人员已知的其它步骤,如洗涤步骤和保温步骤。
免疫测定可以是一步或者两步测定,这些为本领域技术人员所熟知。简而言之,一步免疫测定包括将待检测样品同时与两种结合配偶体接触,而两步免疫测定包括一方面将待检测样品与第一结合配偶体接触,然后将由此形成的分析物-第一结合配偶体复合物与第二结合配偶体接触。
质谱分析可以代替之前研发的技术,特别是如elisa测定,质谱分析是本领域技术人员熟知的方法。这种方法在质谱仪中进行。这是越来越多地用于生物样品中不同类型分子的分析和检测中的有利工具。通常,使用质谱仪根据其分子量可以检测任何类型可以电离的分子。根据待检测的分子、蛋白质或者代谢源的性质,一些质谱分析技术可能更合适。然而,不管用于检测的质谱分析方法如何,后者包括将靶分子电离为称作分子离子的步骤以及根据其质量分离获得的分子离子的步骤。质谱分析仪测量电离的分子的质量与电荷的比率(m/z),其与待分析的靶分子相关。
因此,所有的质谱仪均包括:
i)电离源,用于电离存在于待分析样品中的标志物,即赋予这些标志物正电荷或者负电荷;
ii)质量分析仪,用于根据其质量比电荷的比率(m/z)分离电离的标志物或者分子离子;
iii)检测器,用于测量直接通过分子离子或者通过从分子离子产生的离子而产生的信号,如下文详述。
为进行质谱分析所需的电离步骤可通过本领域技术人员熟知的任何方法进行。电离源使得可以将待测定的分子置于气态和电离状态。可使用处于正离子模式的电离源以研究正离子,或者使用处于负离子模式的电离源以研究负离子。现存在若干类型的电离源并根据所期望的结果和所分析的分子而使用。特别提及的是:
-电子电离(ei)、化学电离(ci)和解吸化学电离(dci),
-快速原子轰击(fab)、亚稳态原子轰击(mab)或者离子轰击(sims、lsims),
-电感耦合等离子体(icp),
-大气压化学电离(apci)和大气压光化电离(appi),
-电喷射(esi),
-基质辅助激光解吸/电离(maldi)、表面增强激光解吸/电离(seldi)或者在硅上的解吸/电离(dios),及
-通过与亚稳态种类相互作用的电离/解吸(dart)。
在其中根据其质量/电荷比率(m/z)进行分离电离的标志物步骤的质量分析仪是本领域技术人员已知的任何质量分析仪。可提及的是四极(q)类型、3d(it)或者线性(lit)离子阱类型的低分辨率分析仪,以及高分辨率分析仪,可以测量分析物的精确质量及特别使用与扇形电场(secteurélectrique)耦合的扇形磁场(secteurmagnétique),飞行时间(tof)。
根据其m/z比率可以进行一次分子离子的分离(单一质谱分析或者ms),或者可以进行几次连续的ms分离。当进行两次连续ms分离时,该分析称作ms/ms或者ms2。当进行三次连续ms分离时,该分析称作ms/ms/ms或者ms3,及更通常地当进行n次连续ms分离时,该分析称作msn。
使用两次连续的单一质谱分析分离的srm(选择反应监测)模式特别是使用ms2分离。
ms/ms模式中这种srm检测包括关于ms模式的两个额外的步骤,即分子离子(称作前体离子)的片段化以提供碎片离子(或者子离子),及根据其质量分离碎片离子。然后是碎片离子的m/z比率,其与被分析的靶分子相关。srm模式的原理是特别选择前体离子,使其片段化,然后特别选择其碎片离子之一。对于这种应用,通常使用“三重四级杆”类型或者“具有离子阱的三重四级杆”混合的装置。
在ms2模式中使用的“三重四级杆”或者“具有离子阱的三重四级杆”装置(q1q2q3)的情况中,鉴于分析或者检测靶蛋白质,第一四级杆(q1)使得可以根据质量比电荷(m/z)比率过滤分子离子,对应于待检测的蛋白质的和在先前消化步骤期间获得的特征性蛋白特征性肽(peptidesprotéotypiques),如下文详细描述。仅具有寻求的蛋白特征性肽的质量/电荷比率(所述比率称作(m/z)1)的肽传送到第二四级杆(q2)并作为随后进行片段化的前体离子。q2分析仪使得可将质量/电荷比率(m/z)1的肽片段化为第一代碎片离子。所述片段化通常可以在q2中通过将前体肽与惰性气体如氮气或者氩气碰撞而获得。将第一代碎片离子传送至第三四级杆(q3)中,其根据特定的质量比电荷比率(所述比率称作(m/z)2)过滤第一代碎片离子。仅将具有寻求的蛋白特征性肽的片段特征的质量/电荷比率(m/z)2的第一代碎片离子传送至检测仪中进行检测或者甚至量化。
这种操作模式具有双重选择性,一方面涉及前体离子的选择,及另一方面涉及第一代碎片离子的选择。srm模式中的质谱分析因此有利于量化。
在本发明中的情况中,“三重四级杆”或者“四级杆离子阱”类型的质谱分析仪可以联用选自亲和分析和高效液相分析(hplc)的色谱分析。优选地,质谱分析仪与高效液相色谱分析系统(hplc)联用。
如上所述,在通过质谱分析检测之前,待分析的样品优选进行预处理以从样品中存在的蛋白质中产生肽,例如通过用蛋白水解酶(蛋白酶)或者通过化学试剂的作用消化。事实上,蛋白质的裂解可以通过物理化学处理、生物学处理或者组合这两种处理方式进行。然而优选通过酶消化而不是物理化学处理处理蛋白质,因为这进一步保护蛋白质的结构及易于控制。
“酶消化”是指一或多种酶在适当反应条件下的单一或者组合作用。进行蛋白水解的酶称作蛋白酶,其在特定位置切割蛋白质。在本发明中,样品优选通过蛋白酶的作用消化,例如胰蛋白酶,其裂解精氨酸(r)和赖氨酸(k)残基的羧基基团的肽键。
在因此获得的肽中,待测定的蛋白质的特征肽被称作蛋白特征性肽。这些是随后通过质谱分析被监测和量化的肽。通过质谱分析技术经由其蛋白特征性肽量化确定蛋白质已经在复杂流体中验证(fortint.etal.,2009)。
根据其在基质中的特异性(利用在网上可免费获得的peptideatlas软件)及其灵敏性(在质谱分析仪中更好应答)选择感兴趣的蛋白特征性肽。
根据样品的复杂性,消化步骤之后可以是对感兴趣的样品中存在的肽进行分级分离的步骤,以降低其复杂性。分级分离是指以常规方式纯化存在的肽数目。这种分级分离可以通过本领域技术人员已知的技术进行,例如固相萃取(spe)、“offgel”分级分离(michelpe.etal.,2003)或者固定ph梯度等电聚焦技术(essaderasetal.,2005)。
使用质谱分析的一个优势是其可特别用于量化分子,在这种情况中是蛋白质标志物如凝溶胶蛋白。为此,使用检测的电流强度,其与靶分子的量成比例。由此测量的电流强度可用作量化措施以能够确定存在的靶分子的量。这是由于在检测仪中测量的由选择的子离子诱导的电流强度与亲离子的量成比例,其自身与蛋白特征性肽的量成比例,其自身与待测定的感兴趣的分子的量成比例。因此测量的由子离子诱导的电流的量与待测定的分子的量直接成比例。与至少一种子离子相关的至少一种定量测量的选择以及这种定量测量与样品中存在的分子的量的相关性使得可以获得定量测定。
对于免疫测定,然而需要校准。这样可以使测量的对应于由检测的离子诱导的电流强度的峰面积与待测定的靶分子的量相关。为此,在本发明范围内可以应用在质谱分析中常规使用的校准。srm测定使用外部标准或者优选使用内部标准常规校准,如t.fortinetal.,2009所述。在靶分子是蛋白特征性肽的情况中,这样可以分析感兴趣的蛋白质,定量测量与靶蛋白特征性肽及由此的感兴趣的蛋白质的量之间的相关性通过相对于已知测定量的标准信号校准测量信号而获得。可通过例如通过连续注射不同浓度的标准蛋白特征性肽(外部校准)、或者优选通过使用重肽(heavypeptide)作为内部标准物根据aqua(绝对量化)方法的内部校准获得的校准曲线进行校准。“重肽”是指合成的肽,其氨基酸序列与所选择的靶蛋白特征性肽(分子离子)相同,但是一些碳12原子(12c)被置换为碳13(13c)和/或氮14原子(14n)被置换为15(15n)。事实上,这些重肽与靶天然肽(除了较高质量之外)具有相同的理化性质且在相同色谱保留时间洗脱。这些肽组成内部标准(is)。在进行质谱分析测定之前,例如在感兴趣的样品中蛋白质消化之前进行,将其以固定量加入每个样品中。因此,合成的肽经历与靶蛋白质相同的处理步骤,且在肽分级分离期间与待测定的天然靶肽共纯化。将其同时注射进质谱分析仪中进行测定。待测定的天然肽(分析物)的峰面积与重肽(内部标准)的峰面积的对比使得可以进行靶天然肽的蛋白质的相对量化,从而反过来确定待测定的蛋白质的相对量。
生物样品中凝溶胶蛋白的剂量可以在两个不同时间t1和t2确定至少两次。在t1和t2取的生物样品是相同性质的样品。优选地,在t1和t2取的生物样品是血液样品如全血、血浆、血清或者任何血液衍生物。
第一次确定凝溶胶蛋白的剂量在t1时间在收入重症监护当天与之后48小时之间获取的生物样品中进行,所述剂量称作g1。根据一个实施方案,第一次确定凝溶胶蛋白剂量(g1)在收入之后的前48小时内进行。根据另一个实施方案,第一次确定凝溶胶蛋白剂量(g1)在收入重症监护当天进行。
第二次确定凝溶胶蛋白的剂量在t2时间在第一次取样后2-3天获取的生物样品中进行,即在收入当天之后3-5天获取样品,所述剂量称作g2。根据一个实施方案,第二次确定凝溶胶蛋白的剂量(g2)在收入之后72-120小时之间进行。
根据本发明,用于确定第一凝溶胶蛋白剂量g1和第二凝溶胶蛋白剂量g2的方法是相同的并如前所述。
在确定第二剂量g2之后,根据本发明预测发生播散性感染风险的方法包括计算凝溶胶蛋白剂量g2与凝溶胶蛋白剂量g1之间的差异的步骤,给出δ值。
δ值可以通过本领域技术人员已知的任何计算方式计算,以证实g2与g1之间的差异。
根据一个具体实施方案,δ值根据下式(i)计算:
g2-g1(i)
在这种情况中,δ值与确定的g2或g1剂量是相同数量级。
根据另一具体实施方案,δ值对应于相对的改变率,根据下式(ii)计算:
在这种情况中,δ值是百分比。
根据另一具体实施方案,δ值对应于每单位时间的剂量差异,根据下式(iii)计算:
在这种情况中,δ值具有剂量单位每单位时间作为其数量级。
预测收入重症监护的患者发生播散性感染的风险的方法包括比较得自前一步骤的δ值与之前从收入重症监护的两群患者确定的参考值s的步骤,其中一群患者未发生播散性感染,另一群患者发生这种感染。
这个s值总是负值,因为本申请人出人意料地示出发生播散性感染的高风险患者在t2与t1之间凝溶胶蛋白的剂量显著降低。
根据本发明确定参考值s基于患者的显著取样,即基于样品的最小数目以获得统计学相关结果,由此代表所研究的群体。
参考值s的这种确定方法为本领域技术人员熟知。其特别包括实施与本发明方法中使用的相同的测定方法,包括来自所研究的两个群体的生物样品,以及包括确定检测值(剂量),使得可以区分这两个群体。
本领域已知可区分这两个群体的检验值(剂量)s的确定方法,并使用受试者操作特征曲线(roc)曲线计算。这个曲线对于不同设定的阈值,通过将假阳性分数(即如下文定义的特异性)绘制在x轴上及将真阳性分数(即如下文定义的灵敏性)绘制在y轴上获得的曲线图。当判定阈(seuildedécision)在观测的检验值范围内变化时,其代表所有的灵敏性/特异性对。量化一检测的诊断效力的总的方式是通过roc曲线下面积表示其性能。按照惯例,该面积总是≥0.5。roc曲线下面积的数值在0.5(两个亚组之间剂量值的分布无差异;roc曲线对应于平分线)至1(两个亚组的剂量值完全分离;roc曲线经过点(0,1))之间变化。roc曲线下的面积是roc曲线相对于点(0,1)的位置的定量表达(hanley,j.a.andmcneil,b.j,1982;zweig,m.h.andcampbellg.,1993)。
灵敏性被认为表示在所有阳性中真阳性百分比。其表示所述测试检测真阳性生物样品的能力,所述样品相当于病理。在“概率性”语言中,其相当于已知样品是阳性时观测阳性结果的概率。
特异性被认为表示在所有阴性中真阴性的百分比。其表示所述测试不将真阴性的那些样品诊断为阳性的能力,所述样品相当于健康个体。在“概率性”语言中,其相当于已知样品是阴性时观测阴性结果的概率。
为了获得参考值s,必须满足如下条件:
-来自两群患者的样品优选源自收入重症监护的具有相同特征或大多
数共同特征的患者,特别是相同性别和/或相似或相同年龄和/或相同种
族来源的那些,和期望确定发生播散性感染风险的那些对象或者患者;
-用于获得参考值s的样品必须是与取自期望预测发生感染风险的患
者的样品具有相同性质;
-患者在取生物样品时不具有播散性感染的症状,且其进展为播散性
或非播散性感染被后验记录在案。
本发明的方法使得可对于生物样品源自于其中的患者发生播散性感染的风险水平(高或无)下结论,δ值低于所述阈值s意味着收入重症监护的患者是处于发生播散性感染的高风险的患者,δ值高于所述阈值s意味着收入重症监护的患者不是处于发生播散性感染的高风险的患者。
高风险患者如上所定义。
根据本发明方法和对患者分层的结果,如果患者被认为是处于发生播散性感染的高风险的患者,则临床医生可以选定如下一或多种行为:施用预防性抗生素治疗或者其它靶向免疫治疗,或者更简单地可限制病原体的进入点(即尽快撤下导管等)。
本发明借助于以非限制性说明的方式给出的如下实施例及参考图1-10将得以更好地理解,其中:
-图1的图表示凝溶胶蛋白的三个合成的蛋白特征性肽在增强的质谱分析(ems)模式中的ms光谱,以选择分子离子(母离子),x轴是以dalton表示的m/z比率,y轴是以每秒计数(cps)表示的强度,其上显示使用的三个蛋白特征性肽。
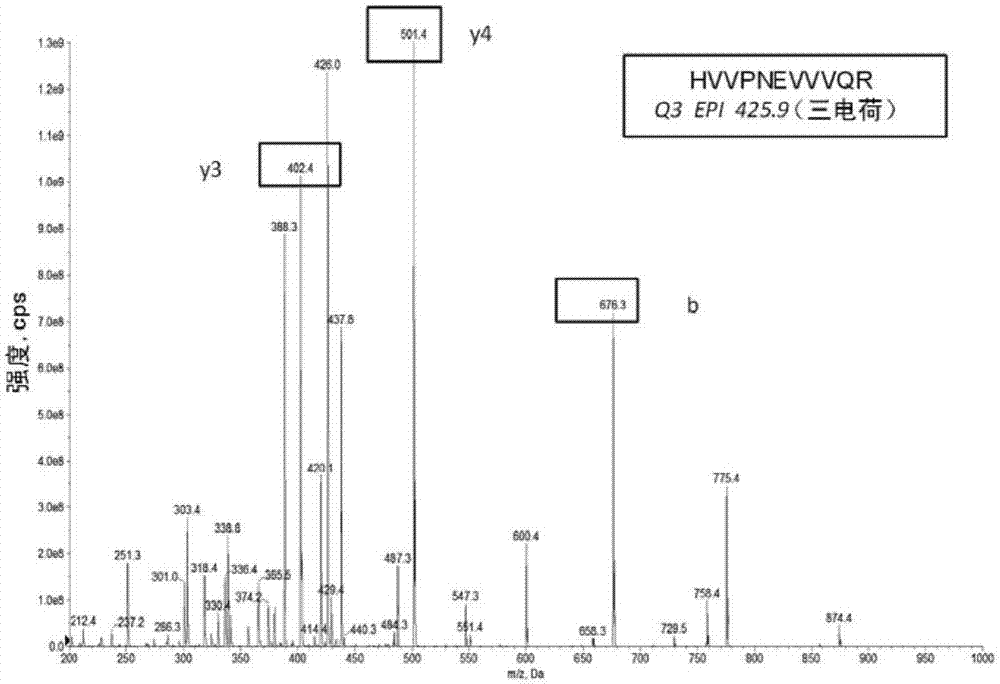
-图2的图表示在增强的子离子(epi)模式中的ms光谱,以选择得自针对肽hvvpnevvvqr选择的亲离子的碎片离子,x轴是以dalton表示的m/z比率,y轴是以每秒计数(cps)表示的强度;
-图3的图表示在增强的子离子(epi)模式中的ms光谱,以选择得自针对肽agalnsndafvlk选择的亲离子的碎片离子,x轴是以dalton表示的m/z比率,y轴是以每秒计数(cps)表示的强度;
-图4的图表示以增强的子离子(epi)模式中的ms光谱,以选择得自针对肽qtqvsvlpeggetplfk选择的亲离子的碎片离子,x轴是以dalton表示的m/z比率,y轴是以每秒计数(cps)表示的强度;
-图5的示意图给出根据收入重症监护的49名患者群,在y轴上表示单位剂量的g2-g1差异,患者是临床随访表示其随后发生播散性感染的患者(di)和临床随访表示其随后不发生这种感染的患者(ndi);
-图6是g2-g1差异的roc(受试者操作特征)曲线,使得可以从图5的结果中选择阈值,达到最小灵敏性为75%;
-图7的示意图给出根据收入重症监护的49名患者群的状态,在y轴上表示变化程度
-图8是的变化程度
-图9的示意图给出根据收入重症监护的49名患者群的状态,在y轴上表示在t2与t1之间根据如下等式
-图10是剂量每单位时间差异的roc(受试者操作特征)曲线,根据如下等式
实施例
实施例1:获得和制备血液样品
这个回顾性观察研究是在lyon的edouard-herriot医院中从2009年至2012年在收入重症监护的重度多创伤患者中进行的。包含的研究标准如下:
-患者年龄为18岁或更大
-iss(损伤严重度评分)高于或者等于25
-在重症监护室内的住院时间长度估计为至少3天
-处于机械通气下
排除的临床标准是吸入性肺炎、创伤期间肠穿孔、免疫抑制治疗,及在前48小时期间死亡。
在这项研究中包含49名重度多创伤患者。所有这些患者均符合如下标准:
-在创伤后前48小时内(t1)取第一血液样品;
-在第一次取样后2-3天(创伤后96-120小时-t2)取第二血液样品;
-相关患者发生初次感染的日期在第二次取样日期之后。
在这些患者中,18名患者在收入重症监护之后平均第5天发生播散性感染(脓毒性综合征)。
根据供应方推荐,研究中包含的每个患者的两个血液样品置于edta管中。然后将该管通过旋转轻轻搅拌15分钟,之后在2750g在15℃离心15分钟。轻取上清,然后在-80℃冷冻直至进行凝溶胶蛋白测定。
实施例2:通过lc-ms技术检测凝溶胶蛋白
srm分析方法的连续步骤是:
1)酶消化
2)spe(固相萃取)分级分离所述肽
3)与ms联用的液相色谱法(lc)。
然而,在进行该方法之前,如下鉴别各种亲离子/碎片离子对,或者srm跃迁:
从得自uniprot(swissprotno.p06396-1)的分泌的凝溶胶蛋白的同种型1的完整序列(seqidno:1),使用skyline软件(brendanmacleanetal.,2010)产生用于测定凝溶胶蛋白标志物的序列为seqidno.2-4的3个选择的蛋白特征性肽的理论srm跃迁列表。该软件可以对蛋白质从其肽序列进行虚拟的胰蛋白酶消化以产生理论肽列表。从该肽列表,预测质量范围从400至1000da的理论胰蛋白酶肽的所有双电荷或者三电荷亲离子及y或b类型的所有可能的碎片离子的srm跃迁。
seqidno.1:凝溶胶蛋白的同种型1
maphrpapallcalslalcalslpvraatasrgasqagapqgrvpearpnsmvvehpeflkagkepglqiwrvekfdlvpvptnlygdfftgdayvilktvqlrngnlqydlhywlgnecsqdesgaaaiftvqlddylngravqhrevqgfesatflgyfksglkykkggvasgfkhvvpnevvvqrlfqvkgrrvvratevpvswesfnngdcfildlgnnihqwcgsnsnryerlkatqvskgirdnersgrarvhvseegtepeamlqvlgppalpagtedtakedaanrklaklykvsngagtmsvslvadenpfaqgalksedcfildhgkdgkifvwkgkqanteerkaalktasdfitkmdypkqtqvsvlpeggetplfkqffknwrdpdqtdglglsylsshianvervpfdaatlhtstamaaqhgmdddgtgqkqiwriegsnkvpvdpatygqfyggdsyiilynyrhggrqgqiiynwqgaqstqdevaasailtaqldeelggtpvqsrvvqgkepahlmslfggkpmiiykggtsreggqtapastrlfqvransagatravevlpkagalnsndafvlktpsaaylwvgtgaseaektgaqellrvlraqpvqvaegsepdgfwealggkaayrtsprlkdkkmdahpprlfacsnkigrfvieevpgelmqedlatddvmlldtwdqvfvwvgkdsqeeektealtsakryietdpanrdrrtpitvvkqgfeppsfvgwflgwdddywsvdpldramalaa
从序列seqidno.1针对凝溶胶蛋白选择的蛋白特征性肽是hvvpnevvvqr(seqidno:2)、agalnsndafvlk(seqidno:3)和qtqvsvlpeggetplfk(seqidno:4)。
然后化学合成所选择的3个蛋白特征性肽并直接注入质谱分析仪中以选择最强的跃迁及针对每一跃迁优化质谱仪的参数:
-碰撞能(ce),
-孔电压(tensiond’orifice)(dp,去簇电压)
-增强的势能(ep),及
-在碰撞室出口的电压(cxp,碰撞室出口势能)。
用于选择亲离子的ems(增强质谱分析)模式中的质谱在图1中示出,那些在epi(增强子离子)模式中选择选自亲离子hvvpnevvvqr、agalnsndafvlk和qtqvsvlpeggetplfk的碎片离子的质谱分别在图2-4中示出。
这个选择的结果概括在表1中。
表1
1)酶消化
将在实施例1中获得的血浆样品(体积100μl,超负载20μl合成重肽)在用碳酸氢铵(ph8,5mm)缓冲并含有15mm二硫苏糖醇的6m尿素溶液中在60℃变性并还原40分钟,然后用35mm碘乙酰胺在室温避光烷化40分钟。然后将样品用50mm碳酸氢铵缓冲液(ph8)稀释8倍,之后在37℃用200μg胰蛋白酶(sigma)消化4小时。进行第二次还原-烷化循环,之后在37℃进行第二次胰蛋白酶消化步骤过夜。
2)spe分级分离
将消化的样品用超声波超声处理15分钟并在15000g离心30分钟。然后将其加样于60mg混合的(疏水性和离子交换)oasismcx(混合阳离子交换)和oasismax(混合阴离子交换)柱(waters)中。将加样于mcx柱的样品预先用由水/2%甲酸组成的ph3溶液酸化。加样于max柱的样品预先用由水/10%氢氧化铵组成的ph12溶液碱化。所述柱预先用甲醇平衡。
分级分离程序在下表2中描述。
表2
将待测定的肽用1ml甲醇/碳酸氢铵缓冲液(v/v)混合物洗脱。根据感兴趣的蛋白特征性肽的等电点选择碳酸氢盐缓冲液的ph。使用
3)液相色谱(lc)和质谱分析(ms):
根据如下特征将100μl等份注入与ms系统联用的lc中。
在具有与以srm模式(q1q2q3)运行的质谱分析仪absciex5500qtrap(三重四级杆-离子阱杂合ms)联用的二元泵和注射器的nexeralc型(shimadzu)的高压色谱系统(hplc)中进行lc-ms分析。在2.1×150mm的3.6μm的c18反相柱(aerispeptide,phenomenex)中进行lc分离,洗脱速度为250μl/分钟。洗脱液a=于水中的0.1%甲酸,洗脱液b=于甲醇中的0.1%甲酸。在5%溶剂b等度梯度进行2分钟,然后在5%b-60%b线性梯度进行37分钟,随后在5%溶剂b等度梯度进行2分钟。在正esi(电喷雾电离)模式中进行ms分析,应用于喷雾针的电压为5500v以在源中电离。雾化气(空气)和气帘气(氮气)的流速分别为40和50psi。turbovtm离子源设置为550℃,辅助氮气流为40psi。
使用analyst1.5.2软件进行仪器控制和数据采集。
使用每个跃迁的特定参数(dp、ep、ce、cxp和保留时间)针对每个级分构建schedule-srm采集方法。在超负载合成肽的血清和血浆样品检测期间观测到的每个肽的保留时间附近的4分钟窗口及1.15秒的靶扫描时间均用于所有的数据采集。
将srm原始数据使用multiquant2.1软件(absciex)和signalfinder积分算法再加工。所述软件使得可以提取对应于每个肽的色谱。
为了校准,合成具有与所选择的靶肽(子离子)相同序列的合成重肽,用赖氨酸或者精氨酸(13c和15n)标记:对于赖氨酸+8dalton,对于精氨酸+10dalton,以可以用作内部标准。样品超负载这些标记的重肽。
对于对应于seqidno:2、seqidno:3、seqidno:4所示肽的所有选择的跃迁(表2),确定天然跃迁的色谱峰的面积除以重跃迁的面积的比率以获得每个样品每个跃迁的相对剂量。然后将相同样品的每个跃迁的相对剂量编译在一起以获得代表研究的生物样品中蛋白质浓度的单一剂量。“编译”是指平均组合在一起的相同蛋白质的一些独立但相关的剂量以获得单一剂量每蛋白质。这种编译通过取比率的中间值进行。
实施例3:数据的统计学分析
将患者分为2组:
·其临床状态示出未发生播散性感染的患者(ndi):n=31
·其临床状态示出其发生播散性感染的患者(di):n=18
通过确定优势率(or)和相关的置信区间(95%ci),进行单变量和多变量逻辑回归分析以鉴别与感染风险相关的变量。
针对δ值g2-g1
结果
收入重症监护的患者中血浆凝溶胶蛋白的剂量与播散性感染发生之间的关联
凝溶胶蛋白变量及其它临床变量与患者的状态(在这种情况中是“发生播散性感染”)之间的关联通过逻辑回归检验。通过优势率(or)计算估计关联强度,优势率是发生播散性感染的可能性与不发生播散性感染的可能性的比率。
研究的临床变量是:性别、创伤严重度评分(iss:损伤严重度评分)、简化的严重度指数(ssiii)、神经创伤、肺创伤、输注红细胞、输注冷冻新鲜血浆。
根据上述方法通过确定t2与t1之间凝溶胶蛋白g2-g1水平差异测量凝溶胶蛋白剂量变量。
对于每个定性变量:神经创伤、肺创伤、输注红细胞和输注冷冻新鲜血浆,优势率如下解释:
-or=1:无关联
-or<1:发生播散性感染的风险对于不具有这种特征的患者更常见
-or>1:发生播散性感染的风险对于具有这种特征的患者更常见。
对于每个性别变量,优势率如下解释:
-or=1:无关联
-or<1:发生播散性感染的风险对于女性更常见
-or>1:发生播散性感染的风险对于男性更常见。
对于每个定量变量:凝溶胶蛋白水平g2-g1的差异、iss和ssiii,优势率如下解释:
-or=1:无关联
-or<1:从第一至第三个四分位数的增加与发生播散性感染的风险降低相关
-or>1:从第一至第三个四分位数的增加与发生播散性感染的风险增加相关。
在收入重症监护的患者中监测所有这些变量,所述患者在收入之后几天内发生播散性感染。
对于这些协变量的每一个变量进行单变量逻辑回归分析。然后,在单变量分析中p值小于0.1的变量保留在多变量分析中,可以确定调节的优势率。
结果在下表3中示出。
表3
表3中的结果示出在2或3天的时间间隔(t2-t1)测量的血浆凝溶胶蛋白剂量的差异与患者的状态(“发生播散性感染”)及因此与发生播散性感染的风险显著相关联。事实上,单变量逻辑回归分析确定在t2与t1之间凝溶胶蛋白差异的优势率是0.11,在多变量分析中是0.1,p值分别为0.0013和0.002,如表3所示。此外,其它变量在多变量分析中不显著。
凝溶胶蛋白g2-g1的差异为-0.288的患者发生播散性感染的风险比凝溶胶蛋白g2-g1的差异为-0.002的患者高10倍。
通过测量血浆凝溶胶蛋白剂量预测播散性感染的发生
除了血浆凝溶胶蛋白的剂量与发生播散性感染的风险之间的关联,我们的研究显示在间隔2或3天连续取的两个样品中测量的血浆凝溶胶蛋白的剂量的差异可以预测在随后的几天内(<d8)播散性感染的发生。
δ值=g2-g1
49名患者的g2-g1差异结果在图5中给出,根据收入重症监护的49名患者的情况在y轴表示以剂量单位表示的g2-g1差异,所述患者是临床随访显示其随后发生播散性感染的患者(di)和临床随访显示其随后不发生这种感染的患者(ndi)。
图5中的结果显示在随后的几天内将发生播散性感染的患者在两次取样之间凝溶胶蛋白的剂量总是降低(g2-g1<0),且这种降低在该群体中与不发生播散性感染的患者相比显著更明显。
使用图6中给出的roc曲线进行阈值确定,使得可以基于使用等式g2-g1获得的δ值在发生播散性感染的高风险患者与非高风险患者之间进行预测。因此,取设定阈值为-0.144839402777984(负值),可以预测δ值低于这个阈值的患者在随后的几天内发生感染,灵敏性为83.3%,特异性为71%。
该结果也通过根据如下等式(ii)计算变化比率以相对变异性表示:
结果在图7中给出,显示将发生播散性感染的患者的中间值;这个中间值是-22%(这些患者中在t1与t2之间凝溶胶蛋白的剂量降低22%(中间值),相比不发生感染的患者中是5.05%)。
当使用roc曲线根据等式
从这个数据集中可以推断这种方法不是最合适的,但是其不限制这种方法用于较大患者群。
另一方面,为了考虑两次取样之间的时间间隔,从一个患者至另一患者不总是均一的,我们通过计算凝溶胶蛋白水平在两次取样之间随着时间间隔的差异比率研究了每天凝溶胶蛋白水平的变化。这个计算包括根据如下等式(iii)计算凝溶胶蛋白在两个取样之间随着时间间隔的差异比率:
结果在图9中示出。根据该计算,我们显示在不发生播散性感染的患者中每天凝溶胶蛋白剂量的差异中间值为-0.02,而在发生播散性感染的患者中这个值为-0.12。
当使用roc曲线根据等式
从这个数据集可推断这种方法不是最合适的,但是其不限制这种方法用于较大患者群。
根据49名患者的数据,第一种方法(δ值=g2-g1)具有最佳折中结果。但是,计算δ值的其它方法也适于较大群的其它数据。
令人惊奇地,我们的研究显示在两次连续取样中测量血浆凝溶胶蛋白水平使得可以在没有表示播散性感染的临床迹象时预测收入重症监护的患者中播散性感染的发生,所述取样第一次是在收入之后前48小时之内进行,第二次是在然后的2-3天后进行。
参考文献
-aliymetal.,2014,low-doserecombinantproperdinprovidessubstantialprotectionagainststreptococcuspneumoniaandneisseriameningitidisinfection,procnatlacadsciu.s.a,111(14):5301-6
-asehnouneketal.,2014,hydrocortisoneandfludrocortisoneforpreventionofhospital-acquiredpneumoniainpatientswithseveretraumaticbraininjury(corti-tc):adouble-blind,multicenterphase3,randomizedplacebo-controlledtrial,lancetrespirmed,2:706-16
-boner.c.etal.,1992,theaccp/sccmconsensusconferencecommittee.americancollegeofchestphysicians/societyofcriticalcaremedicine,chest,101(6):1644-1655
-brendanmacleanetal.,2010,bioinformatics,vol.26no.7:966–968
-buckir.etal.,2005,inactivationofendotoxinbyhumanplasmagelsolin,biochemistry,44(28)
-chahinaetal.,2015,thenovelimmunotherapeuticoligodeoxynucleotideimt504protectsneutropenicanimalsfromfatalpseudomonasaeruginosabacteriemiaandsepsis,antimicrobagentschemother,59(2):1225-9
-eggimanpetal.,2001,infectioncontrolintheicu,chest,120(6):2059-93
-essaderas,etal.,2005,acomparisonofimmobilizedphgradientisoelectricfocusingandstrong-cation-exchangechromatographyasafirstdimensioninshotgun,proteomics,5,24–34
-fortint.etal.,2009,clinicalquantitationofprostate-specificantigenbiomarkerinthelownanogram/milliliterrangebyconventionalboreliquidchromatography-tandemmassspectrometry(multiplereactionmonitoring)couplingandcorrelationwithelisatests.mol.cellproteomics,8(5):1006-1015.
-hanley,j.a.andmcneil,b.j.,1982,themeaninganduseoftheareaunderareceiveroperatingcharacteristic(roc)curve,radiology,143:29-36.
-jensenjuetal.,2011,procalcitonin-guidedinterventionsagainstinfectionstoincreaseearlyappropriateantibioticsandimprovesurvivalintheintensivecareunit:arandomizedtrial,critcaremed,39(9):2048-58
-lambertmlscetal.,2011,clinicaloutcomesofhealth-care-associatedinfectionsandantimicrobialresistanceinpatientsadmittedtoeuropeanintensive-careunits:acohortstudy,lancetinfectdis,11:30-8
-leeps,etal.,2008,plasmagelsolindepletionandcirculatingactininsepsis:apilotstudy.plosone.2008;3(11):e3712.
-ligh,etal.,2012,multifunctionalrolesofgelsolininhealthanddiseases.medresrev.2012sep;32(5):999-1025
-michelpe,etal.,2003,proteinfractionationinamulticompartmentdeviceusingoff-gel,isoelectricfocusing,electrophoresis,24,3–11
-oschsneru.a.etal.,2014,systematicselectionofmodifiedaptamerpairsfordiagnosticsandwichassays,biotechniques,56:125-133
-puisieuxf,etal.,1993,prophylacticantibiotherapyusingcefapirininthesurgeryofduodenalulcer:arandomizedclinicaltrial,annfranesthreanim,12(3):289-92
-vincentjl,2003,nosocomialinfectionsinadultintensive-careunits,lancet,361(9374):2068-77
-wangh,etal.,2008,timecourseofplasmagelsolinconcentrationsduringseveresepsisincriticallyillsurgicalpatients.critcare.2008;12(4):r106.
-xianhuil.etal.,2014,theassociationbetweenplasmagelsolinlevelandprognosisofburnpatients.burns,vol.40,no.8,pages1552-1555
-zweig,m.h.andcampbellg.,1993,receiver-operatingcharacteristic(roc)plots:afundamentalevaluationtoolinclinicalmedicine,clin.chem.,39/4:561-577
序列表
<110>生物梅里埃公司
里昂公立收容所
南特大学医疗中心
<120>收入重症监护病房的患者发生播散性感染的风险预测
<130>gelsoline
<150>fr1554227
<151>2015-05-12
<160>4
<170>patentinversion3.5
<210>1
<211>782
<212>prt
<213>homosapiens
<400>1
metalaprohisargproalaproalaleuleucysalaleuserleu
151015
alaleucysalaleuserleuprovalargalaalathralaserarg
202530
glyalaserglnalaglyalaproglnglyargvalproglualaarg
354045
proasnsermetvalvalgluhisproglupheleulysalaglylys
505560
gluproglyleuglniletrpargvalglulyspheaspleuvalpro
65707580
valprothrasnleutyrglyaspphephethrglyaspalatyrval
859095
ileleulysthrvalglnleuargasnglyasnleuglntyraspleu
100105110
histyrtrpleuglyasnglucysserglnaspgluserglyalaala
115120125
alailephethrvalglnleuaspasptyrleuasnglyargalaval
130135140
glnhisarggluvalglnglyphegluseralathrpheleuglytyr
145150155160
phelysserglyleulystyrlyslysglyglyvalalaserglyphe
165170175
lyshisvalvalproasngluvalvalvalglnargleupheglnval
180185190
lysglyargargvalvalargalathrgluvalprovalsertrpglu
195200205
serpheasnasnglyaspcyspheileleuaspleuglyasnasnile
210215220
hisglntrpcysglyserasnserasnargtyrgluargleulysala
225230235240
thrglnvalserlysglyileargaspasngluargserglyargala
245250255
argvalhisvalserglugluglythrgluproglualametleugln
260265270
valleuglyprolysproalaleuproalaglythrgluaspthrala
275280285
lysgluaspalaalaasnarglysleualalysleutyrlysvalser
290295300
asnglyalaglythrmetservalserleuvalalaaspgluasnpro
305310315320
phealaglnglyalaleulyssergluaspcyspheileleuasphis
325330335
glylysaspglylysilephevaltrplysglylysglnalaasnthr
340345350
glugluarglysalaalaleulysthralaserasppheilethrlys
355360365
metasptyrprolysglnthrglnvalservalleuprogluglygly
370375380
gluthrproleuphelysglnphephelysasntrpargaspproasp
385390395400
glnthraspglyleuglyleusertyrleuserserhisilealaasn
405410415
valgluargvalpropheaspalaalathrleuhisthrserthrala
420425430
metalaalaglnhisglymetaspaspaspglythrglyglnlysgln
435440445
iletrpargilegluglyserasnlysvalprovalaspproalathr
450455460
tyrglyglnphetyrglyglyaspsertyrileileleutyrasntyr
465470475480
arghisglyglyargglnglyglnileiletyrasntrpglnglyala
485490495
glnserthrglnaspgluvalalaalaseralaileleuthralagln
500505510
leuaspglugluleuglyglythrprovalglnserargvalvalgln
515520525
glylysgluproalahisleumetserleupheglyglylyspromet
530535540
ileiletyrlysglyglythrserarggluglyglyglnthralapro
545550555560
alaserthrargleupheglnvalargalaasnseralaglyalathr
565570575
argalavalgluvalleuprolysalaglyalaleuasnserasnasp
580585590
alaphevalleulysthrproseralaalatyrleutrpvalglythr
595600605
glyalaserglualaglulysthrglyalaglngluleuleuargval
610615620
leuargalaglnprovalglnvalalagluglysergluproaspgly
625630635640
phetrpglualaleuglyglylysalaalatyrargthrserproarg
645650655
leulysasplyslysmetaspalahisproproargleuphealacys
660665670
serasnlysileglyargphevalileglugluvalproglygluleu
675680685
metglngluaspleualathraspaspvalmetleuleuaspthrtrp
690695700
aspglnvalphevaltrpvalglylysaspserglnglugluglulys
705710715720
thrglualaleuthrseralalysargtyrilegluthraspproala
725730735
asnargaspargargthrproilethrvalvallysglnglypheglu
740745750
proproserphevalglytrppheleuglytrpaspaspasptyrtrp
755760765
servalaspproleuaspargalametalagluleualaala
770775780
<210>2
<211>11
<212>prt
<213>artificialsequence
<220>
<223>peptide
<400>2
hisvalvalproasngluvalvalvalglnarg
1510
<210>3
<211>13
<212>prt
<213>artificialsequence
<220>
<223>peptide
<400>3
alaglyalaleuasnserasnaspalaphevalleulys
1510
<210>4
<211>17
<212>prt
<213>artificialsequence
<220>
<223>peptide
<400>4
glnthrglnvalservalleuprogluglyglygluthrproleuphe
151015
lys
- 还没有人留言评论。精彩留言会获得点赞!