一种Cu3P@Ti-MOF-NH2复合材料、电化学传感器及其制备方法和应用与流程
本发明属于电化学传感器领域,具体涉及一种cu3p@ti-mof-nh2复合材料、电化学传感器及其制备方法和应用。
背景技术:
水合肼作为重要的化学原料,被广泛应用于农业、精细化工、燃料电池、爆炸物、摄影化学品、防腐剂、武器、乳化剂和药理学等领域。由于具有致突变性,致癌性和神经毒性,肼被美国环境保护局(epa)归类为致癌物。目前,已经有许多分析方法来测定水中的水合肼,包括滴定法,色谱法,分光光度法,化学发光流动注射分析,电位法和电分析方法。采用常规方法测定水合肼时,存在仪器成本高,不易携带,耗时,适用性差的缺点。
电化学方法检测污染物时具有反应快速、操作简单、现场分析、灵敏性和经济性好等特点,非常适用于水合肼检测。然而,常规电极由于高氧化过电位、电子传输慢等限制,不适于用于电化学测定水合肼。铂、金、银等具有较高的催化活性,但价格十分昂贵,在实际应用中受到极大限制。研究低成本、催化活性高的电催化剂,从而能够便捷、灵敏的应用于水合肼的电化学氧化,具有非常重要的意义。
金属有机骨架材料(mof)是由金属阳离子与有机配体相互连接而成的一类新型纳米多孔结晶材料,由于其化学性能可调性和结构多样性,mof在气体存储和分离、分子检测、生物医药、电子、光电器件、催化等领域都有极大的应用。目前,基于mof构建的水合肼检测电催化剂鲜见于报道。
技术实现要素:
本发明的目的在于提供一种cu3p@ti-mof-nh2复合材料,从而解决现有水合肼检测电极材料存在的电催化活性低、选择性差的问题。本发明还提供了一种电化学传感器、制备方法及应用。
为实现上述目的,本发明所采用的技术方案是:
一种cu3p@ti-mof-nh2复合材料,由包括以下步骤的方法制备而成:将2-氨基对苯二甲酸、钛酸四丁酯、cu3p在溶剂中进行溶剂热反应,即得。
本发明提供的cu3p@ti-mof-nh2复合材料,cu3p和ti-mof-nh2之间存在强的协同作用,可以促进催化剂界面上的有效电荷分离和转移,从而促进对水合肼的电催化氧化作用。电化学试验表明,cu3p@ti-mof-nh2复合材料对水合肼的分解显示出突出的电催化活性,以该复合材料制作的电极对水合肼的检测具有较高的灵敏性和选择性,在电化学分析领域的应用前景巨大。
2-氨基对苯二甲酸、钛酸四丁酯、cu3p的用量比为(0.2-0.3)g:(0.2-0.3)ml:(5-100)mg。上述主要原料的实际用量可根据上述比例进行扩大或缩减。优选的,2-氨基对苯二甲酸、钛酸四丁酯、cu3p的用量比为(0.2-0.3)g:(0.2-0.3)ml:50mg。以上原料控制在上述比例范围,即得获得良好的电催化活性效果。
所述溶剂为甲醇和n,n-二甲基甲酰胺。
将cu3p分散于pvp的甲醇溶液中,离心得到固相物,将固相物分散于n,n-二甲基甲酰胺中,即得cu3p分散液,将cu3p分散液作为原料与甲醇、2-氨基对苯二甲酸、钛酸四丁酯进行所述溶剂热反应。cu3p、pvp、甲醇的用量比为(5-100)mg:(0.3-0.4)g:(9-10)ml。优选的,pvp的mw=20000-40000。cu3p以上述分散液形式和混合溶液进行反应,可促进反应均匀、高效进行,有助于进一步优化cu3p@ti-mof-nh2复合材料中cu3p的分散效果,提高复合材料的电催化性能。
cu3p可按照现有技术进行制备。优选的,所述cu3p采用包括以下步骤的方法制备:将cu(oh)2和nah2po2混合后,在保护气氛下于280~320℃反应1~3h,即得。优选的,cu(oh)2、nah2po2的质量比为:0.05:(0.2-0.3)。cu(oh)2可通过cu(no3)2·3h2o溶液和过量的naoh溶液的反应制备得到。采用上述步骤可方便得到cu3p纳米晶体,与ti-mof-nh2的制备过程适应性好,所得cu3p@ti-mof-nh2复合材料的稳定性和可重复性好。
所述溶剂热反应是在140-160℃下反应24~48h。
采用上述优选方案制备的cu3p@ti-mof-nh2复合材料,具有简单经济、电催化活性高的特点,可方便、高效用于水合肼的痕量检测中,应用前景良好。
本发明的电化学传感器所采用的技术方案是:
一种电化学传感器,包括基体电极和附着在基体电极上的cu3p@ti-mof-nh2复合材料。
所述基体电极为玻碳电极。其他直径大小的玻碳电极,cu3p@ti-mof-nh2复合材料的用量可依据上述比例计算确定。
本发明的电化学传感器,对水合肼的检测显示出高催化活性和选择性,可方便用于水合肼的便捷、高效检测。
上述电化学传感器的制备方法,包括将基体电极活化后,使用含有cu3p@ti-mof-nh2复合材料的分散液对活化后的电极进行修饰,干燥,即得。
基体电极可选择玻碳电极。玻碳电极的活化可采用现有技术,优选的,玻碳电极的活化包括以下步骤:使用氧化铝粉末的糊状液对玻碳电极进行抛光处理后,依次用硝酸溶液、乙醇溶液、水进行洗涤,干燥即得。
含有cu3p@ti-mof-nh2复合材料的分散液包括水和cu3p@ti-mof-nh2复合材料组成,控制cu3p@ti-mof-nh2复合材料的浓度为1-2mg·ml-1。
本发明提供的电化学传感器的制备方法,工艺简单、制造成本低,大大降低了水合肼的痕量检测成本,提高了水合肼痕量检测的有效性和适用性。
本发明同时提供上述电化学传感器在水合肼检测中的应用。
在上述电化学传感器的基础上,可按照现有电化学方法实现对水中水合肼的痕量检测。
利用本发明的电化学传感器对水合肼进行检测,在5μm到7.5mm的线性范围内,对水合肼的最低检测限为0.079μm(s/n=3)。此外,当添加一些常见的干扰物时,该电化学传感器对水合肼的检测具有较高选择性、稳定性和实际可行性,反映出良好的检测能力。
附图说明
图1为(i)ti-mof-nh2、(ii)cu3p、(iii)cu3p@ti-mof-nh2-5、(iv)cu3p@ti-mof-nh2-20、(v)cu3p@ti-mof-nh2-50和(vi)cu3p@ti-mof-nh2-100的x-射线衍射光谱图;
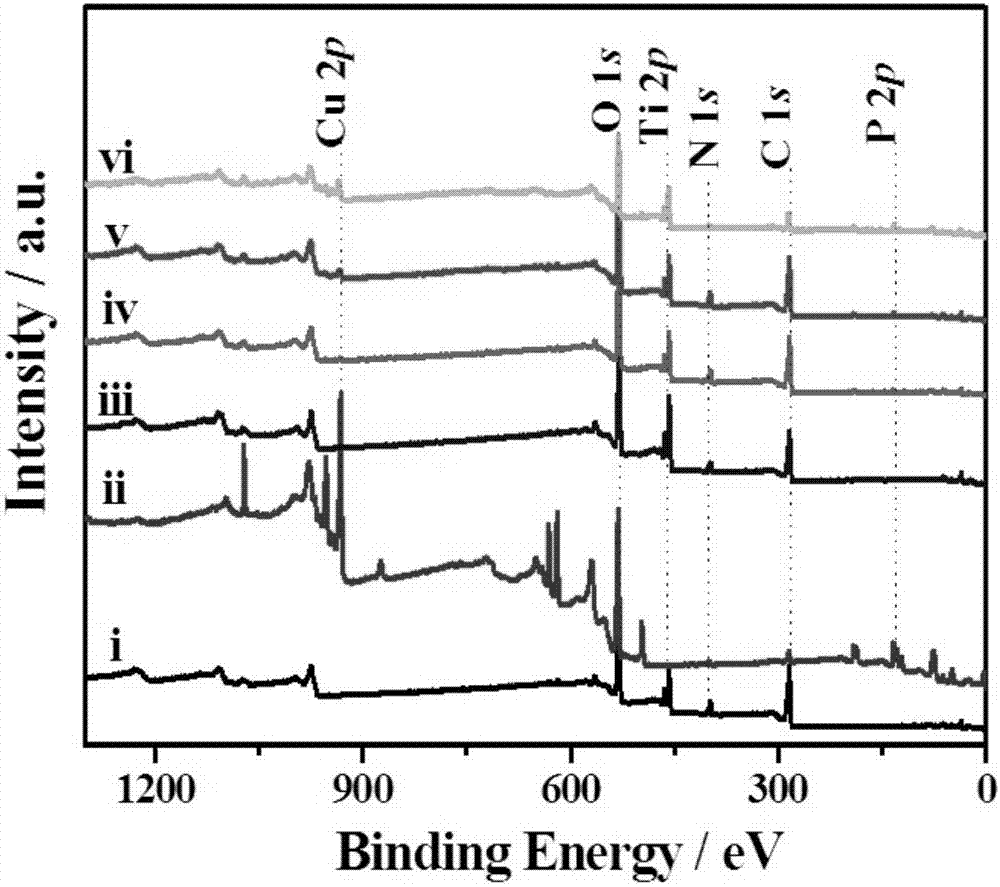
图2为(i)ti-mof-nh2、(ii)cu3p、(iii)cu3p@ti-mof-nh2-5、(iv)cu3p@ti-mof-nh2-20、(v)cu3p@ti-mof-nh2-50和(vi)cu3p@ti-mof-nh2-100的x-射线光电子能谱图;
图3为(a)cu3p@ti-mof-nh2-5,(b)cu3p@ti-mof-nh2-20,(c)cu3p@ti-mof-nh2-50和(d)cu3p@ti-mof-nh2-100复合材料的c1s、cu2p和ti2p的高分辨xps谱图;
图4中,(a)、(b)、(c)和(d)分别是cu3p@ti-mof-nh2-5、cu3p@ti-mof-nh2-10、cu3p@ti-mof-nh2-50和cu3p@ti-mof-nh2-100的fesem图像,(e-g)分别是cu3p@ti-mof-nh2-50复合材料的ti、cu和c的元素分析;
图5中,(a,b)、(c,d)、(e,f)和(g,h)分别是cu3p@ti-mof-nh2-5、cu3p@ti-mof-nh2-20、cu3p@ti-mof-nh2-50和cu3p@ti-mof-nh2-100复合材料的tem和hr-tem图像,(b)、(d)、(f)和(h)中的插图分别是对应的选区电子衍射图像;
图6为cu3p@ti-mof-nh2-50复合材料的氮气吸附-解吸等温线;
图7为cu3p@ti-mof-nh2-50复合材料的孔径分布;
图8为gce、ti-mof-nh2/gce、cu3p/gce、cu3p@ti-mof-nh2-5/gce、cu3p@ti-mof-nh2-20/gce、cu3p@ti-mof-nh2-50/gce和cu3p@ti-mof-nh2-100/gce的奈奎斯特图;
图9为gce、ti-mof-nh2/gce、cu3p/gce、cu3p@ti-mof-nh2-5/gce、cu3p@ti-mof-nh2-20/gce、cu3p@ti-mof-nh2-50/gce和cu3p@ti-mof-nh2-100/gce的循环伏安图;
图10为ti-mof-nh2/gce、cu3p/gce和cu3p@ti-mof-nh2/gce在0.2m的naoh溶液中在扫速为50mv·s-1的条件下测量循环伏安图;
图11是在2.0mm水合肼存在下,以50mv·s-1的扫描速率,在n2饱和的0.2mnaoh溶液中测量的循环伏安图;
图12是在不同扫描速率(从低到高:25、50、75、100、150、200、250和300mv·s-1)的含有2.0mm水合肼的n2饱和的0.2mnaoh溶液中的实施例1的电极的循环伏安图,插图为水合肼电催化氧化电流曲线图;
图13是在不同浓度的水合肼(从低到高:0、1、2、3、4、5、6、7和9mm)存在下,扫描速率为50mv·s-1时,在n2饱和的0.2mnaoh溶液中实施例1的电极的循环伏安图;
图14为实施例1的电极在不同浓度的水合肼中的电流响应图;
图15为实施例1的电极的电流响应与水合肼浓度的校准曲线;
图16为电压为+0.45v(vs.ag/agcl)、浓度为0.2m的naoh溶液中连续加入0.1mm的水合肼(i),50mm的nacl(ⅱ)、na2co3(ⅲ)、柠檬酸钠(ⅳ)、kno3(ⅴ)、na2so4(ⅵ)的电流响应图;
图17为实施例1的电极在n2饱和的0.2mnaoh溶液中对5mm水合肼的电流响应,运行时间为1800s,插图为7天后的cu3p@ti-mof-nh2-50/gce的循环伏安的响应值。
具体实施方式
下面结合具体对本发明的实施方式作进一步说明。以下实施例中,钛酸四丁酯(tbot),2-氨基对苯二甲酸(h2bdc-nh2;c8h7no4),n'-n-二甲基甲酰胺(dmf;(ch3)2ncho),甲醇(ch3oh),硝酸铜三水合物(cu(no3)2·3h2o),次亚磷酸钠(nah2po2),pvp(mw=40000)和水合肼(hha;n2h4·h2o)购自阿拉丁化学有限公司(中国上海)。naoh和氢氧化铵(nh4oh)购自国药化学试剂有限公司。其他试剂为分析纯,无需进一步纯化处理。超纯水从milli-q水净化系统获得。
实施例1
本实施例的cu3p@ti-mof-nh2复合材料,采用以下步骤进行制备:
1)cu3p的制备:在室温和磁力搅拌下,将过量的0.25mol/l的naoh溶液加入50ml浓度为0.05mol/l的cu(no3)2·3h2o溶液中反应0.5h,将沉淀物离心,用水洗涤数次,真空干燥,得到cu(oh)2;
将0.05gcu(oh)2和0.25gnah2po2混合并研磨均匀,得到混合物,将混合物在n2气氛下以2℃·min-1的升温速率加热至300℃,保温2小时,自然冷却,将所得黑色固体用超纯水和乙醇洗涤数次,在真空烘箱中干燥备用;
2)将50mgcu3p加入pvp的甲醇溶液(0.35gpvp和10ml甲醇混合而成)中,在室温下搅拌12h后,离心并用甲醇洗涤三次,将所得固相物分散于3.6mldmf中,得到cu3p分散液;
将0.4ml甲醇、0.22g2-氨基对苯二甲酸和0.24ml钛酸四丁酯加入到烧杯中,磁力搅拌5min后形成混合溶液;
将cu3p分散液和混合溶液混合后,转移到聚四氟乙烯衬里的反应釜中,在150℃下反应48h,离心收集固体物质,并用甲醇洗涤三次,干燥,即得cu3p@ti-mof-nh2-50。
本实施例的电化学传感器,包括玻碳电极和附着在玻碳电极表面上的cu3p@ti-mof-nh2复合材料,玻碳电极的直径为3.0mm,cu3p@ti-mof-nh2-50的用量为0.01mg。该电化学传感器采用以下步骤制备:
1)将玻碳电极依次在粒径为0.3μm、0.05μm的氧化铝粉末的糊状液中抛光,然后用硝酸溶液(浓硝酸:蒸馏水体积比为1:1)、乙醇溶液(无水乙醇:蒸馏水体积比为1:1)、蒸馏水洗涤,得到活化电极;将cu3p@ti-mof-nh2-50分散于水中,制备浓度为1mg·ml-1的悬浮液;
2)取10μl悬浮液滴加到活化电极上,然后在氮气流中干燥,即得电化学传感器cu3p@ti-mof-nh2-50/gce。
实施例2
本实施例的cu3p@ti-mof-nh2复合材料,采用以下步骤进行制备:
1)cu3p的制备同实施例1;
2)将5mgcu3p加入pvp的甲醇溶液(0.35gpvp和10ml甲醇混合而成)中,在室温下搅拌12h后,离心并用甲醇洗涤三次,将所得固相物分散于3.6mldmf中,得到cu3p分散液;
将0.4ml甲醇、0.22g2-氨基对苯二甲酸和0.24ml钛酸四丁酯加入到烧杯中,磁力搅拌5min后形成混合溶液;
将cu3p分散液和混合溶液混合后,转移到聚四氟乙烯衬里的反应釜中,在150℃下反应48h,离心收集固体物质,并用甲醇洗涤三次,干燥,即得cu3p@ti-mof-nh2-5。
本实施例的电化学传感器,参考实施例1的方法制备得到cu3p@ti-mof-nh2-5/gce。
实施例3
本实施例的cu3p@ti-mof-nh2复合材料,采用以下步骤进行制备:
1)cu3p的制备同实施例1;
2)将20mgcu3p加入pvp的甲醇溶液(0.35gpvp和10ml甲醇混合而成)中,在室温下搅拌12h后,离心并用甲醇洗涤三次,将所得固相物分散于3.6mldmf中,得到cu3p分散液;
将0.4ml甲醇、0.22g2-氨基对苯二甲酸和0.24ml钛酸四丁酯加入到烧杯中,磁力搅拌5min后形成混合溶液;
将cu3p分散液和混合溶液混合后,转移到聚四氟乙烯衬里的反应釜中,在150℃下反应48h,离心收集固体物质,并用甲醇洗涤三次,干燥,即得cu3p@ti-mof-nh2-20。
本实施例的电化学传感器,参考实施例1的方法制备得到cu3p@ti-mof-nh2-20/gce。
实施例4
本实施例的cu3p@ti-mof-nh2复合材料,采用以下步骤进行制备:
1)cu3p的制备同实施例1;
2)将100mgcu3p加入pvp的甲醇溶液(0.35gpvp和10ml甲醇混合而成)中,在室温下搅拌12h后,离心并用甲醇洗涤三次,将所得固相物分散于3.6mldmf中,得到cu3p分散液;
将0.4ml甲醇、0.22g2-氨基对苯二甲酸和0.24ml钛酸四丁酯加入到烧杯中,磁力搅拌5min后形成混合溶液;
将cu3p分散液和混合溶液混合后,转移到聚四氟乙烯衬里的反应釜中,在150℃下反应48h,离心收集固体物质,并用甲醇洗涤三次,干燥,即得cu3p@ti-mof-nh2-100。
本实施例的电化学传感器,参考实施例1的方法制备得到cu3p@ti-mof-nh2-100/gce。
对比例1
对比例1的电化学传感器所使用的电极修饰材料为cu3p,参考实施例1的方法制备。然后将cu3p和水配制浓度为1mg·ml-1的悬浮液,参考实施例1的方法制成电化学传感器cu3p/gce。
对比例2
对比例2的电化学传感器所使用的电极修饰材料为ti-mof-nh2,制备方法为:将3.6mldmf、0.4ml甲醇、0.22g2-氨基对苯二甲酸和0.24ml钛酸四丁酯加入到烧杯中,磁力搅拌5min后形成混合溶液;将混合溶液混合后,转移到聚四氟乙烯衬里的反应釜中,在150℃下反应48h,离心收集固体物质,并用甲醇洗涤三次,干燥,即得ti-mof-nh2。参考实施例1的方法制备电化学传感器ti-mof-nh2/gce。
试验例1
本试验例利用xrd和xps对各实施例的复合材料的晶体结构和化学结构进行分析。用cukα辐射的rigakud/max-2500x射线衍射仪上进行x射线衍射测量(xrd),测量结果如图1所示。x射线光电子能谱(xps)数据是用带有单色alkαx射线源(1486.71ev光子)的axishis165光谱仪(kratosanalytical,manchester,uk)测量,测量结果如图2所示。
由图1可知看出,曲线i的所有衍射峰与ti-mof-nh2的模拟衍射峰一致。cu3p(曲线ii)的衍射峰分别为29.0°,36.0°,39.0°,41.6°,45.1°,46.1°,47.3°,53.4°,59.0°,66.5°和73.4°,分别对应(012),(112),(202),(121),(300),(113),(122),(104),(222),(124)和(232)六方晶格的晶格衍射(jcpdsno.65-3628)。在43.3°和50.4°的两个峰值表明有金属铜(jcpdsno.04-0836)。曲线iii和iv对应的cu3p@ti-mof-nh2纳米复合材料,cu3p的衍射特征峰不是很明显,原因可能在于cu3p纳米晶体的用量较少,导致cu3p对ti-mof-nh2单晶框架形成的影响较小。当cu3p用量为50mg(曲线v)时,除了ti-mof-nh2的衍射峰外,还观察到cu3p的特征峰,表明两者复合很好。然而,当cu3p的用量增加到100mg(曲线vi)时,观察到cu3p的衍射峰,而ti-mof-nh2的衍射峰不明显,表明ti-mof-nh2的结晶被抑制。
图2中,在ti-mof-nh2中观察到ti,c,n和o元素,而在cu3p中观察到cu,p和c元素。cu3p@ti-mof-nh2复合材料中观察到cu,ti,c,n,p和o的存在。表1中,随着复合材料中cu3p用量的增加,cu原子百分比从0.27%提高到4.68%,p原子百分比从0.83%提高到7.40%。
表1各实施例和对比例的复合材料的原子百分比
为了研究cu3p@ti-mof-nh2复合材料中各元素的化学成分和电子价态,分析了高分辨xps,如图3所示。
图3中,c1s谱被分解成四个峰,即284.6ev、285.4ev、286.4ev和288.6ev,分别对应于c-c/c-h,c-n,n-c=o/c=o和coo-基团,这些基团来自于mof中含有的有机配体和溶剂残留。由于cu3p@ti-mof-nh2-5的制备中cu3p的用量很少,所以cu2p的信号不明显。随着cu3p用量的进一步增大,cu2p谱可以被分为6个部分,其中932.6ev和952.42ev的峰对应于cu2p3/2和cu2p1/2,表明存在cu(i)价态,而943.26ev和962.85ev的峰分别是它们对应的卫星峰。在934.2ev和954.3ev处的高能峰的信号是由于cu(ii)价态引起的。在458.7ev和464.5ev观察到两个明显的峰,分别对应ti2p3/2和ti2p1/2,表明ti-o团簇中钛为iv氧化态。
试验例2
本试验例观察各实施例的cu3p@ti-mof-nh2复合材料的表面形貌。使用jsm-6490lv扫描电子显微镜(sem,japan)观察各复合材料的形态,如图4所示;在jeoljem-2100高分辨透射电子显微镜下记录高分辨透射电子显微镜图像(hr-tem),如图5所示。
图4中,cu3p@ti-mof-nh2复合材料的表面比较粗糙。cu3p@ti-mof-nh2-5呈现片状,其余三个样品呈现保持八面体结构(图4a-d),cu3p@ti-mof-nh2-50的元素测定证实了纳米复合材料中ti,cu和c的存在(图4e-g)。
图5中,tem和hr-tem图像表明直径约2-5nm的cu3p纳米晶体生长并嵌入到ti-mof-nh2基质中。cu3p的(012),(300)和(113)面分别对应0.307nm,0.201nm和0.196nm的晶格间距,这与xrd的结果相对应。
试验例3
本试验例对各实施例的cu3p@ti-mof-nh2复合材料进行氮气吸附-解吸附研究。使用belsorpmax容积吸附设备,在超高真空下获得n2吸附-解吸数据,结果如图6和图7所示。
图6中,cu3p@ti-mof-nh2-50复合材料的比表面积为327.7m2g-1。图7中,cu3p@ti-mof-nh2-50显示以2-5nm为中心的窄分布,表明该复合材料的孔径是介孔材料。
试验例4
本试验例使用电化学工作站(chi760d,shanghaichenhuainstrumentsco.,china)在室温下进行循环伏安法(cv),电化学阻抗谱(eis)和计时电流分析(i-t曲线)。采用三电极系统,以各实施例和对比例制作的电极为工作电极,ag/agcl(饱和kcl)为参比电极,pt为对电极。eis的测试在5.0mmk3fe(cn)6/k4fe(cn)6(1:1)、0.1mkcl的混合溶液中进行,频率范围0.01hz至100khz,振幅为5mv。cv和i-t曲线在搅拌下以及n2下,在0.2mnaoh电解质溶液进行测量。cv的测量范围是从-0.2v至0.8v,扫描速率为50mv·s-1。水合肼的检测是通过计时电流的方法,加入不同浓度的水合肼,在0.2mnaoh溶液中测量。通过三次重复实验计算每个浓度的平均电流;校正曲线上的误差线显示与平均值的标准偏差。
图8中,所述电极在高频区和低频区表现出与电容回路相似的电化学行为。每个电极的奈奎斯特图具有半圆部分,对应于由电极表面处的氧化还原探针的动力学电化学反应产生的感应电流的过程。此外,所有样品的奈奎斯特图可以使用相同的等效电路(图8的插图)进行模拟。该模型中,rs、rct、w、cpe分别表示溶液电阻、电荷转移电阻、warburg阻抗和恒定相元素。由于半圆直径等于界面中的rct,所以可以通过拟合奈奎斯特曲线推导出所有改性电极的rct值。cu3p/gce的rct值为1604欧姆,这在所有电极中是最高的,表明电极界面的电子转移速率缓慢。ti-mof-nh2/gce的rct值为286欧姆,而实施例1-4的cu3p@ti-mof-nh2复合材料修饰电极的rct值介于cu3p/gce和ti-mof-nh2/gce的中间。cu3p@ti-mof-nh2-5/gce和cu3p@ti-mof-nh2-20/gce的rct值分别为1481欧姆和335欧姆。对于cu3p@ti-mof-nh2-50/gce,其rct值在所有实施例中最小,为319欧姆,表明该复合材料具有增强的界面处电子转移的协同效应。当cu3p的用量进一步增加到100mg时,复合材料修饰电极的rct值增加到661欧姆,表明电子传递速率开始减慢。
图9中,裸gce电极具有明确的可逆氧化还原对峰值,差值约为156mv。使用电极材料进行电极修饰后,峰值分离值增加,氧化还原峰电流略有下降。实施例1-实施例4中,cu3p@ti-mof-nh2-50/gce具有最高的电流和最小峰值分离值(225mv)。该结果表明,实施例1的电极可以更容易和快速地进行水合肼的电化学反应,电催化活性最佳。
图10是在不存在水合肼的情况下,在0.2m的naoh溶液中所有电极的cv图。其中,cu3p/gce的面积最小,而ti-mof-nh2/gce的cv曲线面积最大,说明ti-mof-nh2/gce在0.2m的naoh溶液中表现出最好的电化学活性。
图11是在水合肼存在下,在0.2m的naoh溶液中各电极的cv曲线,由图可知,各电极对水合肼氧化具有明显的阳极峰,其中,cu3p@ti-mof-nh2-50/gce在水合肼存在下响应最高,表明对水合肼具有最佳的电催化活性,也证明了实施例1的复合材料中,cu3p与ti-mof-nh2之间具有很强的协同作用。
图12是扫描速率对水合肼氧化峰电流的影响,可以看出,阳极峰值电流随着扫描速率的增加而增加,峰值电流和扫描速率平方根在25-300mv·s-1范围内存在线性关系(图12的插图)。这表明在碱性溶液中cu3p@ti-mof-nh2-50/gce的电化学行为属于扩散控制电极过程。
图13为通过cv测量水合肼浓度对阳极峰值电流的影响,可以看出,随着水合肼浓度的增加,改性电极的阳极电流显著增加,且阳极峰向正电位处发生偏移。由图10~图13可以看出,各实施例的复合材料对水合肼的氧化具有高催化活性,其中,实施例1的复合材料的电催化活性最佳。
图14为cu3p@ti-mof-nh2-50/gce在+0.45v的外加电位下在n2饱和的0.2mnaoh溶液中加入不同浓度水合肼的典型电流响应,从图15中可以看出电流响应和水合肼的浓度,线性范围是5μm至7.5mm,相关系数为0.998,相应的线性回归方程式表示为i(μa)=0.62+10.87chydrazine(mm)。根据信噪比为3计算得出检测限为0.079μm。这表明,基于cu3p@ti-mof-nh2制备的电化学传感器检测水合肼时显示出优越的传感性能。
图16中,cu3p@ti-mof-nh2-50/gce对0.1mm的水合肼具有较高的响应,而对于50mm的其它干扰物(包括nacl、na2co3、柠檬酸钠、kno3和na2so4)没有显著的电流响应,表明该复合材料修饰的电极在水合肼检测时具有较高的选择性。
图17研究了在n2饱和的0.2mnaoh溶液中,cu3p@ti-mof-nh2/gce电化学传感器的长期稳定性,由图可知,电流在250秒内达到相对稳定的值,并且在运行时间为1800s后保持在稳定值的95.7%。图17中插图表明,在4℃下保存7天后,电极保留了其原始峰电流值的99.0%,表明cu3p@ti-mof-nh2/gce传感器的稳定性很好。
试验例5
本试验例研究cu3p@ti-mof-nh2/gce在实际样品中的实用性,采用加标法,将三种不同的水源分别加入100、300和500μm水合肼,并在n2保护下的0.2mnaoh溶液中测定,外加电压为+0.45v(vs.ag/agcl),结果如表2所示。
表2实际样品中水合肼的测定(n=3)
由表2的结果可知,实际样品检测时回收率在90.3-106.2%,表明开发的传感器在样品分析中检测水合肼的实际实用性良好。
由以上试验例可以看出,各实施例制备的cu3p@ti-mof-nh2改性的gce可以电催化氧化水合肼,传感器在5μm至7.5mm的线性范围内的最低检测限为0.079μm,以及在存在一些常见的检测水合肼的干扰物的情况下具有良好的选择性同时也具有稳定性和实际可行性,表明传感器对水合肼的测定具有良好的检测能力。所有这些结果表明,ti-mof-nh2相关的纳米复合材料具有构建有效传感器以检测环境和生物领域其他分析物的潜在应用。
- 还没有人留言评论。精彩留言会获得点赞!