高通量检测色氨酸及其代谢产物的试剂盒及其应用的制作方法
本发明属于生物医药
技术领域:
,具体涉及一种高通量检测色氨酸及其代谢产物的试剂盒及其应用,被适用于快速高效地检测生物样本中色氨酸及其代谢产物的含量。
背景技术:
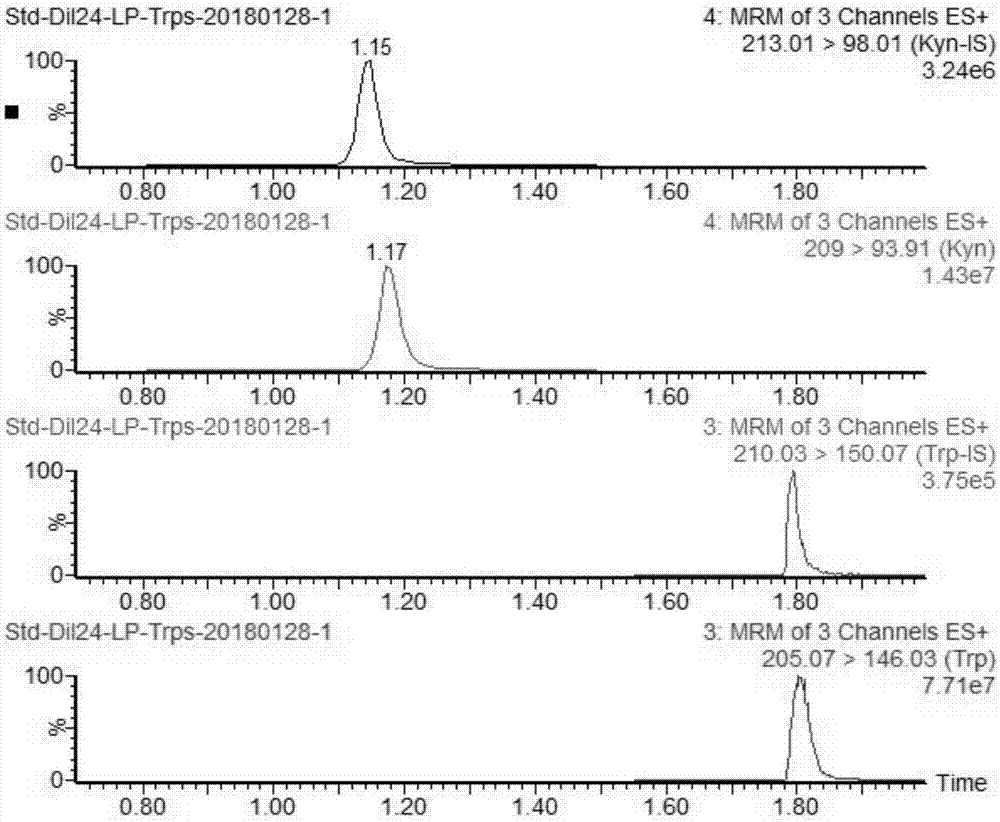
:色氨酸除用于合成各种蛋白质外,主要在肝脑、肾等组织代谢。其途径有三种,其一是大多数色氨酸经犬尿氨酸途径代谢,即色氨酸在吲哚胺-2,3-双加氧酶(indoleamine-2,3-dioxygenase,ido)的作用下生成甲酰犬尿氨酸,后者迅速在犬尿氨酸甲酰胺酶的作用下生成犬尿氨酸,犬尿氨酸在犬尿氨酸氨基转移酶的作用下进一步生成犬尿喹啉酸(kynurenicacid,kyna),体内大部分色氨酸经此途径代谢。其二是少量色氨酸经色氨酸羟化酶生成5-羟色胺酸,进一步脱羧生成5-羟色胺和5羟吲哚乙酸。其三还有极少量色氨酸经吲哚乙酸途径代谢。色氨酸是蛋白质的组成成分之一,参与调节蛋白质的合成,还能促进胃液和胰液的产生,促进人体消化过程。5-羟色胺有抗抑郁、促进睡眠、镇痛、抗高血压的功能。犬尿氨酸是色氨酸最重要的中间代谢产物之一,可被代谢为一系列具有特殊生理功能的生物活性分子。总之,色氨酸及其代谢产物对维持中枢神经系统正常生理功能有重要作用,并且血浆中5-羟吲哚乙酸含量可作为监视类癌患者的生物标志物。目前检测色氨酸、犬尿氨酸、5-羟色胺和5羟吲哚乙酸的方法主要有生物法、放射免疫法、放射酶法、荧光光度法等。早期的生物法现已不用;而放射免疫法虽有较好的灵敏度和特异性,但同位素标记对人体有害;荧光法虽使用较多,但操作麻烦,需要反复萃取,对检测物质有一定量的损失。总之,现有临床上还尚未有针对色氨酸及其代谢产物具有认可性的检测方法,因此,研究开发一套便捷高效地检测色氨酸及其代谢产物的含量方法是具有重大意义及影响力的。技术实现要素:本发明的目的在于提供了一高通量检测色氨酸及其代谢产物的试剂盒及其应用,所述色氨酸及其代谢产物高通量检测方法应用高通量液相色谱串联质谱法高效快速地检测色氨酸及其代谢产物的含量。本发明的目的在于提供了一高通量检测色氨酸及其代谢产物的试剂盒及其应用,所述制备待测样品时,利用两次离心及上清液的制备工作,提高了制备待测样品的纯度,提高其检测的精准度。本发明的目的在于提供了一高通量检测色氨酸及其代谢产物的试剂盒及其应用,所述制备待测样品时,利用其涡旋混合,提高其萃取率,并且操作简单易处理。本发明的目的在于提供一高通量检测色氨酸及其代谢产物的试剂盒及其应用,其中所述色氨酸及其代谢产物高效检测方法具有萃取处理步骤简单,成本低廉,操作简便等优势。本发明的目的在于提供一高通量检测色氨酸及其代谢产物的试剂盒及其应用,其中所述色氨酸及其代谢产物高效检测方法检测时间短,通量高,检测灵敏度高,特异性好。为达上述目的,本发明的主要技术解决手段是提供高通量法检测色氨酸及其代谢产物的试剂盒,被适用检测样本中所述色氨酸及其代谢产物,其特征在于,检测代谢产物包括:色氨酸、犬尿氨酸、5-羟色胺和5-羟吲哚乙酸;所述试剂盒包括如下试剂:①混合内标物:色氨酸-d5、犬尿氨酸-d4、5-羟色胺-d4、5-羟吲哚乙酸-d5;②标准品含:色氨酸、犬尿氨酸、5-羟色胺和5-羟吲哚乙酸;③洗脱液:洗脱液a为0.1%甲酸水溶液,洗脱液b为0.1%甲酸乙腈溶液;④稀释剂:甲醇溶液。所述标准品通过所述甲醇溶液制备成标准品母液,其中所述标准品母液中色氨酸、犬尿氨酸、5-羟色胺、5-羟吲哚乙酸的浓度分别为:3nmol/l~650nmol/l、3nmol/l~650nmol/l、0.99μmo/l~200.00μmo/l以及0.063μmo/l~12.77μmo/l。所述混合内标物通过所述甲醇溶液制备成混合内标液,其中所述混合内标液中色氨酸-d5、犬尿氨酸-d4、5-羟色胺-d4、5-羟吲哚乙酸-d5的浓度均为35~36nmol/l。所述洗脱液a的制备:取1000体积份超纯水,使用移液枪移去1体积份的水,再加入1体积份的甲酸,充分混匀超声5min后备用;洗脱液b的制备:取1000体积份的色谱乙腈,使用移液枪移去1体积份水,再加入1体积份的甲酸,使用充分混匀超声5min后备用。所述的试剂盒的应用,其特征在于,所述采用高通量液相色谱串联质谱技术检测血浆样品中色氨酸及代谢产物,先利用高通量液相色谱将色氨酸及代谢产物分离,再利用串联质谱同位素内标定量法,以标准品的浓度值为x轴,标准品与内标物的峰面积比为y轴,建立标准矫正曲线,计算上述色氨酸及代谢产物的含量。所述色氨酸及其代谢产物高通量检测方法包括以下步骤:s1:获取色氨酸代谢通路类物质定量标准矫正曲线:其中所述色氨酸代谢通路类物质定量标准矫正曲线被实施为不同浓度的色氨酸及其代谢产物与已知浓度的标记色氨酸及其代谢产物的实际比值之间的关系图;s2:待测样品的制备:取血浆样本,加入混合内标液进行涡旋混合,随后产生蛋白沉淀,静置等充分沉淀后,进行第一次离心,获得第一上清液,移取所述第一上清液利用离心浓缩冷冻系统冻干后,加入水溶液后第二次离心,获得第二上清液,取所述第二上清液作为待测样品,放置于96孔板上备用;s3:高通量液相色谱分离色氨酸及代谢产物:高通量液相色谱分离色氨酸及代谢产物利用超高效液相色谱以及相应的流动相,在分析柱上对待测样品中色氨酸及代谢产物进行色谱洗脱分离,通过控制洗脱条件,分离出色氨酸及代谢产物;s4:串联质谱检测所述色氨酸及代谢产物:利用三重四级杆质谱中的多重反应监控模式特异性地检测所述色氨酸及代谢产物,获得检测值,其中所述检测值被反应为所述色氨酸及代谢产物与标记所述色氨酸及代谢产物峰面积的比值;以及s5:获取所述氨酸及代谢产物的含量:将所述检测值代入所述色氨酸代谢通路类物质定量标准矫正曲线,计算得到所述样本中所述色氨酸及其代谢产物的含量。所述步骤s1进一步包括以下步骤:s11:色氨酸及其代谢产物标准溶液的制备:将色氨酸及其代谢产物用已知浓度的甲醇溶液稀释到若干个不同浓度备用,获得不同浓度的标准溶液;s12:第一上清液的制备:分别取若干个不同浓度的标准溶液加入等量的含有已知浓度内标液,高速离心后取得第一上清液;s13:标准检测品的制备:所述第一上清液利用离心浓缩冷冻系统冻干后,加入水溶液后再离心处理后,获得第二上清液,取所述第二上清液作为标准检测品,放置于96孔板上备用;s14:高通量液相色谱分离色氨酸及代谢产物:高通量液相色谱分离色氨酸及代谢产物利用超高效效相色谱以及相应的流动相,在分析柱上对待测样品中色氨酸及代谢产物进行色谱洗脱分离;s15:串联质谱检测色氨酸及代谢产物:利用三重四级杆质谱中的多重反应监控模式特异性地检测色氨酸及代谢产物的含量,根据信号噪音比计算得到定量检测限,根据比值以及已知标准品浓度值绘制标准曲线图。内标液中含有已知浓度混合内标物和含1.58g/l硫酸铵的甲醇-水溶液,所述水溶液选自甲酸水溶液。其中所述高通量液相色谱的分离条件控制如下:分析柱为反向c18分析柱,色谱柱柱温:25℃,进样量:10μl;其中所述离心条件控制为:离心力为18000g,离心温度为4℃,离心时间为5min,其中所述第一次离心条件与所述第二次离心条件相同。其中所述质谱检测条件如下:电喷雾针电压:2.0kv,去溶剂气流速:850l/h,去溶剂气温度:550℃,锥孔气流速:0l/h,检测为正离子模式,扫描方式为多重反应监控,每个待测物质谱参数:附图说明图1和图2是根据本发明的所述色氨酸及其代谢产物高效检测方法的色谱洗脱出峰的绝对保留时间示意图,图3到图6是所述色氨酸及其代谢产物高效检测方法的色氨酸代谢通路类物质定量标准矫正曲线示意图。具体实施方式下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员所获得的所有其他实施例,都属于本发明保护的范围。本领域技术人员应理解的是,在本发明的揭露中,术语“纵向”、“横向”、“上”、“下”、“前”、“后”、“左”、“右”、“竖直”、“水平”、“顶”、“底”“内”、“外”等指示的方位或位置关系是基于附图所示的方位或位置关系,其仅是为了便于描述本发明和简化描述,而不是指示或暗示所指的装置或元件必须具有特定的方位、以特定的方位构造和操作,因此上述术语不能理解为对本发明的限制。可以理解的是,术语“一”应理解为“至少一”或“一个或多个”,即在一个实施例中,一个元件的数量可以为一个,而在另外的实施例中,该元件的数量可以为多个,术语“一”不能理解为对数量的限制。色氨酸(trp)是需要从食物中摄取的必需氨基酸之一,并且人和动物机体自身是无法合成色氨酸的,色氨酸虽然在人和动物体内含量较少,但是也可以通过其多元的代谢途径及其代谢产物发挥着各种重要作用。如图2所示,其中色氨酸在体内主要分解代谢途径:一是沿5-羟色胺(5-ht)的代谢途径,其中5-羟吲哚乙酸(5-hiaa)则是沿5-羟色胺(5-ht)的代谢途径的终产物;二是沿犬尿氨酸(kyn)的代谢途径,换言之,其所述代谢产物包括为5-羟色胺(5-ht)、5-羟吲哚乙酸(5-hiaa)以及犬尿氨酸(kyn),因此,也就证明了这四种物质是存在共同性质的化学结构和元素。通过膳食摄入体内的色氨酸不仅能参与调节蛋白质的合成,还能在控制动物食欲、免疫调节以及改善情绪认知等方面发挥重要作用,因此测定人体色氨酸、犬尿氨酸、5-羟色胺以及5-羟吲哚乙酸浓度对于了解机体免疫状态和与之相关疾病的诊疗具有重要意义,并且色氨酸、犬尿氨酸、5-羟色胺以及5-羟吲哚乙酸都是属于色氨酸代谢通路类物质,但就目前而言,临床上针对这类物质检测方法主要有生物法、放射免疫法、放射酶法、荧光光度法等,但早期的生物法现已不用;而放射免疫法虽有较好的灵敏度和特异性,但同位素标记对人体有害;荧光法虽使用较多,但操作麻烦,需要反复萃取,对检测物质有一定量的损失。为了解决现有技术中检测此类物质的缺陷,本发明提供了一种高通量检测色氨酸及其代谢产物的试剂盒及其应用。其中针对其色氨酸及其代谢产物的共性利用同一种检测方法检测,并且应用高通量液相色谱串联质谱法快速高效地检测生物样本中色氨酸及其代谢产物的含量,其上清液制备两次步骤简单易操作,具有较高的检测灵敏度和检测特异性。本发明提供一种高通量检测色氨酸及其代谢产物的试剂盒及其应用,可直接快速地定量定性地检测色氨酸及其代谢产物,其主要原理是先以已知浓度的色氨酸及其代谢产物以及辅助试剂以一定的方法获得一色氨酸及其代谢产物定量标准矫正曲线,随后以相同方法检测检测样品得到一检测值,将所述检测值代入到所述色氨酸及其代谢产物定量标准矫正曲线内,以计算获取所述色氨酸及其代谢产物的含量。具体而言,如图1到图6所示,高通量检测色氨酸及其代谢产物的试剂盒,被适用检测样本中所述色氨酸及其代谢产物,检测代谢产物包括:色氨酸、犬尿氨酸、5-羟色胺和5-羟吲哚乙酸;所述试剂盒包括如下试剂:①混合内标物:色氨酸-d5、犬尿氨酸-d4、5-羟色胺-d4、5-羟吲哚乙酸-d5;②标准品含:色氨酸、犬尿氨酸、5-羟色胺和5-羟吲哚乙酸;③洗脱液:洗脱液a为0.1%甲酸水溶液,洗脱液b为0.1%甲酸乙腈溶液;④稀释剂:甲醇溶液;此外,试剂盒的应用,被适用检测样本中所述色氨酸及其代谢产物的含量,而所述色氨酸及其代谢产物属于色氨酸代谢通路类物质,其特征在于,所述色氨酸及其代谢产物高通量检测方法包括以下步骤:s1:获取色氨酸代谢通路类物质定量标准矫正曲线:其中所述色氨酸代谢通路类物质定量标准矫正曲线被实施为测试值和不同浓度的色氨酸及其代谢产物与已知浓度的标记色氨酸及其代谢产物的实际比值之间的关系图;s2:待测样品的制备:取0.15ml血浆样本到1.5mlep管中,加入0.45ml内标液进行蛋白沉淀,静置等充分沉淀后,进行第一次离心,获得第一上清液,移取所述第一上清液利用离心浓缩冷冻系统冻干后,加入水溶液后第二次离心,获得第二上清液,取所述第二上清液作为待测样品,放置于96孔板上备用;s3:高通量液相色谱分离色氨酸及代谢产物:高通量液相色谱分离色氨酸及代谢产物利用超高效液相色谱以及相应的流动相,在分析柱上对待测样品中色氨酸及代谢产物进行色谱洗脱分离,通过控制洗脱条件,分离出色氨酸及代谢产物;s4:串联质谱检测所述色氨酸及代谢产物:利用三重四级杆质谱中的多重反应监控模式特异性地检测所述色氨酸及代谢产物,获得检测值,其中所述检测值被反应为所述色氨酸及代谢产物与标记所述色氨酸及代谢产物的比值;以及s5:获取所述氨酸及代谢产物的含量:将所述检测值代入所述色氨酸代谢通路类物质定量标准矫正曲线,计算得到所述样本中所述色氨酸及其代谢产物的含量。重点需强调的是,所述待测样品的制备中,这里进行了两次的上清液的制备,其中所述第二上清液也就是所需的待测样品,另外,所述血浆样本放入ep管中,向其加入内标液,在本实施例里所述内标液被实施为含有已知浓度内标的含1.58g/l硫酸铵的甲醇-水溶液,所述含1.58g/l硫酸铵的甲醇-水溶液被实施为有机试剂,相信从事该技术的自然会明白,所述血浆样本加入含内标的有机试剂后进行涡旋混合,进行涡旋混合是为了提高其萃取率,涡旋混合后产生蛋白沉淀,静置一段时间使得沉淀更加的充分,然后进行第一次离心,本实施例的离心条件被实施为离心力为18000g;离心温度为4℃;离心时间为5min;其中所述第一次离心条件与所述第二次离心条件相同,第一次离心后,取得第一上清液,第一上清液被实施为有机试剂和水的混合物,还有含有待测样品,将所述第一上清液进行冷冻冻干后,加入一定量的水溶液,这里水溶液被实施为甲酸-水溶液,然后进行第二次离心,取得第二上清液,所述第二上清液也就是待测样品。值得特别注意的是,在一些实施例中,可通过各种手段直接获取色氨酸代谢通路类物质定量标准矫正曲线,在另一些实施例中,所述色氨酸代谢通路类物质定量标准矫正曲线需要使用人员自行制备。但在直接获取色氨酸代谢通路类物质定量标准矫正曲线的实施例中,值得一提的是,所述色氨酸代谢通路类物质定量标准矫正曲线的制备条件应相同于所述样本在检测时的检测条件。以下将详细解释所述色氨酸代谢通路类物质定量标准矫正曲线的制备过程,所述色氨酸代谢通路类物质定量标准矫正曲线被实施为测试值和不同浓度的色氨酸及其代谢产物之间的关系图。所述步骤s1进一步包括以下步骤:s11:色氨酸及其代谢产物标准溶液的制备:将色氨酸及其代谢产物用已知浓度的甲醇溶液稀释到若干个不同浓度备用;在本发明的具体实施例中,所述色氨酸及其代谢产物标准溶液的浓度被分别控制在3nmol/l~650nmol/l、3nmol/l~650nmol/l、0.99~200.00μmo/l和0.063~12.77μmo/l。换言之,在色氨酸及其代谢产物标准溶液的制备时,所述色氨酸标准溶液的浓度0.99-200.00μmo/l之间,所述犬尿氨酸标准溶液的浓度0.063-12.77μmo/l之间,所述5-羟色胺标准溶液的浓度3nmol/l-650nmol/l之间以及所述5-羟吲哚乙酸标准溶液的浓度控制在3nmol/l-650nmol/l之间。但熟悉该项技术的人应该明白,所述色氨酸及其代谢产物标准溶液的浓度范围仅仅作为举例,而不作为限制。一具体实施例以操作过程图的形式被详细展示。所述色氨酸及其代谢产物标准品用甲醇稀释到不同浓度,不同浓度的色氨酸及其代谢产物标准溶液被置于不同的ep反应管内,静置以备用。为了避免不必要的因素对实验产生干扰,不同反应管优选在相同反应条件下进行反应。在准备好不同浓度的所述色氨酸及其代谢产物标准溶液后,所述步骤s1进一步包括以下步骤:s12:第一上清液的制备:分别取0.15ml6个不同浓度的标准溶液到1.5mlep管中,再分别加入0.45ml的混合内标液,用旋涡混合器充分混合后,高速离心后取得第一上清液;值得注意的是,在本发明的实施例中,所述内标液被实施为混合内标物和含1.58g/l硫酸铵的甲醇-水溶液的混合溶液,所述混合内标浓度在本发明的实施例中被控制在35.7nmol/l,这里向每个不同浓度的标准溶液加入等量的含有已知浓度内标液为了计算出比例值。在本发明的一实施例中,所述离心条件控制为:离心力为18000g,离心温度为4℃,离心时间为5min。所述步骤s1进一步包括以下步骤:s13:标准检测品的制备:所述第一上清液利用离心浓缩冷冻系统冻干后,加入水溶液后再离心处理后,获得第二上清液,取所述第二上清液作为标准检测品,放置于96孔板上备用;值得一提的是,本发明的所述步骤s12和所述步骤s13适用于每一浓度的色氨酸及其代谢产物标准品溶液的后续处理。换言之,所述步骤s12中,分别以一定比例混合不同浓度的所述色氨酸及其代谢产物标准溶液和已知浓度的内标工作液,得到含有不同浓度色氨酸及其代谢产物的上清液。所述步骤s13中,加入水溶液及离心冷冻处理所述含有不同浓度色氨酸及其代谢产物的上清液,得到含有不同浓度色氨酸及其代谢产物的标准检测品。所述步骤s1进一步包括以下步骤:s14:高通量液相色谱分离色氨酸及代谢产物:高通量液相色谱分离色氨酸及代谢产物利用超高效液相色谱以及相应的流动相,在分析柱上对待测样品中色氨酸及代谢产物进行色谱洗脱分离;具体而言,在一具体实施例中,所述步骤s14中高通量液相色谱分离条件为:分析柱:反向c18分析柱;色谱柱柱温:25℃;进样量:10μl;流动相组成:a相为0.1%甲酸-水溶液,b相为0.1%甲酸-乙腈溶液。洗脱梯度如下,见表1如下:序号时间(min)流速(ml/min)a%b%曲线值1initial0.3595.05.0initial21.000.3595.05.0131.500.4075.025.0641.800.5040.060.0652.000.505.095.0662.800.505.095.0173.300.5095.05.01表1所述步骤s1进一步包括以下步骤:s15:串联质谱检测色氨酸及代谢产物:利用三重四级杆质谱中的多重反应监控模式特异性地检测色氨酸及代谢产物的含量,根据信号噪音比计算得到定量检测限,根据比值以及已知标准品和内标浓度值绘制标准曲线图。值得注意是获得标准曲线后,可进一步获取定量校正方程,所述定量校正方程反映测试值和不同浓度的色氨酸及其代谢产物与已知浓度的标记色氨酸及其代谢产物的实际比值之间的函数关系。在本发明的一具体实施例中,在所述步骤s15当中,所述质谱检测条件为:电喷雾针电压:2.0kv,去溶剂气流速:850l/h,去溶剂气温度:550℃,锥孔气流速:0l/h,检测为正离子模式,多重反应监控,质谱多重反应监控参数,见表2所示:表2值得注意的是,为了保证实验数据的准确性,所述步骤s2当中,所述步骤s2待测样品的制备的反应条件要一致于所述s12中第一上清液制备以及s13中标准样品的制备。相同地,所述步骤s3当中高通量液相色谱分离色氨酸及代谢产物的反应条件也要一致于s14中高通量液相色谱分离色氨酸及代谢产物的反应条件。所述步骤s4当中串联质谱检测所述色氨酸及代谢产物的反应条件液要一致于所述步骤s15中串联质谱检测所述色氨酸及代谢产物的反应条件。以上反应条件,在此不再赘诉。本发明提供一具体实施例,在该具体实施例中,色氨酸、犬尿氨酸、5-羟色胺和5-羟吲哚乙酸以及同位素标记的内标(色氨酸-d5、犬尿氨酸-d4、5-羟色胺-d4、5-羟吲哚乙酸-d5)分别采购于sigma和torontoresearchchemicals公司。标准品用甲醇溶液进行溶解,然后分装保存在-80℃,需要配制标准曲线时,用甲醇溶液将上述标准品稀释至3nmol/l~650nmol/l之间、3nmol/l~650nmol/l之间、0.99~200.00μmo/l,0.063~12.77μmo/l之间,内标的浓度为35.7nmol/l。(1)样品制备:往待测样品中加入一定量的含有已知浓度内标(内标是同位素标记的待测物质)的含1.58g/l硫酸铵的甲醇-水溶液,高速离心后吸取上清液;上清液使用低温离心机在18000g离心力4℃下离心5min,浓缩冷冻系统冻干后,加入一定量的甲酸-水溶液后,再使用低温离心机在18000g离心力4℃下对混合溶液进行离心分离,取上清液于96孔板用于液相色谱串联质谱上样分析;(2)液相色谱分离:利用超高效液相色谱以及相应的流动相,在反向c18分析柱上对样品中色氨酸及代谢产物进行色谱洗脱分离,通过控制洗脱条件,分离出色氨酸及代谢产物;色谱柱:watersacquityuplcc18column:poresizeparticlesize1.7μm,2.1mm×50mm;cat.#186002350ivd;色谱柱柱温:25℃;进样量:10μl;流动相组成:a相为0.1%甲酸-水溶液(体积比),b相为0.1%甲酸-乙腈溶液(体积比)(3)质谱检测并制标准曲线:液相色谱上分离出的色氨酸及代谢产物进入到三重四级杆质谱进行检测,利用三重四级杆质谱中的多重反应监控模式特异性地检测色氨酸及代谢产物的含量,并画制标准曲线图;色谱上分离后的色氨酸及代谢产物进入到watersxevotqd质谱进行检测,利用三重四级杆质谱中的多重反应监控模式,设置特异性地检测色氨酸及代谢产物;5-羟色胺保留时间为0.97min,氘代5-羟色胺保留时间为0.97min,5-羟吲哚乙酸保留时间为1.90min,氘代5-羟吲哚乙酸保留时间为1.90min,色氨酸保留时间为1.80min,氘代色氨酸保留时间为1.80min,犬尿氨酸保留时间为1.17min,氘代犬尿氨酸保留时间为1.15min。样品通过超高效液相色谱分离后,色氨酸及代谢产物在特定的洗脱时间出峰,并且被质谱选择反应监控模式检测到。质谱为watersxevotqdivd(waters,milford,ma);质谱检测条件如下:电喷雾针电压:2.0kv,去溶剂气流速:850l/h,去溶剂气温度:550℃,锥孔气流速:0l/h,检测为正离子模式,多重反应监控,每个待测物的特定反应离子对、驻留时间、锥孔电压、碰撞能量等如表所示(不同类型仪器,碰撞能量、锥孔电压值有所不同,需要独立优化)。多重反应监控通过两次筛选,即第一个四级杆进行特定母离子筛选,第二个四级杆进行母离子碎裂产生子离子,第三个四级杆进行特定子离子筛选,具有非常好的检测特异性。可以通过选择反应监控检测到的离子流,以及对应的保留时间,来确定色氨酸及代谢产物的检测,再利用添加已知量的内标进行定量。检测限定义为信噪比>3,定量限定义为信噪比>10,保留时间为色谱洗脱出峰的绝对保留时间,所有检测物质的相关系数r2均>0.99,每种色酸氨及代谢产物的保留时间,定量限,线性范围以及定量校正方程分别如图中所示;通过三日的精密度测试,包括低、中、高三个浓度,日内日间精密度rsd均小于15%,表明检测结果准确,可重复。色酸氨及代谢产物的保留时间、定量限、线性范围、线性方程、相关系数,见如表3:表3从生物样本中获得待测样品的制备:取血浆样本放入ep管中,加入含有已知浓度内标的含1.58g/l硫酸铵的甲醇-水溶液进行涡旋混合,随后产生蛋白沉淀,静置等充分沉淀后,进行第一次离心,离心条件被控制在离心力为18000g;离心温度为4℃;离心时间为5min,获得第一上清液,移取所述第一上清液利用离心浓缩冷冻系统冻干后,加入水溶液后第二次离心,与第一次离心条件一致,获得第二上清液,取所述第二上清液作为待测样品,放置于96孔板上备用。液相色谱串联质谱分析同步骤(2)和(3),质谱检测得到色氨酸及其代谢产物与标记色氨酸及其代谢产物的比值,将比值代入到定量校正方程,计算得到生物样本中色氨酸及其代谢产物的含量。本发明不局限于上述最佳实施方式,任何人在本发明的启示下都可得出其他各种形式的产品,但不论在其形状或结构上作任何变化,凡是具有与本申请相同或相近似的技术方案,均落在本发明的保护范围之内。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1