抗缪勒氏管激素测定试剂盒、制备方法及检测方法与流程
本发明涉及体外诊断检测
技术领域:
,特别是涉及一种抗缪勒氏管激素测定试剂盒、制备方法及检测方法。
背景技术:
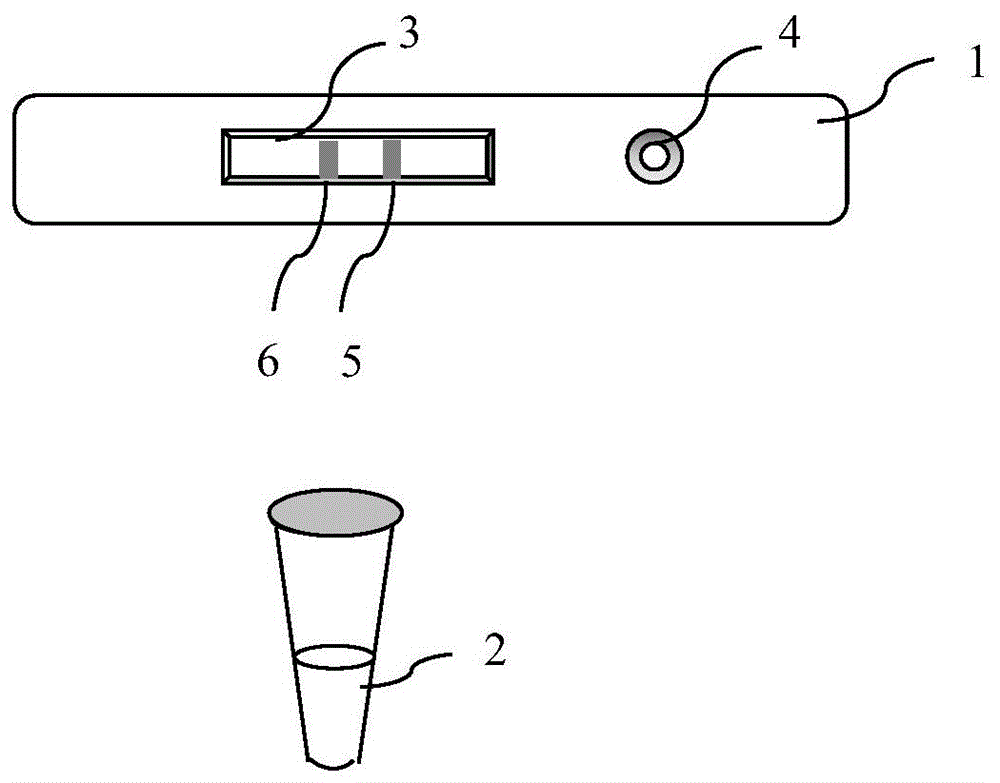
:抗缪勒氏管激素(amh)属于转化生长因子β(tgf-β)家族成员,是由卵巢内窦前卵泡和小窦卵泡分泌而来,是由二硫化物桥连接两个72kda单体组成的140ku的糖蛋白二聚物。抗缪勒氏管激素(amh)在性腺器官发育过程中起着重要作用,是男女性腺功能的重要标记物之一。在男性amh主要由睾丸间质细胞产生,始于胚胎形成并贯穿生命始终,在男性胎儿的发育过程中,amh导致缪勒氏管退化,形成正常发育的男性生殖管道;在女性amh主要由卵巢颗粒细胞产生,amh在卵巢中的卵泡发育中发挥重要作用,从青春期开始,amh水平随时间渐渐降低,并在更年期降低到检测不到的水平,接近绝经期时,amh便渐趋于0。相比较其他传统的生物学指标,amh比fsh、雌二醇、抑制素b和窦卵泡计数更早反映卵巢储备随年龄下降的趋势,且其水平不受月经周期、激素类避孕药和怀孕的影响。传统的评价方法(性激素检测、卵巢刺激试验、卵泡超声监测)在时间及具体操作方面要求甚多,而且对于原发性卵巢功能不足患者会因为生理期的水平上升造成误诊,而amh检测可更为精准的反应卵巢的储备功能。目前amh主要用于卵巢储备功能评估、卵巢早衰、卵巢过度刺激综合征、卵巢颗粒细胞肿瘤,辅助生殖以及某些自身免疫性疾病等的评价。当然,amh的检测仅供临床参考,不能单独作为诊断或排除病例的依据。随着临床检验amh需求的提升,传统检验方法虽然可以在检验标本量、自动化操作、结果精确度、性能稳定性等方面满足临床检验要求,但在便携性、检测速度、检验流程复杂度等方面却无法得以满足。在家庭健康管理及基层医疗机构检验方面,大型检验设备更是难以普及。poct检测能快速而恰当地进行诊疗、护理、病程观察,进而提高医疗质量和患者满意度。cn110412300a中公开了一种抗缪勒氏管激素快速免疫荧光定量检测试剂盒。采用用荧光材料标记的抗抗缪勒氏管激素单克隆抗体-1溶液喷涂经预处理的金标垫,制得包含抗抗缪勒氏管激素单克隆抗体-1的标记垫。该方法在喷涂过程中易造成涂布不均匀,从而影响试剂盒的准确性及重复性。cn106053791a中公开了一种抗缪勒民管激素化学发光免疫检测试剂盒。该试剂盒以全自动化学发光免疫分析仪为检测工具,对仪器设备维护要求较高,且检测中心往往将待测样本收集到一定量后,统一进行检测,其时效性难以满足快速临床诊断要求。因此,仍需开发一种检验准确度高、特异性强、重现性好、操作快捷的抗缪勒氏管激素检测试剂盒。技术实现要素:本发明的目的在于克服现有技术的缺陷,提供一种检验准确度高、特异性强、重现性好、操作快捷的抗缪勒氏管激素检测试剂盒、制备方法及检测方法。为实现上述目的,本发明提供了一种抗缪勒氏管激素检测试剂盒,采取以下技术方案:一种抗缪勒氏管激素测定试剂盒,其特征在于,包括反应物质,所述反应物质包括检测线荧光偶合物及质控线荧光偶合物,所述检测线荧光偶合物含有荧光微球标记的抗缪勒氏管激素单克隆抗体,所述质控线荧光偶合物含有荧光微球标记的鸡igy抗体、兔igg抗体或鼠igg抗体中的一种。进一步地,所述反应物质由检测线荧光偶合物及质控线荧光偶合物在冻干保护液的保护下经过冷冻干燥制成。进一步地,所述荧光微球为时间分辨荧光微球,所述时间分辨荧光微球包埋稀土离子,同时所述时间分辨荧光微球表面修饰有氨基、羧基或羟基中至少一种功能基团;所述稀土离子选自镧系元素中sm钐、eu铕、gd钆、tb铽、dy镝中的至少一种。进一步地,所述冻干保护液含有保护蛋白、糖类的缓冲液;所述缓冲液选自磷酸盐、硼酸盐或tris缓冲液中的至少一种,浓度为10mm-50mm;所述的保护蛋白选自牛血清白蛋白,卵清蛋白或酪蛋白中的至少一种,浓度为0.1%-3%;所述糖类选自海藻糖、蔗糖、乳糖中的至少一种,浓度为0.1%-10%。进一步地,所述试剂盒还包括试剂卡,所述试剂卡包括壳体及试纸条,所述试纸条包括样品垫、硝酸纤维素膜、吸水垫及背衬板,所述硝酸纤维素膜贴在所述背衬板上,所述样品垫和所述吸水垫的一端分别搭接于所述硝酸纤维素膜的两端,所述硝酸纤维素膜上设有检测线与质控线,所述检测线与质控线相互平行,且质控线位于硝酸纤维素膜上靠近吸水垫的一端,所述检测线包被有抗缪勒氏管激素单克隆抗体,所述质控线包被有羊抗鸡igy抗体、羊抗兔igg抗体或羊抗鼠igg抗体中的一种,所述壳体包括能相互扣合的上盖和下盖,所述上盖对应所述硝酸纤维素膜的位置设有显示窗,对应所述样品垫的位置设有加样孔。进一步地,所述试剂盒还包括反应缓冲液,所述反应缓冲液包括表面活性剂、糖类、防腐剂、氯化钠及缓冲液;进一步地,所述表面活性剂选自曲拉通x-100、吐温20、s16、s9中的至少一种,浓度为0.1%-1%;所述糖类选自海藻糖、蔗糖、乳糖中的至少一种,浓度为0.1%-10%;所述nacl的浓度为0.8-2%;所述防腐剂选自山梨酸、苯甲酸或proclin300中的至少一种,浓度为0.01%-0.1%;所述缓冲液选自磷酸盐、硼酸盐或tris缓冲液中的至少一种或几种,浓度为10mm-50mm。本发明还提供了一种抗缪勒氏管激素测定试剂盒的制备方法,采取以下技术方案:所述反应物质的制备方法,包括如下步骤:1)活化荧光微球;2)荧光微球与交联剂交联;3)荧光微球与抗缪勒氏管激素单克隆抗体反应,得到检测线荧光偶合物;4)荧光微球与鸡igy抗体、兔igg抗体或鼠igg抗体中的一种反应,得到质控线荧光偶合物;5)用冻干保护液分别将检测线荧光偶合物与质控线荧光偶合物稀释,配制成反应物质溶液;6)将反应物质溶液分装在塑料试管中,冷冻干燥,得反应物质。进一步地,所述步骤2)中交联剂包括edc和sulfo-nhs,edc终浓度为0.04%-0.2%,sulfo-nhs终浓度为0.12%-0.6%。进一步地,所述步骤5)中冻干保护液将检测线荧光偶合物稀释100至1000倍,冻干保护液将质控线荧光偶合物稀释500至2000倍。本发明还提供了一种用于检测抗缪勒氏管激素的定量检测方法,其特征在于,采用上述的试剂盒,包括以下步骤:步骤a:将冷藏保存的反应物质和反应缓冲液在室温放置,使其充分平衡;步骤b:吸取反应缓冲液放入反应物质试管,并立即吸取全血、血清或血浆加入装有反应缓冲液的反应物质试管中,得样本混合液;步骤c:盖上反应物质试管盖子,摇晃使样本混合液充分混匀;步骤d:吸取样本混合液,加到试剂卡的加样孔中,反应;步骤e:将反应后的试剂卡插入荧光免疫分析仪中,进行结果读取。本发明与现有技术相比,本发明具有以下有益效果:(1)本发明将荧光偶合物即荧光微球标记的抗缪勒氏管激素单克隆抗体及质控线荧光偶合物分装至独立离心管内,再经冷冻干燥的方式制成冻干粉,封装,可最大程度保存了荧光微球标记的抗体的生物活性,且稳定性好,受环境影响小。(2)常规方法通过喷膜机将荧光偶合喷洒结合垫上,再烘干,在喷洒后至烘干的过程中,因湿料无定向扩散,不能迅速地固定保持在玻璃纤维上,导致结合垫单位面积上所含荧光偶合物的活性不均一,使免疫层析试剂变异系数cv较高。而采用本发明的工艺,将荧光偶合物分装至独立离心管内,再经冷冻干燥的方式制成冻干粉,封装,该试剂盒具有较好的均一性及较低的批间差异。(3)本发明的工艺,将反应物质即荧光偶合物分装至独立离心管内,再经冷冻干燥的方式制备冻干粉,封装,加入反应缓冲液后,该荧光偶合物可快速溶解,并能够将荧光偶合物完全释放,极大保持了荧光微球标记的抗缪勒氏管激素单克隆抗体的生物活性,使其能够与样本中的抗缪勒氏管激素充分结合,从而提高了检测的灵敏度及准确度。(4)检测时,将待测样本加入离心管内,先与反应物质进行免疫反应,再取混合液加入至试剂卡加样孔,与检测线和质控线上的抗体进行免疫反应,形成免疫复合物。该方法使荧光偶合物充分释放并与样本中抗缪勒氏管激素发生免疫反应,反应更充分完全,显著提高了检测的灵敏度及重复性。附图说明为了更清楚地说明本申请实施例或现有技术中的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明中记载的一些实施例,对于本领域普通技术人员来讲,还可以根据这些附图获得其他的附图。图1为本发明一实施例的抗缪勒氏管激素检测试剂盒组成示意图;图2为本发明一实施例的免疫层析试剂卡的内部结构示意图;图3为本发明一实施例的抗缪勒氏管激素的标准曲线图;图4为本发明一实施例的抗缪勒氏管激素的线性范围图;图5为本发明一实施例的试剂盒与化学发光发试剂盒的相关性图。其中:1.试剂卡;2.反应物质;3.显示窗;4.加样孔;5.检测线;6.质控线;7.样品垫;8.吸水垫;9.硝酸纤维素膜;10.背衬板。具体实施方式为了使本领域的技术人员更好地理解本发明的技术方案,下面将结合附图对本发明作进一步的详细介绍。显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。下述实施例中的实验方法,如无特殊说明,均为常规方法。下述实施例中所用的试验材料,如无特殊说明,均为自常规生化试剂商店购买得到的。一实施方式的抗缪勒氏管激素测定试剂盒,包括反应物质,所述反应物质包括检测线荧光偶合物及质控线荧光偶合物,所述检测线荧光偶合物含有荧光微球标记的抗缪勒氏管激素单克隆抗体,所述质控线荧光偶合物含有荧光微球标记的鸡igy抗体、兔igg抗体或鼠igg抗体中的一种。所述反应物质由检测线荧光偶合物及质控线荧光偶合物在冻干保护液的保护下经过冷冻干燥制成。本发明人通过大量研究实验考察后发现,传统的荧光免疫方法将待测样本与荧光偶合物垫片上标记的抗缪勒氏管激素单克隆抗体发生特异性免疫结合,形成荧光复合物,该荧光复合物经过测试带,荧光复合物中的抗原与测试带中包被的抗缪勒氏管激素单克隆抗体发生特异性免疫结合,从而固定在测试带中,进行荧光强度检测。该传统荧光免疫方法将荧光偶合物包被在结合垫片上,荧光偶合物在喷洒后至烘干的过程中,因湿料无定向扩散,不能迅速地固定保持在玻璃纤维上,可导致结合垫单位面积上所含荧光偶合物的活性不均,造成检测待测样本中的抗缪勒氏管激素含量准确度不高,精密度低。在上述研究发现的基础上,本发明对传统技术进行了改进,将含有荧光微球标记的抗缪勒氏管激素单克隆抗体和荧光微球标记的鸡igy抗体、兔igg抗体或鼠igg抗体中的一种进行冻干得到反应物质,使用前采用反应缓冲液进行复溶,再加入待测样本,使待测样本中抗缪勒氏管激素与荧光微球标记的抗缪勒氏管激素单克隆抗体充分反应,提高了抗原-抗体结合率,从而提高了检测的准确度及精密度。具体地,所述荧光微球为时间分辨荧光微球,所述时间分辨荧光微球包埋稀土离子,同时所述时间分辨荧光微球表面修饰有氨基、羧基或羟基中至少一种功能基团;所述稀土离子选自镧系元素中sm钐、eu铕、gd钆、tb铽、dy镝中的至少一种。抗体,也叫免疫球蛋白(ig),是一种能特异性结合抗原的糖蛋白。抗体以一个或者多个y字形单体存在,每个y字形单体由4条多肽链组成,包含两条相同的重链和两条相同的轻链。一般的,抗体蛋白分子中可以用于偶联的活性基团有游离氨基(如赖氨酸或末端氨基)、游离羧基(如天冬氨酸残基,谷氨酸残基及末端羧基)、巯基(如半胱氨酸)、羟基(如丝氨酸或苏氨酸)等。在其中一个实施例中,所述的时间分辨荧光微球,与通常的荧光分免疫析不同,示踪物为稀土元素,而不是荧光素;优选的,稀土元素为三价镧系元素eu铕;每个微球中可包裹成千上万个荧光分子,大大提高了荧光的标记效率,有效提高了分析灵敏度;同时荧光微球表面修饰有合适密度的氨基、羧基或羟基等其它功能基团,用于与抗缪勒氏管激素单克隆抗体的共价偶联,提高了标记物的稳定性。在其中一个实施例中,冻干保护液含有保护蛋白、糖类的缓冲液;所述缓冲液选自磷酸盐、硼酸盐或tris缓冲液中的至少一种,浓度为10mm-50mm,所述缓冲液在冷冻干燥中提供稳定溶液的ph,防止ph变化大导致蛋白质发生物理聚集或化学变性;所述的保护蛋白选自牛血清白蛋白,卵清蛋白或酪蛋白中的至少一种,浓度为0.1%-3%,所述保护蛋白为大分子物质,在冷冻干燥中为活性组分提供稳定支撑骨架,起着低温保护和脱水保护;所述糖类选自海藻糖、蔗糖、乳糖中的至少一种,浓度为0.1%-10%,所述糖类起着防止活性组分发生变性,同时具有低温保护和脱水保护作用。在其中一个实施例中,所述反应物质的制备方法,包括如下步骤:1)活化荧光微球;2)荧光微球与交联剂交联;3)荧光微球与抗缪勒氏管激素单克隆抗体反应,得到检测线荧光偶合物;4)荧光微球与鸡igy抗体、兔igg抗体或鼠igg抗体中的一种反应,得到质控线荧光偶合物;5)用冻干保护液分别将检测线荧光偶合物与质控线荧光偶合物稀释,配制成反应物质溶液;6)将反应物质溶液分装在塑料试管中,冷冻干燥,得反应物质。所述步骤2)中交联剂包括edc和sulfo-nhs,edc终浓度为0.04%-0.2%,sulfo-nhs终浓度为0.12%-0.6%。常用的抗体偶联方式有戊二醛法、碳二亚胺法(edc)等。edc〔1-乙基-3-(3-二甲基氨丙基)-碳二亚胺〕其机制一般认为是蛋白残基的羧基先同edc反应,生成活泼的中间产物o-酰基异脲(o-acylisourea)而edc与带有羧基的物质反应形成一个活性中间体,它极不稳定,其活性酯容易水解,并且中间体与氨基反应速度慢。通常加入nhs一起使用,提高活性中间体的溶解性和稳定性。本发明采用sulfo-nhs的连接反应效率比nhs要高,且sulfo-nhs具有负电荷,不易造成连接底物(例如荧光微球)聚合。所述步骤5)中冻干保护液将检测线荧光偶合物稀释100至1000倍,冻干保护液将质控线荧光偶合物稀释500至2000倍。所述抗缪勒氏管激素测定试剂盒还包括反应缓冲液,所述反应缓冲液包括表面活性剂、糖类、防腐剂、氯化钠及缓冲液;所述表面活性剂选自曲拉通x-100、吐温20、s16、s9中的至少一种,浓度为0.1%-1%,所述表面活性剂起到迅速溶解,有利于活性组分快速分散;所述糖类选自海藻糖、蔗糖、乳糖中的至少一种,浓度为0.1%-10%,所述糖类物质起到保护作用,提高溶液黏度;所述nacl的浓度为0.8-2%,所述nacl提高了溶液中的离子强度,有利于抗原抗体免疫反应;所述防腐剂选自山梨酸、苯甲酸或proclin300中的至少一种,浓度为0.01%-0.1%,所述防腐剂可抑制溶液长菌;所述缓冲液选自磷酸盐、硼酸盐或tris缓冲液中的至少一种或几种,浓度为10mm-50mm,所述缓冲液在复溶后提供稳定溶液的ph,防止荧光微球聚合。所述抗缪勒氏管激素测定试剂盒还包括试剂卡,所述试剂卡包括壳体及试纸条,所述试纸条包括样品垫、硝酸纤维素膜、吸水垫及背衬板,所述硝酸纤维素膜贴在所述背衬板上,所述样品垫和所述吸水垫的一端分别搭接于所述硝酸纤维素膜的两端,所述硝酸纤维素膜上设有检测线与质控线,所述检测线与质控线相互平行,且质控线位于硝酸纤维素膜上靠近吸水垫的一端,所述检测线包被有抗缪勒氏管激素单克隆抗体,所述质控线包被有羊抗鸡igy抗体、羊抗兔igg抗体或羊抗鼠igg抗体中的一种,所述壳体包括能相互扣合的上盖和下盖,所述上盖对应所述硝酸纤维素膜的位置设有显示窗,对应所述样品垫的位置设有加样孔。在其中一实施例中,所述抗缪勒氏管激素测定试剂盒还包括id卡,所述id卡存储有产品的项目名称、批号及标准曲线数据。与配套的干式荧光免疫分析仪使用,将id卡插入后,读取相关信息。该抗缪勒氏管激素测定试剂盒基于抗缪勒氏管激素(amh)作为检测标志物,能够对卵巢储备功能评估、卵巢早衰、卵巢过度刺激综合征、卵巢颗粒细胞肿瘤,辅助生殖以及某些自身免疫性疾病等进行快速检测。检测时,将反应缓冲液加入至反应物质,并立即吸取50μl全血、血清或血浆加入装有反应缓冲液的反应物质试管中,使充分混匀,待测样本中的抗缪勒氏管激素能够与反应物质中的荧光微球标记的抗缪勒氏管激素单克隆抗体充分结合形成复合物,再将其加到试剂卡的加样孔上,该复合物通过层析作用与检测线上包被的抗缪勒氏管激素单克隆抗体结合形成抗体-抗原-抗体夹心复合物,将试剂卡插入荧光免疫分析仪中即可测定待测样本中的抗缪勒氏管激素的含量。该检测方法方便快捷、反应充分、操作简单。实施例1反应物质的制备1)活化荧光微球:取0.1mleu铕时间分辨荧光微球-羧基基团置于离心管中,加入活化液,在转数13000rpm离心20min,去上清,沉淀物加入活化液,超声重悬;再清洗一次;2)荧光微球与交联剂交联:按0.1mleu铕时间分辨荧光微球-羧基基团加入交联剂edc和sulfo-nhs,edc终浓度0.12%,sulfo-nhs终浓度0.36%,反应30min,在转数13000rpm离心20min,去上清,沉淀物加入偶联缓冲液,超声重悬;3)荧光微球与抗缪勒氏管激素单克隆抗体反应,得到检测线荧光偶合物:按0.1mleu铕时间分辨荧光微球-羧基基团加入80μg的抗缪勒氏管激素单克隆抗体,室温旋转反应120min,然后在转数13000rpm离心20min,去上清,沉淀物加入封闭液,封闭液浓度为0.5%,超声重悬,室温旋转反应100min;在13000rpm离心20min,去上清,沉淀物加入washingbuffer,清洗两次,去上清,沉淀物用复溶液超声重悬;4)荧光微球与鸡igy抗体、兔igg抗体或鼠igg抗体中的一种反应,得到质控线荧光偶合物:按0.1mleu铕时间分辨荧光微球-羧基基团加入100ug的鸡igy抗体,室温旋转反应120min,然后在转数13000rpm离心20min,去上清,沉淀物加入封闭液,封闭液浓度为0.5%,超声重悬,室温旋转反应100min;在13000rpm离心20min,去上清,沉淀物加入washingbuffer,清洗两次,去上清,沉淀物用复溶液超声重悬;5)用冻干保护液分别将检测线荧光偶合物与质控线荧光偶合物稀释,配制成反应物质溶液:50mmtris缓冲液加入1%酪蛋白,加入3%海藻糖,加入3%蔗糖,充分溶解混匀得冻干保护液,用冻干保护液将检测线荧光偶合物稀释300倍,质控线荧光偶合物稀释1000倍配制成反应物质溶液;6)将反应物质溶液分装在塑料试管中,放置于冻干托盘上,冷冻干燥成粉末,立即将反应物质密封压盖,2℃~8℃避光保存。反应缓冲液的制备:1)反应缓冲液的制备:50mmtris缓冲液加入0.5%吐温20,加入2%海藻糖,加入0.9%nacl,加入0.05%proclin300充分溶解混匀;2)分装:将反应缓冲液分装至的试管中,加盖密封,于2℃~8℃保存。试剂卡的制备1)检测线及质控线的制备:分别配制抗缪勒氏管激素单克隆抗体浓度为2.0mg/ml,羊抗鸡igy抗体浓度为1mg/ml,用喷膜机划线至硝酸纤维素膜上检测线和质控线区域,包被量1.0μl/cm,将划好的硝酸纤维素膜放置鼓风干燥箱,在50℃烘干18小时;2)样品垫的制备:配制封闭溶液,将封闭溶液加入至玻璃纤维上,使玻璃纤维完全湿润,放置鼓风干燥箱,在50℃烘干18小时;3)试剂卡的组装:将硝酸纤维素膜黏贴至背衬板上,样品垫和吸水垫的一端分别搭接于硝酸纤维素膜的两端,切成特定宽度的试纸条,将试纸条放入壳体中固定位置,盖上盖,压卡,封入铝箔袋中,加入硅胶干燥剂,密封。检测抗缪勒氏管激素的定量检测方法,包括以下步骤:步骤a:将冷藏保存的反应物质和反应缓冲液在室温放置30分钟,使其在室温充分平衡;步骤b:吸取反应缓冲液100μl放入反应物质试管,并立即吸取50μl全血或血清或血浆加入装有反应缓冲液的反应物质试管中,得样本混合液;步骤c:盖上反应物质试管盖子,摇晃使样本混合液充分混匀;步骤d:吸取80μl的样本混合液,加到试剂卡的加样孔中,反应20分钟;步骤e:将反应后的试剂卡插入荧光免疫分析仪中,进行结果读取。实施例2反应物质的制备1)活化荧光微球:取0.1mldy镝时间分辨荧光微球-氨基基团置于离心管中,加入活化液,在转数10000rpm离心15min,去上清,沉淀物加入活化液,超声重悬;再清洗一次;2)荧光微球与交联剂交联:按0.1mldy镝时间分辨荧光微球-氨基基团加入交联剂edc和sulfo-nhs,edc终浓度0.2%,sulfo-nhs终浓度0.6%,反应30min,在转数10000rpm离心15min,去上清,沉淀物加入偶联缓冲液,超声重悬;3)荧光微球与抗缪勒氏管激素单克隆抗体反应,得到检测线荧光偶合物:按0.1mldy镝时间分辨荧光微球-氨基基团加入100μg的抗缪勒氏管激素单克隆抗体,室温旋转反应120min,然后在转数10000rpm离心15min,去上清,沉淀物加入封闭液,封闭液浓度为0.1%,超声重悬,室温旋转反应100min;在10000rpm离心15min,去上清,沉淀物加入washingbuffer,清洗两次,去上清,沉淀物用复溶液超声重悬;4)荧光微球与鸡igy抗体、兔igg抗体或鼠igg抗体中的一种反应,得到质控线荧光偶合物:按0.1mldy镝时间分辨荧光微球-氨基基团加入100μg的兔igg抗体,室温旋转反应120min,然后在转数10000rpm离心15min,去上清,沉淀物加入封闭液,封闭液浓度为0.5%,超声重悬,室温旋转反应100min;在10000rpm离心15min,去上清,沉淀物加入washingbuffer,清洗两次,去上清,沉淀物用复溶液超声重悬;5)用冻干保护液分别将检测线荧光偶合物与质控线荧光偶合物稀释,配制成反应物质溶液:30mm磷酸盐缓冲液加入3%牛血清白蛋白,加入10%蔗糖,充分溶解混匀得冻干保护液,用冻干保护液将检测线荧光偶合物稀释1000倍,质控线荧光偶合物稀释2000倍配制成反应物质溶液;6)将反应物质溶液0.1ml分装在塑料试管中,放置于冻干托盘上,冷冻干燥成粉末,立即将反应物质密封压盖,2℃~8℃避光保存。反应缓冲液的制备:1)反应缓冲液的制备:30mm磷酸盐缓冲液加入1%曲拉通x-100,加入0.5%乳糖,加入2%海藻糖,加入2%nacl,加入0.1%proclin300充分溶解混匀;2)分装:将反应缓冲液分装至的试管中,加盖密封,于2℃~8℃保存。试剂卡的制备1)检测线及质控线的制备:分别配制抗缪勒氏管激素单克隆抗体浓度为3.0mg/ml,羊抗兔igg抗体浓度为2mg/ml,用喷膜机划线至硝酸纤维素膜上检测线和质控线区域,包被量0.8μl/cm,将划好的硝酸纤维素膜放置鼓风干燥箱,在45℃烘干20小时;2)样品垫的制备:配制封闭溶液,将封闭溶液加入至玻璃纤维上,使玻璃纤维完全湿润,放置鼓风干燥箱,在45℃烘干20小时;3)试剂卡的组装:将硝酸纤维素膜黏贴至背衬板上,样品垫和吸水垫的一端分别搭接于硝酸纤维素膜的两端,切成特定宽度的试纸条,将试纸条放入壳体中固定位置,盖上盖,压卡,封入铝箔袋中,加入硅胶干燥剂,密封。检测抗缪勒氏管激素的定量检测方法,包括以下步骤:步骤a:将冷藏保存的反应物质和反应缓冲液在室温放置20分钟,使其在室温充分平衡;步骤b:吸取反应缓冲液100μl放入反应物质试管,并立即吸取50μl全血或血清或血浆加入装有反应缓冲液的反应物质试管中,得样本混合液;步骤c:盖上反应物质试管盖子,摇晃使样本混合液充分混匀;步骤d:吸取80μl的样本混合液,加到试剂卡的加样孔中,反应15分钟;步骤e:将反应后的试剂卡插入荧光免疫分析仪中,进行结果读取。实施例3反应物质的制备1)活化荧光微球:取0.1mlsm钐时间分辨荧光微球-羟基基团置于离心管中,加入活化液,在转数13000rpm离心10min,去上清,沉淀物加入活化液,超声重悬;再清洗一次;2)荧光微球与交联剂交联:按0.1mlsm钐时间分辨荧光微球-羟基基团加入交联剂edc和sulfo-nhs,edc终浓度0.04%,sulfo-nhs终浓度0.12%,反应10min,在转数13000rpm离心10min,去上清,沉淀物加入偶联缓冲液,超声重悬;3)荧光微球与抗缪勒氏管激素单克隆抗体反应,得到检测线荧光偶合物:按0.1mlsm钐时间分辨荧光微球-羟基基团加入30μg的抗缪勒氏管激素单克隆抗体,室温旋转反应120min,然后在转数13000rpm离心10min,去上清,沉淀物加入封闭液,封闭液浓度为0.3%,超声重悬,室温旋转反应100min;在13000rpm离心10min,去上清,沉淀物加入washingbuffer,清洗两次,去上清,沉淀物用复溶液超声重悬;4)荧光微球与鸡igy抗体、兔igg抗体或鼠igg抗体中的一种反应,得到质控线荧光偶合物:按0.1mlsm钐时间分辨荧光微球-羟基基团加入30μg的鼠igg抗体,室温旋转反应120min,然后在转数13000rpm离心10min,去上清,沉淀物加入封闭液,封闭液浓度为0.5%,超声重悬,室温旋转反应100min;在13000rpm离心10min,去上清,沉淀物加入washingbuffer,清洗两次,去上清,沉淀物用复溶液超声重悬;5)用冻干保护液分别将检测线荧光偶合物与质控线荧光偶合物稀释,配制成反应物质溶液:10mm硼酸盐缓冲液加入0.1%卵清蛋白,加入0.1%蔗糖,充分溶解混匀得冻干保护液,用冻干保护液将检测线荧光偶合物稀释100倍,质控线荧光偶合物稀释500倍配制成反应物质溶液;6)将反应物质溶液0.1ml分装在塑料试管中,放置于冻干托盘上,冷冻干燥成粉末,立即将反应物质密封压盖,2℃~8℃避光保存。反应缓冲液的制备:1)反应缓冲液的制备:10mm硼酸盐缓冲液加入0.1%吐温s9,加入0.1%蔗糖,加入0.8%nacl,加入0.01%proclin300充分溶解混匀;2)分装:将反应缓冲液分装至的试管中,加盖密封,于2℃~8℃保存。试剂卡的制备1)检测线及质控线的制备:分别配制抗缪勒氏管激素单克隆抗体浓度为0。5mg/ml,羊抗鼠igg抗体浓度为0.5mg/ml,用喷膜机划线至硝酸纤维素膜上检测线和质控线区域,包被量0.5μl/cm,将划好的硝酸纤维素膜放置鼓风干燥箱,在37℃烘干24小时;2)样品垫的制备:配制封闭溶液,将封闭溶液加入至玻璃纤维上,使玻璃纤维完全湿润,放置鼓风干燥箱,在37℃烘干24小时;3)试剂卡的组装:将硝酸纤维素膜黏贴至背衬板上,样品垫和吸水垫的一端分别搭接于硝酸纤维素膜的两端,切成特定宽度的试纸条,将试纸条放入壳体中固定位置,盖上盖,压卡,封入铝箔袋中,加入硅胶干燥剂,密封。检测抗缪勒氏管激素的定量检测方法,包括以下步骤:步骤a:将冷藏保存的反应物质和反应缓冲液在室温放置20分钟,使其在室温充分平衡;步骤b:吸取反应缓冲液100μl放入反应物质试管,并立即吸取50μl全血或血清或血浆加入装有反应缓冲液的反应物质试管中,得样本混合液;步骤c:盖上反应物质试管盖子,摇晃使样本混合液充分混匀;步骤d:吸取80μl的样本混合液,加到试剂卡的加样孔中,反应8分钟;步骤e:将反应后的试剂卡插入荧光免疫分析仪中,进行结果读取。测试例1标准曲线制作配制浓度为0、0.05、0.2、1.0、4.0、10.0、25.0(单位:ng/ml)的样本,采用实施例1的试剂盒及检测方法进行检测,每个浓度的样本重复3次,计算平均值,在荧光免疫分析仪中读取荧光信号,以浓度为纵坐标,荧光信号均值为横坐标绘制拟合曲线,得到标准曲线,该标准曲线线性良好,r=0.9998,见图3。测试例2重复性测试配制浓度1.5、10.0(单位:ng/ml)的样本,采用实施例2的试剂盒及检测方法进行检测,每个浓度的样本重复10次,在荧光免疫分析仪中读取浓度,计算10次测定结果的平均值(m)和标准差(sd),根据公式得出变异系数(cv=sd/m×100%)。结果见表1。表1由表1所示,不同浓度的样本得到的cv值均在10%以下,该抗缪勒氏管激素检测试剂盒重复性良好。测试例3准确度测试将浓度约为15ng/ml(允许其浓度偏差为±20%)和90ng/ml(允许其浓度偏差为±20%)的amh溶液(a)加入到浓度范围在0.1-1ng/ml的样本b中,制成2份回收实验样本。所加入a的体积与b的体积比为1:10,采用实施例3的试剂盒及检测方法进行检测,每个浓度检测3次,计算平均值,根据公式计算回收率。结果见表2。式中:r——回收率;v——样本a的体积;v0——样本b的体积;c——样本b加入a后的检测浓度;c0——样本b的浓度;cs——样本a的浓度。序号加入浓度c1加入浓度c2b液a液1a液21#2.018.510.8115.0090.002#2.048.340.75//3#2.139.260.76//m2.068.700.77//回收率99.51%97.78%///表2由表2所示,回收率在85-115%以内,因此该抗缪勒氏管激素检测试剂盒准确度良好。测试例4干扰试验测试配置血红蛋白母液(120g/l)、甘油三酯母液(240g/l)、胆红素母液(5mg/ml)。选择健康个体的新鲜混合临床血清样本,添加适量的抗缪勒氏管激素校准品,使样本中抗缪勒氏管激素的浓度分别达到约1.5ng/ml和10.0ng/ml。分成2份,一份作为对照样品,另一份作为实验样品。对照样品:不添加干扰物质。实验样品:在对照样品添加纯品的干扰物质:血红蛋白母液(120g/l)、甘油三酯母液(240g/l)、胆红素母液(5mg/ml)。采用实施例1的试剂盒及检测方法进行检测,每份样品各重复检测3次,取平均值作为最终检测结果。计算实验样品与对照样品的相对偏差。相对偏差在±10%以内,则认为所添加的干扰物质对试剂的检测结果不存在干扰。结果见表3。以实验样品的测试均值结果记为m,以对照样品的测试均值结果记为t,根据以下公式计算相对偏差b。式中:b——相对偏差;m——实验样品浓度均值;t——对照样本浓度均值。表3结果显示,血红蛋白小于2.0mg/ml,甘油三脂小于2.0mg/ml,胆红素小于0.1mg/ml,相对偏差在±10%以内,本发明的试剂盒抗干扰效果良好。测试例5特异性测试配置用生理盐水(浓度为0.9%的nacl溶液)制备抑制素a母液(2000ng/ml)、激活素a母液(2000ng/ml)、lh母液(10000miu/ml)、fsh母液(10000miu/ml)。选择健康个体的新鲜混合临床血清样本,添加适量的高浓度amh校准品,使样本中amh的浓度分别达到约1.5ng/ml和10.0ng/ml。分成2份,一份作为对照样品,另一份作为实验样品。对照样品:不添加交叉反应物质。实验样品:在对照样本添加抑制素a、激活素a、lh、fsh纯品的交叉反应物质。采用实施例2的试剂盒及检测方法进行检测,每份样品各重复检测3次,取平均值作为最终检测结果。计算实验样品与对照样品的相对偏差。以实验样品的测试均值结果记为m,以对照样品的测试均值结果记为t,根据以下公式计算相对偏差b。结果见表4。式中:b——相对偏差;m——实验样品浓度均值;t——对照样本浓度均值。表4结果显示,抑制素a(100ng/ml)、激活素a(100ng/ml)、lh(500miu/ml)、fsh(500miu/ml)的实验样品,相对偏差均在±10%以内。本发明的试剂盒抗干扰效果良好。实施例6稳定性试验配制浓度0.05、0.2、1.0、4.0、10.0、25.0(单位:ng/ml)的样本,采用实施例3的试剂盒及检测方法进行检测,每个样本重复3次,将测定浓度的平均值与理论浓度或稀释比例用最小二乘法进行直线拟合,按照公式计算出线性回归的相关系数r。测试结果见表5,相关线性图见图4。xi——理论浓度或稀释比例;yi——实际测定平均值。理论浓度测试1测试2测试3平均值25.0024.3123.1822.9823.4910.009.8410.5810.2510.224.004.124.243.984.111.000.980.940.910.940.200.190.210.210.200.050.050.060.060.06表5如表5及图4所示,相关系数r=0.9993,本发明的试剂盒的稳定性良好。测试例7加速热稳定性测试将试剂卡、反应物质、反应缓冲液分两部分,一部分作为实验组放在37℃的条件下15天,另一部分作为对照组放置2-8℃第15天。配制浓度1.5、10.0(单位:ng/ml)的样本,采用实施例1的试剂盒及检测方法进行检测,每个样本重复3次。结果见表6。表6结果显示,实验组与对照组的结果无明显差异,表明试剂卡、反应物质、反应缓冲液在高温条件下的稳定性良好。测试例8临床样本相关性测试采用实施例1的抗缪勒氏管激素测定试剂盒和进口试剂盒(罗氏诊断公司产的抗缪勒管激素检测试剂盒(电化学发光法)医疗器械注册证编号:国械注进20152400916)分别对40份人血清样本同时进行检测对比。对数据进行相关性分析,其结果如表7所示:表7以进口试剂盒的测定结果(xi)为自变量,以本发明试剂盒的测定结果(yi)为因变量,求出线性回归方程,相关线性图见图5。相关方程为:y==0.9599x+0.3985,相关系数r=0.9804。经统计学处理结果表明,本发明试剂盒同进口试剂盒临床样本测定值相关性良好,符合临床试验要求。对比例对比例的制备:将荧光偶合物用冻干保护液稀释15倍和50倍,用喷膜机喷洒至结合垫上,放置鼓风干燥箱37℃烘干18-24小时。以常规方法制备免疫层析试剂卡,将样品垫、结合垫、硝酸纤维素膜、吸水垫依次粘土至pvc底板上,裁切试纸条,装卡。对比例将荧光偶合物包被在结合垫上,其余结构及步骤与实施例1相同,样本加样量及判读时间与本实施例1相同。分别采用对比例试剂盒与实施例1试剂盒进行重复性测试:配制浓度1.5、10.0(单位:ng/ml)的样本,进行检测,每个重复10次,在荧光免疫分析仪中读取浓度,计算10次测定结果的平均值(m)和标准差(sd),根据公式得出变异系数cv(cv=sd/m×100%)。结果见表8:表8结果表明,实施例1的变异系数cv均在10%以下,与对比例相比,具有更好的重复性。所属领域的普通技术人员应当理解:以上任何实施例的讨论仅为示例性的,并非旨在暗示本公开的范围(包括权利要求)被限于这些例子;在本发明的思路下,以上实施例或者不同实施例中的技术特征之间也可以进行组合,并存在如上所述的本发明的不同方面的许多其它变化,为了简明它们没有在细节中提供。因此,凡在本发明的精神和原则之内,所做的任何省略、修改、等同替换、改进等,均应包含在本发明的保护范围之内。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1