一种检测新型冠状病毒抗体的荧光免疫层析试纸的制作方法
本发明属于生物技术与领域,具体涉及一种检测新型冠状病毒抗体的荧光免疫层析试纸。
背景技术:
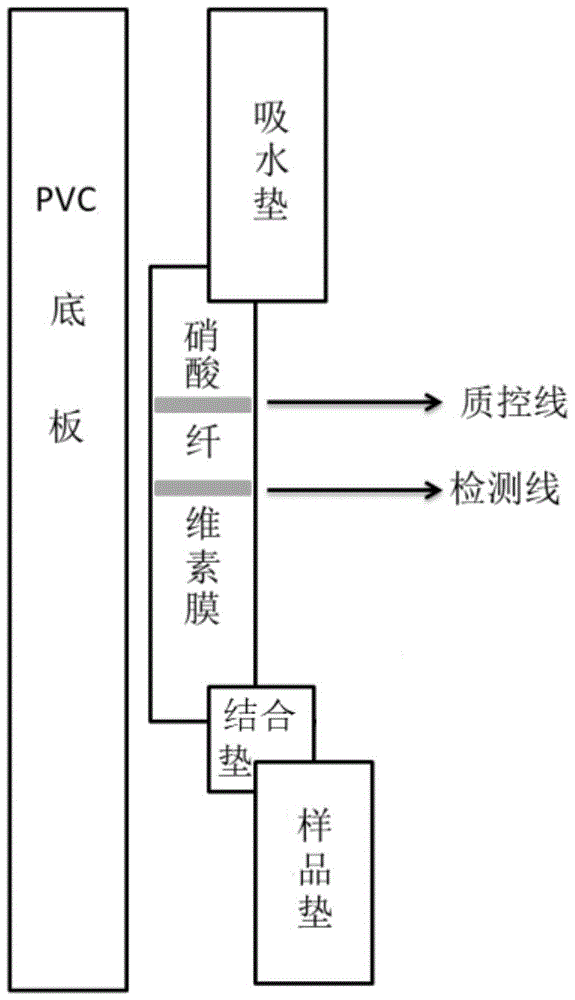
:冠状病毒是一类有包膜的单股正链rna病毒,因电镜下病毒颗粒形似皇冠而得名。冠状病毒的宿主范围主要包括鸟类和哺乳类,迄今为止,已鉴定出七种可感染人类的冠状病毒,其中sars病毒(sars-cov)、中东呼吸综合征冠状病毒(mers-cov)和新型冠状病毒(sars-cov-2)的出现给世界经济卫生造成了极大威胁。新型冠状病毒属于冠状病毒科、冠状病毒属病毒,感染人后可引起不同程度的症状,以发热、乏力、干咳为主要表现,严重者出现肺炎、急性呼吸窘迫综合征甚至死亡。新型冠状病毒的主要传播方式是飞沫传播和接触传播。关于新型冠状病毒的检测,最初通过检测样本中是否含有病毒核酸实现的,但因样本采集、试剂、操作等原因导致阳性率降低。将疑似病例具有肺炎影像学特征者作为临床诊断病例标准。但不同的肺炎类型可能会出现相似的组织学病理变化,且ct检测存在交叉感染的风险。技术实现要素:本发明的目的是检测新型冠状病毒。本发明首先保护一种检测新型冠状病毒抗体的荧光免疫层析试纸,其结合垫上包被了时间分辨荧光微球标记的抗人igm抗体;所述结合垫的制备方法可如下:(1)将时间分辨荧光微球和抗人igm抗体混合,加入含0.1-0.5%(如0.1-0.3%、0.3-0.5%、0.1%、0.3%或0.5%)bsa的硼酸缓冲液封闭;(2)完成步骤(1)后,离心,收集沉淀;(3)完成步骤(2)后,用含0.1-0.5%(如0.1-0.3%、0.3-0.5%、0.1%、0.3%或0.5%)bsa的硼酸缓冲液重悬沉淀,得到标记溶液;(4)将标记溶液喷涂在膜上,干燥,得到包被了时间分辨荧光微球标记的抗人igm抗体的结合垫;所述硼酸缓冲液为ph7.0-8.5(如ph7.0-7.5、ph7.5-8.0、ph8.0-8.5、ph7.0、ph7.5、ph8.0或ph8.5)、10-100mm(如10-25mm、25-50mm、50-100mm、10mm、25mm、50mm或100mm)硼酸缓冲液。上述荧光免疫层析试纸中,所述将标记溶液喷涂在膜上可为将标记溶液喷涂在玻璃纤维素膜上。上述荧光免疫层析试纸中,所述硼酸缓冲液具体可为ph8.0、25mm硼酸缓冲液。上述荧光免疫层析试纸中,所述时间分辨荧光微球可为含铕时间分辨荧光微球。上述荧光免疫层析试纸中,反应膜上的质控线位置可包被所述抗人igm抗体的抗体。检测线位置可包被新型冠状病毒抗原。上述任一所述新型冠状病毒抗原可为新型冠状病毒np抗原。上述任一所述抗人igm抗体可为羊抗人igm抗体、鼠抗人igm抗体或兔抗人igm抗体。上述任一所述羊抗人igm抗体的抗体具体可为兔抗羊igm抗体。上述任一所述反应膜可为硝酸纤维素膜。上述任一所述羊抗人igm抗体的制备方法可参考如下文献:羊抗人μ链血清的制备,中国公共卫生,1985,4(4):38-40。上述任一所述兔抗羊igm抗体的制备方法参考如下文献:制备羊抗兔igg抗体的1种简单方法,首都医科大学学报,1998,19(1)。上述任一所述荧光免疫层析试纸具体可由样品垫(材质为玻璃纤维素膜)、结合垫、包被质控线和检测线的硝酸纤维素膜和吸水垫(如滤纸)四部分组成,具体结构示意图见图1。上述任一所述荧光免疫层析试纸中,所述结合垫的制备方法具体可如下:(1-1)向6-10ml含铕时间分辨荧光微球的溶液中加入800μl浓度为1mg/ml的羊抗人igm抗体,旋转混匀仪上混匀60min;(1-2)加入含0.3%bsa的硼酸缓冲液,过夜封闭;(1-3)15000rpm离心40min,收集沉淀;(1-4)用12ml0.1%(m/v)bsa的硼酸缓冲液重悬沉淀,得到含铕时间分辨荧光微球标记的羊抗人igm抗体的溶液;(1-5)将含铕时间分辨荧光微球标记的羊抗人igm抗体的溶液均匀喷涂在玻璃纤维素膜上,然后冻干机冻干,得到结合垫;所述硼酸缓冲液具体可为ph8.0、25mm硼酸缓冲液。上述任一所述荧光免疫层析试纸中,所述包被质控线和检测线的硝酸纤维素膜的制备方法具体可如下:(2-1)用0.01mpbs缓冲液(ph7.4)稀释新型冠状病毒np抗原,得到浓度为3mg/ml的检测线溶液,用于包被检测线;(2-2)用0.01mpbs缓冲液(ph7.4)稀释兔抗羊igm抗体,得到浓度为2mg/ml的质控线溶液,用于包被质控线;(2-3)取质控线溶液和检测线溶液,分别均匀喷涂在硝酸纤维素膜上(喷样量均为10μl/cm2),形成相互分离的质控线(c)和检测线(t),37℃干燥3-5h,得到包被质控线和检测线的硝酸纤维素膜。包被质控线和检测线的硝酸纤维素膜上,质控线和检测线的间距为0.5cm。本发明还保护采用上述任一所述的荧光免疫层析试纸检测待测液中是否含有新型冠状病毒抗体的方法。本发明所保护的采用上述任一所述的荧光免疫层析试纸检测待测液中是否含有新型冠状病毒抗体的方法,具体可为方法一,包括如下步骤:将上述任一所述的荧光免疫层析试纸的样品垫浸入待测液,静置10min以上(如10min、15min),用荧光(具体可为激发波长为365nm的荧光)照射反应膜,观察反应膜上显出的红色反应线条,进行如下判断:如果检测线和质控线处均显出红色反应线条,则待测液中含有新型冠状病毒抗体;如果质控线处显出红色反应线条且检测线处不显出红色反应线条,则待测液中不含有新型冠状病毒抗体;如果质控线处不显出红色反应线条,则为无效结果。本发明所保护的采用上述任一所述的荧光免疫层析试纸检测待测液中是否含有新型冠状病毒抗体的方法,具体可为方法二,包括如下步骤:将上述任一所述的荧光免疫层析试纸的样品垫浸入待测液,静置10min以上(如10min、15min),检测检测线和质控线处的荧光值,进行如下判断:如果检测线和质控线处的荧光值均大于50,则待测液中含有新型冠状病毒抗体;如果质控线处的荧光值大于50且检测线处的荧光值为50以下,则待测液中不含有新型冠状病毒抗体;如果质控线处的荧光值为50以下,则为无效结果。上述方法二中,所述检测检测线和质控线处的荧光值可为采用干式荧光检测仪检测检测线和质控线处的荧光值。上述任一所述的方法中,所述待测液可为血清或血清稀释液。上述任一所述方法用于非疾病诊断与治疗。上述任一所述的方法中,所述含有新型冠状病毒抗体可意味着感染了或感染过新型冠状病毒。上述任一所述荧光免疫层析试纸用于非疾病诊断与治疗。实验证明,使用本发明所提供的荧光免疫层析试纸可以检测样品中是否含有新型冠状病毒抗体,操作简单,耗时短,准确率高,特异性好且灵敏度高。本发明所提供的荧光免疫层析试纸在现场快速检测血清中是否含有新型冠状病毒抗体中具有重要的应用价值。附图说明图1为检测新型冠状病毒抗体的荧光免疫层析试纸的结构示意图。具体实施方式以下的实施例便于更好地理解本发明,但并不限定本发明。下述实施例中的实验方法,如无特殊说明,均为常规方法。下述实施例中所用的试验材料,如无特殊说明,均为自常规生化试剂公司购买得到的。以下实施例中的定量试验,均设置三次重复实验,结果取平均值。实施例1、检测新型冠状病毒抗体的荧光免疫层析试纸的制备一、结合垫的制备1、用硼酸缓冲液溶解bsa,得到浓度为0.3%(m/v)bsa的工作液1和浓度为0.1%(m/v)bsa的工作液2。2、向6-10ml含铕时间分辨荧光微球(thermoscientifictm公司的产品,货号为93470520010150;粒径为200nm)的溶液中加入800μl浓度为1mg/ml的羊抗人igm抗体(羊抗人igm抗体的制备方法参考如下文献:羊抗人μ链血清的制备,中国公共卫生,1985,4(4):38-40),旋转混匀仪上混匀60min。3、完成步骤2后,加入工作液1,过夜封闭。4、完成步骤3后,15000rpm离心40min,收集沉淀。5、完成步骤4后,用12ml工作液2重悬沉淀,得到含铕时间分辨荧光微球标记的羊抗人igm抗体的溶液。6、将含铕时间分辨荧光微球标记的羊抗人igm抗体的溶液均匀喷涂在玻璃纤维素膜上,然后冻干机冻干,得到结合垫。二、包被质控线和检测线的硝酸纤维素膜的制备1、用0.01mpbs缓冲液(ph7.4)稀释新型冠状病毒np抗原(东方海洋医学研究院的产品,货号为b35-ag1),得到浓度为3mg/ml的检测线溶液,用于包被检测线。2、用0.01mpbs缓冲液(ph7.4)稀释兔抗羊igm抗体(兔抗羊igm抗体的制备方法参考如下文献:制备羊抗兔igg抗体的1种简单方法,首都医科大学学报,1998,19(1)),得到浓度为2mg/ml的质控线溶液,用于包被质控线。3、取质控线溶液和检测线溶液,分别均匀喷涂在硝酸纤维素膜上(喷样量均为10μl/cm2),形成相互分离的质控线(c)和检测线(t),37℃干燥3-5h,得到包被质控线和检测线的硝酸纤维素膜。包被质控线和检测线的硝酸纤维素膜上,质控线和检测线的间距为0.5cm。三、检测新型冠状病毒抗体的荧光免疫层析试纸的组装检测新型冠状病毒抗体的荧光免疫层析试纸由样品垫(材质为玻璃纤维素膜)、结合垫、包被质控线和检测线的硝酸纤维素膜和吸水垫(如滤纸)四部分组成。检测新型冠状病毒抗体的荧光免疫层析试纸的组装步骤如下:将吸水垫用双面胶粘贴在包被质控线和检测线的硝酸纤维素膜的一端(重叠长度为0.2cm),然后在包被质控线和检测线的硝酸纤维素膜的另一端上用双面胶粘贴结合垫的一端(重叠长度为0.2cm),将结合垫的另一端上用双面胶粘贴样品垫(重叠长度为0.2cm),最后将它们用双面胶粘贴在塑料背板(如pvc底板)上,切成宽度为3mm的检测新型冠状病毒抗体的荧光免疫层析试纸。将该检测新型冠状病毒抗体的荧光免疫层析试纸用塑封袋密封后放干燥盒保存备用。检测新型冠状病毒抗体的荧光免疫层析试纸的结构示意图见图1。根据需要,还可以在样品垫上设置加样孔。四、检测新型冠状病毒抗体的荧光免疫层析试纸的使用方法和判断标准取检测新型冠状病毒抗体的荧光免疫层析试纸,向样品垫(或加样孔)中加入100μl待测液(待测者血清或待测者血清稀释液),待测液被样品垫吸取后继续向上端移动,流经结合垫时与含铕时间分辨荧光微球标记的羊抗人igm抗体发生作用,然后向包被质控线和检测线的硝酸纤维素膜渗移,反应15min。用激发波长365nm的荧光手电筒照射硝酸纤维素膜。根据膜上显出的红色反应线条情况进行如下判断:1、如果在硝酸纤维素膜上的检测线和质控线处均显出红色反应线条,则待测液中含有新型冠状病毒抗体,即待测者感染新型冠状病毒;其原理为待测液中的新型冠状病毒抗体与结合垫上的含铕时间分辨荧光微球标记的羊抗人igm抗体结合形成免疫复合物,此复合物流经检测线能与新型冠状病毒np抗原结合、桥联含铕时间分辨荧光微球、因而检测线处显出红色反应线条,此复合物流经质控线能与兔抗羊igm抗体结合、桥联含铕时间分辨荧光微球、因而质控线处显出红色反应线条;2、如果仅在硝酸纤维素膜上的质控线处显出红色反应线条,则待测液中不含有新型冠状病毒抗体,即待测者没有感染新型冠状病毒;其原理为待测液中不含有新型冠状病毒抗体,所以不能与结合垫上的含铕时间分辨荧光微球标记的羊抗人igm抗体结合形成免疫复合物,含铕时间分辨荧光微球标记的羊抗人igm抗体流经检测线不能与新型冠状病毒np抗原结合、因而检测线处不显出红色反应线条,含铕时间分辨荧光微球标记的羊抗人igm抗体流经质控线能与兔抗羊igm抗体结合、因而质控线处显出红色反应线条;3、如果硝酸纤维素膜上的质控线处不显出红色反应线条,则为无效实验结果,需重新测定。需要说明的是,上述是用激发波长365nm的荧光手电筒照射硝酸纤维素膜判读结果,也可采用干式荧光检测仪检测检测线和质控线处的荧光值判读结果,具体如下:如果检测线和质控线处的荧光值均大于50,则待测液中含有新型冠状病毒抗体,即待测者感染新型冠状病毒;如果质控线处的荧光值大于50且检测线处的荧光值为50以下,则待测液中不含有新型冠状病毒抗体,即待测者没有感染新型冠状病毒;如果质控线处的荧光值为50以下,则为无效实验结果,需重新测定。实施例2、实施例1制备的检测新型冠状病毒抗体的荧光免疫层析试纸的优化本发明的发明人对结合垫进行优化,具体对制备结合垫时的硼酸缓冲液进行优化。一、硼酸缓冲液ph值的优化1、分别制备25mm硼酸缓冲液(ph6.0)、25mm硼酸缓冲液(ph6.5)、25mm硼酸缓冲液(ph7.0)、25mm硼酸缓冲液(ph7.5)、25mm硼酸缓冲液(ph8.0)、25mm硼酸缓冲液(ph8.5)、25mm硼酸缓冲液(ph9.0)和25mm硼酸缓冲液(ph9.5)。2、按照实施例1步骤一至三的方法,将步骤一中1的硼酸缓冲液分别替换为25mm硼酸缓冲液(ph6.0)、25mm硼酸缓冲液(ph6.5)、25mm硼酸缓冲液(ph7.0)、25mm硼酸缓冲液(ph7.5)、25mm硼酸缓冲液(ph8.0)、25mm硼酸缓冲液(ph8.5)、25mm硼酸缓冲液(ph9.0)和25mm硼酸缓冲液(ph9.5),其它步骤均不变,依次得到试纸1—试纸8。3、取感染新型冠状病毒的患者的血清,用pbs缓冲液稀释至10倍,得到血清稀释液。4、分别向试纸1—试纸8的样品垫(或加样孔)中加入100μl血清稀释液,反应15min,之后用激发波长365nm的荧光手电筒照射硝酸纤维素膜,观察检测线处显出的红色反应线条情况。检测结果见表1。结果表明,制备含铕时间分辨荧光微球标记的羊抗人igm抗体的溶液时,硼酸缓冲液的最佳ph值为8.0。表1试纸ph值检测线处显出的红色反应线条情况试纸16.0-试纸26.5+试纸37.0++试纸47.5+++试纸58.0++++试纸68.5++试纸79.0-试纸89.5-注:-表示没有显出红色反应线条,+表示有隐约可见微弱条带,++表示有可见条带,+++表示有可见清晰条带,++++表示条带明亮。二、硼酸缓冲液浓度的优化1、分别制备5mm硼酸缓冲液(ph8.0)、10mm硼酸缓冲液(ph8.0)、25mm硼酸缓冲液(ph8.0)、50mm硼酸缓冲液(ph8.0)、100mm硼酸缓冲液(ph8.0)、200mm硼酸缓冲液(ph8.0)和400mm硼酸缓冲液(ph8.0)。2、按照实施例1步骤一至三的方法,将步骤一中1的硼酸缓冲液分别替换为5mm硼酸缓冲液(ph8.0)、10mm硼酸缓冲液(ph8.0)、25mm硼酸缓冲液(ph8.0)、50mm硼酸缓冲液(ph8.0)、100mm硼酸缓冲液(ph8.0)、200mm硼酸缓冲液(ph8.0)和400mm硼酸缓冲液(ph8.0),其它步骤均不变,依次得到试纸a—试纸g。3、取感染新型冠状病毒的患者的血清,用pbs缓冲液稀释至10倍,得到血清稀释液。4、分别向试纸a—试纸g的样品垫(或加样孔)中加入100μl血清稀释液,反应15min,之后用激发波长365nm的荧光手电筒照射硝酸纤维素膜,观察检测线处显出的红色反应线条情况。检测结果见表2。结果表明,制备含铕时间分辨荧光微球标记的羊抗人igm抗体的溶液时,硼酸缓冲液的最佳浓度为25mm。表2注:-表示没有显出红色反应线条,+表示有隐约可见微弱条带,++表示有可见条带,+++表示有可见清晰条带,++++表示条带明亮。上述结果表明,采用实施例1的方法制备检测新型冠状病毒抗体的荧光免疫层析试纸时,最佳硼酸缓冲液为25mm硼酸缓冲液(ph8.0)。实施例3、检测新型冠状病毒抗体的荧光免疫层析试纸的准确性实验1、按照实施例1步骤一至三的方法,将步骤一中1的硼酸缓冲液替换为25mm硼酸缓冲液(ph8.0),其它步骤均不变,得到最优的检测新型冠状病毒抗体的荧光免疫层析试纸。2、随机取16名临床确诊为新型冠状病毒感染者(命名为g1-g16)的血清,分别用pbs缓冲液稀释至10倍,得到感染者血清稀释液。3、随机取15名健康人(命名为j1-j15)的血清,分别用pbs缓冲液稀释至10倍,得到健康人血清稀释液。4、向步骤1制备的荧光免疫层析试纸的样品垫(或加样孔)中加入100μl血清稀释液(感染者血清稀释液或健康人血清稀释液)反应15min,之后采用干式荧光检测仪检测检测线和质控线处的荧光值。根据荧光值进行如下判断:如果检测线和质控线处的荧光值均大于50,则血清稀释液中含有新型冠状病毒抗体,即待测者感染新型冠状病毒;如果质控线处的荧光值大于50且检测线处的荧光值为50以下,则血清稀释液中不含有新型冠状病毒抗体,即待测者没有感染新型冠状病毒;如果质控线处的荧光值为50以下,则为无效实验结果,需重新测定。检测结果见表3。结果表明,步骤1制备的荧光免疫层析试纸可以检测待测者是否为新型冠状病毒感染者,准确率达到100%。表3实施例4、检测新型冠状病毒抗体的荧光免疫层析试纸的灵敏度实验1、取临床确诊为新型冠状病毒感染者的血清,用pbs缓冲液稀释,得到血清稀释液;血清稀释液的稀释倍数为20倍、40倍、80倍、160倍、320倍或640倍。2、向实施例3中步骤1制备的荧光免疫层析试纸的样品垫(或加样孔)中加入100μl血清稀释液,反应15min,之后采用干式荧光检测仪检测检测线和质控线处的荧光值。根据荧光值进行如下判断:如果检测线和质控线处的荧光值均大于50,则血清稀释液中含有新型冠状病毒抗体,即待测者感染了新型冠状病毒;如果质控线处的荧光值大于50且检测线处的荧光值为50以下,则血清稀释液中不含有新型冠状病毒抗体,即待测者没有感染新型冠状病毒;如果质控线处的荧光值为50以下,则为无效实验结果,需重新测定。检测结果见表4。结果表明,当新型冠状病毒感染者的血清稀释倍数为640倍时,检测线和质控线处的荧光值仍均大于50。由此可见,检测新型冠状病毒抗体的荧光免疫层析试纸具有较高的灵敏度。表4实施例5、检测新型冠状病毒抗体的荧光免疫层析试纸的特异性实验1、随机取5名临床确诊为甲型流感病毒感染者(命名为l1-l5)的血清,分别用pbs缓冲液稀释至10倍,得到甲流感染者血清稀释液。2、随机取5名临床确诊为乙型流感病毒感染者(命名为y1-y5)的血清,分别用pbs缓冲液稀释至10倍,得到乙流感染者血清稀释液。3、随机取10名健康人(命名为j21-j30)的血清,分别用pbs缓冲液稀释至10倍,得到健康人血清稀释液。4、随机取5名临床确诊为新型冠状病毒感染者(命名为x1-x5)的血清,分别用pbs缓冲液稀释至10倍,得到新冠感染者血清稀释液。5、向实施例3中步骤1制备的荧光免疫层析试纸的样品垫(或加样孔)中加入100μl血清稀释液(甲流感染者血清稀释液、乙流感染者血清稀释液、健康人血清稀释液或新冠感染者血清稀释液),反应15min,之后采用干式荧光检测仪检测检测线和质控线处的荧光值。根据荧光值进行如下判断:如果检测线和质控线处的荧光值均大于50,则血清稀释液中含有新型冠状病毒抗体,即待测者感染了新型冠状病毒;如果质控线处的荧光值大于50且检测线处的荧光值为50以下,则血清稀释液中不含有新型冠状病毒抗体,即待测者没有感染新型冠状病毒;如果质控线处的荧光值为50以下,则为无效实验结果,需重新测定。检测结果见表5。结果表明,只有加入新型冠状病毒感染者的血清时,检测线和质控线处的荧光值仍均大于50。由此可见,检测新型冠状病毒抗体的荧光免疫层析试纸具有较高的特异性。表5当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1