(E,E)-1,1′-双(2-吡啶乙烯基)二茂铁作为电化学传感器的应用
本发明属于快速检测分析技术领域,具体涉及(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁作为质子电化学传感器的应用,尤其是用于有机相质子性酸浓度的快速检测。
背景技术:
由于二茂铁衍生物在超分子化学、电子传输材料及非线性光学材料等方面巨大的潜在应用,使得对二茂铁衍生物的设计合成及性质研究日益繁荣。
在超分子化学研究中,对底物分子、离子结合片段的合适部位引入二茂铁基团,可使得该主体分子能够利用二茂铁中心良好的氧化还原性质,用来电化学识别特定客体底物。其中含有二茂铁基的共轭体系结构为端基间的电子传递提供了可能性,这使得此类化合物表现出优异的电子传输能力。尽管已报道大量具各种官能团二茂铁基主体化合物,用于各类金属离子、阴离子的识别检测,但是对结合单元以烯键直接与二茂铁片段相连的主体化合物却依然少有报导。
当客体与主体分子结合时,会造成主体化合物分子微环境的改变,引发电化学响应基团的电化学响应,通常以响应基团电位或电流值的改变。beer等人([1]p.d.beer,p.a.gale,g.z.chen,j.chem.soc.,daltontrans.,(1999)1897.)研究表明,键合的客体对主体分子氧化还原活性中心的影响主要通过以下方式起作用:(1)空间的静电微扰;(2)通过联结氧化还原活性中心和键合部位的共轭基团传递;(3)被络合的客体与属于环结构组成部分的氧化还原活性中心的金属离子间直接的相互作用。这些结合信息可通过二茂铁基的表达,利用电化学仪器、技术进行宏观的检测,从而达到识别的目的。常用的电化学监测方法有循环伏安法(cv)、差示脉冲伏安法(dpv)、方波伏安法(swv)、电阻抗法等。在主体化合物中加入客体前后氧化还原过程和主客体间结合解离过程中,kred为中性主体与客体间的结合稳定常数,kox为处于氧化状态的主体分子与客体间的络合稳定常数,e0h、e0hg分别为自由主体分子和主客体结合物的氧化还原峰电位。其有如下关系
δe0=e0hg-e0h=(rt/nf)×ln(kred/kox)
可以预料:当加入正电荷客体时,由于主客体间的空间静电排斥作用,kox应小于kred,这即是配体与阳离子作用导致二茂铁基配体fc+/fc电对式量电位阳极移动的原因;这里δe0值的大小,直接反映了二茂铁中心氧化前后主体分子与客体分子间结合能力的改变,这对发展分子开关器件有着重要意义。
在主客体作用循环伏安(cv)曲线中,较大的δe0(通常大于100mv)值往往给出cv曲线的双波行为,以1986年,saji(t.saji,j.kinoshita,j.chem.soc.,chem.commun.,1986,716.)报道的含二茂铁的大环冠醚类配体为例,在报道中的实列中其与阳离子na+间相互作用会引起fc+/fc电对氧化还原电位的阳极移动,并且随着na+的加入,在较高电位区出现一新峰且伴随着原氧化还原峰的消退;当加入1当量na+后导致了原峰的消失,阳极方向的新峰得到完全的发展;在0.5当量na+的存在下,其循环伏安表现显著的双波行为。
本申请附图8中,可以看到随高氯酸的加入,在较高电位区出现新的氧化还原峰且伴随着原主体分子的氧化还原峰的消退;随着高氯酸量的越来越大高电位处出现的新峰逐渐发展,而原主体分子氧化还原峰则逐渐消失,当主体分子与客体分子结合达到饱和状态后,阳极方向的新峰得到完全的发展,而对应原主体分子的氧化还原峰则彻底消失。这与saji的报道中大环冠醚对na+识别的循环伏安行为曲线结果类似。当体系的的δe0大于100mv时,在电化学检测时,对应自由主体分子和主客体结合物的氧化还原峰会具有较好的分离度,这给分别准确测定相应氧化还原峰的峰电流提供了可能,这类体系可以用来发展电流安培传感器用于客体粒子的电化学识别及含量检测。
本申请设计以1,1’-二茂铁双亚甲基三苯基季鏻碘盐为原料,与2-吡啶甲醛反应制得了(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁,在这一双臂型二茂铁烯烃化合物中,由于分子中吡啶氮原子具有很好的碱性,易于和有机相质子性酸的质子结合从而质子化,这导致了整个分子的变化,可以预料由于烯键的存在,使得二茂铁基团和吡啶构成了一个巨大的的共轭体系,而吡啶氮原子的质子化导致的吡啶环电子状态的变化,必然会通过共轭结构的电子传递传输,反馈到二茂铁中心,从而改变二茂铁的氧化还原电位,进而通过电化学检测实现质子结合过程的电化学信号的输出。这种客体质子性酸的质子与主体分子(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁的结合作用可利用循环伏安、dpv等电化学方法监测。以其作为有机相质子性酸电化学传感器应用于有机相质子性酸[h]+的快速电化学检测,记录电化学检测所得对应氧化还原峰峰电流,做酸浓度与峰电流关系曲线,获得传感器检测酸浓度的标准曲线,将待测液与所制试剂盒按比例混合,记录电化学检测所得到氧化还原峰峰电流,通过标准曲线可换算出将待测液酸值。(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁作为质子电化学传感器用于有机相质子性酸浓度测定,其灵敏度高,制作简单、使用方便、解决了传统滴定操作人为影响大、对操作人员操作技能高、低浓度时误差大乃至无法检测的问题。
技术实现要素:
本发明目的在于克服现有技术缺陷,提供一种(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁作为质子电化学传感器用于有机相质子性酸(如对甲苯磺酸、或高氯酸等)浓度的快速检测,其具有灵敏度高,制作简单、使用方便等优点,解决了传统滴定操作存在人为影响大、低浓度时误差大乃至无法检测的缺陷。
为实现上述目的,本发明采用如下技术方案:
(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁作为有机相质子性酸电化学传感器的应用,所述(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁的结构式如下所示:
具体的,所述(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁经下述步骤制备获得:
1)将碘化钾、1,1’-二茂铁基二甲醇和三苯基膦加至盛有水、氯仿和冰醋酸的圆底烧瓶中,加热回流30-40h;减压蒸出有机溶剂,得黄色固体,经洗涤,真空干燥得二茂铁双亚甲基三苯基鏻碘盐;
2)称取二茂铁双亚甲基三苯基鏻碘盐和叔丁醇钾于圆底烧瓶中,避光、室温氮气氛围搅拌条件下加入无水thf(四氢呋喃),20-40min后加入含有2-吡啶甲醛的无水thf溶液,室温反应1-3h,然后回流条件下反应10-14h,减压蒸出有机溶剂,残留物中加入饱和食盐水,用ch2c12萃取,有机相用无水na2so4干燥,减压蒸出溶剂,分离纯化即得。
上述(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁作为有机相质子性酸电化学传感器的应用,具体的,可以将(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁和支持电解质四正丁基高氯酸铵按比例溶于有机溶剂中,获得试剂盒。
进一步的,试剂盒中,(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁的浓度为2×10-2mol/l-2×10-5mol/l,支持电解质四正丁基高氯酸铵的浓度2×10-1mol/l。四正丁基高氯酸铵的作用在于它在有机溶剂中有很好的溶解性,为电化学检测提供导电介质,也能更好排除常见电解质阳离子和阴离子对测试体系可能带来的干扰。
进一步优选的,所述有机溶剂为乙腈、二氯甲烷、甲醇、乙醇和二甲基甲酰胺等中的一种或两种以上的混合物。溶剂的作用在于:作为(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁的溶解试剂,并利用该类溶剂与待测试样较好的混溶性,用来测定有机相质子性酸待测液。溶剂的纯度选用分析纯。
上述(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁作为有机相质子性酸电化学传感器的应用,检测时,将待测样品液与试剂盒混合,并插入参比电极、工作电极及辅助电极,在三电极体系条件下,用电化学工作站以循环伏安法或差示脉冲伏安法等在-0.2-1.3v电压范围内对测试体系进行测定。记录电化学检测对应所得的氧化或还原峰电流,依据标准曲线计算出待测样品液中的有机相质子性酸浓度(如对甲苯磺酸、或高氯酸等)。
标准曲线制作如下:配制准确浓度的对甲苯磺酸或高氯酸的标准溶液,取一定量标准溶液和试剂盒混合,利用三电极体系测试,记录电化学检测对应所得氧化还原峰的峰电流,作酸浓度与峰电流的关系曲线,获得传感器检测酸浓度的标准曲线;向试剂盒中加入待测样品液,相同条件下进行测定,记录电化学检测对应所得氧化还原峰的峰电流,带入标准曲线得出待测样品液中的有机相质子性酸浓度。
(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁作为有机相质子性酸电化学传感器的应用中,当逐量加入质子性酸时,其cv曲线表现出良好的双波行为(见附图8、10);且较大的式量电位移动值,使得(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁作为电流安培传感器实现质子性酸的定量检测成为了可能。本申请利用精确度较高的dpv法,对不同当量质子性酸进行了存在时体系实验,其结果如附图3、9所示。在dpv曲线中,以峰电流值与加入质子性酸与配体计量比做关系曲线,从关系曲线中可以看出,随质子性酸的加入,峰电流的变化值与加入量成良好相关性,直至质子性酸与(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁达到2:1当量时峰电流达到最大值。
本发明中,(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁为有机相质子性酸电化学传感器,利用其与有机相质子性酸的结合可造成二茂铁的氧化还原电位及氧化还原峰电流的改变,体系中酸的含量与氧化还原峰峰电流的改变呈较好线性关系,由此来实现质子性酸含量的测定。
本发明采用(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁作为电化学传感器,利用分子中吡啶环n原子质子化后造成二茂铁中心氧化还原电位的正向移动,随着质子化程度的增大原二茂铁中心氧化还原峰电流逐渐降低,而在更高的电位处位置得到的新峰的峰电流逐渐增大,直至质子化全部完成,这时达到质子酸浓度检测上限,检测上限受传感器(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁浓度限定,传感器浓度越大检测上限越高,传感器浓度越小检测灵敏度越高。使用中,可配置(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁10-2mol/l-10-5mol/l的梯度溶液,将待测样品液先与低浓度传感器溶液混合测试,如只观察到对应质子化后电位处氧化还原峰,则说明已达该浓度检测上限,进一步换更高浓度传感器试剂盒,至出现双波,记录新峰峰电流及低电位处旧峰电流。此时做该浓度下标准酸浓度与峰电流关系标准曲线,通过作图可得到待测样品液中的质子酸浓度。和现有技术相比,本发明的有益效果如下:
检测试剂盒制作简单、使用方便、测试范围广、无需专业人员操作,特别适用于有机相体系质子性酸含量的测定。在给出实施例中,质子酸检出浓度下限达2.4×10-6mol/l,可很好用于有机相质子性酸浓度测定。在测定环境下酸浓度50倍的k+、ca2+、mg2+以及酸浓度10倍的mn2+、co2+、ni2+、cd2+对酸浓度的测定无干扰。本发明解决了传统滴定操作人为影响大、对操作人员操作技能高、低浓度时误差大乃至无法检测的问题,在快速检测有机相质子性酸含量应用领域中具有重要的应用价值。
附图说明
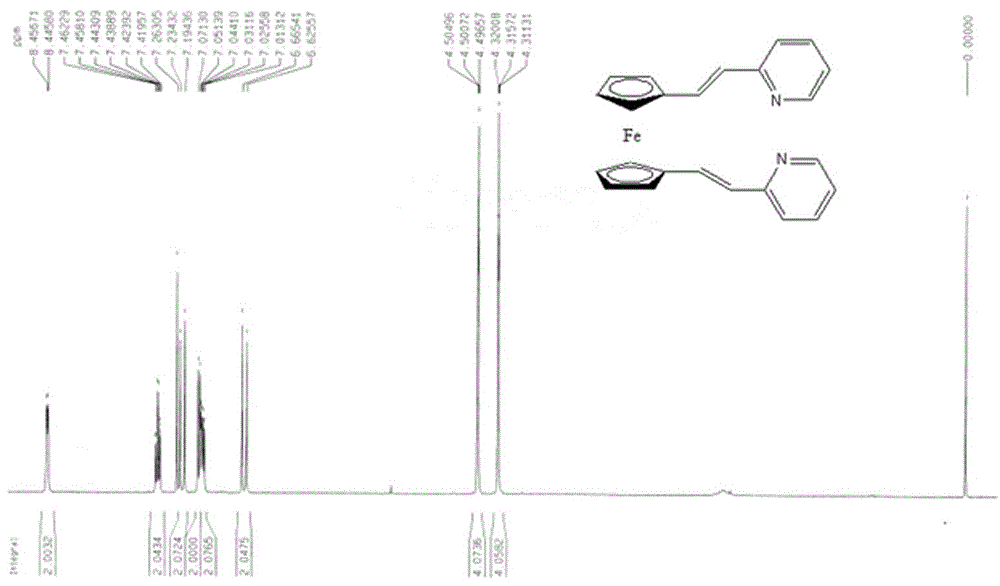
图1为(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁(lig)的核磁共振氢谱图;
图2为(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁(lig)在4当量的不同金属离子、对甲苯磺酸和高氯酸下循环伏安法(cv)测试结果对比图;
图3为(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁(lig)在不同当量高氯酸下差示脉冲伏安法(dpv)测试结果;
图4为差示脉冲伏安法(dpv)(lig)峰的峰电流与hclo4浓度关系曲线;
图5为差示脉冲伏安法(dpv)(lig+hclo4)峰的峰电流与hclo4浓度关系散点图;
图6为差示脉冲伏安法(dpv)(lig+hclo4)峰的峰电流与hclo4浓度关系曲线;
图7为(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁对5ml浓度为3.2×10-3mol/l的hclo4溶液差示脉冲伏安法(dpv)测试结果;
图8为(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁(lig)在不同当量高氯酸下循环伏安(cv)测试结果;
图9为(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁(lig)在不同当量对甲苯磺酸(tsoh)下差示脉冲伏安法(dpv)测试结果;
图10为(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁(lig)在不同当量对甲苯磺酸(tsoh)下循环伏安法(cv)测试结果。
具体实施方式
以下结合实施例对本发明的技术方案作进一步地详细介绍,但本发明的保护范围并不局限于此。
下述实施例中,(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁可通过以下方法制备获得:
将16.6g碘化钾、4.92g1,1’-二茂铁基二甲醇和17.6g三苯基膦加至盛有20ml水、60ml氯仿和30ml冰醋酸的250ml的圆底烧瓶中,加热回流36h,反应瓶中有大量黄色晶体析出,减压蒸出有机溶剂,得大量黄色固体,抽滤,滤饼依次用3×20ml二次水、3×10ml无水乙醇、3×10ml无水乙醚洗涤,真空干燥得二茂铁双亚甲基三苯基鏻碘盐黄色晶体19.2g(产率97%)。
室温下手套箱里,称取6.0g二茂铁双亚甲基三苯基鏻碘盐和1.5g叔丁醇钾于100ml的圆底烧瓶中,避光、室温氮气氛围剧烈搅拌条件下,向体系中加入40ml无水thf(反应液呈暗红色),30min后将含有13.5mmol2-吡啶甲醛的无水thf溶液逐滴加入反应体系,滴加完毕室温反应2h,然后回流条件下反应过夜(12h)。反应液减压蒸出有机溶剂,残留物中加入饱和食盐水,用ch2c12萃取,有机相用无水na2so4干燥过夜,减压蒸出溶剂,得深红色粘稠物,以ch2cl2/ch3cooc2h5(v/v=5:1)混合溶剂为洗脱剂进行硅胶柱色谱分离,得目标产物;暗红色粉末状晶体0.823g,yield:35%;m.p.:160-162ºc;hrms:cacldforc24h21fen2[m+h]+393.1054,found393.1052;irνmax(kbr):1632,1582,1469,1427,963,768cm-1;1hnmr(400mhz):4.32(t,j=1.7hz,4h,cp-h),4.50(t,j=1.7hz,4h,cp-h),6.65(d,j=16.0hz,2h,olefinich),7.01-7.07(m,4h,ar-h),7.21(d,j=16.2hz,2h,olefinich),,7.42-7.46(m,2h,ar-h),8.45(d,2h,j=4.4hz,ar-h);13cnmr(100mhz):68.60,70.75,83.15,120.98,120.99,126.06,130.75,136.35,149.26,155.82;esi-ms:[m+h]+:393.1,[m+na]+:415.0。核磁共振氢谱图详见图1。
金属离子识别和竞争实验:
在电解池中加入配好的(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁的乙腈溶液(1×10-3m),金属离子(以其高氯酸盐的形式)的乙腈溶液(0.2m)由微量进样器加入,加入量为4当量(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁量;电化学测试用chi-650a型综合电化学工作站(上海晨华公司)测定,三电极体系,工作电极为φ3mm的玻碳电极,辅助电极为铂丝,参比电极为232型甘汞电极;工作电极在使用前先经0.05μma12o3抛光粉研磨抛光至镜面,再依次用0.1mnaoh、体积l:1的浓hno3和水、无水乙醇、二次蒸馏水超声清洗;在0.00~0.90v电位范围内、电位扫描速率为100mv/s的条件下利用循环伏安法进行测定。
结果显示:除ca2+、mg2+几乎无响应外,当加入mn2+、co2+、zn2+、cd2+于(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁的乙腈溶液中,所选过渡金属离子均改变了二茂铁中心氧化还原性质(见附图2),导致了二茂铁fc/fc+电对式量电位产生的阳极移动,且电对仍表现出较好的可逆性。尽管mn2+、co2+、zn2+、cd2+有一定电化学响应,但其fc/fc+电对式量电位变化值显著小于质子性酸高氯酸、对甲苯磺酸对fc/fc+电对式量电位的影响值。当同时加入(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁2当量的高氯酸和100当量的ca2+或mg2+时,其氧化还原式峰形仍表现和2当量的高氯酸存在下相同。当同时加入(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁2当量的高氯酸和20当量的mn2+、co2+、zn2+或cd2+时,氧化还原式峰形仍表现和2当量的高氯酸存在下相同,这表明(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁在所测试这些金属离子的存在下,选择性识别质子性酸。
其对于高氯酸、对甲苯磺酸在乙腈溶液里识别检测结果如下实施例所示。
实施例1:
一种有机相质子性酸电化学传感器及其检测方法:
传感器(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁(lig)溶液制备:以乙腈为溶剂,配制含2×10-1mol/l四正丁基高氯酸铵和2×10-3mol/llig的溶液;将配制好的溶液取5ml装瓶作为试剂盒供检测使用;
配置高氯酸的乙腈标准溶液:0mol/l、5×10-4mol/l、1×10-3mol/l、1.5×10-3mol/l、2×10-3mol/l、2.5×10-3mol/l、3×10-3mol/l、3.5×10-3mol/l、4×10-3mol/l、4.5×10-3mol/l、5×10-3mol/l,分别取5ml装瓶供标定标准曲线使用;
电化学测试用chi-650a型综合电化学工作站(上海晨华公司)测定,三电极体系,工作电极为φ3mm的玻碳电极,辅助电极为铂丝,参比电极为232型甘汞电极;工作电极在使用前先经0.05μma12o3抛光粉研磨抛光至镜面,再依次用0.1mnaoh、体积l:1的浓hno3和水、无水乙醇、二次蒸馏水超声清洗。
在0.00~0.90v电位范围内,将配置好的5ml试剂盒和5ml高氯酸的乙腈标准溶液等体积混合,利用差示脉冲伏安法(dpv,操作参数如图3右侧栏中所示)进行传感器对不同高氯酸酸浓度响应的测定。结果如图3所示。从图3中可以看出,在dpv曲线中,随着高氯酸的量的增大,质子化程度的增大,原配体二茂铁中心氧化还原峰电流逐渐降低,而在更高的电位位置处得到的新峰的峰电流逐渐增大,直至酸与配体2:1当量时质子化全部完成,这时对应原配体二茂铁中心氧化还原峰彻底消失,达到质子酸浓度检测上限。
进一步,对所得的dpv测试结果进行处理,在hclo4浓度0-1.5×10-3mol/l范围内,以对应(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁(lig)峰(低电位处峰)的峰电流为纵坐标,以hclo4浓度为横坐标,作图,得图4,从图4中可以看出:在该浓度区间,对应lig的峰的峰电流与高氯酸浓度呈现较好的线性关系。
在hclo4浓度2×10-3-5×10-3mol/l范围内,以对应(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁与hclo4的加合物(lig+hclo4)峰(高电位处峰)的峰电流为纵坐标,以hclo4浓度为横坐标,作图得散点关系图-图5。从图5中可以看出,当高氯酸浓度达到4×10-3mol/l后,在该状态下(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁(lig)与高氯酸已经完全形成了稳定加合物,并达到测试上限,更高的酸浓度并不能够使峰电流得到进一步明显提高。
在hclo4浓度0-4×10-3mol/l范围内,以(lig+hclo4)峰(高电位处峰)的峰电流为纵坐标,以hclo4浓度为横坐标,作图,得图6。从图6中可以看出:在该浓度区间,对应(lig+hclo4)峰的峰电流与高氯酸浓度呈现较好线性关系。
进一步,本申请配置5ml浓度为3.2×10-3mol/l的hclo4溶液,然后与5ml试剂盒等体积混合,利用差示脉冲伏安法(dpv)进行传感器对高氯酸酸浓度响应测定,其结果如图7所示;记录峰电流2.647e-05,代入图6所示标准曲线的线性关系式(y=0.0091x-3e-06)进行求算,得到检测的浓度结果为3.24×10-3mol/l,其偏差为1.25%,结果令人满意。
实施例2:
一种有机相质子性酸电化学传感器及其检测方法:
传感器(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁(lig)溶液制备:以乙腈为溶剂,配制含2×10-1mol/l四正丁基高氯酸铵和2×10-3mol/llig的溶液;将配制好的溶液取5ml装瓶作为试剂盒供检测使用;
配置高氯酸的乙腈标准溶液0mol/l、5×10-4mol/l、1×10-3mol/l、1.5×10-3mol/l、2×10-3mol/l、2.5×10-3mol/l、3×10-3mol/l、3.5×10-3mol/l、4×10-3mol/l,分别取5ml装瓶供标定标准曲线使用;
电化学测试用chi-650a型综合电化学工作站(上海晨华公司)测定,三电极体系,工作电极为φ3mm的玻碳电极,辅助电极为铂丝,参比电极为232型甘汞电极;工作电极在使用前先经0.05μma12o3抛光粉研磨抛光至镜面,再依次用0.1mnaoh、体积l:1的浓hno3和水、无水乙醇、二次蒸馏水超声清洗。
在0.00~0.90v电位范围内,将配置好的5ml试剂盒和5ml高氯酸的乙腈标准溶液等体积混合,利用循环伏安法(cv,操作参数如图8右侧栏中所示)进行传感器对不同高氯酸酸浓度响应的测定。结果如图8所示。从图8中可以看出,在cv曲线中,随着高氯酸的量的增大,质子化程度的增大,原配体二茂铁中心氧化还原峰的峰电流逐渐降低,而在更高的电位位置处得到的新的氧化还原峰的峰电流逐渐增大,直至酸与配体2:1当量时质子化全部完成,这时对应原配体二茂铁中心氧化还原峰彻底消失,达到质子酸浓度检测上限。
进一步,本申请配置5ml浓度为3.0×10-3mol/l的hclo4溶液,然后与5ml试剂盒等体积混合,利用循环伏安进行传感器对高氯酸酸浓度响应测定,记录高电位处对应[lig+hclo4]氧化还原电对的氧化峰的峰电流,利用标准曲线线性关系式进行求算,得到检测的浓度结果为2.92×10-3mol/l,其偏差为2.67%,结果尚可。
实施例3:
一种有机相质子性酸电化学传感器及其检测方法:
传感器(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁(lig)溶液制备:以乙腈为溶剂,配制含2×10-1mol/l四正丁基高氯酸铵和2×10-3mol/llig的溶液;将配制好的溶液取5ml装瓶作为试剂盒供检测使用;
配置对甲苯磺酸(tsoh)的乙腈标准溶液:0×10-3mol/l、2×10-3mol/l、2.5×10-4mol/l、3×10-3mol/l、3.5×10-3mol/l、4×10-3mol/l,分别取5ml装瓶供标定标准曲线使用;
电化学测试用chi-650a型综合电化学工作站(上海晨华公司)测定,三电极体系,工作电极为φ3mm的玻碳电极,辅助电极为铂丝,参比电极为232型甘汞电极;工作电极在使用前先经0.05μma12o3抛光粉研磨抛光至镜面,再依次用0.1mnaoh、体积l:1的浓hno3和水、无水乙醇、二次蒸馏水超声清洗。
在0.00~0.90v电位范围内,将配置好的5ml试剂盒和5ml对甲苯磺酸的乙腈标准溶液等体积混合,利用差示脉冲伏安法(操作参数如图9右侧栏中所示)进行传感器对不同对甲苯磺酸(tsoh)浓度响应的测定。结果如图9所示。从图9中可以看出,在dpv曲线中,随着酸的量的增大,原配体二茂铁中心氧化还原峰电流逐渐降低,而在更高的电位处位置得到的新峰的峰电流逐渐增大,直至酸与配体2:1当量时质子化全部完成,这时对应原配体二茂铁中心氧化还原峰彻底消失,达到质子酸浓度检测上限。
实施例4:
一种有机相质子性酸电化学传感器及其检测方法:
传感器(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁(lig)溶液制备:以乙腈为溶剂,将配制成含2×10-1mol/l四正丁基高氯酸铵和2×10-3mol/llig的溶液;将配制好的溶液取5ml装瓶供检测使用;
配置对甲苯磺酸(tsoh)的乙腈标准溶液0mol/l、2×10-3mol/l、2.5×10-4mol/l、3×10-3mol/l、3.5×10-3mol/l、4×10-3mol/l,分别取5ml装瓶供标定标准曲线使用;
电化学测试用chi-650a型综合电化学工作站(上海晨华公司)测定,三电极体系,工作电极为φ3mm的玻碳电极,辅助电极为铂丝,参比电极为232型甘汞电极;工作电极在使用前先经0.05μma12o3抛光粉研磨抛光至镜面,再依次用0.1mnaoh、体积l:1的浓hno3和水、无水乙醇、二次蒸馏水超声清洗。
在0.00~0.90v电位范围内,将配置好的5ml试剂盒和标准5ml对甲苯磺酸的乙腈标准溶液等体积混合,利用循环伏安法(操作参数如图10右侧栏中所示)进行传感器对不同对甲苯磺酸(tsoh)浓度响应的测定。结果如图10所示。从图10中可以看出,在cv曲线中,随着酸的量的增大,质子化程度的增大,原配体二茂铁中心氧化还原峰电流逐渐降低,而在更高的电位位置处得到的新峰的峰电流逐渐增大,直至酸与配体2:1当量时质子化全部完成,这时对应原配体二茂铁中心氧化还原峰彻底消失,达到质子酸浓度检测上限。
本发明中,(e,e)-1,1'-双(2-吡啶乙烯基)二茂铁为有机相质子性酸电化学传感器,有机相质子性酸浓度测定在检测上限浓度范围下随着待测体系质子浓度的增大,质子化程度的增大原二茂铁中心氧化还原峰电流逐渐降低,而在更高的电位处位置得到的新峰的峰电流逐渐增大,直至质子化全部完成,通过记录不同浓度下标准酸浓度与峰电流关系标准曲线,通过检测和作图可得到未知测试样质子酸浓度。本发明其灵敏度高,制作简单、使用方便、解决了传统滴定操作人为影响大、对操作人员操作技能高、低浓度时误差大乃至无法检测的问题。
上述具体实施方式只是示例性的,是为了更好地使本领域技术人员能够理解本专利,不能理解为是对本专利保护范围的限制;只要是根据本专利所揭示精神的所作的任何等同变更或修饰,均落入本专利包括的范围。
- 还没有人留言评论。精彩留言会获得点赞!