LI-离子电池负极的稳定化的制作方法
相关申请的交叉参考
本专利申请要求2012年2月6日提交的题为“li-离子电池负极的稳定化”的美国非临时专利申请13/366,594的优先权和2011年2月7日提交的题为“包含硅负极的li离子电池的稳定化”的美国临时专利申请61/440,104的优先权,将它们明确地引入本文以作参考。
本公开内容一般涉及储能设备,更特别地涉及锂离子电池技术。
背景技术:
部分地由于锂离子(li-离子)电池相对高的能量密度、轻重量和寿命长的潜力,锂离子(li-离子)电池被广泛用于消费类电子产品。事实上,li-离子电池已经在许多应用中基本上取代了镍-镉和镍-金属-氢化物电池。尽管它们越来越商业普及,但仍需要li-离子电池的进一步开发,特别是对于在低-或零排放混合动力或全电动汽车、消费类电子产品、高效节能的货船和火车、航天和电网中的潜在应用的开发。该高功率应用要求具有比用于当前存在的li-离子电池中的那些更高的电容率的电极。
目前,碳类材料(例如,石墨)用作li-离子电池中的主要负极材料。石墨形式中的碳(c)具有约372毫安小时/每克(mah/g)的最大或理论上的电容率,但是在形成循环期间遭受显著的电容损失。显著地,在第一次充电循环期间,石墨经历高水平的不可逆性,这意味着显著量的锂离子嵌入石墨负极,但是在电池放电时不从负极脱嵌。这导致碳类材料的有限的电容。
已经在研究多种高电容的材料以克服这些缺陷。例如,硅类材料作为负极候选材料得到极大关注,因为它们显示大于常规石墨的电容率的量级的电容率。硅(si)具有所有金属中最高的理论上的电容率,封顶在约4200mah/g。不幸的是,硅遭受其自身的显著的阻碍。
si-类负极材料的首要缺点是在电池的充电循环期间分别由于锂离子合金化或去合金化而出现的体积膨胀和收缩。在一些情况下,硅类负极能够显示增加和随后减少高达约400%体积。这些由负极材料经历的高水平应变可引起对负极的不可逆的机械损害。最终,这能够导致负极和下方集电体之间的接触的损失。
因而,尽管负极材料中得到的优点,但li-离子电池在其应用中仍有一定的限制。因此,仍然存在对于改进li-离子电池中的负极的需要。特别地,实现稳定的负极性能对于许多高电容的材料仍是挑战。这些改进的负极和最终改进的li-离子电池可以开拓新的应用,如上述设想的所谓的高功率应用。
技术实现要素:
这里公开的实施方案通过提供改进的li-离子电池组件、由其制造的改进的li-离子电池以及制造和使用其的方法来解决上述需求。
在一些实施方案中,提供包括以下的li-离子电池:正极、包括活性颗粒的负极、使所述负极和所述正极进行离子连接的电解质、使所述负极和所述正极进行电隔离的隔膜和引入所述负极或所述隔膜中的至少一种氢氟酸中和剂。所述活性颗粒可以包括例如硅(si)、锗(ge)、锡(sn)、钛(ti)、铝(al)或镁(mg)中的至少一种。所述氢氟酸中和剂可以为例如氢氟酸结合性金属衍生物盐或氧化物,或具有自由电子对的路易斯碱。所述氢氟酸中和剂在不同的设计中可以(i)设置在形成所述负极的活性粉末中,(ii)是涂布在所述活性颗粒上的聚合物的一部分,(iii)集成至所述隔膜中或形成在所述隔膜上,或(iv)设置在与所述负极中的所述活性颗粒混合的粘合剂中,或者其组合。
在其它实施方案中,提供包括以下的li-离子电池:正极、包括活性颗粒的负极、使所述负极和所述正极进行离子连接的电解质和使所述负极和所述正极进行电隔离的隔膜,其中所述电解质可以由酰亚胺盐和选自由六氟磷酸锂(lipf6)、四氟硼酸锂(libf4)和高氯酸锂(liclo4)组成的组的至少一种盐的混合物形成。所述酰亚胺盐组成例如所述电解质以重量计的至少50%。在一些设计中,所述酰亚胺盐可以组成所述电解质以重量计的约75%至约90%范围内的百分比。所述酰亚胺盐可以为如下将更详细讨论的特定类别的锂化合物中的一种或多种。
在又一些其它实施方案中,提供锂离子嵌入和脱嵌的li-离子电池负极。所述li-离子负极可以包括活性材料核和至少部分包裹所述活性材料核的保护涂层,其中所述保护涂层包括耐氢氟酸渗透的材料。所述活性材料核可以包括例如硅(si)、锗(ge)、锡(sn)、钛(ti)、铝(al)或镁(mg)中的至少一种。所述保护涂层可以为包括聚合物、金属氧化物、金属氟化物、碳或其组合的li-离子可渗透的且电解质溶剂不可渗透的材料。在一些设计中,所述保护涂层可以为能够在锂化期间伸张和在脱锂期间收缩的挠性材料。在其它设计中,所述保护涂层可以形成围绕所述活性材料核的机械稳定的且可塑性变形的壳。在该情况下,li-离子电池负极可以进一步包括设置在所述保护涂层壳和所述活性材料核之间的碳类层。此外,当所述活性材料核处于脱锂状态时至少一种孔可以设置在所述保护涂层壳和所述活性材料核之间,从而适应在锂化期间所述活性材料核中的体积变化。设置在所述保护涂层壳和所述活性材料核之间的所述至少一种孔可以包括通过也设置在所述保护涂层壳和所述活性材料核之间的碳类中间材料(carbon-basedinterveningmaterial)分隔的多个孔。所述li-离子电池负极也可以进一步包括设置在所述保护涂层壳上的额外的聚合物或碳导电层。所述保护涂层壳可以提供用于形成固体-电解质中间相层的机械稳定的表面。还可以提供包括此类li-离子电池负极的li-离子电池。
附图说明
提供附图以帮助描述本发明的实施方案,并且仅为了实施方案的说明而提供,并非对本发明进行限定。
图1a-1e说明几个电解质组合物的实例和它们对铝正极的腐蚀的不同影响。
图2说明根据一个或多个实施方案的实例的负极保护涂层的配置。
图3a-3b说明分别为根据一个实施方案的碳保护涂层实例的扫描电子显微镜(sem)和透射电子显微镜(tem)图像。
图4说明根据一个或多个实施方案的负极保护涂层壳的配置实例的锂化和脱锂。
图5a-5f说明根据多种实施方案的几个不同的复合负极保护涂层的结构实例。
图6a-6c说明对图5d-5f的复合负极保护涂层的结构实例的锂化和脱锂的影响。
图7为描述根据一个或多个实施方案的图5a-5f的复合负极保护涂层的结构实例形成的图形流程图。
图8为说明根据一个或多个实施方案的形成机械稳定的负极保护涂层壳的方法实例的工艺流程图。
图9说明li-离子电池的实例,其中根据多种实施方案可以应用上述装置、方法和其它技术或者其组合。
具体实施方式
在以下描述和涉及本发明的具体实施方案的相关附图中公开本发明的方面。术语“本发明的实施方案”不要求本发明的所有实施方案包括所讨论的特征、优点、过程或操作模式,并且在不偏离本发明的范围的情况下,可以设计替代的实施方案。此外,本发明中公知的要素可能没有被详细地描述,或者可能被省略,以便使其它更相关的细节清晰。
如在上述背景技术中所讨论的,在li-离子电池中实现稳定的负极性能对于许多高电容负极材料是一种挑战。这对于很多情况适用,但并未完全理解全部情况。本发明人发现,例如,在电池电解质中的或者在li-离子电池循环期间原位产生的氢氟酸(hf)的存在成为主要的硅负极劣化的机理之一。尽管对硅的一般理解为实质上不与氢氟酸进行化学反应,所述氢氟酸通常仅除去硅的原始氧化物(nativeoxide)(sio2)而使下方的硅完好无损。在微电子工业中,例如,将浓缩的氢氟酸有目的地用于在环境条件下蚀刻氧化物而不损害下方的硅。
然而,本发明人发现,在电化学操作期间,在对应的负极偏压/电流条件下,氢氟酸蚀刻硅。例如根据以下方程式,会进行硅表面溶解的整体腐蚀反应:
si+6hf+h+→sif62-+6h++3e-(方程式1)
si+6hf+h+→sif62-+4h++h2+e-(方程式2)
其中h+表示空穴阳离子(holecation)和e-表示电子注入。示出活性材料(在该情况下为硅)产生的损失和其表面积的增加(由于形成孔和表面粗糙化)降低负极电容。
不幸的是,常规li-离子电池在通常操作期间定期生成氢氟酸。例如,氢氟酸可以以未解离或解离的形式存在于电池电解质中,或者可以形成配合物离子如hf2-或h2f3-,这些中的一些或全部将能够参与到上述溶解反应中。在许多电池设计中,用于li-离子电池的电解质由li-类盐和例如碳酸亚乙酯(c3h4o3)、碳酸二甲酯(c3h6o3)和碳酸乙基甲酯(c4h8o3)等的有机溶剂组合构成。关于离子盐,六氟磷酸锂(lipf6)由于其高导电性和迁移数(transferencenumber)而是受欢迎的。四氟硼酸锂(libf4)也是受欢迎的。然而,这些化合物在暴露于残留水分时或在电化学循环期间能够容易地产生氢氟酸。虽然之前已经表明了产生的氢氟酸会化学攻击正极材料表面,所述正极材料表面通常由与氢氟酸化学反应的公知的锂氧化物或磷酸盐构成,例如所有氧化物(例如,licoo2,或者较不常用的,limn2o4、lifepo4或lico1/3ni1/3mn1/3o2),但是之前尚未知晓氢氟酸对于负极材料也可能是有问题的。
因此,这里提供用于通过减少或防止氢氟酸蚀刻的有害效果而改进由高电容材料形成的负极的稳定性的装置、方法或其它技术。在以下描述中,仅作为说明的目的,参照硅负极材料描述几个实施方案。将了解到的是,公开的技术可以应用至各种高电容的负极材料,所述负极材料不仅包括如上所述的硅而且包括容易受到氢氟酸的电化学蚀刻或者在锂的嵌入或脱嵌期间经历显著的体积变化(例如,大于约5%)的其它负极材料。此类材料的实例包括:(i)重(和“超重”)掺杂的硅;(ii)iv族元素;(iii)与金属的二元硅合金(或混合物);(iv)与金属的三元硅合金(或混合物);和(v)与锂形成合金的其它金属和金属合金。
重和超重掺杂的硅包括用高含量的iii族元素如硼(b)、铝(al)、镓(ga)、铟(in)或铊(tl),或者高含量的v族元素如氮(n)、磷(p)、砷(as)、锑(sb)或铋(bi)掺杂的硅。通过“重掺杂”和“超重掺杂”,将理解的是掺杂原子的含量典型地在3,000份/每百万(ppm)至700,000ppm,或全部组合物的约0.3%至70%的范围内。
用于形成高电容的负极材料的iv族元素可以包括ge、sn、pb和它们的合金、混合物或复合物,通式为sia-geb-snc-pbd-ce-df,其中a、b、c、d、e和f可以是零或非零,其中d为选自元素周期表的iii族或v族的掺杂剂。
对于与金属的二元硅合金(或混合物),硅含量也可以在约20%-99.7%的范围中。此类合金(或混合物)的实例包括,但不限于:mg-si,ca-si,sc-si,ti-si,v-si,cr-si,mn-si,fe-si,co-si,ni-si,cu-si,zn-si,sr-si,y-si,zr-si,nb-si,mo-si,tc-si,ru-si,rh-si,pd-si,ag-si,cd-si,ba-si,hf-si,ta-si和w-si。此类二元合金可以掺杂(或重掺杂)有iii族和v族元素。可选地,其它iv族元素可以代替硅来用于形成类似的与金属的合金或混合物。还可以使用各种iv族元素的组合从而形成此类与金属的合金或混合物。
对于与金属的三元硅合金(或混合物),硅含量也可以在约20%-99.7%的范围中。此类三元合金可以掺杂(或重掺杂)有iii族和v族元素。其它iv族元素也可以代替硅用于形成此类与金属的合金或混合物。可选地,其它iv族元素可以代替硅用于形成类似的与金属的合金或混合物。还可以使用各种iv族元素的组合从而形成此类与金属的合金或混合物。
与锂形成合金的其它金属和金属合金的实例包括,但不限于,mg,al,ga,in,ag,zn,cd等,以及由这些金属形成的各种组合,它们的氧化物,等。
在一些实施方案中,通过使用特定的无氟(例如,无f的li盐)或热稳定的电解质盐以便不形成氢氟酸,可以实现改进的负极稳定性。例如,发现了由式rf1so2x-(li+)yza表示的类别的锂化合物当用作li-离子电池单元中的电解质时有效地防止形成氢氟酸。这里,x为c或n,a=0或1,条件是当x为c时a=1和当x为n时a=0。当a=1时,y和z可以为独立地选自由cn,so2rf2,so2r,p(o)(or)2,co2r,p(o)r2,c(o)rf3,c(o)r,由此形成的环烯基、和h组成的组的吸电子基团,条件是y和z不能同时为h。rf1、rf2和rf3可以为任选用一个以上的醚氧取代的1-4个碳的全氟烷基残基。r可以为任选用一个以上的醚氧取代的1-6个碳的烷基,或者进一步任选取代的芳基。可选地,当a=0时,y可以为由式so2rf6表示的吸电子基团,其中rf6为由式(rf4so2n-(li+)so2)mrf5表示的残基,其中m=0或1,和rf4为cnf2n+1和rf5为cnf2n+1,其中n=1-4,它们任选用一个以上的醚氧取代。
此类锂化合物电解质的实例包括以下:cf3so2n-(li+)so2cf3、cf3cf2so2n-(li+)so2cf3、cf3cf2so2n-(li+)so2cf2cf3、f3so2n-(li+)so2cf2ocf3、cf3ocf2so2n-(li+)so2cf2ocf3、c6f5so2n-(li+)so2cf3、c6f5so2n-(li+)so2c6f5或cf3so2n-(li+)so2phcf3。在一些实施方案中以0.2-3摩尔每升(m)范围的浓度使用该类锂化合物。
然而,使用cf3so2n-(li+)so2cf3和其它酰亚胺盐的挑战是它们能够腐蚀铝箔集电体。铝箔集电体普遍用于li-离子电池的正极,并且具有优于其它类型的集电体如由石墨制成的那些的优点。石墨集电体增加体积、降低导电性和热传导性,并且与al箔集电体相比进一步使电池单元(cell)组装过程复杂化。为了解决该腐蚀和仍保留用于正极中的铝箔集电体,一些实施方案使用酰亚胺盐和普通盐(例如,lipf6、libf4或liclo4)的组合。例如,已经发现,与一种以上的上述电解质化合物混和的小百分比的lipf6的(例如,约10-25%)稳定铝箔集电体免于腐蚀,而同时改进高电容的负极的稳定性。
图1a-1e说明几个电解质组合物的实例和它们对铝正极的腐蚀的不同影响。在各情况中,铝正极和锂负极,连同特定的电解质组合物以及由70重量%的碳酸亚乙酯和30重量%的碳酸亚丙酯组成的溶剂和在8重量%下的碳酸亚乙烯酯的电解质添加剂一起使用。各电池单元在80℃下退火约1小时。
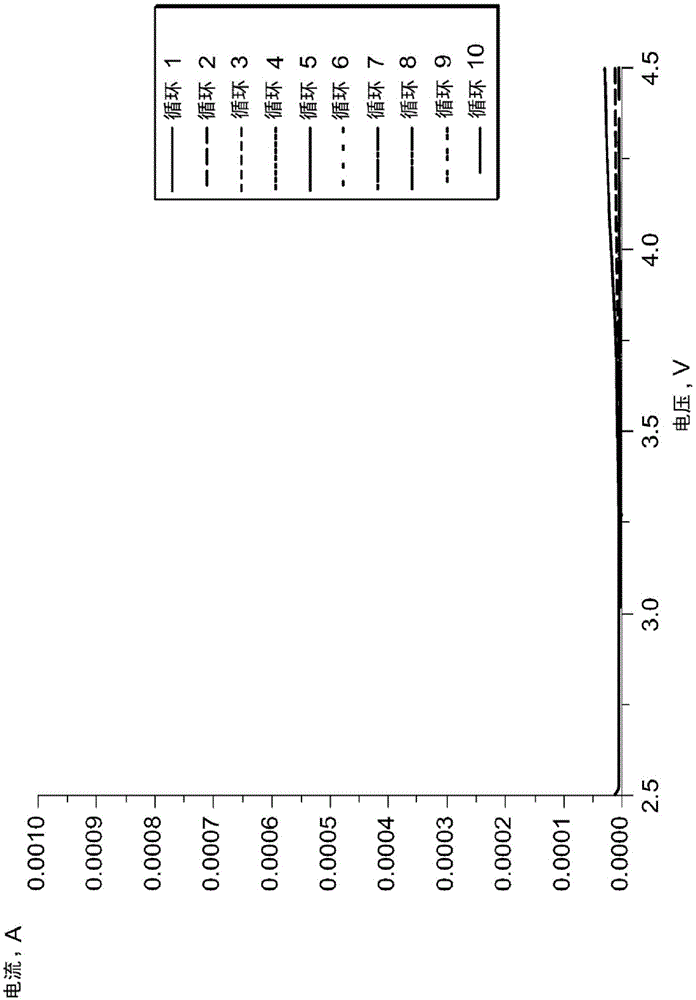
在图1a的图中,使用包括正好1m的lipf6溶液的常规电解质组合物。如从图中可以看出,在正极观察到仅很小的腐蚀电流,而腐蚀电流在重复循环时降低。然而,如上所讨论的该电解质组合物对于许多高电容的负极材料可以导致负极劣化。在图1b的图中,使用包括正好1m的酰亚胺盐(在该情况下,cf3so2n-(li+)so2cf3)的溶液的电解质组合物以改进负极稳定性。然而,与图1a的lipf6溶液相比,在正极观察到显著较大的腐蚀电流,并且没有观察到所得腐蚀电流在重复循环时降低。
在图1c的图中,少量的lipf6加入图1b的酰亚胺盐组成中从而得到约90%酰亚胺盐(在该情况下,cf3so2n-(li+)so2cf3)和约10重量%lipf6的电解质组合物。从图中可以看出,所得腐蚀电流显著低于来自纯酰亚胺盐溶液的所得腐蚀电流,并且在正极观察到仅很小的腐蚀电流,尽管观察到所得腐蚀电流在重复循环时增加。在图1d的图中,lipf6的浓度增加至约15重量%,进一步抑制所得腐蚀电流。在图1e的图中,lipf6的浓度进一步增加至约20重量%,甚至更进一步抑制所得腐蚀电流并且观察到所得腐蚀电流在重复循环时再次降低。如在这里展示的,酰亚胺盐和普通盐以适合于给定的应用的特定浓度的仔细混合可以提供在正极腐蚀和负极稳定性之间的有利折衷。
通常,酰亚胺盐可以组成电解质以重量计的至少50%,并且仍然提供上述关于改进的负极稳定性的优点。在进一步的实施方案中,已经发现在电解质以重量计的约75%至约90%的范围内的酰亚胺盐百分比是特别有利的。
除了上述特定的电解质混合物之外或者作为其代替,通过选择特别的添加剂经由化学或电化学反应中和氢氟酸可以实现改进的负极稳定性,而不牺牲自身的负极材料。例如,可以使用具有碱性的化合物以结合至氢氟酸,因而减轻对电池单元性能的负面影响。路易斯碱为可以用作能够在li-离子电池单元中结合氢氟酸的部分的化合物的示例性类别。路易斯碱通常包括能够贡献自由电子对从而形成与路易斯酸(例如并且包括氢氟酸)的路易斯加合物的任何化合物。此类路易斯碱可以包括,但不限于,胺和硼烷。用于结合氢氟酸的化合物的另一示例性类别包括形成不溶性氟化物的金属离子。此类金属离子可以包括,但不限于,二、三和四价金属离子,如钙(ca)、镁(mg)、铝(al)、铁(fe)、镍(ni)或锰(mn)离子。其它中和剂的实例(可选地称为氢氟酸清除化合物)包括添加至负极材料表面的协助捕获f-离子或另外与氢氟酸反应的官能团,如–coona或–cook基团,和其它氢氟酸结合性金属衍生物盐或氧化物。此类盐和氧化物可以由以下金属:ca,mg,ag,cu,zn,fe,ni和co的一种或多种来形成。所述盐也可以为碳酸盐、乙酸盐、藻酸盐或草酸盐。
可以将氢氟酸中和剂经由包括电解质、活性材料、对应的粘合剂材料、一种以上的电极、电池隔膜等的各种电池单元组件并且使用例如化学结合和物理共混等的各种技术,以各种形式包括以小分子的形式或以聚合物的形式引入至li-离子电池单元。以下描述几个实例。
在一些实施方案中,电池单元电解质可以直接注入有一种上述中和剂。例如,路易斯碱可以溶入电池单元电解质。聚合物和低分子量物质均可以使用。利用叔胺可以有利于一些应用,因为它们不包含连接至氮的氢原子,这可以引起电解质分解。此类胺可以为脂族、芳族或它们混合的结构。实例包括,但不限于,三烷基胺、n-烷基(芳基)哌啶、n-烷基(芳基)吗啉、n,n-二烷基苯胺、n-烷基-n,n-二芳基胺、三芳胺、吡啶和烷基(芳基)取代的吡啶、喹啉及其衍生物等。也可以使用携带胺部分的聚合物。实例包括,但不限于,聚丙烯酸酯、聚甲基丙烯酸酯、聚苯乙烯的氨基衍生物、聚乙烯基吡啶等。
在其它实施方案中,可以将某些电池单元材料(例如,电极)的表面改性以携带至少一种氢氟酸中和剂基团。例如,可以通过与n,n-烷基(芳基)丙基三乙氧基硅烷的反应产生化学结合至基底表面的氨基来使金属氧化物、磷酸盐和硅改性。可以调整反应条件如水分浓度、有无酸性催化剂等以便获得单一的单层涂层或厚的涂层(例如,约2nm至约50nm)。
类似的,任何粉末基底的表面可以覆盖有包含氢氟酸中和剂基团的聚合物的薄层。为制造该聚合物,涂层颗粒可以分散在包含要涂布的聚合物的溶剂中。通过将非溶剂性的聚合物加入分散液中,聚合物可以沉淀至颗粒表面上。通过改变聚合物和颗粒浓度可以实现期望的涂层厚度。如上文所述,此类聚合物的实例包括,但不限于,聚丙烯酸酯、聚甲基丙烯酸酯、聚苯乙烯的氨基衍生物、聚乙烯基吡啶、壳聚糖、壳质(chitin)、聚乙烯亚胺、聚烯丙胺等。
可选地,可以将携带自由电子对的成分(路易斯碱)在粉末基底的合成期间引入至此类粉末基底。例如,通过在合成期间添加硼或氮前体至碳源气体,硼或氮可以用于掺杂碳颗粒。
在又一些其它实施方案中,中和剂基团可以连接至粘合剂。例如,在li-离子电池单元制备中利用的聚合物粘合剂可以用于在其结构中携带一个以上的中和剂基团。这些基团可以为固有地存在于适当选择的聚合物(例如,壳聚糖、壳质、聚苯乙烯的氨基衍生物、聚乙烯基吡啶、聚乙烯亚胺、聚烯丙胺、聚(n,n-二烷基氨基甲基丙烯酸酯等)中,或者可以通过经由化学改性人为引入至粘合剂分子中。例如,聚合物分子中存在的环氧基团可以与各种仲胺和伯胺反应,使胺部分进入聚合物分子。
在又一些其它实施方案中,电池隔膜可以用作携带中和剂基团的载体。例如,中和剂基团或颗粒可以化学结合至隔膜的对应表面,或者浸入隔膜。可以化学结合至隔膜表面或颗粒表面的基团的实例可以源自,但不限于,三烷基胺、n-烷基(芳基)哌啶、n-烷基(芳基)吗啉、n,n-二烷基苯胺、n-烷基-n,n-二芳基胺、三芳胺、吡啶和烷基(芳基)取代的吡啶、喹啉及其衍生物等。也可以使用携带胺部分的聚合物。它们可以以聚合物溶液的形式浸入隔膜,或者隔膜可以浸渍有纳米颗粒。聚合物的实例包括,但不限于,聚丙烯酸酯、聚甲基丙烯酸酯、聚苯乙烯的氨基衍生物、聚乙烯基吡啶、壳聚糖、壳质、聚乙烯亚胺、聚烯丙胺、聚(n,n-二烷基氨基甲基丙烯酸酯)等。
例如,对所选择材料的改性而不是注入电解质对于一些应用可以是有利的,原因在于其使中和剂局限于电池单元中的特定区域,如负极,其中可以利用不同的化学。例如,可以使聚合物携带的路易斯碱不溶于电池单元电解质,并且与粘合剂共混入负极组合物。在该情况下,可以将氢氟酸结合性引入至电极并且局限于电极空间。局限于特定区域使得利用在其它电池单元组件中不期望的化学化合物。例如,胺局限于负极区域能够防止不期望的副反应,否则胺可能在li-离子电池单元的正极上被氧化。
除了上述特定的电解质和添加剂化合物之外或者作为其代替,通过将保护涂层或膜施涂至负极材料的表面可以实现改进的负极稳定性。保护涂层可以由为了减少或防止活性负极材料的氢氟酸蚀刻而特别选择的材料形成,或者包括上述材料,所述材料例如选择的聚合物、氧化物、卤化物(如氟化物或氯化物)、卤氧化物(如氟氧化物或氯氧化物)、碳、其组合或其它材料。为了li-离子电池的有效操作,使保护涂层为li-离子可渗透的。期望地,并且至少在一些设计中,还使保护涂层为耐电解质溶剂渗透的(如果不是不可渗透的话)。
图2说明根据一个或多个实施方案的负极保护涂层的配置实例。在该实例中,负极200通常由包括硅活性材料204和粘合剂208的电互相连接的颗粒的基质形成。在硅类负极中,粘合剂208结合至硅204并且提供稳定性。其通过有助于更稳定的固体-电解质中间相(interphase)(sei)的形成可以增强负极的性能,所述更稳定的固体-电解质中间相(sei)的形成使得由于伴随硅和锂的电化学合金化(和去合金化)产生的体积变化引起的不可逆的电容损失最小化。用于硅类负极的常规粘合剂典型地为羧甲基纤维素(cmc)和聚(偏二氟乙烯)(pvdf),但是如有需要,可以使用其它材料。其它实例包括,但不限于,聚丙烯酸、或藻酸的金属盐,所述藻酸的金属盐可以包括例如,li+,na+,k+,mg2+,ca2+,al3+,ti4+,sn4+等的金属阳离子。在示出的设计中,负极200还包括用于在电池的初始循环期间将硅204和粘合剂208之间的至少一部分界面密封的碳导电性添加剂212。
负极结构200进一步包括至少部分包裹硅204、粘合剂208和导电添加剂212的上述类型的保护涂层220。正如所示的,保护涂层220可以粘附至负极200的表面上并且起到电解质和任何其中包含的氢氟酸的阻隔层(同时保持对li离子可透过)的作用,防止劣化硅活性材料204。如上所讨论的,保护涂层220可以由选择的聚合物、氧化物、氟化物、碳、其组合或其它材料来形成。
图3a-3b说明分别为根据一个实施方案的碳保护涂层实例的扫描电子显微镜(sem)和透射电子显微镜(tem)图像。在该实例中,硅涂布的垂直排列的碳纳米管(vacnt)用作负极材料,然后进一步涂布有用作保护涂层的无定形碳层从而预防氢氟酸蚀刻。正如所示的(和进一步从x-射线衍射研究中显然的),粗糙的、珠状的硅涂布的vacnt结构在沉积之后变平滑,并且硅结晶。外部碳涂层耐氢氟酸蚀刻并且增强在锂化和脱锂期间的硅的结构完整性或导电性。另外,确保了在由于硅的多晶结构而导致各向异性方式中仍然出现孔形成。通过调整此类外部碳涂层的厚度,可以将通过此类外部碳涂层提供的耐氢氟酸蚀刻调整至特定的环境。
在一些实施方案中,使保护涂层为挠性的以致其能够在锂化和脱锂期间与负极活性材料一起膨胀和收缩。例如,保护涂层可以由能够自身滑动的聚合物链制成。其它实例包括在表面上自然形成氧化物保护层的金属。这些包括,但不限于,铝(al)、钛(ti)、铬(cr)、钽(ta)、铌(nb)等。使用多种氧化物涂层沉积技术可以进行此类涂层的沉积,所述多种氧化物涂层沉积技术包括物理气相沉积、化学气相沉积、磁控溅射、原子层沉积、微波辅助的沉积、湿式化学等。
例如,水溶性盐形式的金属氧化物前体可以加入到要涂布的颗粒的悬浮液(水中)。碱(例如,氢氧化钠或胺)的添加引起金属(me)氢氧化物的形成。然后悬浮在混合物中的活性颗粒可以起到me-氢氧化物沉淀的成核位点的作用。一旦颗粒涂布有me-氢氧化物的壳,则可以将它们退火以便使氢氧化物壳转变为对应的氧化物层,然后所述氧化物层良好地粘附至颗粒表面。
在其它实例中,氧化铝涂层可以使用根据以下步骤的湿式化学技术来生产:(i)将异丙醇铝溶解于乙醇中;(ii)在活性硅颗粒的存在下干燥该溶液;和(iii)退火以将异丙醇铝涂层转变为氧化铝涂层。在又一些其它实例中,氟化铁涂层可以使用根据以下步骤的湿式化学技术来生产:(i)将铁(fe)粉溶解于氟硅酸的水溶液中;(ii)在活性硅颗粒的存在下干燥该溶液,从而形成由fesif6·h2o组成的涂层;和(iii)通过在惰性环境如氩气或真空中使涂布的粉末退火而将fesif6·h2o转变为氟化铁(fefx)。
足够挠性的保护涂层的形成可以有利于在循环期间显示增加和随后减少高达约400%的体积某些像硅一样的负极材料。保护涂层的挠性防止裂缝或空隙形成,否则将使氢氟酸渗透到活性材料。
然而,在其它实施方案中,已经发现,使用机械稳定的且可塑性变形的保护涂层当被适当运用时可以提供进一步的优点。例如,壳结构可以用于覆盖或包裹负极表面。在初始嵌入(例如,li-离子电池的第一次循环)期间,此类保护涂层的外表面区域可以塑性变形并且膨胀从而匹配锂化的负极材料的膨胀状态。然而,在锂脱嵌期间,该类保护涂层仍然保持机械稳定并且很大程度上保留其膨胀状态。以这种方式,产生适合处于膨胀锂化状态的负极但却允许在脱锂期间活性材料核收缩而不碎裂的壳结构。
图4说明根据一个或多个实施方案的负极保护涂层壳的配置实例的锂化和脱锂。在该实例中,如在图2中示出的设计的情况下,负极400通常由包括硅活性材料404和如上所述的潜在的其它材料如粘合剂或碳导电性添加剂等(未示出)的电互相连接的颗粒的基质形成。将保护涂层410与负极400的任何其它材料一起设置在硅活性材料404的至少一部分上。
设计保护涂层410,以致至少在初始循环时期之后,空隙或空坑412形成在保护涂层410(处于脱锂状态)内部,这样在锂化期间为了硅404膨胀提供空间。以这种方式,保护涂层410的外表面区域可以在作为一般电池操作一部分的硅-锂膨胀(在锂嵌入期间)和收缩(在锂脱嵌期间)的后续循环期间保持基本上稳定。
sei层420也示出在图4中,其中其形成于(在初始充电时)保护涂层410上方而不是将直接形成于硅404的表面上。通过在锂嵌入/锂脱嵌期间硅颗粒的大体积变化,随着其外表面区域不断地膨胀和收缩,可能损害sei的稳定性和耐氢氟酸、溶剂分子和其它有害的组分的渗透性。该膨胀/收缩典型地引起sei缺陷和空隙的形成,这导致其耐渗透性的劣化。然而,在图4的设计中的保护涂层壳410为其上形成的sei层420提供更稳定的外表面区域的情况下,可以增强sei层420的机械稳定性。更稳定的sei层420提供针对氢氟酸蚀刻以及其它劣化处理的额外的保护。
在一些实施方案中,陶瓷涂布材料可以用于形成保护涂层410。陶瓷涂层的实例包括,但不限于:氧化铝或锂化氧化铝(lithiatedaluminumoxide)、氧化钛或锂化氧化钛(lithiatedtitaniumoxide)、氧化锌或锂化氧化锌(lithiatedzincoxide)、氧化铌或锂化氧化铌(lithiatedniobiumoxide)和氧化钽或锂化氧化钽(lithiatedtantalumoxide)。陶瓷涂层的其它实例包括,但不限于:氟化钒、氟氧化钒、氟化铁、氟氧化铁、氟化铝、氟氧化铝、氟化钛、氟氧化钛、氟化锌、氟氧化锌、氟化铌、氟氧化铌、氟化钽、氟氧化钽、氟化镍、氟氧化镍、氟化镁、氟氧化镁、氟化铜、氟氧化铜、氟化锰和氟氧化锰。这些陶瓷均是li-离子可渗透的且电解质溶剂不可渗透的,使它们非常适合于用在li-离子电池应用中。
在其它实施方案中,聚合物涂层可以用于形成保护涂层410。例如,可以将聚合物涂层施涂至硅404的表面作为牺牲层然后碳化(例如,通过热解或热退火),从而留下作为保护涂层410的碳壳。
在又一些其它实施方案中,材料的组合可以用于形成复合的负极保护涂层。因为可以设计复合物,从而利用在单独各材料中未发现的两种以上的构成材料几种不同的物理或化学性能,根据期望的应用,形成复合涂层的不同材料的适当选择和特别应用可以导致各种进一步的优点。
图5a-5f说明根据多种实施方案的几种不同的复合负极保护涂层的结构的实例。在该情况下,被保护的负极核由为了简单说明的目的作为单一的示例性硅活性材料颗粒504示出的电相互连接颗粒的基质构成。然而,将可以理解的是示例性硅颗粒504事实上可以由颗粒簇、硅复合物的部分、硅-碳复合物的部分等构成。还将可以理解的是,主要活性材料可以为除了硅以外的材料,和其它次要材料也可以包括在负极核中,例如如上所述的粘合剂或碳导电性添加剂等。
在图5a-5c示出的实例设计中,复合的保护涂层由外保护层512(在该情况下,金属氧化物或金属氟化物壳)和内保护层520(在该情况下,碳类材料)形成。金属氧化物或金属氟化物外保护层512的使用防止氢氟酸、溶剂分子和其它有害的或反应性分子的扩散,并且阻止它们到达硅活性材料504的表面。在硅活性材料504和金属氧化物或金属氟化物外保护层512之间的碳类内保护层520的使用提供电流和li离子流动的电子导电和离子导电的传导通道。碳类内保护层520还形成针对氢氟酸、溶剂分子和其它有害的或反应性分子的扩散的额外的阻隔层,进一步减少下方硅活性材料504的潜在劣化。
例如以金属氧化物或金属氟化物外保护层512的形式的作为固体和不溶性离子导体的机械稳定的外壳结构和以碳类内保护层520的形式的柔软的、挠性内涂层的组合因此提供单一、复合设计的两种材料的优点。然而,通过可以以多种形式形成具有不同性能和不同的对应优点的内保护层520的不同结构,可以实现进一步的优点。图5a-5c中示出的各种设计说明几个实例。
在图5a的设计中,内保护层520作为固体层例如电子导电和离子导电碳涂层形成。该类的致密碳层有助于削弱硅活性材料504和外保护层512的内表面之间的结合,当硅活性材料504在锂脱嵌期间在其内部收缩而使外保护层512保持膨胀和机械稳定。如上所讨论的,机械稳定的保护涂层如外保护层512提供更稳定的sei层的形成,这反过来提供针对氢氟酸蚀刻以及其它劣化处理的额外的保护。碳涂层还通常是挠性的,并且为在锂化期间下方硅活性材料504的膨胀提供一些缓冲,缓和对外保护层512的任何应力。
然而,对于一些应用,可能需要额外的膨胀容量。因此,在图5b的设计中,内保护层520作为中空层形成,具有在硅活性材料504的外表面和外保护层512的内表面上并且在其间留有空隙或孔516的碳质材料的薄涂层。孔516的额外体积提供在锂化期间用于硅膨胀的进一步空间,并且与图5a的设计中更致密的碳涂层相比,可以有助于进一步减轻可能施加在外保护层512上的任何应力。这些在硅活性材料504的外表面和外保护层512的内表面上的薄涂层仍然提供如在图5a的设计中的电子传导和离子传导中间涂层的优点,但是是在兼顾改进机械应力减少下更有限的程度上。
因此,图5c的进一步设计表示更普通的和中间的途径,形成内保护层520,其中在硅活性材料504和外保护层512的内表面之间具有一系列小孔516。将可以理解的是,孔516可能不是完美地仅配置在整个活性材料504和外保护层512的内表面之间,相反地,有时在任何电池操作期间可能进入活性材料504并形成于组成活性材料504的颗粒簇或复合物之间。该配置因为形成在硅活性材料504和外保护层512的内表面“之间”而意欲包括在上述孔516的系列中。
可以调整孔516的密度从而使其适于特别的应用(例如,特别的活性材料),并且调整至实现内保护层520中的碳量(因此,其电子导电性和离子导电性)和内保护层520中的自由空间量(因此,其在锂化和脱锂期间的膨胀容量)之间期望的平衡。关于包括硅活性材料的一些应用,已经发现了被硅活性材料核占据的体积的约50%(或更高)的孔总体积提供在锂化期间足以膨胀的空间。
图5d-5f中示出的设计实例除了它们包括在外保护层512周围额外的导电涂层524以外,分别与图5a-5c中示出的那些等同。额外的导电涂层524提供增强负极构成颗粒之间的导电性,这有助于由负极浆料形成导电负极。例如,额外的导电涂层524可以由碳或导电性聚合物形成,并且针对氢氟酸、溶剂分子和其它有害的或反应性分子的扩散提供再进一步的阻隔层,进一步减少下方硅活性材料504的潜在劣化。
图6a-6c说明对图5d-5f的复合负极保护涂层的结构实例的锂化和脱锂的影响。为简单起见,仅图5d-5f的设计明确地示出,但是图5a-5c的效果实质上是类似的。
如图6a中所示,在初始li嵌入(例如,li-离子电池的第一次充电)期间,li离子嵌入硅活性材料504从而形成si-li合金530。形成期间,其外表面区域显著地膨胀,如上所述,使碳类内保护层520偏移和压实(contact)。随后,在进一步的循环期间,li离子可以从si-li合金530中脱嵌,使其返回到其原始(native)硅状态524。根据所用的特定的内保护层520材料和经历的体积变化,内保护层520或其一部分可以保留其如上所示的压实状态。因而,在一些情况下,至少部分地可以使内保护层520压实,并且类似于上述那些的一个孔或多个孔516可以形成在中间空间(interveningspace)中。以该方式形成此类孔516对于一些应用(例如,为适应进一步的体积变化)是有利的。
谈到图6b,关于具有大孔设计的内保护层520的结构,为适应硅膨胀而提供的内在空间可以足以避免任何初始嵌入影响。在该情况下,li离子嵌入硅活性材料504形成si-li合金530,其外表面区域因此膨胀从而填充或部分填充孔516,并且在锂脱嵌期间因为si-li-合金530返回至其原始硅状态524而缩回至其原始尺寸。
谈到图6c,关于中间密度的孔的设计,形成si-li合金530的硅活性材料504的初始li嵌入和伴随的膨胀可以引起多个小孔516的偏移,正如所示的,随着它们被压实,所述多个小孔516典型地聚集在一起。随后,在进一步的循环期间,li离子从si-li合金530中脱嵌并且返回至其原始硅状态524。根据多个孔516的密度和初始配置,以及经历的体积变化,正如所示的,孔516可以返回至其原始构造和密度,或者返回至改变的构造和密度。
初始锂嵌入,如图6a和6c中示出的那样,可以以包括原位(li-离子电池单元组装之后)和异位(ex-situ)(li-离子电池单元组装之前)的多种方式进行。例如,原位锂嵌入至负极材料可以包括在li-离子电池操作期间的电化学锂嵌入,如从含li-正极材料中取出的锂的嵌入。对于异位锂嵌入至负极材料,锂化可以包括在将负极粉末组装至电极之前或在将电极组装至li-离子电池单元之前的气相反应。可选地,异位锂嵌入可以包括负极的室温锂化,根据所述负极的室温锂化,软的、稳定的(友好的室温干燥)锂粉可以沉积和铺展至预形成的多孔负极的表面以便诱发锂化(主要在与电解质接触时)。如果在溶剂存在下进行此类方法,sei层可以同时预形成在负极表面上。在一些设计中可以使用锂箔代替锂粉。
将可以理解的是,图5a-5f的不同的复合负极保护涂层结构可以以多种方式形成。以下描述形成方法的几个实例。
图7为描述形成根据一个或多个实施方案的图5a-5f的实例的复合负极保护涂层结构的图形流程图。在该实例中,形成以在步骤710中的一个或多个硅活性材料颗粒504的供应或聚集开始。而且,将理解的是硅颗粒504以单个示出仅为说明目的,并且事实上可以由颗粒簇构成,由硅复合物的部分、碳复合物的部分等形成。也将再次理解的是主要活性材料可以为除了仅作为实例示出的硅以外的材料,和其它次要材料也可以包括在负极核中,如上所述,如粘合剂或碳导电性添加剂等。
在步骤720中,例如,将牺牲聚合物涂层508施涂至硅颗粒504作为内保护层520的前体。然后,使用一种以上的已知方法,如原子层沉积(ald)、化学气相沉积(cvd)、各种湿式化学方法或本领域中其它已知的方法,牺牲聚合物涂层508和硅颗粒504在步骤730中进一步涂布有外保护层512(例如,金属氧化物或金属氟化物)。
在步骤740中,如有需要,选择图5a-5f的不同的孔设计中之一,并且在牺牲聚合物涂层508中形成。根据期望的内保护层520的结构及其关联的孔516(或者缺乏孔,视情况而定)涉及特定的处理。特别地,牺牲聚合物涂层508可以经由热处理(例如,在气态环境中的退火)、经由水热法或适合于期望结构的其它技术转变为期望的结构。根据聚合物组成和转变条件,牺牲聚合物可以转变为:(a)如在图5a的设计中的致密的碳结构;(b)如在图5b的设计中的覆盖硅颗粒504和外保护层512的内表面的碳质材料的薄层;或(c)如在图5c的设计中的多孔碳结构。
关于图5d-5f的进一步设计,在步骤750中进行额外的处理,从而例如在外保护层512的表面上形成额外的导电性聚合物或碳涂层524。关于由碳形成的额外的导电涂层524,可以通过cvd(例如,烃的气态前体的分解)、聚合物层的形成和分解、水热碳化或其它技术来沉积碳。关于由导电性聚合物形成的额外的导电涂层524,可以经由等离子体辅助的聚合、微波辅助的聚合、在要涂布的颗粒的悬浮液中的溶液聚合、或者颗粒与聚合物在溶液中或以聚合物纳米颗粒形式的接合悬浮液(jointsuspension)的喷雾干燥来沉积导电性聚合物涂层。
图8为说明形成根据一个或多个实施方案的机械稳定的负极保护涂层壳的方法实例的工艺流程图。在该实例中,由聚合物构成的牺牲涂层最初沉积在期望的活性颗粒的表面上(步骤810)。随后,使用一种以上的常规技术(其实例如上所述),将金属氧化物或金属氟化物层沉积(步骤820)。在氧化物层沉积之后,所得核-壳结构体在足够高以使中间聚合物层碳化的温度下退火(步骤830)。由于在碳化期间聚合物体积减少,可以在活性颗粒核和金属氧化物壳之间形成空隙。在聚合物碳化之后获得的薄碳层增强了在复合颗粒内的导电性。通过改变聚合物涂层的厚度和聚合物的使用类型,可以调整活性颗粒和金属氧化物层之间的自由体积量。
如通过任选的步骤815说明的,在一些实施方案中,可以使用额外的步骤以实现金属氧化物层和活性颗粒之间增强的粘合。正如所示的,在牺牲聚合物涂层沉积至活性颗粒的表面上(步骤810)之后,所得组合可以在高于聚合物的玻璃化转变温度的温度下退火(任选的步骤815)。在加热时,聚合物涂层转变为粘性液体并且从颗粒表面部分去湿(dewetts)。最初被聚合物遮蔽的颗粒表面因而露出。因而,当金属氧化物膜沉积在聚合物以及部分暴露的颗粒表面的上部(步骤820)时,去湿的颗粒区域提供在金属氧化物和颗粒表面之间的直接接触的点。随后的碳化步骤(步骤830)再次形成在金属氧化物层下的空隙,这允许在电池使用期间颗粒膨胀。
图9说明li-离子电池实例,其中根据多种实施方案可以应用于上述装置、方法和其它技术或者其组合。为说明目的,这里示出圆柱形电池,但是如有需要也可以使用其它类型的配置,包括方形的或袋形的(层压型)电池。li-离子电池1实例包括负极(negativeanode)2、正极(positivecathode)3、插入负极2和正极3之间的隔膜4、浸渍隔膜4的电解质、电池盒5和密封电池盒5的密封构件6。
将可以理解的是,li-离子电池1实例可以在各种设计中同时体现本发明的多个方面。例如,li-离子电池1可以包含下述:(a)包含通过li-离子可渗透的碳、聚合物和氧化物或氟化物壳保护的硅材料的活性负极;(b)由(i)包含酰亚胺的盐(例如,50-95%的总盐含量),(ii)基于碳酸酯的混合物的溶剂,和(iii)电解质添加剂如二甲基乙酰胺(dmac)构成的电解质;和(c)包含氧化物、氟化物或硫活性材料的正极。另一组合实例可以包括下述的使用:(a)包含通过li-离子可渗透的氧化物壳和hf-清除剂材料保护的硅活性材料的负极;(b)由(i)lipf6盐、(ii)基于碳酸酯的混合物的溶剂,和(iii)路易斯碱电解质添加剂如dmac构成的电解质;和(c)包含氧化物、氟化物或硫活性材料的正极。通常,将理解的是,如有需要可以采用上述实施方案的任何组合。
提供前面的描述以使本领域中任何熟练的技术人员进行或使用本发明的实施方案。然而,将理解的是,本发明不限于这里公开的特定的配方、过程步骤和材料,因为对这些实施方案的各种改造对本领域熟练技术人员是显而易见的。即,这里限定的通用原则可以应用至其它实施方案而没有偏离应当仅由以下权利要求和所有等同物限定的本发明的精神或范围。
- 还没有人留言评论。精彩留言会获得点赞!