一种具有结构记忆特性的细胞生长支架的制备方法与流程
本发明涉及一种应用于材料科学、组织工程学和再生医学领域的无化学交联、有生物活性、有稳定三维结构和有结构记忆特征的多孔细胞生长支架细胞生长支架的制备方法,具体的说是一种具有结构记忆特性的细胞生长支架的制备方法。
背景技术:
因病变、创伤或外科手术常致使人体软组织的缺损,使人体自身机体重新生长所需要的软组织是现代医学需要解决的一个难题。国内外已经研发出多种用于软组织缺损修复的填充材料和敷料,包括基于人工合成高分子材料和天然生物材料制备而成的水凝胶及多孔海绵类填充材料。以动物组织为原料,经过酸处理或酶处理后提纯的胶原蛋白,可以制备成胶原蛋白水凝胶,适当的化学交联处理可提高水凝胶制剂中胶原蛋白的稳定性,在体内较不易于被降解。胶原蛋白悬浮液或水凝胶可以经过冻干制备成多孔的胶原海绵材料,经过进一步的化学交联固定处理,不仅可以增进海绵材料中胶原蛋白的稳定性,同时也以保留胶原海绵材料的多孔结构特性。多孔胶原海绵材料在临床医学上已经广泛地应用于创口的止血、组织缺损部位的填充,以及药物载体等。
中国专利文献cn1235947c、cn101549171b分别提供了制备此类胶原海绵材料的具体方法。其中,cn1235947c专利文献提供的技术方案是在常温下用盐酸或醋酸溶液浸泡含有丰富胶原蛋白的动物组织(皮肤、软骨、板筋、肌腱等),酶解后获得动物组织细胞外胶原框架,研磨和匀浆处理获得胶原悬浮液,将胶原悬浮液置入模具,加压成型和冻干制备胶原海绵填充剂,在冻干前或冻干后用化学交联剂处理。专利文献cn101549171b提出了在提取出的高纯度ii型胶原溶液后,用聚乙二醇对ii型胶原溶液进行浓缩,然后用含碳化二亚胺和n-羟基琥珀酰亚胺作交联剂对浓缩后的ii型胶原进行交联,冷冻干燥制备得到的胶原海绵。
以上技术方案均采用化学交联的方式获得胶原海绵,但缺陷也是显而易见的:经酸化和酶解制备的胶原海绵稳定性差,缺少生物活性及有降解过快等缺点。
除此之外,在技术领域中也有在胶原海绵制备过程中添加透明质酸钠、壳聚糖、甲壳素、硫酸软骨素等其他生物大分子材料来制备成复合海绵材料并改善了胶原海绵的生物性能。例如,中国专利文献cn101862475b披露的技术方案是在胶原溶液中添加了透明质酸钠,经过化学交联制备得到复合的胶原材料。中国专利文献cn103007336a是在鱼皮胶原中添加了壳聚糖,冷冻干燥后经交联再进行二次冷冻干燥制备鱼皮胶原基复合海绵。尽管化学交联处理提高了胶原海绵的稳定性,含有透明质酸和壳聚糖等其他生物大分子的胶原海绵复合材料有较好的生物活性,辐射灭菌后这些海绵材料的稳定性还是明显下降,在大面积软组织填充或伤口修复时容易出现较为严重的炎症。
以上技术方案尽管仍以化学交联处理的方式提高了胶原海绵的稳定性,且含有透明质酸和壳聚糖等其他生物大分子的胶原海绵复合材料有较好的生物活性。但实践中还是存在辐射灭菌后这些海绵材料的稳定性明显下降的问题,尤其是在大面积软组织填充或伤口修复时容易出现较为严重的炎症。
美国专利文献us2012/0263763a1描述了一种基于纤维化后的脱细胞的组织基质海绵材料。制备该材料的方法是以猪皮为原料,经过去脂肪、冷冻超薄切片、脱细胞和去抗原、清洗、纤维化匀浆、病毒灭活、灭菌、以及将脱细胞基质悬浮液冻干制备成组织基质海绵材料,冻干的海绵材料可以用环氧乙烷或辐射灭菌。该方法产生的积极效果是不采用化学交联的方式,使该细胞外组织基质材料较好的保留了原来组织基质的基本结构特征;除胶原蛋白成分外,还包含其他重要的细胞外组织基质成分,如弹性蛋白、纤维蛋白,蛋白聚糖等;制备工艺中没有酸处理、酶解处理的过程,该海绵材料具有良好的生物相容性,支持宿主细胞快速生长,胶原蛋白稳定性较好,降低了炎症反应。但存在的问题是由此方法获得的该海绵材料结构强度差、弹性差,受压后容易碎和变形,且不能保持原有材料结构和不能恢复原有的形状。
总结以上文献披露的技术方法,突显的问题是:无论是使用酸解或酶解后纯化的胶原蛋白水凝胶,还是脱细胞后匀浆的组织基质材料悬浮液,在制备多孔的胶原海绵材料时,现有的技术是先将水凝胶或悬浮液冻干,再经过进一步的化学交联处理来提高材料的力学强度和增进海绵材料中胶原蛋白的稳定性,化学交联处理使组织基质材料损失了作为孔细胞生长支架原本拥有的许多优良的天然特性。
技术实现要素:
本发明所要解决的技术问题是提供一种具有结构记忆特性的细胞生长支架的制备方法,由此方法获得的支架不仅具有优良的生物兼容性和完全的生物可降解性,同时具有支持细胞生长、支持体内和体外的组织和器官生长。
为此,本发明解决所述问题的技术方案是:一种具有结构记忆特性的细胞生长支架的制备方法,其特征是,所述方法包括:步骤一,原料收集:用于制备脱细胞组织基质材料的生物组织原材料的收集,所述原材料包括但不局限于人体或动物的皮肤,软骨,血管、半月板,胃,小肠,大肠,隔膜,肌腱,韧带,神经组织,膀胱和尿道,将富含胶原蛋白的组织切割分离出来,切成1-20毫米的小块或小片;步骤二,原料消毒:将步骤一获取的小块或小片用2%碳酸钠浸泡4~48小时或用其他ph在10.5~12.5的碱性溶液浸泡;步骤三,脱细胞处理:将步骤二浸泡后的小块或小片再用0.1~2.0%的脱氧胆酸钠、聚乙二醇辛基苯基醚、或用每升10~200单位的中性酶脱细胞处理4~36小时;步骤四,脱细胞组织基质材料的清洗:将步骤三脱细胞处理后的小块或小片再用生理盐水或其他中性的渗溶液按每公斤材料1-6升冲洗2-5遍,每次1~12小时;步骤五:脱细胞组织基质绞碎:将步骤四脱细胞组织基质材料清洗后小块或小片再用绞碎机将脱细胞的组织基质材料碎磨成微纤维状或絮状的脱细胞组织基质材料;步骤六,酸化处理:将步骤五获取的微纤维状或絮状脱细胞组织基质材料浸泡在的5~200ml的、ph调至2.8~3.5的盐酸或醋酸溶液中做酸化处理1~24小时,再次将基质材料打碎研磨成水凝胶状颗粒,并用氢氧化钠溶液调节ph至4.0~6.5;步骤七,混合与注模:在20~30℃室温中按60~90%的比例混合微纤维状或絮状脱细胞织基质材料与按40~10的酸化处理的水凝胶状的脱细胞组织基质颗粒混匀后注入包装模具中;步骤八,冰冻处理:将有含有脱细胞组织基质材料悬浮液的模具放入-20℃以下的冻箱中深冻,或在第一次解冻后再次深冻提高其悬浮液空隙结构;步骤九,辐射处理:将深冻的材料用x-射线、伽马射线或电子束处理;步骤十,将步骤九处理后的脱细胞组织基质材料制备成固态的、无化学交联、有生物活性、有稳定三维结构和有结构记忆特征的多孔细胞生长支架型材。并且,本发明内容步骤十中的多孔细胞生长支架,其脱细胞组织基质材料是纤维直径为2–250微米、长度为100–3000微米的微纤维状或絮状的脱细胞组织基质材料和颗粒直径为2–150微米酸化处理水凝胶状的脱细胞组织基质材料。其基质材料中总的脱细胞组织基质材料含量为每立方厘米10~100毫克、总空隙度90~99%,并且,基质材料的颗粒大于25微米的空隙度为80~98%。所述支架中的微纤维状或絮状的脱细胞组织基质材料按干重质量比为60%~90%,所述的酸化处理水凝胶状的脱细胞组织基质材料按干重质量比为40%~10%。
相比现有技术,由本发明提供的制备方法制作的生长支架是一种无化学交联、有生物活性、有稳定三维结构和有结构记忆特征的多孔细胞生长支架,它是通过将纤维或絮状的组织材料和酸化的水凝胶材料按一定比例混合在一起并通过冻/融挤压和辐射工序制成的有特殊性能的多孔材料。该支架不仅具有优良的生物兼容性和完全的生物可降解性,也支持细胞生长,同时支持体内和体外的组织和器官的生长,是适合于体软组织创伤和缺损的修复。
附图说明
图1是本发明的一个实施例结构示意图;
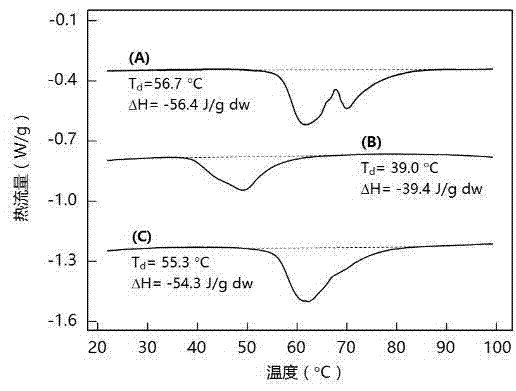
图2是关于图1的支架产品扫描量热仪(dsc)曲线示意图;
图3是关于构成支架产品的两种材料的稳定性与颗粒直径的关系曲线示意图;
图4是关于图1的支架产品生成形态关系的曲线示意图;
图5是本发明制备具有结构记忆特性的细胞生长支架的流程示意图。
具体实施方式
参见附图5,本发明涉及一种具有结构记忆特性的细胞生长支架的制备方法,所述方法包括:步骤一,原料收集:用于制备脱细胞组织基质材料的生物组织原材料的收集,所述原材料包括但不局限于人体或动物的皮肤,软骨,血管、半月板,胃,小肠,大肠,隔膜,肌腱,韧带,神经组织,膀胱和尿道,将富含胶原蛋白的组织切割分离出来,切成1-20毫米的小块或小片;步骤二,原料消毒:将步骤一获取的小块或小片用2%碳酸钠浸泡4~48小时或用其他ph在10.5~12.5的碱性溶液浸泡;步骤三,脱细胞处理:将步骤二浸泡后的小块或小片再用0.1~2.0%的脱氧胆酸钠、聚乙二醇辛基苯基醚、或用每升10~200单位的中性酶脱细胞处理4~36小时;步骤四,脱细胞组织基质材料的清洗:将步骤三脱细胞处理后的小块或小片再用生理盐水或其他中性的渗溶液按每公斤材料1-6升冲洗2-5遍,每次1~12小时;步骤五:脱细胞组织基质绞碎:将步骤四脱细胞组织基质材料清洗后小块或小片再用绞碎机将脱细胞的组织基质材料碎磨成微纤维状或絮状的脱细胞组织基质材料;步骤六,酸化处理:将步骤五获取的微纤维状或絮状脱细胞组织基质材料浸泡在的5~200ml的、ph调至2.8~3.5的盐酸或醋酸溶液中做酸化处理1~24小时,再次将基质材料打碎研磨成水凝胶状颗粒,并用氢氧化钠溶液调节ph至4.0~6.5;步骤七,混合与注模:在20~30℃室温中按60~90%的比例混合微纤维状或絮状脱细胞织基质材料与按40~10的酸化处理的水凝胶状的脱细胞组织基质颗粒混匀后注入包装模具中;步骤八,冰冻处理:将有含有脱细胞组织基质材料悬浮液的模具放入-20℃以下的冻箱中深冻,或在第一次解冻后再次深冻提高其悬浮液空隙结构;步骤九,辐射处理:将深冻的材料用x-射线、伽马射线或电子束处理;步骤十,将步骤九处理后的脱细胞组织基质材料制备成固态的、无化学交联、有生物活性、有稳定三维结构和有结构记忆特征的多孔细胞生长支架型材。并且,本发明内容步骤十中的多孔细胞生长支架,其脱细胞组织基质材料是纤维直径为2–250微米、长度为100–3000微米的微纤维状或絮状的脱细胞组织基质材料和颗粒直径为2–150微米酸化处理水凝胶状的脱细胞组织基质材料。其基质材料中总的脱细胞组织基质材料含量为每立方厘米10~100毫克、总空隙度90~99%,并且,基质材料的颗粒大于25微米的空隙度为80~98%。所述支架中的微纤维状或絮状的脱细胞组织基质材料按干重质量比为60%~90%,所述的酸化处理水凝胶状的脱细胞组织基质材料按干重质量比为40%~10%。
例如图1所示,是指本发明涉及的部分产品的形态结构示意图。其中,图中的(a)是圆片形和圆柱形细胞生长支架;图中的(b)是直径1.8厘米、高3.0厘米的柱形细胞生长支架在(手指捏的)压力作用下收缩形态;图中的(c)是(指捏)压力释放后支架完全恢复了原有稳定三维结构和形状。具体地说,本制备的细胞生长支架每立方厘米含有43毫克脱细胞基质材料,即组织基质的干重含量4.3%。细胞生长支架有很好的弹性,直径1.8厘米和高3厘米的园柱形支架在压力作用下可收缩至高5毫米,压力释放后支架完全恢复原有的稳定三维结构和形状,多次反复受压不变形。
例如图2所示,是经0.5%脱氧胆酸钠溶液脱细胞后组织基质材料的差示扫描量热仪(dsc)曲线示意;其中,图中的(a)是微纤维状或絮状的脱细胞组织基质材料;图中的(b是)经50mm醋酸溶液处理后的脱细胞组织基质水凝胶状颗粒;图中的(c)是按70%微纤维状的脱细胞组织基质材料和30%酸化处理的水凝胶状颗粒制备而成的细胞生长支架。具体地说,差示扫描量热仪(dsc)比较测定了一下材料的热稳定性能:(a)微纤维状或絮状的组织基质材料,(b)酸化处理后的水凝胶状组织基质材料,(c)按干重比70%微纤维状的脱细胞组织基质材料和30%酸化处理的水凝胶状颗粒制备而成的细胞生长支架。微纤维状或絮状的组织基质材料的起始变性温度是56.7℃,热焓值为-56.4j/gdw(克干重);酸化处理后的水凝胶状组织基质材料的起始变性温度是39.0℃,热焓值为-39.4j/gdw,表明酸化处理后的胶原蛋白三螺旋结构已经膨胀松动、不稳定;最后制备成的细胞生长支架的起始变性温度是55.3℃,热焓值为-54.3j/gdw,基本上保留了天然猪真皮细胞外基质材料的稳定性。
例如图3所示,是经0.5%脱氧胆酸钠溶液脱细胞处理和50mm醋酸处理后的脱细胞组织基质水凝胶状颗粒的稳定性与颗粒直径的关系曲线示意图。具体地说,50mm醋酸处理后的脱细胞组织基质水凝胶状颗粒的稳定性与颗粒直径有关(图3)。当平均颗粒直径从140微米减少到约15微米时,起始变性温度从55℃降至35℃,低于人体的正常体温。水凝胶状颗粒越小,热稳定性越差。
结合以上附图可以清楚地看出关于广泛应用于普外科、骨科、整形外科、组织工程和再生医学等领域的具有结构记忆特性的细胞生长支架是如何由本发明的制备方法实现的。
再详细地说,所谓细胞生长的基质材料是由两种性质不同的脱细胞组织基质材料按一定比例组成的材料,即,原材料的来源是脱细胞组织基质材料是从但不局限于人体或动物的皮肤,软骨,血管、半月板,胃,小肠,大肠,隔膜,肌腱,韧带,神经组织,膀胱,和尿道等。将富含胶原蛋白的组织切割分离出来,切成1-20毫米的小块或小片中获取。在获取两种性质不同的脱细胞组织基质材料后就可以制作具有结构记忆特性的细胞生长支架了。例如,首先解决的生物细胞生长支架的组织构架问题,本例中所说的支架是由纤维直径为2–250微米、长度为100–3000微米的微纤维状或絮状的脱细胞组织基质材料和颗粒直径为2–150微米酸化处理水凝胶状的脱细胞组织基质材料按各自干重质量比例混合后再经注模、冰冻,挤压、辐射、重新交织工序所构成;在这当中,细胞生长的基质材料是细胞生长支架的基质材料,其基质材料中总的脱细胞组织基质材料含量应限定在每立方厘米10~100毫克、总空隙度90~99%的方位内;并且,将基质材料的颗粒限定在大于25微米的空隙度为80~98%的范围内。在制作细胞生长支架的过程中优选的方案是支架中的微纤维状或絮状的脱细胞组织基质材料应按干重质量比为60%~90%、酸化处理水凝胶状的脱细胞组织基质材料应按干重质量比为40%~10%调比;在注模工序中应将微纤维状或絮状的脱细胞组织基质材料和酸化处理水凝胶状的脱细胞组织基质材料均匀混合成悬浮液后再注入模具;在冰冻工序中应在-20℃条件下并经伽马射线辐射处理才可将模具内的混合悬浮液制成冰晶或者将模具内的混合悬浮液通过至少两次以上的冻融过程完成冰冻程序;在挤压、重新交织工序中应将冰晶挤压使悬浮液中微纤维状或絮状的脱细胞组织基质材料和酸化处理的水凝胶状的脱细胞组织基质颗粒材料重新交织在一起后再制成具有稳定三维结构和有结构记忆特征的多孔细胞生长支架材料。经过上述工序后才能将具有稳定三维结构和有结构记忆特征的多孔细胞生长支架材料制成形态各异的支架产品。
实施例:
例一,从刚屠宰和脱毛的猪体身上收集新鲜猪皮,机械去除皮下脂肪和表皮,取约1.5毫米厚的真皮。洗清完皮肤中血液和其它污垢,人工拔除皮肤上剩余的毛发。将猪真皮切成约1厘米见方的小块,用纯化水冲洗干净。称取200克真皮原料放于1升的高密度聚丙烯瓶中,加入800毫升含有2%的碳酸钠和10mm氢氧化钠的碱液,在摇床上处理20小时(ph=12.5)。碱液处理后用0.5m的醋酸溶液进行酸碱中和。倒去中和后的溶液,加入800毫升含有0.5%脱氧胆酸钠和5mm乙二胺四乙酸二钠的5mm羟乙基哌嗪乙硫磺酸缓冲液(ph=7.5),在室温下摇床上处理过夜(约20小时)脱细胞。用无菌生理盐水快速冲洗经过脱细胞处理的小块真皮材料2次,每次30-60分钟。将小块真皮材料用高速研磨机研磨,制备成细小的脱细胞组织基质材料,使组织颗粒平均宽度在500–2000微米之间、长度在2000–5000微米之间。用离心法收集基质材料,倒去上面的上清液。加入无菌生理盐水,将离心沉降基质材料悬浮起来,再次离心清洗基质材料。加入800毫升0.1%过氧乙酸溶液,处理60分钟。离心、收集基质材料。用无菌生理盐水,通过悬浮、摇换、离心和收集基质材料洗2次,每次30~60分钟。按每50克基质材料加入500毫升10mm乙二胺四乙酸二钠磷酸盐缓冲溶液(ph=7.5),并用高速研磨机研磨打碎,制备成微纤维状或絮状的脱细胞组织基质材料,使微纤维的直径为2–250微米之间、长度为100–3000微米之间。离心,倒去上清液,收集离心沉降的基质微纤维材料。将微纤维状或絮状的基质材料悬浮于0.9%盐水中,得到细胞外组织基质材料悬浮液,悬浮液中微纤维基质材料含量为4.9%。然后取部分微纤维状或絮状的基质材料,加入醋酸,使最终的醋酸浓度为50mm。酸化处理导致基质材料膨胀后,用高速研磨机继续研磨,制备成大小10–250微米的水凝胶颗粒,用氢氧化钠溶液将酸化的水凝胶调ph至6.5,水凝胶材料含量为1.5%。将微纤维状或絮状的组织基质材料和酸化处理的水凝胶状的组织基质材料按干重比70%对30%混合。将混合后的基质材料悬浮液加入到圆片形和圆柱形模具中,放入-20℃冰箱中冷冻。利用结冰形成多孔结构。冷冻后采用25kgy伽马辐射处理,制备得到稳定的、有结构记忆特征的细胞生长支架,且可放于室温中保存。
实施例二,从刚屠宰和脱毛的猪体身上收集新鲜猪皮,去除皮下脂肪和表皮,洗清皮肤中血液和其它污垢,人工机械拔除皮肤上剩余的微小毛发后,将猪真皮切成约厚2毫米、宽1厘米见方的小块,用纯化水冲洗一次,称取原料200克,放于高密度聚丙烯瓶中。加入碱液(含2%碳酸钠,10mm氢氧化钠和0.2%聚乙二醇辛基苯基醚),放置于摇床,在碱液中处理20小时。加入醋酸溶液进行酸碱中和。加入0.5%十二烷基硫酸钠(溶于5mm乙二胺四乙酸二钠和5mm羟乙基哌嗪乙硫磺酸缓冲液中)进行脱细胞,室温下摇床振荡处理20小时。无菌生理盐水快速冲洗2次,每次30-60分钟。将材料用高速研磨机研磨打碎,将材料打碎成长约2.0~4.0mm,宽约0.5~2.0mm大小。离心,收集基质材料,倒去上清液。将收集到的基质材料浸泡于0.1%过氧乙酸溶液中处理2小时。用无菌生理盐水冲洗1~2次,每次30~60分钟。将生理盐水冲洗过的材料用10mm乙二胺四乙酸二钠磷酸盐缓冲溶液进行清洗,并用高速研磨机研磨打碎,将材料打碎成长约500~2500毫米,宽约50~500毫米大小,离心,收集基质微纤维,倒去上清液。将基质微纤维悬浮于0.9%盐水中,制备得到细胞外组织基质微纤维材料悬浮液,材料含量为4.6%。取三分之一的微纤维材料悬浮液,用50mm醋酸溶液将材料进行稀释和酸化。将酸化处理过的材料用高速研磨机研磨打碎,制备成水凝胶材料。用氢氧化钠溶液将酸化的水凝胶材料进行中和,ph调至6.5,制备得到的水凝胶材料含量为1.7%。将微纤维状或絮状组织基质材料和酸化的水凝胶材料按干重比80%对20%混合,混合后的基质材料倒入到模具中。在-20℃冰箱中冷冻后,采用25kgy伽马辐射处理,制备得到生物组织细胞生长支架。如图4所示,用差示扫描量热仪(dsc)比较测定了一下材料的热稳定性能:(a)0.5%十二烷基硫酸钠脱细胞的微纤维状或絮状的组织基质材料,(b)酸化处理后的水凝胶状组织基质材料,(c)按干重比80%微纤维状的脱细胞组织基质材料和20%酸化处理的水凝胶状颗粒制备而成的细胞生长支架。0.5%十二烷基硫酸钠脱细胞的微纤维状或絮状的组织基质材料的起始变性温度是53.1℃,热焓值为-49.2j/gdw;酸化处理后的水凝胶状组织基质材料的起始变性温度是34.9℃,热焓值为-30.2j/gdw;最后制备成的细胞生长支架的起始变性温度是53.3℃,热焓值为-50.3j/gdw,基本上保留了天然猪真皮细胞外基质材料的稳定性。
- 还没有人留言评论。精彩留言会获得点赞!