具有互连框架的电极阵列导管的制作方法
本发明涉及电生理(EP)导管,具体地讲,涉及用于在心脏中标测电信号和/或消融组织的EP导管。
背景技术:
现在,常常使用包括用于标测心脏电活动的电生理传感器的心脏导管来进行对心脏中电势的标测。通常,根据心脏内的位置感测并记录心内膜中的时变电势,然后将其用于标测局部电描记图或局部激活时间。由于通过心肌传导电脉冲所需的时间,心内膜中各点的激活时间不同。在心脏中任何点处的该电传导的方向常规地由激活矢量表示,该激活矢量垂直于等电激活波前,这两者都可来自激活时间的标测图。该激活波前通过心内膜中任意点的传播速率可表示为速度矢量。标测激活波前和传导场有助于医师识别并诊断异常情况,诸如室性和房性心动过速以及心室和心房纤颤,这可能由于心脏组织中受损的电传播的区域造成。
可通过观察现象诸如多个激活波前、激活矢量的反常集聚、或速度矢量的变化或矢量与正常值的偏差来识别心脏的激活信号的传导中的局部缺陷。此类缺陷的示例包括内曲区域,该内曲区域可与称为复杂碎裂电描记图的信号图案相关联。一旦缺陷通过此类标测定位,就可对其进行消融(如果其功能反常)或以其他方式治疗,以便尽可能恢复心脏的正常功能。作为例证,当心脏组织的区域异常地将电信号传导到相邻组织、由此扰乱正常的心动周期并导致心律不齐时,可发生包括心房纤颤的心律失常。用于治疗心律失常的手术包括扰乱导致心律失常的信号来源,以及诸如通过形成消融灶以隔离异常部分来扰乱用于此类信号的传导通路。因此,通过经由导管施加能量来选择性地消融心脏组织,有时可终止或更改无用电信号从心脏一部分传播到另一部分。消融过程通过形成非传导性的消融灶来破坏无用电通路。
可通过下述方法获得多个优点:提供具有多个电极的导管,以允许同时或者不需要重新定位导管的情况下标测较大区域和/或产生多个消融灶。在共同转让的美国专利No.6,961,602(其以引用方式并入本文)中描述的一个合适的构型采用具有由多个脊形成的多射枝电极组件的导管,每个脊承载一个或多个诊断或消融电极。该组件具有两个或更多个脊,每个脊具有附接在导管主体的远侧端部处的近侧端部和自由远侧端部。已经采用的另一个构型称为篮形电极组件。示例在共同转让的美国专利No.5,772,590、6,748,255和No.6,973,340中有所描述,这些专利中的每个的全部公开内容以引用方式并入本文。篮式导管还采用多个脊,该脊连接在导管的远侧端部以及近侧端部处。在任一个构型中,所述脊可布置成膨胀布置,其中每个脊的至少一部分从导管主体径向向外延伸,或布置成塌缩布置,其中每个脊大体沿导管主体的纵向轴线设置。塌缩布置有利于诸如以经皮方法通过脉管系统将电极组件推进到患者体内的期望位置。当电极组件呈现膨胀布置时,在脊上的电极中的一个或多个与组织接触以允许测量电信号和/或消融组织。
通过采用多个脊,这些电极组件适于提供电极阵列以占据由患者的解剖结构限定的三维空间,诸如例如心脏腔室或孔口脉管。一般来讲,期望以限定的构型部署脊以及相应的电极以获得任何数量的益处,诸如提供以一定密度的电极覆盖所部署的区域,在特定区域中提供集中覆盖,帮助确定电极相对于彼此的位置,更紧密地符合其中部署电极的容积,或任何其它益处。然而,常规的多个脊柱电极组件可以不部署有处于预期构型的脊,从而产生次优的电极阵列。例如,在多射枝电极组件中,脊相对于彼此仅固定在近侧端部处,而在篮形电极组件中,它们仅固定在其近侧端部和远侧端部处。因此,脊可以不呈现其预期的径向分布,特别是在远离固定端部的位置处。值得注意的是,脊可更紧密地聚束在一起或者可比期望张开至更大程度。多个脊电极组件呈现此类非预期分布的趋势可通过患者解剖结构中的不规则部分而加重。
因此,存在对于具有改进的稳定性的电极阵列组件的需要。例如,期望提供一种电极阵列组件,其中电极具有更大的保持与彼此限定的关系的趋势。以下材料中所描述的本公开的技术满足这些和其它需要。
技术实现要素:
本公开包括具有细长导管主体和电极阵列组件的导管,所述细长导管主体具有近侧端部、远侧端部,所述电极阵列组件具有近侧端部和远侧端部、安装在导管主体的远侧端部处。电极阵列组件可由互连框架形成,所述互连框架具有多个元件,所述多个元件通过在电极阵列组件的近侧端部和远侧端部的中间位置处的多个接头互连,其中互连框架具有塌缩构型和膨胀构型,在塌缩构型中元件大体沿导管主体的纵向轴线布置,在膨胀构型中元件从纵向轴线径向向外定位以部署安装在互连框架上的电极阵列。
在一个方面中,互连框架中的每个元件在接头之间具有减小的自由长度。减小的自由长度可小于从所述电极阵列组件的近侧端部延伸到远侧端部的最短轮廓线的长度的一半。另外,减小的自由长度可小于从电极阵列组件的近侧端部延伸到远侧端部的最短轮廓线的长度的三分之一。
在一个方面,互连框架可包括聚合物层和多个印刷电极。互连框架还可具有基底,聚合物层施加在该基底上。基底可为整体的。例如,基底可包括切割管。另外,基底可由形状记忆材料形成。因此,互连框架可为柔性电路。
在一个方面,互连框架可具有在电极阵列组件的远侧端部处的互连元件之间的至少一个接头以限定闭合形状。在互连元件之间的接头可集中在极区域处或者可跨所述互连框架基本上均匀地分布。
在一个方面,互连框架可包括多个自由远侧突出射枝。
本公开还包括一种用于治疗的方法,该方法可涉及:提供具有细长导管主体和电极阵列组件的导管,所述细长导管主体具有近侧端部、远侧端部,所述电极阵列组件安装在导管主体的远侧端部处、具有互连框架,所述互连框架具有多个元件,所述多个元件通过在电极阵列组件的近侧端部和远侧端部的中间位置处的多个接头互连;在互连框架处于塌缩构型的情况下,将具有电极阵列组件的导管的远侧端部推进到患者体内的期望区域,在塌缩构型中互连框架的元件大体沿导管主体的纵向轴线布置;以及使电极阵列组件呈现膨胀构型,在膨胀构型中元件从导管主体的纵向轴线径向向外定位以部署安装在互连框架上的电极阵列,使得至少一个电极与组织接触。
在一个方面,可从与组织接触的至少一个电极接收电信号。
在一个方面,可将射频能量递送到与组织接触的至少一个电极以形成消融灶。
附图说明
其它特征和优点将通过本公开的优选实施方案的如下的和更具体的说明而变得显而易见,如在附图中所示,并且其中类似的引用字符在整个视图中通常指相同部分或元件,并且其中:
图1为根据一个实施方案的具有电极阵列组件的导管的顶部平面图。
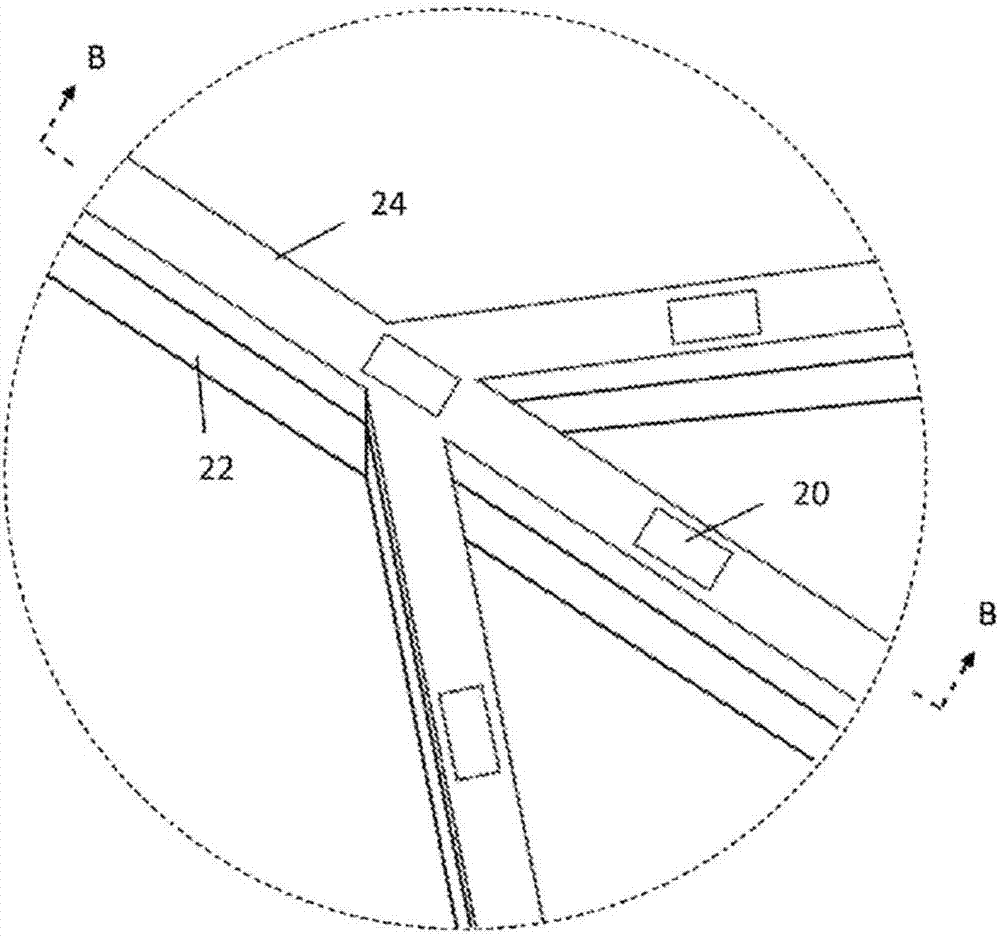
图2为根据一个实施方案的在电极阵列组件的互连元件之间的接头的细部图。
图3为图2的接头的横截面。
图4为根据一个实施方案的电极阵列组件的基底的透视图。
图5为根据一个实施方案的电极阵列组件的互连部的第一图案的示意图。
图6为根据一个实施方案的电极阵列组件的互连部的第二图案的示意图。
图7为根据一个实施方案的电极阵列组件中的均匀分布的接头的示意图。
图8为根据一个实施方案的具有多个远侧突出射枝的电极阵列组件的示意图。
图9为根据一个实施方案的定位在左心房内的电极阵列组件的示意图。
图10为根据一个实施方案的使用电极阵列组件的侵入式医疗手术的示意图。
具体实施方式
首先,应当理解本公开不受具体示例性材料、构造、常规、方法或结构的限制,因为这些均可变化。因此,尽管本文描述了优选材料和方法,但与本文所述那些相似或等价的许多此类选项可用于本公开的实施方案的实践中。
另外应当理解,本文使用的术语只是为了描述本公开的具体实施方案的目的,并非旨在进行限制。
下文结合附图示出的具体实施方式旨在作为本公开的示例性实施方案的描述,并非旨在表示可实践本公开的唯一示例性实施方案。本说明书通篇使用的术语“示例性”是指“用作示例、实例或例证”,并且不一定要理解为优选的或优于其它示例性实施方案。具体实施方式包括具体细节,其目的在于提供对本说明书的示例性实施方案的透彻理解。对于本领域的技术人员将显而易见的是,可在不具有这些具体细节的情况下实践本说明书的示例性实施方案。在一些情况下,熟知的构造和装置示出于框图中,以便避免使本文所述的示例性实施方案的新颖性模糊。
仅为简洁和清楚起见,可相对于附图使用定向术语,诸如顶部、底部、左侧、右侧、上、下、之上、之下、下方、下面、后面、后部和前部。这些术语及类似的定向术语不应被理解为以任何方式限制本公开的范围。
除非另有定义,否则本文使用的所有技术和科学术语具有与本公开所属领域的普通技术人员通常理解相同的含义。
最终,如本说明书和所附权利要求中所用,除非内容另有明确说明,否则单数形式“一个”、“一种”和“所述”包括复数含义。
如上所述,心脏腔室内的某些类型的电活动不是周期性的。示例包括动脉颤动或动脉纤颤,以及源于梗死所致的心室壁中的疤痕的室性心动过速。此类电活动是随机跳动的。为了分析或“标测”这种类型的电活动,希望尽可能快地诸如在一次心跳之内获得“图片”。换句话讲,可在十分之一秒内同时获得标测图或图片的所有点。根据本公开的技术,具有高电极密度的篮形电极组件可用于精确地标测这种电活动。另外,可将射频能递送到所选择的治疗区域以用于基于消融的治疗,包括例如通过阻断电传导而隔离不规则的电信号源。使用单极装置的焦点消融在空间上和相对于组织接合两者,得益于射频能的定向递送连同导管放置的局部反馈。然而,由于医师需要进行一系列“量化”RF消融以形成具有期望特性的消融灶,诸如产生包围目标静脉的连续周向块,因此焦点消融手术通常涉及相对长的手术时间。另外,使用焦点单极电极需要用周边导航系统增强的相当高的医师技能水平,以便精确和可靠地定位电极。对应地,多电极装置可呈现在多个位置处同时记录电信号和/或递送消融能量的机会。如本文将描述,本公开涉及具有电极阵列组件的导管,所述电极阵列组件具有互连框架以在部署时帮助稳定电极。具体地,互连框架采用多个元件,该多个元件中的每个可具有在互连部之间的减小的自由长度以帮助稳定框架。
为了帮助示出本公开的方面,在图1中示意性地示出具有电极阵列组件的电生理导管的示例性实施方案。导管10包括:具有近侧端部和远侧端部的细长导管主体12;在导管主体12的近侧端部处的控制手柄14;以及电极阵列组件16,其包括安装在导管主体12的远侧端部处的互连框架18。多个电极20安装在互连框架18上,形成电极阵列。
电极20和互连框架18的细节在图2和图3中示出。图1的区域A的细节在图2中示出。互连框架18可由结构基底22形成,该结构基底22具有使用本领域已知的产生柔性电路或“挠性电路”的技术构造的聚合物层24。聚合物层24可为任何合适的柔性聚合物,诸如聚酯、聚酰亚胺、聚萘二甲酸乙二醇酯(PEN)、聚醚酰亚胺(PEI)、含氟聚合物(FEP)、PEEK等,包括共聚物。一般来讲,聚合物层24可根据需要使用金属箔和光刻或等同技术,提供有导电元件诸如电极20以及引线、迹线等,但合适图案的导电胶带可层合在聚合物层之间或者也可使用电沉积方法。在图3中描绘沿线B-B截取的横截面。可看出,聚合物层24被施加在基底22上并且电极20被印刷在顶部上。根据实施方案,电极20可与聚合物层24的表面相对齐平或者可突出以有利于组织接合。电极20可被配置为单极、双极或单极和双极两者,并且可以是诊断电极、消融电极、参考电极或其它,或者可以是多功能的。如果采用不同的电极构型,则可根据预期应用来提供任何组合和不同数量的构型。通过采用挠性电路技术,任何数量的电极20可容易地定位在互连框架18上的任何位置处。例如,电极20可定位在互连的框架上并且以大约4mm的距离彼此等距地间隔开以允许标测其中部署导管的区域。
在图1所示的实施方案中,电极阵列组件16可具有类似于常规的篮形电极组件的构型,使得互连框架18可具有塌缩构型,其中形成互连框架18的元件大体沿导管主体12的纵向轴线设置,使得脊能够装配在引导鞘管腔内,如下文进一步讨论。另外,当部署时互连框架18可具有膨胀构型以呈现电极20的阵列。互连框架18可具有大致球形、卵形体、椭球形或其它闭合形状,但是也可经设计采取其它形状,该形状为规则或不规则的以及开放的或闭合的。例如,如下所述,体现本公开的方面的互连框架可被配置成具有带有多个射枝的开放远侧端部。当根据患者的解剖结构膨胀用于部署时,互连框架18还可具有不同的尺寸以提供与被研究的患者的区域(诸如右心房或左心房)的紧密配合。
根据实施方案,可由互连框架18的特性、由机械致动或由组合引起塌缩构型和膨胀构型之间的转变。例如,互连框架18可在未受引导鞘约束时具有预成形构型,使得其径向向外膨胀以呈现膨胀构型。另选地,机构诸如牵拉线可用来调节在互连框架18的远侧端部和近侧端部之间的相对距离,使其向外弓形弯曲成膨胀布置。
因此,基底22可由形状记忆材料形成以帮助互连框架18呈现膨胀构型和塌缩构型。例如,可使用被称为镍钛诺的镍-钛合金。在体温下,镍钛诺线具有柔韧性和弹性,并且当经受最小力时,像大多数的金属一样,镍钛诺线变形,并且在不存在该力时恢复到它们的形状。镍钛诺属于被称为形状记忆合金(SMA)的一类材料,形状记忆合金具有超出柔韧性和弹性的令人感兴趣的机械性能,包括形状记忆和超弹性,其允许镍钛诺具有取决于其温度相的“记忆的形状”。奥氏体相是镍钛诺的较强的、较高温度相,具有简单的立方晶体结构。超弹性行为发生在此相(超过50℃-60℃的温差)中。对应地,马氏体相是相对较弱、较低温度相,具有双孪晶体结构。当镍钛诺材料处于马氏体相时,其相对容易变形并将保持变形。然而,当加热到高于其奥氏体转变温度时,镍钛诺材料将恢复到其变形前的形状,从而产生“形状记忆”效应。将加热时镍钛诺开始转化成奥氏体的温度称为“As”温度。将加热时镍钛诺已完成转化成奥氏体的温度称为“Af”温度。
因此,电极阵列组件16可具有三维形状,其可易于塌缩以馈送到引导鞘中且然后在移除引导鞘时在递送到患者的期望区域时易于恢复到其膨胀形状记忆构型。在一些实施方案中,互连框架18可通过激光切割或其它类似技术由镍钛诺海波管形成以提供整体框架。例如,根据实施方案,壁厚为大约8密耳至9密耳的3mm管可用来形成互连基底22。本领域技术人员将理解具有其它直径和壁厚的管可用来形成互连的基底22。作为替代构造的示例,聚合物层24可具有足够的弹性特性以允许省略基底22。用于此类实施方案的一种示例性材料可为PEEK,由此使得互连框架18可从PEEK管切割或者通过使用任何其它合适的技术。
在图4中示出互连框架18的基底22处于其膨胀、部署的构型的透视图。应当理解,框架的元件之间的互连部帮助稳定部署的构型并因此稳定电极阵列组件16。形成结构元件的网络的任何数量的不同互连部设计可与本公开的技术一起使用。为了形成互连框架18,互连元件之间的接头位于电极阵列组件16的近侧端部和远侧端部之间的中间位置处。互连框架18的一个特征是任何元件的自由长度短于由互连框架18限定的表面上方的最短轮廓线。在图4的上下文中,元件28在互连接头30和互连接头32之间延伸。互连框架18限定大致球形表面,但互连框架18可被配置成呈现如上所述的其它部署形状。因此,可看到球形表面具有近侧极34(其中电极阵列组件接合到导管主体12)和相对的远侧极36。在常规的篮形电极组件中,偏转的脊将位于球体的表面上,对应于在极之间的最短轮廓线,从在其近侧端部处的近侧极34延伸到在其远侧端部处的远侧极36。另选地,该距离可被理解为子午线距离或关于其它部署形状的合适等同距离。因此,脊的整个长度基本上应当是自由的。相比之下,即使元件28可具有最长的自由长度或者可等于互连框架18内的最长自由长度,但相较之下元件28具有减小的自由长度。例如,在一些实施方案中,减小的自由长度可为最短轮廓线的对应长度的一半或更小,并且在其它实施方案中可为三分之一或更小。假定互连框架18的每个元件具有至多这种减小的自由长度,应当理解元件将经历从预期部署形状偏转的较小趋势,从而产生更稳定的电极阵列组件16。
按照上述讨论,可看出,每个元件与其它元件具有至少一个互连部以便形成互连框架18的网络。可采用任何期望的互连元件的图案。在一个方面,元件可通过激光切割管来形成,如上所述。通过增加互连元件的数量,互连框架18可占据由部署形状限定的表面中的更多者,这继而在电极20的放置中呈现更多的灵活性并且可允许阵列中的电极密度增加。相反地,减少互连元件的数量可增加电极阵列组件16的整体适形能力以适应其中部署电极阵列组件的空间,同时相比于常规设计仍然增加阵列的稳定性。根据预期应用,可采用在这些设计约束之间的合适平衡。
如图4所示,可邻近极(或与可采用的其它形状相关联的等效结构)提供或者可更均匀地分布更大量的互连部。仅作为例证而非限制地,由基底38形成的互连元件和接头的另一合适图案在图5的极视图中示出,其中一个半球已经平坦化并且其中互连部集中在极区域中。可看出,基底38具有朝向相对极延伸的八个辐射元件40,其中互连图案可重复或者可采用不同的图案。另一个示例性图案在图6的极视图中示出,其示出基底42。虽然类似,但是该构型产生起六个辐射元件42。作为对比示例,图7示出处于部署构型和膨胀构型的基底44的一半。虽然该构型也呈现与常规篮形电极组件的形状相似的形状,但该实施方案中的互连元件46的图案表现出接头48跨所述表面的更均匀分布。
虽然已经与常规篮形电极组件相比较地描述了以上实施方案,但本领域技术人员将认识到,体现本公开的技术的互连框架可用于产生其它电极组件构型。如上所述,常规多射枝电极组件可涉及多个脊,其从近侧连接点辐射,具有自由远侧端部。如图8所示,可实现类似构型,其中电极阵列组件16由互连框架50形成。与导管主体12的连接部相邻的互连部帮助稳定互连框架50,同时呈现远侧突出射枝52,其可更易于符合限定其中部署电极阵列组件16的空间以将电极20与组织接合。射枝52具有自由端部并且可被配置成从导管主体20的纵向轴线向外辐射成任何期望的程度。在该上下文中,互连框架50的远侧端部由射枝52的远侧端部限定,由此使得跨电极阵列组件16的表面的最短轮廓线应当起源于导管主体12的近侧连接部处并延伸到互连框架50的远侧端部。对应地,具有最长自由长度的互连框架50的元件可为射枝52,相比于最短轮廓线,该射枝52表现出减小的自由长度。与上述其它实施方案一样,互连框架50可通过切割材料管(例如镍钛诺海波管)形成。
导管主体12包括细长管状构造,该细长管状构造具有单个轴向或中心管腔,但如果需要可任选地沿其全部长度或部分长度具有多个管腔。导管主体12是柔性的,即能够弯曲的,但沿其长度基本上不可压缩。导管主体12可具有任何合适构造并由任何合适材料诸如通过使用聚氨酯或(聚醚嵌段酰胺)的外壁来制成。外壁可具有由不锈钢等(如本领域中通常已知的)制成的嵌入式编织网,以增加导管主体12的扭转刚度,使得当旋转控制手柄14时导管主体12的远侧端部将以对应的方式旋转。
导管主体12的长度不是关键的,但可在约90cm至约120cm的范围内,诸如约110cm。导管主体12的外径也不是关键的,但通常适于呈现足以容纳电极阵列组件16和任何相关联的引线、冲洗管腔、牵拉线、位置或其它传感器等的构造的外径,同时保持允许通过患者脉管系统的推进的插入轮廓。在一些实施方案中,导管主体12可为约10弗伦奇或更小,诸如8弗伦奇或7弗伦奇。同样,导管主体12的外壁的厚度不是关键的,但可足够薄以提供足够尺寸的一个或多个管腔。美国专利No.6,064,905中描述并示出了适于与本发明结合使用的导管主体构造的示例,该专利的全部公开内容以引用方式并入本文。
在一个方面,电生理学者可将引导鞘、导丝和扩张器引入患者体内,如本领域通常已知的。例如,与本发明的导管结合使用的引导鞘为适当设定尺寸的PREFACETM编织引导鞘(可从Biosense Webster,Inc.,Diamond Bar,CA商购获得)。插入导丝,移除扩张器,并且通过引导鞘引入导管,由此膨胀器中的导丝管腔允许导管穿过导丝。在如图9所示的一个示例性手术中,首先经由下腔静脉(IVC)通过右心房(RA)将导管引入患者的心脏(H),其中导管穿过隔膜(S)以便到达左心房(LA)。应当理解,电极阵列组件16可偏转成拉直构型并且被约束在引导鞘54内,以允许导管10穿过患者的脉管系统到达期望的位置。一旦导管的远侧端部到达期望的位置,例如左心房,就抽出引导鞘54以暴露电极阵列组件16,从而允许其部署,呈现膨胀构型。应当理解,可借助本公开的技术进行采用电极阵列组件的手术,并且可包括涉及测量电信号和/或消融患者体内的组织的任何期望的操作。例如,通过使用具有互连框架的电极阵列组件,电生理学者可从电极获得心脏的海绵状区域(包括心房)的真实解剖结构,从而允许该区域的更快速的标测。
为了帮助示出电极阵列组件16的使用,图10为根据本发明的实施方案的侵入性医疗手术的示意图。在远侧端部处具有电极阵列组件16(在该视图中未示出)的导管10可在近侧端部处具有用于将电极和传感器(在该视图中未示出)的引线联接到控制台62的连接器60,该控制台62用于记录和分析它们检测到的信号以及用于供应消融能量。电生理学者64可将导管10插入患者66体内,以便从患者的心脏68获得电势信号。电生理学者64使用附接到导管的控制手柄14来进行插入。控制台62可包括处理单元70,该处理单元70分析所接收的信号并可在附接到控制台的显示器72上呈现分析结果。该结果通常是来源于信号的标测图、数字显示和/或图的形式。处理单元70还可控制能量到一个或多个电极20的递送用于产生一个或多个消融灶,诸如在与通过分析接收的信号识别的异常电活动相关联的位置处。
另外,处理单元70还可接收来自一个或多个位置传感器诸如传感器56(如图1所示)的信号。一个或多个传感器各自可包括磁场响应线圈或多个此类线圈。使用多个线圈允许确定六维位置和取向坐标。因此传感器可响应于来自外部线圈的磁场产生电位置信号,从而使得处理器70能够确定导管10的远侧端部在心腔内的位置(例如,位置和取向)。电生理学者然后可在显示器72上观察电极阵列组件16在患者心脏图像上的位置。以举例的方式,这种位置感测的方法可使用由Biosense Webster Inc.(Diamond Bar,Calif.)制造的CARTOTM系统实现并且在美国专利No.5,391,199、No.6,690,963、No.6,484,118、No.6,239,724、No.6,618,612和No.6,332,089、PCT专利公布WO 96/05768、以及美国专利申请公布2002/0065455 A1、2003/0120150 A1和2004/0068178 A1中有所描述,这些专利的公开内容以引用方式全文并入本文。应当理解,也可采用其它位置感测技术。如果需要,至少两个位置传感器可相对于电极阵列组件16定位在近侧和远侧。远侧传感器相对于近侧传感器的坐标可被确定,并且利用与电极阵列组件16的构型有关的其它已知信息,用于找到电极20中的每个的位置。
已参考本发明的当前所公开的实施方案进行了以上描述。本发明所属技术领域的技术人员将会认识到,在不有意脱离本发明的原则、精神和范围的前提下,可对所述结构作出变更和更改。如本领域的普通技术人员应理解的,附图未必按比例绘制。因此,上述描述不应视为仅与附图中描述和示出的精确结构有关,而应视为符合以下具有最全面和合理范围的权利要求书并且作为权利要求书的支持。
- 还没有人留言评论。精彩留言会获得点赞!