化合物helicascolideA在制备抗肿瘤药物中的应用的制作方法
本发明属于生物医药技术领域,具体涉及化合物helicascolide A在制备抗肿瘤药物中的应用。
背景技术:
:
癌症是目前严重危害人类健康的多发病和常见病。据世界卫生组织(WHO)统计,每年世界上有1000万人患上癌症,而死于癌症的人数约600万,并且,人口老龄化、吸烟人数增加、体育运动减小、饮食中缺少蔬菜水果不良习惯可能会导致全球癌症人数猛增,已严重危害人类生命和生活质量,因此,寻找有效的抗癌药物是世界医学界重要的研究课题。
内生真菌长期生活在植物体内的特殊环境中,与宿主协同进化,在演化过程中二者形成了互惠共生关系。在“内生真菌—植物”这个稳定的共生系统中,内生真菌能产生很多种类结构复杂的次级代谢产物,且这些代谢产物有些与宿主的某些代谢产物相同或相似,此外,内生真菌也能产生其他有潜在药用价值的次生代谢产物,并且更容易得到新颖结构的化合物,已成为发现高效、新颖、低毒的天然活性物质的重要资源。
本发明所涉及的化合物helicascolide A为从广藿香内生真菌光轮层炭壳菌(Daldinia esc hscholzii)A630发酵液中分离、纯化得到,其结构式如式(Ⅰ)所示,其公开于文献“Tarma n K,Palm GJ,Porzel A,et al.Helicascolide C,a new lactone from an Indonesian marine algicolous strain of Daldinia eschscholzii(Xylariaceae,Ascomycota)[J].Phytochem Lett,20 12,5(1):83-86”中,但到目前为止,国内外文献尚未有关于化合物helicascolide A抗肿瘤活性的报道。
技术实现要素:
:
本发明的第一个目的是提供化合物helicascolide A在制备抗肿瘤药物中的应用。
本发明通过对神经胶质瘤细胞SF-268、乳腺癌细胞MCF-7、大细胞肺癌细胞NCI-H460、人肝癌细胞HepG-2细胞毒活性测试发现,helicascolide A对上述4株肿瘤细胞的IC50值分别为21.74、16.52、21.86、21.07μmol/L。实验结果表明:化合物helicascolide A具有显著的肿瘤细胞毒活性,可用于抗肿瘤药物。因此,化合物helicascolide A能应用于制备抗肿瘤药物中。
所述的抗肿瘤药物优选为抗神经胶质瘤、乳腺癌、大细胞肺癌或人肝癌的药物。
本发明的第二个目的是提供一种抗肿瘤药物,包括有效剂量的helicascolide A和药学上可以接受的载体。
所述的抗肿瘤药物优选为抗神经胶质瘤、乳腺癌、大细胞肺癌或人肝癌的药物。
本发明发现化合物helicascolide A对神经胶质瘤细胞SF-268、乳腺癌细胞MCF-7、大细胞肺癌细胞NCI-H460、人肝癌细胞HepG-2都具有很强的细胞毒活性,表明化合物helicascolide A具有较好的抗肿瘤活性,可应用于制备抗肿瘤药物。因此,本发明为研究与开发新的抗肿瘤药物提供了候选药物,为开发利用植物内生真菌来源的天然活性物质提供了科学依据。
本发明所涉及的广藿香内生真菌光轮层炭壳菌(Daldinia eschscholzii)A630公开于文献:“王营,李浩华,谭国慧等.广藿香内生真菌类群分析及其抗菌活性研究.中国中药杂志,2017,42(4):657-662”。该菌株本申请人也持有,并保证自申请日起20年内向公众提供。
附图说明:
图1是化合物6的1H-NMR谱;
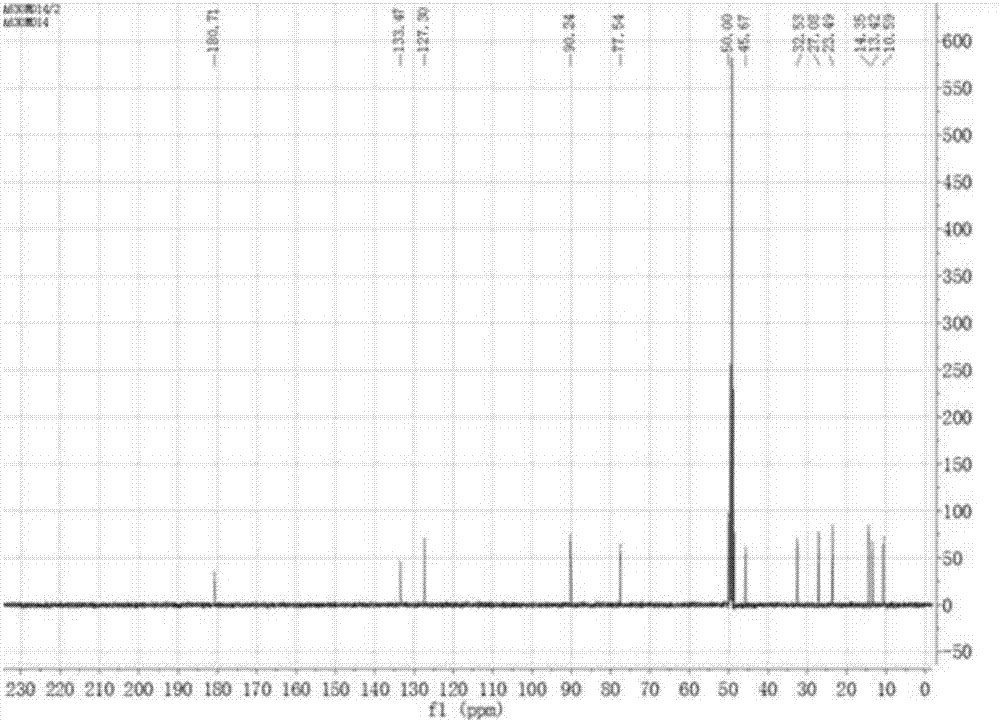
图2是化合物6的13C-NMR谱。
具体实施方式:
以下实施例是对本发明的进一步说明,而不是对本发明的限制。
实施例1:
本发明所涉及的化合物helicascolide A为从广藿香内生真菌光轮层炭壳菌(Daldinia eschscholzii)A630发酵液中分离、纯化得到,其结构式如式(Ⅰ)所示:
所述的化合物helicascolide A的制备方法具体如下:
发酵培养物的制备:将活化的Daldinia eschscholzii A630菌种接入马铃薯葡萄糖液体培养基中,28℃,120rpm,培养5d制得种子液,将种子液以体积比10%的接种量接入到马铃薯葡萄糖液体培养基中,相同条件下培养7d,制得发酵培养物。
将该发酵培养物的发酵液和菌丝体分离,发酵液用乙酸乙酯萃取,萃取液经蒸馏浓缩后得到浸膏;浸膏经MCI柱(洗脱剂:甲醇-水体积比70︰30、80︰20、90︰10和100%甲醇)梯度洗脱,用薄层色谱(TLC)检测(显色剂:茴香醛-浓硫酸),合并相似组分,得到M5组分。M5组分经Sephadex LH-20以纯甲醇洗脱得到M5-1组分,M5-1组分通过反相制备柱(洗脱剂:乙腈-水体积比70︰30)洗脱纯化,得到化合物6(3.1mg)。
化合物6经核磁共振波谱分析(如图1、2所示),其结构鉴定如下:
化合物6具有以下理化和波谱特性:白色粉末(CD3OD),ESI-MS[M+H]+m/z:212.14;1H-NMR(500MHz,CD3OD)δ:5.58(1H,m,H-7),4.65(1H,d,J=11.2Hz,H-5),3.46(1H,d,J=3.5Hz,H-3),2.34(2H,m,H-4),1.67(3H,m,H-12),1.64(3H,t,J=1.2Hz,H-11),1.29(4H,overlapped,H-8,H-9),0.90(3H,d,J=6.7Hz,H-10);13C-NMR(125MHz,CD3OD)δ:180.7(C-1),133.5(C-6),127.3(C-7),90.2(C-5),77.5(C-3),45.7(C-2),32.5(C-4),27.1(C-8),23.5(C-9),14.4(C-10),13.4(C-12),10.6(C-11)。该化合物存在5个甲基信号δH1.29(6H,d,H-8,H-9),0.9(H-10),1.64(H-11),1.67(H-12),3个次甲基信号δH3.46(H-3),4.65(H-5),5.58(H-8),一个亚甲基信号δH 2.34(H-4),甲醇溶剂中不显示活泼氢信号。δC(13C-NMR,CD3OD,125Hz):180.7(C-1),45.7(C-2),77.5(C-3),32.5(C-4),90.2(C-5),133.5(C-6),127.3(C-7),27.1(C-8),23.5(C-9),14.4(C-10),10.6(C-11),13.4(C-12)。δC(10.59-27.08)为甲基信号。以上数据与文献报道“Tarman K,Palm GJ,Porzel A,et al.Helicascolide C,a new lactone from an Indonesian marine algicolous strain of Daldinia eschscholzii(Xylariaceae,Ascomycota)[J].Phytochem Lett,2012,5(1):83-86”基本一致,鉴定该化合物为helicascolide A,其结构式如式(Ⅰ)所示:
采用SRB法测定化合物helicascolide A的细胞毒活性。本实验所用的肿瘤细胞为大细胞肺癌细胞NCI-H460、神经胶质瘤细胞SF-268、乳腺癌细胞MCF-7、人肝癌细胞HepG-2。
将本发明制备的化合物helicascolide A用二甲基亚砜(DMSO)溶解得浓度为10mmol/L的母液,再用RPMI-1640培养基稀释至所需浓度,阳性对照药物为顺铂。取对数生长期的NCI-H460、SF-268、MCF-7和HePG-2细胞,用胰酶消化,台盼蓝染色计数,台盼蓝排斥实验检测细胞活力大于95%后,用新鲜RPMI-1640培养基调整细胞浓度为3×104个/mL,细胞接种于96孔板,每孔加入180μL的细胞悬液,并设3个空白孔调零,于37℃、5%CO2培养箱中培养24h。待细胞贴壁后,每孔加入20μL一定浓度的化合物helicascolide A溶液,阴性对照加20μL RPMI-1640培养基,以顺铂作阳性对照。置37℃、5%CO2培养箱中培养72h后,加入50μL 50%冷三氯醋酸固定细胞,4℃放置1h后用蒸馏水洗涤5次,空气中自然干燥。然后加入由1%冰醋酸配制的浓度为4mg/mL的SRB溶液100μL/孔,室温中染色30min,去上清,用1%冰醋酸洗涤5次。最后加入200μL/孔10mmol/mL的Tris溶液溶解,用酶标仪测定570nm处的吸光值(A),用以下公式计算药物对细胞生长的抑制率,采用SigmaPlot10.0软件计算对肿瘤细胞半数致死浓度(IC50值)
细胞生长抑制率(%)=(1-A样品组/A阴性对照组)×100%。
实验结果如表1所示:
表1 化合物helicascolide A对肿瘤细胞的细胞毒活性n=3)
综合所述,化合物helicascolide A对神经胶质瘤细胞SF-268、乳腺癌细胞MCF-7、大细胞肺癌细胞NCI-H460、人肝癌细胞HepG-2具有很强的细胞毒活性,可应用于制备抗肿瘤药物。因此,本发明的实现为研究与开发新的抗肿瘤药物提供了候选药物,为开发利用植物内生真菌来源的天然活性物质提供了科学依据。
- 还没有人留言评论。精彩留言会获得点赞!
- 一种制备Kahalalide F的方法
- kahalalide F及相关化合物的制作方法
- Neonectrolide A在制备治疗促进小肠蠕动药物中的应用的制作方法
- Neonectrolide A在制备治疗或预防慢性心衰药物中的应用的制作方法
- Neonectrolide A在制备治疗肾功能不全药物中的应用的制作方法
- Neonectrolide A在制备治疗急性肾衰药物中的应用的制作方法
- KahalalideF制剂的制作方法
- Eryngiolide A在抑制肝脏成纤维细胞增殖药物中的应用的制作方法
- Eryngiolide A在备MAO抑制剂中的应用的制作方法
- Eryngiolide A在抗缺氧药物中的应用的制作方法
- Linderolide H在制备治疗前列腺癌药物中的应用的制作方法与工艺
- Linderolide H在制备治疗回盲肠癌药物中的应用的制作方法与工艺
- linderolide H 在制备防治肝脏损伤药物中的应用的制作方法与工艺
- Linderolide H 在制备降低血糖药物中的应用的制作方法与工艺
- Linderolide H在制备治疗急性痛风药物中的应用的制作方法与工艺
- Linderolide H在制备治疗膀胱癌药物中的应用的制作方法与工艺
- Tilifodiolide及其衍生物在制备治疗或预防II型糖尿病药物中的应用的制作方法与工艺
- Linderolide H在制备治疗肝癌药物中的应用的制造方法与工艺
- Linderolide H在制备治疗和预防肾纤维化药物中的应用的制造方法与工艺
- Linderolide H在制备治疗鼻炎药物中的应用的制造方法与工艺