一种呋喃官能化笼型多面体低聚倍半硅氧烷及其制备方法与流程
本发明属于有机/无机杂化材料领域,涉及一种呋喃官能化笼型多面体低聚倍半硅氧烷及其制备方法。
背景技术:
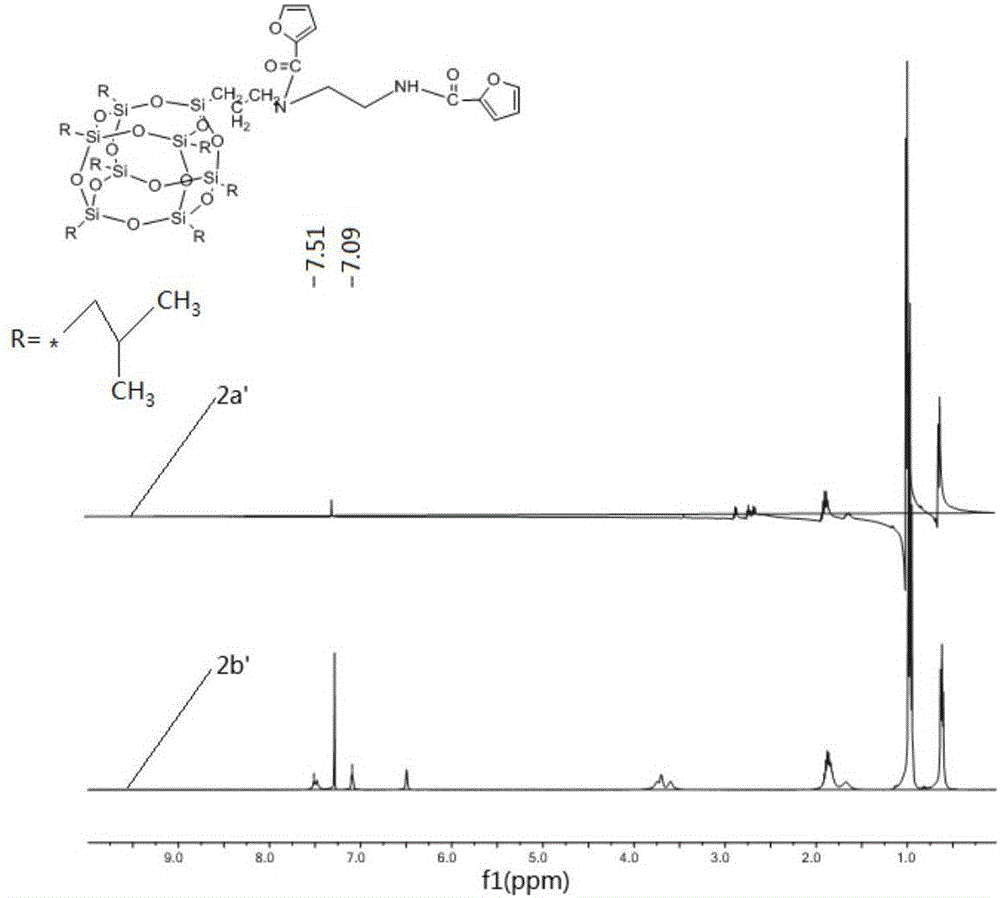
:多面体低聚倍半硅氧烷(POSS)是化学式为[RSiO1.5]n的物质总称,其中n可以为6、8、10、12等。常见多面体低聚倍半硅氧烷的结构包括无定型、梯形、笼型、半笼型和双塔型,其中,多面体低聚倍半硅氧烷(DDSQ)是一种特殊结构的POSS,其含有10个硅原子,自身具有优异的性能。多面体低聚倍半硅氧烷作为一种有机/无机杂化纳米材料,有着很多优异的性能,其不但具有有机材料密度低、溶解性好、热稳定好的优点,兼备灵活的官能化可设计性,还拥有无机材料强度高、耐高温的传统特点和纳米材料的量子尺寸效应、小尺寸效应等,正因为多面体低聚倍半硅氧烷集多种材料性能于一身,对它的研究也成为当前材料科学中的一个热点。目前,共有三种合成POSS的路线方法:(1)三氯硅烷水解缩合法;(2)用三氯硅烷或者三烷氧基硅烷将不完全笼形的倍半硅氧烷(T7-POSS)封端法;(3)以常见的POSS为原料,利用POSS上R基团的反应活性与不同的化合物反应生成新的种类的POSS的官能团衍生法(参见VoronkovMG,Lavrent'yevVI.Polyhedraloligosilsesquioxanesandtheirhomoderivatives[J].TopicsinCurrentChemistry,1982:199-236.);DDSQ单体的合成主要有以下两种方法:水解缩合法,官能团衍生法(参见Md.AsadulHoque,YurikoKakihana,SatoshiShinke,andYusukeKawakami.PolysiloxaneswithPeriodicallyDistributedIsomericDouble-DeckerSilsesquioxaneintheMainChain,Macromolecules2009)。现有技术对低聚倍半硅氧烷的研究,主要有以下几方向:(1)双羟基官能化,如KunWei,LeiWangandSixunZheng.Organic–inorganicpolyurethaneswith3,13-dihydroxypro-pyloctaphenyldouble-deckersilsesquioxanechainextender.Polym.Chem.,2013,4,1491;(2)叠氮官能化,如KunWei,LeiWang,SixunZheng.Organic–InorganicCopolymerswithDouble-DeckerSilsesquioxaneintheMainChainsbyPolymerizationviaClickChemistry.Journalofpolymerscience,PartA:Polymerchemistry,2013,51,4221;(3)炔基官能化,如中国专利201110442074.7,公开了一种含炔基的官能化笼型多面体聚倍半硅氧烷及其制备方法。在现有技术中尚未发现对POSS进行呋喃官能化的研究。技术实现要素:为了解决上述问题,本发明人进行了锐意研究,结果发现:以具有端烯基的笼型多面体低聚倍半硅氧烷与具有呋喃基团的硫醇反应,或者以具有端羧基的笼型多面体低聚倍半硅氧烷与具有呋喃官能团的胺反应,或者具有端胺基的笼型多面体低聚倍半硅氧烷与具有呋喃官能团的酰氯反应,均能够直接制得呋喃官能化笼型多面体低聚倍半硅氧烷,从而完成了本发明。本发明的目的在于提供以下方面:第一方面,本发明提供一种呋喃官能化笼型多面体低聚倍半硅氧烷,其特征在于,该呋喃官能化笼型多面体低聚倍半硅氧烷结构式如下式I、式II、式III和式IV所示:第二方面,本发明还提供一种制备上述第一方面中式I所示呋喃官能化笼型多面体低聚倍半硅氧烷的方法,其特征在于,所述方法包括以下步骤:(I-1)将八乙烯基笼型多面体低聚倍半硅氧烷与具有呋喃基团的硫醇混合,溶解于溶剂,向体系中加入热引发剂;(I-2)在加热搅拌的条件下进行反应,反应结束后,停止加热,纯化体系中制得的产物,得到固相产物;(I-3)将步骤I-2中制得的固相产物干燥,制得式I所示的呋喃官能化笼型多面体低聚倍半硅氧烷。第三方面,本发明还提供一种制备上述第一方面中式II所示呋喃官能化笼型多面体低聚倍半硅氧烷的方法,其特征在于,所述方法包括以下步骤:(II-1)将具有一个乙烯基的笼型多面体低聚倍半硅氧烷与呋喃基团的硫醇混合,溶解于溶剂,向体系中加入热引发剂;(II-2)在加热搅拌的条件下进行反应,反应结束后,停止加热,纯化 体系中制得的产物,得到固相产物;(II-3)将步骤II-2中制得的固相产物干燥,制得式II所示的呋喃官能化笼型多面体低聚倍半硅氧烷。第四方面,本发明还提供一种制备上述第一方面中式II所示呋喃官能化笼型多面体低聚倍半硅氧烷的方法,其特征在于,所述方法包括以下步骤:(II-1’)将具有端羧基的笼型多面体低聚倍半硅氧烷与具有呋喃基团的胺混合,溶解于溶剂,向体系中加入第一催化剂和缚水剂;(II-2’)在加热搅拌的条件下进行反应,反应结束后,停止加热,纯化体系中制得的产物,得到固相产物;(II-3’)将步骤II-2’中制得的固相产物干燥,制得式II所示的呋喃官能化笼型多面体低聚倍半硅氧烷。第五方面,本发明还提供一种制备上述第一方面中式III所示呋喃官能化笼型多面体低聚倍半硅氧烷的方法,其特征在于,所述方法包括以下步骤:(III-1)将具有一个氨丙基基团的笼型多面体低聚倍半硅氧烷与呋喃甲酰氯混合,溶解于溶剂,向体系中加入第二催化剂和第一缚酸剂;(III-2)在加热搅拌的条件下进行反应,反应结束后,停止加热,纯化体系中制得的产物,得到固相产物;(III-3)将步骤III-2中制得的固相产物干燥,制得式III所示的呋喃官能化笼型多面体低聚倍半硅氧烷。第六方面,本发明还提供一种制备上述第一方面中式IV所示呋喃官能化笼型多面体低聚倍半硅氧烷的方法,其特征在于,所述方法包括以下步骤:(IV-1)将具有两个氨基的笼型多面体低聚倍半硅氧烷与呋喃甲酰氯混合,溶解于溶剂,向体系中加入第三催化剂和第二缚酸剂;(IV-2)在加热搅拌的条件下进行反应,反应结束后,停止加热,纯化体系中制得的产物,得到固相产物;(IV-3)将步骤IV-2中制得的固相产物干燥,制得式IV所示的呋喃官能化笼型多面体低聚倍半硅氧烷。第七方面,本发明还提供上述第一方面所述呋喃官能化笼型多面体低聚倍半硅氧烷用于低介电材料及耐高温阻燃材料的用途。附图说明图1示出实施例1制得产品的红外光谱图;图2示出实施例1制得产品的1HNMR谱图;图3示出实施例2制得产品的红外光谱图;图4示出实施例2制得产品的1HNMR谱图;图5示出实施例3制得产品的红外光谱图;图6示出实施例3制得产品的1HNMR谱图。具体实施方式下面通过对本发明进行详细说明,本发明的特点和优点将随着这些说明而变得更为清楚、明确。以下详述本发明。根据本发明的第一方面,提供一种呋喃官能化笼型多面体低聚倍半硅氧烷,其特征在于,该呋喃官能化笼型多面体低聚倍半硅氧烷结构式如下式I、式II、式III和式IV所示:其中,在式I化合物中,D为在式II化合物、式III化合物和式IV化合物中,R各自独立地为氢、烷基、芳基、脂环基或其它有机基团;其中,所述烷基优选选自C1~C16的烷基,更优选选自C1~C8的烷基,如甲基、乙基、正丙基、异丙基、正丁基、异丁基、叔丁基等;和/或所述芳基优选选自苯基或取代苯基,更优选选自苯基和烷基取代苯基、磺基取代苯基、硝基取代苯基等,进一步优选选自苯基、对甲苯基、邻甲苯基、间甲苯基、对磺基苯基、间磺基苯基,如苯基;和/或所述脂环基优选选自C3~C8的脂环基,更优选选自C3~C6的脂环基,如 环丙烷基、环丁烷基、环戊烷基、环己烷基等;和/或所述其它有机基团优选选自腈基、硝基,更优选为腈基;在式II化合物中,n1为2~12,优选为2~5,如2或3;R’各自独立地选自其中,n为1~25,更优选为1~18,如1~12;n’为2~25,更优选为2~20,如2~12。根据本发明的第二方面,还提供一种制备第一方面中式I所示呋喃官能化笼型多面体低聚倍半硅氧烷的方法,其特征在于,所述方法包括以下步骤:步骤I-1,将八乙烯基笼型多面体低聚倍半硅氧烷与具有呋喃基团的硫醇混合,溶解于溶剂,向体系中加入热引发剂。在本发明中,所述八乙烯基笼型多面体低聚倍半硅氧烷为结构式如下式Ia所示的化合物,本发明中,八乙烯基笼型多面体低聚倍半硅氧烷可以为商购,也可以为由已知方法制备而得,如按照中国专利CN103172657A的方法制得的八乙烯基笼型多面体低聚倍半硅氧烷。在本发明中,所述具有呋喃基团的硫醇为在硫醇分子链上具有呋喃基团的化合物,优选选自糠硫醇、2-甲基-3-巯基呋喃、2-甲基-4-巯基呋喃、2,5-二甲基-3-呋喃硫醇等,优选选自糠硫醇、2-甲基-3-巯基呋喃,如糠硫醇。在本发明中,所述八乙烯基笼型多面体低聚倍半硅氧烷与所述具有呋喃基团的硫醇的摩尔比为八乙烯基笼型多面体低聚倍半硅氧烷的摩尔量:具有呋喃基团的硫醇的摩尔量=1:(8~20),优选为1:(9~18),其中,八乙烯基笼型多面体低聚倍半硅氧烷的摩尔量以八乙烯基笼型多面体低聚倍半硅氧烷分子的摩尔量计,具有呋喃基团的硫醇的摩尔量以具有呋喃基团的硫醇分子的摩尔量计。在本发明中,所述溶剂优选为有机溶剂,本发明对所述有机溶剂的种类不做特别限定,可以使用任意一种现有技术中能够溶解上述具有端烯基的笼型多面体低聚倍半硅氧烷和具有呋喃基团的硫醇的有机溶剂,如四氢呋喃、二氯甲烷、三氯甲烷、丙酮、甲醇、乙醇等,优选为四氢呋喃。在本发明步骤I-1中,将上述反应原料加入溶剂中充分溶解后,加入热引发剂,优选地,搅拌反应体系,使反应原料充分接触。在本发明中,对热引发剂不做特别限定,只要其能在加热条件下产生自由基引发反应即可,选自有机过氧化物类引发剂、无机过氧化物类引发剂、偶氮类引发剂,优选选自酰类过氧化物、氢过氧化物、二烷基过氧化物、酯 类过氧化物、酮类过氧化物、二碳酸酯过氧化物、过硫酸盐类化合物、偶氮二异腈类化合物,更优选选自过氧化苯甲酰、过氧化月桂酰、异丙苯过氧化氢、叔丁基过氧化氢、过氧化二叔丁基、过氧化二异丙苯、过氧化苯甲酸叔丁酯、过氧化叔戊酸叔丁基酯、过氧化甲乙酮、过氧化环己酮、过氧化二碳酸二异丙酯、过氧化二碳酸二环己酯、过硫酸钾、过硫酸钠、过硫酸铵、偶氮二异丁腈、偶氮二异庚腈。在本发明中,所述热引发剂与八乙烯基笼型多面体低聚倍半硅氧烷的重量比为热引发剂的重量:八乙烯基笼型多面体低聚倍半硅氧烷的摩尔量=(0.5~3):100,优选为(1~2.5):100,如2:100。步骤I-2,在加热搅拌的条件下进行反应,反应结束后,停止加热,纯化体系中制得的产物,得到固态产物。在本发明中,加热的温度根据所用的热引发剂来确定,以加热的温度能够使热引发剂分解产生自由基为优选,如,当使用偶氮二异丁腈(AIBN)为热引发剂时,选择加热温度为30℃~150℃,优选为50℃~120℃,更优选60℃~100℃,如90℃。在本发明中,加热的时间选择0.5~15h,优选为1~12h,更优选为3~10h,如8h。当反应结束后,停止加热,并对体系中制得的产物进行纯化,本发明对纯化的方法不做特别限定,可以使用现有技术中任意一种能够纯化的方法。在本发明一种优选的实施方式中,采用包括以下子步骤的方法进行纯化:子步骤I-2-1,用水对反应体系进行洗涤。本发明对洗涤方法不做特别限定,可以使用现有技术中任意一种用水对有机体系进行洗涤的方法,如萃取法等,优选采用萃取的方法进行洗涤,更优选地,洗涤3次。子步骤I-2-2,除去洗涤后体系中的溶剂。本发明对除去溶剂的方法不做特别限定,可以使用现有技术中任意一种除去溶剂的方法,如自然挥发法、减压蒸馏法等。在本发明另一种优选的实施方式中,采用结晶的方法进行纯化,其包括以下步骤:子步骤I-2-1’,向反应体系中加入产物的不良溶剂,使其结晶析出。在本发明中,所述产物的不良溶剂是指易与体系中溶剂混溶,且产物在其中的溶解度小,易于析出结晶的溶剂,本发明对产物的不良溶剂不做特别限定,以制得产物在其中溶解度小,且易与反应体系的溶剂混溶为优选,如水、甲醇、乙醚、乙腈等,优选为水和乙醚。在本发明中,不良溶剂与反应体系中溶剂的体积比优选为不良溶剂的体积:反应体系中溶剂的体积=5:1~15:1,优选为7:1~13:1,更优选为8:1~11:1,如10:1。本发明人发现,向体系中加入的不良溶剂越多,产物的析晶效果越好,收率越高,但为了节约成本,本发明选择上述体积比。子步骤I-2-2’,将子步骤1-1’得到的固液混合体系过滤,得到固相产物。本发明对过滤的方法不做特别限定,可以使用现有技术中任意一种固液分离的方法,如常压过滤、减压过滤等,优选为减压过滤。步骤I-3,将步骤I-2中制得的固相产物干燥,制得式I所示的呋喃官能化笼型多面体低聚倍半硅氧烷。本发明对干燥的方法不做特别限定,可以使用现有技术中任意一种能够干燥固态产物的方法,如自然干燥法、常压加热干燥法和减压加热干燥法等,优选为减压加热干燥法。在使用加热干燥法时,加热温度选择低于产物 的熔点,优选为30℃~50℃,如40℃。根据本发明的第三方面,还提供一种制备第一方面中式II所示呋喃官能化笼型多面体低聚倍半硅氧烷的方法,其特征在于,所述方法包括以下步骤:步骤II-1,将具有一个乙烯基的笼型多面体低聚倍半硅氧烷与具有呋喃基团的硫醇混合,溶解于溶剂,向体系中加入热引发剂。在本发明中,所述具有一个端烯基的笼型多面体低聚倍半硅氧烷是指在笼型多面体低聚倍半硅氧烷一个硅原子上连接有端烯基基团,而其它硅原子上连接有非端烯基基团的笼型多面体低聚倍半硅氧烷,优选为结构式如IIa所示的化合物,其中,R各自独立地为氢、烷基、芳基、脂环基或其它有机基团,其中,所述烷基优选选自C1~C16的烷基,更优选选自C1~C8的烷基,如甲基、乙基、正丙基、异丙基、正丁基、异丁基、叔丁基等;所述芳基优选选自苯基或取代苯基,更优选选自苯基和烷基取代苯基、磺基取代苯基、硝基取代苯基等,进一步优选选自苯基、对甲苯基、邻甲苯基、间甲苯基、对磺基苯基、间磺基苯基,如苯基;所述脂环基优选选自C3~C8的脂环基,更优选选自C3~C6的脂环基,如环丙烷基、环丁烷基、环戊烷基、环己烷基等;所述其它有机基团优选选自腈基、硝基,更优选为腈基;n2为0~10,优选为0~3。优选地,所述具有一个端烯基的笼型多面体低聚倍半硅氧烷为结构式如下式IIb所示的化合物:其中,n2为0~10,优选为0~3;更优选地,所述具有一个端烯基的笼型多面体低聚倍半硅氧烷为结构式如下式IIc和式IId所示的化合物:在本发明中,所述具有呋喃基团的硫醇的选择如上述第二方面中步骤I-1中所述。在本发明中,所述具有一个端烯基的笼型多面体低聚倍半硅氧烷与所述具有呋喃基团的硫醇的摩尔比为具有一个端烯基的笼型多面体低聚倍半硅氧烷的摩尔量:具有呋喃基团的硫醇的摩尔量=1:(2~10),优选为1:(3~8),其中,具有一个端烯基的笼型多面体低聚倍半硅氧烷的摩尔量以具有一个端烯基的笼型多面体低聚倍半硅氧烷分子的摩尔量计,具有呋喃基团的硫醇的摩尔量以具有呋喃基团的硫醇分子的摩尔量计。在步骤II-1中,所述溶剂的选择如上述第二方面中步骤I-2中所述。在步骤II-1中,所述热引发剂的选择如上述第二方面中步骤I-2中所述。在本发明中,所述热引发剂与具有一个端烯基的笼型多面体低聚倍半硅氧烷的重量比为热引发剂的重量:具有一个端烯基的笼型多面体低聚倍半硅氧烷的重量=(0.5~3):100,优选为(1~2.5):100,如2:100。步骤II-2,在加热搅拌的条件下进行反应,反应结束后,停止加热,纯化体系中制得的产物,得到固相产物。在步骤II-2中,加热温度的选择如上述第二方面中步骤I-2中所述。在步骤II-2中,加热时间的选择如上述第二方面中步骤I-2中所述。在步骤II-2中,纯化方法的选择如上述第二方面中步骤I-2中所述。步骤II-3,将步骤II-2中制得的固相产物干燥,制得式II所示的呋喃官能化笼型多面体低聚倍半硅氧烷。在步骤II-3中,干燥方法的选择如上述第二方面中步骤I-3中所述。优选地,制得的呋喃官能化笼型多面体低聚倍半硅氧烷的结构式优选为如下式IIc’和式IId’所示:根据本发明的第四方面,还提供一种制备上述第一方面中式II所示呋喃官能化笼型多面体低聚倍半硅氧烷的方法,其特征在于,所述方法包括以下步骤:步骤II-1’,将具有端羧基的笼型多面体低聚倍半硅氧烷与具有呋喃基团的胺混合,溶解于溶剂,向体系中加入第一催化剂和缚水剂。在本发明中,所述具有端羧基的笼型多面体低聚倍半硅氧烷优选选自具有端单羧基的笼型多面体低聚倍半硅氧烷和/或具有端双羧基的笼型多面体低聚倍半硅氧烷,进一步优选选自如下式IIe、式IIf、式IIg和式IIh所示的笼型多面体低聚倍半硅氧烷:其中,R各自独立地为氢、烷基、芳基、脂环基或其它有机基团,其中,所述烷基优选选自C1~C16的烷基,更优选选自C1~C8的烷基,如甲基、乙基、正丙基、异丙基、正丁基、异丁基、叔丁基等;所述芳基优选选自苯基或取代苯基,更优选选自苯基和烷基取代苯基、磺基取代苯基、硝基取代苯基等,进一步优选选自苯基、对甲苯基、邻甲苯基、间甲苯基、对磺基苯基、间磺基苯基,如苯基;所述脂环基优选选自C3~C8的脂环基,更优选选自C3~C6的脂环基,如环丙烷基、环丁烷基、环戊烷基、环己烷基等;所述其它有机基团优选选自腈基、硝基,更优选为腈基;在本发明一个优选的实施方式中,R优选为异丁基。在本发明一个优选的实施方式中,所述具有端羧基的笼型多面体低聚倍半硅氧烷优选为结构式如式IIi、式IIj、式IIk和IIn式的化合物:在本发明一个优选的实施方式中,具有端羧基的笼型多面体低聚倍半硅氧烷是按照包括以下子步骤的方法制得的:子步骤II-1’-1,将具有端烯基的笼型多面体低聚倍半硅氧烷和具有端羧基的硫醇混合、溶解于溶剂,向体系中加入热引发剂。在本发明中,具有端烯基的笼型多面体低聚倍半硅氧烷优选如步骤I-1中所述。在本发明中,所述具有羧基的硫醇在硫醇的主链上具有羧基基团的化合物,优选选自2-巯基乙酸、3-巯基丙酸、巯基丁二酸,更优选选自2-巯基乙酸和/或巯基丁二酸。在本发明中,所述具有端烯基的笼型多面体低聚倍半硅氧烷与所述具有羧基基团的硫醇的摩尔比为具有端烯基的笼型多面体低聚倍半硅氧烷的摩尔量:具有羧基基团的硫醇的摩尔量=1:(2~5),其中,具有端烯基的笼型多面体低聚倍半硅氧烷的摩尔量以具有端烯基的笼型多面体低聚倍半硅氧烷分子的摩尔量计,具有羧基基团的硫醇的摩尔量以具有羧基基团的硫醇分子的摩尔量计。在子步骤II-1’-1中,所述溶剂如步骤I-1中所述。在子步骤II-1’-1中,将上述反应原料加入溶剂中充分溶解后,加入热引发剂,优选地,搅拌反应体系,使反应原料充分接触。在子步骤II-1’-1中,所述热引发剂如步骤I-1中所述。子步骤II-1’-2,在加热搅拌的条件下进行反应,反应结束后,停止加 热,纯化体系中制得的产物,得到固态产物。在子步骤II-1’-2中,加热温度的选择如步骤I-2中所述。在子步骤II-1’-2中,加热时间的选择如步骤I-2中所述。在子步骤II-1’-2中,对体系中制得产物纯化方法的选择如步骤I-2中所述。子步骤II-1’-3,将步骤II-1’-2中制得的固态产物干燥,制得具有端烯基的笼型多面体低聚倍半硅氧烷。在本发明另一个优选的实施方式中,具有端羧基的笼型多面体低聚倍半硅氧烷是按照包括以下子步骤的方法制得的:子步骤II-1’-1’,将含有端烯基的笼型多面体低聚倍半硅氧烷和含有端羧基的硫醇混合,溶解于溶剂中,向体系中加入光引发剂。在子步骤II-1’-1’中,所述含有端烯基的笼型多面体低聚倍半硅氧烷如子步骤II-1’-1中所述。在子步骤II-1’-1’中,所述含有端羧基的硫醇如子步骤II-1’-1中所述。在子步骤II-1’-1’中,所述溶剂如子步骤II-1’-1中所述。在子步骤II-1’-1’中,对所述光引发剂不做特别限定,只要其能在紫外光照射下产生自由基,引发反应即可,优选选自2-羟基-2-甲基-1-苯基丙酮、2-甲基-2-(4-吗啉基)-1-[4-(甲硫基)苯基]-1-丙酮、1-羟基环己基苯基甲酮、二苯甲酮、安息香甲醚、4-二甲氨基吡啶,更优选为4-二甲氨基吡啶(DMAP)。在本发明中,可以单独使用选自上述光引发剂中的任一种,或任意组合使用其中的多种。子步骤II-1’-2’,将子步骤II-1’-1’中的反应体系在紫外光照射下反应。在子步骤II-1’-2’中,所选择的紫外光能够使得光引发剂产生自由基,从而引发反应即可,优选紫外光的波长为250~400nm,优选照射时间为0.5~12h,优选为1~10h,更优选为3~8h,如5h。子步骤II-1’-3’,反应结束后,纯化体系中制得的产物,得到固态产物。在子步骤II-1’-2’中,对体系中制得产物的纯化方法如子步骤II-1’-2中所述。子步骤II-1’-4’,将步骤II-1’-3’中制得的固态产物干燥,制得具有端烯基的笼型多面体低聚倍半硅氧烷。在步骤II-1’中,所述具有呋喃基团的胺是指在胺主链上具有呋喃基团的化合物,优选选自糠胺、3-氨基-5-(2-呋喃基)吡唑、5-呋喃-2-1,3,4-恶二唑-2-氨基、2-氨基呋喃-3-腈和3-氨基呋喃-2-甲醛3-氨基呋喃-2-甲醛等,更优选选自糠胺、3-氨基呋喃-2-甲醛,如糠胺。在步骤II-1’中,具有端羧基的笼型多面体低聚倍半硅氧烷与具有呋喃基团的胺的摩尔比为具有端羧基的笼型多面体低聚倍半硅氧烷的摩尔量:具有呋喃基团的胺的摩尔量=1:(2~10),优选为1:(3~8),其中,具有端羧基的笼型多面体低聚倍半硅氧烷的摩尔量以具有端羧基的笼型多面体低聚倍半硅氧烷分子的摩尔量计,具有呋喃基团的胺的摩尔量以具有呋喃基团的胺分子的摩尔量计。在步骤II-1’中,所述溶剂如步骤I-1中所述。在步骤II-1’中,对所述第一催化剂不做特别限定,以能够催化反应为优选,优选选自4-二甲氨基吡啶(DMAP)、二环己基碳二亚胺(DCC)、N,N'-二异丙基碳二亚胺(DIC)、1-乙基-3-(3-二甲胺丙基)碳二亚胺盐酸盐(EDCI)、[1-(3-二甲氨基丙基)-3-乙基碳二亚胺](EDC)、六氟磷酸苯并三唑-1-氧基三(二甲氨基)磷(BOP)、2-(7-偶氮苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(HATU)和2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲四氟硼酸盐(TATU)中的一种或多种,优选选自4-二甲氨基吡啶(DMAP)二环己基碳二亚胺(DCC)、N,N'-二异丙基碳二亚胺(DIC)、1-乙基-3-(3-二甲胺丙基)碳二亚胺盐酸盐(EDCI)和[1-(3-二甲氨基丙基)-3-乙基碳二亚胺](EDC) 中的一种或多种,更优选为4-二甲氨基吡啶(DMAP)。所述第一催化剂与具有端羧基的笼型多面体低聚倍半硅氧烷的重量比为第一催化剂的重量:具有端羧基的笼型多面体低聚倍半硅氧烷的重量=(0.5~3):100,优选为(1~2.5):100,如2:100。在步骤II-1’中,所述缚水剂能够吸附反应过程中生成的水,本发明对缚水剂不做特别限定,优选选自1-乙基-3-(3-二甲胺丙基)碳二亚胺盐酸盐(EDCI)、五氧化二磷、碳酸钾、分子筛、无水硫酸镁、无水硫酸钾等中的一种或多种,更优选为1-乙基-3-(3-二甲胺丙基)碳二亚胺盐酸盐(EDCI)。所述缚水剂与具有端羧基的笼型多面体低聚倍半硅氧烷的摩尔比为缚水剂的摩尔量:具有端羧基的笼型多面体低聚倍半硅氧烷摩尔量=(1.0~3.0):1,优选为(1~1.2):1,其中,缚水剂的摩尔量以缚水剂分子的摩尔量计,具有端羧基的笼型多面体低聚倍半硅氧烷的摩尔量以具有端羧基的笼型多面体低聚倍半硅氧烷分子的摩尔量计。步骤II-2’,在加热搅拌的条件下进行反应,反应结束后,停止加热,纯化体系中制得的产物,得到固相产物。在步骤II-2’中,加热的温度如步骤II-2中所述。在步骤II-2’中,加热的时间如步骤II-2中所述。在步骤II-2’中,对体系中制得产物的纯化方法如步骤II-2中所述。步骤II-3’,将步骤II-2’中制得的固相产物干燥,制得式II所示的呋喃官能化笼型多面体低聚倍半硅氧烷。在步骤II-3’中,干燥的方法如步骤II-3中所述。在本发明一个优选的实施方式中,制得的呋喃官能化笼型多面体低聚倍半硅氧烷的结构式优选为如下式IIi’、式IIj’、式IIk’和式IIn’所示:根据本发明的第五方面,本发明还提供一种制备上述第一方面中式III所示呋喃官能化笼型多面体低聚倍半硅氧烷的方法,其特征在于,所述方法包括以下步骤:步骤III-1,将具有一个氨丙基基团的笼型多面体低聚倍半硅氧烷与呋喃甲酰氯混合,溶解于溶剂,向体系中加入第二催化剂和第一缚酸剂。在本发明中,所述具有一个氨丙基基团的笼型多面体低聚倍半硅氧烷优选结构式如下式IIIa所示的化合物:其中,R的选择范围如步骤II-1’中所述;在本发明一个优选的实施方式中,R为异丁基。在本发明中,所述具有两个氨基的笼型多面体低聚倍半硅氧烷可以为商购,也可以为根据已知方法制备而得。在步骤III-1中,所述溶剂的选择范围如上述第二方面步骤I-1中所述。在步骤III-1中,对所述第二催化剂不做特别限定,以能够催化反应为优选,优选选自4-二甲氨基吡啶(DMAP)、二环己基碳二亚胺(DCC)、N,N'-二异丙基碳二亚胺(DIC)、1-乙基-3-(3-二甲胺丙基)碳二亚胺盐酸盐(EDCI)、[1-(3-二甲氨基丙基)-3-乙基碳二亚胺](EDC)、六氟磷酸苯并三唑-1-氧基三(二甲氨基)磷(BOP)、2-(7-偶氮苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(HATU)和2-(7-氮杂苯并三氮唑)-N,N,N',N'-四甲基脲四氟硼酸盐(TATU)中的一种或多种,优选选自4-二甲氨基吡啶(DMAP)二环己基碳二亚胺(DCC)、N,N'-二异丙基碳二亚胺(DIC)、1-乙基-3-(3-二甲胺丙基) 碳二亚胺盐酸盐(EDCI)和[1-(3-二甲氨基丙基)-3-乙基碳二亚胺](EDC)中的一种或多种,更优选为4-二甲氨基吡啶(DMAP)。在步骤III-1中,所述第二催化剂与具有一个氨丙基基团的笼型多面体低聚倍半硅氧烷的重量比为第二催化剂的重量:具有一个氨丙基基团的笼型多面体低聚倍半硅氧烷的重量=(0.5~3):100,优选为(1~2.5):100,如2:100。所述第一缚酸剂选自有机弱碱性化合物和无机碱性物质,优选为吡啶、三乙胺、乙二胺和碳酸钾中的一种或多种。所述第一缚酸剂与具有一个氨丙基基团的笼型多面体低聚倍半硅氧烷的摩尔比为第一缚酸剂的摩尔量:具有一个氨丙基基团的笼型多面体低聚倍半硅氧烷的摩尔量=(1.0~3.0):1,优选为(1~1.2):1,其中,第一缚酸剂的摩尔量以第一缚酸剂分子的摩尔量计,具有一个氨丙基基团的笼型多面体低聚倍半硅氧烷的摩尔量以具有一个氨丙基基团的笼型多面体低聚倍半硅氧烷分子的摩尔量计。步骤III-2,在加热搅拌的条件下进行反应,反应结束后,停止加热,纯化体系中制得的产物,得到固相产物。在步骤III-2中,加热温度的选择如步骤II-2中所述。在步骤III-2中,加热时间的选择如步骤II-2中所述。在步骤III-2中,对体系中制得产物的纯化方法如步骤II-2中所述。步骤III-3,将步骤III-2中制得的固相产物干燥,制得式III所示的呋喃官能化笼型多面体低聚倍半硅氧烷。在步骤III-3中,干燥的方法如步骤II-3中所述。在本发明一个优选的实施方式中,制得产物的结构式如下式IIIa’所示:根据本发明的第六方面,还提供一种制备上述第一方面中式IV所示呋喃官能化笼型多面体低聚倍半硅氧烷的方法,其特征在于,所述方法包括以下步骤:步骤IV-1,将具有两个氨基的笼型多面体低聚倍半硅氧烷与呋喃甲酰氯混合,溶解于溶剂,向体系中加入第三催化剂和第二缚酸剂。在本发明中,所述具有两个氨基的笼型多面体低聚倍半硅氧烷优选结构式如下式IVa所示的化合物:其中,R的选择范围如步骤II-1’中所述;在本发明一个优选实施方式中,R为异丁基。在本发明中,所述具有两个氨基的笼型多面体低聚倍半硅氧烷可以为商购,也可以为根据已知方法制备而得。在步骤IV-1中,所述溶剂的选择范围如上述第二方面步骤I-1中所述。在步骤IV-1中,所述第三催化剂的选择范围与上述第五方面步骤III-1中第二催化剂选择范围相同。在步骤IV-1中,所述第三催化剂与具有两个氨基的笼型多面体低聚倍半硅氧烷的重比为第三催化剂的重量:具有两个氨基的笼型多面体低聚倍半硅氧烷的重量=(0.5~3):100,优选为(1~2.5):100,如2:100。在步骤IV-1中,所述第二缚酸剂的选择范围与上述第五方面步骤III-1中第一缚酸剂选择范围相同。所述第二缚酸剂与具有两个氨基的笼型多面体低聚倍半硅氧烷的摩尔比为第二缚酸剂的摩尔量:具有两个氨基的笼型多面体低聚倍半硅氧烷的摩尔量=(1.0~3.0):1,优选为(1~1.2):1,其中,第二缚酸剂的摩尔量以第二缚酸剂分子的摩尔量计,具有两个氨基的笼型多面体低聚倍半硅氧烷的摩尔量以具有两个氨基的笼型多面体低聚倍半硅氧烷分子的摩尔量计。步骤IV-2,在加热搅拌的条件下进行反应,反应结束后,停止加热,纯化体系中制得的产物,得到固相产物。在步骤IV-2中,加热温度的选择如步骤II-2中所述。在步骤IV-2中,加热时间的选择如步骤II-2中所述。在步骤IV-2中,对体系中制得产物的纯化方法如步骤II-2中所述。步骤IV-3,将步骤IV-2中制得的固相产物干燥,制得式IV所示的呋喃官能化笼型多面体低聚倍半硅氧烷。在步骤IV-3中,干燥的方法如步骤II-3中所述。在本发明一个优选的实施方式中,制得产物的结构式如下式IVa’所示:根据本发明的第七方面,还提供上述第一方面所述呋喃官能化笼型多面体低聚倍半硅氧烷用作低介电材料添加剂及耐高温阻燃材料添加剂的用途。本发明人经大量研究发现,将本发明提供的呋喃官能化笼型多面体低聚倍半硅氧烷作为添加剂改性聚合物时,制得聚合物的介电常数降低、耐火性增强,因此,适于制备低介电材料及耐高温阻燃材料。此外,本发明人还发现,本发明提供的呋喃官能化笼型多面体低聚倍半硅氧烷,具有密度低、在有机溶剂中的溶解性好、与其它聚合物的相容性好、热稳定好、介电常数小、电导率低的优点,其上的呋喃官能轩兼备灵活的官能化可设计性,可与其它官能团反应,进而对多面体低聚倍半硅氧烷进 行进一步的结构优化,而且,本发明提供的呋喃官能化笼型多面体低聚倍半硅氧烷还拥有无机材料强度高、耐高温的传统特点,由于其分散于其它聚合物中以纳米尺寸的粒子存在,因此,其存在量子尺寸效应、小尺寸效应等,更重要的是,由于笼型多面体低聚倍半硅氧烷的两个端部具有活性官能团,因此,可以直接引入聚合物反应中,参加反应。将具有上述优异性能的双官能化笼多面体低聚倍半硅氧烷直接引入到聚合物的骨架上,能够使得制备得到的改性聚合物更加稳定。根据本发明提供的呋喃官能化笼型多面体低聚倍半硅氧烷及其制备方法和用途,具有以下有益效果:(1)本发明提供的呋喃官能化笼型多面体低聚倍半硅氧烷用作添加剂,能够使制得的产品介电常数小,导电率低,化学性质稳定,适于制备低介电材料;(2)本发明提供的呋喃官能化笼型多面体低聚倍半硅氧烷用作添加剂,能够使制得的产品导热系数低,不易燃烧,适于制备阻燃耐火材料;(3)本发明提供的制备方法简单易行,只需要一步反应即可制得产品,反应时间短,反应过程易于控制操作,后处理简便,易于提纯,产率高;(4)本发明提供的制备方法原料来源广泛,易于获取,生产成本低;(5)本发明提供的制备方法适用于具有特定基团的一类呋喃官能化笼型多面体低聚倍半硅氧烷的制备。实施例(一)红外(IR)测试采用美国Nicolet公司Nexsus670-FTIR,KBr涂膜,扫描范围:4000cm-1~400cm-1,对实施例制备得到的产物进行红外测试。(二)核磁(1H-NMR)测试采用BrukerAvance400MHz液体核磁共振谱仪,氘代氯仿为溶剂,在室温(25℃)下对实施例制备得到的产物进行测试。(三)八乙烯基笼型多面体低聚倍半硅氧烷(结构式如下式Ia所示)的制备制备方法参见中国专利CN103172657A。(四)七异丁基乙烯基笼型多面体低聚倍半硅氧烷(结构式如下式IIc所示)的制备制备方法参见张韬毅,张倩,李滔等.单官能POSS的合成及性质研究[J].化工新型材料,2013,41(3).DOI:10.3969/j.issn.1006-3536.2013.03.029.。(五)单氨基笼型多面体低聚倍半硅氧烷,购自Hybridplastics,商品名为AM0265-AminopropylIsobutyl其结构式如下式所示(六)双氨基笼型多面体低聚倍半硅氧烷,购自Hybridplastics,商品名为AM0275-AminoethylaminopropylIsobutyl其结构式如下式所示(七)七异丁基烯丙基笼型多面体低聚倍半硅氧烷(结构式如下式IId所示)的制备实施例11)将6.122g(7mmol)(五)中所述单氨基笼型多面体低聚倍半硅氧烷和0.758ml(7.7mmol)呋喃甲酰氯,完全溶解在40ml二氯甲烷中,然后加入0.123g引发剂DMAP,0.62ml缚酸剂吡啶,搅拌均匀;2)将反应体系置于40℃的恒温油浴中回流15h,进行缩合反应;3)反应结束后,将反应体系用200ml去离子水分三次进行洗涤,再减压除去有机相中的溶剂,将所得固相产物在40℃下真空干燥,得到单呋喃基的笼型多面体低聚倍半硅氧烷(即,单呋喃基POSS),产率为90%。对上述所得单呋喃基POSS按照(一)的方法进行红外(IR)测试,按照(二)的方法进行核磁测试(1H-NMR),以表征产物结构。所得产物的IR谱图如图1所示,其中,曲线1a表示原料单氨基POSS的红外光谱曲线,曲线1b表示产物单呋喃POSS的红外光谱曲线,由图1可知:与原料单氨基POSS相比,在1680cm-1羰基的红外特征吸收峰,在1536cm-1处出呋喃基团的红外吸收特征峰,在1110cm-1处为硅氧键的红外吸收特征峰,证明POSS的骨架结构没有发生变化。所得产物的1H-NMR谱图如图2所示,由图2可知:合成出的单呋喃POSS与单氨基POSS相比上氨基的质子峰由在δ=2.85ppm转移到δ=3.45ppm处消失;异丁基上次甲基,甲基,亚甲基上氢的质子峰依次在δ=1.97ppm,δ=0.97ppm,δ=0.65ppm处;与氮原子相连的亚甲基的质子峰在分别在δ=1.22ppm,δ=1.51ppm,δ=3.39ppm处。在δ=7.45ppm,δ=7.13ppm,δ=6.46ppm出现了呋喃质子峰。综上可知,实施例1中成功制备了单呋喃基POSS,结构式如下式所示:实施例21)将3.384g(3.483mmol)(六)中所述双氨基笼型多面体低聚倍半硅氧烷和0.758ml(7.7mmol)呋喃甲酰氯,完全溶解在40ml二氯甲烷中,然后加入0.102g引发剂DMAP,0.62ml缚酸剂吡啶,搅拌均匀;2)将反应体系置于50℃的恒温油浴中回流8h,进行缩合反应;3)反应结束后,将反应体系用200ml去离子水分三次进行洗涤,再减压除去有机相中的溶剂,将所得固相产物在40℃下真空干燥,得到双呋喃基的笼型多面体低聚倍半硅氧烷(即,双呋喃基POSS),产率为90%。对上述所得单呋喃基POSS按照(一)的方法进行红外(IR)测试,按照(二)的方法进行核磁测试(1H-NMR),以表征产物结构。所得产物的IR谱图如图3所示,其中,曲线2a表示原料单氨基POSS的红外光谱曲线,曲线2b表示产物单呋喃POSS的红外光谱曲线,由图3可知:与原料双氨基POSS相比,在1622cm-1羰基的红外特征吸收峰,在1528cm-1处出呋喃基团的红外吸收特征峰。所得产物的1H-NMR谱图如图4所示,其中,曲线2a’表示原料单氨基POSS的1H-NMR谱曲线,曲线2b’表示产物单呋喃POSS的1H-NMR谱曲线,由图4可知:双氨基POSS由于发生酰胺化反应,氨基质子峰由δ=2.90移至δ=3.70;而呋喃基特征谱线则从δ=7.76,7.49,6.64分别移至δ=7.51,7.09,6.50。产物中同时出现氨基、呋喃基特征谱线,且与POSS笼连接的亚甲基信号峰基本不变。综上可知,实施例2中成功制备了双呋喃基酰胺POSS,结构式如下式所示:实施例31)将3g(3.6mmol)(四)中制得的七异丁基乙烯基笼型多面体低聚倍半硅氧烷和1.0688g(7.12mmol)的巯基丁二酸,完全溶解在50ml四氢呋喃 中,然后加入0.06g引发剂偶氮二异丁腈搅拌均匀;2)将反应体系置于90℃的恒温油浴中回流10h,进行热引发反应;3)反应结束后,将反应液滴加到200ml乙醚中进行析晶,减压过滤,将过滤所得固相产物在50℃下真空干燥,得到双羧基含硫的笼型多面体低聚倍半硅氧烷,产率为90%;4)将步骤3制得的产物1.01mmol,与0.23mL(2.5mmol)糠胺混合,溶解于40mL二氯甲烷中,向体系中加入0.0449g引发剂DMAP,0.386g缚水剂EDCI搅拌均匀;5)将反应体系置于40℃的恒温油浴中回流5h,进行缩合反应;6)反应结束后,将反应液滴加到150ml乙醚中进行沉淀,减压过滤,将过滤所得固相产物在35℃下真空干燥,得到双呋喃基酰胺的笼型多面体低聚倍半硅氧烷(双呋喃基酰胺POSS),产率90%。对上述所得双呋喃基POSS按照(一)的方法进行红外(IR)测试,按照(二)的方法进行核磁测试(1H-NMR),以表征产物结构。所得产物双呋喃基POSS的IR谱图如图5所示,其中,曲线3a表示原料双羧基POSS的红外光谱曲线,曲线2b表示产物双呋喃酰胺POSS的红外光谱曲线,由图5可知:七异丁基双羧基POSS谱图中1717cm-1处羧基中C=O键的伸缩振动特征吸收峰在双呋喃酰胺POSS的IR谱图中出现在1646cm-1处,而且在图中1550cm-1处出现了亚氨基伸缩振动特征吸收峰。所得产物双呋喃基POSS的1H-NMR谱图如图6所示,由图6可知:呋喃环质子峰出现在6.17-6.34ppm,其相邻的亚甲基上的氢原子的质子峰分别出现在δ=6.17,δ=6.34ppmδ=7.38ppm亚氨基中氢原子的质子峰出现在δ=6.93ppm处,异丁基中甲基、亚甲基和次甲基上氢(b,a,c)的质子峰分别出现在δ=0.97-0.99ppm、δ=0.62-0.64ppm与δ=1.83-1.92ppm处。综上可知,实施例3中成功制备了双呋喃基酰胺POSS,结构式如下式所示:实施例41)将3g(3.6mmol)(四)中制得的七异丁基乙烯基笼型多面体低聚倍半硅氧烷和0.499ml(7.2mmol)的2-巯基乙酸,完全溶解在40ml四氢呋喃中,然后加入0.06g引发剂偶氮二异丁腈搅拌均匀;2)将反应体系置于90℃的恒温油浴中回流10h,进行热引发反应;3)反应结束后,将反应液滴加到200ml乙醚中进行析晶,减压过滤,将过滤所得固相产物在50℃下真空干燥,得到单羧基含硫的笼型多面体低聚倍半硅氧烷,产率为90%;4)将步骤3制得的产物1.01mmol,与0.23mL(2.5mmol)呋喃甲酰氯混合,溶解于40mL二氯甲烷中,向体系中加入0.0449g引发剂DMAP,0.386g缚水剂EDCI搅拌均匀;5)将反应体系置于40℃的恒温油浴中回流5h,进行热引发反应;6)反应结束后,将反应液滴加到150ml乙醚中进行沉淀,减压过滤,将过滤所得固相产物在35℃下真空干燥,得到单呋喃基酰胺的笼型多面体低 聚倍半硅氧烷(单呋喃基酰胺POSS),产率90%,结构式如下式所示:实施例51)将3.05g(3.6mmol)(七)中制得的七异丁基烯丙基笼型多面体低聚倍半硅氧烷和0.649g(4.32mmol)的巯基丁二酸,完全溶解在30ml四氢呋喃中,然后加入0.06g引发剂偶氮二异丁腈搅拌均匀;2)将反应体系置于90℃的恒温油浴中回流10h,进行热引发反应;3)反应结束后,将反应液滴加到200ml乙醚中进行析晶,减压过滤,将过滤所得固相产物在50℃下真空干燥,得到双羧基含硫的笼型多面体低聚倍半硅氧烷,产率为90%;4)将步骤3制得的产物1.01mmol,与0.23mL(2.5mmol)糠胺混合,溶解于40mL二氯甲烷中,向体系中加入0.0449g引发剂DMAP,0.386g缚水剂EDCI搅拌均匀;5)将反应体系置于40℃的恒温油浴中回流12h,进行热引发反应;6)反应结束后,将反应液滴加到150ml乙醚中进行沉淀,减压过滤,将过滤所得固相产物在35℃下真空干燥,得到双呋喃基酰胺的笼型多面体低聚倍半硅氧烷(双呋喃基酰胺POSS),产率90%,结构式如下式所示:实施例61)将2g(2.4mmol)(七)中制得的七异丁基烯丙基笼型多面体低聚倍半硅氧烷和0.25ml(3.6mmol)的2-巯基乙酸,完全溶解在35ml四氢呋喃中,然后加入0.04g引发剂偶氮二异丁腈搅拌均匀;2)将反应体系置于90℃的恒温油浴中回流10h,进行热引发反应;3)反应结束后,将反应液滴加到200ml乙醚中进行析晶,减压过滤,将过滤所得固相产物在50℃下真空干燥,得到单羧基含硫的笼型多面体低聚倍半硅氧烷,产率为90%;4)将步骤3制得的产物1.01mmol,与0.23mL(2.5mmol)糠胺混合,溶解于40mL二氯甲烷中,向体系中加入0.0449g引发剂DMAP,0.386g缚水剂EDCI搅拌均匀;5)将反应体系置于40℃的恒温油浴中回流8h,进行热引发反应;6)反应结束后,将反应液滴加到150ml乙醚中进行沉淀,减压过滤,将过滤所得固相产物在35℃下真空干燥,得到单呋喃基酰胺的笼型多面体低聚倍半硅氧烷(单呋喃基酰胺POSS),产率90%,结构式如下式所示:实施例71)将5.93g(7mmol)(七)中所述七异丁基烯丙基笼型多面体低聚倍半硅氧烷和1.061ml(10.5mmol)糠硫醇,完全溶解在40ml四氢呋喃中,然后加入0.119g引发剂偶氮二异丁腈搅拌均匀;2)将反应体系置于40℃的恒温油浴中回流8h,进行加成反应;3)反应结束后,将反应体系滴入200ml水中,将所得固相产物在40℃下真空干燥,得到单呋喃基含硫的笼型多面体低聚倍半硅氧烷(即,单呋喃基含硫POSS),产率为90%,结构式如下式所示:实施例81)将5.831g(7mmol)(四)中所述七异丁基乙烯基笼型多面体低聚倍半硅氧烷和1.061ml(10.5mmol)糠硫醇,完全溶解在40ml四氢呋喃中,然后加入0.14g引发剂偶氮二异丁腈(AIBN),搅拌均匀;2)将反应体系置于80℃的恒温油浴中回流8h,进行缩合反应;3)反应结束后,将反应体系滴入200ml水中,将所得固相产物在40℃下真空干燥,得到单呋喃基含硫的笼型多面体低聚倍半硅氧烷(即,单呋喃基含硫POSS),产率为90%,结构式如下式所示:实施例91)将4.424g(7mmol)(三)中所述八乙烯基笼型多面体低聚倍半硅氧烷和7.073ml(70mmol)糠硫醇,完全溶解在45ml四氢呋喃中,然后加入0.0885g引发剂偶氮二异丁腈,搅拌均匀;2)将反应体系置于80℃的恒温油浴中回流8h,进行缩合反应;3)反应结束后,将反应体系滴入200ml水中,将所得固相产物在40℃下真空干燥,得到八呋喃基的笼型多面体低聚倍半硅氧烷(即,八呋喃基POSS),产率为90%,结构式如下式所示:其中,实施例10双马来酰亚胺-三嗪树脂/双呋喃基酰胺POSS复合材料的制备1)将50g双马来酰亚胺和50g三嗪树脂溶解于20mL四氢呋喃中;2)用溶液超声分散的方法将步骤1制得的双马来酰亚胺-三嗪树脂均匀分散在四氢呋喃中,制得BT树脂;3)将0.25g双呋喃基酰胺POSS(由实施例2制得)与50g双马来酰亚胺-三嗪树脂(BT树脂)混合,溶解于四氢呋喃中;4)用溶液超声分散的方法将双呋喃基酰胺POSS均匀分散在混合溶液中;5)将溶剂四氢呋喃挥发干后,将产物制成厚度5mm,直径30mm的圆片,放置于真空干燥烘箱中,在160℃下保温1小时,180℃下保温1小时,200℃下保温1小时,220℃下保温1小时,250℃下保温1小时,固化完成后自然冷却至室温(25℃),制得复合材料。实施例11苯并噁嗪树脂(BZ)/单呋喃POSS产物复合材料的制备1)将0.25g双呋喃基酰胺基产物,50g苯并噁嗪树脂混合,溶解于30mL丙酮中;2)用溶液超声分散的方法将单呋喃POSS(由实施例1制得)均匀分散在混合溶液中;3)将溶剂丙酮挥发干后,将产物制成厚度5mm,直径30mm的圆片,放置于真空干燥烘箱中,在160℃下保温1小时,180℃下保温1小时,200℃下保温1小时,220℃下保温1小时,250℃下保温1小时,固化完成后自然冷却至室温(25℃),制得复合材料。对比例对比例1本对比例与实施例10所用方法相同,区别仅在于不加入由实施例2制得的双呋喃基酰胺POSS。对比例2本对比例与实施例11所用方法相同,区别仅在于不加入由实施例1制得的单呋喃POSS。实验例实验例1样品的相对介电常数本实验例所用样品为实施例10~11和对比例1~2中制得,相对介电常数根据(三)方法进行测定,结果如下表1所示:表1样品的相对介电常数样品实施例10实施例11对比例1对比例2相对介电常数3.283.993.714.30实验例2样品的热重(TGA)分析本实验例所用样品为实施例11和对比例2中制得。所用仪器型号:TGA-50;测试条件:N2,升温速度为10℃/min,测试温度范围:室温(25℃)~800℃,结果如下表2所示。表2样品的TGA以上结合具体实施方式和范例性实例对本发明进行了详细说明,不过这些说明并不能理解为对本发明的限制。本领域技术人员理解,在不偏离本发明精神和范围的情况下,可以对本发明技术方案及其实施方式进行多种等价替换、修饰或改进,这些均落入本发明的范围内。本发明的保护范围以所附权利要求为准。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1