一种高分子母液及3D生物芯片的制作方法与流程
本发明涉及一种生物芯片用材料及生物芯片的制作方法,特别涉及一种高分子母液及3D生物芯片的制作方法。
背景技术:
多肽,抗体,蛋白药物在近10年来发展快速,其突出特点是特异性高,反应速度快,副作用少等,特别适合肿瘤相关的疾病的治疗。当前抗体筛选主要还是基于384孔板的酶联免疫快速筛选技术,无论是通量还是速度上,都有待进一步提高。特别是,当前抗体筛选时需要用二抗荧光标记来读取数据,给实验带来了额外的经济负担,潜在的假阳性不可避免。2000年以来,以美国Plexera公司的高通量相互作用筛选仪器为代表,越来越多的无标记,高通量筛选装备进入人们的视野。其代表产品PlexeraHT仪器可能在20分钟内快速筛选高达5000个相互作用点位,并且具备无标记,动力学特点。从其已经报道的芯片来看,虽然有众多蛋白芯片供选择,但开发出一款价格便宜,性能稳定的通用型蛋白芯片仍然有着极大的需求与挑战。
生物芯片一般是通过在玻璃,金属等表面修饰一层高分子,将蛋白,抗体,药物分子,多肽等生物分子固定在表面,然后制作成微流控芯片,在表面检测表面所固定物质与蛋白,血清,细胞裂解液等物质的相互作用,进而实验对生物组分进行定性定量分析【1-2】。当前,生物芯片的表面修饰的主要模式是先在芯片表面自组装一层单分子引发剂,然后在表面进行高分子合成,形成二维或三维生物膜。这种方式合成的高分子,因自身空间位阻作用,能在表面形成具有三维空间的分子刷结构,具有良好的抗非特异性和生物兼容性。通过调节低部自组装引发剂密度,可以一定程度上控制表面形成的高分子密度与厚度【3-4】。但是,这种制作方法操作复杂,合成时间长,几乎所有反应都在表面进行,导致反应效率极低(10%左右),对原料利用率低。特别是高分子合成这一步,因整个芯片要密封在无严格氧条件下,整个处理过程需要在手套箱内操作,极大地阻碍了芯片生产的工业化与标准化,实际生产出的芯片质量也难以保证。因此,如何进一步优化芯片合成步骤,提高芯片生产效率,完善芯片质量控制,使得芯片能真正从实验室走向工厂是一个新的富有挑战的工作。
参考文献:
[1]Christopher Lausted, Zhiyuan Hu1 Leroy Hood and Charles T. Campbell; SPR Imaging for High Throughput, Label-Free Interaction Analysis;Combinatorial Chemistry & High Throughput Screening, 2009, 12, 741-751
[2]一种芯片,制备就去,用途及筛选药物的方法 申请号 201210371255.X
[3]基于ATRP 技术的多嵌段共聚物研究进展 高分子通报 6期 36-43页,2006年
[4]Ma H, He,J, Liu X,Gan J, Jin G, Zhou j. Surface Initiated Polymerization from Substrates of Low Initiator Density and Its Applications in Biosensors; ACS applied materials & interfaces. 2010:2:3223-40。
技术实现要素:
本发明的一个目的在于提供一种简易的用于生物芯片的高分子母液的合成方法。
本发明的另一个目的在于提供一种易于实现的3D生物芯片制作方法。
本发明所采取的技术方案是:
一种高分子母液的合成方法,包括如下步骤:
1)将OEGMA和甲基丙烯酸衍生物单体溶解在极性溶剂中 ,去除气泡,保护气保护下避光搅拌,得到单体混合液A,备用;
2)将适量络合配位体和催化剂过渡金属卤化物溶解于水中,得到溶液B;
3)保护气保护下将单体混合液A和溶液B混合均匀,至反应液变色;
4)在反应液中加入弱还原剂,搅拌均匀后加入引发剂引发聚合反应;
5)反应完全后,通过含氧气体,氧化溶液,得到高分子母液。
作为上述合成方法的进一步改进,络合配位体为联吡啶。
作为上述合成方法的进一步改进,过渡金属卤化物为卤化铜。
作为上述合成方法的进一步改进,弱还原剂选自抗坏血酸、葡萄糖或辛酸亚锡。
作为上述合成方法的进一步改进,引发剂选自单巯基卤代硫醇、单巯基聚乙二醇低聚物、双巯基卤代硫醇、双巯基聚乙二醇低聚物。
作为上述合成方法的进一步改进,OEGMA和甲基丙烯酸衍生物单体的摩尔比为(1:4)~(4:1)。
作为上述合成方法的进一步改进,合成的高分子的数均分子量为50万~500万。
作为上述合成方法的进一步改进,甲基丙烯酸衍生物单体为含羟基的甲基丙烯酸衍生物单体。
一种3D生物芯片的制作方法,包括使用改性剂在上述的高分子母液中的高分子上引入锚定基团,得到衍生化高分子母液;之后取衍生化高分子母液铺于载体上,反应完全后清洗去除未固定的高分子,干燥得到3D生物芯片。
作为上述制作方法的进一步改进,锚定基团选自-COOH、-NH2、-OH、环氧基、-OCH3,-COCNH2,氰基,炔基,叠氮基。
作为上述制作方法的进一步改进,载体为具有纳米金、纳米银、纳米铬、三氧化二铝或二氧化钛表面的芯片。
本发明的有益效果是:
本发明的高分子母液合成方法,将表面化学反应转移到溶液中进行,一次性合成大量高分子母液,提高高分子末端衍生化产率与反应时间,避免了手套箱等昂贵仪器的使用,节约了时间与人力成本。
本方案改进了芯片制作流程与工艺,缩短了芯片制作周期 ,避免了手套箱等昂贵仪器的使用,节约了时间与人力成本。将表面化学反应转移到溶液中进行,一次性合成大量高分子母液,提高高分子末端衍生化产率与反应时间,增加了芯片质量的稳定性,使得芯片能适用于大规模工业化生产需求。
本发明方法反应条件极为温和,易于实现。本发明方法制作得到的生物芯片,具有很好的抗非特异性。
附图说明
图1是芯片表面样品打印阵列图;
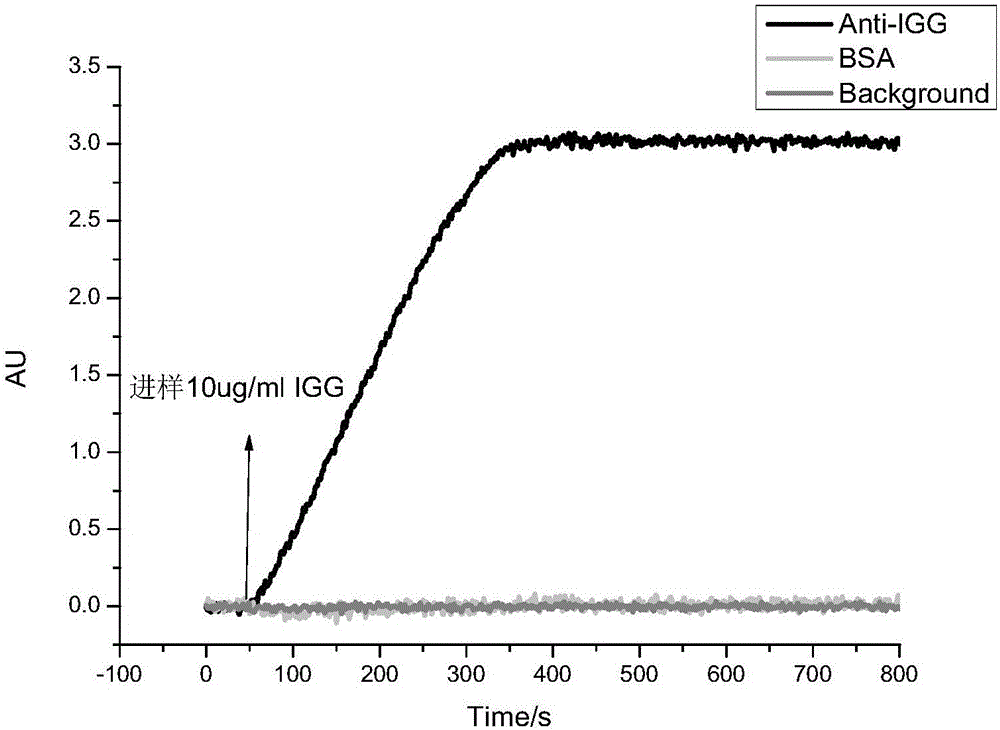
图2是各样品点与 IgG蛋白结合信号图。
具体实施方式
一种高分子母液的合成方法,包括如下步骤:
1)将OEGMA和甲基丙烯酸衍生物单体溶解在极性溶剂中 ,去除气泡,保护气保护下避光搅拌,得到单体混合液A,备用;
2)将适量络合配位体和催化剂过渡金属卤化物溶解于水中,得到溶液B;
3)保护气保护下将单体混合液A和溶液B混合均匀,至反应液变色;
4)在反应液中加入弱还原剂,搅拌均匀后加入引发剂引发聚合反应;
5)反应完全后,通过含氧气体,氧化溶液,得到高分子母液。
极性溶剂作用在于有效地溶解OEGMA和甲基丙烯酸衍生物单体,其溶解性高有利于液相合成的进行。常用的极性溶剂可以是甲醇和水的混合液,如甲醇与水等体积混合得到的混合液。极性大的溶液可提高高分子合成速率,降低最终高分子的分子量大小,甲醇的加入,一方面是降低反应速率,提高分子量,另一方面是增加体系对高分子单体溶解度。
作为上述合成方法的进一步改进,络合配位体为联吡啶。特别的,联吡啶为2,2-联吡啶。
作为上述合成方法的进一步改进,过渡金属卤化物为卤化铜。特别的,卤化铜为CuCl2、CuBr2等稳定存在的卤化物。
弱还原剂为本领域常用的弱还原剂,指在本实验体系下可以选择性地将二价铜离子还原成一价铜离子的还原剂,使反应体系中同时存在一价铜离子和二价铜离子,利于高分子的合成。而相对较强的还原剂如Pd-C、NaH等强还原剂可将二价铜离子还原成铜单质,不适合此反应体系。作为上述合成方法的进一步改进,弱还原剂选自抗坏血酸、葡萄糖或辛酸亚锡。考虑到使用的方便性等,弱还原剂最佳为抗坏血酸。
作为上述合成方法的进一步改进,引发剂优选为含硫引发剂,选自单巯基卤代硫醇、单巯基聚乙二醇低聚物、双巯基卤代硫醇、双巯基聚乙二醇低聚物等。具体的可以是HS-(CH2)6-OC(O)-IzoButyrate-Br,HS-(CH2)12OC(O)-IzoButyrate-Br,HS-(CH2)18OC(O)-IzoButyrate-Br等。含硫引发剂在参与高分子聚合反应过程中,同时可以在高分子中引入S键,便于高分子在后续的反应中固定在芯片表面。
作为上述合成方法的进一步改进,OEGMA和甲基丙烯酸衍生物单体的摩尔比为(1:4)~(4:1)。通过调节两者的比例,可以精确调控高分子最终分子量大小及高分子间的空间大小。
特别的,OEGMA单体的分子量在300Da~2000Da之间。
作为上述合成方法的进一步改进,合成的高分子的数均分子量为50万~500万。实验结果表明这一分子量范围内的高分子,可以有效提高生物芯片的抗非特异性。
作为上述合成方法的进一步改进,甲基丙烯酸衍生物单体为含羟基的甲基丙烯酸衍生物单体。含羟基的甲基丙烯酸衍生物单体可以是甲基丙烯酸羟乙酯,羟乙基甲基丙烯酸羟乙酯,羧甲基甲基丙烯酸羟乙酯,羧乙基甲基丙烯酸羟乙酯等。
一种3D生物芯片的制作方法,包括使用改性剂在上述的高分子母液中的高分子上引入锚定基团,得到衍生化高分子母液;之后取衍生化高分子母液铺于载体上,反应完全后清洗去除未固定的高分子,干燥得到3D生物芯片。
作为上述制作方法的进一步改进,锚定基团选自-COOH、-NH2、-OH、环氧基、-OCH3,-COCNH2,氰基,炔基,叠氮基。锚定基团的引入可以使用现有方法进行,如Jia P, Tang Y C, Ning X, et al. Covalently derivatized NTA microarrays on porous silicon for multi-mode detection of His-tagged proteins [J]. Science China, 2011, 54(3):526-535.等公开的方法实现。
作为上述制作方法的进一步改进,载体为具有纳米金、纳米银、纳米铬、三氧化二铝或二氧化钛表面的芯片。
本发明中为本领域常用的缩写,如有不同,以下方定义的名词缩写为准:
OEGMA:寡聚乙二醇甲醚甲基丙烯酸酯
HEMA:甲基丙烯酸羟乙酯
BPY:2,2-联吡啶
DMAP:4-二甲氨基吡啶
DMF:二甲基甲酰胺
EDC:1-乙基-3-(3-二甲基氨丙基)-碳化二亚胺
NHS:N-羟基琥珀酰亚胺。
下面结合实施例,进一步说明本发明的技术方案。
高分子母液1的合成:
1)将10mmol OEGMA 500和10mmol HEMA溶解于MeOH(25 mL)和水(25 mL)的混合溶液中,超声振荡去除气泡后,避光、通入氮气保护下磁力搅拌30 min,得到单体混合液A;
2)将32 mg BPY、2.5 mL 0.04 M CuCl2的水溶液混合均匀,得到溶液B;
3)持续氮气保护下,用注射器把B溶液注入A溶液中,磁力搅拌5 min,呈淡蓝色;
4)用注射器吸取1.5 mL 0.04 M 抗坏血酸水溶液注射到上述反应溶液中,磁力搅拌5 min溶液呈棕色;
5)用注射器吸取1mL 1 mM 含硫引发剂HS-(CH2)6-OC(O)-IzoButyrate-Br注射到上述溶液中,溶液呈棕色,反应20 h后,通入空气氧化溶液,得到高分子母液。
高分子母液2的合成:
1)将10mmol OEGMA 500溶解于MeOH(25 mL)和水(25 mL)的混合溶液中,超声振荡去除气泡后,避光、通入氮气保护下磁力搅拌30 min,得到单体混合液A;
2)将32 mg BPY、2.5 mL 0.04 M CuCl2的水溶液混合均匀,得到溶液B;
3)持续氮气保护下,用注射器把B溶液注入A溶液中,磁力搅拌5 min,呈淡蓝色;
4)用注射器吸取1.5 mL 0.04 M 抗坏血酸水溶液注射到上述反应溶液中,磁力搅拌5 min溶液呈棕色;
5)用注射器吸取1mL 1 mM 含硫引发剂HS-(CH2)6-OC(O)-IzoButyrate-Br注射到上述溶液中,溶液呈棕色,反应20 h后,通入空气氧化溶液,得到高分子母液2。
高分子母液3的合成:
1)将2.5mmol OEGMA 500和10mmol HEMA溶解于MeOH(25 mL)和水(25 mL)的混合溶液中,超声振荡去除气泡后,避光、通入氮气保护下磁力搅拌30 min,得到单体混合液A;
2)将32 mg BPY、2.5 mL 0.04 M CuCl2的水溶液混合均匀,得到溶液B;
3)持续氮气保护下,用注射器把B溶液注入A溶液中,磁力搅拌5 min,呈淡蓝色;
4)用注射器吸取1.5 mL 0.04 M 抗坏血酸水溶液注射到上述反应溶液中,磁力搅拌5 min溶液呈棕色;
5)用注射器吸取1mL 1 mM 含硫引发剂HS-(CH2)6-OC(O)-IzoButyrate-Br注射到上述溶液中,溶液呈棕色,反应20 h后,通入空气氧化溶液,得到高分子母液3。
高分子母液4的合成:
1)将10mmol OEGMA 500和2.5mmol HEMA溶解于MeOH(25 mL)和水(25 mL)的混合溶液中,超声振荡去除气泡后,避光、通入氮气保护下磁力搅拌30 min,得到单体混合液A;
2)将32 mg BPY、2.5 mL 0.04 M CuCl2的水溶液混合均匀,得到溶液B;
3)持续氮气保护下,用注射器把B溶液注入A溶液中,磁力搅拌5 min,呈淡蓝色;
4)用注射器吸取1.5 mL 0.04 M 抗坏血酸水溶液注射到上述反应溶液中,磁力搅拌5 min溶液呈棕色;
5) 用注射器吸取1mL 1 mM 含硫引发剂HS-(CH2)6-OC(O)-IzoButyrate-Br注射到上述溶液中,溶液呈棕色,反应20 h后,通入空气氧化溶液,得到高分子母液4。
高分子母液5的合成:
1)将10mmol HEMA溶解于MeOH(25 mL)和水(25 mL)的混合溶液中,超声振荡去除气泡后,避光、通入氮气保护下磁力搅拌30 min,得到单体混合液A;
2)将32 mg BPY、2.5 mL 0.04 M CuCl2的水溶液混合均匀,得到溶液B;
3)持续氮气保护下,用注射器把B溶液注入A溶液中,磁力搅拌5 min,呈淡蓝色;
4)用注射器吸取1.5 mL 0.04 M 抗坏血酸水溶液注射到上述反应溶液中,磁力搅拌5 min溶液呈棕色;
5)用注射器吸取1mL 1 mM 含硫引发剂注射HS-(CH2)6-OC(O)-IzoButyrate-Br到上述溶液中,溶液呈棕色,反应20 h后,通入空气氧化溶液,得到高分子母液5。
合成高分子的分子量主要受以下条件影响:1,高分子单体比例;2,反应时间;3,反应温度;4,引发剂比例。在上述实验中,通过控制其他反应条件不变,只改变高分子单体比例,可以精确控制得到不同分子量的高分子母液(见表1)。
表1、原料混合比对分子量的影响
相同条件下,延长反应时间可以获得更高分子量的高分子;反应温度越高反应分子量分布越广泛,分子量越小;引发剂比例越大,合成高分子分子量越小,反之,则分子量越大。本领域技术人员也可以选择通过控制反应时间、反应温度、引发剂比例来精确控制合成的高分子的分子量。
高分子的改性:
1)室温配制1g丁二醋酐,0.75g DMAP,100ml DMF酸化溶液,搅拌反应1小时,得到反应酸化液;
2)取上述高分子母液100ml及反应酸化液100ml,室温搅拌24 h,去除溶剂DMF,得干燥样品;
3)将干燥样品溶于100ml乙醇,配制得到衍生化高分子母液。
或采用本领域其他公知的方法,如Jia P, Tang Y C, Ning X, et al. Covalently derivatized NTA microarrays on porous silicon for multi-mode detection of His-tagged proteins [J]. Science China, 2011, 54(3):526-535.等公开的对高分子进行改性,引入所需要的锚定基团。
裸金表面自组装高分子薄膜:
乙醇冲洗芯片三次,干燥后用等离子清洗机清洗5分钟,吹干裸金玻璃芯片,备用;
取1ml上述合成的衍生化高分子母液,铺在裸金玻璃芯片上,反应5分钟;
经乙醇,水各清洗一次后,氮气吹干,至此裸金表面自组装高分子薄膜合成完毕,得到3D裸金生物芯片。
裸银表面自组装高分子薄膜:
1)乙醇冲洗芯片三次,干燥后用等离子清洗机清洗5分钟,吹干祼银玻璃芯片,备用;
2)取1ml上述合成的衍生化高分子母液,铺在裸银玻璃芯片上,反应5分钟;
3)经乙醇,水各清洗一次后,氮气吹干,至此祼银表面自组装高分子薄膜合成完毕,得到3D祼银生物芯片。
三氧化二铝表面自组装高分子薄膜:
1)乙醇冲洗芯片三次,干燥后用等离子清洗机清洗5分钟,吹干三氧化二铝玻璃芯片,备用;
2)取1ml上述合成的衍生化高分子母液,铺在三氧化二铝玻璃芯片上,反应5分钟;
3)经乙醇,水各清洗一次后,氮气吹干,至此三氧化二铝表面自组装高分子薄膜合成完毕,得到3D三氧化二铝生物芯片。
3D裸金生物芯片用于多肽、抗体、蛋白固定
1)使用摩尔比为1:1的10mM EDC/NHS的活化液对上述裸金自组装高分子芯片进行活化处理30分
2)纯水快速清洗,氮气吹干,然后用Q Array Mini高通量点样机,对多肽,抗体,蛋白样品按照预先设定程序进行点样处理,保持点样过程处于湿润状态;
3)使用pH=8.5的1M乙醇胺水溶液对芯片进行封闭处理,反应半个小时;
4)然后依次用10XPBS,2XPBS, 1XPBS, 对芯片各清洗15分钟,氮气吹干后,4℃冰箱保存备用,至此,多肽,抗体,蛋白样品的固定完成。
高分子修饰的裸金芯片用于抗体-抗原检测
实验组:
按照图1中所示阵列 ,Q Array Mini高通量点样机上将1mg/mL Anti-IGG抗体蛋白打印在活化后的裸金芯片表面。经过液孵育,封闭,清洗后,加上Plexera公司微流控COVER后,在Plexera HT仪器上,按照标准测试程序进行测试。
对照组:
按照图1中所示阵列 ,Q Array Mini高通量点样机上将1mg/mLBSA抗体蛋白打印在活化后的裸金芯片表面。经过液孵育,封闭,清洗后,加上Plexera公司微流控COVER后,在Plexera HT仪器上,按照标准测试程序进行测试。所选择缓冲液体为1×PBST(0.05%T-20),重生液体为1:200 H3PO4水溶液,流通样品深度为10μg/ml IGG抗体蛋白。
空白组:
按照图1中所示阵列 ,Q Array Mini高通量点样机上将1mg/mL1XPBS溶液打印在活化后的裸金芯片表面。经过液孵育,封闭,清洗后,加上Plexera公司微流控COVER后,在Plexera HT仪器上,按照标准测试程序进行测试。所选择缓冲液体为1×PBST(0.05%T-20),重生液体为1:200 H3PO4水溶液,流通样品深度为10μg/ml IgG抗体蛋白。
检测:所选择缓冲液体为1XPBST(0.05%T-20),重生液体为1:200 H3PO4水溶液,流通样品深度为10μg/ml IGG抗体蛋白。依次在芯片上,流通重生液(3μl/s, 300s),缓冲液(2μl/s, 300s), 10μg/ml IGG样品(2μl/s, 300s),通过PlexeraDE.exe软件分析得到各样品点与流通抗体蛋白结合信号,结果如图2所示。
实验组:Anti-IGG样品点有明显结合信号,信号大小为3个Au单位,亲和力大小为10-15 M;
对照组:BSA样品点无明显结合信号,信号大小为0个Au单位,亲和力大小为0 。
空白组:样品点无明显结合信号,信号大小为0个Au单位,亲和力大小为0。
对照组与空白组均无明显结合信号。对比三组数据,可知本方法制作的高分子修饰的裸金芯片(3D裸金生物芯片)具有较强的抗非特异性能,可用于抗体-抗原相互作用的高通量筛选。
- 还没有人留言评论。精彩留言会获得点赞!