一种集成了光电检测装置的手持式蓝牙PCR仪的制作方法
本发明属于分子生物学与医疗检测仪器技术领域,特别涉及一种集成了光电检测装置的手持式蓝牙PCR(Polymerase Chain Reaction,聚合酶链式反应)仪。
背景技术:
生物信息是调节和控制生命活动的信号,是构成生物体的三大要素(物质、能量、信息)之一,对生物体生存、繁殖及代谢等都起着重要作用。生物信息包含的范围很广,通常狭义上是指包含遗传信息的DNA、RNA等。这些带有遗传信息的序列因人而异,也有可能受物理、化学、生物等因素的影响而发生突变,或在自我复制过程中发生错误,而有的复制、转录错误或突变会造成人体的各种疾病,如癌症,因而对生物信息进行分析、找出突变信息对预测和诊断疾病有着重要意义。分析处理生物信息往往要求有一定量的样本才能进行基因测序等工作,然而从人体直接提取所得的一些致病基因序列尤其是早期癌症筛查所需的基因序列的量往往是很小的,故需要对其进行体外扩增以达到可以观察和分析的量级。当前,遗传信息序列的体外扩增主要是通过在基因扩增仪(PCR仪)中进行聚合酶链式反应(Polymerase Chain Reaction)得到。
DNA的半保留复制是生物进化和传代的重要途径,而聚合酶链式反应是一种用于放大扩增特定DNA片段的分子生物学技术,可被看作是体外特殊的DNA半保留复制。继1983年美国生物化学家K.B.Mullis提出设想并在1985年发明了聚合酶链式反应,即简易DNA扩增法之后,该技术已持续发展到第三代,有了耐热、稳定的DNA聚合酶——Taq酶。PCR反应先利用DNA在体外95℃左右的高温下变性的性质使之解旋成单链,再降温至60℃左右,使两个引物分别和上一步解旋得到的两条单链按碱基互补配对的原则结合,最后再调节温度至72℃左右(DNA聚合酶最适反应温度),使DNA聚合酶能以引物为起始点沿着5’端到3’端的方向用游离的碱基A、T、G、C合成互补链。每完成一个这样的循环,DNA序列的数量就增长一倍,多个循环后目标序列就能被扩增至可观量级,以作为下一步生物信息分析的样本。
随着生命科学和生物信息学研究的不断发展,聚合酶链式反应技术及仪器也得到了更多关注和发展,逐渐成为生命科学研究和实验中不可或缺的部分。PCR仪一般分为普通PCR仪、梯度PCR仪、原位PCR仪以及实时荧光定量PCR仪四类。普通PCR仪一次扩增反应只能设定一个特定温度,一般用于对特定的目标基因进行扩增,而梯度PCR仪则能设定一系列不同的温度(温度梯度),在一次扩增中找到最适宜的反应温度,更有效的进行扩增;原位PCR仪利用完整的细胞作为一个反应体系来扩增细胞内的目的序列片段,并在不破坏细胞的前提下用一些特定检测手段检测细胞内的扩增产物,适用于检测病理切片中含量较少的靶序列;实时荧光定量PCR仪是带有荧光信号采集系统和计算机分析处理系统的普通PCR仪,其进行PCR扩增时所用的引物是用同位素、荧光素等标记过的,扩增结果可通过荧光信号采集系统实时采集并传输到计算机分析处理系统中处理以得到实时的量化结果输出。
由于PCR仪在生命科学研究和医疗检测中显现出的越发重要的地位及良好的市场前景,许多医疗设备厂商都已进入PCR仪市场,并积极抢占市场份额,其中不乏知名公司如ABI美国应用生物公司、ROCHE罗氏诊断、MJ、伯乐等,以及国内的杭州博日、杭州朗基、上海枫岭、厦门安普利等,带动了全球体外检测市场的迅速发展。
现有的PCR仪,尤其是国产仪器,多是面向实验室及大中型医疗机构的,体型大、价格高,家庭及小型的医疗机构,如社区医院等尚没有能力配备。然而,由于我国人口基数大,医疗资源相对匮乏,大中型的医疗机构只能解决小部分人的看病问题,而大部分人无法享受到这部分医疗资源来进行疾病筛查或诊断,耽误病情及最佳治疗时机。同时,随着国民收入和生活水平的提高,人们对身体健康越发关注,对精准医疗的需求也随之日益增长。
综上所述,将PCR仪等便利、有效的医疗诊断设备下放到基础医疗服务机构和家庭中去,才能最大化PCR仪效用及其市场,同时有效解决基层医疗单位和家庭疾病检测和诊断困难的问题。
当前市场上主流的PCR仪体积较大、笨重不便携带,操作复杂,需专业实验人员操作,且测试时间平均在2小时以上。这类PCR仪暂无系统的数据管理系统且EB染色的染料具有高致癌性,价格还高达几万人民币。因而,一种体积小、轻便易携、操作简单迅速的低成本、有数据管理功能的PCR仪器会是市场需求发展的趋势,也终将取代传统的PCR仪发挥更广泛的作用。
技术实现要素:
为了克服上述现有技术的缺点,本发明的目的在于提供一种集成了光电检测装置的手持式蓝牙PCR仪,基于PID调节来控制升降温装置对反应温度进行实时调节,配合蓝牙装置实现和电脑或手机客户端之间的数据实时传输,并利用光电检测装置快速鉴定实验结果,其特点包括高效、易操作、精确控制,且能避免对反应失败的产物再进行下一步的特异性分析,造成时间和成本损耗。
为了实现上述目的,本发明采用的技术方案是:
一种集成了光电检测装置的手持式蓝牙PCR仪,包括:
一个放置PCR反应管的金属反应平台1,包括下部底座和上部热盖;
一个基于PID反馈调节的控制电路2;
一个或者多个加热装置3;
一个或者多个降温装置4;
一个或者多个通用的温度传感器5;
一个或者多个光电检测装置6;
一个蓝牙装置7,用于向接收端设备实时发送温度等相关信息;
其特征在于:所述控制电路2利用PID调节控制加热装置3和降温装置4对放置有PCR反应管的金属反应平台1进行加热或降温,并利用温度传感器5的反馈进行实时温度修正,通过蓝牙装置7将实时温度信息发送给接收端设备以便于实时监控,并在反应前后利用光电检测装置6检测反应液中特定物质含量变化以初步鉴定反应结果。
所述金属反应平台1由良导热性的金属制成,包括但不限于铝、铝合金或镀银铝块等,其作为介质的导热性比空气更均匀、比液体更快,上、下、四周全包围的方式又能保证反应管温度变化更均匀。
用于放置PCR反应管的反应槽101布置在下部底座和上部热盖的交接位置,即:当PCR反应管安装在反应槽101时,其一部分位于下部底座中,另一部分位于上部热盖中。反应槽101为纵向槽,反应平台上半部分,即上部热盖上每个反应槽101中设置有一根PCR反应管盖固定弹簧102,以保证PCR反应管能被严密地固定在反应槽101内且受热均匀。金属反应平台1主体为圆柱体或长方体或其它转盘结构,外部设置转盘固定卡口对103。反应槽101以圆柱轴心为中心呈放射状均匀分布或呈一排均匀分布在长方体中,以保证不同反应槽101的受热均匀。
所述控制电路2以MCU为控制中心,通过向MCU写入控制程序,对加热装置3、降温装置4、温度传感器5、光电检测装置6以及蓝牙装置7进行调度控制,所述MCU通过USB接口与外设或上位机直接进行通信;MCU通过ISP(In-System Programming)接口进行内部存储器读写以及对自身的重置,而ISP接口的数据在片上由SPI(Serial Peripheral Interface)总线进行传输;片上时钟频率由外接晶振定义;该MCU与外设或上位机的数据传输可通过USB通信模块实现;控制电路中使用了电源管理模块对输入电压进行转换,为MCU、USB接口以及其他模块供电。
所述控制电路2调节控制反应温度时,温度设置的方式包括但不限于对特定扩增对象设定固定的变性、退火及复性温度,或设定一系列的温度梯度并在一次扩增中找到最适反应温度,以便后续更有效地扩增。
所述蓝牙装置7与所述MCU连接,接收MCU处理过的数据,通过无线通信方式将数据实时传输给手机等装有蓝牙接收装置的设备,便于在设备客户端实时监测反应情况。
所述控制电路2采用PID控制原理对反应温度进行精准控制,当温度传感器5采集的被测温度偏离所希望的给定值时,PID控制根据反馈回的测量信号与给定值的偏差进行比例P、积分I、微分D运算,从而输出某个适当的控制信号给加热装置3或降温装置4,促使测量值恢复到给定值,达到自动控制的效果。
所述加热装置3包括但不限于发热电阻带或薄膜发热电阻,所述降温装置4包括但不限于风扇、热电制冷器或液冷系统,所述温度传感器5包括但不限于热敏器件或数字温度传感器。
当加热装置3为多个时,应保证其加热功率一致,且均匀分布在金属反应平台1的底部以及顶部,以保证反应平台整体升温均匀。
当降温装置4为多个时,应并联以保证多个同时工作且功率相同。
所述PCR反应管在金属反应平台1上环绕金属反应平台1的中心布置,加热装置3布置在金属反应平台1的上下两侧位置,分别位位于上部热盖的上侧和下部底座的下侧;所述降温装置4布置在金属反应平台1及加热装置3的外侧,分别位于相应的加热装置3的上方或者下方,所述温度传感器5布置在金属反应平台1的边缘和中心的表面位置。由于金属反应平台1和PCR反应液升温速率不同,故在反应平台温度达到阶段设定值后仍需实时测量并反馈,控制反应平台温度持续一段时间以保证反应液达到与反应平台一致的温度。
反应结果的判定是通过光电检测装置6利用PCR反应产物的光谱特性对其浓度进行检测得到的,所述光电检测装置6对反应产物含量进行初步鉴定(应在反应开始前先检测一次反映产物含量作为基准组,该值通常很小或为零),以判断已结束的反应结果是否符合预期要求,若反应产物在数量上位于合理范围内则认为反应成功完成,对反应产物进行下一步特异性分析,若反应产物数量极少甚至没有则认为反应不成功,则需再次进行反应以验证结果。
所述光电检测装置6包括布置在金属反应平台1下部底座和上部热盖交接处的光电发射器601和光电接收器602,其中光电发射器601位于边缘,具体布置在金属反应平台1和PCR仪外壳之间,光电接收器602位于金属反应平台1中心,光电发射器601面向光电接收器602,沿半径方向向金属反应平台1的中心方向发射特定波长的光波,光电接收器602面向光电发射器601方向接收光波;光波经过PCR反应管及其中反应液,以接收到的光强判定反应液对该光的吸收情况,进而判定反应产物的含量。
光电发射器601和光电接收器602固定于下部底座上,位于金属反应平台1的下部底座和上部热盖交界处,下缘与交界面平齐,在反应开始前以及结束后,开启上部热盖,光电发射器601发射的光波就能不受阻挡,经过PCR反应管射向光电接收器602方向;光电检测装置6也可将中心高度设置在下部底座和上部热盖交界处,即光电检测装置6一半在下部底座中一半在上部热盖中,但这样设置,需在光电发射器601和光电接收器602之间对应每个反应槽101留出一条光通道,不仅增加了制造成本,也不利于整个金属反应平台1升温和降温的均匀性。
所述光电发射器601包括但不限于激光二极管或发光二极管,所述光电接收器602包括但不限于光敏二极管、光敏电阻或光电倍增管,光电发射器601固定发射490nm的光波,检测反应液中反应副产物焦磷酸(PPi)的量,以判定反应结果。
本发明手持式PCR仪体积小重量轻,可单手抓握,有便携性,相对同类产品更易携带,且操作简单、测试迅速,适合基层医疗机构及家庭使用。基于PID反馈调节的控制电路2能实现反应温度的精准调节,蓝牙装置7的集成使得反应过程能被实时监控,光电检测装置6则能预判反应的结果,避免在未得到预期产物的情况下进行后续的检测和特异性分析,在一定程度上降低了检测时间和成本。
与现有技术相比,本发明集成了光电检测装置的手持式蓝牙PCR仪,通过对反应的实时、精准控制和低成本器件以及检测手段的应用,在实现高速、高效扩增反应的同时,达到了设备小型化和价格亲民的目标,对于PCR设备基层化和进入家庭有着重要意义。
附图说明
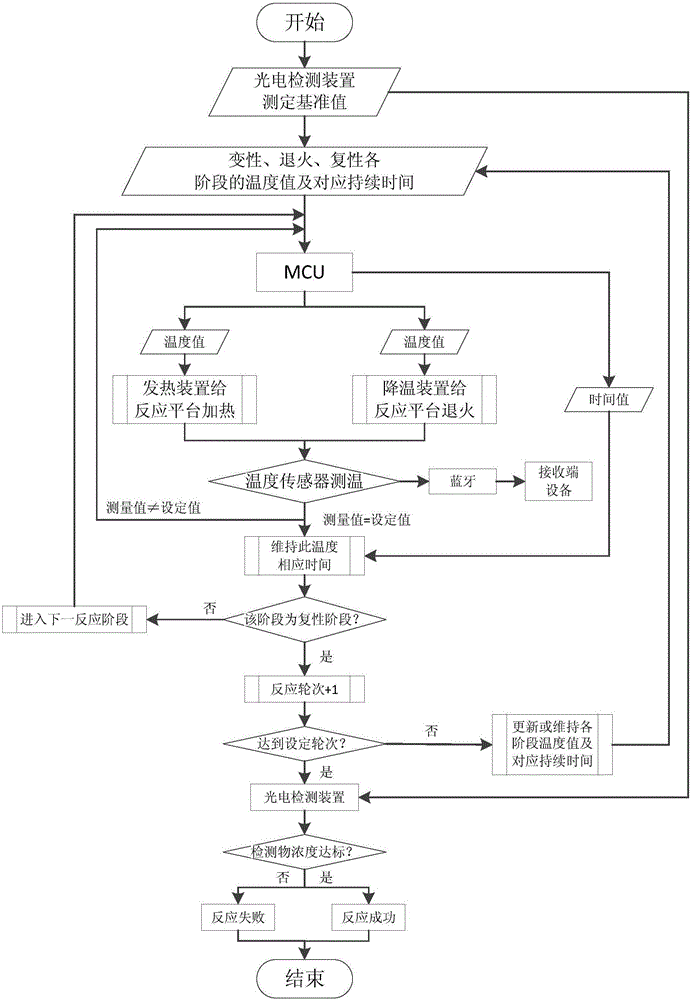
图1为本发明PCR仪应用时的操作执行流程图。
图2为本发明的一种整体结构的剖面示意图。
图3为本发明的一种热盖的截面仰视示意图。
图4为本发明的一种PCR仪主体的截面俯视示意图。
图5为本发明控制系统的电路示意图。
图6为本发明采用的PID温控调节的原理示意图。
图7为本发明采用的PID温控调节执行部件示意图。
图8为本发明采用的一种加热装置及其电路示意图。
图9为图8中发热装置主体的结构示意图。
具体实施方式
下面结合附图和实施例详细说明本发明的实施方式。
本发明提出的一种集成了光电检测装置的手持式蓝牙PCR仪应用时的操作执行流程如图1所示,当反应液制备完毕、放入PCR反应管并置放于反应平台的反应槽中后,先调用光电检测装置对反应液中待检测的特定物质的含量进行测量,作为基准组(正常情况下该值通常为零或极小);接着,盖上热盖,通电启动PCR仪;控制电路中MCU根据程序设定的各阶段反应温度值调动加热装置或降温装置对反应平台进行加热或降温,温度传感器实时测定反应温度,该温度值可通过蓝牙装置发送给接收端设备用于实时监控,同时需反馈给MCU,MCU根据测量温度值与设定温度值的差值,应用比例(P)调节或比例积分(PI)调节或比例积分微分(PID)调节,控制加热或降温过程以达到设定温度;当温度传感器测量的温度值与设定温度值一致时,MCU根据程序设定的持续时间值,控制加热或降温装置使反应平台维持该温度相应时间;判断当前反应阶段为变性、退火还是复性,若最后一个反应阶段已完成,则认为该轮反应结束,否则继续下一阶段反应,直到本轮反应结束;每一轮反应结束对反应轮次进行计数,并与设定轮次进行比对,若未达到设定轮次则维持或更新各阶段反应时间及温度(初始时各阶段设定温度为固定值则维持,为温度梯度则更新),继续进行下一轮反应,若达到则反应停止;再次启动光电检测装置,发射特定波长光波对特定产物含量进行检测以初步判断反应结果,若产物含量如预期则认为反应成功,反之,则可能需要再次实验以验证结果。
附图2提供了本发明的一种整体结构图,即该PCR仪中心剖面的正视图,整个PCR仪在结构上主要分为机壳、上部热盖和下部主体三个部分,其中上部热盖和下部主体包含了所有功能部件。具体包括:一个放置PCR反应管的金属反应平台1;一个基于PID反馈调节的控制电路2;一个或者多个加热装置3;一个或者多个降温装置4;一个或者多个通用的温度传感器5;一个或者多个光电检测装置6;以及一个蓝牙装置7。
整个反应仪的最中心部件为金属反应平台1,被上部热盖和下部主体分为上下两个可紧密拼合的部分,其中反应槽101也同样地被分为上下两个可紧密拼合的部分,在反应槽101上部有PCR反应管盖固定弹簧102固定住反应槽101中的PCR反应管以保证其与金属反应平台1接触严密;反应平台一侧设置有光电发射器601(激光二极管),向反应平台中心固定发射特定波长光波,而在反应平台中心则有一个光电接收器602(光敏电阻),用来检测穿透PCR反应管及反应液射出的这种光波的强度以初步判断PCR反应的结果。温度传感器5分别置于金属反应平台1的不同位置,测量到的温度数据传回MCU后应用相关算法计算出反应管中的温度,并作为控制系统PID调节的反馈以实现反应温度的精准控制。加热装置3,在本例中为在金属反应平台1上下表面均匀盘绕的折叠发热电阻带,与金属反应平台1直接接触,受MCU控制,在反应的变性和复性阶段加热金属反应平台1,上下表面对称放置可以保证升温更均匀。降温装置4,在本例中为在金属反应平台1和加热装置3外侧的风扇,同样受MCU控制,主要在反应的退火步骤中给反应平台降温,上下对称放置是为了使降温更均匀,下部的风扇同时还能给控制控制电路2降温。
本发明PCR仪通过控制电路2控制加热装置3和降温装置4对金属反应平台1进行加热或降温,同时通过温度传感器5实时测量反应平台温度,通过蓝牙装置7将数据实时传送到接收端以便用户实时监控反应温度,并反馈给控制电路2以便其控制加热装置3和降温装置4对反应温度进行精准调节。反应完成后,进行下一步特异性分析前,用光电检测装置6对反应结果进行初步判定以避免后续步骤不必要的时间和成本耗费。
附图3为本发明的一种热盖的截面图,热盖主体为金属反应平台1上部、紧贴反应平台的加热装置3层以及更上方的风扇,金属反应平台1中反应槽101的上方都有PCR反应管盖固定弹簧102用以将PCR反应管紧密固定在反应槽101中。
附图4为本发明的一种PCR仪主体的截面图,金属反应平台1下部底座紧邻置放于加热装置3(与反应平台直接接触)层上,反应平台中间有着多个间距相同且距反应平台中心距离相同的反应槽101,反应平台的不同位置还装有温度传感器5以实时测量反应平台的温度,而加热装置3向下则有非紧邻的风扇和控制电路2。由于反应完成后进行光电检测时需要依次对多个PCR反应管中的反应液进行检测,而光电检测装置是固定在圆柱体反应平台一条半径的两端,故需要金属反应平台能绕轴心旋转以使各个反应槽位置依次转动到光电检测装置的光路上(即使各个反应槽所在半径依次与光电检测装置所在半径重合),而反应平台一侧装有的卡扣对103就可以在每个对应检测位置处固定金属平台防止光电检测时平台转动产生偏移,每检测完一个PCR反应管且收到数据后即可手动转动反应平台换到下一个PCR反应管位置并用卡扣对103固定反应平台。
附图5为本发明控制系统的电路示意图,该控制系统的中心是MCU,控制程序被写入MCU并执行,发热装置、风扇、温度传感器、光电发射器、光电接收器、蓝牙模块分别通过不同接口与MCU连接并在其调度下执行相应功能,MCU与外设、上位机等可通过USB模块通信,而温度等数据也会通过蓝牙模块实时发送出去,可在装有蓝牙接收器的设备上接收查看,且控制电路中使用了电源管理模块对输入电压进行转换,为MCU、USB接口以及其他模块供电。
附图6提供了本发明采用的PID温控调节的原理图,附图7提供了其执行部件示意图,PID控制系统是一种闭环反馈控制系统,系统初始输入为一个或几个相对合适的温度设定值(温度梯度)以及对应温度的维持时间,Kp、Ki、Kd分别表示比例(P)、积分(I)、微分(D)作用的系数,三者共同作用得到控制系统传递函数H(s),输入量在传递函数作用下得到并输出控制量u,作用于对象,即反应平台,结果y即为实时温度测量值,被反馈给控制系统后,PID控制器根据温度设定值与测量值的差值重新计算并调动执行机构对对象温度进行调节,直到输入值r与输出值y差值为零。本发明中MCU承担了PID控制器的工作,加热装置和降温装置作为控制系统的执行机构在PID控制器控制下给对象(反应平台)进行加热或降温,温度传感器作为反馈机构承担了将对象(反应平台)实时温度传送回MCU的工作,而无线通信模块(蓝牙装置)则可以实时地将温度等数据发送给接收端设备以实现实时监控。
附图8提供了本发明采用的一种加热装置及其电路示意图,发热装置主体为均匀盘绕的折叠发热电阻带,如附图9所示,其均匀分布在金属反应平台上下表面(直接接触),每条电阻带并联一个电容,一端接电源,一端通过互补达林顿管接地,达林顿管作为功率开关,其基极连接MCU管脚,在MCU调度下控制电阻带工作。
本发明的一种具体实施方式描述如下:
先将反应液定量加入多个PCR反应管,反应液包含目标模版DNA、引物、Taq DNA聚合酶、4种dNTP混合物、扩增缓冲液、正2价镁离子以及双蒸水。将PCR反应管放入金属反应平台1中的反应槽101中,接通电源,先启动光电检测装置,光电发射器(激光二极管)601发射490nm波长的光波,转动反应平台使光波依次经过各个PCR反应管,光电接收器(光敏电阻)602感知投射光强度以大致确定PCR反应管中焦磷酸(PPi)的含量,该值将作为与反应结果进行比对的基准(正常情况下,该值通常为零或极小);接着,关闭热盖使PCR反应管盖固定弹簧102能将PCR反应管紧密固定在反应槽101中;根据写入MCU的控制程序,先启动加热装置3对反应平台进行预热以激活反应物,接着继续加热至95℃左右并维持一定时间,使反应液中的模版DNA双链变性解旋成为两条分离的DNA单链;在退火(复性)阶段,MCU控制加热装置3停止工作、降温装置4(即风扇)工作,对反应液进行降温至合适温度并维持一段时间,该温度一般为55-60℃左右,但根据不同反应物有所不同,这时引物与模版DNA单链的互补序列结合配对;在复性阶段,MCU控制降温装置4停止工作、加热装置3重新启动,对反应液进行再加热至72℃左右并维持一段时间,这时DNA聚合酶达到最佳复制温度,因而在DNA聚合酶作用下以4种dNTP为反应原料,按碱基互补配对和半保留式复制原理,与上一阶段的产物合成新的DNA双链。整个过程中,反应温度由温度传感器5检测并实时反馈给MCU以进行PID调节并由蓝牙装置向外发送,每一阶段的具体温度和持续时间可能因反应物不同而不同,都由控制程序给定。重复循环“变性-退火-延伸”三个过程多次,可将所需DNA扩增至便于检测的浓度,该循环数也由程序给定,且决定了PCR扩增的产量,一般循环数为25-30次,当循环数超过30个以后,DNA聚合酶活性会逐渐达到饱和,产物的量也不再随循环数增加而增加,即出现“平台期”,故一般循环数不超过30。反应结束后,打开热盖,MCU控制光电发射器601发射490nm波长的光波,转动反应平台使光波依次经过各个PCR反应管,检测PCR反应管中反应副产物焦磷酸(PPi)的浓度,若反应成功且充分则应产生足够的PPi,由于PPi对波长为490nm的光有吸收性,透过PCR反应管射向光电接收器602的光强会变弱,而若反应不成功则不会产生或只产生少量的PPi,对490nm光不会有很强吸收度,则透过PCR反应管射向光电接收器602的光强依然很强。根据光敏电阻的特性,其在不同强度光照下会表现不同阻值。由此可以初步判定反应结果,若反应成功则可进行电泳等后续步骤,以对反应结果进行特异性分析,若反应不成功则不需要再耗费时间和成本进行电泳,而可能需要重新进行PCR反应以复核反应结果。
- 还没有人留言评论。精彩留言会获得点赞!