肿瘤相关抗原XAGE‑1b短肽及应用的制作方法
本发明涉及肿瘤相关抗原肽及其应用,特别涉及肿瘤相关抗原XAGE-1b短肽及其应用。
背景技术:
众所周知,T细胞过继治疗肿瘤是目前最令人瞩目的技术,尤其是受体工程化T细胞的应用正成为振奋人心的癌症治疗方法,同样对病毒感染及自身免疫性疾病具有广泛的应用前景。
人体免疫监视系统在抵抗肿瘤生长过程中的重要作用,免疫监视系统通过协调各类免疫细胞得以实现抑制肿瘤生长的目的,其中细胞毒性T细胞(cytotoxic T lymphocyte,CTLs)扮演极其重要的角色,是最关键的杀伤效应细胞。肿瘤抗原特异性CD8+T细胞可以特异性识别并直接杀伤肿瘤细胞而不对正常细胞造成伤害。T细胞治疗因此成为最理想的肿瘤治疗策略。美国NIH曾预言,细胞治疗可能会成为“能够彻底治愈肿瘤的唯一手段”。因此,获得能够特异性识别、杀伤肿瘤细胞的CTL是治疗肿瘤的核心。利用肿瘤相关抗原(Tumor-associated antigen,TAA)多肽诱导建立肿瘤抗原肽特异性CTL,即可获得具有特异性杀伤肿瘤细胞的CTL克隆,并为下一步开发具有临床实际应用价值的T细胞过继治疗肿瘤奠定了重要基础,同时发明人还可以获得如下成果:
1)这些经过鉴定筛选出的肿瘤相关抗原肽氨基酸序列,将可被用于构建有效的抗肿瘤肽疫苗、DC疫苗;
2)通过分子克隆技术可以使发明人获得明确的具有特异性识别肿瘤抗原的TCR编码基因,用于TCR基因修饰T细胞的建立。
3)通过合成与短肽特异性结合的荧光探针,可开发具有自主知识产权的分子探针试剂盒,用于非小细胞肺癌的早期诊断与治疗。
目前,T细胞受体(T cell receptor,TCR)基因修饰T细胞(TCR-T),如同嵌合抗原受体(chimeric antigen receptor,CAR)修饰T细胞(CAR-T)技术一样倍受关注。CAR-T应用于血液肿瘤治疗已取得令人瞩目的疗效。CAR由单链Fv融合CD3信号单元,其功能活性依赖于信号单元的敏感性,信号单元由共刺激分子和(或)细胞因子组成。然而,有研究显示,表达CAR的T细胞对多肽的敏感性不如表达αβTCR异源二聚体的T细胞。TCR-T即通过TCR基因修饰T细胞技术,将已获得的具有特异性识别肿瘤抗原多肽的TCR编码基因转导循环CD8+T细胞,通过这一方法可在极短的时间内获得大量的稳定高表达特异性TCR的、具有与亲代CTL同样的肿瘤特异性识别与杀伤效应的基因修饰T细胞,从而满足实际临床应用所需。
发明人从2005年就开始从事肿瘤相关抗原肽特异性CTL的诱导建立,TCR相关研究(Int J Hematol.2011,93:176–185)及TCR基因修饰T细胞的研究,分别成功将肿瘤相关抗原WT1及Aurora kinase A特异性TCR转导循环CD8+T细胞(Blood,2011,118:1495-1503;Blood,2012,119:368-376),获得TCR-T克隆,经体外、体内鉴定,证实了其抗肺癌或白血病细胞的有效性。
TCR基因修饰T细胞技术越来越显现出它在肿瘤免疫治疗中的重要价值及美好前景,而生成TCR-T的关键前提是获得具有特异识别肿瘤抗原的TCR,通过体外诱导建立肿瘤相关抗原肽特异性CTL是实现这一目标的一个重要途径。
XAGE-1(X antigen family member 1)是癌-睾丸抗原(Cancer-Testis antigen,CTA)家族成员之一,CTA又称肿瘤-生发系(Tumor-Germline,TG)抗原。该类抗原,只表达于睾丸精原细胞,而不表达于正常组织细胞,同时,研究发现CTA表达于多种不同组织类型的肿瘤,因而又称为肿瘤特异共享抗原(tumor-specific shared antigens,TSSA)。由于睾丸精原细胞不表达主要组织相容性抗原复合物(major histocompatibility complex,MHC)I类分子,因此CTA诱导的CTL的免疫应答对睾丸细胞无伤害,只杀伤肿瘤细胞。正是因为这种特性使得CTA成为肿瘤免疫治疗的理想抗原。人类XAGE-1属于GAGE/PAGE家族,XAGE-1基因定位于Xp11.21-Xp11.22,包括XAGE-1a、XAGE-1b、XAGE-1c、XAGE-1d四种剪接体,XAGE-1b(X antigen family,member 1b)基因全长622bp,编码由81个氨基酸组成的蛋白前体。
XAGE-1b在多种肿瘤包括乳腺癌、前列腺癌、各种类型的肺癌(腺癌、鳞癌和小细胞肺癌等)、卵巢癌、黑色素瘤、恶性胶质瘤、淋巴瘤以及白血病等中均有表达。该基因有XAGE-1a、XAGE-1b、XAGE-1c和XAGE-1d4种转录异构体,其中XAGE-1b是能够被免疫细胞识别的优势抗原,免疫原性很强,在NSCLC中特别是肺腺癌中高表达,已成为肺癌免疫治疗的一个新靶点。然而,目前尚未有已建立XAGE-1b抗原肽特异性CTL的报道。尽管一些CTA多肽特异性CTL已经建立并通过鉴定,如:NY-ESO-1(New York esophageal squamous cell carcinoma 1)抗原特异性CTL,MAGE抗原(melanoma-associated antigens),MAGE-1特异性CTL等。但由于肿瘤的异质性以及肿瘤患者间的个体差异,获得足够多的肿瘤抗原肽特异性CTL克隆是非常必要的。
一般认为多肽的长度越短,其能诱导的特异性免疫能力越弱,甚至完全无法诱导出具有治疗价值的CTL克隆;反之,多肽长度越长,越能诱导出特异性CTL克隆。然而多肽的长度越长,合成难度越大,越难以获得纯的多肽,杂质肽的存在对克隆的形成存在不可预知的影响,而多肽的纯化成本极高但是依然难以避免杂质肽的存在,这种方案的成本极其高昂。因此,人们希望在尽可能保留多肽抗原性的情况下缩短多肽的长度。CN102428102A公开的技术方案中尝试截取XAGE-1b抗原中的一部分来诱导对肿瘤的体液免疫或细胞免疫,但是其结果并不能令人满意,其多肽的长度依然不短于16AA。
短肽还可能存在特异性差的问题,如何获得特异性好的且具有良好免疫原性的短肽是一项极具挑战性的工作。
技术实现要素:
本发明的目的在于提供肿瘤相关抗原XAGE-1b短肽及其应用。
本发明所采取的技术方案是:
XAGE-1b短肽,其序列为SEQ ID NO:2~SEQ ID NO:15中一条。
如SEQ ID NO:2~SEQ ID NO:15所示的XAGE-1b短肽可诱导肿瘤特异性细胞毒性T细胞的产生。
肿瘤特异性细胞毒性T细胞的诱导方法,使用SEQ ID NO:2~SEQ ID NO:15的XAGE-1b短肽中的至少一条经树突状细胞提呈与CD8+T细胞共培养,诱导筛选得到肿瘤特异性细胞毒性T细胞。
一种肿瘤多肽疫苗,由活性抗原成分和辅剂组成,活性抗原成分为如SEQ ID NO:2~SEQ ID NO:15XAGE-1b短肽中的至少一条。
一种用于肿瘤治疗的DC疫苗,主要由SEQ ID NO:2~SEQ ID NO:15的XAGE-1b短肽中的至少一条和树突状细胞加载得到。
由于本发明所选短肽在非小细胞肺癌中的高度特异性表达,通过合成与SEQ ID NO:2~SEQ ID NO:15所示XAGE-1b短肽特异性结合的荧光探针,可开发具有自主知识产权分子探针的试剂盒,用于非小细胞肺癌的早期诊断与治疗,并建立相关的研究平台。
本发明的有益效果是:
本发明的XAGE-1b抗原肽诱导建立的CTL对睾丸细胞不会产生免疫应答,只杀伤肿瘤细胞。诱导得到的CTL克隆具有良好的肿瘤细胞特异性杀伤效应。同时在建立CTL过程中,发明人发现筛选出的XAGE-1b抗原肽具有与DC细胞上HLA适当的亲和力并能有效地刺激、诱导产生特异性CTLs,说明其具备良好的多肽疫苗及DC疫苗的潜力。通过克隆XAGE-1b抗原肽特异性TCR基因,构建病毒载体,转导外周循环CD8+T细胞,获得TCR基因修饰的T细胞(TCR-T)克隆,同样具有与亲代CTL相似的肿瘤细胞特异性杀伤效应,提示其具有良好的临床转化及实际应用前景。
附图说明
图1是XAGE-1b在肺腺癌细胞中的表达情况;
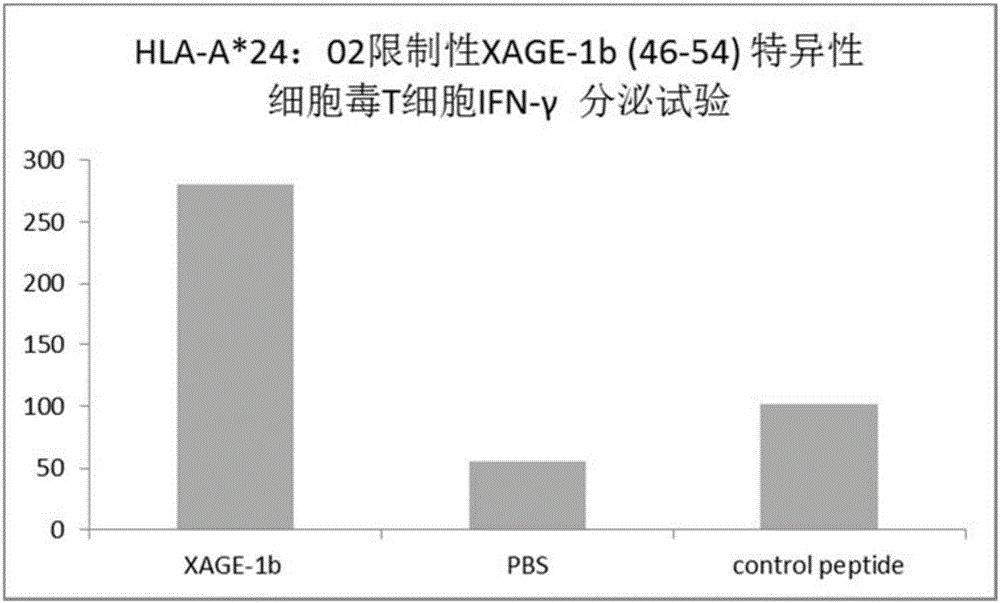
图2是XAGE-1b(46-54)特异性CTL IFN-γ释放试验;
图3是XAGE-1b(31-39)特异性CTL IFN-γ释放试验。
具体实施方式
肿瘤抗原选用XAGE-1b抗原,XAGE-1b基因位于X染色体(Xp11.21-Xp11.22),全长622bp,编码由81个氨基酸组成的蛋白前体。氨基酸序列如下(源自GenBank:NM_001097594.2):
MESPKKKNQQLKVGILHLGSRQKKIRIQLRSQCATWKVICKSCISQTPGINLDLGSGVKVKIIPKEEHCKMPEAGEEQPQV(SEQ ID NO:1)
下面结合实验,进一步说明本发明的技术方案。
XAGE-1b在非小细胞肺癌中的表达
XAGE-1是CTA家族中重要成员,除在非小细胞肺癌中有较广泛的表达外,在多种恶性肿瘤中有表达,建立XAGE-1b抗原肽特异性CTL克隆具有极其重要的意义。前期研究中发明人随机选取外科手术切除肺癌标本(均经病理检查确诊并征得患者同意),常规行RT-PCR检测XAGE-1b mRNA在NSCLC中的表达水平(PCR引物:F:5'-TTTCTCCGCTACTGAGACAC-3'(SEQ ID NO:16),R:5'-CAGGTGCTGGGAAGGGAAAT-3'(SEQ ID NO:17))。结果如图1,显示XAGE-1b在肺腺癌细胞中有较广泛的表达。
发明人通过自有方法,对XAGE-1b抗原的CTL表位进行综合评分,以不同的两个数据库(美国国立卫生研究所BIMAS,http://www-bimas.cit.nih.gov/molbio/hla_bind/和德国海德堡生物医学信息中心SYFPEITHI,http://www.syfpeithi.de/)评分之乘积为该预测表位的总评分,根据总评分预测其CTL的表位。所得候选肽由专业公司合成。具体多肽序列根据与不同HLA亚型结合分类,具体如下:
HLA-A*2402组:
基于预测结果,发明人随机选择其中的2条进行结果验证,具体实验如下。
XAGE-1b短肽特异性CTL克隆建立的操作如下:
同一健康捐献者的105个CD8+T细胞通过负载XAGE-1b(57-65)肽的104个Mo-DCs间隔1周刺激2次后,再通过自体105个丝裂霉素C处理过的负载XAGE-1b短肽的PBMC刺激1次后,经标准细胞毒试验筛选获得。
T2细胞加载5uM XAGE-1b短肽作为靶细胞,CTL的XAGE-1b短肽特异性细胞毒性通过LDH释放试验得以证实。
采用以上体外诱导建立XAGE-1b短肽特异性CTL克隆的方法,发明人还建立了HLA-A*2402限制性XAGE-1b(46-54)(SEQ ID NO:3)及XAGE-1b(31-39)(SEQ ID NO:13)特异性CTL克隆,通过IFN-γ释放试验证实其多肽特异性免疫应答效应(如图2,3)。
上述实验数据表明,发明人建立的CTL表位是极其有效的,预测结果与实验结果符合性非常好。
可见,通过将上述XAGE-1b短肽中的至少一条(SEQ ID NO:2~15)经树突状细胞提呈与细胞毒性淋巴T细胞共培养,可诱导筛选得到肿瘤抗原特异性细胞毒性T淋巴细胞。这种肿瘤抗原特异性细胞毒性T淋巴细胞可用于肿瘤的治疗。
将上述XAGE-1b短肽中的至少一条(SEQ ID NO:2~15)与树突状细胞(dendritic cell,DC)加载回输,可以作为DC疫苗用于肿瘤免疫,刺激机体产生多肽特异性抗肿瘤T细胞,进而实现肿瘤的治疗。
上述XAGE-1b短肽中的至少一条(SEQ ID NO:2~15)可以用于测定受试体样本中针对多肽的抗体水平,进而用于非小细胞肺癌的诊断。
本发明的XAGE-1b短肽长度仅为9个氨基酸,化学合成难度小,可以直接合成得到高纯的产物,应用成本大大降低,同时效果明确,具有很好的应用潜力。
<110> 安, 军
张, 蓓
<120> 肿瘤相关抗原XAGE-1b短肽及应用
<130> XAGE-1b*2402
<160> 17
<170> PatentIn version 3.5
<210> 1
<211> 81
<212> PRT
<213> 人类
<400> 1
Met Glu Ser Pro Lys Lys Lys Asn Gln Gln Leu Lys Val Gly Ile Leu
1 5 10 15
His Leu Gly Ser Arg Gln Lys Lys Ile Arg Ile Gln Leu Arg Ser Gln
20 25 30
Cys Ala Thr Trp Lys Val Ile Cys Lys Ser Cys Ile Ser Gln Thr Pro
35 40 45
Gly Ile Asn Leu Asp Leu Gly Ser Gly Val Lys Val Lys Ile Ile Pro
50 55 60
Lys Glu Glu His Cys Lys Met Pro Glu Ala Gly Glu Glu Gln Pro Gln
65 70 75 80
Val
<210> 2
<211> 9
<212> PRT
<213> 人类
<400> 2
His Leu Gly Ser Arg Gln Lys Lys Ile
1 5
<210> 3
<211> 9
<212> PRT
<213> 人类
<400> 3
Gln Thr Pro Gly Ile Asn Leu Asp Leu
1 5
<210> 4
<211> 9
<212> PRT
<213> 人类
<400> 4
Leu Gly Ser Gly Val Lys Val Lys Ile
1 5
<210> 5
<211> 9
<212> PRT
<213> 人类
<400> 5
Asn Gln Gln Leu Lys Val Gly Ile Leu
1 5
<210> 6
<211> 9
<212> PRT
<213> 人类
<400> 6
Ser Cys Ile Ser Gln Thr Pro Gly Ile
1 5
<210> 7
<211> 9
<212> PRT
<213> 人类
<400> 7
Gly Ser Gly Val Lys Val Lys Ile Ile
1 5
<210> 8
<211> 9
<212> PRT
<213> 人类
<400> 8
Ser Pro Lys Lys Lys Asn Gln Gln Leu
1 5
<210> 9
<211> 9
<212> PRT
<213> 人类
<400> 9
Lys Asn Gln Gln Leu Lys Val Gly Ile
1 5
<210> 10
<211> 9
<212> PRT
<213> 人类
<400> 10
Gln Leu Lys Val Gly Ile Leu His Leu
1 5
<210> 11
<211> 9
<212> PRT
<213> 人类
<400> 11
Arg Gln Lys Lys Ile Arg Ile Gln Leu
1 5
<210> 12
<211> 9
<212> PRT
<213> 人类
<400> 12
Gly Ser Arg Gln Lys Lys Ile Arg Ile
1 5
<210> 13
<211> 9
<212> PRT
<213> 人类
<400> 13
Ser Gln Cys Ala Thr Trp Lys Val Ile
1 5
<210> 14
<211> 9
<212> PRT
<213> 人类
<400> 14
Trp Lys Val Ile Cys Lys Ser Cys Ile
1 5
<210> 15
<211> 9
<212> PRT
<213> 人类
<400> 15
Ile Ser Gln Thr Pro Gly Ile Asn Leu
1 5
<210> 16
<211> 20
<212> DNA
<213> 人工引物
<400> 16
tttctccgct actgagacac 20
<210> 17
<211> 20
<212> DNA
<213> 人工引物
<400> 17
caggtgctgg gaagggaaat 20
- 还没有人留言评论。精彩留言会获得点赞!
- 一种具抗肿瘤活性的不对称双1‑取代5‑N杂靛红席夫碱类化合物的合成方法与制造工艺
- 一种具抗肿瘤活性的不对称双7‑N杂靛红席夫碱类化合物的合成方法与制造工艺
- 一种具抗肿瘤活性的不对称双取代靛红席夫碱类化合物及其合成方法与制造工艺
- 一种全人源抗MAGEA1的全分子IgG抗体及其应用
- 基于特异性单克隆或多克隆抗体建立的ny-eso-1抗原检测方法
- 一种规模化制备人前列腺癌pc-3细胞的方法
- 一种肿瘤抗原gpc3的ctl识别表位肽及其应用
- 一种<sup>18</sup>F标记的多肽化合物及其制备方法和应用
- 一种靶向Mesothelin的复制缺陷性重组慢病毒CAR-T转基因载体及其构建方法和应用
- 一种靶向cd123的复制缺陷性重组慢病毒car-t转基因载体及其构建方法和应用