大戟二萜千金子二萜A的制备方法和应用与流程
本发明属于特色民族药用植物中的有效成分提取分离以及活性筛选的技术领域,具体涉及一种大戟二萜类化合物及其制备方法和应用。
背景技术:
千金子系大戟科植物续随子的干燥成熟种子,是我国传统中药材之一。千金子性温,味辛,有小毒,主要功效为逐水消肿、破血消瘤,用于治疗水肿、痰饮、积滞胀满、二便不通、血癖经闭,外治顽癣、疵赘。在国外,该植物种子早有用于癌症治疗的记载,并且其甲醇提取物对于抗恶性肿瘤相关活性的初步筛选测定中已显示具有抗癌的效果。就是这样的一类化合物,是广泛存在于大戟科植物的一种重要的天然活性成分,其结构如下:
技术实现要素:
本发明的第一目的是提供一种大戟二萜类化合物;第二目的在于提供所述大戟二萜类化合物的制备方法;第三目的在于提供所述大戟二萜类化合物在制备抗癌中的应用。
本发明的第一目的是这样实现的,所述的大戟二萜类化合物是以大戟科大戟属药用植物续随子(euphorbialathylrisl)的种子为原料,经有机溶剂提取、萃取、硅胶柱层析、高压液相色谱分离步骤而得到的,其结构式为:
所述的大戟二萜a化合物,其特征是:分子式为c26h36o8,该化合物命名千金子二萜a,英文名为epoxyboetiranesa。
本发明的第二目的是这样实现的,所述的大戟二萜类化合物是以大戟科大戟属药用植物续随子(euphorbialathylrisl)的种子为原料,经有机溶剂提取、萃取、硅胶柱层析、高压液相色谱分离步骤而得到的,具体为:
一种权利要求1所述的大戟二萜类化合物的制备方法,其特征在于以大戟科大戟属药用植物续随子(euphorbialathylrisl)的种子为原料,经有机溶剂提取、萃取、硅胶柱层析、高压液相色谱分离步骤而得到的,具体为:
a、样品浸膏有机溶剂提取过程:将大戟科大戟属药用植物续随子(euphorbialathylrisl)的种子用有机溶剂超声提取2~5次,每次30~60分钟,或者冷浸提取2~5次,每次3天,提取液合并;提取液过滤,减压浓缩提取液,静置,滤除沉淀物,浓缩成浸膏a;
b、有机溶剂萃取:a步骤所得的浸膏a中加入重量比1~2倍量的乙醇,用与乙醇等体积的有机溶剂萃取3~5次,合并有机溶剂萃取相,减压浓缩成浸膏b;
c、硅胶柱层析:将b步骤所得的浸膏b用重量比1.5~3倍量的甲醇或者丙酮溶解,用浸膏重0.8~1.2倍的80~100目硅胶拌样,然后上硅胶柱层析(装柱硅胶为160~200目),用量为浸膏b重量6~10倍量;用体积比为1:0~0:1的混合有机溶剂梯度洗脱,收集梯度洗脱液、浓缩,经tlc监测,合并相同的部分;
d、高效液相色谱分离:将以体积含量50~90%的石油醚乙酸乙酯溶液洗脱得到的洗脱液经高效液相色谱分离纯化,即得所述的大戟二萜类化合物千金子二萜a;该步骤所述的高效液相色谱分离纯化是以60-80%的甲醇或者45~75%的乙腈为流动相,流速8~12ml/min,21.2×250mm,5μm的zorbaxprephtgf反相制备柱为固定相,紫外检测器检测波长为202~280nm,每次进样10~100μl,收集10~40min的色谱峰,多次累加后蒸干。即得所述的大戟二萜类化合物千金子二萜a。
根据权利要求3所述的大戟二萜类化合物的制备方法,其中a步骤所述的有机溶剂为100%的二氯甲烷或70~100%的丙酮。
根据权利要求3所述的大戟二萜类化合物的制备方法,其中b步骤所述的有机溶剂为乙酸乙酯、石油醚、氯仿或二氯甲烷。
根据权利要求3所述的大戟二萜类化合物的制备方法,其中c步骤所述的混合有机溶剂石油醚和乙酸乙酯的体积配比为20:1,9:1,8:2,7:3,6:4和1:1。
本发明大戟二萜类千金子二萜结构是通过核磁共振和质谱测定方法确定为大戟二萜类化合物,并表征其具体结构为:
化合物千金子二萜a能通过本发明的方法分离出来。
本发明的第三目的是这样实现的,所述的大戟二萜类化合物在制备抗癌中的应用。
本发明的第三目的是以千金子二萜a为原料,经对白血病急性早幼粒nb4细胞、肺腺癌a549细胞、人骨髓神经母细胞瘤shsy5y细胞、人前列腺癌pc3细胞、人乳腺癌mcf7细胞的细胞毒别达5.8、6.5、和8.6μm。
本发明化合物结构简单活性好,可作为抗癌的先导性化合物,在药物发现方面有良好的应用前景。
附图说明
图1为化合物千金子二萜a的核磁共振碳谱(13cnmr)。
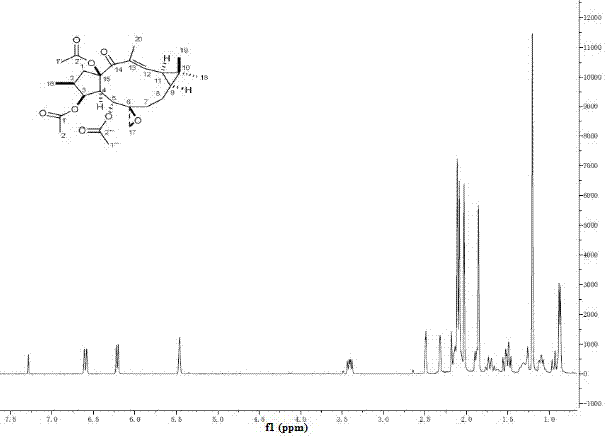
图2为化合物千金子二萜a的核磁共振氢谱(1hnmr)。
图3化合物的1h和13cnmr数据(溶剂为cdcl3)(100and400mhz)。
图4化合物腊肠素a的细胞毒活性。
具体实施方式
下面结合附图对本发明作进一步的说明,但不以任何方式对本发明加以限制,基于本发明教导所作的任何变换或改进,均落入本发明的保护范围。
本发明所述的大戟二萜类化合物是以大戟科大戟属药用植物续随子(euphorbialathylrisl)的种子为原料,经有机溶剂提取、萃取、硅胶柱层析、高压液相色谱分离步骤而得到的,其结构式为:
所述的大戟二萜a化合物,其特征是:分子式为c26h36o8,该化合物命名千金子二萜a,英文名为epoxyboetiranesa。
本发明的第二目的是这样实现的,所述的大戟二萜类化合物是以大戟科大戟属药用植物续随子(euphorbialathylrisl)的种子为原料,经有机溶剂提取、萃取、硅胶柱层析、高压液相色谱分离步骤而得到的,具体为:
一种权利要求1所述的大戟二萜类化合物的制备方法,其特征在于以大戟科大戟属药用植物续随子(euphorbialathylrisl)的种子为原料,经有机溶剂提取、萃取、硅胶柱层析、高压液相色谱分离步骤而得到的,具体为:
a、样品浸膏有机溶剂提取过程:将大戟科大戟属药用植物续随子(euphorbialathylrisl)的种子用有机溶剂超声提取2~5次,每次30~60分钟,或者冷浸提取2~5次,每次3天,提取液合并;提取液过滤,减压浓缩提取液,静置,滤除沉淀物,浓缩成浸膏a;
b、有机溶剂萃取:a步骤所得的浸膏a中加入重量比1~2倍量的乙醇,用与乙醇等体积的有机溶剂萃取3~5次,合并有机溶剂萃取相,减压浓缩成浸膏b;
c、硅胶柱层析:将b步骤所得的浸膏b用重量比1.5~3倍量的甲醇或者丙酮溶解,用浸膏重0.8~1.2倍的80~100目硅胶拌样,然后上硅胶柱层析(装柱硅胶为160~200目),用量为浸膏b重量6~10倍量;用体积比为1:0~0:1的混合有机溶剂梯度洗脱,收集梯度洗脱液、浓缩,经tlc监测,合并相同的部分;
d、高效液相色谱分离:将以体积含量50~90%的石油醚乙酸乙酯溶液洗脱得到的洗脱液经高效液相色谱分离纯化,即得所述的大戟二萜类化合物千金子二萜a;该步骤所述的高效液相色谱分离纯化是以60-80%的甲醇或者45~75%的乙腈为流动相,流速8~12ml/min,21.2×250mm,5μm的zorbaxprephtgf反相制备柱为固定相,紫外检测器检测波长为202~280nm,每次进样10~100μl,收集10~40min的色谱峰,多次累加后蒸干。即得所述的大戟二萜类化合物千金子二萜a。
根据权利要求3所述的大戟二萜类化合物的制备方法,其中a步骤所述的有机溶剂为100%的二氯甲烷或70~100%的丙酮。
根据权利要求3所述的大戟二萜类化合物的制备方法,其中b步骤所述的有机溶剂为乙酸乙酯、石油醚、氯仿或二氯甲烷。
根据权利要求3所述的大戟二萜类化合物的制备方法,其中c步骤所述的混合有机溶剂石油醚和乙酸乙酯的体积配比为20:1,9:1,8:2,7:3,6:4和1:1。
本发明所述的大戟二萜类化合物在制备抗癌药物中的应用。
本发明所述的大戟属植物不受地区和品种限制,均可以实现本发明。
实施例1
取大戟科大戟属药用植物续随子(euphorbialathylrisl)的种子2.2kg,粗粉碎至40目,用70%的丙酮超声提取4次,每次60分钟,提取液合并;提取液过滤,减压浓缩至体积的1/4;静置,滤除沉淀物,浓缩成63.5g的浸膏a;在浸膏a中加入130g乙醇,用与乙醇等体积的石油醚萃取5次,合并萃取相,减压浓缩成30g浸膏b;浸膏b在浸膏b中加入62g的丙酮溶解,然后加入100目硅胶32g拌样,拌样后,用200目硅胶200g装柱;用体积比分别为20:1,9:1,8:2,7:3,6:4和1:1的石油醚-乙酸乙酯混合有机溶剂梯度洗脱,收集梯度洗脱液、浓缩,经tlc监测,合并相同的部分,得到6个部分a-f,其中,对收集到的样品b部分6.42g,再重复硅胶柱层析,用体积比9:1-1:2的石油醚-丙酮混合有机溶剂梯度洗脱,收集梯度洗脱液、浓缩,经tlc监测,合并相同的部分,得到6个部分b1-b6,其中第b3部分,即7:3部分约650mg,再以73%的甲醇为流动相,流速10ml/min,21.2×250mm,5μm的zorbaxprephtgf反相制备柱为固定相,紫外检测器检测波长为254nm,每次进样50μl,收集25min的色谱峰,多次累加后蒸干,即得所述的大戟二萜类化合物千金子二萜a。
实施例2
取大戟科大戟属药用植物续随子(euphorbialathylrisl)的种子10.0kg,粗粉碎至40目,用100%的二氯甲烷冷浸提取4次,每次3天,提取液合并;提取液过滤,减压浓缩至体积的1/4;静置,滤除沉淀物,浓缩成300g浸膏a;在浸膏a中加入350g乙醇,用与乙醇等体积的石油醚萃取5次,合并萃取相,减压浓缩成148g浸膏b;浸膏b中加入300g的丙酮溶解,然后加入100目硅胶150g拌样,用200目硅胶1kg装柱,拌样后上柱;用体积比分别为20:1,9:1,8:2,7:3,6:4和1:1的氯仿-丙酮混合有机溶剂梯度洗脱,收集梯度洗脱液、浓缩,经tlc监测,合并相同的部分,得到6个部分a-f,其中,对收集到的样品b部分32g,再重复硅胶柱层析,用体积比9:1-1:2的石油醚-丙酮混合有机溶剂梯度洗脱,收集梯度洗脱液、浓缩,经tlc监测,合并相同的部分,得到6个部分b1-b6,其中第b3部分,即7:3部分约2.8g,再以55%的乙腈为流动相,流速10ml/min,21.2×250mm,5μm的zorbaxprephtgf反相制备柱为固定相,紫外检测器检测波长为254nm,每次进样80μl,收集15min的色谱峰,多次累加后蒸干,即得所述的大戟二萜类化合物千金子二萜a。
实施例3
取实施例1制备的化合物千金子二萜a,为白色晶体;测定方法为:用核磁共振,结合其它波谱技术鉴定结构。
(1)紫外光谱(溶剂为甲醇),λmax(logε):272(1.04)nm;
(2)红外光谱(溴化钾压片)νmax:3031,1734,1671,1619,1377,1255,1026cm–1;
(3)hresims显示本发明化合物准分子离子峰m/z499.23041[m+na]+(计算值为466.1261),结合13c和1hnmr谱(图1和图2,碳谱氢谱数据归属见图3)给出其分子式为c26h36o8,其不饱和度为8。1hnmr(cdcl3,400mhz)和13cnmr(cdcl3,100mhz)数据,见图3。
实施例4
取实施例2制备的化合物千金子二萜a分别按实施例3中的方法进行结构测定,结果为:其结构同实施例3,分子式分别为c26h36o8。
实施例5
取实施例1和2所制备的任一大戟二萜类化合物进行细胞毒活性检测试验,试验情况如下:
细胞株:白血病细胞(nb4)、肺癌细胞(a549)、人神经母细胞瘤细胞(shsy5y)、前列腺癌细胞(pc3)、乳腺癌细胞(mcf7)均由中国科学院上海药物研究所提供;实验设计:以上细胞与不同浓度化合物温育72小时,每株细胞的实验均重复一次,用两次实验的结果进行数据处理,采用改良mtt法及srb法评价化合物对细胞增殖的抑制程度,计算抑制率,根据抑制率采用logit方法计算ic50,比较化合物的体外抗肿瘤活性;
细胞的增殖抑制率=(空白对照od值-加药孔的od值)/空白对照od值×100%。
改良mtt法
取处于对数生长期的悬浮细胞,将细胞浓度调整为4×104/ml,加入96孔培养板,90µl/孔。阳性对照为顺铂,用生理盐水溶解。每孔分别加入10μl不同浓度的样品(1号试液-5号试液)。加样组及对照组均设4个复孔,加样组、阳性对照组的高浓度组还设培养基的加药平行孔,每块板均设有4个空白对照孔(仅加培养基)。样品的终浓度分别为10-2、10-1、1、10及102µg/ml,相应dmso的终浓度分别为0.1%、0.01%、0.001%、0.0001%、0.00001%。样品在终浓度102µg/ml时,用0.1%dmso作为溶剂对照,其余浓度均用生理盐水作阴性对照。阳性对照药顺铂的终浓度为10-1、1、10µg/ml。细胞在37℃,5%co2培养箱中分别孵育48h后,加入mtt(5mg/ml,sigma),10µl/孔。继续培养4h后,加入三联液[10%sds–5%异丁醇–0.012mol/lhcl(w/v/v)],100µl/孔,放置过夜后用酶标仪在570nm、630nm双波长下测定各孔的od值。
srb法
取处于对数生长期的贴壁细胞株,用25%胰酶常规消化后,再用15%小牛血清完全rpmi-1640培养基将细胞浓度调整为5×104/ml,加入96孔培养板,90μl/孔。细胞在37℃,5%co2培养箱中分别孵育24h后加入阳性对照、阴性对照以及受试样品(各受试浓度同上mtt法,10μl/孔),样品的终浓度分别为10-2、10-1、1、10、102μg/ml,相应dmso的终浓度分别为0.1%、0.01%、0.001%、0.0001%、0.00001%。样品在终浓度102μg/ml时用0.1%dmso作为溶剂对照,其余浓度均用生理盐水作阴性对照。阳性对照药顺铂的终浓度为10-1、1、10μg/ml,阴性对照为等体积的生理盐水。加样组及对照组均设4复孔,加样组、阳性对照组的高浓度组还设培养基的加药平行孔,每块板均设有4个空白对照孔(仅加培养基)。将96孔培养板置于37℃,5%co2培养箱中孵育(细胞与样品作用)48h后,加入4℃、50%的tca(三氯乙酸)50μl/孔。加完tca后,将96孔培养板置于4℃孵育1小时,取出培养板,轻轻倾去板内液体。用自来水轻轻冲洗5遍(将自来水由烧杯中轻轻倒入板中,轻晃后再将水倒去),置于空气中风干至不见水痕。然后加入配制好的0.4%srb(用1%乙酸稀释),50μl/孔,于室温下静置染色30分钟后倾去srb溶液,用1%乙酸冲洗4遍,以除去未与蛋白质结合的染料。置于空气中风干至无水痕后,加入10mm未缓冲tris(缓血氨酸)溶液150μl/孔(ph10,用三蒸水配制),将染料溶解后,于振荡器上振荡5分钟,用酶标仪在570nm波长下读取各孔od值。
实验结果
实验结果表明:经对白血病急性早幼粒nb4细胞、肺腺癌a549细胞、人骨髓神经母细胞瘤shsy5y细胞、人前列腺癌pc3细胞、人乳腺癌mcf7细胞的细胞毒活性实验,腊肠素a对nb4,a549和mcf7细胞株具有较好的细胞毒活性,ic50值分别达5.5、4.6、和8.8μm。
- 还没有人留言评论。精彩留言会获得点赞!