一种检测包含潜伏期结核感染的试剂盒及其引物对和探针的制作方法
本发明涉及一种结核感染的试剂盒,尤其涉及采用实时荧光定量聚合酶链式反应技术来检测包含潜伏期在内的全程结核感染的试剂盒及其引物对和探针。
背景技术:
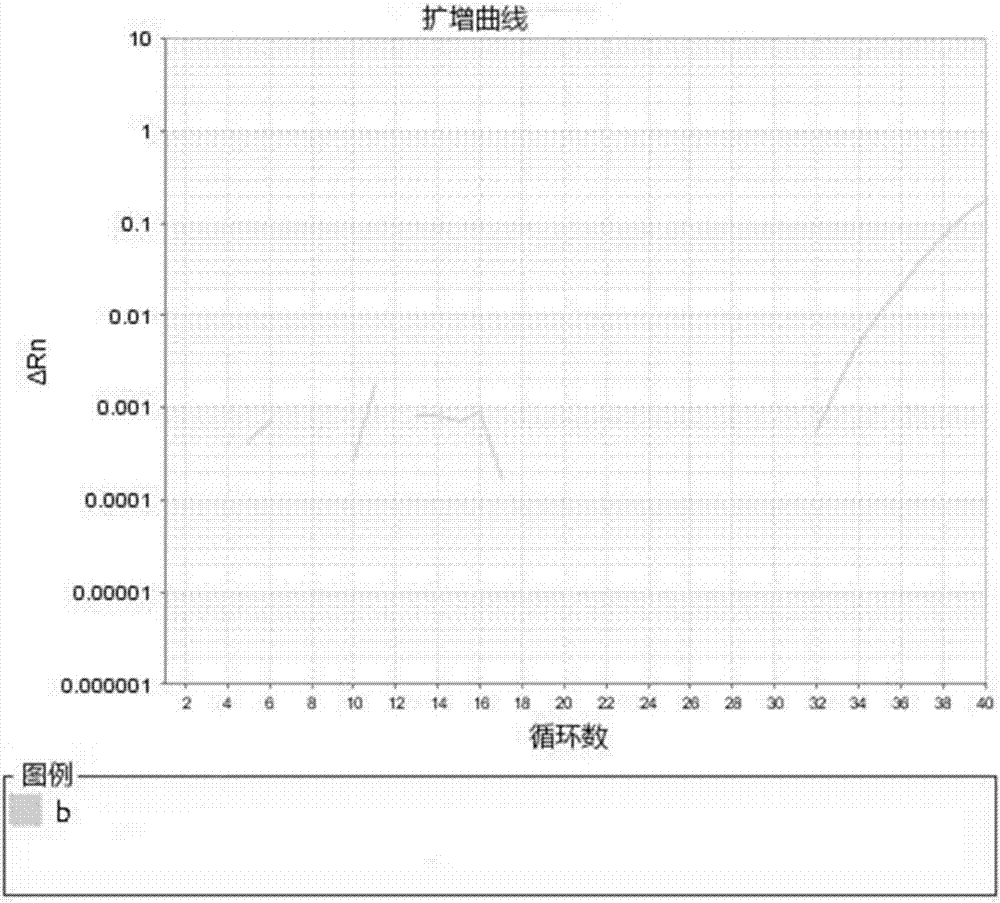
:从全球范围来看,结核至今为止仍然是传染病中发病率和死亡率最高的疾病之一,据估计每年新发病例约900,0000人,每年约有200,0000人死于结核病。结核病是由结核杆菌引起的一种人畜共患传染病,是单一致病菌感染导致死亡率最高的感染性疾病。我国是结核病高负担国家之一,2000年全国结核病流行病学抽样调查资料显示:全年龄组结核感染率为44.5%,活动性结核患者451万,每年死亡人数达13万,结核病死亡占各种传染病,寄生虫病死亡的65.1%,几乎为其它各种传染病、寄生虫病死亡总和的2倍。由于人类免疫缺陷病毒的广泛传播及耐药结核分枝杆菌的日益增多,使得这一古老的疾病再次引起人们的广泛关注。结核病成为危害人类健康的重要传染病之一。由于诊断潜伏性结核感染的检测方法研究进展缓慢,导致结核疫情控制不佳。目前,全血γ-干扰素释放试验(igra)已经在欧美地区和日本等多个低结核疫情国家广泛使用,igra采用起源于卡介苗接种菌及大多数非结核分枝杆菌所缺失的结核菌致病菌中的rd1-区所编码的特异性刺激蛋白如esat-6和cfp-10来进行检测,该类刺激物已经有商品化igra试剂,例如quantiferontbgoldtest和tspot.tbtest。有研究者在igra检测中量化干扰素-γ(ifn-γ)mrna表达水平,将其作为ifn-γ指示物,但ifn-γrt-pcr的特异性和灵敏度较差,且无法鉴别活跃期和潜伏期结核感染(ltbi)。在中国,tst作为一种基于对结核菌衍生的纯化蛋白(ppd)所产生的迟发型变态反应的检测方法仍然是用来诊断结核菌潜伏性感染(ltbi)的主要方法。tst的敏感度和特异度都依赖于一个特定群体中所定义的不同截断值而定。如果提高反应硬结直径截断值特异度就会增加(同时敏感度下降)。该实验的特异度变化很大而且主要依赖与非结核分支杆菌之间的交叉反应的可能性而定。另外,tst不能区分陈旧感染与新近感染,与卡介苗及环境非结核分支杆菌之间存在交叉免疫而导致假阳性,更由于在免疫抑制人群中检测结果存在假阴性甚至可能导致误诊。重复tst反应或者两步法tst检测可能导致助推效应从而引起敏感度的增加。tst和igras均不能鉴别潜伏期和活动期结核,而根除结核的关键之一在于鉴别潜伏性结核感染。因此,探索一种特异性强、灵敏度高的诊断潜伏性结核感染的检测方法至关重要。实时荧光定量pcr(fq-pcr)是近年在普通pcr基础上发展起来的核酸检测方法,它将荧光值的积累与pcr产物的扩增过程相结合,通过测量指数扩增期的荧光值来计算待测样本中核酸的原始量。其具有操作简便、耗时短、可定量等传统方法无可比拟的优点。另外,趋化因子是一类结构功能相似,具有趋化吸引性的小分子量蛋白,其一级结构十分相似,当趋化因子与其相应受体相结合后,通过激活g蛋白偶联受体,产生级联信号传导,对多种炎性细胞趋化和激活,在呼吸系统、心血管和肝肾等疾病中起重要作用。比如,由活化的淋巴细胞分泌的下游趋化因子γ-干扰素在结核感染检测中敏感度达80%。技术实现要素:本发明所要解决的技术问题是为克服现有技术中存在的针对结核感染的检测方法不能鉴别潜伏性结核感染以及现有检测方法特异性或敏感度不强等缺陷,提供一种检测包含潜伏期在内的全病程结核感染的试剂盒、特别是荧光定量聚合酶链反应(fq-pcr)试剂盒及其引物对和探针。该试剂盒具有操作简便、特异性强、灵敏度高、耗时短以及可定量等优点,特别能够检测潜伏期和/或早期的结核感染。本发明人首先选择结核感染、特别是潜伏结核感染时,活化的t细胞被激活时,特异的靶分子会发生上调,意外发现趋化因子cxcl9、cxcl11和cxcl13中的一种或两种以上的组合均对于潜伏结核感染有较好的灵敏度和特异性。然后进一步针对上述趋化因子挑选合适的检测方法。由于与基于扩增反应完成后进行单一终点检测的传统pcr方法不同,fq-pcr方法可以在扩增反应进行的过程中随时监测扩增产物的产生,从而极大的提高了定量检测的准确性和精密度,故本发明优选fq-pcr方法。实时荧光定量pcr(taqman探针法)在pcr的扩增中,同时加入了引物和在5’末端和3’末端分别标记有荧光发生基团和荧光淬灭基团的特异性寡核苷酸探针。如果探针没有与靶序列互补结合,探针序列保持完整,荧光发生基团发射的荧光信号被淬灭基团吸收,故没有荧光信号的产生,而当探针与靶序列能够互补结合时,在pcr扩增进行的过程中,dna聚合酶在引导dna序列复制的同时其5’-3’端外切酶活性将切断荧光探针,导致荧光发生基团与荧光淬灭基团的分离,从而荧光检测系统可以接收并记录荧光信号。每扩增一条dna链即有一个荧光信号的产生,荧光信号的积累与pcr产物的形成完全同步,故可以实时地监测整个pcr反应过程,并可借助标准曲线或表达量恒定的内对照产物对未知的靶多核苷酸进行绝对或相对的定量分析。因此,探针和引物的设计对于实现靶多核苷酸的定量检测至关重要。本发明人为此反复试验和研究,在特异性和敏感度等方面进行平衡,筛选出了测定趋化因子cxcl9、cxcl11和cxcl13的相关引物对和探针。本发明解决上述技术问题的技术方案之一是:一种检测包含潜伏期结核感染的试剂盒,其包括至少一种反应液,所述反应液包括目的基因的一引物对和一探针,所述的引物对和探针针对结核分枝杆菌特异性t细胞分泌的下游趋化因子cxcl9、cxcl11或cxcl13的基因序列设计;其中,针对趋化因子cxcl9设计的所述引物对的正向引物(引物1)是如seqidno.1所示序列的核酸,反向引物(引物2)是如seqidno.2所示序列的核酸,所述探针(探针1)的核苷酸序列如seqidno.9所示;针对趋化因子cxcl11设计的所述引物对的正向引物(引物3)是如seqidno.3所示序列的核酸,反向引物(引物4)是如seqidno.4所示序列的核酸,所述探针(探针2)的核苷酸序列如seqidno.10所示;或者针对趋化因子cxcl13设计的所述引物对的正向引物(引物5)是如seqidno.5所示序列的核酸,反向引物(引物6)是如seqidno.6所示序列的核酸,所述探针(探针3)的核苷酸序列如seqidno.11所示。其中,引物1位于人的cxcl9基因序列的197-221位,引物2位于289-265位,扩增片段长度为93bp,所对应的探针位于234-260位;引物3位于人的cxcl11基因序列的113-136位,引物4位于255-230位,扩增片段长度为143bp,所对应的探针位于184-211位;引物5位于人的cxcl13基因序列的199-224位,引物6位于314-293位,扩增片段长度为116bp,所对应的探针位于226-249位。较佳地,使结果可靠,抗干扰能力更强,作为表达量参照,本发明选用管家基因作为内部参照,优选人β-globin(β-球蛋白)基因,所述的反应液均还包括针对人β-globin基因设计的管家基因的一引物对和一探针;所述引物对中,正向引物(引物7)是如seqidno.7所示序列的核酸,反向引物(引物8)是如seqidno.8所示序列的核酸,所述探针(探针4)的核苷酸序列如seqidno.12所示。其中,引物7位于人β-globin基因组序列的hbb基因(62137-63742)的62627-62647位,引物8位于62756-62775位,扩增片段长度为149bp,所对应的探针位于β-globin基因序列反向序列的62731-62755位。较佳地,所述的反应液均还包括pcr反应缓冲液和2’-脱氧核苷三磷酸;较佳地,所述2’-脱氧核苷三磷酸的浓度为100mm。本发明所述的试剂盒优选为实时荧光定量pcr(fq-pcr)试剂盒。较佳地,上述试剂盒还可以包括普通pcr、荧光pcr、尤其fq-pcr的其他常规试剂:eztaq混合液和阴性质控品等;所述eztaq混合液包括热启动taq酶,浓度优选1-5u/μl。更佳地,为提高血液样本中趋化因子的含量,相应地提高试剂盒检测的灵敏度和特异性,所述试剂盒还可以包括结核抗原管和本底对照管,所述结合抗原管中包含抗原刺激物或其组合物;所述抗原刺激物或其组合物优选抗原cfp10衍生肽、抗原esat6衍生肽、抗原ppe衍生肽以及抗原ag85a衍生肽中的至少一种。所述抗原cfp10衍生肽的氨基酸序列更优选如seqidno.13所示,所述抗原esat6衍生肽的氨基酸序列更优选如seqidno.14所示,所述抗原ppe衍生肽的氨基酸序列更优选如seqidno.15所示,所述抗原ag85a衍生肽的氨基酸序列更优选如seqidno.16所示。本发明解决上述技术问题的技术方案之二是:一种检测包含潜伏期结核感染的探针,所述探针的核苷酸序列如seqidno.9、seqidno.10、seqidno.11或者seqidno.12所示。较佳地,上述探针为适用fq-pcr检测的荧光探针,其上述序列的两端连接的均为常规的荧光报告基团和淬灭基团。其中,目的基因(seqidno.9-11)报告基团:fam;管家基因报告基团(seqidno.12):vic;目的基因和管家基因的淬灭基团:bhqmgb)。本发明解决上述技术问题的技术方案之三是:一种检测包含潜伏期结核感染的引物对,所述引物对的一条是如seqidno.1所示序列的核酸,另一条是如seqidno.2所示序列的核酸;所述引物对的一条是如seqidno.3所示序列的核酸,另一条是如seqidno.4所示序列的核酸;所述引物对的一条是如seqidno.5所示序列的核酸,另一条是如seqidno.6所示序列的核酸;或者所述引物对的一条是如seqidno.7所示序列的核酸,另一条是如seqidno.8所示序列的核酸。本发明解决上述技术问题的技术方案之四是:一种反应液,其包括一引物对和一探针,所述的引物对和探针针对结核分枝杆菌特异性t细胞分泌的下游趋化因子cxcl9、cxcl11或cxcl13的基因序列设计;其中,针对趋化因子cxcl9设计的所述引物对的正向引物是如seqidno.1所示序列的核酸,反向引物是如seqidno.2所示序列的核酸,所述探针的核苷酸序列如seqidno.9所示;针对趋化因子cxcl11设计的所述引物对的正向引物是如seqidno.3所示序列的核酸,反向引物是如seqidno.4所示序列的核酸,所述探针的核苷酸序列如seqidno.10所示;或者针对趋化因子cxcl13设计的所述引物对的正向引物是如seqidno.5所示序列的核酸,反向引物是如seqidno.6所示序列的核酸,所述探针的核苷酸序列如seqidno.11所示。较佳地,所述反应液均还包括作为表达量参照检测管家基因人β-globin基因的管家基因的一引物对和一探针;所述引物对中,正向引物是如seqidno.7所示序列的核酸,反向引物是如seqidno.8所示序列的核酸,所述探针的核苷酸序列如seqidno.12所示。本发明解决上述技术问题的技术方案之四是:所述的探针、所述的引物对或者所述的反应液在制备检测包括潜伏期结核感染的试剂盒、优选fq-pcr试剂盒中的应用。较佳地,所述应用为将上述试剂盒用于血液样本的检测。在符合本领域常识的基础上,上述各优选条件,可任意组合,即得本发明各较佳实例。本发明所用试剂和原料均市售可得。本发明的积极进步效果在于:如上所述,为了检测出临床血液样本是否为潜伏结核感染样本,本发明将趋化因子cxcl9、cxcl11、cxcl13的核苷酸序列进行分析,特别设计适用本发明检测试剂盒的寡核苷酸引物和探针。使用这些引物和探针完成的实时定量检测,不仅操作简便、耗时短、特异性强,而且极大地提高了结核检测灵敏度,避免卡介苗或陈旧感染等的干扰导致假阳性而结果不准确,降低了模板使用量。实验证明,本发明对潜伏结核检测的灵敏度在97%以上。利用本发明的试剂盒能够及早发现潜伏的结核感染并采取应对措施,以减轻患者痛苦,提高结核治愈率。附图说明图1为扩增曲线不呈现“s”型或ct值>35的样本。图2为ct值空白样本。图3为扩增曲线呈现“s”型且结核刺激样本ct值<本底对照样本ct值;其中,图1-3中的“a”和“b”分别指的是“目的基因”和“管家基因”。具体实施方式下面通过实施例的方式进一步说明本发明,但并不因此将本发明限制在所述的实施例范围之中。下列实施例中未注明具体条件的实验方法,按照常规方法和条件,或按照商品说明书选择。实施例1试剂盒各组成成分的制备以及试剂盒的组装表1.各组分名称、浓度以及含量上述反应缓冲液选用市售商品(购自上海多泽生物科技有限公司),dntp(购自上海兆维科技发展有限公司),eztaq酶或混合液(购自上海多泽生物科技有限公司),引物和探针(商业合成,英潍捷基(上海)贸易有限公司(abi))。(1)制备包括下列组成成份的试剂盒:反应液1(650μl/管)1管:pcr反应缓冲液、2’-脱氧核苷三磷酸、用于扩增cxcl9的正向引物(引物1)和反向引物(引物2),寡核苷酸探针为探针1;用于管家基因人β-globin基因靶多核苷酸扩增的引物7和引物8,寡核苷酸探针为探针4。反应液2(650μl/管)1管:反应液2由如下组分组成:pcr反应缓冲液、2’-脱氧核苷三磷酸、用于cxcl11靶多核苷酸扩增的正向引物(引物3)和反向引物(引物4),寡核苷酸探针为探针2;用于管家基因人β-globin基因靶多核苷酸扩增的引物7和引物8,寡核苷酸探针为探针4。反应液3(650μl/管)1管:反应液3由如下组分组成:pcr反应缓冲液、2’-脱氧核苷三磷酸、用于cxcl13靶多核苷酸扩增的正向引物(引物5)和反向引物(引物6),寡核苷酸探针为探针3;用于管家基因人β-globin基因靶多核苷酸扩增的正向引物(引物7)和反向引物(引物8),寡核苷酸探针为探针4。eztaq酶混合液(150μl/管)1管:taq酶。表2eztaq酶混合液组成标准液:阴性质控品(80μl/管):纯化水。结核抗原管(采血管1):抗原刺激物放到采血管中,每支采血管含有抗原刺激物20μg(0.5mg/ml)和肝素钠干粉30iu(900iu/ml)。本底对照管(采血管2):采血管中只含有肝素钠干粉30iu(900iu/ml)。反应液1与eztaq酶混合液、标准液以及结核抗原管和本底对照管作为体系i;反应液2与eztaq酶混合液、标准液以及结核抗原管和本底对照管作为体系ii;反应液3与eztaq酶混合液、标准液以及结核抗原管和本底对照管作为体系iii。其中,引物1-8构成了各体系中的核酸扩增体系,探针1-4构成了各体系中的荧光检测体系;各引物和探针具体组成如下:表3各引物和探针具体组成引物名称核苷酸组成序列号引物15’-ccacctacaatccttgaaagacctt-3’seqidno.1引物25’-tgaactccattcttcagtgtagcaa-3’seqidno.2引物35’-tcaatttcctttcatgttcagcat-3’seqidno.3引物45’-acacaatatcacagccaaggctatag-3’seqidno.4引物55’-gtctttatccctagacgcttcattga-3’seqidno.5引物65’-gggtccacacacacaattgact-3’seqidno.6引物75’-ttcctcctcctgagcagt-3’seqidno.7引物85’-aaggtcataacctggttcatc-3’seqidno.8探针15’-ccaagcccttcctgcgagaaaattgaa-3’seqidno.9探针25’-caccagcagcaacagcaaaaaacaaaca-3’seqidno.10探针35’-cgaattcaaatcttgccccgtggg-3’seqidno.11探针45’-ccctggcgtcgtgattagtgatgatgaac-3’seqidno.12上述探针1~3的5’端连接有报告基团fam,3’端连接有淬灭基团bhqmgb;探针4的5’端连接有报告基团vic,3’端连接有淬灭基团bhqmgb。(2)试剂盒的组装根据需求,可将eztaq酶混合液、标准液等试剂管以及结核抗原管和本底对照管分别与装有上述反应液1~3的单个离心管分隔包装组成分别测定趋化因子cxcl9、cxcl11、cxcl13的试剂盒;也可以将上述各试剂管以及采血管和2个以上分别装有不同的上述反应液1~3的离心管包装成双靶点或三靶点的试剂盒。实施例2试剂盒的使用方法1)抽取样本血液至本底对照管和结核抗原管中样本采集、运送和保存:用一次性真空采血器,无菌操作,取待检个体血液样本,做好标示后将获取的血液样本置于低温冰箱(-70℃或-20℃)中冷冻保存。如集中检验,标本需在0℃以下环境中运送并于24小时内送达实验室。临床抽取2ml样本血液加入本底对照管中,标记为本底对照样本;另抽取同一个体样本血液2ml,加入含有20μg抗原刺激物(包含cfp10、esat6、ppe4和ag85a的衍生肽段(摩尔比为1:1:1:1),由金斯康科技(南京)有限公司合成)的结核抗原管中于35℃下刺激6h后,标记为结核抗原样本。其中,4种抗原衍生肽的序列为:cfp10衍生肽:qgqwrgaagtaa(如seqidno.13所示);esat6衍生肽:elnnal(如seqidno.14所示);ppe衍生肽:agwqtlsaaldaqaveltar(seqidno.15所示);ag85a衍生肽:rhvkptgsavvgl(如seqidno.16所示)。2)提取本底对照管和结核抗原管血液样本中的rna取两管中待测血样各300μl(所述待测血液是指需要检测是否为潜伏结核感染的临床血液样本),用磁珠法同批次提取(提取试剂购自深圳市安必胜科技有限公司)血液样本mrna,使用rna逆转录试剂盒(购自宝生物工程(大连)有限公司)逆转录为cdna,用分光光度计或类似的仪器确认cdna的质量(od260/280在1.8-2.0之间)。3)将所述cdna加入到反应液中,通过核酸扩增体系、用实时荧光pcr仪进行扩增反应,循环扩增待测样品中的靶多核苷酸;使所述荧光检测体系中的荧光发生基团与被扩增的靶多核苷酸序列间接结合。将逆转录的每份结核抗原管cdna和本底对照管cdna分别置于3个pcr反应管或pcr板的3个孔中,每孔2μl。然后,在加入同一dna样本的3个孔中各加入一种pcr反应液(反应液1、反应液2、反应液3)15μl,再在每个孔中加入3μl的eztaq酶混合液。混匀离心后,将pcr反应体系置于自动荧光检测热循环仪(abi7500)上,选择fam通道(reporter:fam,quencher:none)收集特异扩增信号;选择vic通道(reporter:vic,quencher:none)检测内标;参比荧光(passivereference)设置为none;设置samplevolume为20。按照仪器操作说明做好相应设置后开始试验。具体pcr扩增反应体系、反应条件见表4和表5。表4pcr扩增反应体系组分含量反应液1或2或315μleztaq酶混合液3μl模板2μl总计20μl表5pcr扩增反应条件4)通过比较待检样品和标准品的循环阈值判定荧光发生基团所产生的荧光量,从而确定靶多核苷酸的存在。反应结束后保存检测数据文件,点选仪器的数据分析选项后可查看各个pcr反应体系的结果,如pcr扩增曲线,待检样本和标准样本的ct值等。计算方法:以扩增过程前3~15循环的荧光值的10倍标准差为阈值(threshold),以荧光值超过阈值的循环数为阈值循环数(值)ct值。若管家基因ct值>35,结果不可靠,请重新测定或观察血液本身是否存在问题。若管家基因ct值≦35时进行以下计算:本底对照管:△cta=ct值(目的基因)-ct值(管家基因)结核抗原管:△ctb=ct值(目的基因)-ct值(管家基因)结果判读:t值=△ctb–△cta。1.无效结果判定:与存在于体系ⅰ、ⅱ、ⅲ中的寡核苷酸荧光探针1、探针2、探针3和探针4相关的扩增曲线不呈现“s”型或ct值空白又或ct值>35的样本,报告为无效(见图1、图2);2.阳性结果判定:满足与体系ⅰ或体系ⅱ或体系ⅲ中的寡核苷酸探针1、探针2、探针3和探针4相关的扩增曲线呈现“s”型且t值≤-1.04,报告为阳性(见图3);3.阴性结果判定:属于无效结果判定和阳性结果判定以外的情况且t值>-1.04。则报告为阴性(阴性对照品就是没有出现扩增,说明本实验体系未受到外界污染)。实施例3使用本发明的试剂盒检测30例临床血液样本的结果与分析采用单盲实验法,从来自(南京胸科医院)的500例血液样本中选择30例(均为需要检测是否为潜伏结核感染的临床血液样本)用本发明的试剂盒进行试验,以临床诊断对实验结果进行复核。实验过程:临床抽取2ml样本血液至本底对照管中,标记为本底对照样本;另抽取2ml血液样本,加入到含有20μg抗原刺激物的结核抗原管中,于35℃刺激6h后,标记为结核抗原样本。将待检测血样取300μl,用磁珠法同批次提取血液样本mrna,购买市售rna逆转录试剂盒逆转录为cdna,用分光光度计或类似的仪器确认cdna的质量(od260/280在1.8-2.0之间),将逆转录的每份待检样本cdna和标准品cdna分别置于3个pcr反应管或pcr板的3个孔中,每孔2μl。然后,在加入同一dna样本的3个孔中各加入一种pcr反应液(反应液1、反应液2、反应液3)15μl,再在每个孔中加入3μl的eztaq酶混合液。具体pcr扩增反应体系见表3。混匀离心后,将pcr反应体系置于自动荧光检测热循环仪上,选择fam通道(reporter:fam,quencher:none)收集特异扩增信号;选择vic通道(reporter:vic,quencher:none)检测内标;参比荧光(passivereference)设置为none;设置samplevolume为20。按照仪器操作说明做好相应设置后开始试验。本试剂盒的所使用的反应条件(如表5所示)是:(1)95℃预变性5分钟;(2)95℃15秒;(3)58℃35秒;(4)72℃20秒;步骤(2)-(4)循环40次。试验数据以及数据分析:表6反应液1检测结果表7反应液2检测结果表8反应液3检测结果表93种反应液的检测结果比较表10不同反应液组合时的灵敏度实验结果显示,本发明对潜伏结核检测的灵敏度最高达97%以上。<110>苏州创澜生物科技有限公司<120>一种检测包含潜伏期的结核感染的试剂盒及其引物对和探针<130>p1611497c<160>16<170>patentinversion3.5<210>1<211>25<212>dna<213>artificialsequence<220><223>引物1<400>1ccacctacaatccttgaaagacctt25<210>2<211>25<212>dna<213>artificialsequence<220><223>引物2<400>2tgaactccattcttcagtgtagcaa25<210>3<211>24<212>dna<213>artificialsequence<220><223>引物3<400>3tcaatttcctttcatgttcagcat24<210>4<211>26<212>dna<213>artificialsequence<220><223>引物4<400>4acacaatatcacagccaaggctatag26<210>5<211>26<212>dna<213>artificialsequence<220><223>引物5<400>5gtctttatccctagacgcttcattga26<210>6<211>22<212>dna<213>artificialsequence<220><223>引物6<400>6gggtccacacacacaattgact22<210>7<211>18<212>dna<213>artificialsequence<220><223>引物7<400>7ttcctcctcctgagcagt18<210>8<211>21<212>dna<213>artificialsequence<220><223>引物8<400>8aaggtcataacctggttcatc21<210>9<211>27<212>dna<213>artificialsequence<220><223>探针1<400>9ccaagcccttcctgcgagaaaattgaa27<210>10<211>28<212>dna<213>artificialsequence<220><223>探针2<400>10caccagcagcaacagcaaaaaacaaaca28<210>11<211>24<212>dna<213>artificialsequence<220><223>探针3<400>11cgaattcaaatcttgccccgtggg24<210>12<211>29<212>dna<213>artificialsequence<220><223>探针4<400>12ccctggcgtcgtgattagtgatgatgaac29<210>13<211>12<212>prt<213>artificialsequence<220><223>cfp10衍生肽段<400>13glnglyglntrpargglyalaalaglythralaala1510<210>14<211>6<212>prt<213>artificialsequence<220><223>esat6衍生肽段<400>14gluleuasnasnalaleu15<210>15<211>20<212>prt<213>artificialsequence<220><223>ppe衍生肽段<400>15alaglytrpglnthrleuseralaalaleuaspalaglnalavalglu151015leuthralaarg20<210>16<211>13<212>prt<213>artificialsequence<220><223>ag85a衍生肽段<400>16arghisvallysprothrglyseralavalvalglyleu1510当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1